-
Medical journals
- Career
Léčba chylothoraxu embolizací hrudního mízovodu
Authors: V. Chovanec 1; J. Drugda 2; Miroslav Lojík 1; P. Vodárek 2; P. Žák 2; I. Hanke 3; V. Koblížek 4
Authors‘ workplace: Radiologická klinika Fakultní nemocnice v Hradci Králové a Lékařská fakulta Univerzity Karlovy v Hradci Králové 1; IV. interní hematologická klinika, Fakultní nemocnice v Hradci Králové a Lékařská fakulta Univerzity Karlovy v Hradci, Králové 2; Kardiochirurgická klinika Fakultní nemocnice v Hradci Králové a Lékařská fakulta Univerzity Karlovy v Hradci Králové 3; Plicní klinika Fakultní nemocnice v Hradci Králové a Lékařská fakulta Univerzity Karlovy v Hradci Králové 4
Published in: Rozhl. Chir., 2022, roč. 101, č. 12, s. 607-611.
Category: Case Report
doi: https://doi.org/10.33699/PIS.2022.101.12.607–611Overview
Autoři prezentují případ netraumatického nádorového pravostranného chylothoraxu, který byl úspěšné léčen embolizací ductus thoracicus. Výkon byl proveden transabdominálně, antegrádním přístupem přes cisterna chyli zobrazenou pomocí intranodální lymfografie. K embolizaci byly použity mikrospirály a akrylátové tkáňové lepidlo. Nemocný je sledován 5 měsíců a je bez recidivy chylothoraxu.
Klíčová slova:
embolizace – chylothorax – ductus thoracicus – lymfografie – intranodální
ÚVOD
Chylothorax je definován jako nahromadění mízy (chylu) v pleurální dutině. Jedná se o závažný stav, který pokud se neléčí, má vysokou morbiditu a mortalitu. Léčba je konzervativní a zahrnuje nízkotučnou dietu, úplnou parenterální výživu, podávání analogů somatostatinu, drenáž hrudníku a v případech netraumatického maligního chylothoraxu i léčbu základního onemocnění [1,2]. Pokud není konzervativní léčba úspěšná, nastupuje invazivní léčba, do které patří chirurgické a radiologické postupy. V chirurgické léčbě chylothoraxu se využívá ligace ductus thoracicus, pleurodéza, pleurektomie, pleuroperitoneální shunt nebo našití lymfovenózní spojky. Radiologická léčba spočívá v provedení lymfografie a následné embolizaci ductus thoracicus, která může být provedena antegrádně, a to perkutánním přístupem přes cisterna chyli nebo retrográdně, buď nasondováním venózního ústí hrudního mízovodu, anebo přímou punkcí ductus thoracicus v místě jeho vyústění do angulus venosus. Punkce se provádí pod UZ nebo skiaskopickou kontrolou. V české literatuře byly publikovány zkušenosti s konzervativní a chirurgickou léčbou chylothoraxu, ale zatím nebyla popsána perkutánní embolizace ductus thoracicus [2–4].
KAZUISTIKA
Pacient, 55 let, s postupně vzniklou dušností, pro kterou byl hospitalizován ve Fakultní nemocnici Hradec Králové v listopadu 2021. Snímek hrudníku odhalil významný fluidothorax vlevo. Nemocný podstoupil punkci fluidothoraxu se zavedením hrudního drénu a odsátím 1650 ml mléčné tekutiny. Biochemické a cytologické vyšetření punktátu potvrdilo, že se jedná o chylothorax, a pro přítomnost velkého množství lymfocytů bylo vyjádřeno podezření na lymfom. Z biopsie krční uzliny a po provedení CT krku a trupu byla stanovena diagnóza folikulárního lymfomu, gr. 2, stadium IV A. Hrudní drén byl vytažen za 10 dní po jeho zavedení. Nemocný podstoupil 3 cykly chemoterapie, po kterých se objevil chylothorax vpravo. K chemoterapii byla nasazena nízkolipidová dieta a podávání octreotidu, což nevedlo k regresi chylothoraxu a byly nutné jeho opakované punkce. Na multioborovém semináři bylo rozhodnuto o provedení olejové intranodální lymfografie za účelem zástavy tvorby chylothoraxu a zjištění místa extravazace lymfy do pravé pleurální dutiny. Ultrazvukové vyšetření srdce v únoru 2022 neprokázalo zkratovou vadu, a tak byla provedena intranodální lymfografie. Při daném výkonu byly za sterilních podmínek pod UZ kontrolou punktovány lymfatické uzliny v obou tříslech. K punkci se použily jehly o průměru 22 G a délky 100 mm (Sprotte Lumbar, Pajunk, Geisingen, Německo). Následně se přes dané jehly podalo 14 ml olejové kontrastní látky, aby se naplnily retroperitoneální uzliny do úrovně 2. bederního obratle. Další den bylo provedeno nativní CT vyšetření s nálezem kapiček olejové kontrastní látky v pravé pleurální dutině. Po lymfografii nedošlo k zástavě tvorby chylothoraxu, a proto nemocný podstoupil opakovanou intranodální lymfografii 29. den po prvním vyšetření za účelem zobrazení cisterna chyli a embolizace ductus thoracicus antegrádním přístupem. Opět byly punktovány tříselné uzliny pod UZ kontrolou (Obr. 1) s podáním 19 ml olejové kontrastní látky (Obr. 2). Po opacifikaci cisterna chyli (Obr. 3) byla provedena její punkce Chiba jehlou průměru 21 G a délky 15 cm (Obr. 4). Punkce je bolestivá, a proto se provádí v analgosedaci. Poté byl přes jehlu zaveden do ductus thoracicus hydrofilní vodič o průměru 0,018 palce a délky 300 cm. Po vodiči se zavedl 2,4 F mikrokatétr a po podání jodové kontrastní látky se zobrazily patologické lymfatické cévy směřující do pravé pleurální dutiny (Obr. 5). Ductus thoracicus byl pak embolizován zavedením dvou spirál 4×140 mm a aplikací směsí tkáňového akrylátového lepidla a olejové kontrastní látky (Obr. 6). Dva dny po embolizaci se objevila horečka a kašel způsobené onemocněním covid-19 s nutností podávání antivirotika remdesiviru a antibiotik piperacillinu + tazobaktamu a levofloxacinu. Postupně došlo ke zlepšení klinického stavu a nemocný byl propuštěn domů 21 dnů po provedení embolizace. Dle kontrolního PET CT vyšetření z května 2022 byla dosažena kompletní remise základního onemocnění a nebyl přítomen fluidothorax. Nemocný je sledován 5 měsíců po výkonu a je bez recidivy chylothoraxu.
Image 1. UZ obraz jehly (bílá šipka) zavedené do lymfatické uzliny (černé šipky)
Fig. 1. Ultrasound image of needle (white arrow) inserted into the lymph node (black arrows)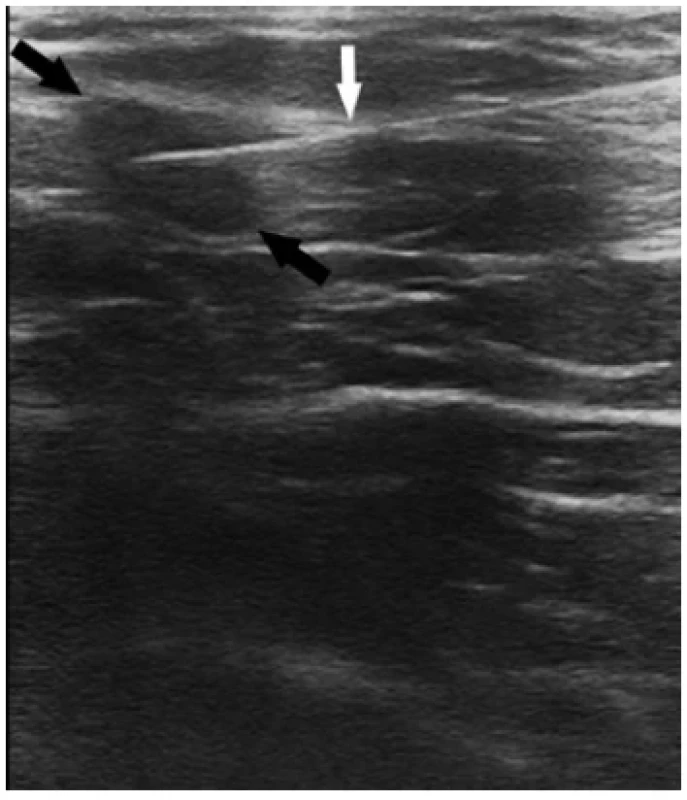
Image 2. Podávání olejové kontrastní látky do lymfatických uzlin. V pravém třísle zavedeny 2 jehly, v levém třísle zavedena 1 jehla
Fig. 2. Administration of an oil contrast agent to the lymph nodes. Two needles inserted in the right groin, 1 needle inserted in the left groin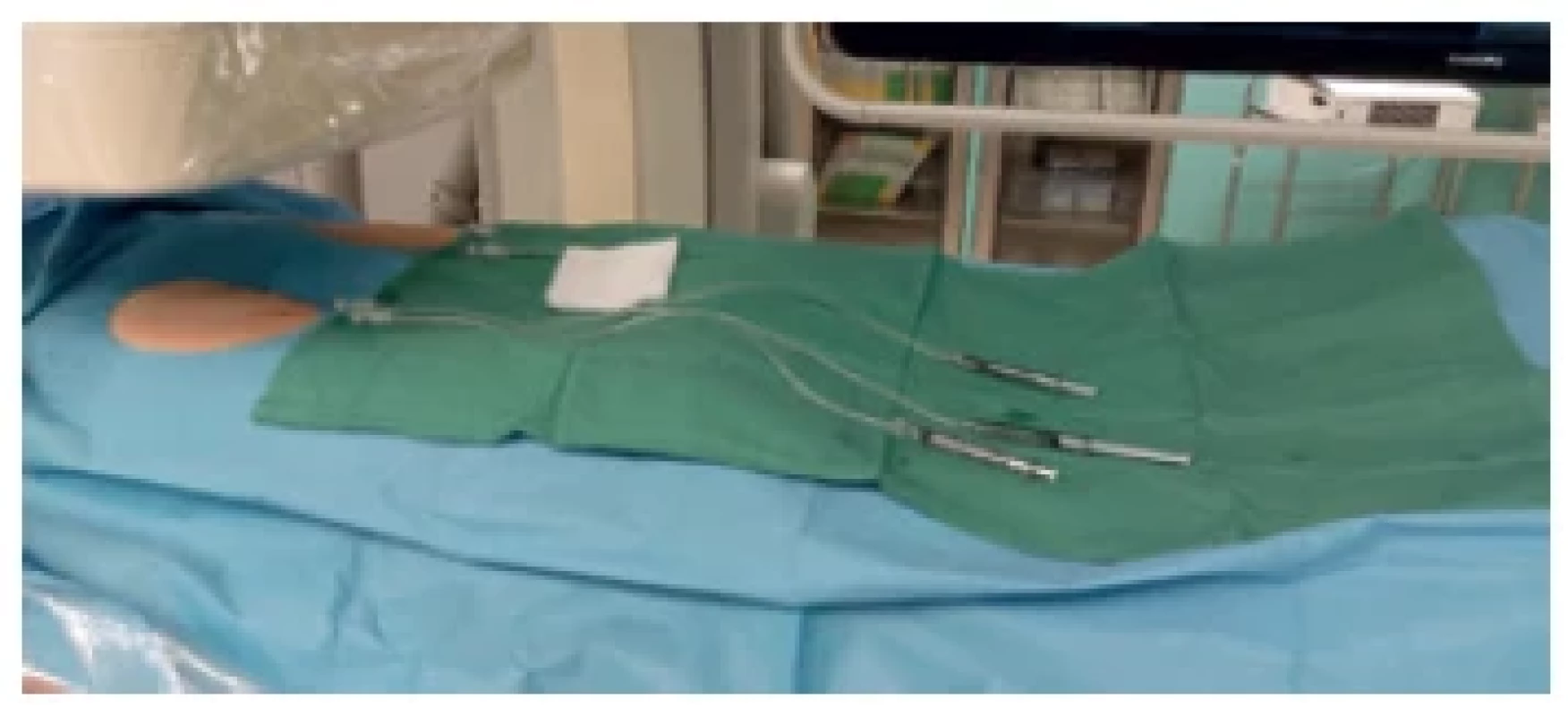
Image 3. Naplnění cisterna chyli (bílá šipka) v plnicí fázi lymfografie
Fig. 3. Opacification of the cisterna chyli (white arrow) during filling phase of lymphography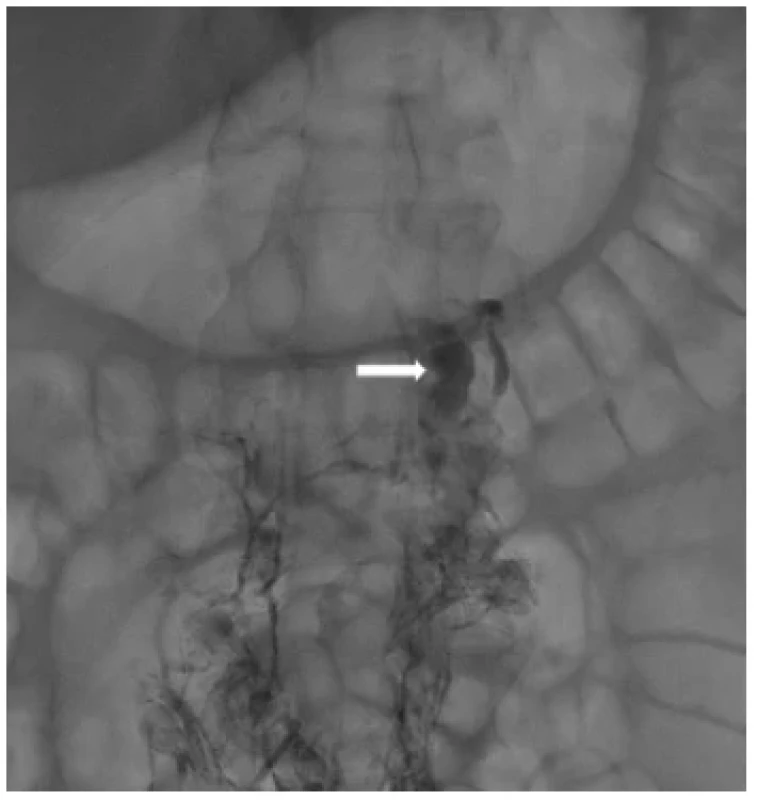
Image 4. Punkce cisterna chyli Chiba jehlou
Fig. 4. Cisterna chyli puncture with a Chiba needle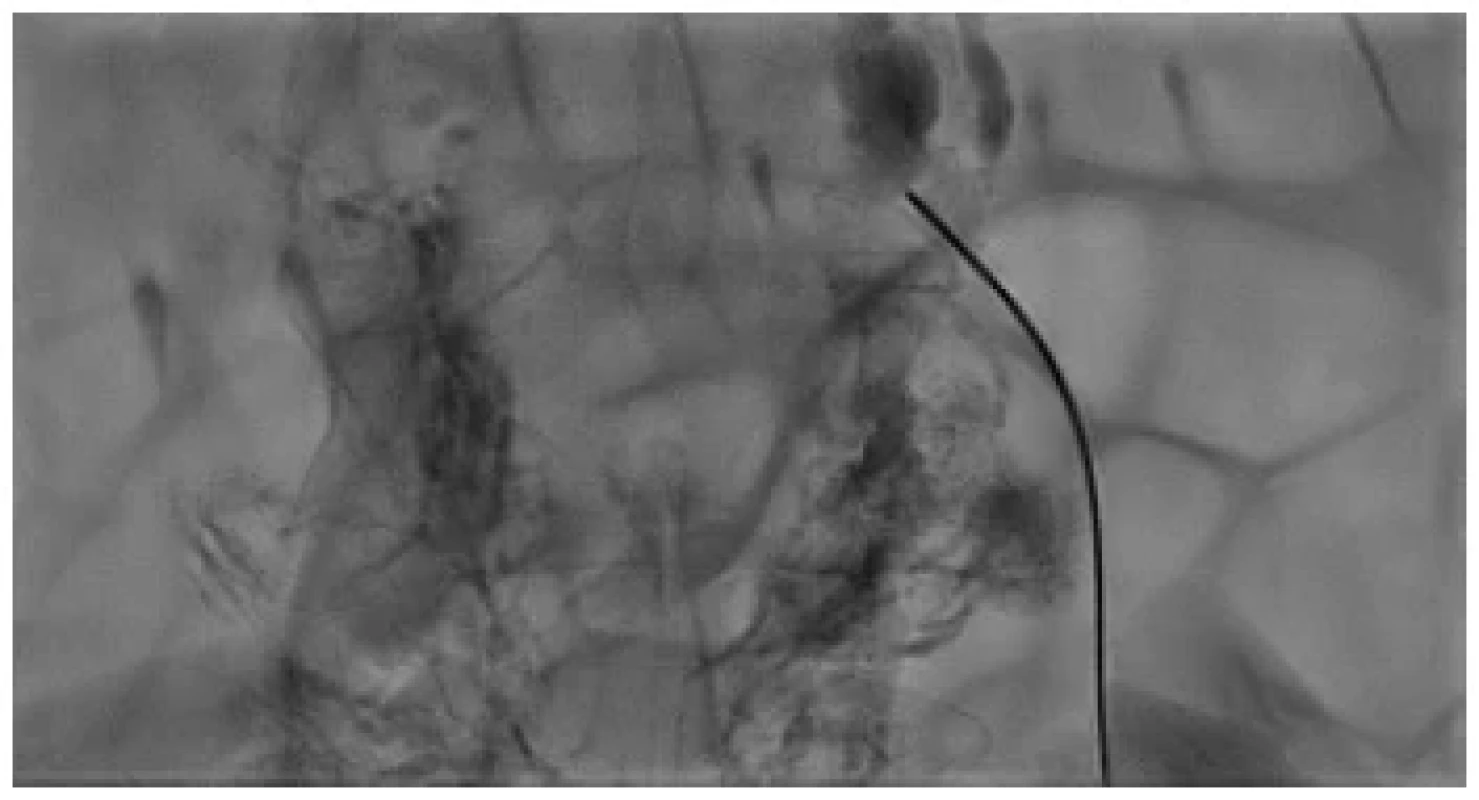
Image 5. Skiaskopické zobrazení ductus thoracicus podáním jodové kontrastní látky do mikrokatétru
Fig. 5. Fluoroscopy of thoracic duct during administration of iodine contrast medium into microcatheter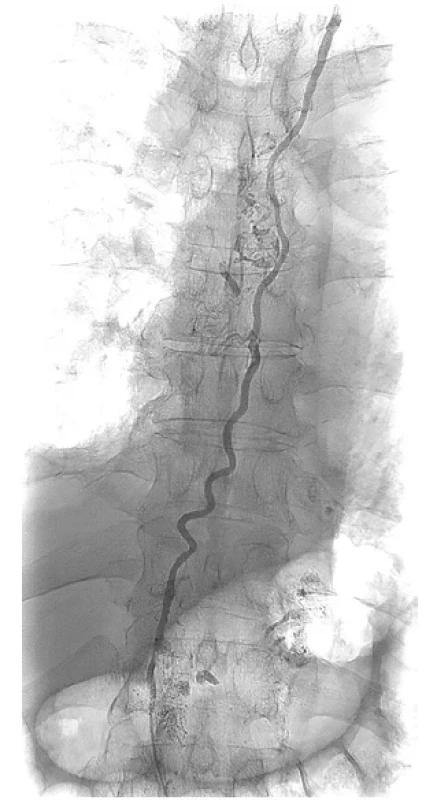
Image 6. Snímek po embolizaci ductus thoracicus pomocí mikrospirál (bílá šipka) a akrylátového tkáňového lepidla smíchaného s olejovou kontrastní látkou (černá šipka)
Fig. 6. X ray image after embolization of the thoracic duct using microspirals (white arrow) and acrylic tissue glue mixed with oil contrast medium (black arrow)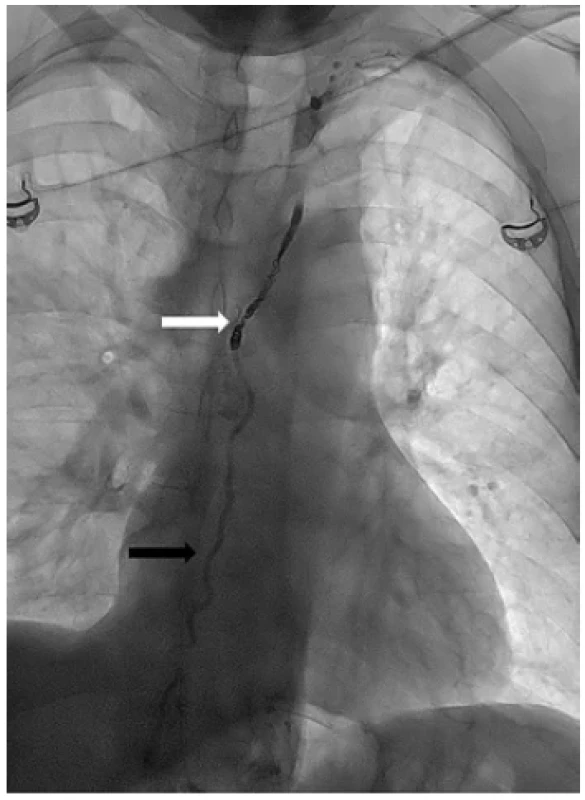
DISKUZE
Chylothorax je závažný stav s významnou morbiditou a mortalitou. Nejčastěji se dělí na traumatický a netraumatický. Traumatický chylothorax má 2 podskupiny, a to iatrogenní a neiatrogenní. Mezi iatrogenní příčiny patří hrudní chirurgie (operace plíce, jícnu, mediastina a páteře), kardiochirurgie, chirurgie hlavy a krku a výkony spojené s kanylací centrální žíly (zavádění centrálních žilních katétrů a zavádění kardiostimulátorů). Do skupiny neiatrogenních příčin se řadí tupá poranění, penetrující poranění, kašel, úporné zvracení a porod. Skupinu netraumatických příčin lze rozdělit na nádorovou, nenádorovou a idiopatickou. Diagnóza chylothoraxu je laboratorní a cytologická. Pokud dochází ke ztrátám chylu, tak je pacient ohrožen hyponatremií, hypokalemií, hypokalcemií, hypofosfatemií, metabolickou acidózou, koagulopatií a deficitem T lymfocytů [2]. Ze zobrazovacích metod se uplatňuje rtg snímek hrudníku, který určí stranu výpotku. Pomocí CT vyšetření hrudníku a břicha s podáním kontrastní látky lze určit i příčinu netraumatického chylothoraxu. K určení místa extravazace chylu se používá lymfoscintigrafie, často ve spojení se SPECT, rtg lymfografií a CT nebo MR lymfografií [2]. Klasická rentgenová lymfografie neboli lymfangiografie se v České republice provádí pouze na několika pracovištích. Na našem pracovišti v současnosti provádíme i intranodální lymfografii, při které se aplikuje olejová kontrastní látka do tříselné uzliny, která byla napíchnuta tenkou jehlou pod UZ navigací [5]. V posledních letech dané vyšetření nabývá na významu. Přínos není jenom v průkazu místa extravazace lymfy, ale zejména v terapeutické roli samotné lymfografie, která dosahuje v závislosti na velikosti chylothoraxu až 70 % při ztrátách do 500 ml/den a 35 % při ztrátách nad 500 ml/den [6]. Dalším důvodem lymfangiografie je možnost navázat embolizací ductus thoracicus, která se provádí z přímého nápichu cisterna chyli. MR lymfangiografie zahrnuje i aplikaci kontrastní látky. Doporučuje se provedení tzv. dynamické MR lymfografie s podáním kontrastní látky do lymfatické uzliny [7]. Tato metoda umožňuje velmi přesně definovat místo úniku lymfy a naplánovat invazivní léčebný postup, který v našich podmínkách nejčastěji zahrnuje chirurgickou ligaci ductus thoracicus [2].
V současnosti nejsou dostupná mezinárodní doporučení pro diagnostiku a léčbu chylothoraxu. Léčebné postupy zahrnují: a) konzervativni terapii, b) intervenční terapii a c) terapii primární patologie, která se nejvíce uplatňuje u netraumatického maligního chylothoraxu a zahrnuje chemoterapii a radioterapii. Konzervativní léčba spočívá v hrudní drenáži nebo hrudní punkci, nízkotučné dietě s omezením mastných kyselin s dlouhým řetězcem a s podáváním mastných kyselin se středně dlouhým řetězcem nebo totální parenterální výživě, dále v podávání hormonu somatostatinu a jeho derivátů, jako je ocreotid. Úspěšnost konzervativní terapie dosahuje 75 %, a to zejména v případech malých chylothoraxů. Pokud je ztráta větší než 1000 ml/den, je úspěšnost konzervativní léčby nízká, tj. kolem 35 % [2,6]. V případech selhání konzervativní terapie je indikována intervenční léčba. Intervenční terapie chylothoraxu zahrnuje chirurgické postupy a radiointervenční miniivazivní metody. V současnosti je chirurgickou metodou volby videothorakoskopie s ligaci ductus thoracicus. Thorakotomický přístup je využíván jen v případě, že chylothorax je komplikací primárně otevřené operace [2,8]. Další operační metody jsou prováděny ojediněle a jedná se o pleurektomii, chemickou pleurodézu, vytvoření lymfovenózní spojky nebo pleuroperitoneálniho shuntu [2]. Radiointervenční metody zahrnují provedení rentgenové lymfografie a následně antegrádní embolizace ductus thoracicus, retrográdní embolizace ductus thoracicus z transvenózního přístupu, nebo z transcervikální punkce ústí hrudního mízovodu, která může být provedena pod UZ kontrolou nebo skiaskopicky [9–11]. Při rtg lymfografii se aplikuje olejová kontrastní látka buď do vypreparované lymfatické cévy na noze (pedální lymfografie), anebo do lymfatické uzliny (intranodální lymfografie) [12]. Lymfografie má i terapeutický účinek, který byl opakovaně popsán v literatuře. Uvádí se, že samotná pedální lymfografie vede k zástavě chylothoraxu v 51–70 % a intranodální lymfografie v 33–100 % [12]. Další nechirurgickou možností zástavy tvorby chylothoraxu je embolizace ductus thoracicus. Embolizace ductus thoracicus z antegrádního přístupu navazuje na lymfografii, při které se zobrazí cisterna chyli. První zkušenosti byly popsány v roce 1998 Constantinem Copem [9]. Vlastní výkon probíhá tak, že se cisterna chyli, zobrazená při lymfografii, punktuje Chiba jehlou průměru 21–22 G. Po punkci cisterna chyli se přes jehlu zavede do ductus thoracicus vodič průměru 0,014–0,018 palce. Po vodiči je pak do ductus thoracicus zaveden mikrokatétr, přes který se zobrazí hrudní mízovod aplikací vodní jodové kontrastní látky, následně je provedena embolizace. Embolizace se provádí pomocí mikrospirál, tkáňového lepidla anebo kombinací daných embolizačních materiálů. Z tkáňových lepidel je nejčastěji používáno akrylátové lepidlo, které se míchá s olejovou kontrastní látkou lipiodol. Poměr akrylátového lepidla k olejové kontrastní látce je nejčastěji 1 : 1 – 1 : 5. Komplikace embolizace ductus thoracicus z transabdominálního přístupu zahrnují komplikace spojené s lymfografií a komplikace vázané na punkci ductus thoracicus a jeho embolizaci. V roce 2018 byl publikován přehledový článek s metaanalýzou lymfatických intervencí při léčbě chylothoraxu [13]. Do metaanalýzy bylo zahrnuto celkem 9 studií se 407 pacienty. Pedální lymfangiografii podstoupilo 88,7 % nemocných a intranodální 11,3 %. Komplikace lymfografie se vyskytly v 2,6 % pacientů (9/407). Embolizaci ductus thoracicus se podařilo provést v 62,9 % nemocných. Klinický úspěch byl u 79,5 % pacientů, u kterých byla provedena embolizace. V případech neúspěšné punkce byla provedena tzv. disrupce ductus thoracicus. Zástava tvorby chylothoraxu se v zahrnutých studiích pohybovala v rozmezí 38,7–75,7 %. Komplikace embolizace se v této metaanalýze vyskytly v 5,1 %, z toho závažné v 1 %. U závažných komplikací se jednalo o biliární leak do peritoneální dutiny. Jako nezávažné komplikace byly popsány embolizace do plic, fragmentace vodiče, embolizace do portálního řečiště a perihepatální hematom [13]. Jak bylo zmíněno v popisu techniky daného výkonu, k punkci se používá tenká Chiba jehla a punkce je naváděna skiaskopicky. Schild ve své práci z roku 2020 analyzoval CT vyšetření provedené do 1 hodiny po embolizaci ductus thoracicus se zaměřením na lokalizaci tkáňového lepidla [14]. V souboru 35 pacientů popsal 106 struktur, ve kterých byly diagnostikovány zbytky embolizačního materiálu. Všichni pacienti měli po výkonu mírnou bolest v epigastriu. Celkem se komplikace vyskytly u 4 pacientů, z toho 2× se jednalo o významnou komplikaci. Klinicky a laboratorně se projevila jedna punkce slinivky pankreatitidou a punkce žlučníku vznikem biliární peritonitidy s nutností provedení cholecystektomie. Z dané práce je zřejmé, že punkce orgánů tenkou jehlou nevede k významnému výskytu komplikací [14]. Chirurgické postupy léčby chylothoraxu jsou v České republice běžně dostupné, doposud však nebyla antegrádní embolizace ductus thoracicus v české literatuře publikována [2–4]. V našich podmínkách by měla být embolizace ductus thoracicus primárně určena pro pacienty, u kterých selhal chirurgický výkon (ligace) anebo kteří jsou v horší fyzické kondici a chirurgický výkon je u nich nepřiměřeně rizikový. Na našem pracovišti lymfografii olejovou kontrastní látkou provádíme pouze z terapeutické indikace od roku 2015. Do srpna 2022 jsme provedli celkem 17 lymfografií u 13 pacientů. Intranodální lymfografii provádíme od roku 2020 a embolizaci ductus thoracicus od března 2022. Doposud jsme ductus thoracicus embolizovali u 2 pacientů.
ZÁVĚR
Embolizace ductus thoracicus antegrádním přístupem z transabdominálního nápichu cisterna chyli je miniivazivní metoda léčby chylothoraxu, která je možnou alternativou chirurgického podvazu ductus thoracicus. Cisternu chyli lze zobrazit pomocí intranodální lymfografie, která je výrazným zjednodušením a zkrácením klasické pedální olejové kontrastní lymfografie.
Tento výstup vznikl v rámci programu Cooperatio, vědní oblasti DIAG.
Konflikt zájmů
Autor článku prohlašuje, že není v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise, s výjimkou kongresových abstrakt a doporučených postupů.
MUDr. Vendelín Chovanec, Ph.D.
Radiologická klinika FN HK
a LF UK v Hradci Králové
e-mail: vendelin.chovanec@fnhk.cz
ORCID: 0000-0001-9860-3616Rozhl Chir. 2022;101 : 607–611
Sources
1. Pospiskova J, Smolej L, Belada D, et al. Experiences in the treatment of refractory chylothorax associated with lymphoproliferative disorders. Orphanet J Rare Dis. 2019;14(1):9. doi:10.1186/s13023-018 - 0991-3.
2. Szkorupa M a kol. Chylothorax: průvodce pro chirurgy, pediatry a interní obory. 1. vydání, Praha, Maxdorf Jessenius 2022 : 118.
3. Szkorupa M. Pooperační chylothorax – souhrnné sdělení. Rozhledy v chirurgii 2020;99(10):427–437. doi: 10.33699/ PIS.2020.99.10.427-437.
4. Šafánek J, Špidlen V, Vodička J, et al. Chylotorax. Kazuistika a literární přehled. Rozhledy v chirurgii 2006;85(12):604–608.
5. Chovanec V, Bělobrádek Z, Žák P, et al. Intranodální lymfografie. Česká radiologie 2022;76(2):577–583.
6. Alejandre-Lafont E, Krompiec C, Rau WS, et al. Effectiveness of therapeutic lymphography on lymphatic leakage. Acta Radiol. 2011;52(3):305–311. doi:10.1258/ ar.2010.090356.
7. Pieper CC. Nodal and pedal MR lymphangiography of the central lymphatic system: echniques and applications. Semin Intervent Radiol. 2020;37(3):250–262. doi:10.1055/s-0040-1713442.
8. Arshava EV, Parekh KR. Thoracoscopic thoracic duct ligation: How I each it. Ann Thorac Surg. 2020 May;109(5):1330–1334. doi:10.1016/j.athoracsur.2020.01.004. Epub 2020, Feb 6. PMID: 32035916.
9. Cope C. Diagnosis and treatment of postoperative chyle leakage via percutaneous transabdominal catheterization of the cisterna chyli: a preliminary study. J Vasc Interv Radiol. 1998;9(5):727–7234. doi: 10.1016/s1051-0443(98)70382-3.
10. Crawford D, Guevara CJ, Kim SK. Thoracic duct embolization using transabdominal antegrade and transcervical retrograde access J Vasc Interv Radiol. 2022 Aug 23;S1051–0443(22)011575. doi:10.1016/j. jvir.2022.08.022.
11. Kariya S, Nakatani M, Ueno Y, et al. Transvenous retrograde thoracic ductography: initial experience with 13 consecutive cases. Cardiovasc Intervent Radiol. 2018;41(3):406–414. doi:10.1007/s00270 - 017-1814-y.
12. Sommer CM, Pieper CC, Itkin M, et al. Conventional lymphangiography (CL) in the management of postoperative lymphatic leakage (PLL): A systematic review. Rofo. 2020;192(11):1025–1035. doi:10.1055/a-1131-7889.
13. Kim PH, Tsauo J, Shin JH. Lymphatic interventions for chylothorax: A systematic eview and meta-analysis. J Vasc Interv Radiol. 2018;29(2):194–202,e4. doi:10.1016/j.jvir.2017.10.006.
14. Schild HH, Pieper CC. Where have all the punctures gone? An analysis of thoracic duct embolizations. J Vasc Interv Radiol. 2020;31(1):74–79. doi:10.1016/j. jvir.2019.09.012.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2022 Issue 12-
All articles in this issue
- Experimentální chirurgie
- Umělé neuronové sítě a počítačové vidění v medicíně a chirurgii
- Tepny hlavy a krku prasete domácího z pohledu zobrazovacích metod a experimentální chirurgie
- Permanentní žilní přístup v experimentální chirurgii – naše zkušenosti
- Chirurgie v době koronavirové
- Zavedení in vivo modelů karcinomu pankreatu pro studium nových terapeutických režimů
- Konfokální laserová endomikroskopie v pooperačním hodnocení perfuze kolorektální anastomózy – experimentální studie
- Experimentální chirurgie jako součást vývoje degradabilních biomateriálů v kardiovaskulární chirurgii
- Léčba chylothoraxu embolizací hrudního mízovodu
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Tepny hlavy a krku prasete domácího z pohledu zobrazovacích metod a experimentální chirurgie
- Léčba chylothoraxu embolizací hrudního mízovodu
- Zavedení in vivo modelů karcinomu pankreatu pro studium nových terapeutických režimů
- Permanentní žilní přístup v experimentální chirurgii – naše zkušenosti
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

