-
Medical journals
- Career
Nová strategie chirurgické léčby mnohočetného nádorového postižení jater – ALPPS
Authors: M. Peteja 1,2,3; L. Martínek 2,3; M. Mazur 2,3; P. Vávra 2,3; P. Zonča 2,3; V. Janout 1
Authors‘ workplace: Ústav epidemiologie a ochrany veřejného zdraví, Lékařská fakulta Ostravské univerzity v Ostravě vedoucí ústavu: Prof. MUDr. V. Janout, CSc. 1; Chirurgická klinika, FN Ostrava, přednosta: Doc. MUDr. P. Zonča, Ph. D., FRCS 2; Katedra chirurgických oborů, Lékařská fakulta Ostravské univerzity v Ostravě vedoucí katedry: Doc. MUDr. P. Zonča, Ph. D., FRCS 3
Published in: Rozhl. Chir., 2014, roč. 93, č. 6, s. 301-306.
Category: Review
Overview
Úvod:
Cílem této práce je formou souhrnného sdělení představit techniku resekce jater při mnohočetném nádorovém postižení (Associating Liver Partition and Portal Vein Ligation for Staged Hepatectomy – ALPPS) a prezentovat její aktuální výsledky.Materiál a metodika:
Systematický přehled literatury databáze PubMed pro klíčová slova ALPPS nebo stage liver resection. Inkluzním kritériem byly randomizované nebo kohortové studie. Exkluzním kritériem byly kazuistiky. Primárním cílem studie bylo vyhodnocení potenciálu této metody vedoucí k hypertrofii jaterní tkáně. Sekundárními cíli byla analýza morbidity a mortality.Výsledky:
Po zadání klíčových slov do databáze PubMed s přihlédnutím k inkluzním a exkluzním kritériím bylo identifikováno 6 kohortových studií, které hodnotily celkem 96 pacientů. Nebyla nalezena žádná prospektivní randomizovaná studie. Analýzou výsledků jednotlivých prací jsme zjistili, že hypertrofie jaterního parenchymu se pohybovala v rozmezí 74–87 %. Morbidita publikovaných souborů byla 53–71 %, mortalita 0–13 %.Závěr:
Přes aktuálně vysokou morbiditu i mortalitu se ALPPS technika v současnosti jeví jako slibná technika pro vybranou skupinu pacientů s mnohočetným nádorovým postižením jater. Dlouhodobé výsledky však zatím nejsou ještě dostupné.Klíčová slova:
ALPPS – hypertrofie jater – ligace portální žíly – resekce jater – mnohočetné jaterní metastázyÚvod
Není to tak dávno, co metastatické postižení jater bylo považováno za známku inoperability primárního ložiska. Jaterní chirurgie v dnešním pojetí má počátek v roce 1967, kdy Flanagan a Foster poprvé provedli resekci metastáz jater. Dalším výrazným zlomem byl začátek 80. let, kdy vznikla nomenklatura anatomických resekcí a bylo zavedeno peroperační ultrazvukové vyšetření jater (Bismuth a Makuuhi 1988) [1]. V té době byla Makuuhim a spol. provedena první portální embolizace (PVE) s cílem indukování kompenzační hypertrofie kontralaterálního laloku jater pro možnost resekce vícečetných metastatických ložisek [2]. Zhruba o dekádu později Adam a spol. představili dvouetapovou resekci jater spojenou s jejich regenerací/hypertrofií v intervalu mezi jednotlivými operačními kroky [3]. Zanedlouho po nich Jaeck a spol. zkombinovali embolizaci pravé větve portální žíly spolu s odstraněním ložisek z levého laloku [4]. Tento postup se stal základem pro novou strategii kombinující pravostrannou PVE s neanatomickou resekcí levého jaterního laloku [2,5]. Metoda nebyla ve své podstatě špatná, ale měla a má jeden závažný hendikep. Hypertrofie jaterního parenchymu si vyžádá časový interval dlouhý až 8 týdnů, v průběhu kterého často dochází k recidivám, resp. k nádorové progresi, která znemožní druhý krok resekce u 20–30 % pacientů [6,7]. V té době již začalo být jasné, že důležitým faktorem resekability jaterních lézí není jen objem ponechané tkáně, ale i její kvalita, na níž závisí funkčnost. Techniku dvoudobé resekce, kdy v prvním kroku dojde k podvázání portální větve pro postiženější jaterní lalok a současně ke splittingu jater, poprvé popsal Schlitt v Regensburgu [5,8,9]. Zdá se, že tato metoda, nazvaná ALPPS – Associating Liver Partition and Portal Vein Ligation for Staged Hepatectomy, má potenciál ukázat nový směr, kterým se bude v budoucnu ubírat jaterní chirurgie. Je to metoda nová, zatím s velmi omezenými statistickými výsledky vzhledem ke krátkému intervalu a malým souborům. Tato práce si klade za cíl představit tuto slibnou techniku české a slovenské chirurgické veřejnosti.
Materiál a metodika
Při sestavování souhrnného sdělení jsme vycházeli z elektronické databáze PubMed, kde jsme po zadání klíčových slov „ALPPS“ a „stage liver resection“ získali soubor prací, které se této problematice věnují. Pro analýzu dat jsme vyloučili jednotlivé kazuistiky a hodnotili jen ucelené soubory pacientů.
Indikace a kontraindikace
Indikací k ALPPS je pacient s hraničně operabilním, resp. inoperabilním lokálně pokročilým mnohočetným nádorovým postižením jater různé etiologie, jehož index FLR/TLV (future liver remnant/total liver volume) je menší než 30 % u zdravé tkáně, resp. 40 % u postižených jater [5,10]. Může se jednat o metastázy kolorektálního karcinomu, karcinomu prsu, Klatskinův tumor (ALPPS může být vhodné pro typ Bismuth IV), karcinom žlučníku, cholangiokarcinom, hepatocelulární karcinom (HCC) nebo neuroendokrinní tumor [5,6]. Kontraindikací jsou zejména lokálně inoperabilní metastázy v laloku, který by měl zůstat po ukončení druhé etapy výkonu, inoperabilní metastázy v extrahepatální lokalitě, závažná portální hypertenze, inoperabilní primární nádor, vysoké anesteziologické riziko a nemožnost dosáhnout R0 resekce [5,11]. Nejednoznačný názor zatím panuje ohledně cholestázy a biliární drenáže. Dle některých autorů je pacient po biliární drenáži s cholestázou jater a sníženou regenerační schopností kontraindikován k ALPPS pro neúměrně zvýšené riziko bakteriemie, která dle četných zkušeností skoro nereaguje na antibiotickou léčbu [5,11]. Indikační kritéria momentálně procházejí podrobným hodnocením na základě zkušeností různých pracovišť s cílem vyselektovat skupinu pacientů, pro které je tato metoda přínosem [12,13].
Předoperační příprava
Předoperační příprava pacienta probíhá dle standardního protokolu konkrétního centra hepatální chirurgie pro resekční výkony na játrech. Je nutné zvážení jak kardiálního, tak i respiračního a nefrologického rizika, přičemž posledně jmenované není absolutní kontraindikací výkonu. Kromě standardních laboratorních odběrů odebíráme nádorové markery: AFP, CEA,CA19-9. PET-CT zatím není obligátně doporučeno, ale kromě primární diagnózy HCC by mělo být provedeno k vyloučení extrahepatických metastáz [14].
Operační postup
Fáze 1
Jako přístup do dutiny břišní se volí oboustranný subkostální řez rozšířený směrem k processus xyphoideus – tzv. Mercedes. Výkon začíná peroperačním ultrazvukovým vyšetřením (USG) pro upřesnění polohy nádorových ložisek a posouzení jejich počtu, velikosti, lokalizace hlavně v oblasti budoucího ponechaného jaterního parenchymu. Výkon začíná buď cholecystektomií [6], nebo radikální lymfadenektomií hepatoduodenálního ligamenta a oblasti a. hepatica communis [5]. Lymfadenektomie je prováděna jak z onkologického hlediska, tak i z důvodu ujasnění anatomických poměrů. Po úplné mobilizaci pravého laloku jater následuje podvázání a přerušení portální větve pro pravý lalok a I. segment. Retrohepatické žilní spojky do v. cava inferior jsou rovněž podvázány a přerušeny. Hepatické žíly, tepny a žlučovody se označí barevnými závěsy pro lehčí identifikaci při druhém kroku (Obr. 1) [5,6]. Při preparaci v jaterním hilu je klíčové vyhnout se poranění tepenného zásobení pro lalok určený k pozdějšímu odstranění, protože po podvazu portální větve je tepna jediným zdrojem jak nutrice, tak přísunu kyslíku, a tudíž po jejím poranění může dojít k nekróze celého laloku [6]. Dalším krokem je splitting jater. Resekční linie je buď Rex-Cantlieova linie při pravostranné hepatektomii, nebo rozhraní segmentů podle výkonu – pravá strana lig. falciforme při rozšířené pravostranné hepatektomii (segmenty 4–8+ev. segment 1) nebo hranice segmentů 6–7 při rozšířené levostranné hepatektomii (1–5+segment 8). Splitting se dělá až po úroveň dolní duté žíly (Obr. 2). Nejčastěji je použit ultrazvukový disektor (CUSA) v kombinaci s koagulací, argon-plazma koagulací nebo ultrazvukovým (harmonickým) skalpelem. Lze použít i disekci vodním paprskem (WaterJet) nebo koagulaci typu LigaSure [5,6]. Obecně převládá názor, že důležitější než typ nástroje je míra zkušeností chirurga [15]. Následuje metastazektomie z „future liver remnant“ (FLR) – budoucí ponechaný jaterní parenchym s dostatečným bezpečnostním lemem. Po této fázi některá pracoviště vkládají vyřazenou část jater do sáčku, do kterého vloží drén a zavážou. Jiná používají jen polyetylenové pásky do resekční linie (Obr. 3). Sáček má výhodu v zabránění vzniku srůstů a navíc ve druhé době ho lze odstranit i se sekretem. Nevýhodou je cizí materiál, který vytváří predispozici bakteriální kolonizace [5]. Objevují se i první zprávy o využití laparoskopického přístupu ve snaze zabránit vzniku srůstů [16]. Na konci první fáze je vhodné provést ultrazvukovou kontrolu portálních větví, protože zadní portální větev je v určitém počtu případů natolik velká, že může imitovat pravou portální žílu. Pokud by nebyla podvázána, selhal by proces hypertrofie. Na závěr se provádí zkouška těsnosti žlučového stromu v resekční linii kanylou zavedenou do d. cysticus [5,6,11]. Drény se vkládají do pravého subhepatického prostoru a do oblasti resekční linie jater [5,6,11].
Image 1. Označení větví VCI modrým vláknem (šipka) Fig. 1: Marking IVC branches with blue thread (black arrow) 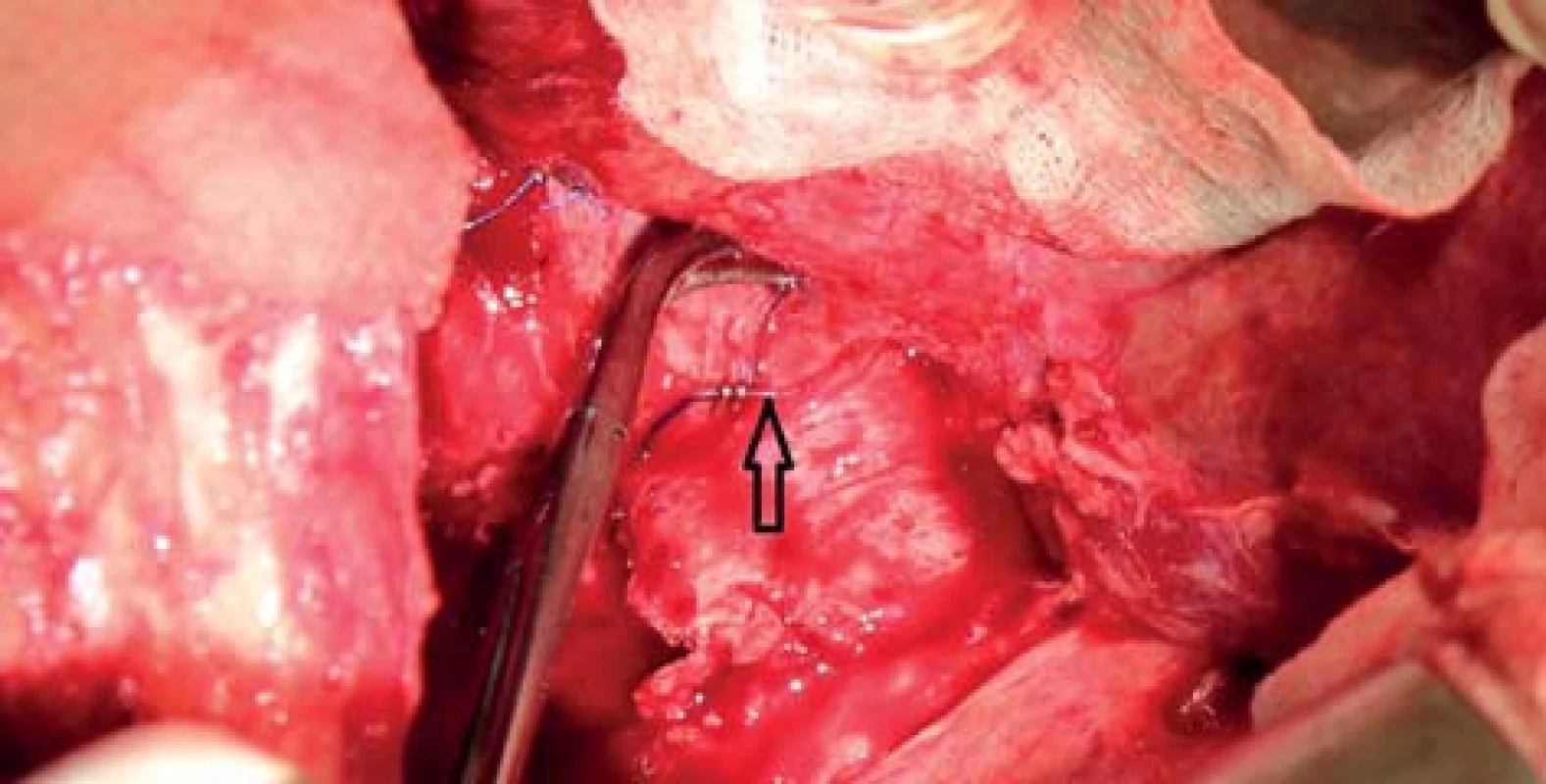
Image 2. Rozdělené jaterní laloky Fig. 2: Split liver lobes 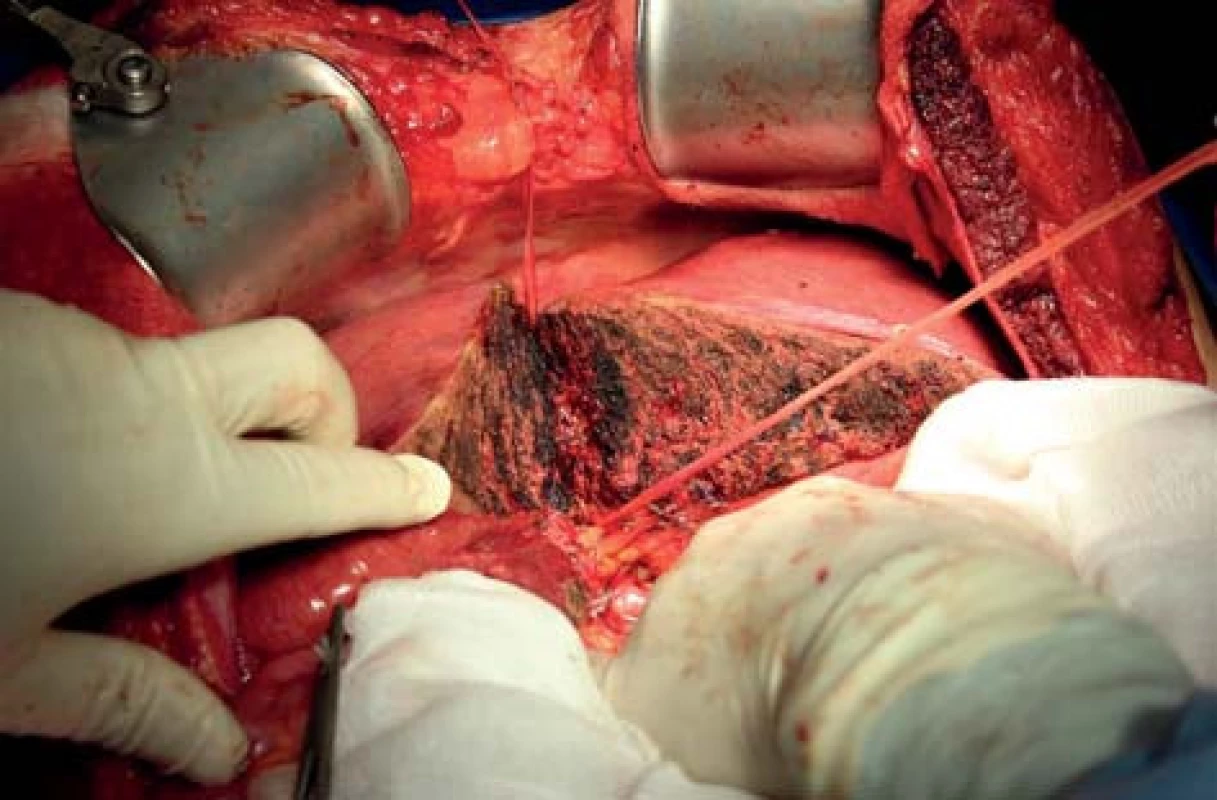
Image 3. Rozdělené laloky s vloženými polyetylénovými páskami Fig. 3: Split lobes with inserted polyethylene strips 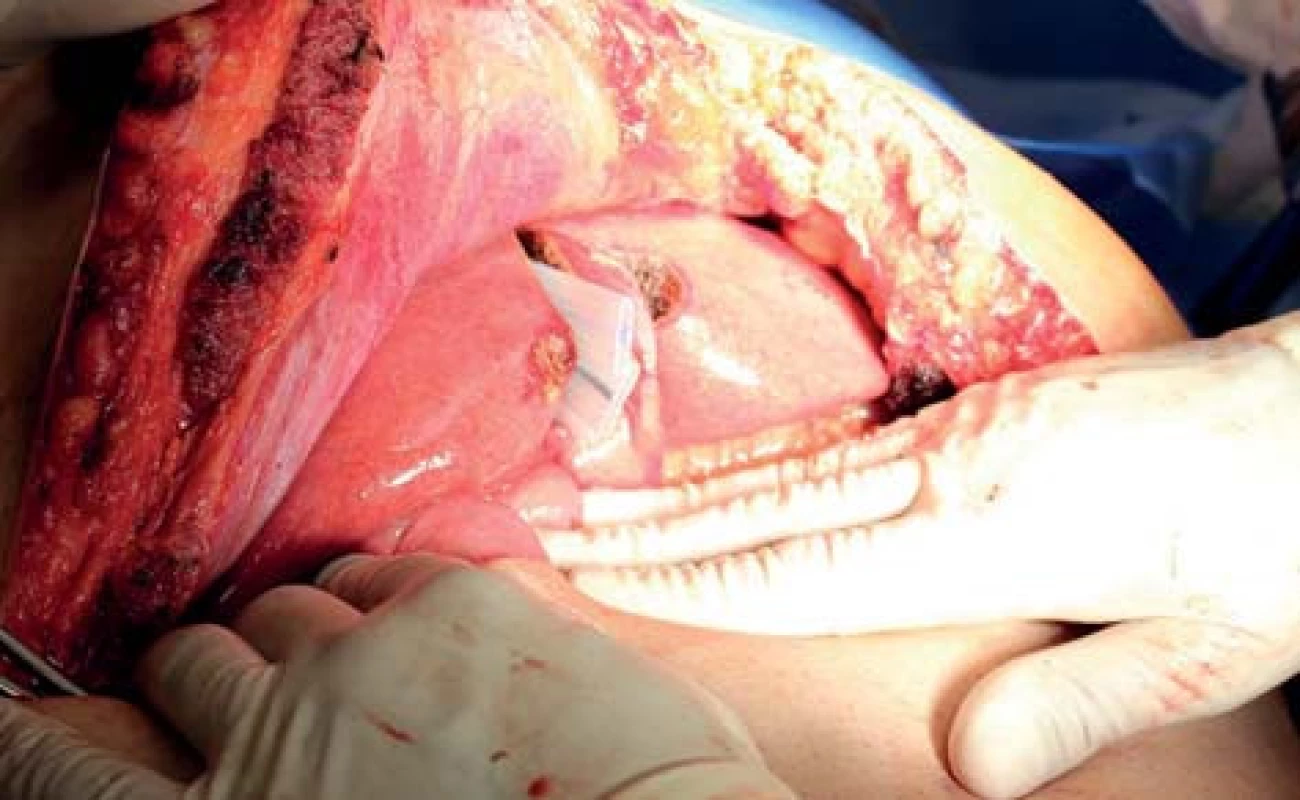
Fáze 2
Vzhledem k riziku bakteriální infekce, cizího materiálu v dutině břišní, jakož i ischemické tkáně je indikováno ATB krytí po celou dobu mezi první a druhou fází výkonu. Do druhé fáze většina autorů upřednostňuje kombinaci parenterální a enterální výživy. Po druhé fázi je preferována pouze enterální výživa jako prevence metabolického přetížení FLR [5]. 6–7. den po druhé fázi se provádí volumometrie počítačovou tomografií nebo magnetickou rezonancí. V případě požadovaného stupně hypertrofie a dobré pacientovy kondice následuje další krok (Obr. 4). Stejným přístupem jako u předchozí operace se proniká do dutiny břišní. Je vhodné odebrání bakteriálních stěrů. Vzhledem k určité změně anatomických poměrů (zvětšující se FLR může dislokovat jiné struktury nestandardním způsobem) je nutná zvýšená opatrnost při preparaci [3]. Postižený lalok se odstraňuje vcelku, vaskulární i biliární struktury doporučuje většina autorů přerušovat vaskulárními staplery (Obr. 5) [5]. Po odstranění laloku se vloží drény do stejných pozic jako u prvního kroku – pravé subfrenium a oblast resekční linie [5,6].
Image 4. CT obraz hypertrofovaných segmentů S2 a S3 (šipka) Fig. 4: CT scan with hypertrophy of S2 and S3 segments (black arrow) 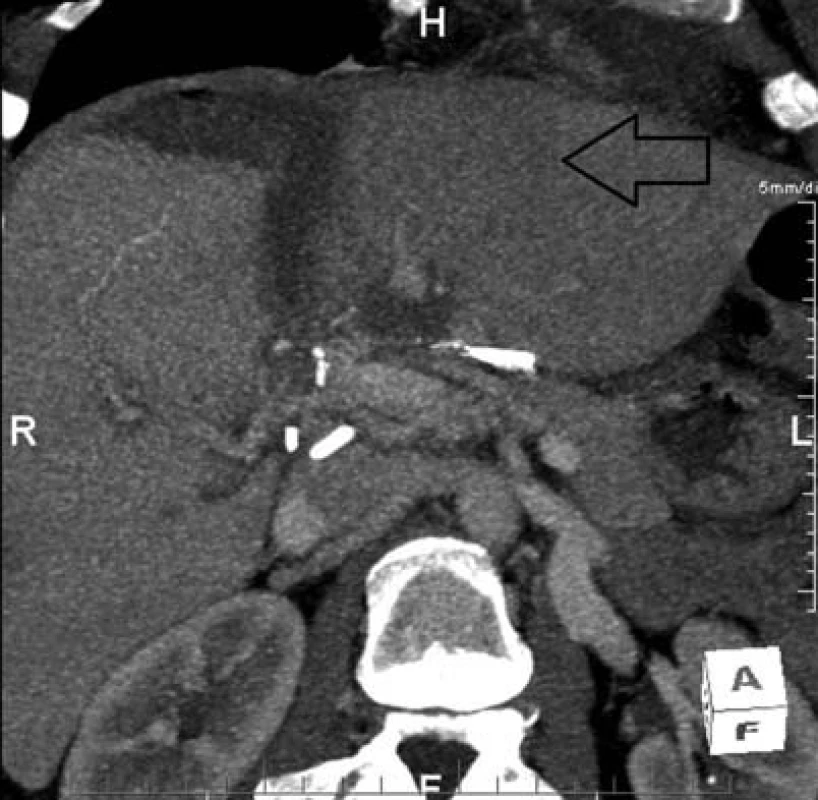
Image 5. Nakládání vaskulárního stapleru na pravou jaterní žílu Fig. 5: Division of right liver vein with vascular stapler 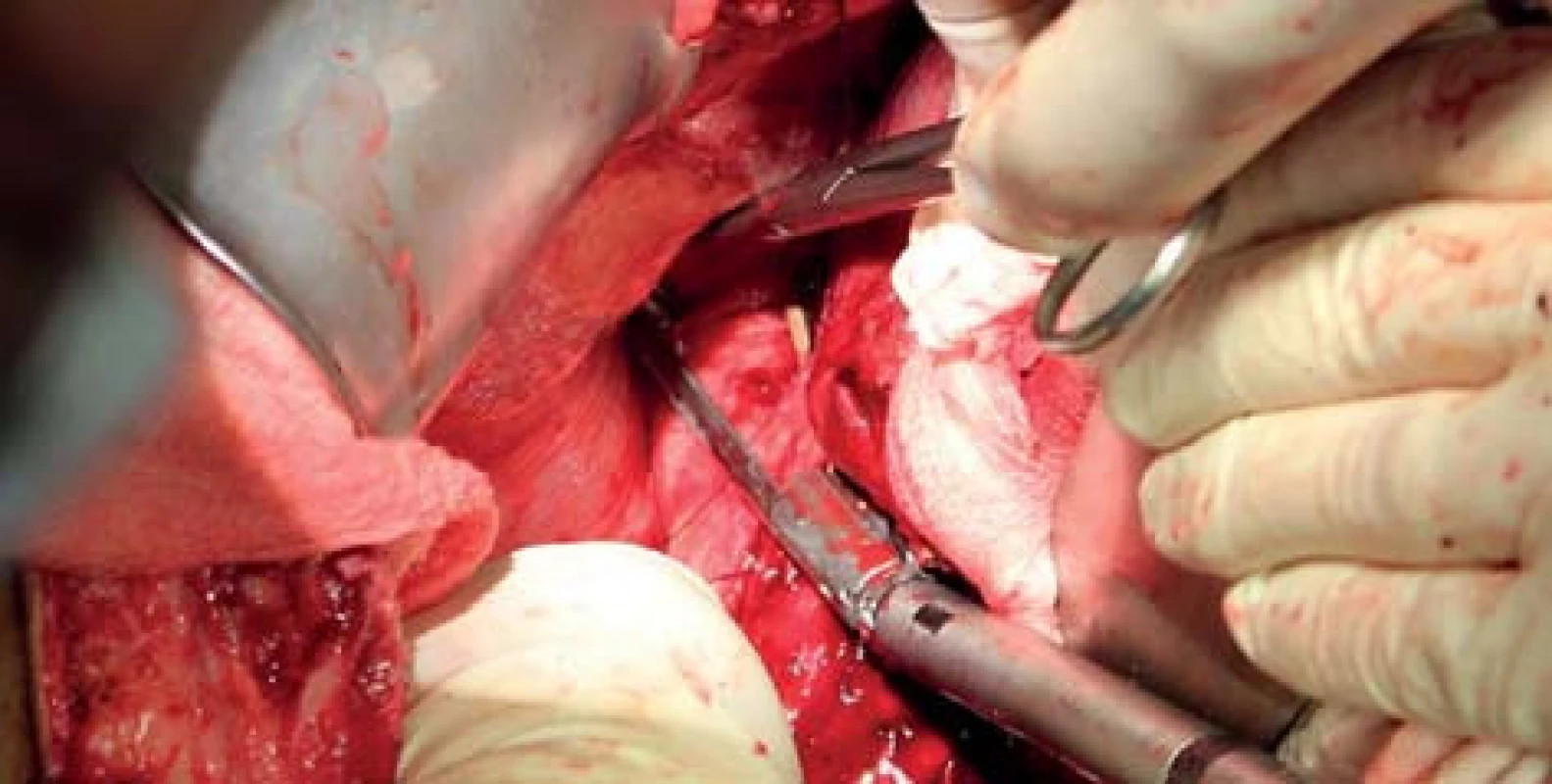
Výsledky
Počet pacientů, kteří podstoupili výkon ALPPS, se blíží ve světě k číslu 300. Mezi největší soubory patří soubor prof. Schnitzbauera, který vznikl spojením pacientů z 5 velkých německých pracovišť – Regensburg, Tübingen, Mainz, Göttingen a Giessen [9,17], dále soubor prof. Claviena z Curychu [2,8] a v neposlední řadě i soubor prof. de Santibanese z Buenos Aires [2,5,8,18]. Soubor prof. Claviena zatím nemá oficiálně zveřejněné definitivní výsledky, protože se jedná o randomizovanou mezinárodní studii se zapojením více pracovišť po celém světě [8]. Soubor prof. Schnitzbauera byl první ucelenou skupinou pacientů s proběhlou ALPPS operací. Šlo o 25 pacientů, z toho 9 pacientů s primární jaterní malignitou (hepatocelulární karcinom, cholangiokarcinom, karcinom žlučníku, maligní hemangioendoteliom) a 16 pacientů se sekundárním, metastatickým postižením (kolorektální karcinom, karcinom ovaria a karcinom žaludku). Předoperační objem FLR kolísal v rozmezí 192–444 ml (průměr 310 ml) a po průměrné době 9 dnů (5–28) došlo ke zvětšení objemu na 536 ml (273–881 ml), tudíž nárůst o 73 % (21–192 %). Pooperační morbidita činila 68 % a hospitalizační mortalita byla 12 % [9]. Soubor prof. de Santibanese obnášel 15 pacientů, kteří podstoupili ALPPS. I tady je popsán nárůst objemu o 78,4 %, s morbiditou 53 % a mortalitou 0 % [5]. V poslední době byl ještě prezentován brazilský soubor autorů Torres a kol. s 39 pacienty [19] a německé soubory autorů Jun Lia (9 pacientů) a Knoefela (7 pacientů) [6,11]. Skutečně mikrosouborem je soubor 3 pacientů vyjmutých z obrovské multicentrické studie resekcí jaterních metastáz vedené prof. Clavienem a prof. de Santibanesem. Tento soubor je v podstatě jenom soupis case reportů, protože při počtu 3 pacientů nelze statisticky hodnotit výsledky [20]. Průměrný věk pacientů a interval mezi operacemi dokumentuje Tab. 1, změny FLR ukazuje Tab. 2, morbidita a mortalita jsou shrnuty v Tab. 3. Bohužel se jedná o nehomogenní soubory vylučující možnost analýzy získaných dat ve smyslu metaanalýzy. Dlouhodobé výsledky chybějí, protože metoda se zatím používá velmi krátkou dobu [21].
Table 1. Soubor pacientů Tab. 1: Patient group 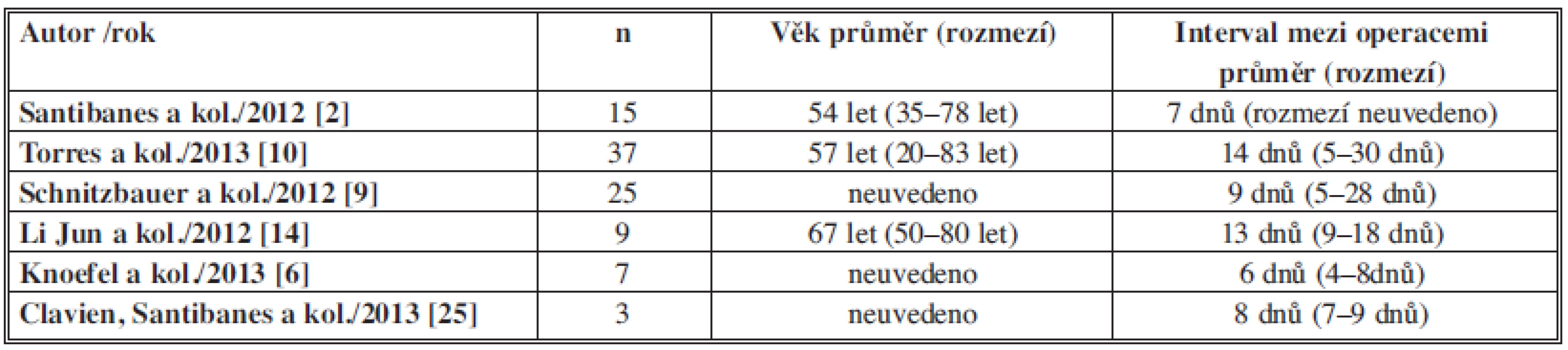
Table 2. Změny objemu rezidua jater Tab. 2: Changes in FLR volume 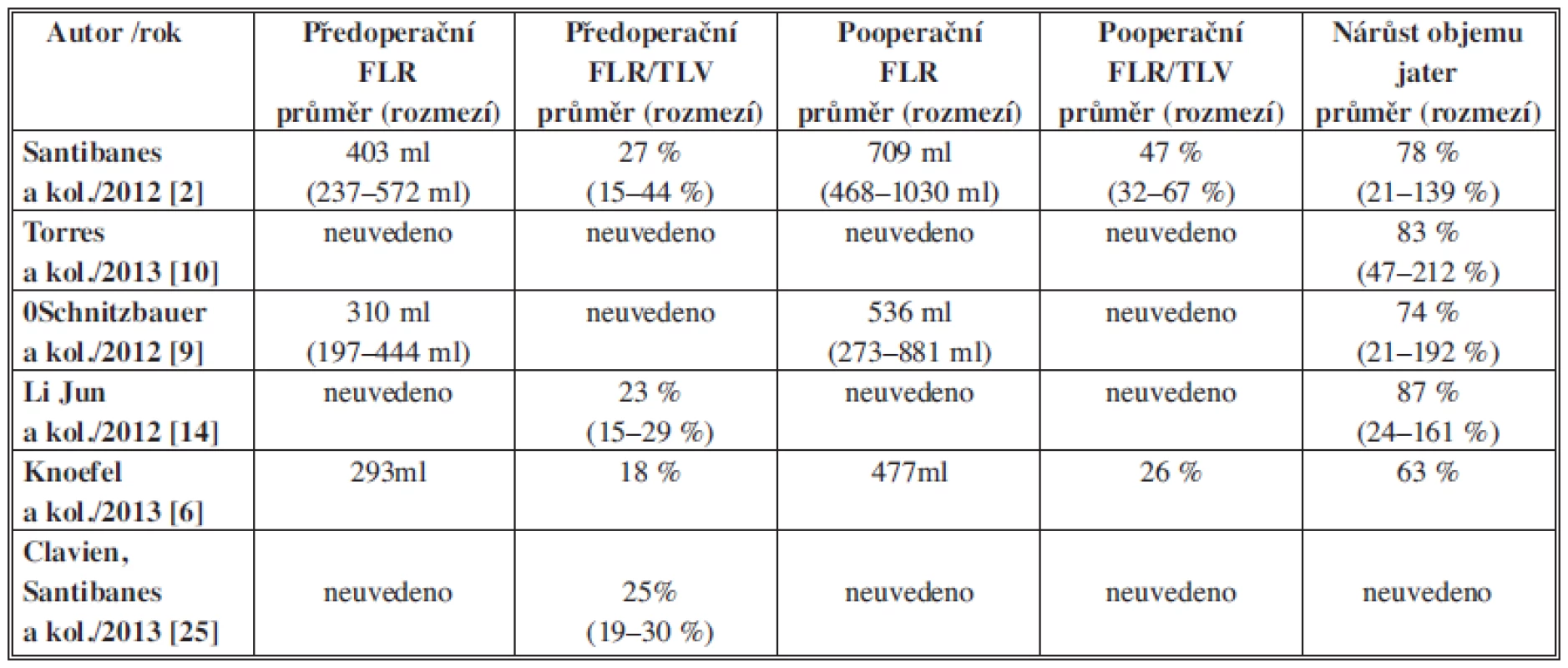
Table 3. Morbidita, mortalita Tab. 3: Morbidity, mortality 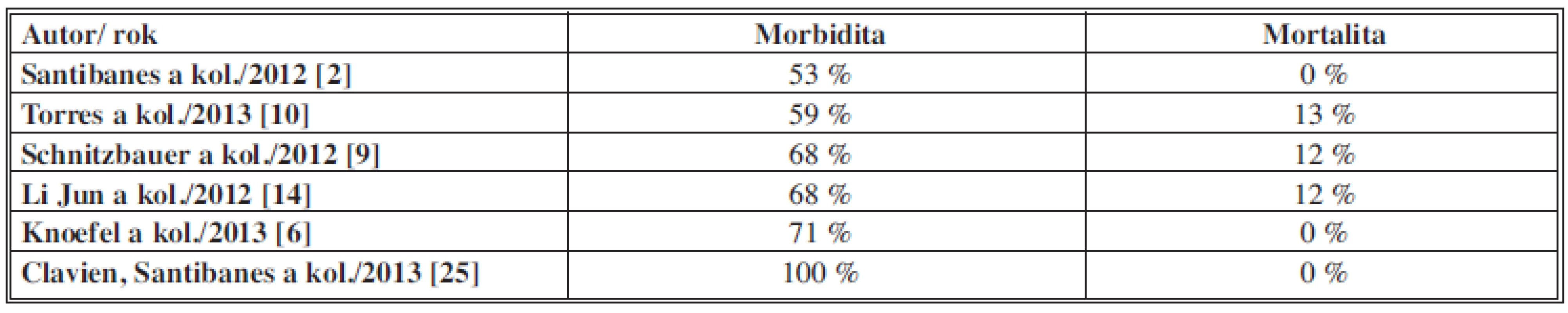
Diskuze
Dle současných onkologických doporučených postupů je jediným kurativním řešením maligních jaterních nádorů chirurgická resekce [5,10,18,22,23]. Bohužel v době diagnostiky nádorového postižení má již velké procento pacientů mnohočetná ložiska v obou jaterních lalocích [5]. ALPPS je metoda založená na principu hypertrofie jaterního parenchymu indukované podvazem portální větve pro lalok, který má být v budoucnu odstraněn. Tento lalok je v období několika dní vyživován jen arteriální krví a jako kompenzace tohoto faktu dochází k hypertrofii druhého laloku, který má v budoucnu zůstat. Limitujícím faktorem resekce je tzv. ponechaná jaterní tkáň (FLR-future liver remnant), protože nejtěžší pooperační komplikací jaterních resekcí je jaterní selhání s mortalitou kolem 32 % [18]. Z hlediska posouzení množství ponechané jaterní tkáně jsou důležité 2 ukazatele: FLR/TLV (total liver volume), který určuje podíl ponechané tkáně k celkovému objemu zdravých jater, a FLR/BW (body weight) pro určení poměru váhy ponechané tkáně k tělesné hmotnosti pacienta. Hodnota FLR/TLV je nutná vyšší než 25–30 % u zdravých jater, respektive 35–40 % u jater významně steatotických, po chemoterapii nebo s cholestázou nad 50 mmol/l. Index FLR/BW musí být minimálně 0,5 u zdravých jater, resp. 0,8 u postižených [5,6,9,10,11,14,24,25]. Pooperační volumometrie by měla být prováděna i s denzitometrií k odlišení pooperačního edému od pravé hypertrofie jaterní tkáně. Při edému dochází k poklesu hustoty, zatímco po splittingu jater dochází dle dosavadních statistik k vzestupu hustoty parenchymu v rozmezí 80–120 HU [6]. Časový harmonogram dvoudobé resekce vychází z patofyziologického faktu, že po transekci jater in situ s podvazem portální větve pro nemocný lalok je denní přírůstek hmoty parenchymu 22 %/den proti 3 %/den po PVE [6]. Příčina tohoto jevu není zatím podrobně prozkoumána ani vysvětlena a diskutuje se možný vliv 4 faktorů: 1) ligace portální větve redistribuuje hepatotrofické látky do FLR [18,26], 2) rozdělení jater je významný traumatický impulz ke zvýšení regenerační aktivity, 3) ovlivnění portálního toku ve smyslu zvýšení průtoku větví pro FLR, 4) ponechaná patologická tkáň jater si vždycky zachovává nějakou metabolickou aktivitu, která je významným pomocným faktorem v období klíčového prvního týdne po první fázi resekce do doby, než FLR hypertrofuje do potřebné velikosti [5,18]. I když přesný patofyziologický mechanismus hypertrofie zatím není dopodrobna prozkoumán, je zjištěno, že ani předchozí radiologická embolizace portální větve nevede k „vyčerpání“ hypertrofického potenciálu jater [6]. Na první pohled je metoda embolizace a ligace stejná, přičemž ALPPS je zatížen vyšší morbiditou a mortalitou. Podle literárních údajů se morbidita pro ALPPS techniku pohybuje mezi 53–100 % a mortalita v rozmezí 0–13 % [2,6,9,11,20,22]. Tato vysoká morbidita je způsobená nejčastěji komplikacemi ze strany laparotomie, jako další časté příčiny pooperačních komplikací jsou v literatuře udávány ascites a biliární leak [8,9]. Když ale vezmeme v úvahu 30 % pacientů po embolizaci, kteří se nedostanou k druhé fázi hepatektomie pro progresi nádorového onemocnění v průběhu intervalu hypertrofie, je pohled na vysokou četnost pooperačních komplikací trošku jiný [6,27]. Celkově je metoda ALPPS postavená na dvoudobé resekci jater, přičemž však ligace portální větve zkrátila čas potřebný k hypertrofii na minimum. Splitting jater odstraňuje limitaci ligace, kterou se zdá být poměrně výrazná tvorba intrahepatálních porto-portálních neokolaterál snižujících účinnost portální ligatury v porovnání s embolizací, kde zmíněná indukce není tak výrazná [15,27]. V pooperačním období jsou pacienti kryti antibiotiky a vzhledem k ochraně jaterního parenchymu se v tomto období nepodává chemoterapeutická léčba. Ascites je korigován diuretiky a albuminem, který bývá obvykle substituován při poklesu plazmatické hladiny albuminu pod 30 g/l. V každém případě navzdory rychlé hypertrofii FLR je zatím metoda zatížena vysokým procentem komplikací, a proto se její použití zatím omezuje na multicentrické studie a registry [20].
Obrazová dokumentace této práce je pořízena z operací, které byly provedeny na pracovišti autora v rámci registrované studie ALPPS vedené prof. Clavienem v Curychu.
Závěr
Metoda ALPPS je metodou novou, rozvíjející se a jako taková se potýká s nadšením a důvěrou na jedné straně a skepticismem a odmítáním na straně druhé. Bezesporu je to metoda s příslibem šance do budoucna pro značné procento pacientů s nádorovým postižením jater. Zároveň je to ale metoda zatížená vysokou morbiditou a mortalitou, vyžadující dlouhodobé sledování a porovnávání diagnostických postupů, indikací, kontraindikací, operační strategie a v neposlední řadě hlavně monitoring a zhodnocení dlouhodobých výsledků tzv. high-volume center po celém světě.
Zkratky:
PVE – portal vein embolisation
ALPPS – Associating Liver Partition and Portal Vein Ligation for Staged Hepatectomy
FLR – future liver remnant
TLV – total liver volume
BW – body weight
HCC – hepatocelulární karcinom
USG – ultrasonografie
MUDr. Matúš Peteja
Chirurgická klinika FN Ostrava
17. listopadu 1790
708 52 Ostrava
e-mail: matus.peteja@fno.cz
Sources
1. Skalický T. Historie jaterní chirurgie. In: Skalický T, Třeška V, Šnajdauf J, Kala Z a kol. Hepato-pankreato-biliární chirurgie. Praha, Maxdorf 2011.
2. SantibaĖes E, Clavien PA. Playing Play-Doh to prevent postoperative liver failure: the „ALPPS“ approach. Ann Surg 2012; 255 : 415–7.
3. Adam, R, Laurent A, Azoulay D, Casting D, Bismuth H, et al. Two-stage hepatectomy: A planned strategy to treat irresectable liver tumors. Ann Surg 2000;232 : 777–785.
4. Jaeck D, Oussoultzoglou E, Rosso E, Greget M, Weber JC, et al. A two-stage hepatectomy procedure combined with portal vein embolization to achieve curative resection for initially unresectable multiple and bilobar colorectal liver metastases. Ann Surg 2004;240 : 1037–1051.
5. Alvarez FA, Ardiles V, Sanchez Claria R, Pekolj J, de SantibaĖes E. Associating liver partition and portal vein ligation for staged hepatectomy (ALPPS): Tips and tricks. J Gastrointest Surg 2013;17 : 814–821.
6. Knoefel WT, Gabor I, Rehders A, Alexander A, Krausch M, et al. In situ liver transection with portal vein ligation for rapid growth of the future liver remnant in two-stage liver resection. Br J Surg 2013;100 : 388–394.
7. Abulkhir A, Limongelli P, Healey AJ, Damrah O, Tait P, et al. Preoperative portal vein embolization for major liver resection: a meta-analysis. Ann Surg 2008;247 : 49–57.
8. www.alpps.net
9. Schnitzbauer AA, Lang SA, Goessmann H, Nadalin S, Baumgart J, et al. Right portal vein ligation combined with in situ splitting induces rapid left lateral liver lobe hypertrophy enabling two-staged extended right hepatic resection in small-for-size settings. Ann Surg 2012;255 : 405–414.
10. Loos M, Friess H. Is there new hope for patients with marginally resectable liver malignancies. World J Gastrointest Surg 2012;4 : 163–165.
11. Li J, Girotti P, Königsrainer I, Ladurner R, Königsrainer A, et al. ALPPS in Right Trisectionectomy: a Safe Procedure to Avoid Postoperative Liver Failure? J Gastrointest Surg 2013 [Epub ahead of print].
12. Andriani OC. Long-term results with associating liver partition and portal vein ligation for staged hepatectomy (ALPPS). Ann Surg 2012;256:e5; author reply e16–19.
13. Narita M, Oussoultzoglou E, Ikai I, Bachellier P, Jaeck D. Right portal vein ligation combined with in situ splitting induces rapid left lateral liver lobe hypertrophy enabling 2-staged extended right hepatic resection in small-for-size settings. Ann Surg 2012;256:e7–8; author reply e16–7.
14. Primrose JN. Surgery for colorectal liver metastases, BJC 2010;102:C1313–1318.
15. Jaeck D, et al. One or two-stage hepatectomy combined with portal vein emboilization for initially nonresectable colorectal metastase. Am Surg 2003;185 : 221–229
16. Machado MA, Makdissi FF, Surjan RC. Totally laparoscopic ALPPS is feasible and may be worthwhile. Ann Surg 2012;256:e13; author reply e16–9.
17. Aloia TA, Vauthey JN. Associating liver partition and portal vein ligation for staged hepatectomy (ALPPS): what is gained and what is lost? Ann Surg 2012;256:e9; author reply e16–9.
18. de SantibaĖes E, Alvarez FA, Ardiles V. How to avoid postoperative liver failure: a novel method. WJS 2012;36 : 125–128.
19. Torres OJG, et al. Associating liver partition and portal vein ligation for staged hepatectomy (ALPPS): the Brazilian experience. ABCD Arq Bras Cir Dig [online] 2013;26 : 40–43. Available from: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0102 -
20. Tschuor Ch, Sergeant G, Schadde E, Slankamenac K, Clavien PA, et. al. Salvage parenchymal liver transection for patients with insufficient volume increase after portal vein occlusion? An extension of the ALPPS approach. Europ J Surg Oncol 2013;39 : 1230–1235.
21. Jain HA, Bharathy KG, Negi SS. Associating liver partition and portal vein ligation for staged hepatectomy: will the morbidity of an additional surgery be outweighed by better patient outcomes in the long-term? Ann Surg 2012;256:e10; author reply e16–7.
22. Torres OJ, Moraes-Junior JM, Lima NC, Moraes AM. Associating liver partition and portal vein ligation for staged hepatectomy (ALPPS): a new approach in liver resections. Arq Bras Cir Dig 2012;25 : 290–292.
23. Maroulis I, Karavias DD, Karavias D. General principles of hepatectomy in colorectal liver metastases. Tech Coloproctol 2012;15:S13.
24. Cavaness KM, Doyle MB, Lin Y, Maynard E, Chapman WC. Using ALPPS to induce rapid liver hypertrophy in a patient with hepatic fibrosis and portal vein thrombosis. J Gastrointest Surg 2013;17 : 207–12.
25. Sala S, Ardiles V, Ulla M, Alvarez F, Pekolj J, et a. Our initial experience with ALPPS technique: encouraging results. Updates Surg 2012;64 : 167–72.
26. Yokoyama Y, Nagino M, Nimura Y. Mechanisms of hepatic regeneration following portal vein embolization and partial hepatectomy: a review. World J Surg 2007;31 : 367–374.
27. Robles R, et al. Comparative study of right portal vein ligation versus embolisation for induction of hypertrophy in two-steged hepatectomy for multiple bilateral colorectal liver metastases, Eur J Surg Oncol 2012; 38 : 586–593.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2014 Issue 6-
All articles in this issue
- Nová strategie chirurgické léčby mnohočetného nádorového postižení jater – ALPPS
- Studie morfologie r. descendens a. circumflexae femoris lateralis jako možné cévní náhrady pro rekonstrukci koronárního řečiště pomocí angio CT vyšetření
- Karcinom tlustého střeva – zhodnocení komplikací a rizik plánovaných resekčních výkonů
- Srovnání chirurgického bypassu a subintimální rekanalizace v léčbě kritické končetinové ischemie
- Primární volvulus tenkého střeva u mladého nemocného
- Kombinovaný chirurgický management infekce hemodialyzačního cévního přístupu bakteriologickým agens Clostridium perfringens
- Klostridiová myonekróza břišní stěny – kazuistika
- Základní principy diagnostiky a léčby sekundární peritonitidy – doporučení odborníků s podporou SIS
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Základní principy diagnostiky a léčby sekundární peritonitidy – doporučení odborníků s podporou SIS
- Primární volvulus tenkého střeva u mladého nemocného
- Klostridiová myonekróza břišní stěny – kazuistika
- Nová strategie chirurgické léčby mnohočetného nádorového postižení jater – ALPPS
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

