-
Medical journals
- Career
Poranění periferních nervů při laparoskopických operacích
Authors: L. Sákra; L. Kohoutek; E. Ehler 1; M. Košťál 2; M. Kanta 3
Authors‘ workplace: Chirurgická klinika, PKN a. s. a FZS Univerzita Pardubice, doc. MUDr. Jiří Šiller, Ph. D. ; Neurologická klinika PKN a. s. a FZS Univerzita Pardubice, doc. MUDr. Edvard Ehler, CSc. 1; Porodnicko-gynekologická klinika PKN a. s. a FZS Univerzita Pardubice, doc. MUDr. Milan Košťál, CSc. 2; Neurochirurgická klinika FN a LF UK Hradec Králové, přednosta: doc. MUDr. Svatopluk Řehák, CSc. 3
Published in: Rozhl. Chir., 2011, roč. 90, č. 4, s. 244-249.
Category: Monothematic special - Original
Overview
Laparoskopické operační přístupy převažují téměř u všech operačních výkonů. Proti klasickým přístupům jsou šetrnější pro většinu tkání. Přesto i po zvládnutí laparoskopické operační techniky dochází k iatrogenním lézím periferních nervů. Autoři předkládají přehled nejčastějších laparoskopických operací a výskyt lézí periferních nervů při jednotlivých operacích. Snaží se poukázat na situace vedoucí k těmto iatrogenním lézím, identifikovat příčiny poškození nervů a z nich pak vyvodit nutná preventivní opatření.
Klíčová slova:
laparoskopie – poranění periferních nervů – iatrogenní léze – preventivní opatřeníÚVOD
Laparoskopická operační technika je ve srovnání s klasickým operačním přístupem méně invazivní a šetrnější pro většinu tkání. Avšak i při laparoskopických přístupech dochází k poranění periferních nervů. I přes zvládnutí operační techniky se na výskytu lézí periferních nervů podílejí specifické anatomické poměry (např. v oblasti tříselného kanálu), četné abnormity průběhu periferních nervů, náchylnost periferních nervů (např. u diabetu), špatně přehledné operační pole i zkušenosti operatéra. Léze periferních nervů při operacích jsou iatrogenní léze, způsobené lékařem (či jiným zdravotnickým pracovníkem), a jsou v tomto smyslu hlášeny, mohou být předmětem stížnosti, soudního sporu i plnění pojišťovnou.
Vzhledem k závažnosti této problematiky i na podkladě našich zkušeností předkládáme současný přehled problematiky.
V břišní chirurgii došlo k širokému rozvoji laparoskopie a laparoskopických operačních metod. S narůstajícím počtem laparoskopií došlo k nárůstu počtu různě závažných komplikací. Jednou z typických komplikací laparoskopického přístupu je poranění periferních nervů. Poranění nervů břišní stěny je společné pro všechny břišní operace. Při průniku trokarem přes laterální část horní poloviny břišní stěny může dojít k poškození n. subcostalis (Th12), kaudálních interokostálních nervů (Th7-Th11) a ventrálních větví nn. thoracici (Th7-12). Při umístění trokaru v dolní části břišní stěny je nebezpečí poranění n. ilioinguinalis (L1 či L2) a iliohypogastricus (Th12-L1). Léze nervů břišní stěny se projevují bolestí (pásovitou s dalším vyzařováním), poruchou čití (hypestézie i s ostrůvky hyperestézie v dermatomu nervů) a chabou parézou daného segmentu břišní stěny. Paréza (chabá, s oslabením stěny břišní a při kontrakci s případným přetahováním středočárových struktur na zdravou stranu) břišní stěny se většinou klinicky neprojeví, vzhledem k plurisegmentální intervaci břišní stěny a k překrývání areálů jednotlivých nervů [1].
V celém souborů břišních operací u mnoha typů výkonů již po mnoho let zcela převažují laparaskopické přístupy (např. cholecystektomie). V současnosti také u celé řady dalších operací (inguinální hernioplastika, operace v oblasti jícnového hiátu) již také jednoznačně převažují laparoskopické přístupy. Laparoskopická operace je technicky dobře zvládnutelná, bezpečná, je menší poranění anatomických struktur, hospitalizace je kratší a hojení i doba vyřazení z aktivní činnosti jsou znatelně redukovány. Jsou však operace, kde vedle vyložených výhod laparoskopie bylo nutno zvládnout i celou řadu problémů (bolesti, léze senzitivních nervů). Proto se laparoskopický přístup u inguinální hernitomie rozšířil až po dokonalém zvládnutí technických problémů a v současnosti je již inguinální laparoskopická hernioplastika standardním postupem.
INGUINÁLNÍ HERNIOPLASTIKA
Bolesti v třísle po inguinální hernioplastice se vyskytují až u 34 %. Existuje celá řada příčin těchto bolestí, a to od léze nervů, přes tah jizev i bolesti vyzařující z poškozených vazů a dalších anatomických struktur s bohatou senzitivní inervací. Vlastní neuralgie po laparoskopických hernioplastikách, jejímž podkladem je poranění senzitivních nervů, je udávána v rozmezí 0,1–7 %, obvykle okolo 1 % [2, 3].Vyskytuje se po klasických chirurgických přístupech i u laparoskopického přístupu. K postoperační bolesti v třísle je nutno dlouhodobě léčit konzervativně, vyčkávat a k revizi operačního pole s případným odstraněním síťky a k neurektomii poškozených nervů je možno uchýlit se až jako k naprosto poslední možnosti. Zcela výjimečně je možno použít i „kombinovaný přístup“ – otevřený s vyjmutím síťky a neuroektomií s následným laparoskopickým vložením nové síťky [4].
Při dlouhodobém hodnocení bolestí v třísle, a to s odstupem 2, 3 a 5 let po operaci při hodnocení velkých souborů nemocných (487 nemocných laparoskopicky a 507 klasických přístupem) se prokázalo, že laparoskopické operace vedou k nižší četnosti recidiv hernie a rovněž k nižšímu výskytu chronické bolesti v třísle, než u klasických operací. Při klasických operacích dochází k poranění n. iliohypogastricus či n. ilioinguinalis, kdežto při laparoskopických operacích n. cutaneus femoris lateralis či n. genitofemoralisr. femoralis (). (Schéma 1, Schéma 2).
Schéma 1. N. genitofemoralis (kořeny L1-2) Scheme 1. N. genitofemoralis (L1-2 roots) <em>1 – průstup svalem a fascií m. psoas major, 2 – r. genitalis v tríselném kanálu, 3 – r. femoralis pod tříselným vazem. Svaly: a – m. psoas major, b – m. iliacus. 1 – the nerve´s route through the m. psoas major and fascia, 2 – r. genitalis within the inguinal canal, 3 – r. femoralis under the inguinal ligament. Muscles: a – m. psoas major, b – m. iliacus.</em> 
Schéma 2. N. cutaneus femoris lateralis (kořeny L2-3) Scheme 2. N. cutaneus femoris lateralis (L2-3 roots) <em>1 – průstup břišní stěnou pod tříselným vazem. Svaly: a – m.psoas major, b – m. iliacus. Vytečkovaná oblast vyznačuje poruchu čití 1 – the nerve’s route through the abdominal wall under the inguinal ligament. Muscles: a – m. psoas major, b – m. iliacus. The dotted area marks a sensation disorder</em> 
Rizikovými faktory pro chronickou bolest v třísle je trvání operace, typ konvenční operace i perioperační léze n. ilioinguinalis [5]. Při použití síťky ke zpevnění břišní stěny (nejméně 10 x 15 cm) dojde rovněž ke snížení výskytu postoperačních bolestí [6]. Síťky se mohou fixovat mnoha způsoby (vstřebatelnými, nevstřebatelnými svorkami či klipy, fibrinem). Právě použití fibrinového lepidla vede k dalšímu snížení postoperačních bolestí neuralgického charakteru [7]. Při souhrnném zhodnocení celé řady studií srovnávajících laparoskopické a klasické operace mají laparoskopické hernioplastiky méně přetrvávajících bolestí v třísle, menší výskyt perzistující hypestézie a nemocní se vracejí ke své předchozí aktivitě rychleji. Jsou však provázeny vyšším výskytem viscerálních komplikací (zejména poškozením močového měchýře) a poraněním cév [8] (Obr. 1, Obr. 2, Obr. 3).
Image 1. TAPP levého třísla. Špička disektoru ukazuje na n. cutaneus femoris lateralis Fig. 1. TAPP of the left groin. The dissector tip points at n. cutaneus femoris lateralis 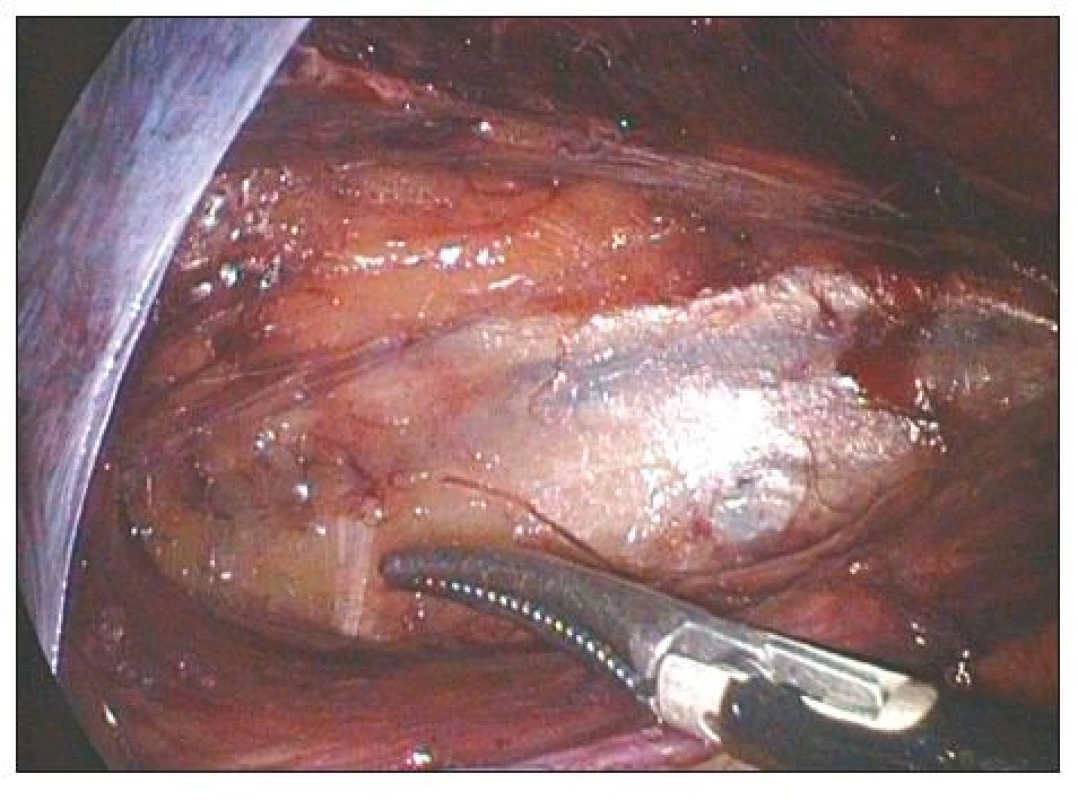
Image 2. TAPPlevého třísla. Špička disektoru ukazuje na r. femoralis n. genitofemoralis Fig. 2. TAPPof the left groin. The dissector tip points at r. femoralis n. genitofemoralis 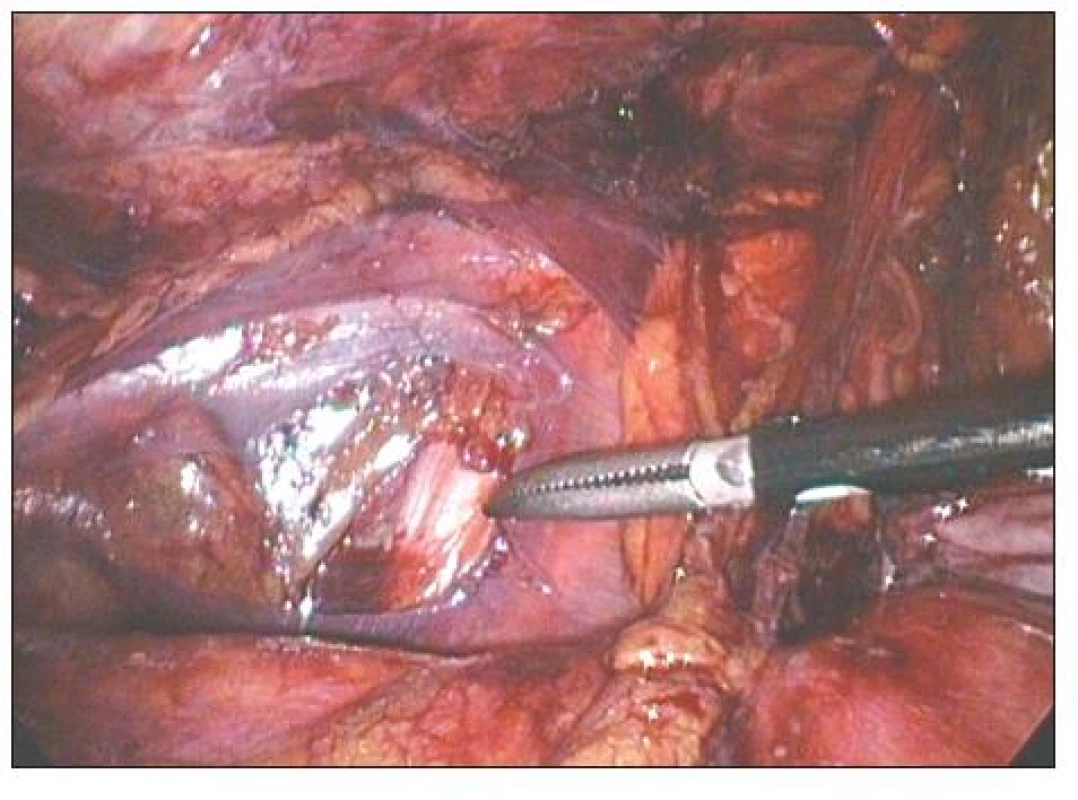
Image 3. TAPP levého třísla. Mediálně (šipka) je r. femoralis n. genitofemoralis, laterálně (špička šipky) je n. cutaneus femoris lateralis Fig. 3. TAPP of the left groin. R. femoralis n. genitofemoralis is located medially (arrow), n. cutaneus femoris lateralis is located laterally (arrowhead´s tip) 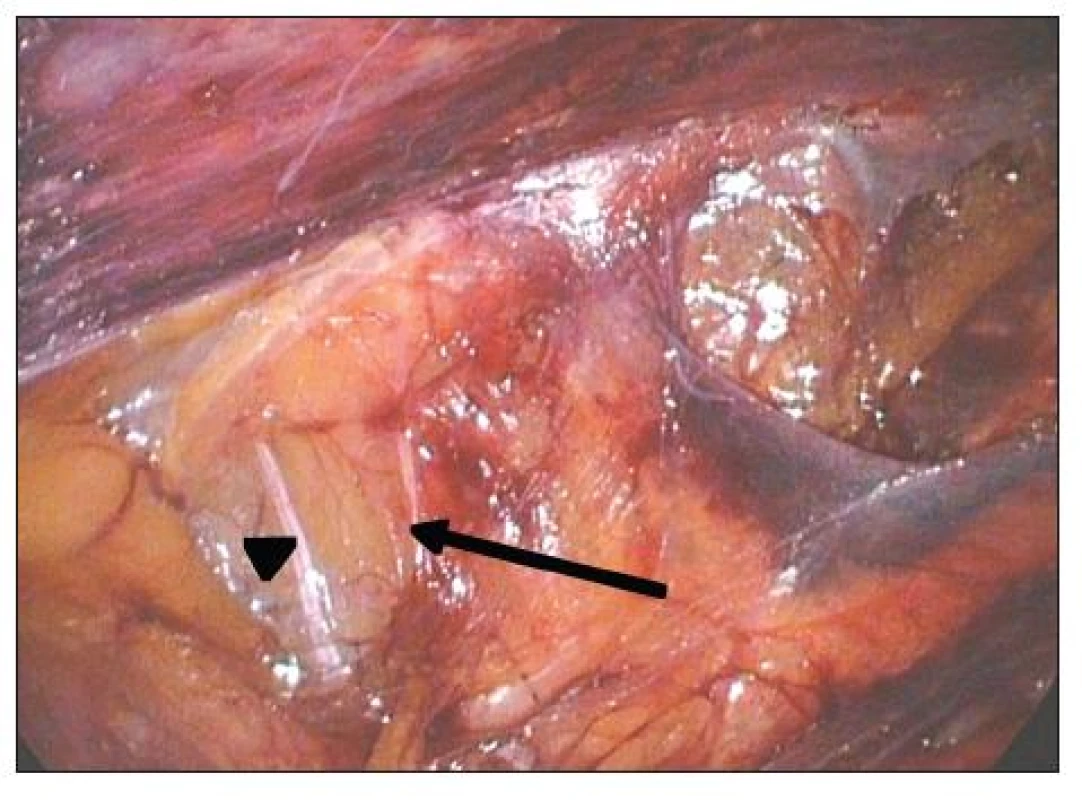
Při hodnocení četnosti poškození nervů se v souboru 448 nemocných operovaných laparoskopicky vyskytla léze nervů u 19 (4,2 %) a v souboru 448 řešených konvenční metodou u 8 nemocných (1,8 %). N. genitofemoralis byl posižen ve 2 %, n. ilioinguinalis a n. cutaneus femoris lateralis po 1,1 % [9]. Z početného souboru 2500 nemocných operovaných laparoskopicky se vyskytly různé kombinace u 89 nemocných (3,56 %). Poškození nervů s irritací a neuralgickými bolestmi s následnou operační revizí se vyskytly u 3 nemocných [10]. V souboru 30 nemocných operovaných pro inguinální hernii mělo 14 (47 %) elektrofyziologické známky poškození motorické větve n. genitofemoralis (kreasterický reflex a nález fibrilací při vyšetření m. cremaster) [11].
FEMORÁLNÍ HERNIE
Operace femorální hernií není častá. Ve velké sestavě 1097 operovaných laparoskopickou transabdominální preperitoneální technikou bylo pouze 51 nemocných (4,6 %) operovaných pro femorální hernii. Z nich se pouze u dvou nemocných objevily iritace senzitivních nervů v třísle (n. ilioinguinalis, r. femoralis n. genitofemoralis), které spontánně v průběhu 6 měsíců zcela odezněly [12]. Laparoskopický přístup je stejný jako u inguinální hernioplastiky a provází jej stejný typ i četnost komplikací (včetně bolestí a poškození nervů).
APENDEKTOMIE
Přes blízkost nervových a cévních struktur dochází jen zřídka k poranění nervů. Tak Polidori et al. 2003 [13], popsali lézi n. cutaneus femoris lateralis jako komplikaci laparoskopické apendektomie u mladé ženy. Kim et al. [14] mezi 119 nemocnými operovanými pro poškození n. femoralis identifikovali 52 iatrogenních lézí. Mezi nimi byli i dva nemocní, u nichž došlo k iatrogenní lézi n. femoralis při operaci apendixu, ovšem klasickým přístupem (Schéma 3).
Schéma 3. N. femoralis (kořeny L2-L4) Scheme 3. N. femoralis (L2-L4 roots) <em>Místa komprese nervu: 1 – pod fascií m. psoas major, 2 – v oblasti ligamentum inguinale, 3 – v canalis vastoadductorius (Hunter), 4 – rr. patellares. Svaly: a – m. psoas major, b – m. iliacus, c – m. sartorius, d – m. rectus femoris, e – m. vastus lateralis. Sites of the nerve compression: 1 – under the m. psoas major fascia, 2 – in the ligamentum inguinale region, 3 – within canalis vastoadductorius (Hunter), 4 – rr. patellares. Muscles: a – m. psoas major, b – m. iliacus, c – m. sartorius, d – m. rectus femoris, e – m. vastus lateralis.</em> 
CHOLECYSTEKTOMIE
Při průniku trokarem břišní stěnou jsou popsány léze kaudálních interkostálních nervů (Th7-11) a n. subcostalis (Th12) [1].
ADRENALEKTOMIE
Laterální laparoskopická transabdominální adrenalektomie je výhodnější než klasická otevřená adrenalektomie ze zadního přístupu (menší krevní ztráty, nižší dávka anestetika, nižší morbidita a kratší doba hospitalizace). Mezi 40 nemocnými operovanými laparoskopicky se vyskytly i 2 léze n. subkostalis, které autoři zařadili mezi závažné komplikace. Další 2 nemocní měli iritaci kožních nervů, která byla hodnocena jako malá komplikace [15].
LAPAROSKOPICKÁ FUNDOPLIKACE KARDIOEZOFAGEÁLNÍHO SPOJENÍ
Ukleja et al. [16], popsali kazuistiku 76letého muže, u kterého byla provedena laparoskopická fundoplikace (podle Nissena) pro gastroezofageální reflux. Nemocný měl od operace vodnaté průjmy, s inkontinencí stolice, zhubl o 30 kg a byl opakovaně hospitalizován pro těžkou dehydrataci. Byla diagnostikována iatrogenní léze n.vagus, která byla příčinou průjmů. Přitom postvagotomický průjem se vyskytuje ve 20–30 % a pouze u 1 % vede k těžké nezvládnutelné dehydrataci. Poranění n. vagus je velmi časté, ale většinou nevytváří podstatnější problémy. Celá řada autorů postupují tak, že peroperačně identifikují hepatickou větev vagu, kterou šetří.
OPERACE JÍCNU
Při minimálně invazivní laparoskopické transhiatální ezofagektomii u 18 nemocných (13 adenokarcinomů, 4 skvamózní karcinomy a 1 dysplazie v rámci Barrettova jícnu) došlo k 15 komplikacím. U 10 nemocných se diagnostikovala léze laryngeálních nervů [17].
BARIATRICKÉ OPERACE
U extrémně super-super-obézního 45letého muže (BMI 78,04 kg/m2) došlo při 7 hodin trvající laparoskopické operaci (sleeve gastrectomy) k rozvoji těžké oboustranné léze n. ischiadicus. Léze byly nejspíše tlakového, ischemického původu. Elektromyograficky byl prokázán těžký denervační syndrom oboustranně. Po rehabilitaci a podstatné redukci váhy (BMI 47,34 kg/m2) byl po 18 měsících schopen samostatné chůze, bez pomůcek (berlí) [18]. Při velké části operací je pacient v tzn. Schautově poloze, kdy může velkou hmotností nemocného dojít jak k otlaku n. ischiadicus tak – a to snad častěji – k lézi n. peroneus, na které se podílí jak zevní tlak na nerv proti hlavičce fibuly, tak i dlouhodobá flexe v kolenním kloubu.
OPERACE REKTA
Při laparoskopické totální mezorektální excizi (podle Healda) mobilních nefixovaných karcinomů rekta je provázena výskytem recidiv nižších než 10 % a rovněž komplikace urogenitální mají nízký výskyt. Poškození nervů s následnou inkontinencí moči a poruchami erekce je při laparoskopickém přístupu podstatně nižší než při otevřeném přístupu [19]. Parasympatické splanchnické pelvické nervy, které vznikají z druhého až čtvrtého sakrálního nervu jdou jako nervi errigentes dorzálně od rekta až dorzálně od presakrální fascie (synonymum pro Waldeyerovu fascii). Teprve v oblasti hranice mezi dolní a střední třetinou rekta pronikají fascií a podél bočních stěn rekta vedou k močovému měchýři a semenným váčkům. Kromě inervace urogenitálních orgánů jsou zodpovědné za schopnost erekce.
Pregangliová sympatická inervace pochází z prvních 3 lumbálních segmentů a dále prochází přes lumbální splanchnické nervy do aortálního a mezenterického plexu. Odtud jako postgangliová vlákna hypogastrického nervu sestupují přes promontorium podél zadní stěny malé pánve kaudálně v prostoru mezi Waldeyerovou fascií a fascia propria recti. Při poruše těchto postgangliových sympatických vláken dochází k poruše ejakulace. Jak tyto nervy sympatické tak parasympatické tvoří společně rektální nervový plexus nazývaný dolní hypogastrický plexus. Kontrakce močového měchýře jsou iniciovány jak sympatickými tak parasympatickými vlákny [20, 21].
K větší incidenci poranění autonomních nervových struktur při operacích rekta došlo po zavedení možnosti staplerových resekcí k oblasti dolní třetiny rekta. Též větší rozšíření abdominálních rektopexí vedlo ke zvýšené incidenci poranění těchto nervových struktur.
V závislosti na poškozených nervových strukturách dochází k poruchám erekce, ejakulace nebo retrográdní ejakulaci. Vzhledem k možnosti současného poškození parasympatických i sympatických nervových pletení u daného pacienta při nízkých resekcích rekta je poškození sexuálních funkcí většinou kombinované. Vzhledem k množství kolaterál mezi nervovými pleteněmi však musí dojít k poměrně rozsáhlému perioperačnímu poškození, aby došlo ke klinickým projevům. Přesto podle literárních zdrojů je pooperační kompletní sexuální impotence je pozorována až u 30,5 % pacientů [22].
Při plánování cílené prevence poranění autonomních pánevních nervů je nutno vzít v úvahu, že cílená vizualizace nervů před vlastní mobilizací rekta a před totální mezorektální excizí je detailně možná v oblasti promontoria, kde lze identifikovat horní hypogastrický plexus a tímto ho chránit před poraněním. Dále je nutné se zaměřit na distální preparaci a disekci rekta ve správné „vrstvě“, tak aby byla zachována onkologická radikalita a přitom nebyly nervové struktury poraňovány. Je nutné preparovat podle zásad „totální mezorektální excize“ formulované Healdem, tedy distálně od promontoria preparovat dorzálně od rekta v avaskulární vrstvě mezi parietální a viscerální pánevní fascií. Tímto postupem jsou pánevní autonomní nervové struktury šetřeny a pouze v místě hranice dolní a střední třetiny rekta jsou vypreparována vlákna jdoucí z mediální strany transverzálně k rektu a tato jsou přerušena. Vlákna jdoucí podél okrajů malé pánve jsou šetřena. Vpředu je nutné disekci provádět anteriorně od Denonvillierově fascie [23, 24].
LYMFADENEKTOMIE
Při operaci pánevních uzlin v gynekologii jsou nejčastěji popsány léze n. obturatorius a n. genitofemoralis [25, 26]. Prevencí je opatrná operační technika, dokonalá znalost anatomie retroperitonea a v blízkostí nervů nepoužívat elektrokoagulaci, kterou lze nahradit např. disekcí tkání pomocí ultrazvuku (harmonický skalpel). Laparoskopická retroperitoneální lymfadenektomie je součástí celé řady gynekologických zákroků: totální laparoskopické hysterektomie s adnexektomií nebo laparoskopicky asistované vaginální hysterektomie u rakoviny děložního těla, u radikální abdominální nebo vaginální hysterektomie pro rakovinu děložního hrdla, u radikální trachelektomie jako fertilitu šetřící operace mladých bezdětných žen s rakovinou hrdla děložního, u stagingových operací pro jiné gynekologické malignity.
Při laparoskopické extirpaci retroperitoneálních uzlin může dojít k poranění cév s následnou ischemií dolních končetin a rozvojem compartment syndromu (s lézemi nervů, které probíhají compartmenty), ramdomyolýzou a selháním ledvin [27].
RADIKÁLNÍ PROSTATEKTOMIE
Při laparoskopické radikální prostatektomii pro karcinom se využívá laparoskopické transperitoneální techniky, a to ascendentní nebo descendentní. Při těchto technikách je možno zachovat nn. pudendales, a tím i sexuální funkce (v 35–67 %), což při klasickém přístupu nebylo možné [28].
GYNEKOLOGICKÉ OPERACE
Laparoskopické operace v gynekologii jsou vzhledem k lokalizaci vstupu méně zatíženy lézemi nervů břišní stěny [29], avšak může dojít k poškození dalších nervů – n. obturatorius, n. femoralis [30, 31, 32, 33] (Schéma 4). Jsou popsány i léze n. cutaneus femoris lateralis s následnou nepříjemnou dysestezií zevní plochy stehna – meralgia paresthetica [34]. Zčásti se na lézích nervů při operaci podílí také nevýhodná poloha (litotomická). Batres a Barclay [35], popsali lézi n. ischiadicus u dvou mladých žen, z nich prvá podstoupila diagnostickou laparoskopii a další explorativní laparotomii. Bezprostředně po operaci zjištěná léze n. ischiadicus byla přechodná a autoři ji přisuzovali nevýhodné poloze. Berhane et al. [36], popsali u 34leté ženy, u které provedli laparoskopickou ovariální cystectomii pro cystadenom, oboustrannou parézu dolních končetin. Zobrazovací i neurofyziologické metody neprokázaly patologický nález a paréza se v průběhu několika dnů upravila.
Při rozšířených radikálních operacích pro rakovinu hrdla děložního (laparoskopicky prováděné – Wertheimova-Meigsova operace, nebo pouze laparoskopicky asistované – Schautova operace) dochází také k poškození plexus hypogastricus superior et inferior. To má často za následek poruchy mikce ve smyslu retence moči. Tyto poruchy se většinou do měsíce upraví, ale někdy přetrvávají celý život a je nutné sebecévkování. Prevencí je tzv. nervy šetřící chirurgie a zachování těchto plexů (nerve sparing surgery).
ZÁVĚR
Stále se rozšiřuje spektrum laparoskopických vyšetření a laparoskopických operací. Úspěšnost a zejména komplikace se liší od klasických chirurgických přístupů. Laparoskopické techniky mají určité riziko v omezeném přehledu operačního pole, jsou náročnější na technické vybavení i na nácvik laparoskopické techniky. Právě z těchto důvodů tvoří iatrogenní léze periferních nervů důležitou položku komplikací. Dokonalá znalost anatomie, zvládnutí náročné techniky a přehled o typických iatrogenních lézích nervů při laparoskopických operacích je důležitým preventivním krokem. I když velká většina lézí vyžaduje pouze konzervativní postup a neurochirurg ošetří jen malý počet těžkých denervačních či bolestivých lézí nervů, přesto i tyto iatrogenní léze mohou být příčinou stížností, pojišťovacích posudků i soudního řízení.
Za originální a přesvědčivá anatomická schémata děkujeme PhDr. Josefu Bavorovi z Ústavu anatomie LF UK v Hradci Králové.
Doc. MUDr. Edvard Ehler, CSc.
Pernerova 2802
530 02 Pardubice
e-mail: edvard.ehler@nemocnice-pardubice.cz
Sources
1. van Ramshorst, G. H., Kleinrensink, G. J., Hermans, J. J., Terkivatan, T., Lange, J. F. Abdominal wall paresis as a complication of laparoscopic surgery. Hernia, 2009; 13(5): 539–543.
2. Chobota, L. Neuralgie po laparoskopické operaci tříselné kýly. Lék. Zpr. LF UK HK, 2005, 50, 3–4, s. 99–107.
3. Takata, M., Duh, Q. Laparoscopic Inguinal Hernia Repair. Surg. Clin. N. Am., 2008, 88, s. 157–178.
4. Keller, J. E., Stafanidis, D., Dolce, C. J., Iannitti, D. A., Kercher, K. W., Hemiford, B. T. Combined open and laparoscopic approach to chronic pain after inguinal hernia repair. The American Surgeon, 2008; 74(8): 695–700.
5. Liem, M. S., van Duyn, E. B., van der Graaf, Y., van Vroonhoven, T. H., Coala Trial Group Recurrences after conventional anterior and laparoscopic inguinal hernia repair: a randomized comparison. Ann. Surg., 2003; 237(1): 136–141.
6. Gainant, A. Causes of complications and failures of hernia repair: how to avoid them. J. Chir. (Paris), 2007; 144(4): 5S45–5S49.
7. Santoro, E., Agresta, F., Buscaglia, F., et al. Preliminary experience using fibrin glue for mesh fixation in 250 patients undergoing minilaparoscopic transabdominal preperitoneal hernia repair. J. Laparoendosc. Adv. Surg. Tech., 1, 2007; 17(1): 12–15.
8. McCormack, K., Scott, N. V. V., Go, P. M., Ross, S., Grant, A. M., EU Hernia Trialis collaboration. Laparoscopic techniques versus open techniques for inguinal hernia repair. Cochrane Database Syst. Rev., 2003; (1): CD001785.
9. Stark, E., Oestreich, K., Wendl, K., Rumstadt, B., Hagmüller, E. Nerve irritation after laparoscopic hernia repair. Surg. Endosc., 1999; 13(9): 878–881.
10. Schultz, C., Baca, I., Götzen, V. Laparoscopic inguinal hernia repair. Surg. Endosc., 2001; 15 : 582–584.
11. Bademkiram, F., Tataroglu, C., Odedeli, K., Altay, B., Aydogdu, I., Uludag, B., Ertekin, C. Electrophysiological evaluation of the genitofemoral nerve in patients with inguinal hernia. Muscle Nerve, 2005; 32(5): 600–604.
12. Hernandez-Richter, T., Schardley, H. M., Rau, H. G., Schildberg, F. W., Meyer, G. The femoral hernia: an ideal approach for the transabdominal preperitoneal technique (TAPP). Serg. Endosc., 2000; 14(8): 736–740.
13. Polidori, L., Magarelli, M., Tramutoli, R. Meralgia paresthetica as a complication of laparoscopic appendectomy. Surg. Endosc., 2003; 17(5): 832–834.
14. Kim, D. H., Murovic, J. A., Tiel, R. L., Kline, D. G. Intrapelvic and thigh-level femoral nerve lesions: management andoutcomes in 119 surgically treated cases. J. Neurosurg., 2004; 100(5): 989–996.
15. Hallfeldt, K. K., Mussack, T., Trupka, A., Hohebleicher, F., Schmidbauer, S. Laparoscopic lateral adrenalectomy versus open posterior adrenalectomy for the treatment of benign adrenal tumors. Surg. Endosc., 2003; 17(2): 264–267.
16. Ukleja, A., Woodward, T. A., Achem. S. R. Case report: Vagus nerve injury with severe diarrhea after laparoscopic antireflux surgery. Digestive Diseases and Science, 2002; 47(7): 1590–1596.
17. Sanders, G., Borie, F., Husson, E., Blanc, P. M., Die Mauro, G., Claus, C., Milost, B. Minimally invasive transhiatal esophagectomy: lessons learned. Surg. Endosc., 2007; 21 : 1190–1193.
18. Yasin, A., Patel, A. G. Bilateral sciatic nerve palsy following a bariatric operation. Obesity Surgery, 2007; 17 : 983–985.
19. Bretagnol, F., de Calan, L. Surgery treatment of rectal cancer. J. Chir., 2006; 143(6): 366–372.
20. Havenga, K., Enker, W. E., McDermott, K., Cohen, A. M., Minsky, B. D., Guillem, J. Male and female sexual and urinary function after total mesorectal excision with autonomic nerve preservation for carcinoma of the rektum. J. Am. Coll. Surg., 1996, 182 : 495–502.
21. Mancini, R., Cosimelli, M., Filippini, A., et al. Nerve - sparing surgery in rectal cancer: feasibility and functional results. J. Expert Clin. Cancer Res., 2000, 19 : 35–40.
22. Fazio, W. V., Churych, J. M., Delaney, P. C. Current Therapy in Colon and Rectal Surgery, 2005, Mosby, Sekond Edition, s. 118–120.
23. Breukink, S. O., Pierie, J. P. E. N., Wiggers, T., Miejerink, W. J. H. J. Technique for laparoscopic autonomic nerve preserving total mesorectal excision. Int. J. Colorectal Dis., 2006, 21 : 308–313.
24. Heald, R. J., Moran, B. J., Ryall, R. D., Sexton, R. Rectal cancer: the Basingstone experience of total mesorectal excision, 1978-1997. Arch. Surg, 1998, 133(8): 894–849.
25. Holub, Z. Obturator neuropathy after laparoscopic retroperitoneal surgery. Int. J. Gynaecol. Obstet, 2006; 95(2): 165–166.
26. Rafii, A., Querleu, D. Laparoscopic obturator nerve neurolysis after pelvic lymphadenectomy. J. Mini. Invasive Gynecol., 2006; 13(1): 17–19.
27. Hauser, J., Lehnhardt, M., Steinau, H. U., Homann, H. H. Trocar injury of the retroperitoneal vessels followed by life-threatening postischemic compartment syndrome of both lower extremities. Surg. Laparsc. Endosc. Percutan. Tech., 2008; 18(2): 222–224.
28. Rassweiler, J., Stoltzenburg, J., Sulser, T., et al. Laparoscopic radical prostatectomy – the experience of the German Laparoscopic Working Group. Eur. Urol., 2006; 49(1): 113–119.
29. Stewart, J. D. (ed). Focal peripheral neurpathies. 3rd ed., Philadelphia, 2000, 580 s.
30. Ehler, E., Ambler, Z. Mononeuropatie. Praha: Galén, 2002, 176 s.
31. Spinner, R. J., Winfree, C. J. Peripheral nerves: injuries. Neurosurgery Clinics of North America, 2009, 20. 1, s. 1–136.
32. Sorenson, E. J., Chen, J. J., Daube, J. R. Obturator neuropathy: causes and outcome. Muscle Nerve, 2002, 25, s. 605–607.
33. Porzionato, A., Macchi, V., Fenato, F., Parenti, A., De Caro, R. Femoral nerve injury after gynecologic laparoscopy. J. Minim. Invasive Gynecol., 2008, 15, 1, s. 105–107.
34. Peters, G., Larner, A. J. Meralgia paresthetica following gynecologic and obstetric surgery. Ing. J. Gynaecol. Obstet, 2006, 95, 1, s. 41–43.
35. Batres, F., Barclay, D. L. Sciatic nerve injury during gynecologic procedures using the lithotomy position. Obstet Gynecol., 1983; 62 (3 Suppl): 92–94.
36. Berane, L., Kurman, R., Smith, S. Lower extremity paralysis after operative laparoscopy from conversion disorder. A case report. J. Reprod. Med., 1998; 43(9): 831–835.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2011 Issue 4-
All articles in this issue
- Pľúcna alveolárna hemorágia – zriedkavá komplikácia izolovaného poranenia hrudníka
- Traumatická ruptura perikardu – zdroj masivního hemotoraxu, kazuistika
- Časové trendy chirurgické terapie bronchogenního karcinomu
- Česká bariatrie v roce 2010
- Ošetření ruptury močového měchýře při zlomenině pánve bez epicystostomie – kazuistika
- Perforácia rekta a vagíny u dieťaťa
- Hypokoagulačný stav a jeho neobvyklá komplikácia u pacienta s obturujúcim karcinómom c. sigmoideum
- Pneumoskrotum: nezvyklý symptom při perforaci duodena (kazuistika)
- Inveterovaná súčasná luxácia proximálneho a distálneho radioulnárneho kĺbu bez pridruženej zlomeniny
- Poranění periferních nervů při laparoskopických operacích
- Zmeny alveolárnej šírky rozštepu u detí do jedného roka s jednostranným kompletným rozštepom pery a podnebia
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Hypokoagulačný stav a jeho neobvyklá komplikácia u pacienta s obturujúcim karcinómom c. sigmoideum
- Poranění periferních nervů při laparoskopických operacích
- Inveterovaná súčasná luxácia proximálneho a distálneho radioulnárneho kĺbu bez pridruženej zlomeniny
- Perforácia rekta a vagíny u dieťaťa
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

