-
Medical journals
- Career
Časné biliární komplikace po transplantaci jater
: M. Kučera; M. Adamec; M. Oliverius; L. Janoušek; M. Kočík; J. Špičák 1; P. Štirand 1; P. Drastich 1; J. Peregrin 2; P. Trunečka 3
: Klinika transplantační chirurgie, IKEM, Praha, přednosta: prof. MUDr. Miloš Adamec, CSc. ; Klinika hepatogastroenterologie, IKEM, Praha, přednosta: prof. MUDr. Julius Špičák, CSc. 1; Pracoviště radiodiagnostiky a intervenční radiologie, IKEM, Praha, přednosta: prof. MUDr. Jan Peregrin, CSc. 2; Transplantcentrum, IKEM, Praha, přednosta: MUDr. Pavel Trunečka, CSc. 3
: Rozhl. Chir., 2011, roč. 90, č. 2, s. 117-121.
: Monothematic special - Original
Úvod:
Biliární komplikace (BK) po transplantaci jater (TxJ) jsou závažným problémem a vyskytují se v 6–35 %. BK rozdělujeme na časné a pozdní. Časné BK se objeví do 30 dnů po TxJ, resp. v průběhu první hospitalizace po TxJ. Na jejich výskytu se podílejí především ischemie žlučovodu (žlučovod transplantovaného játra je zásoben pouze descendentně z pravé větve a. hepatica, chybí ascendentní zásobení z a. gastroduodenalis) a chirurgická technika provedení biliární anastomózy. Řešení BK se odehrává ve spolupráci chirurga, gastroenterologa a radiologa.Cíl:
Zhodnotit časné biliární komplikace u nemocných po TxJ.Metoda a soubor nemocných:
Do souboru nemocných byli zařazeni pacienti s časnou BK po TxJ v období 4/2004 – 12/2009. Časnou BK jsme definovali jako komplikaci, která se objevila do 30 dnů po TxJ nebo v průběhu první hospitalizace po TxJ .Výsledky:
Ve sledovaném období jsme provedli 384 TxJ. Primárně jsme rekonstruovali žlučové cesty 312x jako choledochocholedochoanastomózu (CHCHA) a 72x jako hepaticojejunoanastomózu (HJA). Časnou BK jsme pozorovali u 68 pacientů (17,7 %), z toho biliární leak 25x (6,5 %), stenózu v anastomóze 40x (10,4 %) a kombinaci leaku a stenózy 3x (0,8 %). Většina komplikací byla vyřešena endoskopicky provedením ERCP s papilosfinkterotomií, balonkovou dilatací stenózy a zavedením stentu s event. opakovanou výměnou stentu (45x, všichni nemocní se stenózou v anastomóze). 22 pacientů bylo reoperováno (16x HJA, 3x re-CHCHA, 2x opich aberantního žlučovodu, 1x sutura žlučovodu) a u 1 nemocného byla provedena perkutánní transhepatální drenáž žlučových cest (PTD). Žádný z nemocných s časnou BK nezemřel.Závěr:
BK po TxJ zůstávají závažným chirurgickým problémem. Metodou první volby v řešení BK je u většiny nemocných ERCP, jehož úspěšnost se pohybuje okolo 70 % a více.Operační revize s re-anastomózou je indikována při neúspěchu ERCP či PTD nebo při průkazu biliární peritonitidy. Pro úspěšnost léčby je zásadní dobrá spolupráce chirurga, gastroenterologa a radiologa. Četnost časných biliárních komplikací po TxJ v IKEM je plně srovnatelná s publikovanými údaji ze světových center.Klíčová slova:
transplantace jater – časné biliární komplikace – endoskopická léčba – chirurgická léčbaÚVOD
Již v roce 1976 označil R. Calne biliární anastomózu za Achillovu patu transplantace jater (TxJ). I dnes zůstávají biliární komplikace (BK) asi největším problémem v rámci chirurgických komplikací, po TxJ se vyskytují v 6–35 % případů [1]. Podle jiných autorů, kteří hodnotí pouze transplantaci celého jaterního štěpu, je četnost BK 10–30 % [2]. Biliární systém jater je velmi vulnerabilní a má omezenou regenerační schopnost. Krevní zásobení biliárního stromu je výhradně zabezpečováno arteriální krví. Extrahepatické žlučové cesty jsou zásobovány ze 40 % descendentně z pravé větve a. hepatica a ze 60 % ascendentně z paraduodenální vaskulatury z a. gastroduodenalis. Při odběru jaterního štěpu dochází k přerušení žlučovodu nad horní hranou duodena a při následné TxJ je žlučovod zásoben arteriální krví pouze z a. hepatica. Při TxJ dochází i k poruše inervace žlučovodu a následné poruše motility žlučovodu a Oddiho svěrače. 30 % všech BK se objeví v prvním měsíci po TJ a 80 % všech BK je diagnostikováno do konce šestého měsíce po TxJ [3]. Po prvním roce po TxJ se BK vyskytují vzácně. Mezi časné BK patří především leak žluče z anastomózy a stenóza v anastomóze. Diferenciálně diagnosticky je třeba vyloučit především akutní rejekci, ischemicko-reperfuzní postižení jaterního štěpu, cytomegalovirovou hepatitidu či rekurenci základního onemocnění ve štěpu. Řešení BK probíhá v rámci multidisciplinární spolupráce endoskopisty, radiologa a chirurga.
MATERIÁL A METODA
Do souboru sledovaných nemocných byli zařazeni všichni pacienti, u kterých byla provedena TxJ na Klinice transplantační chirurgie (KTCH) IKEM v období 4/2004 – 12/2009 a současně byla prokázána časná BK. Časnou BK jsme definovali jako komplikaci, která se projevila během první hospitalizace po TxJ nebo do jednoho měsíce po TxJ. V rámci standardního pooperačního sledování byly pravidelně prováděny krevní odběry včetně jaterních testů (JT) a ultrasonografické (USG) vyšetření břicha. Při podezření na BK byl další postup řešen v rámci mezioborové spolupráce hepatologa, endoskopisty, radiologa a chirurga.
VÝSLEDKY
Ve sledovaném období jsme provedli 384 TxJ. Primárně jsme rekonstruovali žlučové cesty 312x jako choledochocholedochoanastomózu (CHCHA) a 72x jako Y-Roux hepaticojejunoanastomózu (HJA). CHCHA byla prováděna vždy end-to-end se suturou jednotlivými či pokračujícím PDS stehem. V závislosti na zkušenostech jednotlivých chirurgů byl v některých případech použit vnitřní tzv. „letmý“ stent, jehož proximální konec byl umístěn nad anastomózu a distální konec čněl přes Vaterskou papilu do duodena. T-drain jako zajištění biliární anastomózy nebyl v naší sestavě nemocných použit. HJA byla obvykle provedena při TxJ pro primární sklerózující cholangitidu (PSC) či v případě nevhodného příjemcovského distálního žlučovodu k anastomóze. Časnou BK jsme pozorovali u 68 pacientů (17,7 %), z toho biliární leak 25x (6,5 %), stenózu v anastomóze 40x (10,4 %) a kombinaci leaku a stenózy 3x (0,8 %) (Obr. 1, Obr. 2). V 66,1 % bylo úspěšné endoskopické řešení, kdy bylo provedeno ERCP s papilosfinkterotomií, balonkovou dilatací stenózy a zavedením stentu s event. opakovanou výměnou stentu (45x, všichni nemocní se stenózou v anastomóze) (Obr. 3, Obr. 4). 22 pacientů bylo reoperováno (16x HJA, 3x re-CHCHA, 2x opich aberantního žlučovodu, 1x sutura žlučovodu) a u 1 nemocného byla provedena perkutánní transhepatální drenáž žlučových cest (PTD). Žádný z nemocných s časnou BK nezemřel (Tab. 1).
1. MRCP – stenóza žlučovodu Fig. 1. MRCP – biliary duct stenosis 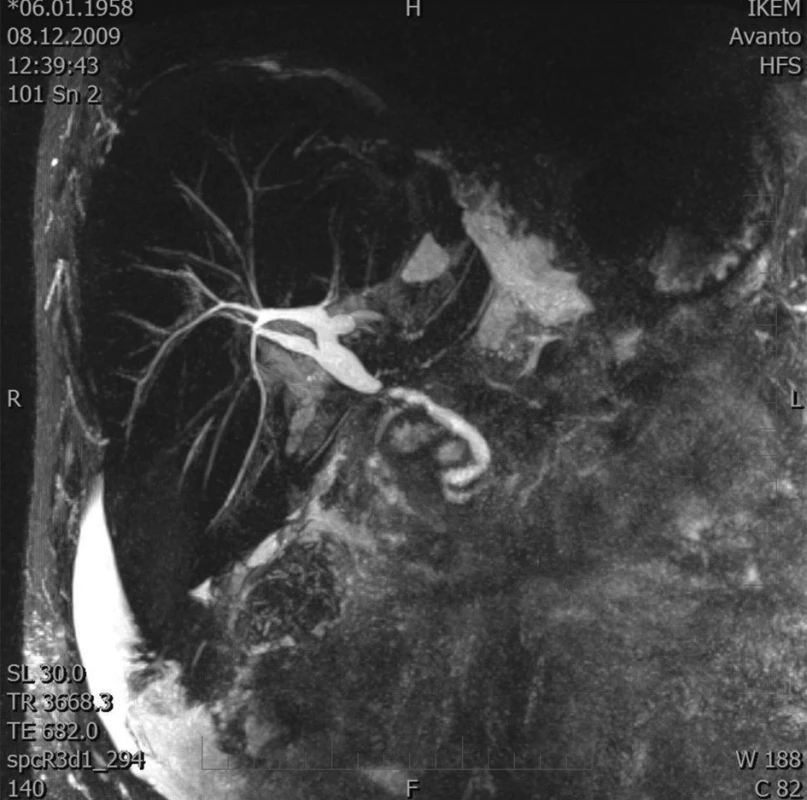
2. ERCP – stenóza žlučovodu Fig. 2. ERCP – biliary duct stenosis 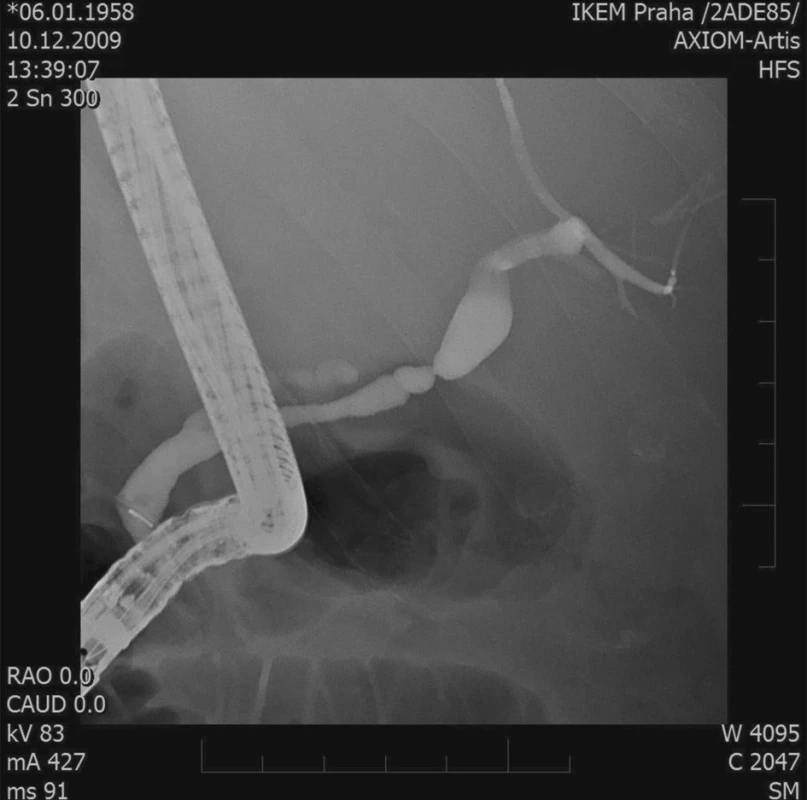
1. Časné biliární komplikace po TxJ a jejich řešení Tab. 1. Early biliary complications after LTx and their treatment 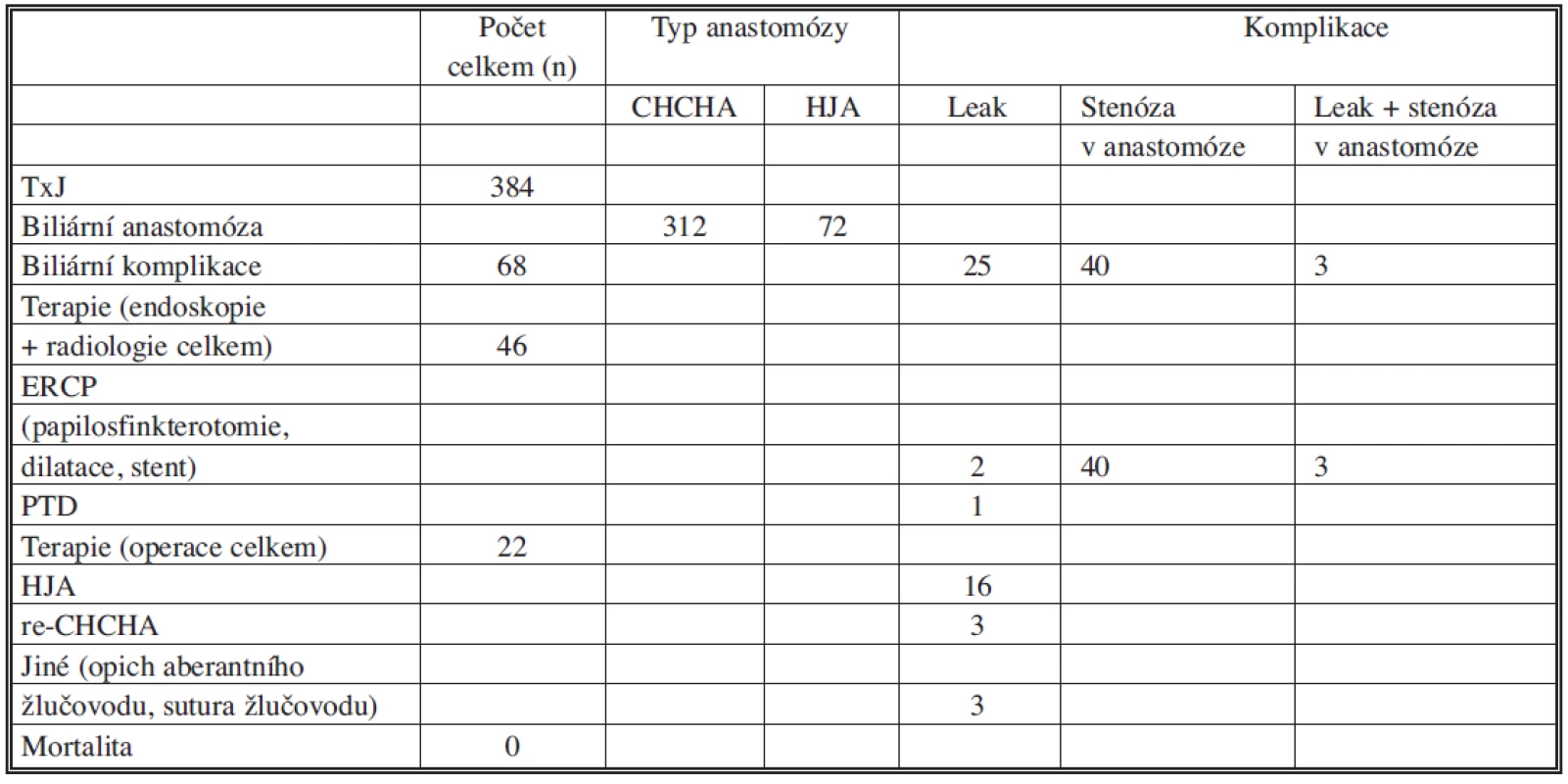
3. ERCP – stenóza žlučovodu, 1 stent Fig. 3. ERCP – biliary duct stenosis, 1 stent 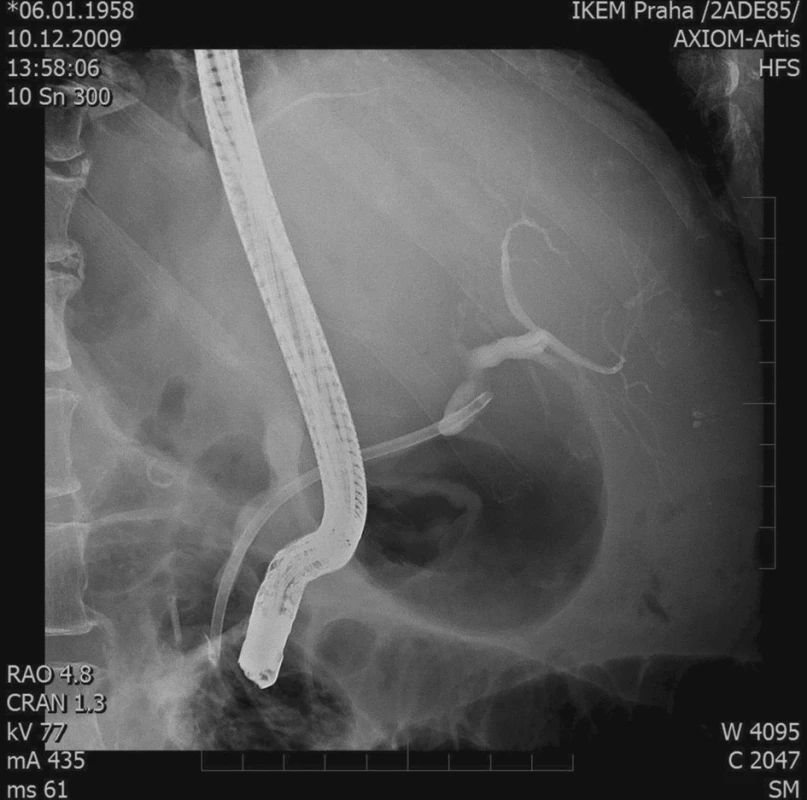
4. ERCP – stenóza žlučovodu, 3 stenty Fig. 4. ERCP – biliary duct stenosis, 3 stents 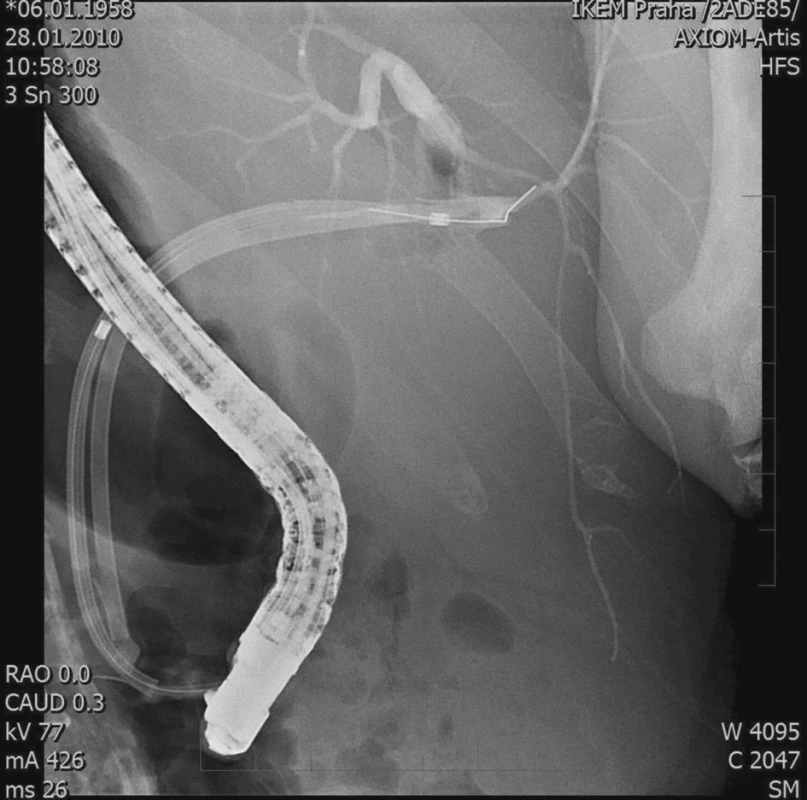
DISKUSE
Biliární komplikace po TxJ zůstávají vážným problémem i přes zlepšující se chirurgickou techniku, imunosupresivní léčbu a možnosti zobrazovacích metod.Při odhadu výskytu BK je třeba vidět, že 30 % všech těchto komplikací se objeví v prvním měsíci po TxJ a 80 % komplikací do konce šestého měsíce po TxJ [3]. Biliární leak se vyskytuje ve 2–21 %, přičemž rozdělujeme únik žluče z oblasti anastomózy a mimo anastomózu [4]. Biliární leak z anastomózy se většinou projeví do 1 měsíce po TxJ a nejčastěji je způsoben technickou chybou nebo nekrózou okrajové části suturovaného žlučovodu v důsledku jeho ischemie. Obvykle jde o nekrózu dárcovského žlučovodu, který je výrazněji ohrožen ischemií v důsledku krevního zásobení pouze z pravé větve a. hepatica (AH) [4]. Nejčastější příčinou úniku žluče mimo anastomózu je v časném pooperačním období d. cysticus (uvolněná ligatura) nebo oblast zavedeného T-drénu. Biliární stenózy se vyskytují ve 3–14 % [2, 3] a lze je rozdělit opět na stenózy v anastomóze a mimo anastomózu. Stenóza v anastomóze se nejčastěji objevuje v časném pooperačním období a příčinou je obvykle technická chyba. Někdy hovoříme o relativní stenóze, to v případě nepoměru mezi žlučovodem dárce a příjemce. Pozdější výskyt je způsoben lokální ischemií žlučovodu a následným fibrózním hojením. Stenózy mimo anastomózu jsou způsobeny trombózou AH, vyskytují se v pozdějším období a postihují žlučovody intrahepatální a extrahepatální proximálně od anastomózy. Pozdní stenózy mimo anastomózu se vyskytují i v rámci „ischaemic-type biliary lesions“ (ITBL) [1]. Mezi vzácnější BK řadíme cystické zvětšení dárcovského d. cysticus (mucocele) a dysfunkci Oddiho svěrače. Mucocele d. cysticus je způsobena zavzetím d. cysticus do biliární anastomózy. Tím vzniká slepý vak uzavřeného d. cysticus, jehož zvětšování může způsobit vnějším tlakem na žlučovod jeho stenózu. Prevencí vzniku této komplikace je excize dárcovského d. cysticus. Dysfunkce Oddiho svěrače je způsobena denervací při hepatektomii příjemce, výskyt se udává v 0–7 % [1, 2]. Mezi klinické projevy BK patří subfebrilie, neurčité bolesti břicha, v laboratoři se objevuje zhoršení jaterních testů (JT) a cholestáza. Cholestatické JT také mohou být jediným projevem BK. Ultrasonografie (USG) břicha může prokázat patologické ložisko tekutiny v okolí jater. Punkcí patologického ložiska v dutině břišní pod USG kontrolou a stanovením bilirubinu z této tekutiny lze urychlit průkaz úniku žluče. V případě stenózy v anastomóze nemusí po TxJ dojít k dilataci žlučových cest. Senzitivita a specificita USG vyšetření je 68 a 91 %. Při podezření na biliární komplikaci je indikováno MRCP (zobrazení žlučovodů na magnetické rezonanci) či ERCP. Senzitivita a specificita MRCP je více než 90 %, výhodou vyšetření je malá invazivita, nevýhodou je cena a nemožnost terapeuticky zasáhnout [3, 5]. ERCP bez předchozího vyšetření na magnetické rezonanci je indikováno v případě jasných klinických známek BK. Výhodou ERCP je kromě přesné diagnostiky rovněž možnost terapeuticky zasáhnout. Diferenciálně diagnosticky je nutné BK odlišit především od rejekce, CMV hepatitidy, rekurence základního onemocnění v jaterním štěpu či jiné chirurgické komplikace. V 80–90 % je při TxJ provedena choledocho-choledochoanastomóza (CHCHA). Y-Roux hepatikojejunoanastomóza (HJA) se provádí při nemožnosti použít k anastomóze vlastní žlučovod příjemce, při základní diagnóze primární sklerozující cholangitidy (PSC) či biliární atrézie, při retransplantaci či významném rozdílu ve velikosti obou žlučovodů [5]. Většina pracovišť provádí CHCHA end-to-end, další možností je provedení anastomózy side-to-side. Obě modifikace mají stejné procento biliárních komplikací [1, 3, 6]. Diskutabilní otázkou je použití stentu při konstrukci biliární anastomózy ať už ve formě T-drénu či vnitřního stentu. Riediger hodnotí celkem 15 retrospektivních a 5 randomizovaných prospektivních studií na použití T-drénu [7]. Výsledky nejsou jednoznačné. Užití T-drénu nesnižuje celkový výskyt BK, ale z dlouhodobého pohledu snižuje procento stenóz v anastomóze. Z těchto studií ovšem nevyplývá doporučení T-drén užívat. Jiní autoři dokonce uvádějí až 60% podíl BK vzniklých v přímé souvislosti s T-drénem [7, 8]. V našem souboru nemocných jsme T-drén nepoužili. K odlehčení anastomózy byl v některých případech implantován vnitřní stent, který odešel přirozenou cestou nebo byl extrahován při ERCP. Při diagnóze PSC je většinou provedena HJA. V přísně indikovaných případech, kdy nejsou známky postižení extrahepatálních žlučových cest, lze provést primárně CHCHA. Schmitz srovnává ve své studii HJA, choledocho-duodenoanastomózu (CHDA) a CHCHA u nemocných s PSC a uzavírá, že metodou volby je HJA a CHDA je dobrou alternativní metodou, která zajišťuje endoskopický přístup k biliární anastomóze v pooperačním období [9]. Ke stejným závěrům dochází i Benet, který považuje CHDA za bezpečnou bez většího procenta BK ve srovnání s HJA [10]. Metodou první volby v řešení BK po TxJ je u většiny nemocných endoskopické ošetření žlučovodu – ERCP, papilosfinkterotomie, balonková dilatace stenózy se zavedením stentu a většinou opakované výměny stentů v pravidelných tříměsíčních intervalech. Úspěšnost této metody při léčbě BK po TxJ je více než 70%, a hodnotíme-li pouze biliární stenózy, pak úspěšnost dosahuje až 100 % [11, 12]. Podobných výsledků bylo dosaženo také u pacientů v našem souboru. V případě neúspěchu endoskopie či BK při HJA je vhodné zvážit perkutánní transhepatální drenáž (PTD) [13]. Chirurgická revize je u většiny nemocných indikována až při neúspěchu ERCP či PTD. Pouze při rozvoji biliární peritonitidy v časném potransplantačním období je operační řešení indikováno primárně. Obvykle se provádí HJA [14].
ZÁVĚR
Závěrem lze zdůraznit, že řešení BK po TxJ je multidisciplinárním úkolem, ve spolupráci endoskopisty, radiologa a chirurga. Metodou první volby je ERCP, případně PTD. Až při neúspěchu těchto metod je indikováno chirurgické řešení.
MUDr. Miloš Kučera
IKEM
Vídeňská 1958/9
140 21 Praha 4
e-mail: miku@ikem.cz
Sources
1. Verdonk, R. C., Buis, C. I., Porte, R. J., Haagsma, E. B. Biliary complications after liver transplantation: a review. Scand. J. Gastroenterol. Suppl., 2006, May; (243): 89–101.
2. Wojcicki, M., Milkiewicz, P., Silva, M. Biliary tract complications after liver transplantation: a review. Dig. Surg., 2008; 25(4): 245–257.
3. Pascher, A., Neuhaus, P. Biliary complications after deceased-donor orthotopic liver transplantation. J. Hepatobiliary Pancreat. Surg., 2006; 13(6): 487–496.
4. Scanga, A. E., Kowdley, K. V. Management of biliary complications following orthotopic liver transplantation. Curr. Gastroenterol. Rep., 2007, Mar; 9 (1): 31–38.
5. Sharma, S., Gurakar, A., Jabbour, N. Biliary strictures following liver transplantation: past, present and preventive strategies. Liver Transpl., 2008.
6. Duailibi, D. F., Ribeiro, M. A. Jr. Biliary complications following deceased and living donor liver transplantation: a review. Transplant. Proc., 2010 Mar; 42(2): 517–520.
7. Riediger, C., Müller, M. W., Michalski, C. W., Hüser, N., Schuster, T., Kleeff, J., Friess, H. T-Tube or no T-tube in the reconstruction of the biliary tract during orthotopic liver transplantation: systematic review and meta-analysis. Liver Transpl., 2010, Jun; 16(6): 705–717. Review.
8. Wojcicki, M., Lubikowski, J., Klek, R., Post, M., Jarosz, K., Białek, A., Wunch, M., Czuprynska, M. Reduction of biliary complication rate using continuous suture and no biliary drainage for duct-to-duct anastomosis in whole-organ liver transplantation. Transplant. Proc., 2009, Oct; 41 (8): 3126–3130.
9. Schmitz, V., Neumann, U. P., Puhl, G., Tran, Z. V., Neuhaus, P., Langrehr, J. M. Surgicalcomplications and long-term outcome of different biliary reconstructions in livertransplantation for primary sclerosing cholangitis-choledochoduodenostomy versus choledochojejunostomy. Am. J. Transplant., 2006, Feb; 6 (2): 379–385.
10. Bennet, W., Zimmerman, M. A., Campsen, J., Mandell, M. S., Bak, T., Wachs, M., Kam, I. Choledochoduodenostomy is a safe alternative to Roux-en-Y choledochojejunostomy for biliary reconstruction in liver transplantation. World J. Surg., 2009, May; 33(5): 1022–1025.
11. Alexopoulos, S. P., Henningsen, J. A., Jeffrey, R. B., Bonham, C. A., Ahmed, A., Gonzalez, S. A. Management of biliary strictures following liver transplantation. Dig. Dis. Sci., 2009 Jan; 54 (1): 25–27.
12. Holt, A. P., Thorburn, D., Mirza, D., Gunson, B., Wong, T., Haydon, G. A prospective study of standardized nonsurgical therapy in the management of biliary anastomotic strictures complicating liver transplantation. Transplantation, 2007, Oct 15; 84 (7): 857–863.
13. Aytekin, C., Boyvat, F., Harman, A., Ozyer, U., Sevmi, S., Haberal, M. Percutaneous management of anastomotic bile leaks following liver transplantation. Diagn. Interv. Radiol., 2007, Jun; 13 (2): 101–104.
14. Mercado, M. A., Vilatobá, M., Chan, C., Domínguez, I., Leal, R. P., Olivera, M. A. Intrahepatic bilioenteric anastomosis after biliary complications of liver transplantation: operative rescue of surgical failures. World J. Surg., 2009, Mar; 33(3): 534–538.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2011 Issue 2-
All articles in this issue
- Simultaneous Transplantation of the Kidney and the Islets of Langerhans
- Liver Transplantation in Patients with Portal Vein Thrombosis
- Early Biliary Complications Following Liver Transplantation
- First Czech and Slovak Domino Liver Transplantation
- Development of Pancreas Transplantation Surgical Techniques in IKEM
- Immunosuppression Following Venous Allografts Transplantations – The Authors’ experience
- Effect of Biological Glues on Vascular Wall in an Experimental Model of Aortic Dissection
- Technique of Implantation and Experience with Temporary Mechanical Cardiac Support in Right Ventricular Failure
- Outcomes of Combined Mitral Valve Repair Surgery and Aortic Valve Replacement in IKEM Praha
- Cardiosurgical Procedures in Patients Refusing Blood Transfusions: IKEM Outcomes
- Vascular Complications in Transcatheter Aortic Valve Implantation in IKEM
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Early Biliary Complications Following Liver Transplantation
- Cardiosurgical Procedures in Patients Refusing Blood Transfusions: IKEM Outcomes
- Outcomes of Combined Mitral Valve Repair Surgery and Aortic Valve Replacement in IKEM Praha
- Development of Pancreas Transplantation Surgical Techniques in IKEM
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

