-
Medical journals
- Career
Metastatické onemocnění páteře
Authors: T. Brož 1; J. Šiller 2; K. Zinek 1
Authors‘ workplace: Neurochirurgické oddělení, Chirurgická klinika, Krajská nemocnice Pardubice primář MUDr. P. Hájek, Ph. D. 1; Chirurgická klinika, Krajská nemocnice Pardubice, přednosta doc. MUDr. K. Havlíček, CSc. Ústav zdravotnických studií Univerzity Pardubice, přednosta prof. MUDr. A. Pellant, DrSc. 2
Published in: Rozhl. Chir., 2007, roč. 86, č. 6, s. 320-322.
Category: Monothematic special - Original
Overview
Cílem sdělení je snaha přiblížit odborné veřejnosti problematiku léčby páteřních metastáz. Vlivem zdokonalování grafických metod dochází k časné detekci tohoto onemocnění a tím se zvyšuje benefit pacienta při včasném zahájení adekvátní terapie. Autoři v tomto sdělení hodnotí literárně dostupné studie týkající se terapeutických metod pro léčbu páteřních metastáz a srovnávají je se souborem vlastních pacientů.
ÚVOD
Metastatické onemocnění páteře představuje závažný medicínský a sociální problém. Pokroky v onkologické léčbě spolu se zlepšujícími se možnostmi grafické dokumentace vedou v poslední době ke zvyšujícímu se počtu včasně zachycených pacientů s metastatickým onemocněním páteře. Tyto faktory jsou také příčinou delšího přežívání nemocných se zhoubným nádorem. Tím vzrůstá počet pacientů, u kterých se projeví metastatické postižení páteře [1]. Metastázy jsou nejčastější sekundární nádorové postižení páteře. Vlivem výše uvedených faktů se předpokládá zvýšení incidence daného onemocnění během příštích 20 let až o 50 %. Metastázy se vyskytují ve všech úsecích páteře s incidencí – C páteř v 10 %, Th páteř v 20 %, LS páteř v 70 %. Neurologické postižení vzniká v 70 % v oblasti Th páteře, v 20 % v LS úseku a 10 % v C úseku páteře. Po játrech a plicích je kostní tkáň třetí anatomickou strukturou, ve které dochází k šíření zhoubného nádoru [2]. Nejčastější zhoubné nádory se šířením do axiálního skeletu pochází z primárního ložiska v plíci, v ledvině, u žen z prsu, u mužů v prostatě, dále jsou primárním ložiskem, štítná žláza, myelom, gastrointestinální trakt (Tab. 1) [3].
Table 1. Frekvence výskytu páteřních metastáz podle primárního zdroje Tab. 1. The frequency of occurrence of vertebral metastasis according of prime source 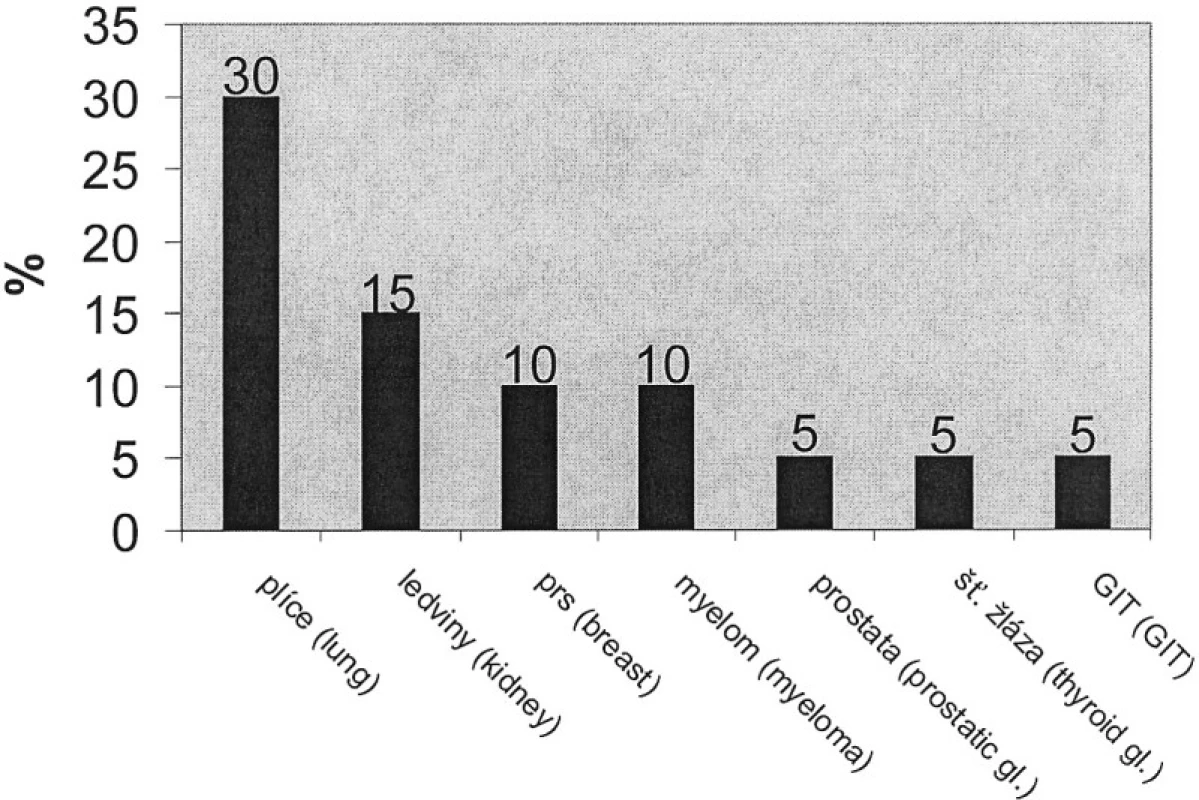
KLASIFIKACE PÁTEŘNÍCH METASTÁZ
Dělení provádíme podle lokalizace procesu na extradurálně uložené, které tvoří 95 % z celkového počtu páteřních metastáz, intradurálně extramedulárně uložené tvořící 4,5 % (zejména melanom, lymfom) a intradurálně uložené tvořící 0,5 %. Tvrdá plena je ochrannou bariérou proti šíření nádoru intradurálně, a proto je maximum páteřních nádorů uloženo extradurálně. Dělení podle patofyziologie vzniku – nejčastější formou je přenos hematogenní cestou a to jak arteriální, tak i venózní cestou retrográdně.
Klinika
Základním a prvním příznakem je bolest, kterou uvádí až 95 % nemocných. Lokální bolest odpovídá zhruba výšce nádorové léze, jsou charakteristická noční maxima, bolesti jsou typicky stálého charakteru, které neustupují ani v klidu [4]. Tím, jak dochází k šíření nádoru do páteřního kanálu, rozvíjejí se také neurologické příznaky. Tyto se odvíjí od stupně komprese míchy a míšních kořenů. Bolesti páteře souvisí s osteolytickým charakterem metastáz a vzniklou instabilitou poškozeného segmentu.
Diagnostika
Základem diagnostického postupu jsou RTG snímky páteře. Je to nejen z důvodů finančních, ale i dostupností této metody a její neinvazivitou. V současné době je zlatým standardem vyšetření MRI. MRI vyšetření páteře je cenné především přesnou lokalizací, rozsahem nádoru a zhodnocením komprese míchy. Senzitivita MRI metody je 92–95 %, specificita je okolo 85 % [5]. Další modalitou v diagnostice páteřních metastáz je CT vyšetření, které spolehlivě zobrazí postižení skeletu. Ve speciálních případech se doplňuje předoperační spinální angiografie, která je cenná při verifikaci vaskularizace tumoru a je jí proto možno využít pro následnou předoperační embolizaci u bohatě vaskularizovaných nádorů. Z dalších grafických vyšetření se využívá scintigrafie skeletu, která má vysokou senzitivitu a nízkou specificitu. V poslední době roste možnost vyšetření PET, jehož senzitivita je menší než u vyšetření MRI, ale specificita je větší.
TERAPIE
Léčba metastatického onemocnění páteře je více než kontroverzní. Do této doby neexistuje prospektivní randomizovaná studie (Class I.) srovnávající různé terapeutické metody pro léčbu páteřních metastáz. V literatuře je evidovaná jedna práce Class I. od Younga a spolupracovníků z roku 1980. Výsledky této studie však nemají dostatečnou statistickou průkaznost a to vzhledem jednak k malému počtu zhodnocených pacientů – 29, ale i krátké doby sledování – pouhé 4 měsíce. Co se týká studií zařazených do Class II., jedná se o čtyři práce (Siegal T, et al 1985, Sundaresan N, et al 1991, Tomita K, et al 2001, Wai EK, et al 2003).
Dosud neexistuje studie hodnotící doporučenou léčbu. Z tohoto důvodu je zatím každý případ posuzován individuálně. Cílem léčby páteřních metastáz je stanovit definitivní diagnózu, provést dekompresi nervových struktur se snahou o zachování stability páteře. Vlastní terapii můžeme rozdělit na konzervativní a chirurgickou. Chirurgickou léčbu dále dělíme podle lokalizace a rozsahu nádorového postižení na intervenční, paliativní a radikální. Intervenční léčba spočívá v biopsii, embolizaci či perkutánní vertebroplastice.
Biopsie je indikovaná u pacientů s neznámým primárním tumorem. Úspěšnost se pohybuje okolo 70–90 %. Paliativní léčba spočívá pouze v dekompresi nervových struktur. Radikální je vedena snahou o co největší odstranění nádorového postižení se zachováním páteřní integrity. Cílem je co největší profit léčby pro pacienta.
Jako další léčebné možnosti využíváme onkologickou léčbu – radioterapii, chemoterapii a doplňkovou léčbu [6].
Radioterapie je metodou volby v léčbě páteřních metastáz. Má efekt nejen analgetický, ale v určitých případech i kurativní, který spočívá ve zlepšení a stabilizaci výchozího neurologického nálezu. Indikace je zejména u radiosenzitivních typů páteřních metastáz, paraplegie trvající více než 24 hodin, multietážového postižení páteře, diseminace primárního procesu. Dále u pacientů s neurodeficitem s předpokládanou dobou přežití od 3 do 6 měsíců.
Hormonální léčba je využívána u hormonálně dependentních nádorů, jako jsou karcinomy prsu, prostaty a štítné žlázy.
Chemoterapie se uplatňuje u chemosenzitivních tumorů.
Steroidy jsou standardně využívány při známkách neurologického postižení (redukují edém míšní a tím zlepšují neurologický outcome). Přesné schéma dávkování není literárně určeno. Je doporučeno zahájit léčbu dávkou 10 mg Dexametazonu a následně 4 mg každých 6 hodin [7]. Konzervativní léčba je indikována při očekávaném přežití pacienta do 6 měsíců se snahou o odstranění bolestí. Cílem chirurgické léčby je redukce bolesti, zachování či zlepšení neurologických funkcí, obnovení páteřní integrity, redukce tumorózních mas. Je indikována při očekávaném přežití pacienta více než 6 měsíců. Mezi výkony paliativní chirurgie se řadí dekompresivní laminektomie, částečné odstranění tumoru, stabilizační výkony.
Chirurgická léčba u kompletního neurologického výpadu trvajícího déle než 24 hodin, není doporučována. Zde je metodou první volby radioterapie.
Indikace k chirurgickému řešení je selhání radioterapie, neznámý primární zdroj, příznaky míšní komprese, solitární léze, radiorezistentní tumor, instabilita páteře, neztišitelná bolest. K doplnění indikačního schématu dále využíváme upraveného skórovacího Tokuhashiho systému, který používá šest parametrů hodnocených od 0 do 5 bodů. Totální součet může dosáhnout 15 bodů. Konzervativní léčba je indikována při dosažení 8 a méně bodů – zde je očekávaná délka přežití 6 měsíců. Při dosažení 9–11 bodů je indikovaná paliativní léčba, očekávaná délka přežití je 6–12 měsíců. Při dosažení 12–15 bodů je indikovaná radikální léčba, zde je očekávaná délka přežití více než jeden rok. Shoda mezi předpokládanou dobou přežití stanovenou na podkladě skórovacího systému (Tokuhashiho) a skutečnou délkou života byla vysoká u pacientů v každé skupině [8]. Chirurgické přístupy užívané při léčbě metastatického onemocnění páteře mohou být přední, zadní či kombinované. Lze využít i minimálně invazivních či endoskopicky navigovaných přístupů. Ke stabilizačním výkonům používáme různé typy instrumentací. Při provedení předozadního výkonu je vhodné operace rozdělit do dvou kroků.
SOUBOR
Hodnotili jsme 32 nemocných v letech 2003–2005. Do souboru jsme zařadili pouze nemocné, kteří byli dispenzarizováni na našem pracovišti s úvahou o operačním řešení. Jednalo se o 13 mužů a 19 žen s průměrným věkem 54,6 a 57,2 roku. U šesti se jednalo o první záchyt maligního onemocnění, další byli již onkologicky sledováni. Výskyt v jednotlivých úsecích páteře byl v 18 % v oblasti C páteře, v 23 % Th a v 59 % LS oblasti páteře, tedy odpovídajícím i na malém souboru literárním údajům [9]. Operační řešení jsme indikovali u 28 nemocných. Z čtyřech dále léčených konzervativně nebyla indikace pro mnohočetné metastatické postižení páteře. Neurologické postižení jsme zjistili u 84,3 % nemocných. Pouze bolest jako příznak maligního onemocnění mělo 5 nemocných – 3 ženy a 2 muži. K indikačnímu rozhodnutí bylo použito upraveného Tokuhashiho systému. Typ operačního řešení byl zvolen s ohledem na místo výskytu v oblasti obratlového těla a útlaku nervových struktur. Zadní přístup jsme indikovali u 7 nemocných, přední přístup u 14 a kombinovaný u 7 nemocných, což odpovídá literatuře. Pooperační radioterapie byla provedena u všech pacientů. Pouze radioterapie byla použita u čtyřech nemocných, kteří nebyli indikováni podle Tokuhashiho systému k operačnímu řešení. Vzhledem ke zvolenému terapeutickému řešení jsme hodnotili schopnost lokomoce pomocí vlastních sil. Pacienti léčení kombinovaným způsobem (operace doplněná radioterapií) byli schopni lokomoce mnohem déle než nemocní, kteří byli pouze ozářeni a to v poměru 183 ku 39 dnům. Porovnáním našeho souboru v kontextu s dostupnými literárními údaji jsme došli i přes malý počet námi hodnocených pacientů ke srovnatelným výsledkům léčby [9].
ZÁVĚR
I přes rozvoj nových diagnostických a terapeutických metod je nadále léčba páteřních metastáz více než problematická. Stále chybí studie srovnávající jednotlivé modality léčby páteřních metastáz. Časná detekce tohoto onemocnění rozšiřuje pole zejména pro chirurgické řešení. Základním cílem terapeutického postupu by měl zůstat především co největší profit pro pacienta a za předpokladu prodloužení života v dobré kvalitě. Z tohoto důvodu je zatím nutno každý případ posuzovat individuálně a se snahou o multidisciplinární přístup.
MUDr. T. Brož
Neurochirurgické oddělení
Chirurgická klinika Krajské nemocnice
Kyjevská 44
532 03 Pardubice
e-mail: broz.tomas@centrum.cz
Sources
1. Bailar, J. C., Gornik, H. L. Cancer undefeated. N. Engl. J. Med., 1997, Vol. 336, 1569–1574.
2. Hatrick, N. C., Lucas, J. D., Timothy, A. R., et al. The surgical treatment of metastatic disease of the spine. Radiother. Oncol., 2000, Vol. 56, p. 335–339.
3. Solberg, A., Bremnes, R. M. Metastatic spinal cord compression: diagnostic delay, treatment, and outcome. Anticancer. Res., 1999, Vol. 19, p. 677–684.
4. Gilbert, R. W., Kim, J. H., Posner, J. B. Epidural spinal cord compression from metastatic tumor: diagnosis and treatment. Ann. Neurol., 1978, Vol. 3, p. 40–51.
5. Seidl, Z., Obenberger, J. Úloha magnetické rezonance v diagnostice vertebrogenních metastáz. Čes. a Slov. Neurol. Neurochir., 1998, Vol. 5, p. 278–284.
6. Janjan, N. Bone metastases: approaches to management. Semin. Oncol., 2001, Vol. 28, p. 28–34.
7. Greenberg, H. S., Kim, J. H., Posner, J. B. Epidural spinal cord compression from metastatic tumor: results with a new treatment protocol. Ann. Neurol., 1980, Vol. 8, p. 361–366.
8. Tokuhashi, Y., Matsuzaki, H., Oda, H., Oshima, M., Ryu, J. A revised scoring system for preoperative evaluation of metastatic spine tumor prognosis. Spine, 2005, Vol. 30, p. 2186–2191.
9. Prasat, D., Schoff, D. Malignant spinal-cord compression. Lancet Oncol.,2005, Vol. 5, p. 15–24.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2007 Issue 6-
All articles in this issue
- Pyogenní abscesy jater
- Komplikace laparoskopické apendektomie
- Kontroverze v indikaci chirurgické léčby při akutním krvácení při vředové chorobě gastroduodena
- Odložená rekonstrukce defektů měkkých tkání obličeje
- Chirurgická technika odběru tenkého střeva pro transplantaci
- Benigní lymfoepiteliální cysta pankreatu – kazuistika
- Akutní masivní krvácení z rekanalizované umbilikální žíly jako komplikace portální hypertenze
- Synchrónny nádor rekta a obličky. Kazuistika
- Infikovaná pseudoaneuryzma a. brachialis – raritní kazuistika u dlouholetého intravenózního narkomana
- Laparoskopické řešení epidermoidní cysty sleziny – kazuistika
- Metastatické onemocnění páteře
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Laparoskopické řešení epidermoidní cysty sleziny – kazuistika
- Komplikace laparoskopické apendektomie
- Pyogenní abscesy jater
- Metastatické onemocnění páteře
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

