-
Medical journals
- Career
Autofluorescenčná videotorakoskopia – prvé vlastné skúsenosti
Authors: J. Belák 1; M. Kudláč 1; I. Čavarga 2; M. Janík 1; C. Sauka 1
Authors‘ workplace: II. chirurgická klinika UPJŠ LF, FN L. Pasteura, Košice, Slovenská republika, prednosta: MUDr. J. Belák, PhD. 1; Klinika pneumológie a ftizeológie, UPJŠ LF, FN L. Pasteura, Košice, Slovenská republika, prednosta: prof. MUDr. R. Tkáčová, CSc. 2
Published in: Rozhl. Chir., 2007, roč. 86, č. 10, s. 558-561.
Category: Monothematic special - Original
Overview
Autori prezentujú prvé klinické skúsenosti s využitím autofluorescenčnej videotorakoskopie pri diagnostike ochorení pleury. V práci bola použitá fluorescenčná endoskopická súprava Richard Wolf DAFE. Predbežné výsledky ukazujú, že autofluorescenčné zobrazovanie presnejšie lokalizuje patologický proces, čo vedie k zvýšeniu výťažnosti videotorakoskopie pri diagnostike príčiny pleurálneho postihnutia. Výsledný nepriamy autofluorescenčný obraz znázorňuje zdravé tkanivá v belavozelenej farbe, zhrubnutý povrch tkaniva v dôsledku hyperplastických zápalových procesov (pachypleura, zrasty) a nádorových prípadne dysplastických procesov sa znázorňuje ako sýte vysokodenzitné ložisko modrej farby .
Kľúčové slová:
videotorakoskopia – autofluorescencia – pleurálny výpotokÚVOD
V súčasnosti predstavuje videotorakoskopia štandardnú torakochirurgickú diagnostickú a liečebnú metódu. Pri exudatívnej pleurálnej efúzii pri neznámom origu vo viac ako 90 % dokáže určiť presne diagnózu [1]. Pri malígnych pleurálnych výpotkoch je senzitivita torakoskopie 93–97 %, cytológie pri pleurálnej punkcii 62–80 %, pleurálnej perkutánnej biopsie 50 % [2, 3, 4].
Konvenčná endoskopia a taktiež aj torakoskopia využíva reflektančné zobrazovanie, pri ktorom lúče polychromatického zdroja svetla (bieleho svetla pochádzajúceho najčastejšie z xenónových žiariviek) dopadajú na tkanivo a dochádza k viacerým optickým procesom. Prvým je priamy odraz svetla od povrchu tkaniva nazývaný spekulárna reflexia. Po prechode svetla do tkaniva je časť svetelného žiarenia rozptýlená a časť absorbovaná. Časť rozptýleného svetla sa opätovne dostáva k povrchu tkaniva a vyžaruje do vzduchového prípadne tekutinového rozhrania. Tento proces sa nazýva difúzna reflexia. Oko operatéra prípadne detektorové systémy (CCD kamery) snímajú len vlnové dĺžky svetla odrazené v procese spekulárnej a difúznej reflexie. Tieto odrazené vlnové dĺžky registruje endoskopista ako farebný a štrukturálny zrakový vnem, ktorý využíva v diagnostickom procese na základe svojich praktických skúseností. Tento diagnostický proces má svoju limitovanú senzitivitu a špecificitu, ktorá nie je určovaná len skúsenosťami operatéra. Napríklad vlhký povrch tkanív (typický pre pleuru a peritoneum) spôsobuje nadmerný odraz svetla, v ktorom sa jemné farebné a štrukturálne zmeny strácajú [5, 6]. Zlepšiť nedostatky reflektančného zobrazovaní môže fluorescenčné zobrazovanie. Fluorescenčný fenomén vyvoláva spomínaná absorbovaná frakcia svetla pochádzajúca z excitačného zdroja. Fotóny absorbovaného svetla interagujú so špecifickými molekulami v tkanive-fluorofórmi a uvádzajú ich do excitovaného stavu s vyššími energetickými hladinami. Po deexcitácii späť do základného stavu tieto látky vyžiaria fotóny fluorescenčného svetla, ktoré majú inú vlnovú dĺžku ako excitačné svetlo. Medzi významné fluorescenčné molekuly patria napríklad kolagén, elastín, pyridínnukleotidy, flavíny, flavoproteíny porfyríny a lipopigmenty. Fluorescenčné svetlo poskytuje nové informácie o metabolickom a štrukturálnom zložení tkaniva. Nevýhodou je jeho nízka intenzita a nutnosť použiť špeciálne detektorové systémy so sústavou optických filtrov [5]. Metodika fluorescenčného zobrazovania si nachádza uplatnenie v bronchoskopii, cystoskopii, gastrointestinálnej endoskopii a laparoskopii [7, 8]. Recentné publikácie referujú o využití fluorescenčného zobrazovania v torakoskopii [1, 9, 10]. V našej práci sa pokúsime prezentovať vlastné skúsenosti s touto metodikou.
MATERIÁL A METÓDY
V práci využívame fluorescenčnú endoskopickú súpravu firmy Richard Wolf, SRN. Zariadenie je schopné snímať autofluorescenciu tkanív ako aj exogénne indukovanú fluorescenciu pomocou fluorescenčných substancii a prekurzorov (hematoporfyríny, chloríny, kyselina 5-aminolevulová). Sústavu tvorí zdroj svetla Combilight DAFE PDD 5138 s 300W xenónovou žiarivkou pre reflektančné zobrazovanie a nastaviteľným optickým filtrom na tvorbu modrofialového excitačného svetla vlnových dĺžok 390–460 nm.
Konvenčný obraz v bielom svetle a fluorescenčný obraz sníma kamera (1 CCD Endocam 5520) pripojená na rigídnu Hopkinsovu optiku 30°. Pri práci vo fluorescenčnom móde využíva kamera emisný filter prepúšťajúci vlnové dĺžky svetla v rozmedzí 475–700 nm. Emisný filter je konštruovaný tak aby prepustil do zorného poľa aj malé množstvo modrofialového svetla – asi 1% celkovej intenzity pocházajúcej z xenónovej žiarivky. Toto svetlo sa uplatní ako farebný kontrast v miestach s oslabeným autofluorescenčným svetelným signálom. Výsledný nepriamy fluorescenčný obraz kalibrovaný počítačom v kontrolnej jednotke kamery je nasledovný:
- zdravé tkanivá s fyziologickou koncentráciou kolagénnych a elastických vláken sa znázorňujú v belavozelenej farbe (Obr. 1, 2),
Image 1. Pohľad na parietálnu pleuru bez postihnutia v bielom svetle, viditeľné je presvitanie interkostálnej svaloviny a cievnych štruktúr Fig. 1. A view of unaffected parietal pleura, in white light. Intercostal musculature and vascular structures can be detected (show through) 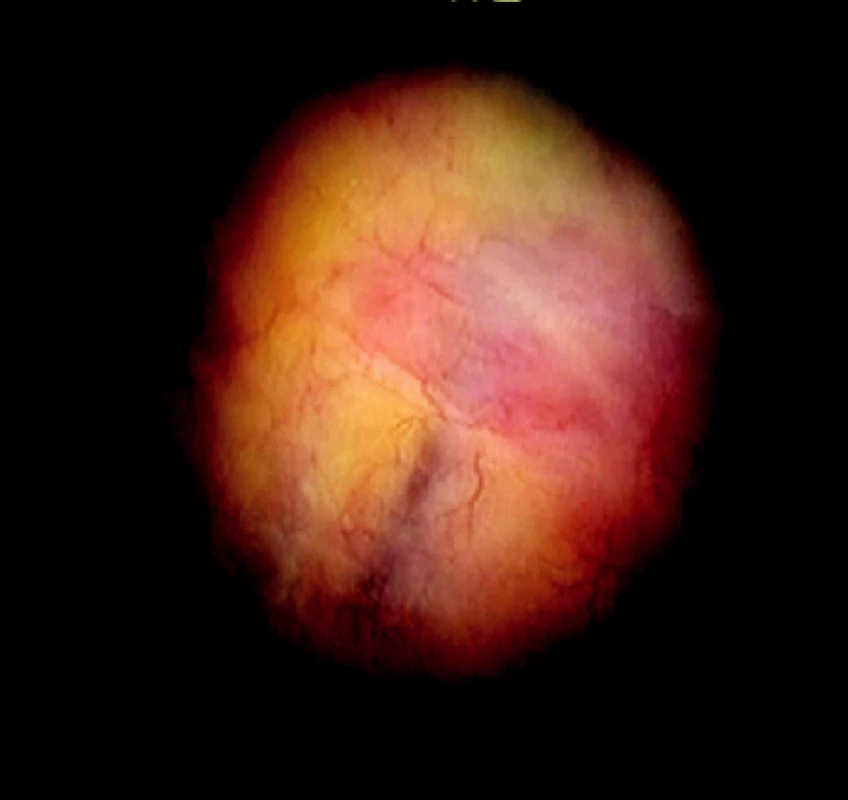
Image 2. Pohľad na parietálnu pleuru bez postihnutia v autofluorescenčnom obraze Fig. 2. An autofluorescence view of the unaffected parietal pleura 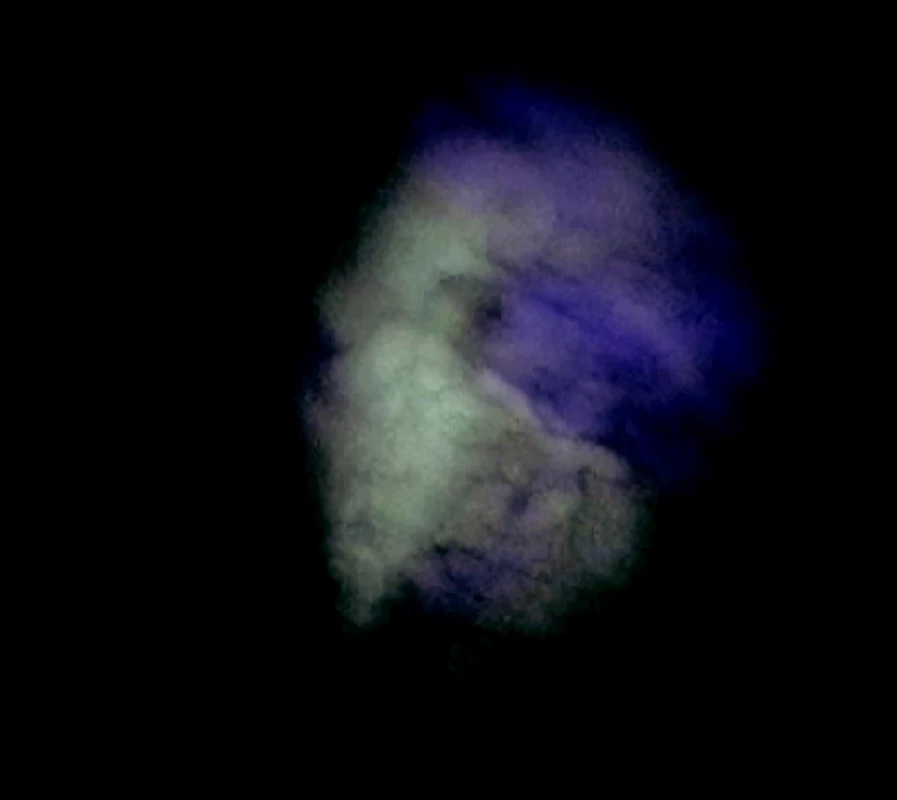
- tkanivá so zvýšenou koncentráciou hemoglobínu alebo zápalového infiltrátu v hlbších vrstvách (1 až 2 mm) sa znázorňujú ako modrá farba nízkej denzity,
- tkanivá so zvýšenou povrchovou koncentráciou hemoglobínu napríklad zakrvácaný povrch alebo povrchovo lokalizovaná cieva sa znázorňujú ako čierna prípadne sivá plocha,
- zhrubnutý povrch tkaniva v dôsledku hyperplastických zápalových procesov (pachypleura, zrasty) a nádorových prípadne dysplastických procesov sa znázorňuje ako sýte vysokodenzitné ložisko modrej farby (Obr. 3, 4).
Image 3. Ložisko adenokarcinómu v bielom svetle Fig. 3. A focus of adenocarcinoma in white light 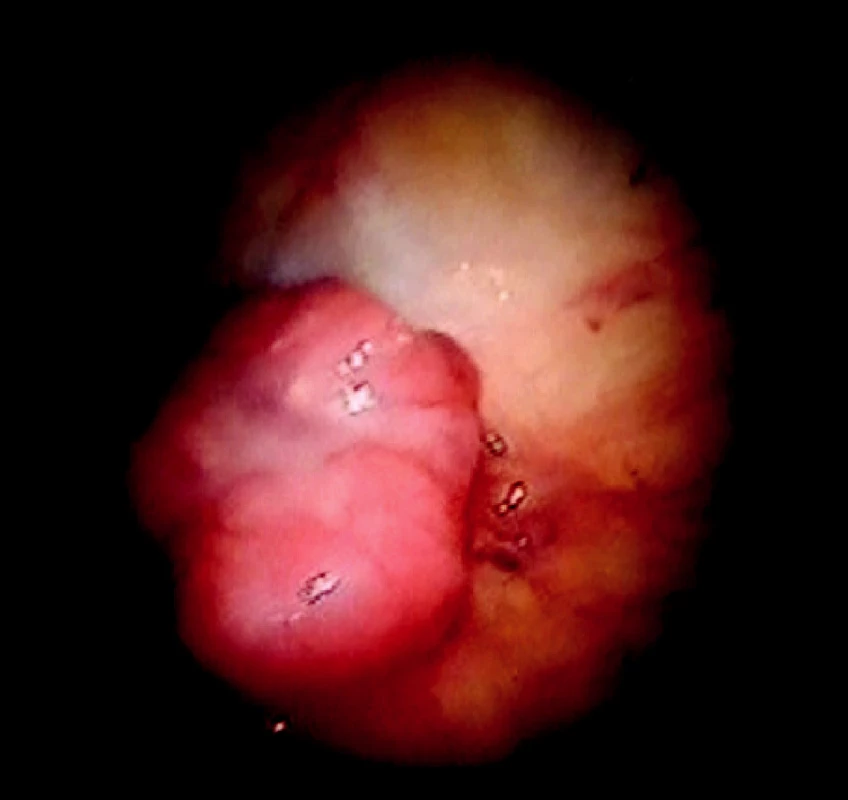
Image 4. Ložisko adenokarcinómu v autofluorescenčnom obraze Fig. 4. An autofluorescence view of the adenocarcinoma focus 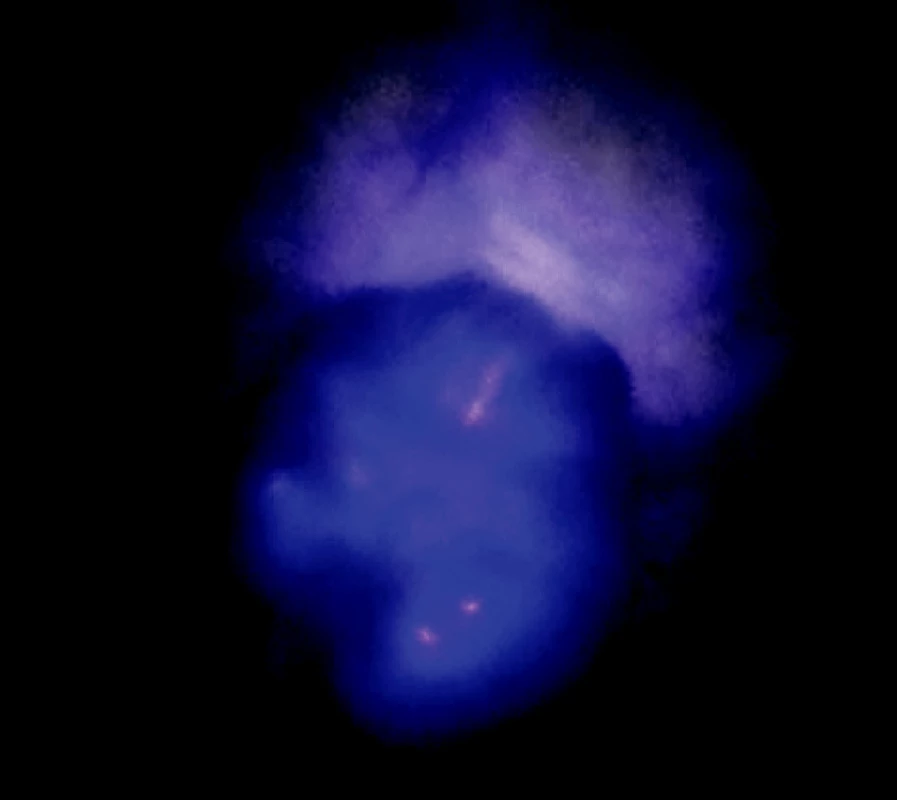
Na II. chirurgickej klinike UPJŠ LF, FN L. Pasteura v Košiciach sme v období marec až júl 2007 využili autofluorescenčnú videotorakoskopiu pri diagnostike ochorení pleury u 11 pacientov. Videotorakoskopia bola indikovaná pre pretrvávanie pleurálnej efúzie aj po opakovaných punkciách pri neznámej diagnóze. U 7 pacientov bolo diagnostikované malígne ochorenie (u 6 adenokarcinóm, u 1 metastatický rozsev malígneho melanómu), u 3 pacientov bolo diagnostikované zápalové postihnutie pleury a 1 pacienta difúzne poškodenie pľúc (chronická obliterujúca bronchiolitída) s chronickou nešpecifickou pleuritídou. Prvé skúsenosti ukázali, že využitím autofluorescenčnej videotorakoskopie môže operatér presnejšie určiť miesto chorobného ložiská na pleure, čím sa zvyšuje výťažnosť tejto metódy (Obr. 5, 6). Podobné farebné zmeny v autofluorescenčnom obraze sú viditeľné aj na viscerálnej pleure (Obr. 7, 8).
Image 5. Okraje nádorovej infiltrácie v bielom svetle Fig. 5. Tumorous infiltration margins in white light 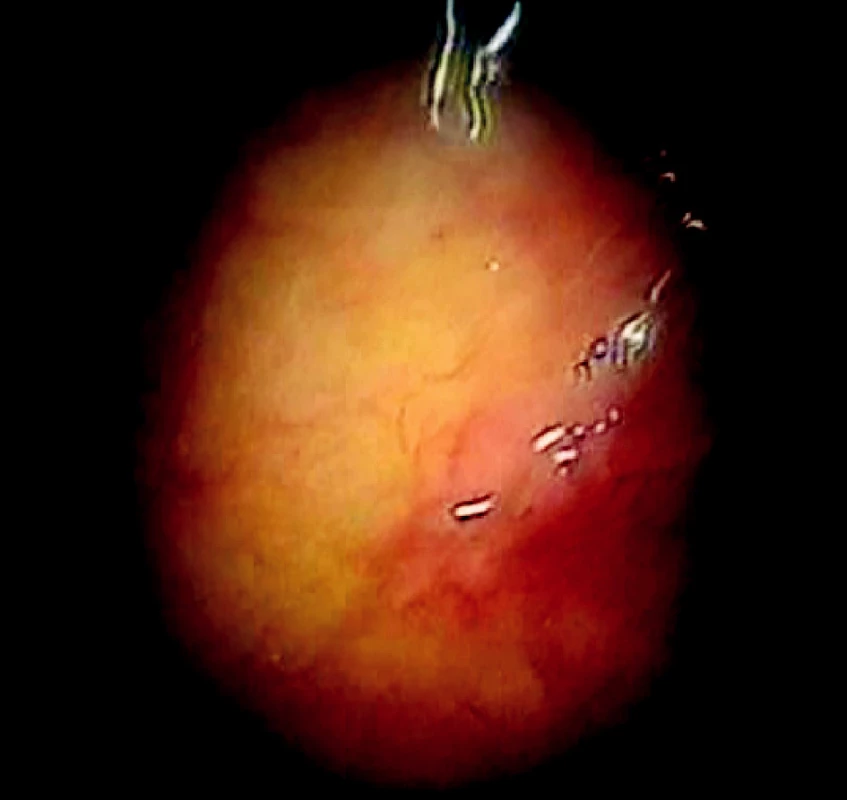
Image 6. Okraje nádorovej infiltrácie v autofluorescenčnom obraze Fig. 6. An autofluorescence view of the tumorous infiltration margins 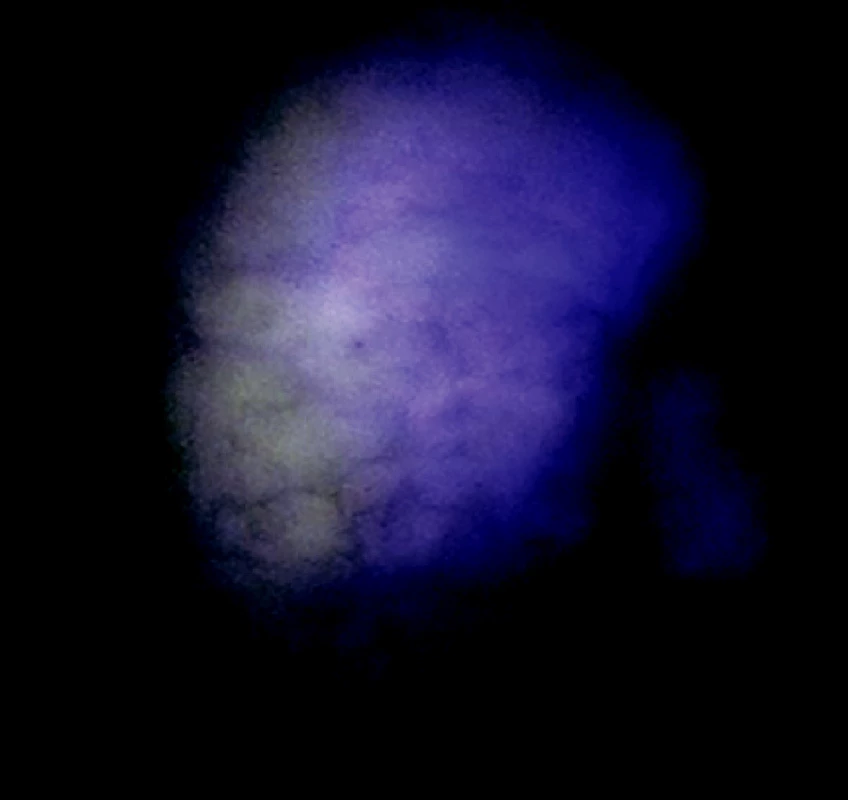
Image 7. Ložisko adenokarcinómu na viscerálnej pleure v bielom svetle Fig. 7. A visceral pleura adenocarcinoma focus in white light 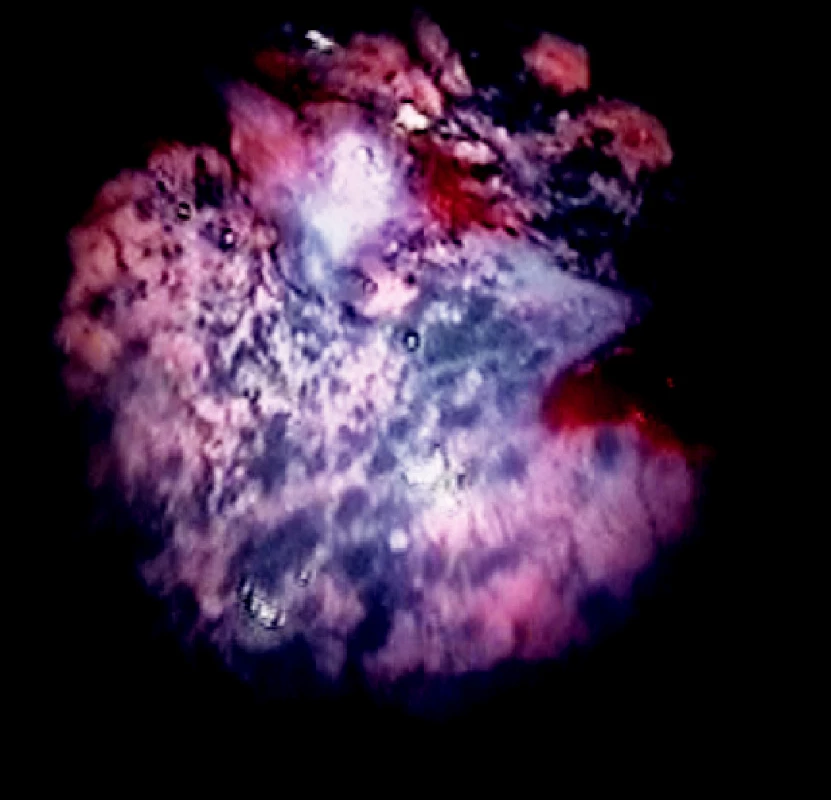
Image 8. Ložisko adenokarcinómu na viscerálnej pleure v autofluorescenčnom obraze Fig. 8. An autofluorescence view of the visceral pleura adenocarcinoma focus 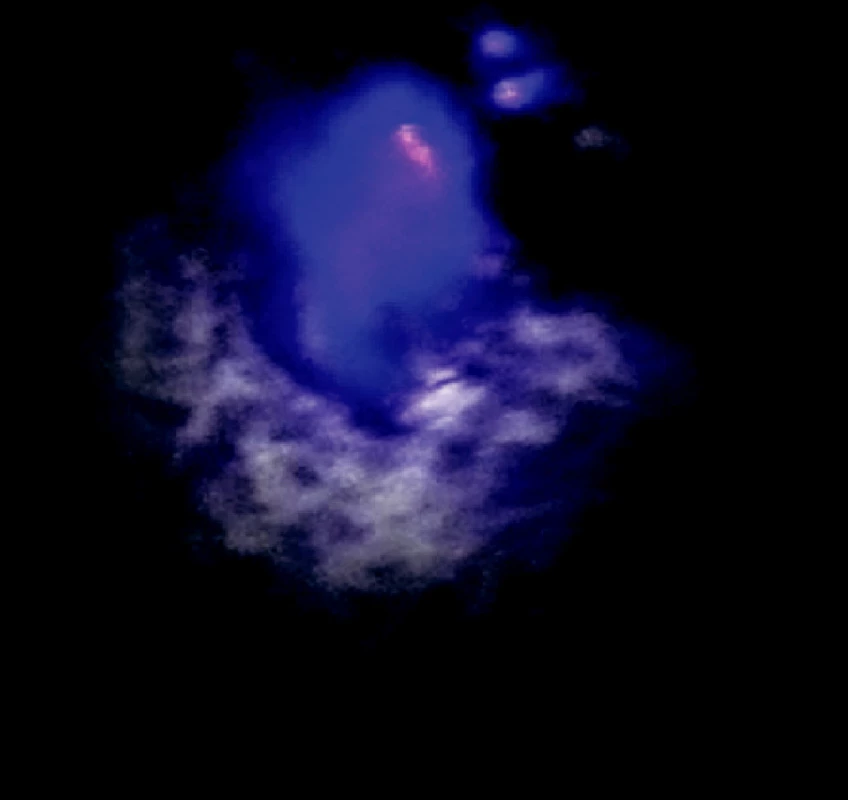
DISKUSIA
Pleurálny výpotok predstavuje každodenný klinický problém postihujúci viac ako milión pacientov ročne [11, 12]. Až 22 % týchto výpotkov je spôsobených malígnym ochorením, viac ako 100 000 malígnych výpotkov ročne si vyžaduje realizáciu primeraných liečebných opatrení [13]. Dominuje metastatické postihnutie pleury (95 %) oproti primárnym nádorom pleury. Pri exudatívnej pleurálnej efúzii pri neznámom origu vo viac ako 90 % dokáže videotorakoskopia určiť presne diagnózu [2, 3, 4, 14, 15]. Diagnostickú presnosť videotorakoskopie môže zlepšiť využitie autoflorescencie, ktorá umožní detekovať chorobne zmenené ložiská neviditeľné alebo nedostatočne viditeľné v bielom svetle [1].
Fluorescenčné zobrazovanie sa stalo atraktívnym pre endoskopické odbory pri zistení, že zdravé, nádorové a dysplastické tkanivá majú odlišnú emisiu fluorescenčného svetla po excitácii tkaniva modrofialovým svetlom. Po odblokovaní modrofialového svetla odrazeného od tkaniva vhodne konštruovaným emisným filtrom sa vizualizuje natívna fluorescencia (autofluorescencia) prevažne zelenej farby. Zelené svetielkovanie produkujú najmä štruktúry subepitelového väziva. Ak povrchová epiteliálna vrstva zhrubne pri dysplastickom a nádorovom procese, fluorescencia zelenej farby sa oslabí. To umožňuje lepšiu diagnostiku spomínaných procesov ako pri konvenčnej endoskopii. Výzvou pre zdokonalovanie techniky ostáva falošná pozitivita pri zápalových hyperplastických procesoch [5, 6].
Aj naše sledovanie ukázalo prínos autofluorescenčnej videotorakoskopie pri lokalizácii chorobného procesu pleury. Oproti bielemu svetlu pri autofluorescencii operujúci má možnosť presnejšie určiť okraj lézie a z väčšou presnosťou odobrať materiál na histologické vyšetrenie a po peroperačnej histologizácii procesu zvoliť adekvatné liečebné opatrenia.
ZÁVER
Touto prácou sme chceli upozorniť na možnosť využitia autofluorescenčnej videotorakoskopie pri diagnostike ochorení pleury. Autofluorescencenčné zobrazovanie presnejšie lokalizuje patologický proces, čo vedie k zvýšeniu výťažnosti videotorakoskopie pri diagnostike príčiny pleurálneho výpotku. Ďalšie skúsenosti budú publikované po vyhodnotení výsledkov sledovania využitia tejto metódy na väčšom súbore pacientov.
MUDr. J. Belák, PhD.
Lomonosovova 30
040 10 Košice
Slovenská republika
e-mail: belakjoz@central.medic.upjs.sk
Sources
1. Chrysanthidis, M. G., Janssen, J. P. Autofluorescence video-thoracoscopy in exudative pleural effusions: preliminary results. Eur. Respir. J., 2005; roč. 26, č. 6, s. 989–992.
2. Loddenkemper, R., Boutin, C. Thoracoscopy: present diagnostic and therapeutic indications. Eur. Respir. J., 1993, roč. 6, č. 10, s. 1544–1555.
3. Blanc, F. X., Atassi, K., Bignon, J., Housset, B. Diagnostic value of medical thoracoscopy in pleural disease. Chest, 2002, roč. 121, č. 5, s. 1677–1683.
4. Colt, H. G. Thoracoscopy window to the pleural space. Chest, 1999, roč. 116, č. 5, s. 1409–1415.
5. Wagnieres, G. A., Star, W., Wilson, B. C. In vivo fluorescence spectroscopy and imaging for oncological applications. Photochem. Photobiol., 1998, roč. 68, č. 5, s. 603–632.
6. Zeng, H., McWiliams, A., Lam, S. Optical spectroscopy and imaging for early lung cancer detection: a review. Photodiagnosis and Photodynamic Therapy, 2004, roč. 1, s. 111–122.
7. Babjuk, M., Petřík, R., Jirsa, M. Fluorescenční diagnostika nádorů močového měchýře. Praha: Triton, 2001, 126 s. ISBN 80-7254-195-1.
8. Horváth, T. Autofluorescenční diagnostika (AF) v bronchologii. Klin. Onkol., 1997, roč. 10, s. 195–196.
9. Prosst, R. L., Winkler, S., Boehm, E., Gahlen, J. Thoraco-scopic fluorescence diagnosis (TFD) of pleural malignancies :experimental studies. Thorax, 2002, roč. 57, č. 12, s. 1005–1009.
10. Baas, P., Triesscheijn, M., Burgers, S., van Pel, R., Stewart, F., Aalders, M. Fluorescence detection of pleural malignancies using 5-aminolaevulinic acid. Chest, 2006, roč. 129, č. 3, s. 718–724.
11. Light, R. W. Pleural diseases. Dis. Mon., 1992, roč. 38, č. 5, s. 261–331.
12. Marel, M., Zrustova, M., Stastny, B., Light, R. W. The incidence of pleural effusion in a well-defined region. Epidemiologic study in central Bohemia. Chest, 1993, roč. 104, č. 5, s. 1486–1489.
13. Lynch, T. J. Jr. Mangement of malignant pleural effusions. Chest, 1993, roč. 103, č., Suppl. 4, s. 3858–3898.
14. Benej, R., Haruštiak, S., Krajč, T. Nové trendy v hrudníkovej chirurgii. Medicínsky monitor, 2001, č. 3, s. 14–16.
15. Janík M., Haruštiak, S., Benej, R., Bohucký Š., Krajč, T. Management of malignant pleural diseases. Brat. lek. listy, 2002, roč. 102, č. 6, s. 304–305.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2007 Issue 10-
All articles in this issue
- Interdisciplinární přístup k řešení mnohočetných tepenných aneuryzmat u pacienta s osmou recidivou incizionální kýly – kazuistika
- Endovaskulární léčba stenóz karotických tepen s použitím cerebrální protekce: pětileté zkušenosti
- Léčba infekce cévní protézy a aorto-enterické píštěle jako pozdní komplikace rekonstrukčního výkonu na abdominální aortě – kazuistika
- Biliárny ileus – zriedkavá komplikácia cholecystolitiázy
- Role intersticiální brachyterapie v multimodalitní léčbě solidních tumorů
- Chirurgická léčba karcinomu prsu v MOÚ
- Nádorová kmenová buňka – nový pohled v onkologii?
- Nový přístup k léčbě jaterních metastáz: manuálně asistovaná laparoskopická radiofrekvenční resekce jater
- Autofluorescenčná videotorakoskopia – prvé vlastné skúsenosti
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Biliárny ileus – zriedkavá komplikácia cholecystolitiázy
- Chirurgická léčba karcinomu prsu v MOÚ
- Endovaskulární léčba stenóz karotických tepen s použitím cerebrální protekce: pětileté zkušenosti
- Nádorová kmenová buňka – nový pohled v onkologii?
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

