-
Medical journals
- Career
Role zobrazovacích metod v diagnostickém a terapeutickém postupu u cholesteatomu spánkové kosti
Authors: T. Bakaj 1; L. Bakaj Zbrožková 2; Richard Salzman 1; M. Heřman 2; I. Stárek 1
Authors‘ workplace: Otolaryngologická klinika LF UP a FN Olomouc 1; Radiologická klinika LF UP a FN Olomouc 2
Published in: Otorinolaryngol Foniatr, 65, 2016, No. 3, pp. 173-178.
Category: Review Article
Overview
V současné době se v chirurgické terapii cholesteatomu preferuje zavřená operační technika (canal wall up – CWU) nebo sekundárně zavřená technika (canal wall down – CWD s rekonstrukcí zadní-horní stěny zvukovodu, případně s obliterací trepanační dutiny). Vzhledem k relativně vysokému riziku ponechání reziduálního a/nebo vzniku rekurentního cholesteatomu je součástí postupů kontrolní, second-look operace. U většiny pacientů se ovšem recidiva neprokáže, a tím jsou vystaveni zbytečnému operačnímu riziku. Z toho vyplývá tendence detekovat recidivující cholesteatom pomocí méně invazivních metod. Významnou roli sehrávají zobrazovací metody, v poslední době především magnetická rezonance (MR), která vysokou prediktivní hodnotou překonala dříve používanou výpočetní tomografii s vysokým rozlišením (HRCT).
Práce shrnuje současné poznatky o možnostech zobrazovacích metod v primární diagnostice cholesteatomu středouší i jeho pooperačních recidiv. Jsou popsány a diskutovány možnosti HRCT a zejména význam nových technik MR: odloženého postkontrastního zobrazení (delayed postcontrast imaging – DPI), konvenčního echo-planárního (EPI) zobrazení difuze (difussion-weighted imaging – DWI) a non-echo-planárního zobrazení difuze (non-EPI DWI). Non-EPI DWI technika je dnes preferovaná a má největší přínos při hodnocení pooperačních změn a případných recidiv cholesteatomu.Klíčová slova:
cholesteatom, střední ucho, MR, non-EPI DWIÚVOD
Cholesteatom je cystický pseudotumor, lokalizovaný nejčastěji ve středním uchu, méně často v jiných oblastech skalní kosti (hrot pyramidy, zevní zvukovod). Extrapyramidálně se ponejvíce vyskytuje v mostomozečkovém koutu ve formě epidermoidní cysty. Jeho stěnu tvoří matrix, pozůstávající ze dvou vrstev, rohovějícího dlaždicobuněčného epitelu produkujícího koncentrické vrstvy keratinu, které vyplňují dutinu vaku cholesteatomu a plochého epitelu, který odpovídá epitelu mediální stěny bubínku (23). Na zevním obvodu matrix se v některých případech nachází vrstva granulační tkáně – perimatrix, která se podílí na jeho invazivním růstu. Ten je zapříčiněn působením enzymů (alkalická fosfatáza, kolagenáza atd.) a osteoklastů, které způsobují erozi kostěných struktur spánkové kosti i středoušních kůstek.
Etiopatogeneticky jde o nejednotné onemocnění, na němž se vedle embryonálních poruch (kongenitální cholesteatom) účastní i další postnatálně se uplatňující faktory (metaplázie epitelu, retrakční kapsy, dysfunkce Eustachovy tuby) (získaný cholesteatom).
Celková incidence všech forem cholesteatomu činí u dospělých 10–13/100 000, u dětí 3/100 000.
V současné době je jediným racionálním řešením cholesteatomu jeho chirurgické odstranění, které splňuje i preventivní aspekt vzniku intratemporálních a/nebo intrakraniálních komplikací. Jen v ojedinělých případech, zejména u starších pacientů, u kterých je celková narkóza riziková, je možné konzervativní řešení, tj. dispenzarizace a udržování cholesteatomu pod kontrolou pomocí otomikroskopické debridement techniky.
Chirurgicky je možno postupovat otevřenou operační technikou, tzv. canal wall down (CWD), při které se snáší zadní stěna zvukovodu a laterální stěna atiku za účelem vytvoření společné trepanační dutiny zahrnující zvukovod a bradavkový výběžek (6). Tato technika umožňuje velmi dobrý přehled v exponované oblasti a je spojena s nižším rizikem recidivy choleseteatomu (27). Její nevýhodou je otevřená dutina, která vyžaduje ochranu před vniknutím vody a v závislosti na velikosti a individuální reaktibilitě může být zdrojem větších či menších pooperačních obtíží. Mezi ty patří hlavně akumulace keratinu a ušního mazu s nutností pravidelné toalety a opakující se infekce vyžadující intenzivní konzervativní terapii.
Další možností je zachování zadní stěny zvukovodu, tzv. canal wall up (CWU) technika (28). Její výhodou je absence trepanační dutiny a podle některých autorů přináší i lepší sluchový zisk (38). Pro tyto důvody je v dnešní době, zejména u dětských pacientů, upřednostňována (11, 38). Tato technika je však ve srovnání s CWD spojena s asi trojnásobně vyšším rizikem reziduální nebo rekurentní choroby (48). Je to způsobeno menším přehledem operačního pole (21) a přetrváváním výše uvedených rizikových etiopatogenetických faktorů vzniku tohoto onemocnění.
Snaha o úplnou eliminaci problémů spojených s trepanačními dutinami při možnosti kompletní peroperační expozice vedla k vytvoření sekundární zavřené techniky (CWD s rekonstrukcí zadní-horní stěny zvukovodu, případně s obliterací trepanační dutiny) (9, 34). Procento recidiv cholesteatomu u tohoto postupu dosahuje hodnot porovnatelných s CWD, pohybuje se v rozmezí 12–24 % (12, 19).
Protože se, na rozdíl od otevřené techniky, u CWU i sekundárně zavřené techniky recidiva ve většině případů objeví v oblastech skrytých otomikroskopickému vyšetření (36), indikuje se u těchto postupů kontrolní, tzv. second-look operace s odstupem 9–24 měsíců (11).
U většiny pacientů se ovšem recidiva cholesteatomu neprokáže, tito nemocní jsou tudíž vystaveni zbytečnému operačnímu riziku.
Z toho vyplývá snaha detekovat recidivu cholesteatomu neinvazivně – pomocí zobrazovacích metod. Klasický sumační RTG snímek i tomografie vykazovaly velmi nízkou senzitivitu i specificitu a s nástupem moderních zobrazovacích metod se staly zcela obsolentní. Významnou roli sehrává výpočetní tomografie (CT) a v poslední době především magnetická rezonance (MR).
CT ZOBRAZOVÁNÍ CHOLESTEATOMU
Velký posun v dané problematice znamenalo zavedení CT, zejména výpočetní tomografie s vysokým rozlišením (high resolution computed tomography HRCT) (45). Při současné technologii je doba vyšetření krátká, což představuje minimální diskomfort pro nemocného a rovněž umožňuje vyšetření dětského pacienta bez celkové narkózy.
Vyšetření poskytuje jak excelentní kontrast mezi kostěnými strukturami, vzduchem, měkkou tkání a tekutinou, tak i výborné prostorové rozlišení. Proto je metodou volby v zobrazení spánkové kosti a hraje důležitou roli v předoperační i pooperační diagnostice cholesteatomu.
HRCT se indikuje před primárním operačním výkonem k určení anatomických poměrů, rozsahu patologie a vyloučení případných zánětlivých komplikací vyplývajících z osteitidy (37, 55). Zobrazí středoušní dutinu, řetěz kůstek, vnitřní ucho, polohu kanálu lícního nervu esovitého splavu, strop epitympana, antra i mastoidu, bulbus jugulární žíly, kanál vnitří karotidy. Může odhalit různé anatomické variace, jako vysoce postavený bulbus jugulární žíly, významnou asymetrii foramen jugulare, anteponovaný nebo lateralizovaný sigmoidální splav, hluboký sinus tympani nebo aberatní vnitřní krkavici, které mohou mít následně vliv na operační výkon (49). Varuje chirurga před možným nebezpečím vyplývajícím z povahy nemoci, jako např. obnažená dura střední lební jámy nebo dehiscence kanálu lícního nervu.
Cholesteatom se na HRCT zobrazí jako homogenní, nekalcifikovaná léze s měkkotkáňovou denzitou v pneumatizovaných oblastech středního ucha (4). Léze je typicky uzlovitá s okrouhlými, polycyklickými konvexními okraji. Toto zobrazení je možné pouze při normální nebo částečně omezené vzdušnosti středoušní dutiny. Pokud je pneumatizace značně redukována nebo vymizelá, na přítomnost cholesteatomu lze soudit jen z nepřímých známek, osteolýzy přilehlé kosti a/nebo částečné či kompletní demineralizace středoušních kůstek (32, 44) (obr. 1).
Image 1. HRCT spánkové kosti, primární cholesteatom levého středouší. 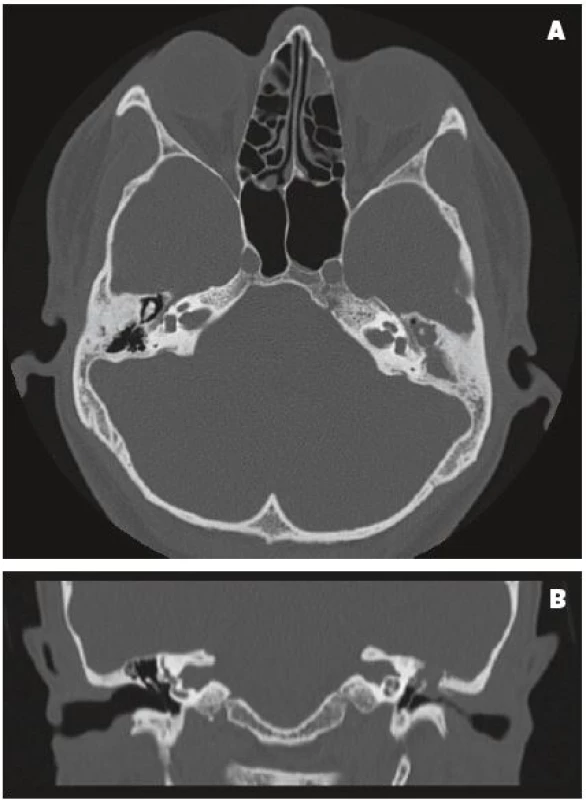
A – axiální rovina, levostranné epitympanum, aditus a antrum mastoidu je kompletně vyplněné patologickou hmotou s měkkotkáňovou denzitou, patrná eroze hlavičky kladívka a osteolýza těla a krátkého výběžku kovadlinky. B – koronární rovina, levostranné epitympanum je vyplněné patologickou hmotou s měkkotkáňovou denzitou s konvexními okraji, přítomná parciální osteolýza scuta a eroze tegmen tympani. Tři základní znaky pro primární cholesteatom na HRCT shrnuje Chee a spol. (22): nodulární měkkotkáňová masa, typická lokalizace pro cholesteatom a osteolýza přilehlé kosti. Senzitivita metody se pohybuje od 61 % do 94 % (16, 18, 22, 41, 46), specificita od 56 % do 95 % (16, 41, 46), zejména v závislosti na typu cholesteatomu podle lokalizace a jeho rozsahu. Navíc, HRCT v kombinaci s otoskopickým nálezem zvyšuje diagnostickou senzitivitu na 89 %, hodnota specificity je 92 %, pozitivní prediktivní hodnoty 97 % a negativní prediktivní hodnoty 73 % (16).
U pooperačního HRCT se posuzují zejména operačně změněné kostní poměry a přítomnost možného cholesteatomu. Pro druhé uvedené dosahuje vyšetření vysokou, téměř 100% negativní prediktivní hodnotu, ale jen za podmínky absence hmot s měkkotkáňovou denzitou a kompletně vzdušného středouší (26). Tento stav je ovšem vzácný. Při částečné a/nebo kompletní opacifikaci středoušní dutiny HRCT nedokáže na základě hodnot denzity odlišit recidivující cholesteatom od granulační tkaně, cholesterolového granulomu, edému sliznice, fibrózy, jizvy nebo tekutiny (26, 32, 47). V těchto případech, s odstupem 9–18 měsíců od primární operace, se recidiva cholesteatomu peroperačně prokázala ve 46–64 % (4, 51, 56). Rovněž diferenciace kostních změn způsobených sanačním operačním výkonem od patologické destrukce kosti zapříčiněné cholesteatomem není spolehlivá. Proto HRCT v zobrazení cholesteatomu spánkové kosti v pooperačním období dosahuje nízkou senzitivitu (43 %), specificitu (47 %) i prediktivní hodnotu (29 %) (5, 47).
MR ZOBRAZOVÁNÍ CHOLESTEATOMU
MR se donedávna používala jen při podezření na intrakraniální komplikace středoušních zánětů (meningitida, epidurální nebo subdurální empyém, trombóza žilního splavu, cerebritida nebo absces) (52).
Při použití standardních sekvencí (T1-vážených obrazů, T2-vážených obrazů) v zobrazování patologií středouší jsou výsledky nespecifické. Není možné navzájem rozlišit edém sliznice, granulační tkáň, tekutinu, jizvu a cholesteatom. Tyto patologické jednotky mají variabilně nízký stupeň intenzity signálu na T1-váženém obraze a různě vysoký signál na T2-váženém obraze v závislosti na obsahu vody a proteinů (31). Výjimkou je cholesterolový granulom, který vykazuje charakteristickou vysokou intenzitu signálu na T1-váženém obraze. Další možnou patologií středouší je encefalokéla, jejíž diagnostika na T1 a T2-vážených obrazech v koronální nebo sagitální rovině většinou nečiní potíže.
Cholesteatom, stejně jako epidermoidní cysta, je neprokrvená, cystická léze bohatá na keratin. Nové, specifické MR techniky využívají právě tyto histopatologické charakteristiky k přesnému rozlišení od jiných lézí. První zobrazovací technikou, která se začala využívat v diagnostice cholesteatomu, byla technika odloženého postkontrastního zobrazení (delayed postcontrast imaging – DPI) (56).
Podstatou odloženého postkontrastního zobrazování je zhotovení T1-vážených obrazů po 30–60 minutách od intravenózní aplikace paramagnetické kontrastní látky. V neperfundovaném cholesteatomu nedojde ke zvýšení intenzity signálu na rozdíl od fibrózních a zánětlivých tkání, granulací a jizev, které jsou v této fázi nasycené (4) (obr. 2). Časný náběr dat by mohl vést k falešně negativnímu nálezu (56). Falešně pozitivní nálezy, které vedou ke snížení specificity DPI techniky, mohou být zapříčiněny záměnou operačního výplňového materiálu obsahujícího silikon, zachovaných středoušních kůstek či kalcifikované jizvy za cholesteatom. Nejvíce falešně negativních nálezů je u velmi malých lézí (menších než 3 mm) v důsledku limitované rozlišovací schopnosti MR (4, 56). V literatuře udávaná senzitivita u recidivujících cholesteatomových lézí větších než 3 mm činí 85–100 %, specificita 75–100 % (4, 51, 56). Nevýhodou DPI vyšetření je jeho časová náročnost a obtížnější vyhodnocení nálezu vyžadující zkušeného radiologa (51).
Image 2. MR spánkové kosti, technika odloženého postkontrastního zobrazení (DPI) po 40 minutách od i. v. aplikace paramagnetické kontrastní látky, axiální rovina. V levostranném středouší je přítomná oválná, homogenní hyposignální léze s hypersignálními okraji odpovídající cholesteatomu o velikosti 6 mm, který byl i peroperačně potvrzen. 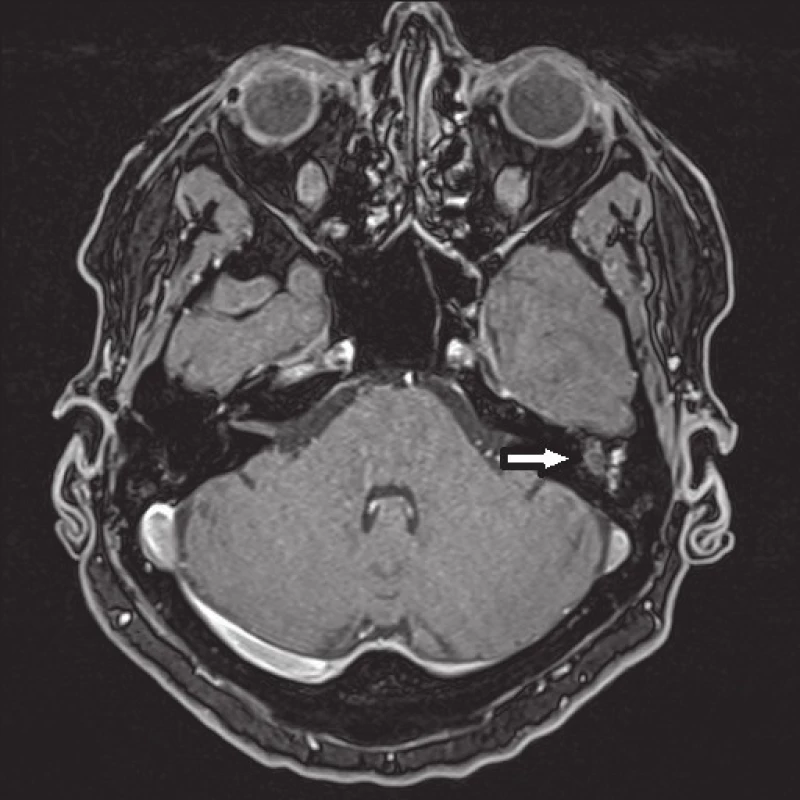
Nověji se v diagnostice cholesteatomu pomocí MR využívá zobrazování difuze (diffusion-weighted imaging – DWI). Metoda je založena na detekci neuspořádaného pohybu molekul vody ve tkáních, vyvolaného působením silných gradientů magnetického pole. Tento difuzní pohyb je omezen u cholesteatomu. V něm akumulovaný keratin obsahuje minimální množství vody, což se při vysoké b hodnotě (800–1000 s/mm2) na DWI sekvencích a i s přispěním T2 „shine-through“ efektu projeví zvýšenou intenzitou signálu v porovnání s mozkovou tkání. Podobný obraz má i intrakraniální epidermoidní cysta. K diagnostice cholesteatomu je možné využít konvenční echo-planární (EPI) DWI nebo s výhodou novější non-echo-planární (non-EPI) DWI techniku (35, 50).
EPI DWI jsou sekvence využívající princip gradientního echa. Jsou rutinně používané v diagnostice patologií mozkové tkáně. Při zobrazování cholesteatomu středního ucha vykazují jisté limitace, a to především z důvodu přítomnosti četných susceptibilních artefaktů vznikajících na rozhranní vzduch/kost a nižší rozlišovací schopnosti. Ty se projeví výrazně nižší senzitivitou u lézí menších než 5 mm (1, 14, 15, 16, 51, 53). Celková senzitivita metody se pohybuje od 60 do 80 %, specificita je uváděna v rozmezí 73–100 % (14, 16, 51, 53). Někteří autoři prokázali zvýšení výtěžnosti kombinací EPI DWI s odloženým postkontrastním zobrazením (DPI) (14, 51). Ovšem tento postup pro již výše uvedené důvody nenašel v klinické praxi širší uplatnění.
V průběhu poslední dekády byly vyvinuty non-EPI DWI techniky mající různé firemní názvy: single-shot turbo spin-echo DWI, half-Fourier acquisition single-shot turbo spin-echo (HASTE) DWI (Siemens) (obr. 3), multi-shot DWI turbo spin-echo, PROPELLER DWI (GE), BLADE DWI (Siemens), MultiVane (Philips). Tyto sekvence, pracující na principu spinového echa, mají díky redukované šířce vrstvy a minimalizaci většiny susceptibilních artefaktů lepší rozlišovací schopnost a umožňují zobrazení lézí menších velikostí než u echo-planárního DWI (24, 30). Senzitivita této metody se pohybuje se v rozmezí 82–96 % (2, 3, 7, 8, 17, 20, 25, 33, 42). Někteří autoři udávají dokonce absolutní čísla (10, 13, 29, 39, 43). Oproti tomu nižší senzitivitu uvádí von Kalle a kol. – 76 % (54) a Plouin a kol. – 62 % (40). Důvodem je relativně vysoký počet falešně negativních nálezů a ve druhém případě i menší počet probandů, kteří byli zahrnuti do studie.
Image 3. MR spánkové kosti , technika non-echo-planárního difuzně váženého zobrazení (non-EPI DWI), axiální rovina. 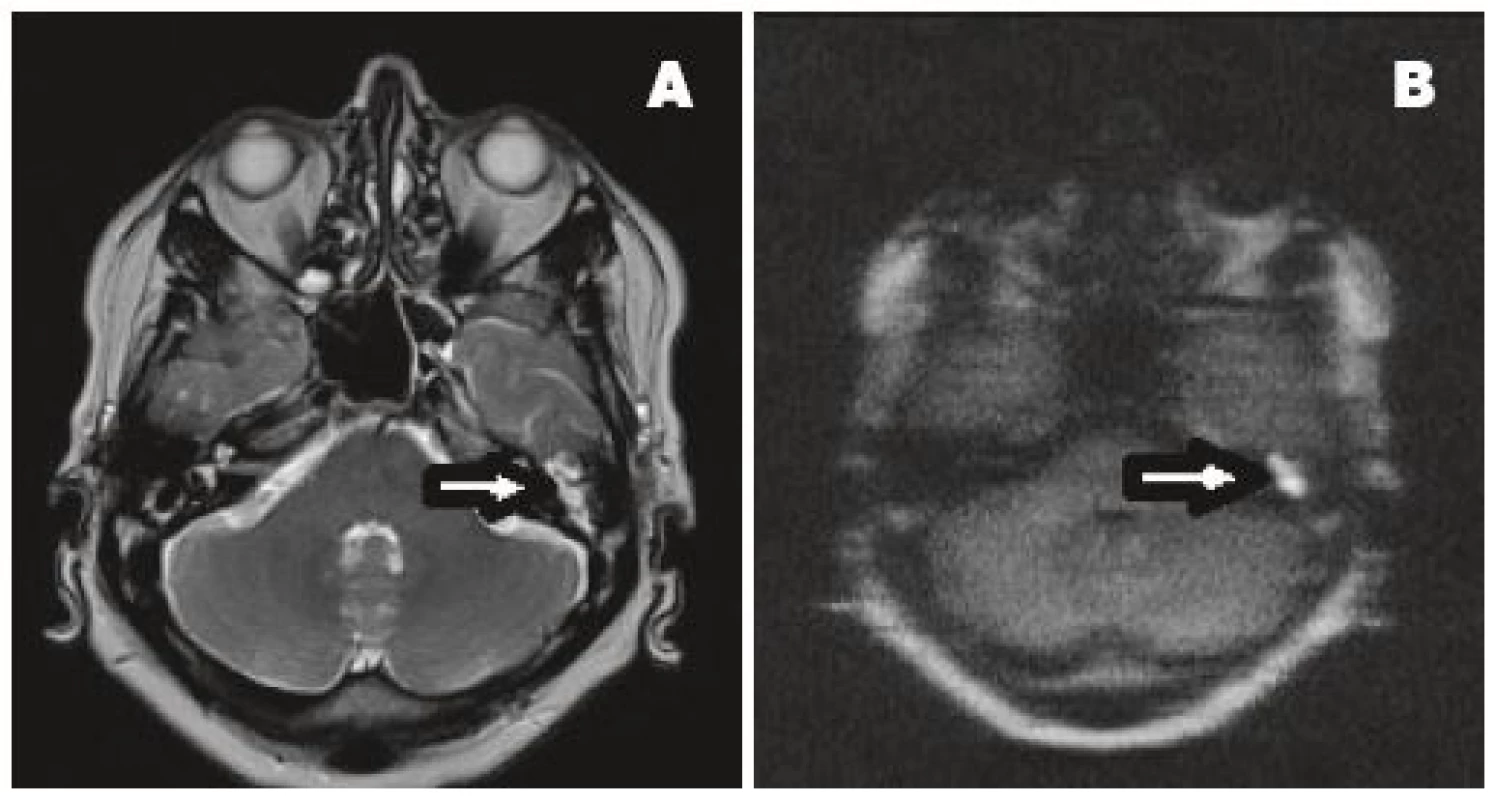
A – T2-vážený obraz, v oblasti levostranného epitympana, aditu a antra mastoidu je patrná homogenní hypersignální léze. B – DWI (HASTE sekvence), daná léze je hypersignální, nález svědčí pro cholesteatom o velikosti 17x8 mm, který byl i peroperačně potvrzen. Hodnoty specificity jsou uváděny většinou v rozmezí 88–93 % (2, 8, 13, 25, 33, 54). Další autoři dosahují 100% hodnot (3, 7, 10, 20, 29, 39, 43). Výjimečně udávané nižší hodnoty 71 % (40) a 55 % (17) byly způsobeny relativně vysokým výskytem falešně pozitivních nálezů u prvně jmenovaného a malým počtem vyšetření u následujícího.
Různí autoři udávají odlišnou kritickou velikost cholesteatomu pro jeho detekci na non-EPI DWI MR. Ta podle některých, bez závislosti na technických parametrech přístrojů, činí 2 mm (2, 7, 25, 39), dle jiných 3 mm (3, 8, 10, 20, 29, 42, 43, 54 ) nebo 4 mm (40). Senzitivita metody u malých cholesteatomů je nižší než u cholesteatomů větších rozměrů (7, 54). Důvody proč takto malé léze nejsou zobrazitelné na DWI MR vyplývají z možností prostorového rozlišení MR přístroje.
Zdrojem signálu na DWI MR je restrikce difuze v keratinu. Z tohoto důvodu nacházíme pozitivní nález i u jím vyplněných retrakčních kapes (3). Oproti tomu tyto útvary s malým (2, 25, 54) či žádným obsahem keratinových hmot (8, 54) nejsou pomocí DWI detekovatelné. Stejně je tomu i u nástěnného cholesteatomu, u kterého došlo ke spontánní evakuaci obsahu (33, 40).
Mezi falešně negativní nálezy na MR se řadí i cholesteatom asociovaný s cholesterolovým granulomem (2), cholesteatom v koexistenci s hematomem (42) či okolním zánětem (3). Další možnou příčinou falešné negativity jsou pohybové artefakty (20).
Metoda je zatížena i falešně pozitivní nálezy, mezi které patří artefakty vznikající na rozhranní kost/vzduch (7, 8) a artefakty ze zubních rovnátek (40). Pozitivní nález může imitovat i kostní prach (17), např. použitý k uzávěru píštěle laterálního kanálku (13), kostní apozitum v nadbubínkové dutině (33) či cizorodý materiál na bázi polymerních silikonových sloučenin (Silastic) (51). Falešně pozitivní nález byl popsán i u abscesu (17, 42) nebo purulentního obsahu v bradavčitém výběžku (2).
ZÁVĚR
HRCT zhotovené v předoperačním období je schopno zobrazit rozsah cholesteatomu i případné ostitické změny. Při nejasném klinickém nálezu zvyšuje přítomnost hmot s měkkotkáňovou denzitou, konvexními konturami spolu s erozí středoušních kůstek a/nebo přilehlé kosti na HRCT senzitivitu diagnostických metod. Na pooperačním HRCT je pro operačně změněné kostní poměry nález hmot s měkkotkáňovou denzitou nespecifický a jednoznačné rozlišení recidivy cholesteatomu od zánětlivých změn, granulační tkáně, tekutiny, fibrózy nebo cholesterolového granulomu není možné.
MR s využitím non-EPI DWI zobrazení je vhodná metoda k detekci jak primárního, tak i recidivujícího cholesteatomu u dospělých i dětských pacientů. Největší přínos má u recidivujícího cholesteatomu, kde je výhodnou alternativou k second-look operacím. Metoda má vysokovu senzitivitu, specificitu, pozitivní i negativní prediktivní hodnotu.
Práce byla podpořena MZ ČR – RVO (FNOL 00098892) a RVO (LF UP 61989592).
Adresa ke korespondenci:
MUDr. Tomáš Bakaj
Otolaryngologická klinika FN Olomouc
I. P. Pavlova 6
779 00 Olomouc
e-mail: bakaj.t@seznam.cz
Sources
1. Aikele, P., Kittner, T., Offergeld, C. et al.: Diffusion-weighted MR imaging of cholesteatoma in pediatric and adult patients who have undergone middle ear surgery. AJR Am. J. Roentgenol., 181, 2003, 1, s. 261-265.
2. Akkari, M., Gabrillargues, J., Saroul, N. et al.: Contribution of magnetic resonance imaging to the diagnosis of middle ear cholesteatoma: analysis of a series of 97 cases. Eur Ann. Otorhinolaryngol. Head Neck Dis., 131, 2014, 3, s. 153-158.
3. Alvo, A., Garrido, C., Salas, Á. et al.: Use of non-echo-planar diffusion-weighted MR imaging for the detection of cholesteatomas in high-risk tympanic retraction pockets. AJNR Am. J. Neuroradiol., 35, 2014, 9, s. 1820-1824.
4. Ayache, D., Williams, M. T., Lejeune, D. et al.: Usefulness of delayed postcontrast magnetic resonance imaging in the detection of residual cholesteatoma after canal wall-up tympanoplasty. Laryngoskope, 115, 2005, 4, s. 607-610.
5. Blaney, S. P., Tierney, P., Oyarazabal, M. et al.: CT scanning in „second look“ combined approach tympanoplasty. Rev. Laryngál. Otol Rhinol. (Bord), 121, 2000, 2, s. 79-81.
6. Brown, J. S.: A ten year statistical follow-up of 1142 consecutive cases of cholesteatoma: the closed vs. the open technique. Laryngoskope, 92, 1982, 4, s. 390-396.
7. De Foer, B., Vercruysse, J. P., Bernaerts, A. et al.: Detection of postoperative residual cholesteatoma with non-echo-planar diffusion-weighted magnetic resonance imaging. Otol. Neurotol., 29, 2008, 4, s. 513-517.
8. De Foer, B., Vercruysse, J. P., Bernaerts, A. et al.: Middle ear cholesteatoma: non-echo-planar diffusion-weighted MR imaging versus delayed gadolinium-enhanced T1-weighted MR imaging–value in detection. Radiology, 255, 2010, s. 866-872.
9. Deveze, A., Rameh, C., Puchol, M. S. et al.: Rehabilitation of canal wall down mastoidectomy using a titanium ear canal implant. Otol. Neurotol., 31, 2010, 2, s. 220-224.
10. Dhepnorrarat, R. C., Wood, B., Rajan, G. P.: Postoperative non-echo-planar diffusion-weighted magnetic resonance imaging changes after cholesteatoma surgery: implications for cholesteatoma screening. Otol. Neurotol., 30, 2009, 1, s. 54-58.
11. Dodson, E. E., Hashisaki, G. T., Hobgood, T.C. et al.: Intact canal wall mastoidectomy with tympanoplasty for cholesteatoma in children. Laryngoskope, 108, 1998, 7, s. 977-983.
12. Dornhoffer, J. L.: Retrograde mastoidectomy with canal wall reconstruction: a follow-up report. Otol. Neurotol., 25, 2004, 5, s. 653-660.
13. Dubrulle, F., Souillard, R., Chechin, D. et al.: Diffusion-weighted MR imaging sequence in the detection of postoperative recurrent cholesteatoma. Radiology, 238, 2006, 2, s. 604-610.
14. Emonot, G., Richard, C., Dumollard, J. M. et al.: Contribution of MRI to diagnosis of residual cholesteatoma. Fr. ORL, 94, 2008, s. 366-374.
15. Fitzek, C., Mewes, T., Fitzek, S. et al.: Diffusion-weighted MRI of cholesteatomas of the petrous bone. J. Magn. Reson Imaging, 15, 2002, 6, s. 636-641.
16. Ganaha, A., Outa, S., Kyuuna, A. et al.: Efficacy of diffusion-weighted magnetic resonance imaging in the diagnosis of middle ear cholesteatoma. Auris Nasus Larynx, 38, 2011, 3, s. 329-334.
17. Garrido, L., Cenjor, C., Montoya, J. et al.: Diagnostic capacity of non-echo planar diffusion-weighted MRI in the detection of primary and recurrent cholesteatoma. Acta Otorrinolaringol. Esp., 66, 2015, 4, s. 199-204.
18. Gomaa, M. A., Abdel Karim, A. R., Abdel Ghany, H. S. et al.: Evaluation of temporal bone cholesteatoma and the correlation between high resolution computed tomography and surgical finding. Clin. Med. Insights Ear Nose Throat, 23, 2013, 6, s. 21-28.
19. Hatano, M., Ito, M., Yoshizaki, T.: Retrograde mastoidectomy on demand with soft-wall reconstruction in pediatric cholesteatoma. Acta Otolaryngol., 130, 2010, 10, s. 1113-1118.
20. Huins, C. T., Singh, A., Lingam, R. K. et al.: Detecting cholesteatoma with non-echo planar (HASTE) diffusion-weighted magnetic resonance imaging. Otolaryngol. Head Neck Surg., 143, 2010, 1, s. 141-146.
21. Hulka, G. F., McElveen, J. T. Jr.: A randomized, blinded study of canal wall up versus canal wall down mastoidectomy determining the differences in viewing middle ear anatomy and pathology. Am. J. Otol., 19, 1998, 5, s. 574-578.
22. Chee, N. W., Tan, T. Y.: The value of pre-operative high resolution CT scans in cholesteatoma surgery. Singapore Med. J., 42, 2001, 4, s. 155-159.
23. Chrobok, V., Pellant, A., Profant, M.: Cholesteatom spánkové kosti, Havlíčkův Brod, Tobiáš, 2008, s. 70-79.
24. Jindal, M., Riskalla, A., Jiang, D. et al.: A systematic review of diffusion-weighted magnetic resonance imaging in the assessment of postoperative cholesteatoma. Otol. Neurotol., 32, 2011, s. 1243-1249.
25. Khemani, S., Lingam, R. K., Kalan, A. et al.: The value of non-echo planar HASTE diffusion-weighted MR imaging in the detection, localisation and prediction of extent of postoperative cholesteatoma. Clin. Otolaryngol., 36, 2011, 4, s. 306-312.
26. Khemani, S., Singh, A., Lingam, R. K. et al.: Imaging of postoperative middle ear cholesteatoma. Clin. Radiol., 66, 2011, 8,, s. 760-767.
27. Kerckhoffs, K. G., Kommer, M. B., Van Strien, T. H. et al.: The disease recurrence rate after the canal wall up (CWU) or canal wall down (CWD) technique in adults. Laryngoskope, 25, 2005.
28. Koval, J.: Chirurgická liečba chronického stredoušného zápalu, Bratislava, USPO, 1998, s. 81-90.
29. Lehmann, P., Saliou, G., Brochart, C. et al.: 3T MR imaging of postoperative recurrent middle ear cholesteatomas: value of periodically rotated overlapping parallel lines with enhanced reconstruction diffusion-weighted MR imaging. AJNR Am. J. Neuroradiol., 30, 2009, 2, s. 423-427.
30. Li, P. M., Linos, E., Gurgel, R. K. et al.: Evaluating the utility of non-echo-planar diffusion-weighted imaging in the preoperative evaluation of cholesteatoma: a meta-analysis.Laryngoscope, 123, 2013, 5, s. 1247-1250.
31. Martin, N., Sterkers, O., Nahum, H.: Chronic inflammatory disease of the middle ear cavities: Gd-DTPA-enhanced MR imaging. Radiology, 176,1990, 2, s. 399-405.
32. Más-Estellés, F., Mateos-Fernández, M., Carrascosa-Bisquert, B. et al.: Contemporary non-echo-planar diffusion-weighted imaging of middle ear cholesteatomas.Radiographics, 32, 2012, 4, s. 1197-1213.
33. Mateos-Fernández, M., Mas-Estellés, F., de Paula-Vernetta, C. et al.: The role of diffusion-weighted magnetic resonance imaging in cholesteatoma diagnosis and follow-up. Study with the diffusion PROPELLER technique. Acta Otorrinolaringol. Esp., 63, 2012, ec, 6, s. 436-442.
34. Mokbel, K. M., Khafagy, Y. W.: Single flap with three pedicles, bone paté and split-thickness skin graft for immediate mastoid obliteration after canal wall down mastoidectomy. Eur Arch. Otorhinolaryngol., 269, 2012, 9, s. 2037-2041.
35. Nash, R., Wong, P. Y., Kalan, A. et al.: Comparing diffusion weighted MRI in the detection of post-operative middle ear cholesteatoma in children and adults. Int. J. Pediatr. Otorhinolaryngol., 79, 2015, 12, s. 2281-2285.
36. Neudert, M., Lailach, S., Lasurashvili, N. et al.: Cholesteatoma recidivism: comparison of three different surgical techniques. Otol. Neurotol., 35, 2014, 10, s. 1801-1808.
37. Ng, J. H., Zhang, E. Z., Soon, S. R. et al.: Pre-operative high resolution computed tomography scans for cholesteatoma: has anything changed? Am. J. Otolaryngol., 35, 2014, 4, s. 508-513.
38. Osborn, A. J., Papsin, B. C., James, A. L.: Clinical indications for canal wall-down mastoidectomy in a pediatric population. Otolaryngol. Head Neck Surg., 147, 2012, 2, s. 316-322.
39. Pizzini, F. B., Barbieri, F., Beltramello, A. et al.: HASTE diffusion-weighted 3-Tesla magnetic resonance imaging in the diagnosis of primary and relapsing cholesteatoma. Otol. Neurotol., 31, 2010, 4, s. 596-602.
40. Plouin-Gaudon, I., Bossard, D., Fuchsmann, C. et al.: Diffusion-weighted MR imaging for evaluation of pediatric recurrent cholesteatomas. Int. J. Pediatr. Otorhinolaryngol., 74, 2010, 1, s. 22-26.
41 Prata, A. A. S, Antunes, M. L., de Abreu, C. E. C. et al.: Comparative study between radiological and surgical findings of chronic otitis media. Intl. Arch. Otorhinolaryngol, 15, 2011, 1, s. 72-78.
42. Profant, M., Sláviková, K., Kabátová, Z. et al.: I. Predictive validity of MRI in detecting and following cholesteatoma. Eur Arch. Otorhinolaryngol., 269, 2012, 3, s. 757-765.
43. Rajan, G. P., Ambett, R., Wun, L. et al.: Preliminary outcomes of cholesteatoma screening in children using non-echo-planar diffusion-weighted magnetic resonance imaging. Int. J. Pediatr. Otorhinolaryngol., 74, 2010, 3, s. 297-301.
44. Stasolla, A., Magliulo, G., Cortese, A. et al.: Preoperative imaging assessment of chronic otitis media: what does the otologist need to know? Radiol. Med., 116, 2011, 1, s. 114-124.
45. Swartz, J. D., Goodman, R. S., Russell, K. B. et al.: High-resolution computed tomography of the middle ear and mastoid. Part III: Surgically altered anatomy and pathology. Radiology, 148, 1983, 2, s. 461-464.
46. Tatlipinar, A., Tuncel, A., Öğredik, E. A. et al.: The role of computed tomography scanning in chronic otitis media. Eur Arch. Otorhinolaryngol., 269, 2012, 1, s. 33-38.
47. Tierney, P. A., Pracy, P., Blaney, S. P. et al.: An assessment of the value of the preoperative computed tomography scans prior to otoendoscopic ‚second look‘ in intact canal wall mastoid surgery. Clin. Otolaryngol. Allied Sci., 24, 1999, 4, s. 274-276.
48. Tomlin, J., Chang, D., McCutcheon, B. et al.: Surgical technique and recurrence in cholesteatoma: a meta-analysis. Audio. Neurootol., 18, 2013, 3, s. 135-142.
49. Tomura, N., Sashi, R., Kobayashi, M. et al.: Normal variations of the temporal bone on high-resolution CT: their incidence and clinical significance. Clin. Radiol.. 50, 1995, 3, s. 144-148.
50. Van Egmond, S. L., Stegeman, I., Grolman, W. et al.: A systematic review of non-echo planar diffusion-weighted magnetic resonanceiImaging for detection of primary and postoperative cholesteatoma. Otolaryngol. Head Neck Surg., 2015, 2. pii: 0194599815613073.
51. Venail, F., Bonafe, A., Poirrier, V. et al.: Comparison of echo-planar diffusion-weighted imaging and delayed postcontrast T1-weighted MR imaging for the detection of residual cholesteatoma. AJNR, Am. J. Neuroradiol., 29, 2008, 7, s. 1363-1368.
52. Verbist, B. M., Mancuso, A. A., Antonelli, P. J. et al.: Chronic otomastoiditis and acquired cholesteatoma. Head and neck radiology. Philadelphia, Lippincott Williams & Wilkins, 2011, s. 756-776.
53. Vercruysse, J. P., De Foer, B., Pouillon, M. et al.: The value of diffusion-weighted MR imaging in the diagnosis of primary acquired and residual cholesteatoma: a surgical verified study of 100 patients. Eur Radiol., 16, 2006, 7, s. 1461-1467.
54. Von Kalle, T., Amrhein, P., Koitschev, A.: Non-echoplanar diffusion-weighted MRI in children and adolescents with cholesteatoma: reliability and pitfalls in comparison to middle ear surgery. Pediatr. Radiol., 45, 2015, 7, s. 1031-1038.
55. Walshe, P., McConn Walsh, R., Brennan, P. et al.: The role of computerized tomography in the preoperative assessment of chronic suppurative otitis media. Clin. Otolaryngol. Allied Sci., 27, 2002, 2, s. 95-97.
56. Williams, M. T., Ayache, D., Alberti, C. et al.: Detection of postoperative residual cholesteatoma with delayed contrast-enhanced MR imaging: initial findings. Eur Radiol., 13, 2003, 1, s. 169-174.
Labels
Audiology Paediatric ENT ENT (Otorhinolaryngology)
Article was published inOtorhinolaryngology and Phoniatrics

2016 Issue 3-
All articles in this issue
- Změny hladin vybraných cytokinů Th1, Th2 a Treg v séru u chronických infekcí (vč. H. pylori) v orofaryngu v závislosti na podání DHA a EPA a/nebo tonzilektomii – pilotní studie
- Endoskopická ušní chirurgie: první zkušenosti
- Role zobrazovacích metod v diagnostickém a terapeutickém postupu u cholesteatomu spánkové kosti
- Nanočástice, nanotoxikologie, nanomedicína: definice pojmů, perspektivy v otorinolaryngologii
- Endoskopická ušní chirurgie: shrnutí problematiky
- Sekreční karcinom slinných žláz
- Ganglioneurom, raritní příčina nádoru měkkých tkání krku v dospělosti
- Orbitální absces - možná komplikace akutní rinosinusitidy i při důsledné konzervativní terapii
- Otorhinolaryngology and Phoniatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Nanočástice, nanotoxikologie, nanomedicína: definice pojmů, perspektivy v otorinolaryngologii
- Orbitální absces - možná komplikace akutní rinosinusitidy i při důsledné konzervativní terapii
- Sekreční karcinom slinných žláz
- Ganglioneurom, raritní příčina nádoru měkkých tkání krku v dospělosti
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

