-
Medical journals
- Career
Spektrum požadovaných vyšetrení nukleárnej medicíny pri karcinóme prostaty po registrácii 18F fluorocholínu: dvojročné sledovanie v nemocnici Tenon
Authors: Soňa Balogová () 1,2; Virginie Huchet () 1; Laure Michaud () 1,3; Khaldoun Kerrou () 1; Fréderique Paycha () 1; Valérie Nataf () 3,4; Marika Vereb () 5,6; Lucia Kaliská () 7; Françoise Montravers () 1,3; J.-N. Talbot () 1,3
Authors‘ workplace: Médecine nucléaire, Hôpital Tenon, AP–HP, Paris, Francúzsko 1; Klinika nukleárnej medicíny LF UK a OÚSA Bratislava, Slovensko 2; Université Pierre-et-Marie-Curie, Paris, Francúzsko 3; Radiopharmacie, Hôpital Tenon, AP–HP, 7 020 Paris, Francúzsko 4; Klinikum Kassel Nuklearmedizin, Kassel, Nemecko 5; Oddelenie nukleárnej medicíny, Reimanus s. r. o., Prešov, Slovensko 6; INMM Košice & Agel diagnostics s. r. o., Pracovisko Banská Bystrica, Slovensko 7
Published in: NuklMed 2012;1:42-47
Category: Original Article
Overview
Úvod:
Registrácia nového rádiofarmaka pre pozitrónovú emisnú tomografiu (PET) je výnimočným javom a je zaujímavé sledovať, aký vplyv má dostupnosť nového PET produktu na preskripciu vyšetrenia príslušnými klinikmi. 18F fluorocholín (FCH) bol vo Francúzsku zaregistrovaný v apríli 2010 pri karcinóme prostaty (KP) pre detekciu jeho kostných metastáz.Metódy:
Počas 8 štvrťrokov od apríla 2010 do marca 2012 bolo analyzované spektrum požadovaných vyšetrovacích metód nukleárnej medicíny u pacientov s KP. K dispozícii boli: konvenčná gamagrafia skeletu (GS), PET/CT s 18F fluorodeoxyglukózou (FDG), PET/CT s 18F fluoridom sodným (FNa) a PET/CT s FCH.Výsledky:
Počas dvoch rokov od registrácie FCH bolo u pacientov v rôznych klinických situáciách KP realizovaných 721 vyšetrení. Dopyt po PET/CT s FCH sa rýchlo zvyšoval: z 11 % v prvom štvrťroku na 37 % v druhom štvrťroku a 56 % v ôsmom štvrťroku. Zvýšil sa tiež celkový počet vyšetrení. Z celkového počtu vyšetrení PET/CT s FCH tvorila 42 %, PET/CT s FNa 27 %, GS 25 % a PET/CT s FDG 6 %. Vyšetrenia zamerané na detekciu kostnej reakcie na kostné metastázy (GS a PET/CT s FNa) boli žiadané najmä v rámci iniciálneho stagingu, PET/CT s FCH bola žiadaná najmä pri lokalizácii okultnej recidívy karcinómu prostaty pri nízkych hodnotách PSA. PET/CT s FDG bola indikovaná len zriedkavo, zväčša pri hormonálne refraktérnom KP. Monitorovanie efektu liečby je sľubnou indikáciou pre PET/CT s FCH, zodpovedalo 19 % všetkých PET/CT s FCH a vo všetkých prípadoch išlo o restaging KP pred nasadením ďalšej línie liečby.Záver:
Krátko po registrácii FCH bol zaznamenaný rýchly vzostup požiadaviek PET/CT s FCH a zvýšil sa aj celkový počet vyšetrení nukleárnej medicíny pri KP.Kľúčové slová:
karcinóm prostaty, fluorocholín (FCH), fluorid sodný (FNa), fluorodeoxyglukóza (FDG), gamagrafia skeletu (GS), preskripcia zobrazovacích metódÚvod
V súčasnosti sú na funkčné zobrazenie rozsahu karcinómu prostaty k dispozícii štyri zobrazovacie metódy nukleárnej medicíny 1-3:
- konvenčná gamagrafia skeletu (GS) s bifosfonátmi značenými 99mTc (planárna, SPECT, SPECT/CT)
- PET/CT skeletu s fluoridom sodným 18F-FNa
- PET/CT s fluorodeoxyglukózou 18F-FDG
- PET/CT s fluorocholínom 18F-FCH
Na oddelení nukleárnej medicíny nemocnice Tenon Assistance Publique-Hôpitaux de Paris & Université Pierre et Marie Curie (ďalej nemocnica Tenon), podobne ako na mnohých iných pracoviskách nukleárnej medicíny vo Francúzsku, sú k dispozícii všetky štyri vyšetrovacie metódy, ktoré sú indikované najmä urológmi a onkológmi: GS od roku 1980 (od vzniku pracoviska), FDG od roku 1997 (PET od roku 2000), FNa od roku 2008, kedy bol vo Francúzsku FNa zaregistrovaný a FCH v rámci protokolov klinického výskumu od roku 2005. Technika PET/CT je k dispozícii od roku 2004 4.
Karcinóm prostaty je jednou z mála malignít s vysoko elektívnou kostnou lokalizáciou metastáz 5-8 a rozdiel medzi zobrazovacími metódami identifikujúcimi kostnú reakciu na nádorovú masu (GS resp. PET/CT s FNa) a zobrazovacími metódami umožňujúcimi priame zobrazenie nádoru (PET/CT s FCH, s FDG) je zjavný.
FCH je prvým PET produktom zaregistrovaným na základe klinických štúdií a z dôvodu orientácie pivotných klinických štúdií 7 je FCH pri KP v súčasnosti registrovaný pre detekciu jeho kostných metastáz, umožňuje však tiež zobrazenie lokálneho nádoru 2, uzlinového 9 a mäkkotkanivového 10 postihnutia, prípade aj iných primárnych nádorov 11 so zásadným významom pre manažment pacienta.
Pacienti a metódy
Analyzované údaje
Počas ôsmich štvrťrokov od apríla 2010 do marca 2012 (vrátane) bolo analyzované spektrum požadovaných typov vyšetrení nukleárnej medicíny zameraných na identifikáciu rozsahu KP. Pacienti s anamnestickým údajom o inom malígnom nádore v minulosti resp. s aktívnou malignitou boli do analýzy zahrnutí len ak bolo príslušné vyšetrenie indikované v rámci hodnotenia rozsahu KP.
Zaznamenaný bol:
- typ realizovaného vyšetrenia,
- vek pacienta,
- klinická situácia: iniciálny staging, okultná recidíva KP (stúpajúca hladina PSA bez známej lokalizácie), restaging pri známej recidíve KP, monitorovanie terapeutickej odpovede počas resp. na konci liečby.
Ak bolo zo žiadanky známe, zaznamenané boli aj:
- PSA v čase vyšetrenia (u 471 pacientov),
- iniciálna hodnota Gleasonovho skóre (u 342 pacientov),
- PSA v čase vyšetrenia a iniciálna hodnota Gleasonovho skóre (u 243 pacientov).
Z údajov výkazníctva boli analyzované celkové počty všetkých 4 skúmaných vyšetrení (GS, PET/CT s FDG, FCH a FNa) vo všetkých indikáciách a stanovený bol percentuálny podiel vyšetrení realizovaných v indikácii KP.
Štatistické metódy
Pre každý štvrťrok bol stanovený počet vyšetrení každej zo 4 vyšetrovacích metód (GS, PET/CT s FNa, FCH, FDG). Pomocou chí-kvadrát multicases testu boli porovnávané hodnoty zo zodpovedajúcich štvrťrokov v dvoch po sebe nasledujúcich rokoch, čo umožnilo odfiltrovanie sezónnych vplyvov na požiadavky vyšetrení.
Závislosť požadovaného vyšetrenia od veku, PSA a Gleasonovho skóre boli skúmané pomocou Kruskal-Wallisovho resp. Mann-Whitneyho testu.
Ak boli u jedného pacienta počas skúmaného obdobia realizované viaceré vyšetrenia, analyzované boli aj ich počet, typ a časová postupnosť.
Výsledky
Vývoj požiadaviek vyšetrení
Vývoj požiadaviek vyšetrení ilustruje Tab. 1. Celkovo bolo počas uvedeného obdobia realizovaných 721 vyšetrení u 568 pacientov v rôznych klinických situáciách KP. Celkovo najčastejšie požadovaným vyšetrením bola PET/CT s FCH (42 %), v poradí druhým najčastejšie požadovaným vyšetrením bola PET/CT s FNa (27 %). Konvenčná gamagrafia skeletu bola celkovo požadovaná v 25 % prípadov a najmenej často požadovaná bola PET/CT s FDG (6 %).
Table 1. Časový vývoj požiadaviek vyšetrení pri KP 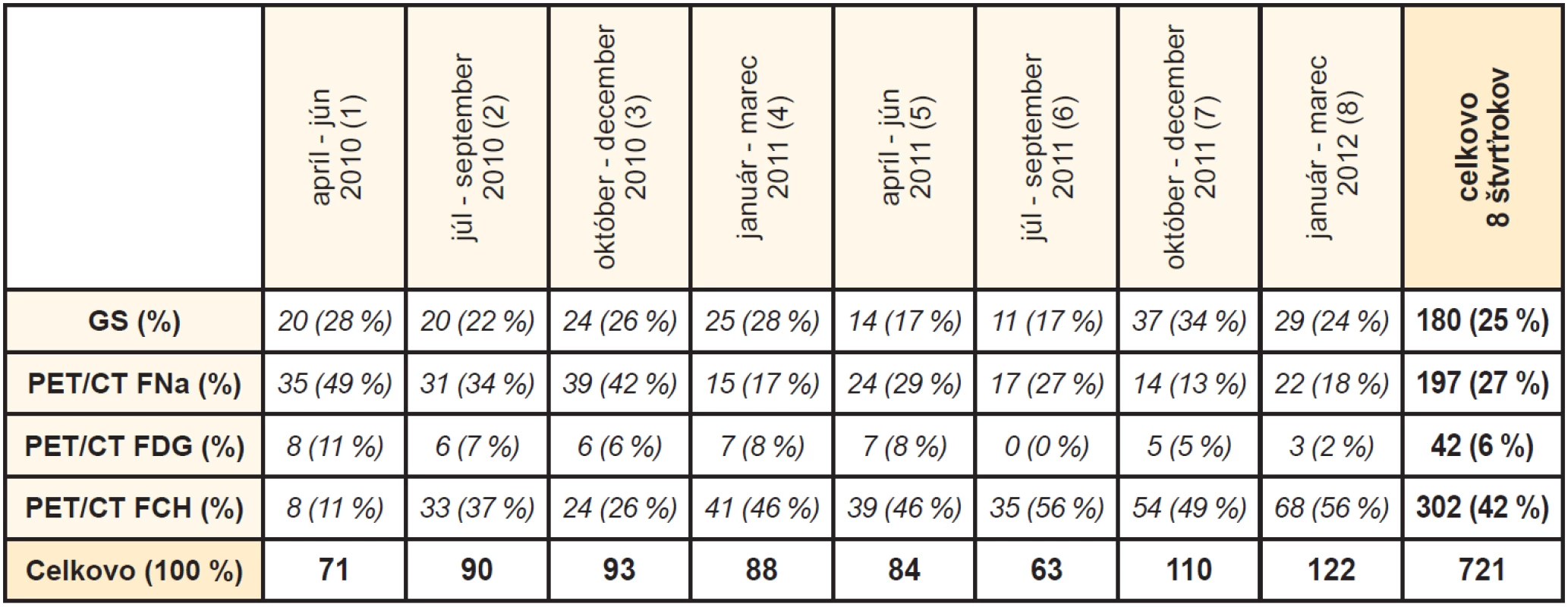
Dominancia požiadaviek PET/CT s FCH bola pozorovaná od druhého štvrťroka po registrácii FCH a ostala bez zmeny počas nasledujúceho obdobia s výnimkou tretieho štvrťroka (od októbra do decembra 2010), kedy viedla PET/CT s FNa.
V prvom roku (1.-4. štvrťrok) bola pri KP najžiadanejšia PET/CT s FNa (122 vyšetrení) nasledovaná PET/CT s FCH (106 vyšetrení). V druhom roku (5.-8. štvrťrok) sa situácia zmenila a na prvom mieste sa ocitla PET/CT s FCH (196 vyšetrení), zatiaľ čo PET/CT s FNa klesla s počtom 77 vyšetrení na tretie miesto a bola prekonaná aj GS, ktorá bola realizovaná v 91 prípadoch.
Celkový výsledok chí-kvadrát testu z údajov v Tab. 1 je vysoko signifikantný (p<0.001) a potvrdzuje zmenu v spektre žiadaných vyšetrení počas sledovaného obdobia: pri porovnaní zodpovedajúcich štvrťrokov dvoch po sebe nasledujúcich rokov, absolútny počet požiadaviek PET/CT s FCH stúpol vo všetkých obdobiach. Štatisticky signifikantný rozdiel bol dosiahnutý pri porovnaní počtu PET/CT s FCH v 1. a 5. štvrťroku (p<0,01). Pri porovnaní počtu PET/CT s FCH v 4. a 8. štvrťroku už výsledok signifikantný nebol (p>0,2), čo dokumentuje prudký začiatočný nárast počtu vyšetrení a jeho stabilizáciu s mierne stúpajúcou tendenciou v ďalšom období.
Celkový počet sledovaných vyšetrení pri KP medziročne stúpol z počtu 342 počas 1.-4. štvrťroka na 379 počas 5.-8. štvrťroka (+11 %). Nárast počtu vyšetrení bol zaznamenaný počas všetkých zodpovedajúcich štvrťrokov z výnimkou letného v roku 2011, kedy bol celkový počet vyšetrení nižší, ako v zodpovedajúcom štvrťroku predchádzajúceho roku.
Aký bol podiel indikácie KP na celkovom počte realizovaných vyšetrení?
Vývoj podielu indikácie KP na všetkých vyšetreniach uvádza Tab. 2.
Table 2. Percentuálny podiel požiadaviek vyšetrení v indikácii KP z celkového počtu vyšetrení 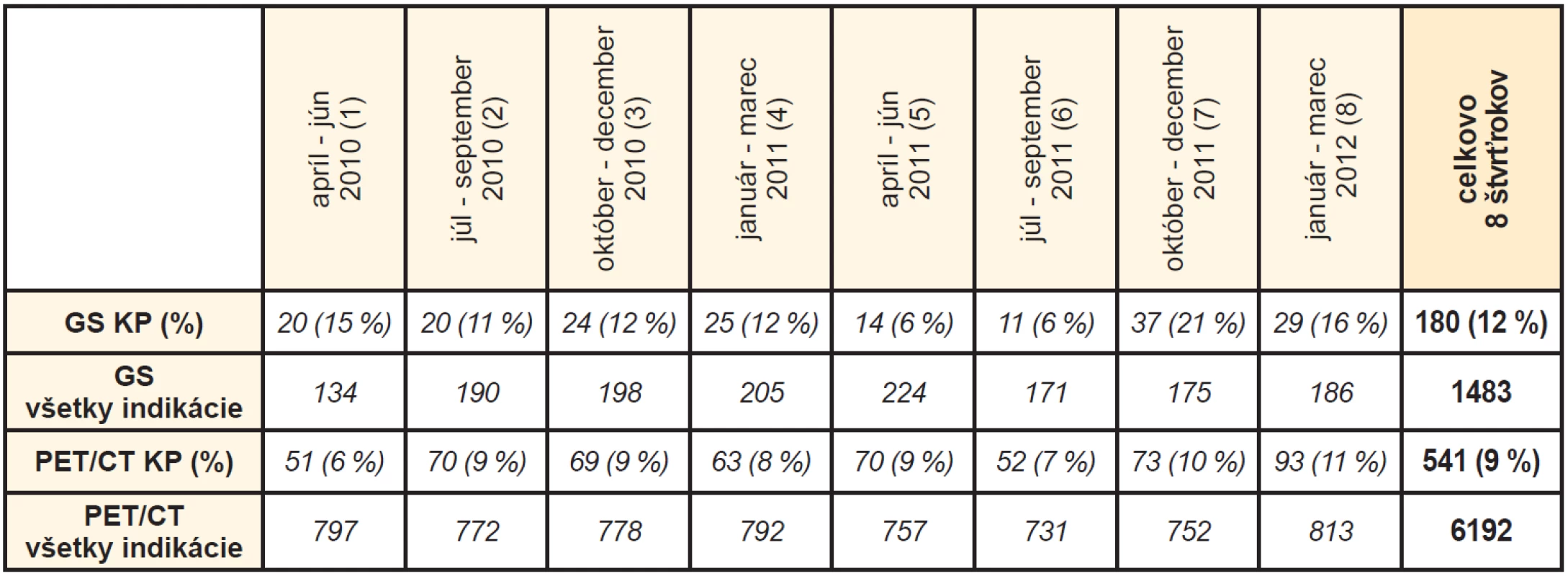
Počas skúmaného obdobia bolo realizovaných celkovo 1483 GS a 6192 PET/CT vyšetrení, z toho 12 % všetkých GS a 9 % všetkých PET/CT bolo realizovaných v indikácii KP.
Podiel GS klesol z 15 % v 1. štvrťroku a dosiahol minimum (6 %) v 5.-6. štvrťroku s následným vzostupom na 16 % v 8. štvrťroku, čo súviselo najmä s jej lepšou dostupnosťou danou kratšou čakacou dobou v porovnaní s PET/CT vyšetreniami.
Čo sa týka percentuálneho podielu indikácie KP na všetkých realizovaných PET/CT, jeho podiel bol 6 % v 1. štvrťroku so vzostupom na 9 % v 2. štvrťroku, s následnou stabilizáciou okolo 7 % a vzostupom na 11 % (spolu so vzostupom celkového počtu vyšetrení) v 8. štvrťroku.
Analýza požiadaviek viacerých vyšetrení u jedného pacienta
Viac ako jedno vyšetrenie nukleárnej medicíny bolo počas dvoch po sebe nasledujúcich rokov realizované u 74 pacientov (13 %).
Celkový počet vyšetrení u jedného pacienta bol od 2 do 13. Dve vyšetrenia boli realizované u 47 pacientov, tri u 16 pacientov a viac ako tri u 11 pacientov.
Dôvody multiplikácie vyšetrení
Dva rôzne typy vyšetrení boli realizované z nasledovných dôvodov:
- získanie chýbajúcej informácie alebo potvrdenie nejasného nálezu: dva odlišné typy vyšetrení PET/CT s FCH a s FNa boli v rámci jedného mesiaca realizované u 15 pacientov, PET/CT s FNa a FDG, PET/CT s FCH a FDG a PET/CT s FCH a GS u jedného pacienta,
- sledovanie KP pomocou jedného typu vyšetrenia v intervale viac ako jeden mesiac: PET/CT s FCH u 14 pacientov, GS u 6 pacientov, PET/CT s FNa u 5 pacientov a PET/CT s FDG u jedného pacienta,
- sledovanie KP pomocou dvoch typov vyšetrení v intervale viacerých mesiacov: GS ako prvá, sledovaná PET/CT s FCH u 7 pacientov, PET/CT s FNa nasledovaná PET/CT s FCH u 4 pacientov, striedanie PET/CT s FNa a FCH u 4 pacientov, PET/CT s FCH a následne s FNa, PET/CT s FCH a následne s FDG a napokon GS a následne PET/CT s FNa v každom prípade u jedného pacienta.
Viac ako 3 typy vyšetrení boli realizované u 12 pacientov, vo väčšine prípadov bola žiadaná aj PET/CT s FDG.
Klinický kontext
Priemerný vek pacientov bol 69 rokov (42-97 rokov) s významnými rozdielmi v klinickej situácii KP: pacienti odoslaní v rámci iniciálneho stagingu boli celkovo mladší (67,6 rokov) ako ostatní pacienti (69 rokov a viac), p=0,02.
Pri jednotlivých typoch vyšetrenia nebol zaznamenaný signifikantný vekový rozdiel a nebolo pozorované, že by niektoré vekové skupiny pacientov boli dominantne odosielané na určitý typ vyšetrenia.
V závislosti od klinickej situácie KP (Tab. 3) boli GS a PET/CT s FNa najčastejšie žiadané v rámci iniciálneho stagingu, zatiaľ čo PET/CT s FCH bola v polovici prípadov realizovaná pri okultnej recidíve KP. PET/CT s FDG bola žiadaná v prípadoch pokročilého KP, najmä v rámci monitorovania terapeutickej odpovede.
Table 3. Indikácia vyšetrení pri KP 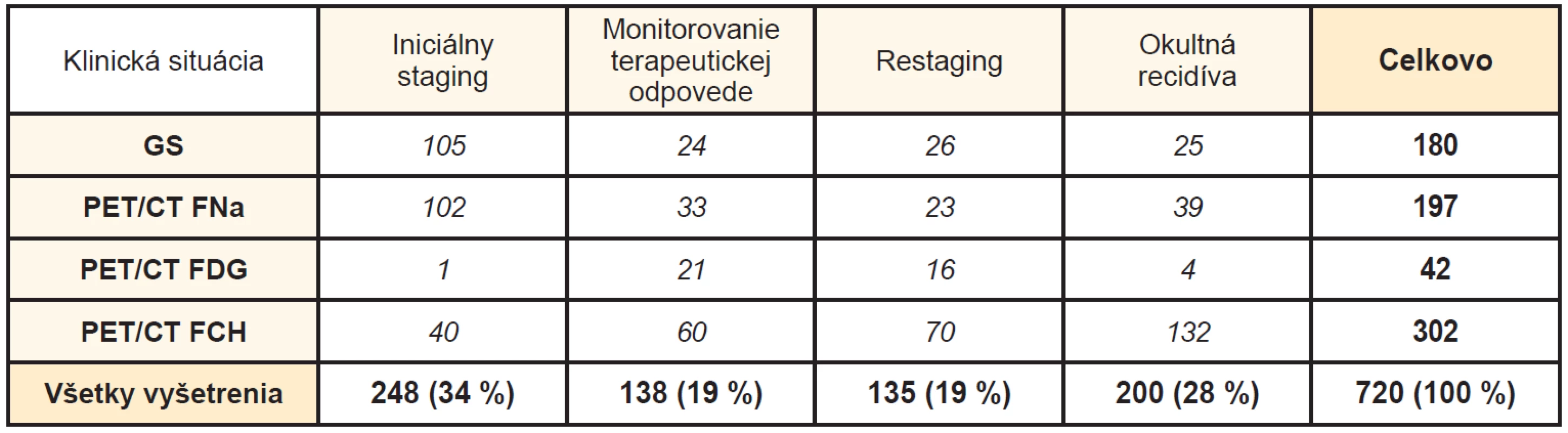
Laboratórny kontext
Výber jednotlivých typov vyšetrení významne závisel od sérových hladín PSA (p<0,001).
Priemerná hodnota PSA bola pri PET/CT s FCH 17 ng/ml, pri PET/CT s FDG 45 ng/ml, pri PET/CT s FNa 59 ng/ml a pri GS 192 ng/ml.
V závislosti od klinickej situácie bola sérová hladina PSA signifikantne nižšia pri okultnej recidíve KP (priemer = 15 ng/ml) a restagingu KP (priemer = 36 ng/ml), ako pri iniciálnom stagingu KP (priemer = 105 ng/ml) (p<0,001).
U pacientov odoslaných na PET/CT s FDG bola pozorovaná najvyššia hodnota Gleasonovho skóre (priemer 8,4), vo väčšine prípadov išlo o pacientov s multimetastatickým KP.
Iniciálna hodnota Gleasonovho skóre u pacientov odoslaných na PET/CT s FNa bola priemerne 7,6 a najnižšie priemerné iniciálne hodnoty Gleasonovho skóre boli zaznamenané u pacientov odoslaných na PET/CT s FCH a GS (7,3 a 7,2) (p<0,001).
V závislosti od klinickej situácie boli iniciálne hodnoty Gleasonovho skóre signifikantne vyššie u pacientov odoslaných v rámci restagingu a v rámci monitorovania terapeutickej odpovede, ako u pacientov odoslaných v rámci iniciálneho stagingu (p<0,001).
Podľa nedávno publikovaných odporúčaní je GS v rámci iniciálneho stagingu KP indikovaná u pacientov so sérovou hladinou PSA>10 ng/ml, s KP T2 alebo s hodnotou Gleasonovho skóre >7 12,13. V ostatných prípadoch nebolo potvrdené, že by vyšetrenie prinieslo očakávaný klinický osoh.
V našom súbore zodpovedalo uvedeným odporúčaniam 33/47=70 %.
Pre ostatné typy vyšetrení nukleárnej medicíny pri KP nie sú oficiálne odporúčania k dispozícii.
U 17 % pacientov odoslaných na PET/CT s FCH, u 7 % pacientov odoslaných na PET/CT s FNa a u 2 % pacientov odoslaných na GS bola sérová hodnota PSA<1 ng/ml. U všetkých pacientov odoslaných na PET/CT s FDG bola sérová hladina PSA>1 ng/ml.
Diskusia
Za hlavný nález analýzy vývoja požiadaviek vyšetrení nukleárnej medicíny pri KP po registrácii FCH považujeme rýchly vzostup počtu PET/CT s FCH a pokles počtu vyšetrení zameraných na nepriamu detekciu kostných metastáz (GS a PET/CT s FNa).
Celkový počet vyšetrení pri KP stúpol a to najmä u pacientov so sérovou hladinou PSA<10 ng/ml a stúpol tiež percentuálny podiel indikácie KP na celkovom počte PET/CT vyšetrení.
Na realizáciu jednotlivých vyšetrení nebol stanovený žiaden limit a boli indikované na základe zváženia klinika.
Analyzovaný bol dostatočne veľký súbor (721 vyšetrení) a dosiahnuté boli štatisticky významné výsledky, je však možné namietať, že ide o monocentrickú analýzu, ktorá v mnohom odráža lokálne faktory ovplyvňujúce indikáciu jednotlivých vyšetrení.
Pri pohľade na výkyvy krivky bol zaznamenaný pokles počtu vyšetrení v letnom štvrťroku oboch po sebe nasledujúcich rokov (Tab. 1), hoci percentuálny pokles počtu požadovaných PET/CT vyšetrení v indikácii KP taký evidentný nebol. Pre tento jav nemáme uspokojivé vysvetlenie, je možné predpokladať, že bol zapríčinený obdobím letných dovoleniek.
Za osobitne zaujímavý však možno považovať jesenný štvrťrok oboch nasledujúcich rokov poznamenaný nárastom počtu indikácií všeobecne dobre známych vyšetrení skeletu (GS a PET/CT s FNa). Predpokladáme, že tento posun bol poznamenaný každoročnou jesennou výmenou cirkulujúcich rezidentov prichádzajúcich z nemocničných zariadení s inými vyšetrovacími možnosťami a zvyklosťami. Iný faktor, ktorý je potrebné brať do úvahy, je relatívne ľahšia dostupnosť GS v porovnaní s PET/CT.
Pri transpozícii výsledkov našej analýzy na podmienky pracoviska, ktoré začína ponúkať PET/CT s FCH, je potrebné brať do úvahy aj skutočnosť, že v nemocnici Tenon bola PET/CT s FCH dostupná v rámci protokolov klinického výskumu od roku 2005 a vyšetrenie bolo pre klinikov známe už pred registráciou FCH. Preto predpokladáme, že pracovisko nukleárnej medicíny, ktoré pri KP doposiaľ ponúkalo len GS, resp. v osobitných prípadoch aj PET/CT s FDG a nemá k dispozícii FNa (na Slovensku je FNa registrovaný), zaznamená podobný, hoci pravdepodobne o niečo pomalší vzostup požiadaviek na PET/CT s FCH.
V literatúre nie sú k dispozícii analýzy podobné prezentovanej. V USA, kde zatiaľ FCH nie je k dispozícii, bolo podľa National Oncologic registry 14 v období máj/2006 – máj/2008 realizovaných 40 863 PET vyšetrení v neregistrovanej onkologickej indikácii, z toho na prvom mieste KP s 5 309 vyšetreniami (13 %) so zmenou manažmentu indukovanou vyšetrením v 35 % prípadov.
V roku 2008 bolo v Nemecku realizovaných asi 63 500 PET vyšetrení, z toho asi 2 000 (3 %) pri KP 15. PET s FCH bola realizovaná u 2 285 pacientov (3,6 %), s FNa u 1000 pacientov (1,6 %), bez presného údaja o indikácii.
GS ani PET/CT s FDG pri KP v mnohých prípadoch neumožnia spoľahlivo zodpovedať klinické otázky, čo v kontexte nových terapeutických možností nie je postačujúce a potreba presnejšieho zobrazenia je vysoko aktuálna. PET/CT s FCH túto možnosť ponúka.
Preferencia jednotlivých typov vyšetrení v závislosti od klinickej situácie KP
Cieľom našej práce bolo analyzovať vplyv uvedenia novej metódy na vývoj požiadaviek jednotlivých typov vyšetrení pri KP. Diagnostické parametre ani vplyv výsledkov vyšetrení na manažment pacienta neboli v prezentovanej práci hodnotené. Je však zaujímavé analyzovať preferenciu jednotlivých typov vyšetrení príslušnými klinikmi v závislosti od klinickej situácie pri KP:
Iniciálny staging
PET/CT s FCH má v rámci iniciálneho stagingu KP obmedzenú senzitívnosť pre metastázy v nezväčšených lymfatických uzlinách (menších ako 5 mm), zmena plánovaného terapeutického postupu u pacientov s rizikom extrakapsulárneho šírenia bola zaznamenaná v 20 % prípadov 9.
V rámci iniciálneho stagingu KP bola v našom súbore najčastejšie indikovaným vyšetrením GS (Tab. 3). Celková preferencia PET/CT s FNa pred GS (197 vs 180) je však v súlade s dostupnými publikovanými údajmi potvrdzujúcimi lepšiu senzitívnosť a špecifickosť PET/CT s FNa v porovnaní s GS 16.
Od roku 2006 boli prinášané dôkazy o priaznivejších diagnostických parametroch PET/CT s FCH v porovnaní s GS pri stagingu vysoko rizikového KP 5. Systematické porovnanie PET/CT s FCH a s FNa pri stagingu a restagingu KP bolo publikované v roku 2008 6 a v roku 2011 7 s rovnakými závermi: PET/CT s FCH umožňuje identifikáciu dreňových kostných metastáz nezobraziteľných pomocou FNa resp. GS. FCH má nesignifikantne nižšiu senzitívnosť pri detekcii sklerotických kortikálnych metastáz, ktoré sú však zobraziteľné pomocou CT. FCH má naopak vyššiu špecifickosť ako FNa, nakoľko FCH nie je akumulovaný benígnymi kostnými léziami 8.
Pátranie po recidíve KP
Význam PET/CT s FCH pri pátraní po recidíve KP bol dokumentovaný viacerými autormi či už na izolovaných klinických prípadoch alebo malých súboroch pacientov 17, 18. Frekvencia pozitívnych nálezov PET/CT s FCH je priamo úmerná sérovej hladine PSA 19-23, času jej zdvojnásobenia a miere vzostupu 24,25 alebo hodnote Gleasonovho skóre 19.
Recidívu KP možno pomocou PET/CT s FCH lokalizovať v 20 % pacientov so sérovou hladinou PSA<1 ng/ml 22. V našom súbore bola PET/CT s FCH žiadaná najmä pri pátraní po recidíve KP pri nízkych sérových hladinách PSA a v 17 % pacientov bola sérová hladina PSA v čase PET/CT s FCH<1 ng/ml.
V prípade agresívnych alebo hormonálne refraktérnych foriem KP môžu niektoré lézie akumulovať FDG. Indikácia PET/CT s FDG bola v našom súbore celkovo zriedkavá.
Bolo tiež pozorované, že akumulácia FCH nádorovými masami je zachovaná aj pri hormonálne refraktérnych formách KP 26, 27 a PET/CT s FCH tak možno považovať za odôvodnenú aj v tejto situácii.
S vývojom nových možností hormónoterapie a chemoterapie pri agresívnych formách a pokročilých štádiách KP sa tak PET/CT, najmä s FCH a FDG, stáva osobitne zaujímavým nástrojom. V našom súbore bolo 19 % vyšetrení realizovaných v rámci monitorovania terapeutickej odpovede, s jasnou dominanciou PET/CT s FCH.
V súčasnosti nie sú k dispozícii európske odporúčania pre monitorovanie terapeutickej odpovede pri KP a National Comprehensive Cancer Network (NCCN, USA) 12 odporúča v rámci monitorovania terapeutickej odpovede GS, čo je však dané aj skutočnosťou, že FCH v USA nie je dostupný.
Záver
PET/CT s FCH sa stala pri KP od prvého štvrťroka po registrácii FCH najčastejšie realizovaným vyšetrením nukleárnej medicíny v nemocnici Tenon.
Požiadavky na GS poklesli, ale nevymizli, hoci GS je v súčasnosti realizovaná najmä v rámci iniciálneho stagingu KP, pravdepodobne pre potrebu rýchleho rozhodnutia o liečbe pri dlhších čakacích lehotách na PET/CT s FCH resp. FNa. V našom súbore 33 % pacientov odoslaných na GS zodpovedalo oficiálnym odporúčaniam pre realizáciu GS pri KP, čo je v súlade s nedávno publikovanými údajmi na väčšom súbore pacientov 28.
U 13 % pacientov boli v sledovanom období realizované viaceré vyšetrenia, podiel iteratívnych resp. dopĺňajúcich vyšetrení je na ich celkovom počte obmedzený.
Adresa pro korespondenci:
Soňa Balogová1,2,
Virginie Huchet1,
Laure Michaud1,3,
Khaldoun Kerrou1,
Fréderique Paycha1,
Valérie Nataf3,4,
Marika Vereb5,6,
Lucia Kaliská7,
Françoise Montravers1,3,
J.-N. Talbot1,3
1Médecine nucléaire, Hôpital Tenon, AP–HP, Paris, Francúzsko,
2Klinika nukleárnej medicíny LF UK a OÚSA Bratislava, Slovensko,
3Université Pierre-et-Marie-Curie, Paris, Francúzsko,
4Radiopharmacie, Hôpital Tenon, AP–HP, 75020 Paris, Francúzsko,
5Klinikum Kassel Nuklearmedizin, Kassel, Nemecko,
6Oddelenie nukleárnej medicíny, Reimanus s. r. o., Prešov, Slovensko,
7INMM Košice & Agel diagnostics s. r. o., Pracovisko Banská Bystrica, Slovensko
sbalogov@ousa.sk
Sources
1. Talbot JN, Gutman F, Huchet V, et al. Utilité clinique de la tomographie par émission de positons dans le cancer de la prostate. Presse Med 2007;36 : 1794-806
2. Kwee S, De Grado T, Talbot JN, et al. Cancer imaging with fluorine-18-labeled choline derivatives. Semin Nucl Med 2007;37 : 420-8
3. Huchet V, Kerrou K, Balogova S, et al. Tomographie par émission de positons et cancer de la prostate. Méd Nucl 2008;32 : 409-17
4. Huchet V, Kerrou K, Derhy S, et al. TEP/TDM à la fluorométhylcholine-(18F) dans l’imagerie de la récidive du cancer de la prostate: jalons pour un PHRC national. Méd Nucl 2007;31 : 338-44
5. Gutman F, Aflalo-Hazan V, Kerrou K, et al. 18F-choline PET/CT for initial staging of advanced prostate cancer. AJR Am J Roentgenol 2006;187:W618-21
6. Beheshti M, Vali R, Waldenberger P, et al. Detection of bone metastases in patients with prostate cancer by 18F fluorocholine and 18F fluoride PET-CT: a comparative study. Eur J Nucl Med Mol Imaging 2008;35 : 1766–74
7. Langsteger W, Balogova S, Huchet V, et al. Fluorocholine (18F) and sodium fluoride (18F) PET/CT in the detection of prostate cancer: prospective comparison of diagnostic performance determined by masked reading. Q J Nucl Med Mol Imaging 2011;55 : 448-57
8. Talbot JN, Paycha F, Balogova S. Diagnosis of bone metastasis: recent comparative studies of imaging modalities. Q J Nucl Med Mol Imaging 2011;55 : 374-410
9. Beheshti M, Imamovic L, Broinger G, et al. 18F choline PET/CT in the preoperative staging of prostate cancer in patients with intermediate or high risk of extracapsular disease: a prospective study of 130 patients. Radiology 2010;254 : 925-33
10. Balogova S, Nataf V, Gutman F, et al. Récidive biologique de cancer de la prostate: intérêt de la TEP/TDM à la fluorocholine (18F) du corps entier. Méd Nucl 2010;34 : 540-5
11. Balogova S, Bumsel F, Kerrou K, et al. La fluorocholine(18F) a une utilité clinique dans le cancer de la prostate et le carcinome hépatocellulaire parfois chez le même malade, Méd Nucl 2010; 34 : 378-82
12. Mohler JL. NCCN Guidelines. Prostate cancer, version 4.2011. J Natl Compr Canc Netw 2011:Epub
13. Briganti A, Passoni N, Ferrari M, et al. When to perform bone scan in patients with newly diagnosed prostate cancer: external validation of the currently available guidelines and proposal of a novel risk stratification tool. Eur Urol 2010;57 : 551-8
14. Hillner BE, Siegel BA, Shields AF, et al. Relationship between cancer type and impact of PET and PET/CT on intended management: findings of the National Oncologic PET Registry. J Nucl Med 2008;49 : 1928–35
15. Kotzerke J, Oehme L, Lindner O, et al. Positron emission tomography 2008 in Germany - results of the query and current status. Nuklearmedizin 2010;49 : 58-64
16. Even-Sapir E, Metser U, Mishani E, et al. The detection of bone metastases in patients with high-risk prostate cancer: 99mTc-MDP planar bone scintigraphy, single - and multi-field-of-view SPECT, 18F-Fluoride PET, and 18F-Fluoride PET/CT. J Nucl Med 2006; 47 : 287-97
17. Schmid DT, John H, Zweifel R, et al. Fluorocholine PET/CT in patients with prostate cancer: initial experience. Radiology 2005; 235 : 623-8
18. Gutman F, Thomassin J, Kerrou K et al. L’intérêt de la TEP/TDM à la fluorocholine-(18F) illustré par l’exemple. 2006;30 : 391-8
19. Cimitan M, Bortolus R, Morassut S et al. (18F)fluorocholine PET/CT imaging for the detection of recurrent prostate cancer at PSA relapse: experience in 100 consecutive patients. Eur J Nucl Med Mol Imaging 2006;33 : 1387-98
20. Heinisch M, Dirisamer A, Loidl W et al. Positron emission tomography/computed tomography with F-18-fluorocholine for restaging of prostate cancer patients: meaningful at PSA < 5 ng/ml? Mol Imaging Biol 2006;8 : 43-8
21. 21. Husarik, Miralbell R, Dubs M et al. Evaluation of (18F)-choline PET/CT for staging and restaging of prostate cancer. Eur J Nucl Med Mol Imaging 2008;35 : 253-63
22. Pelosi E, Arena V, Skanjeti A, et al. Role of whole-body 18F-choline PET/CT in disease detection in patients with biochemical relapse after radical treatment for prostate cancer. Radiol Med 2008;113 : 895-904
23. Steiner Ch, Vees H, Zaidi H, et al. Three-phase 18F-fluorocholine PET/CT in the evaluation of prostate cancer. Nuklearmedizin 2009;48 : 1-9
24. Graute V, Jansen N, Ubleis C, et al. Relationship between PSA kinetics and [(18)F]fluorocholine PET/CT detection rates of recurrence in patients with prostate cancer after total prostatectomy. Eur J Nucl Med Mol Imaging 2012;39 : 271-82
25. Huchet V , Gutman F, Kerrou K, et al. Evaluation of PSA velocity as a selection criterion for FCH PET/CT in patients with biological recurrence of prostate cancer. Eur J Nucl Med Mol Imaging 2007; 34(Suppl 2):S123
26. Price DT, Coleman RE, Liao RP, et al. Comparison of [18F]fluorocholine and [18F]fluorodeoxyglucose for positron emission tomography of androgen dependent and androgen independent prostate cancer. J Urol 2002;168 : 273-80
27. McCarthy M, Siew T, Campbell A, et al. 18F-Fluoromethylcholine (FCH) PET imaging in patients with castration-resistant prostate cancer: prospective comparison with standard imaging. Eur J Nucl Med Mol Imaging 2011;38 : 14-22
28. Lavery HJ, Brajtbord JS, Levinson AW, et al. Unnecessary imaging for the staging of low-risk prostate cancer is common. Urology 2011;77 : 274-8
Labels
Nuclear medicine Radiodiagnostics Radiotherapy
Article was published inNuclear Medicine

2012 Issue 3
Most read in this issue- Stanovení mozkové smrti
- Spektrum požadovaných vyšetrení nukleárnej medicíny pri karcinóme prostaty po registrácii 18F fluorocholínu: dvojročné sledovanie v nemocnici Tenon
- Hemodialyzovaný pacient s karcinomem štítné žlázy léčený 131I
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

