-
Medical journals
- Career
Hodnocení hemodynamické významnosti koronárních stenóz metodou frakční průtokové rezervy
Authors: MUDr. Štěpán Jeřábek; doc. MUDr. Ph.D. Tomáš Kovárník
Authors‘ workplace: II. interní klinika − klinika kardiologie a angiologie 1. LF UK a VFN v Praze
Published in: Čas. Lék. čes. 2016; 155: 183-187
Category: Review Article
Overview
Rozhodnutí o provedení koronární intervence by mělo být spojeno s objektivním průkazem ischemie. Koronární angiografie poskytuje morfologický obraz věnčitých tepen, zpravidla však nedokáže přesně odpovědět na základní otázku, jaký je vliv konkrétní léze na koronární průtok a zda ošetření této stenózy povede ke zlepšení prognózy pacienta.
Frakční průtoková rezerva se v průběhu let stala nejen zlatým standardem, ale i rutinní metodou hodnocení hemodynamické významnosti koronárních stenóz. V následujícím sdělení budou probrány základy koronární fyziologie a princip metody spolu s praktickými aspekty měření a přehledem nejdůležitějších klinických studií.Klíčová slova:
frakční průtoková rezerva, koronární fyziologie, ischemická choroba srdečníÚvod
Princip měření průtoku v místě koronární stenózy je stejně starý jako koronární angioplastika sama. Již první balónkové katétry zkonstruované Andreasem Grüntzigem měly lumen pro měření proximálních a distálních tlaků (1). Vzhledem k četným technickým komplikacím, zejména pak velikosti instrumentaria, však metoda ve své době nedoznala většího rozmachu a koncept začaly znovu rozvíjet až počátkem 90. let týmy kolem De Bruyna a Pijlse [2−4]. Potřeba hodnotit funkční dopad koronárních stenóz byla zdůrazněna výsledky řady studií, ve kterých bylo prokázáno, že hemodynamicky nevýznamné léze řešené konzervativně mají velmi dobrou prognózu, kterou může nevhodně indikovaná intervence zhoršit (5, 6).
Angiografie zůstává přes rozvoj neinvazivních zobrazovacích metod diagnostickým zlatým standardem s dosud nepřekonaným prostorovým a časovým rozlišením. Přesto má pouze limitovanou výpovědní hodnotu v posuzovaní hraničních stenóz v rozmezí 40−80 % (7, 8). Bez ohledu na morfologii lze za významnou stenózu považovat pouze takovou, která způsobuje ischemii myokardu a tím symptomy nemocného. Neinvazivní radionuklidové zátěžové testy či dobutaminová echokardiografie umožňují detekovat myokardiální ischemii s vysokou mírou specificity i senzitivity, selhávají však v bližším určení ischemického povodí a vyvolávající léze. V případě nukleárních perfuzních modalit existuje riziko podhodnocení rozsahu ischemie nebo falešně negativní nález při pokročilém postižení více tepen (9−13).
Spolu s vývojem intrakoronárních tlakových vodičů a narůstajícím množstvím klinických dat se postupně stala zlatým standardem invazivního stanovení funkční významnosti koronárních stenóz metoda frakční průtokové rezervy (FFR). Přesvědčivé výsledky rozsáhlých randomizovaných studií upevnily v aktuálních evropských doporučeních indikaci intervencí na základě měření FFR na úroveň IA (14, 15).
Koronární fyziologie a koncept FFR
Koronární řečiště je ve zjednodušeném kompartmentovém modelu rozděleno do tří úseků: proximálně jsou epikardiální tepny o průměru > 0,5 mm, které se dále větví na prearterioly a arterioly o průměru 100−500 um, resp. < 100 um (viz obr. 1).
Image 1. Kompartmentový model koronárního řečiště (upraveno dle: Camici et al., 2007) 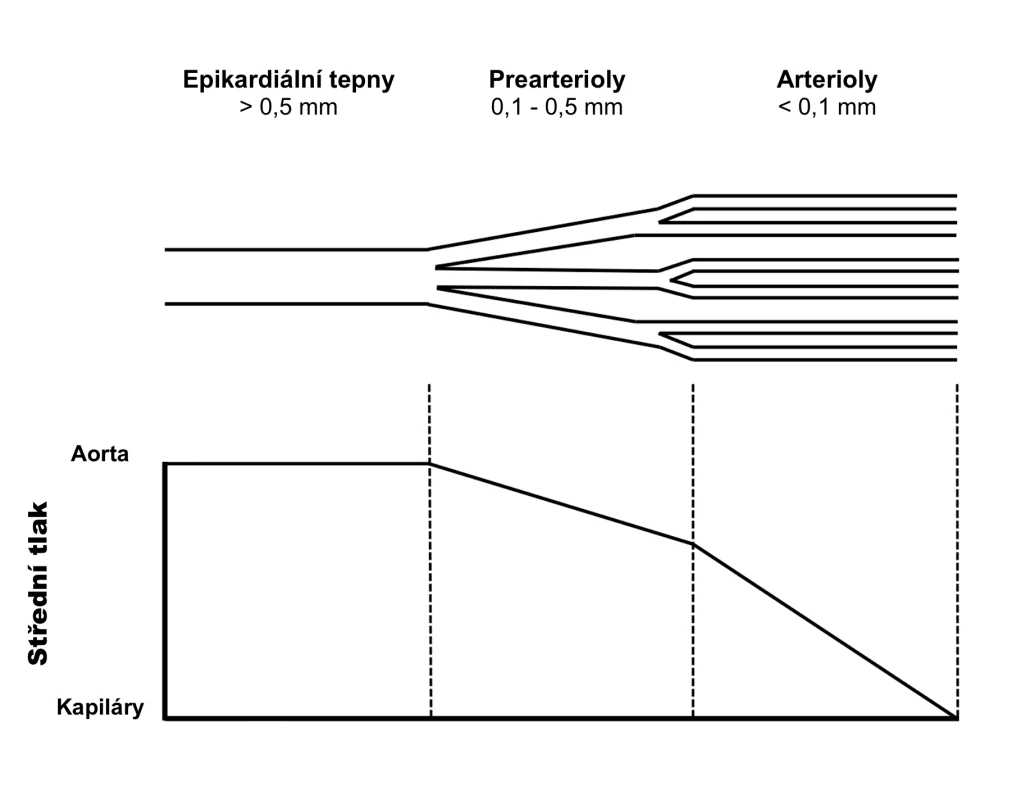
Jednotlivé kompartmenty jsou stanoveny arbitrárně podle převažující funkce, anatomicky není možné přesné hranice určit. Velké tepny probíhající v epikardu (v myokardu interventrikulárního septa v případě septálních větví) jsou konduktivními cévami, ve kterých za normálních podmínek téměř nedochází k poklesu tlaku. Střední a distální arteriální kompartment tvoří tzv. mikrocirkulaci, která je zodpovědná za vlastní koronární rezistenci.
Tonus prearteriol, jejichž hlavní funkcí je udržování vyrovnaného perfuzního tlaku na úrovni arteriol, je dominantně řízen koronárním průtokem a modulovaný autonomním nervovým systémem a funkcí endotelu. Arterioly jsou regulovány metabolismem myokardu (16, 17).
FFR specificky posuzuje pouze epikardiální kompartment, nezávisle na stavu mikrovaskulárního řečiště.
Frakční průtoková rezerva je definována jako poměr maximálního průtoku krve distálně za stenózou a normálního průtoku ve stejném povodí za hypotetické absence stenózy. Vzhledem k autoregulačním schopnostem koronárního řečiště je za klidových podmínek odvození průtoku z tlakové křivky obtížné. Toto lze obejít farmakologickým navozením stavu maximální hyperemie, kdy je vztah mezi perfuzním tlakem a průtokem lineární. Průtok je za těchto podmínek přímo úměrný rozdílu středního arteriálního tlaku a centrálního žilního tlaku a nepřímo úměrný rezistenci. Při hyperemii je hodnota rezistence minimální, centrální žilní tlak se obecně u většiny pacientů blíží nule, hodnota FFR je tedy vypočtena jako poměr středního tlaku za stenózou a středního tlaku v aortě (viz obr. 2).
Image 2. Zjednodušené teoretické odvození výpočtu průtoku koronární tepnou z tlaku měřeného před a za stenózou. Předpokladem je dosažení maximální hyperemie. 
Praktické aspekty
Před začátkem měření je nutná intrakoronární aplikace nitrátu k prevenci spasmů. Vodicí drát s tlakový senzorem je následně zaveden přes vodicí katétr do koronární tepny a umístěn distálně za stenózu (viz obr. 3). Tlak v aortě je měřen vodicím katétrem a obě tlakové křivky jsou simultánně zobrazovány spolu s vypočtenou hodnotou FFR (viz obr. 4). Hyperemie je navozena nejčastěji adenosinem ve formě intrakoronárního bolusu, případně intravenózní infuzí. Alternativou je papaverin, který však již není prakticky využíván pro riziko maligních komorových arytmií. Nově je v klinické praxi testován regadenoson (viz tab. 1) (18−20).
Image 3. Intrakoronární vodič připravený k zavedení do katétru. Tlakový senzor je umístěn 3 cm od hrotu. 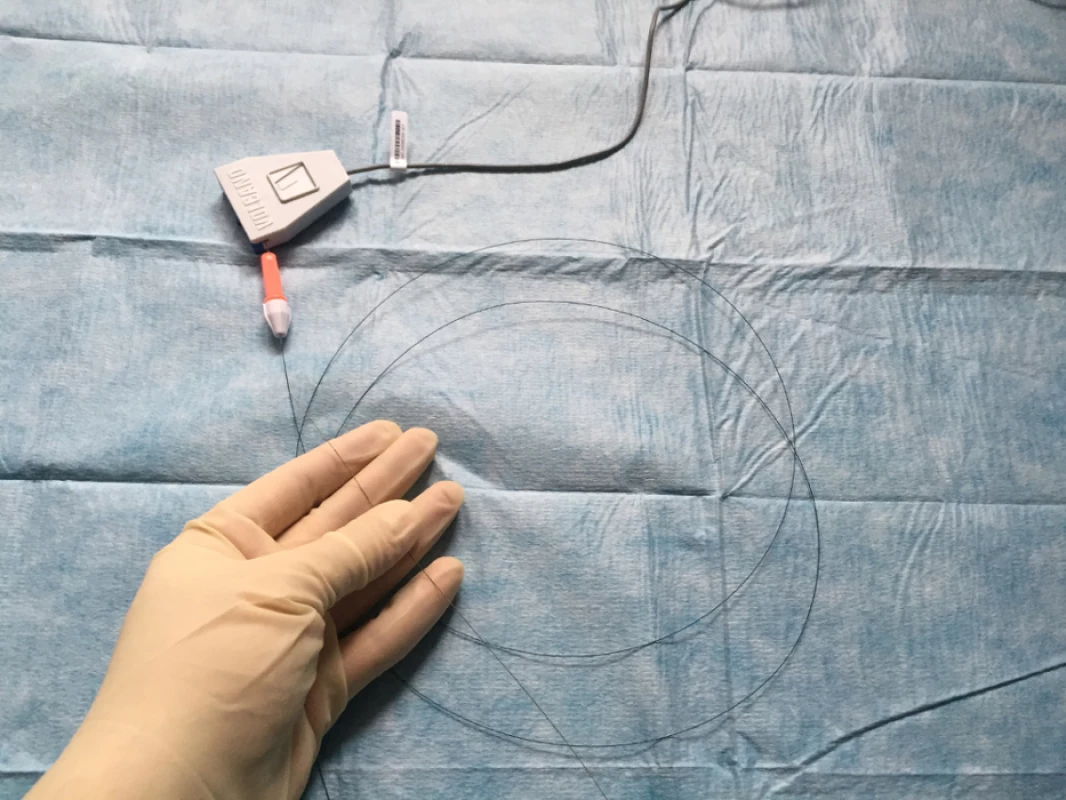
Image 4. Záznam měření po intrakoronárním podání adenosinu. Hodnota FFR 0.66, ale i nízký poměr klidových tlaků Pd/Pa ještě před navozením hyperemie svědčí pro jasně významnou stenózu. 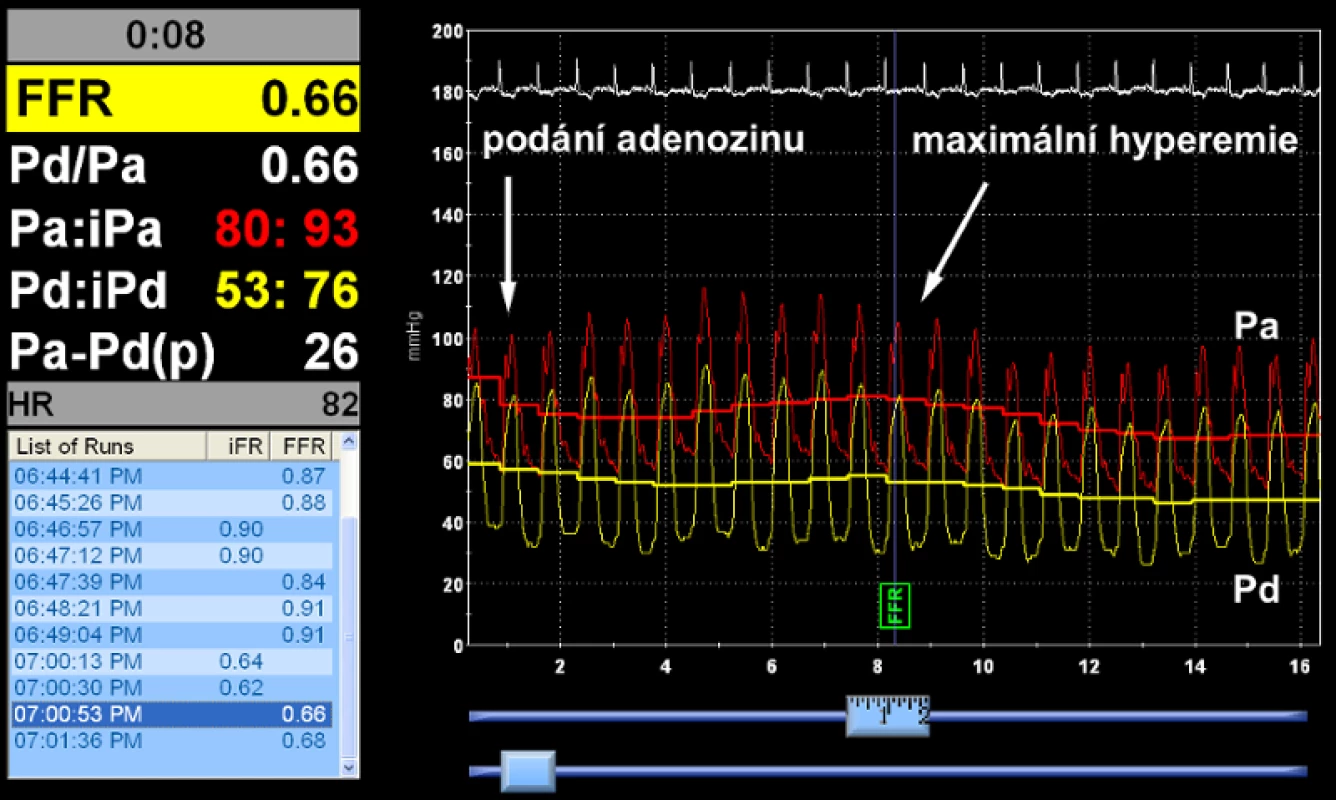
Table 1. Farmaka užívaná k indukci hyperemie koronárního řečiště 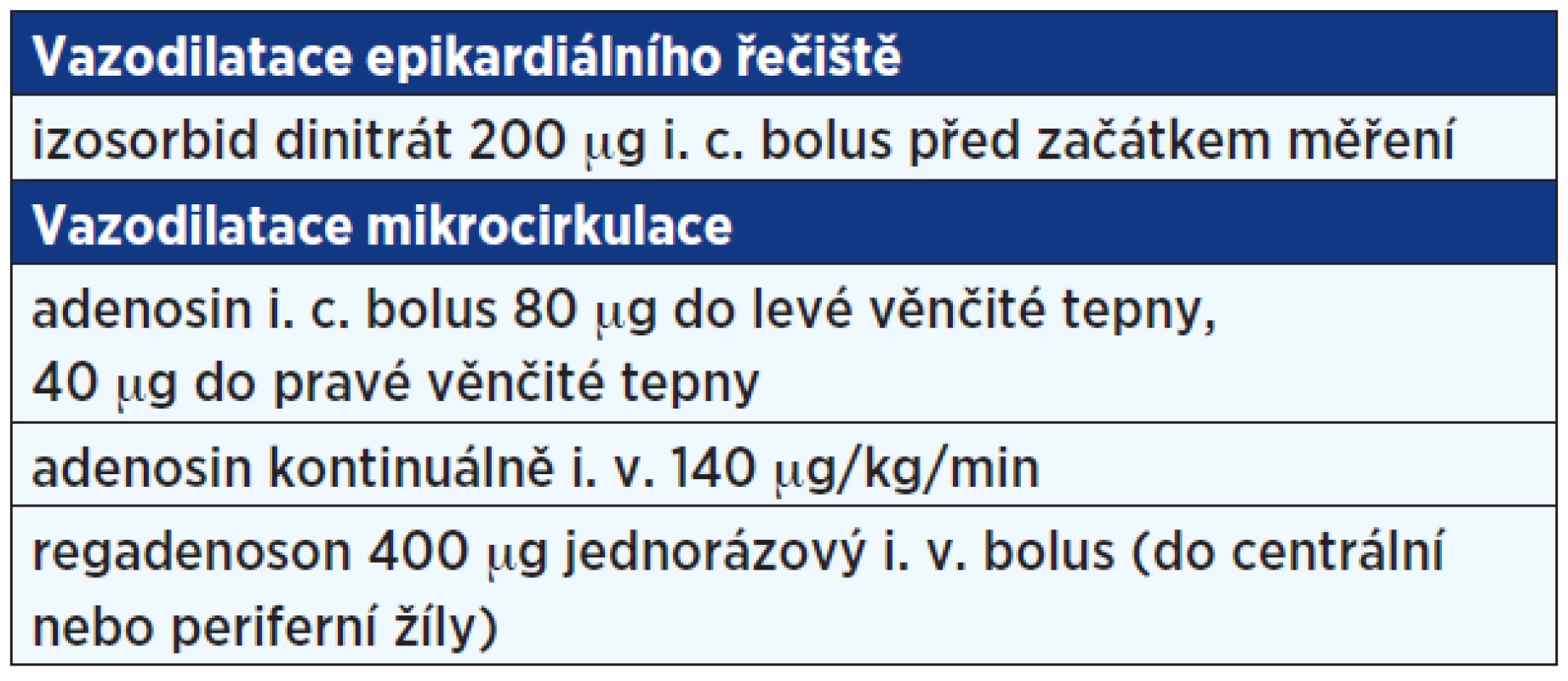
Dosažení maximální hyperemie je indikované konstantní stabilní hodnotou FFR, při bolusovém podání pak nesmí být odchylka mezi jednotlivými měřeními větší než 0,01. Normální hodnota FFR pro jakoukoliv tepnu u kohokoliv je vždy rovna 1, což je dáno vlastností epikardiálního kompartmentu, ve kterém v nepostižené tepně nedochází k poklesu tlaku, a to ani při hypermii. Za průkaz ischemie je brána hodnota FFR 0,75, při hodnotě > 0,80 je naopak bezpečné lézi neintervenovat; úzkou šedou zónu tvoří FFR v pásmu 0,76−0,80. Dle výsledků studie FAME, ze které vycházejí i současná evropská doporučení pro revaskularizaci myokardu, je prahovou hodnotou a indikací k intervenci FFR 0,80 (viz tab. 2) (14, 23).
Table 2. Prahové hodnoty FFR měření 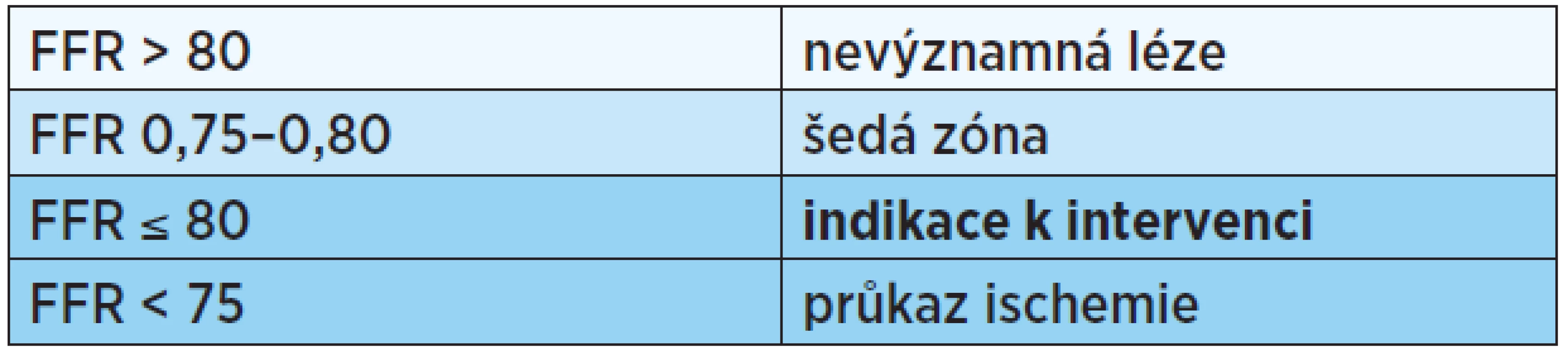
Frakční průtoková rezerva vykazuje velmi vysokou reprodukovatelnost, není závislá na systémovém krevním tlaku ani tepové frekvenci a zohledňuje velikost zásobeného povodí (viz obr. 5) stejně jako přítomnost kolaterál nebo graftů. Přes všechny zmíněné výhody zůstává zcela zásadním předpokladem správného měření dosažení maximální vazodilatace (21).
Image 5. Diskrepance mezi morfologickým nálezem a funkčním dopadem. FFR zohledňuje masu viabilního myokardu, který je postiženou tepnou zásobován (upraveno dle: Pijls, Sels, 2012). 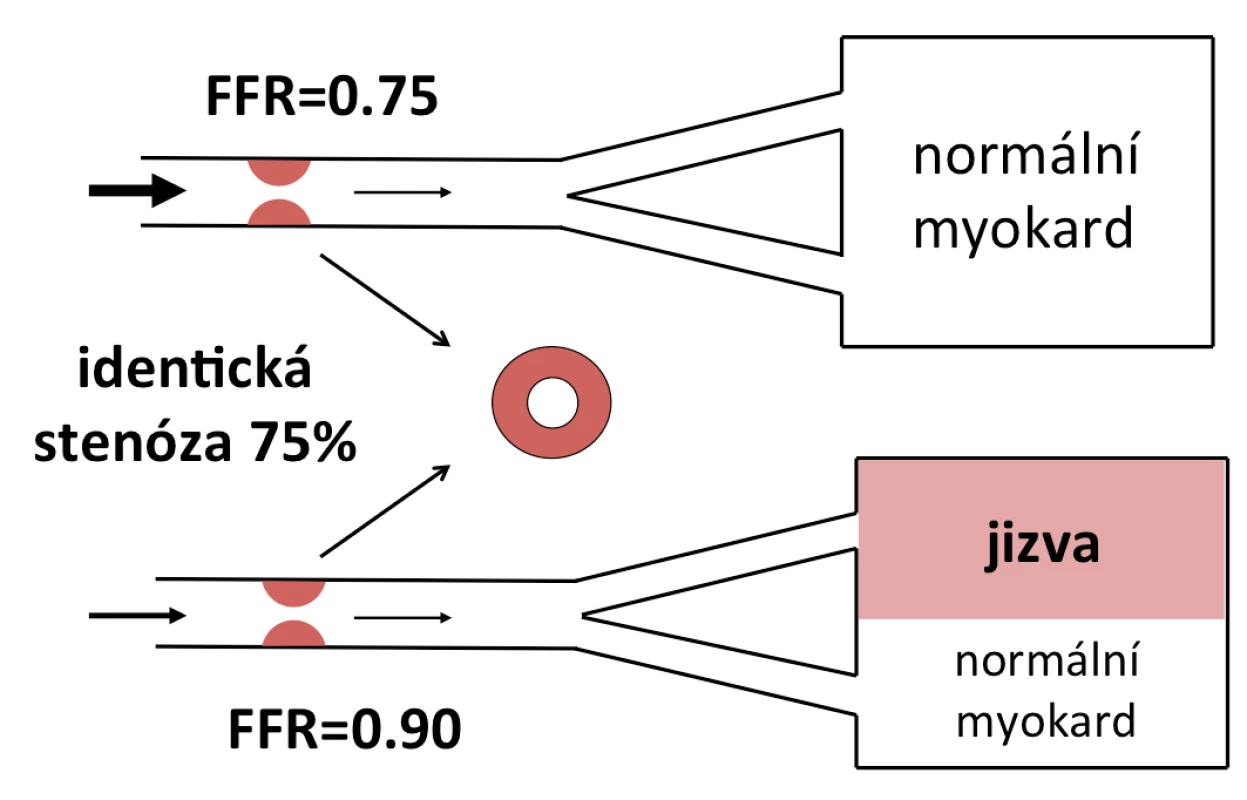
Při nedostatečné hyperemii FFR poskytuje falešně vyšší hodnoty a hrozí podhodnocení funkční významnosti stenózy. To je i jedním z hlavních omezení metody, kdy neexistuje spolehlivý ukazatel, který by verifikoval, že bylo maximální hyperemie dosaženo. FFR není validována u pacientů s akutním koronárním syndromem s elevacemi úseku ST a u nemocných s dekompenzovaným srdečním selháním. Do studií rovněž nebyli zahrnuti nemocní s hypertrofií levé komory (interventrikulární septum > 13 mm). Při významně zvýšeném tlaku v pravé síní je nutné tuto hodnotu zahrnout do výpočtu podle upraveného vzorce.
Klinické studie DEFER, FAME, FAME-2
DEFER byla první větší randomizovanou studií sledující klinický dopad funkční revaskularizace oproti intervencím vedených pouze za základě morfologického nálezu. Pacienti se stabilní ischemickou chorobou srdeční a angiograficky hraniční stenózou jedné tepny podstoupili revaskularizaci při hodnotě FFR < 0,75, zatímco nemocní s hodnotou FFR ≥ 0,75 byli rozděleni do invazivně léčené skupiny a do skupiny s podáváním samotných farmak.
Po 5letém sledování studie DEFER prokázala bezpečnost odložení intervence funkčně nevýznamné léze [6]. Obdobně ani po 15 letech nebyl shledán přínos koronární intervence při FFR ≥ 0,75, úmrtnost v intervenované a konzervativní větvi činila 31,1 vs. 33 % (p = 0,79) (22). Jistou limitací je doba vzniku studie (probíhala v letech 1997 a 1998) a tehdejší postupy, které již neodpovídají současným standardům.
Studie FAME a FAME-2 se zaměřily na pacienty se stabilní ischemickou chorobou srdeční a postižením více koronárních tepen, indikací k intervenci ve funkční skupině byla hodnota FFR ≤ 80. První zmíněná studie ukázala při ročním sledování u celkem 1005 pacientů významně menší výskyt infarktu myokardu nebo úmrtí ve skupině intervenovaných podle FFR ve srovnání s nemocnými ošetřenými intervencí na základě angiografického obrazu (7,3 vs. 11,1 %; p = 0,04) (23).
Je nutné zmínit, že po 5 letech nebyl prokázán statisticky významný rozdíl mezi oběma skupinami. K primárnímu kombinovanému cíli zahrnujícímu úmrtí, infarkt myokardu a opakovanou revaskularizaci došlo u 31 % pacientů v angiograficky vedené větvi a u 28 % v FFR větvi (p = 0,31). Potvrdila se ovšem dlouhodobá bezpečnost při odložení výkonu u hemodynamicky nevýznamné stenózy, ve skupině FFR byla i významně menší spotřeba stentů (1,9 vs. 2,7; p < 0,0001) (24).
Studie FAME-2 porovnávající výsledky funkčně vedené revaskularizace s optimální farmakoterapií proti samotné farmakologické léčbě byla předčasně ukončena po randomizaci 1230 pacientů pro významný nárůst urgentních revaskularizací ve skupině léčené pouze farmakologicky (12,7 vs. 4,3 %; HR = 0,32; 95% CI = 0,19–0,53; p < 0.001) (25, 26).
Aktuálně probíhá studie FAME-3, která si dala za cíl prokázat non-inferioritu perkutánních koronárních intervencí vůči chirurgické revaskularizaci (CABG) u nemocných s postižením více tepen (27). Zda se v době lékových stentů druhé generace a za použití metody FFR podaří změnit postupy vycházející ze studie SYNTAX, jejíž výsledky ukázaly u choroby tří tepen převahu CABG (28), bude jednou z očekávaných událostí intervenční kardiologie.
Klidové indexy
V posledních několika letech došlo k výraznému rozvoji nových metod, které nejsou závislé na maximální hyperemii v koronárním řečišti, tzv. klidových indexů. Jedná se především o index iFR (instantaneous wave-free ratio), jehož základním principem je měření tlakového gradientu ve střední části diastoly, kdy je hodnota intramyokardiální rezistence spontánně nízká a stabilní.
Metoda využívá stejný intrakoronární vodič jako FFR, vlastní měření všakprobíhá při normální perfuzi věnčitých tepen. Řada dosud publikovaných prací potvrdila správnost konceptu iFR i dobrou korelaci s FFR, širšímu klinickému užití nicméně zatím brání absence větších randomizovaných studií (29−31).
Závěr
Funkční vyšetření se dnes právem stává rutinní součástí invazivního hodnocení věnčitých tepen. Odstraňuje pochyby, zda daná léze způsobuje ischemii myokardu, či nikoliv. Jedná se o zásadní informaci, neboť jen odstranění ischemie vede ke zlepšení prognózy nemocných. Intervence stenózy, která nezpůsobuje ischemii myokardu, byť technicky bezchybná, má za následek zatížení pacienta rizikem vzniku restenózy nebo trombózy ve stentu a podmiňuje nutnost užívání duální antiagregace, aniž by pacientovi přinášela prospěch.
Vyšetření pomocí měření frakční průtokové rezervy je však nutné brát jen jako jeden z faktorů v rozhodování o typu léčby. Bylo by jistě chybou redukovat indikaci koronární intervence pouze na jediné číslo. Je také třeba mít na paměti omezení stanovení FFR, jakými jsou neexistence ukazatele dosažení maximální hyperemie (jež je dle definice základním předpokladem správného FFR měření), inherentní variabilita, udávaná až v rozsahu 10 %, nebo možná falešná pozitivita v situaci výrazně zvýšeného průtoku přes stenózu u lézí nezpůsobujících omezení koronární rezervy. Některé z těchto limitů by mohly být překonány tzv. klidovými indexy.
Tento typ vyšetření zatím není zahrnut v doporučeních a před potvrzením jejich validity bude nutné vyčkat na výsledky probíhajících randomizovaných studií. Pro rutinní praxi v katetrizační laboratoři je ovšem zásadní přijmout změnu paradigmatu, že morfologická vyšetření selhávají v hodnocení funkční významnosti lézí, které označujeme pojmem „hraniční“ a u nichž je jednoznačně nutné ověřit jejich hemodynamický dopad před indikací koronární intervence.
Podpořeno Grantovou agenturou Univerzity Karlovy v Praze (projekt č. 191415).
Seznam použitých zkratek
CABG aortakoronární bypass
FFR frakční průtoková rezerva
i. v. intravenózně
i. c. intrakoronárně
iFR instantaneous wave-free index
Adresa pro korespondenci:
MUDr. Štěpán Jeřábek
II. interní klinika − klinika kardiologie a angiologie 1. lékařské fakulty UK a Všeobecné fakultní nemocnice v Praze
U Nemocnice 2
128 08 Praha 2
Tel.: 724 306 768
e-mail: stepan.jerabek@lf1.cuni.cz
Sources
1. Gruentzig A, Senning A, Siegenthaler WE. Nonoperative dilatation of coronary artery stenosis: percutaneous transluminal coronary angioplasty. N Engl J Med 1979; 301(2): 61–68.
2. Pijls NH, van Son JA, Kirkeeide RL et al. Experimental basis of determining maximum coronary, myocardial, and collateral blood flow by pressure measurements for assessing functional stenosis severity before and after percutaneous transluminal coronary angioplasty. Circulation 1993; 87(4): 1354–1367.
3. Pijls NH, Van Gelder B, Van der Voort P et al. Fractional flow reserve: A useful index to evaluate the influence of an epicardial coronary stenosis on myocardial blood flow. Circulation 1995; 92(11): 3183–3193.
4. Pijls NH, De Bruyne B, Peels K et al. Measurement of fractional flow reserve to assess the functional severity of coronary artery stenoses. N Engl J Med 1996; 334(26): 1703–1708.
5. Boden WE, O’Rourke RA, Teo KK et al. Optimal Medical Therapy with or without PCI for Stable Coronary Disease. N Engl J Med 2007; 356(15): 1503–1516.
6. Pijls NH, van Schaardenburgh P, Manoharan G et al. Percutaneous coronary intervention of functionally nonsignificant stenosis: 5-year follow-up of the DEFER Study. J Am Coll Cardiol 2007; 49(21): 2105–2111.
7. Uren NG, Melin JA, De Bruyne B. Relation between myocardial blood flow and the severity of coronary-artery stenosis. N Engl J Med 1994; 330(25): 1782–1788.
8. Johnson NP, Kirkeeide RL, Gould KL. Coronary anatomy to predict physiology: fundamental limits. Circ Cardiovasc Imaging 2013; 6(5): 817–832.
9. Heijenbrok-Kal MH, Fleischmann KE, Hunink MG. Stress echocardiography, stress single-photon-emission computed tomography and electron beam computed tomography for the assessment of coronary artery disease: a meta-analysis of diagnostic performance. Am Heart J 2007; 154(3): 415–423.
10. McArdle BA, Dowsley TF, deKemp RA et al. Does rubidium-82 PET have superior accuracy to SPECT perfusion imaging for the diagnosis of obstructive coronary disease?: A systematic review and meta-analysis. J Am Coll Cardiol 2012; 60(18): 1828–1837.
11. de Jong MC, Genders TS, van Geuns RJ et al. Diagnostic performance of stress myocardial perfusion imaging for coronary artery disease: a systematic review and meta-analysis. Eur Radiol 2012; 22(9): 1881–1895.
12. Nandalur KR, Dwamena BA, Choudhri AF et al. Diagnostic performance of stress cardiac magnetic resonance imaging in the detection of coronary artery disease: a meta-analysis. J Am Coll Cardiol 2007; 50(4): 1343–1353.
13. Lima RS, Watson DD, Goode AR et al. Incremental value of combined perfusion and function over perfusion alone by gated SPECT myocardial perfusion imaging for detection of severe three-vessel coronary artery disease. J Am Coll Cardiol 2003; 42(1): 64–70.
14. Montalescot G, Sechtem U, Achenbach S et al. 2013 ESC guidelines on the management of stable coronary artery disease: the Task Force on the management of stable coronary artery disease of the European Society of Cardiology. Eur Heart J 2013; 34(38): 2949–3003.
15. Windecker S, Kolh P, Alfonso F et al. 2014 ESC/EACTS Guidelines on myocardial revascularization: the task force on myocardial revascularization of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS) developed with the special contribution of the European Association of Percutaneous Cardiovascular Interventions (EAPCI). Eur Heart J 2014; 35(37): 2541–2619.
16. Camici PG, Crea F. Coronary microvascular dysfunction. N Engl J Med 2007; 356(8): 830–840.
17. Lanza GA, Crea F. Primary coronary microvascular dysfunction: clinical presentation, pathophysiology, and management. Circulation 2010; 121(21): 2317–2325.
18. De Bruyne B, Pijls NH, Barbato E et al. Intracoronary and intravenous adenosine 5‘-triphosphate, adenosine, papaverine, and contrast medium to assess fractional flow reserve in humans. Circulation 2003; 107(14): 1877–1883.
19. McGeoch RJ, Oldroyd KG. Pharmacological options for inducing maximal hyperaemia during studies of coronary physiology. Catheter Cardiovasc Interv 2008; 71(2): 198–204.
20. Nair PK, Marroquin OC, Mulukutla SR et al. Clinical utility of regadenoson for assessing fractional flow reserve. J Am Coll Cardiovasc Interv 2011; 4(10): 1085–1092.
21. Pijls NH, Tonino PA. The crux of maximum hyperemia: The last remaining barrier for routine use of fractional flow reserve. J Am Coll Cardiovasc Interv 2011; 4(10): 1093–1095.
22. Zimmermann FM, Ferrara A, Johnson NP et al. Deferral vs. performance of percutaneous coronary intervention of functionally non-significant coronary stenosis: 15-year follow-up of the DEFER trial. Eur Heart J 2015; 36(45): 3182–3188.
23. Tonino PA, De Bruyne B, Pijls NH et al. Fractional flow reserve versus angiography for guiding percutaneous coronary intervention. N Engl J Med 2009; 360(3): 213–224.
24. van Nunen LX, Zimmermann FM, Tonino PAL et al. Fractional flow reserve versus angiography for guidance of PCI in patients with multivessel coronary artery disease (FAME): 5-year follow-up of a randomised controlled trial. Lancet 2015; 386(10006): 1853–1860.
25. De Bruyne B, Pijls NH, Kalesan B et al. Fractional flow reserve-guided PCI versus medical therapy in stable coronary disease. N Engl J Med 2012; 367(11): 991–1001.
26. De Bruyne B, Fearon WF, Pijls NH et al. Fractional flow reserve-guided PCI for stable coronary artery disease. N Engl J Med 2014; 371(13): 1208–1217.
27. Zimmermann FM, De Bruyne B, Pijls NHJ et al. Rationale and design of the Fractional Flow Reserve versus Angiography for Multivessel Evaluation (FAME) 3 Trial: A comparison of fractional flow reserve-guided percutaneous coronary intervention and coronary artery bypass graft surgery in patients with multivessel coronary artery disease. Am Heart J 2015; 170(4): 619–626.
28. Serruys PW, Morice MC, Kappetein AP et al. Percutaneous coronary intervention versus coronary-artery bypass grafting for severe coronary artery disease. N Engl J Med 2009; 360(10): 961–972.
29. Sen S, Escaned J, Malik IS et al. Development and validation of a new adenosine-independent index of stenosis severity from coronary wave-intensity analysis: results of the ADVISE (ADenosine Vasodilator Independent Stenosis Evaluation) study. J Am Coll Cardiol 2012; 59(15): 1392–1402.
30. Sen S, Asrress KN, Nijjer S et al. Diagnostic classification of the instantaneous wave-free ratio is equivalent to fractional flow reserve and is not improved with adenosine administration. Results of CLARIFY (Classification Accuracy of Pressure-Only Ratios Against Indices Using Flow Study). J Am Coll Cardiol 2013; 61(13): 1409–1420.
31. Petraco R, Al-Lamee R, Gotberg M et al. Real-time use of instantaneous wave–free ratio: Results of the ADVISE in-practice: An international, multicenter evaluation of instantaneous wave-free ratio in clinical practice. Am Heart J 2014; 168(5): 739–748.
32. PijlsNH, Sels JW. Functional measurement of coronary stenosis. J Am Coll Cardiol 2012; 59(12): 1045–1057.
Labels
Addictology Allergology and clinical immunology Angiology Audiology Clinical biochemistry Dermatology & STDs Paediatric gastroenterology Paediatric surgery Paediatric cardiology Paediatric neurology Paediatric ENT Paediatric psychiatry Paediatric rheumatology Diabetology Pharmacy Vascular surgery Pain management Dental Hygienist
Article was published inJournal of Czech Physicians

-
All articles in this issue
- Studie SPRINT: Kam až snižovat systolický krevní tlak
- Hodnocení hemodynamické významnosti koronárních stenóz metodou frakční průtokové rezervy
- Matrix Gla protein jako přirozený inhibitor vaskulárních kalcifikací a potenciální léčebný cíl
- Angiologie kráčí vpřed
- Psychiatrie v realitě všedního dne
- Péče na konci života v České republice
- Význam HPV vakcinace mužů
- Dermatomyozitída
- Zemřel profesor Radomír Čihák
- Prognostické faktory idiopatické plicní fibrózy (IPF) – analýza Českého registru IPF
- Roger Wolcott Sperry (1913–1994)
- Journal of Czech Physicians
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Význam HPV vakcinace mužů
- Dermatomyozitída
- Hodnocení hemodynamické významnosti koronárních stenóz metodou frakční průtokové rezervy
- Matrix Gla protein jako přirozený inhibitor vaskulárních kalcifikací a potenciální léčebný cíl
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

