-
Medical journals
- Career
Prevencia a liečba venózneho tromboembolizmu spojeného s malignitou – interdisciplinárny konsenzus
Authors: Ivar Vacula 1; Zuzana Rusiňáková 2; Denisa Čelovská 3; Peter Jackuliak 4; Ján Slopovský 5; Patrik Palacka 5; Matej Moščovič 6; Stanislav Špánik 7; Ján Staško 8; Alexander Wild 9; Angelika Bátorová 10; Juraj Ma Arič 11
Authors‘ workplace: Angiologická‑interná ambulancia, Trnava 1; Klinika onkohematológie LF UK a NOÚ, Bratislava 2; I. interná klinika LF UK a UN, Bratislava 3; V. interná klinika LF UK a UN, Bratislava 4; II. onkologická klinika LF UK a NOÚ, Bratislava 5; Klinika angiológie VÚSCH, a. s., Košice 6; I. onkologická klinika LF UK a OÚSA, Bratislava 7; Klinika hematológie a transfuziológie JLF UK Martin 8; Hematologické oddelenie, FNsP F. D. Roosevelta, Banská Bystrica 9; Klinika hematológie a transfúziológie LF UK, SZU a UN, Bratislava 10; Klinika angiológie LF UK a NÚSCH, a. s., Bratislava 11
Published in: Vnitř Lék 2022; 68(4): 221-226
Category: Review Articles
Overview
Narastajúci objem dát a skúseností s použitím priamych orálnych antikoagulancií (DOAK) v primárnej aj sekundárnej prevencii venózneho tromboembolizmu u onkologických pacientov (CAVTE) viedol ku zmenám v početných medzinárodných odporúčaniach. Reflektujeme tieto zmeny s ohľadom na podmienky v SR. V primárnej prevencii CAVTE rozlišujeme onkologických pacientov na tých, ktorí podstupujú v súvislosti s ochorením chirurgický zákrok a na nechirurgických pacientov: hospitalizovaných a ambulantne liečených. Za základné liečivá v primárnej prevencii naďalej považujeme heparíny s nízkou molekulovou hmotnosťou (LMWH). V liečbe a sekundárnej prevencii CAVTE odporúčame uvažovať vždy aj o možnosti použiť DOAKy ako z hľadiska účinnosti rovnocennú alternatívu LMWH. LMWH je potrebné preferovať pred DOAKmi aj warfarinom u všetkých pacientov s klinicky nestabilnou situáciou s vysokým rizikom krvácania a vysokým rizikom interakcie so systémovou liečbou. Predovšetkým ide o pacientov s intraluminálnymi nádormi hornej časti gastrointestinálneho traktu a urogenitálnymi malignitami s vysokým rizikom krvácania. Pre nedostatočný objem dát sú LMWH stále preferované aj u pacientov s primárnymi nádormi a metastatickým postihnutím centrálnej nervovej sústavy a u hematoonkologických pacientov.
Klíčová slova:
krvácanie – malignita – venózny tromboembolizmus (VTE – CAVTE) – onkologické ochorenie – priame orálne antikoagulans (DOAK) – heparín s nízkou molekulovou hmotnosťou (LMWH)
Úvod
Posledné dve desaťročia sme svedkami rozsiahlych programov klinických štúdií v oblasti antitrombotík, obzvlášť s tzv. novými alebo priamymi orálnymi antikoagulanciami (Direct Oral Anticoagulants − DOAK). Nielen v oblasti prevencie a liečby venózneho tromboembolizmu znamenajú po desiatkach rokoch doslova revolúciu. Venózny tromboembolizmus spojený s malignitou (ďalej v texte Cancer Associated Venous Thromboembolism – CAVTE) reprezentuje azda najkontroverznejšiu časť skúmanej oblasti. Veľmi heterogénna skupina pacientov s malignitami, navyše u každého chorého s dynamicky sa meniacim stavom v jednotlivých fázach vývoja onkologického ochorenia a s vedľajšími účinkami systémovej liečby, neumožňuje vytvoriť jednotný všeobecne aplikovateľný algoritmus. Počas trvania aktívneho onkologického ochorenia však až približne 20 % pacientov prekoná, alebo podľahne epizóde CAVTE. Pľúcna embólia (PE) je na druhom mieste príčin úmrtia onkologických pacientov (1). CAVTE je jedným z najzávažnejších faktorov limitujúcim prežívanie onkologických pacientov. Na výsledky originálneho výskumu reagovali v posledných 3 rokoch viaceré národné aj medzinárodné odborné, prevažne onkologické a hematologické spoločnosti úpravou odporúčaní pre prevenciu a liečbu CAVTE. Cieľom tohto dokumentu je priniesť kritické zhodnotenie ich prínosu a reálnej aplikácie v podmienkach SR.
V celom procese diagnostiky, prevencie a liečby CAVTE je nevyhnutná interdisciplinárna spolupráca, v ktorej kľúčovú úlohu zohrávajú onkológ, angiológ, hematológ a internista, ale často sa podieľajú na starostlivosti aj všeobecný lekár, kardiológ, cievny chirurg alebo onkochirurg. Adekvátnou diagnostickou metódou pre diagnostiku hlbokej žilovej trombózy (HŽT) je kompresívna ultrasonografia. Štandardom diagnostiky PE zostáva CT pulmoangiografia, iné diagnostické metódy sa používajú len vo výnimočných prípadoch.
Farmakologický prehľad
Základnými liečivami, ktoré sa v SR používajú v súčasnosti v prevencii a liečbe CAVTE sú heparíny s nízkou molekulovou hmotnosťou (LMWH), warfarín a zatiaľ menej často − lieky zo skupiny DOAK. Fondaparinux sa využíva skôr výnimočne, napríklad u pacientov s heparínom indukovanou trombocytopéniou. V tabuľke 1 uvádzame prehľad liečiv a ich základné charakteristiky.
Table 1. Prehľad antikoagulancií pri liečbe a prevencii CAVTE (prevzaté a adaptované (podľa 2)) 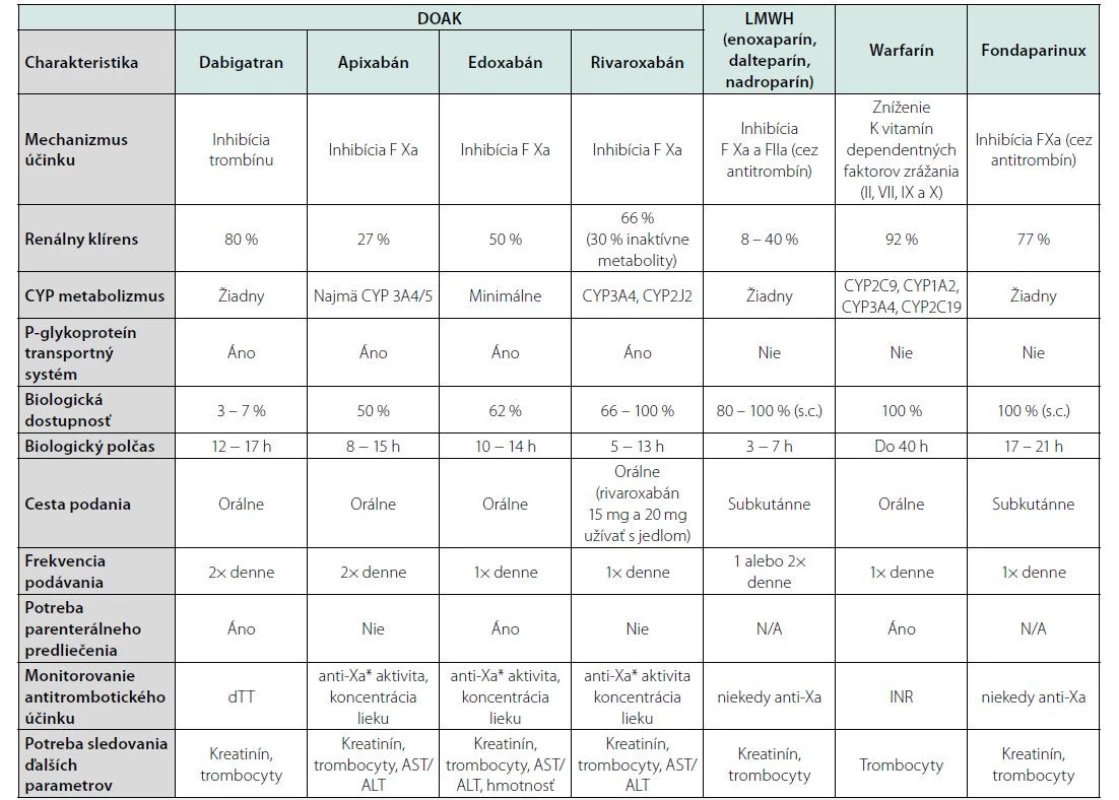
Vysvetlivky: CYP – cytochróm P 450, dTT − diluovaný trombínový čas, anti‑Xa* − aktivita kalibrovaná na príslušný Xabán AST – aspartátaminotransferáza, ALT − alanínaminotransferáza, N/A – neaplikovateľné, INR – international normalized ratio – medzinárodný normalizovaný pomer Primárna prevencia CAVTE
Na účely rozhodovania o indikácii primárnej farmakologickej prevencie CAVTE je nevyhnutné rozdeliť onkologických pacientov na tých, ktorí podstupujú v súvislosti s ochorením chirurgický výkon a pacientov s aktívnym nádorovým ochorením liečených systémovou liečbou (tzv. „nechirurgických“). Osobitnú skupinu chorých s nádorovým ochorením tvoria nechirurgickí pacienti, ktorí nevyžadujú hospitalizáciu.
Prevencia CAVTE v onkochirurgii
U onkologického pacienta, ktorý podstupuje chirurgický výkon, je indikovaná farmakologická tromboprofylaxia za predpokladu, že pre ňu nie je prítomná kontraindikácia (Tab. 2). V opačnom prípade sa používa mechanická tromboprofylaxia (3).
Table 2. Kontraindikácie perioperačnej tromboprofylaxie 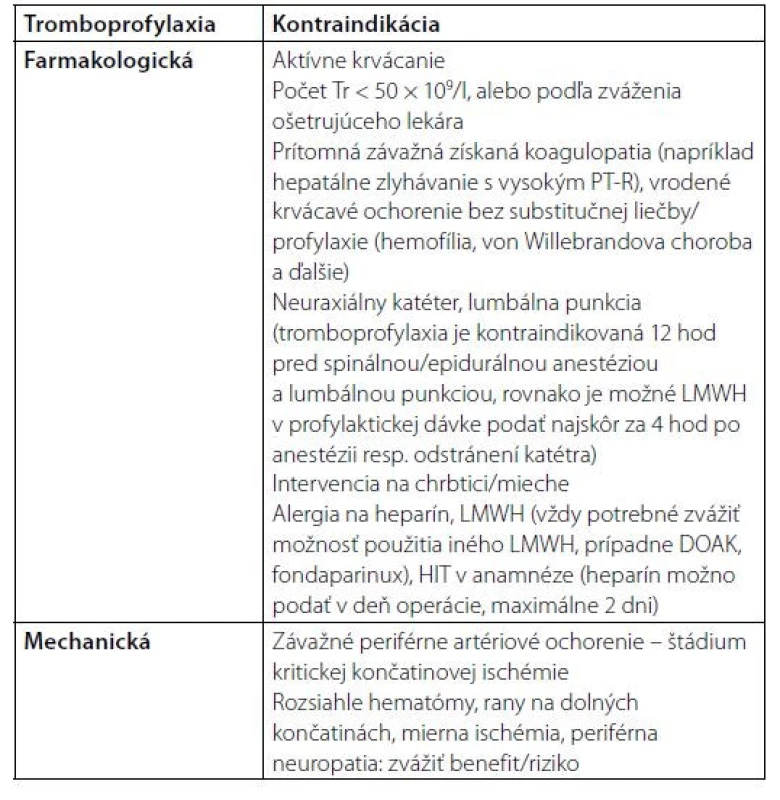
Spôsob farmakologickej tromboprofylaxie určuje ošetrujúci lekár, v súčasnosti sú v SR dostupné v tejto indikácii výlučne preparáty LMWH. Podávanie lieku sa začne spravidla 2 hodiny (1 − 4 podľa zvoleného LMWH, ale 2 hodiny sú zjednodušením, aplikovateľným pre všetky) pred operačným výkonom. Alternatívne sa podá dávka 12 hodín pred plánovaným veľkým operačným výkonom a potom najskôr 6 − 8 hodín po výkone. Profylaxia pokračuje o 24 hodín a ďalej raz denne subkutánne (s.c.), minimálne do prepustenia do ambulantnej starostlivosti. Pri vysokorizikových abdominálnych a pelvických chirurgických výkonoch pokračujeme po prepustení do 28. pooperačného dňa (výkon s anestéziou dlhšou ako 2 hodiny, pripútaní na lôžko 4 a viac dní po operácii, vek nad 60 rokov, alebo pokročilé onkologické ochorenie) (4). V medzinárodných odporúčaniach v prípade gynekologických malignít už figuruje aj apixabán, očakávame ďalšie dáta k širšiemu použitiu a tiež k schváleniu legislatívnych zmien v SR.
U obéznych onkologických pacientov s BMI > 40 kg/m2 sa odporúča podávať profylaktickú dávku 2× denne (5).
V prípade kontraindikácie farmakologickej tromboprofylaxie je potrebné zabezpečiť mechanickú tromboprofylaxiu (intermitentná pneumatická kompresia alebo kompresívne pančuchy) a opakovane prehodnocovať pomer riziko/benefit farmakologickej tromboprofylaxie.
Nechirurgickí hospitalizovaní onkologickí pacienti
Hospitalizácia pacienta s onkologickým ochorením často vyžaduje podávanie tromboprofylaxie (vek nad 40 rokov, akútne interkurentné ochorenie ako dôvod hospitalizácie, pridružené rizikové faktory, najmä hospitalizácia dlhšia ako 6 dní, pokoj na lôžku alebo obmedzenie hybnosti počas 3 a viac dní, anamnéza prekonanej príhody venózneho tromboembolizmu (VTE) – ak nie je na trvalej antikoagulačnej liečbe) (4). Podmienka veku je z nášho pohľadu kontroverzná a prikláňame sa k názoru, že sám vek pacienta nad 40 rokov nie je indikáciou na použitie farmakologickej tromboprofylaxie. Preparáty LMWH sa všeobecne favorizujú pred nefrakcionovaným heparínom (UFH). V podmienkach SR sa používajú nasledovné dávky liečiv: dalteparín 5 000 IU, enoxaparín 40 mg, nadroparín pri hmotnosti ≤ 70 kg 0,4 ml (3 800 anti‑Xa IU) a pri hmotnosti > 70 kg 0,6 ml (5 700 anti‑Xa IU), všetky podávané s.c. raz denne. Trvanie tromboprofylaxie ohraničuje termín prepustenia do ambulantnej starostlivosti, výnimočne je možné zvažovať jej predĺženie, napr. pri pretrvávaní obmedzenej hybnosti pacienta (samostatná skupina vysokorizikových ambulantne liečených pacientov je uvedená nižšie).
Nechirurgickí ambulantne liečení onkologickí pacienti
Jednou z najvýraznejších zmien vo všetkých odporúčaniach je individualizovaný prístup k primárnej prevencii VTE u ambulantne liečených onkologických pacientov. Je to súčasne najkontroverznejšia časť odporúčaní. Pre odhad rizika VTE sa najčastejšie odporúča používať validovaný Khoranov prediktívny model (Tab. 3) (6).
Table 3. Khoranov prediktívny model – hodnotenie rizika VTE u ambulantne liečených onkologických pacientov (6) 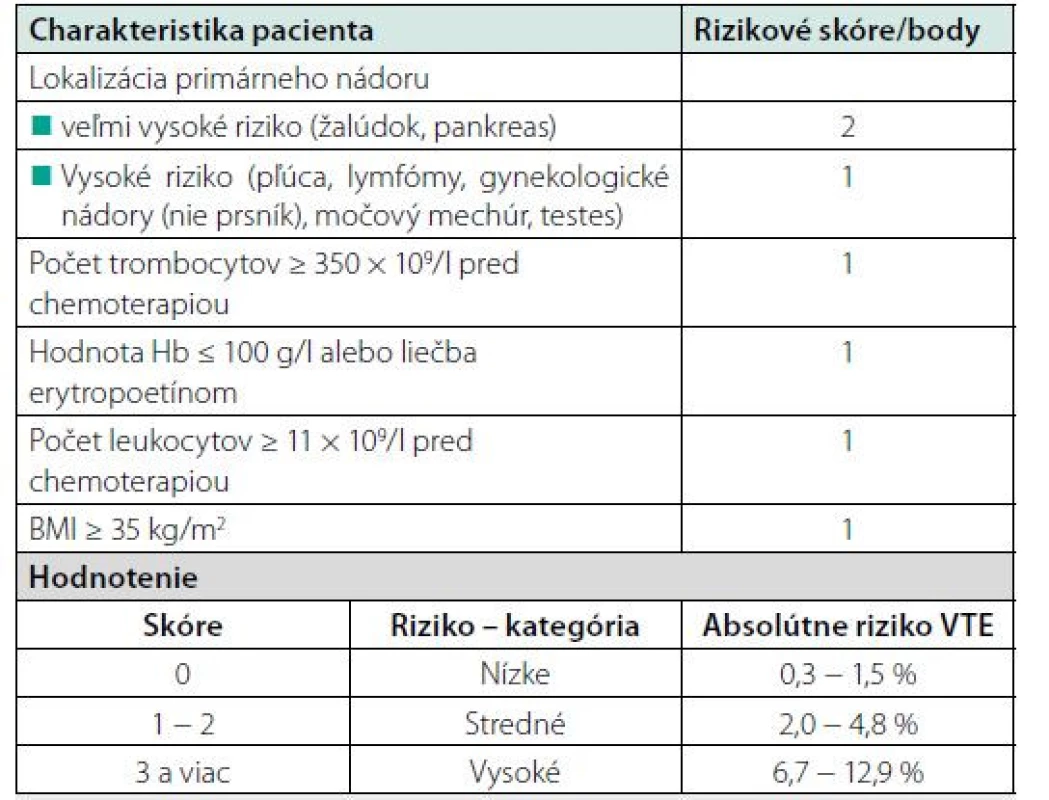
BMI – body mass index, Hb – hemoglobín, VTE – venózny tromboembolizmus Na základe výsledkov klinických štúdií AVERT (7) a CASSINI (8) sa zmenili odporúčania s podporou primárnej farmakologickej prevencie u pacientov so stredným a vysokým rizikom s Khorana score ≥ 2 a to po dobu 6 mesiacov, resp. aj dlhšie, ak riziko pretrváva (LMWH a/alebo DOAC – rivaroxabán a/alebo apixabán) (9). K tomuto odporúčaniu predkladáme nasledovný komentár s výhradami:
• Metaanalýza klinických štúdií s LMWH v primárnej prevencii v tejto skupine pacientov viedla k nasledujúcim záverom: profylaxia s LMWH signifikantne znížila riziko VTE pri štatisticky nevýznamnom zvýšení krvácavých komplikácií v porovnaní s placebom. Výskyt VTE však bol všeobecne nízky (Khoranov model nebol použitý na selekciu pacientov vo všetkých zahrnutých štúdiách). NNT (number needed to treat) bolo vyčíslené na 32, NNH (number needed to harm) predstavovalo 191 pacientov. Tieto výsledky, hoci z roku 2016, neviedli k zmene odporúčaní, rovnako ani k zavedeniu rutinnej profylaxie u ambulantne liečených onkologických pacientov.
• Výsledky spomínaných klinických štúdií AVERT a CASSINI sa nedajú interpretovať ako jednoznačné. Zatiaľ čo v klinickej štúdii AVERT došlo k štatisticky významnému zníženiu rizika VTE počas 180 dní (apixabán: 4,2 % vs. placebo: 10,2 %, hazard ratio [HR], 0,41; 95% CI, 0,26 − 0,65; p < 0,001), súčasne sa zistilo signifikantne viac závažných krvácaní (apixabán 2,5 mg BID: 3,5 % vs. placebo: 1,8 %; HR 2,00; 95 % CI, 1,01 − 3,95; p = 0,046). Vypočítané NNT bolo 17, NNH: 59. Klinická štúdia CASSINI nepreukázala štatisticky významné zníženie výskytu VTE udalostí (rivaroxabán: 6,0 % vs. placebo: 8,8 %, HR: 0,66; 95 % CI, 0,40 − 1,09; p = 0,10) pri rovnako nevýznamnom rozdiele vo výskyte závažného krvácania (rivaroxabán 10 mg denne: 2,0 % vs. placebo: 1,0 %; HR: 1,96; 95 % CI, 0,59 − 6,49; p = 0,26). Vypočítané NNT bolo 35 a NNH 101 pacientov.
Podľa nášho názoru zatiaľ nie sú pre primárnu prevenciu CAVTE u nechirurgických pacientov jednoznačné dôkazy na úrovni EBM (evidence based medicine – medicína dôkazov).
Preto sa domnievame, že v súčasnosti neexistuje dôvod pre rutinnú tromboprofylaxiu ambulantne liečených onkologických pacientov. Khoranove skóre odporúčame používať v súvislosti s klinickým zhodnotením celkového funkčného stavu pacienta, pričom rozhodnutie o prípadnej primárnej farmakologickej tromboprofylaxii je vždy závislé od ošetrujúceho klinického onkológa alebo hematológa. Protinádorovou terapiou liečení pacienti s vysokým rizikom VTE, predovšetkým s lymfoproliferatívnymi ochoreniami, karcinómom pankreasu, pokročilým metastatickým ochorením pri zachovanom funkčnom stave môžu vyžadovať dočasné podávanie tromboprofylaxie v určitých fázach systémovej liečby. Špecifickú skupinu predstavujú pacienti s mnohopočetným myelómom liečení thalidomidom, lenalidomidom alebo pomalidomidom, u ktorých sa v tromboprofylaxii používa kyselina acetylosalicylová (10). U ostatných pacientov možno v súčasnosti v SR na tento účel použit len LMWH v tromboprofylaktickej dávke podávanej raz denne (dalteparín 5 000 IU, enoxaparín 40 mg a nadroparín 0,4 ml (3 800 anti‑Xa IU). V prípade nadroparínu možno u pacientov s hmotnosťou nad 70 kg zvážiť dávku 0,6 ml (5 700 anti‑Xa IU) (konsenzus autorov). Potrebu zmeniť alebo doplniť uvedené odporúčanie o skupinu liekov zo skupiny DOAK budeme naďalej monitorovať.
Terapia CAVTE
Pod terapiou v tomto dokumente rozumieme akútnu fázu liečenia hlbokej žilovej trombózy a/alebo pľúcnej embólie a sekundárnu prevenciu recidívy VTE.
Terapia sa má začať už pri klinickom podozrení na VTE a spravidla sa začína terapeutickou dávkou LMWH. V prípade absolútnej kontraindikácie antikoagulačnej liečby a v prípade recidívy pľúcnej embólie napriek účinnej antikoagulačnej liečbe sa výnimočne zvažuje implantácia dočasného kaválneho filtra, ale aj to iba v prípade, že ide o závažnú, proximálnu trombózu v akútnom štádiu, do 4 týždňov od vzniku symptómov.
Table 4. Kontraindikácie terapeutickej dávky antikoagulácie 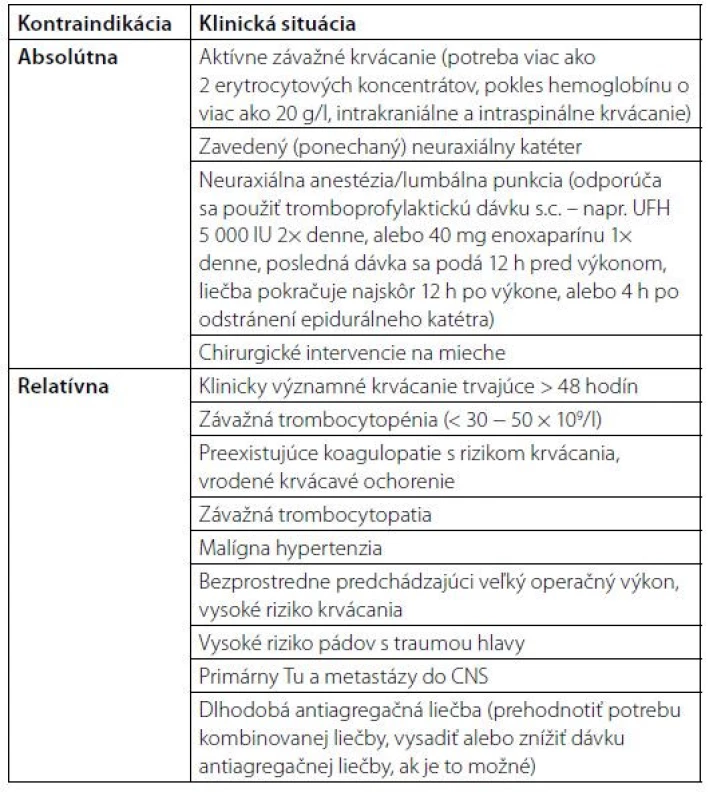
Špecifické kontraindikácie jednotlivých liekov sú uvedené v jednotlivých SPC a je potrebné ich rešpektovať. Najvýznamnejšou kontraindikáciou DOAK je zníženie glomerulárnej filtrácie CrCl < 30 ml/min (ďalšie dáta ohľadom bezpečnosti pri intervale 15 – 30 ml/min sa očakávajú) a zvýšenie AST nad 2 – 3-násobok hornej hranice normy.
Nález asymptomatickej HŽT alebo PE (relatívne častý záchyt je už pri stagingu a/alebo restagingu základného ochorenia) si vyžaduje minimálne 3-mesačnú antikoagulačnú liečbu. Neprikláňame sa k možnosti neliečiť pacientov so subsegmentálnou PE alebo distálnou HŽT, pričom platia rovnaké kontraindikácie antikoagulačnej liečby, ako je uvedené vyššie.
Naopak, v liečbe život ohrozujúcej pľúcnej embólie sa u onkologického pacienta uplatňuje podobný princíp ako u pacientov bez onkologického ochorenia. U pacientov s kurabilným onkologickým ochorením bez znakov aktívneho krvácania je pri PE s cirkulačnou instabilitou plne indikovaná systémová trombolytická liečba. Alternatívou sú pri vysokom riziku krvácania a súčasne dobrej časovej dostupnosti katétrová alebo chirurgická embolektómia.
Výber liečby
Doterajším štandardom liečby CAVTE je LMWH. Napriek tomu, že najviac údajov zo štúdie má dalteparín a tinzaparín, v SR sa v klinickej praxi používajú aj nadroparín a enoxaparín. Sú zaužívané počas celej doby liečby epizódy VTE u onkologického pacienta, pričom sa signifikantne menej často indikuje warfarín a lieky zo skupiny DOAK. Klinické štúdie porovnávajúce LMWH a warfarín – CLOT (11) a CATCH (12) zmenili pohľad na liečbu CAVTE a dnes sa všeobecne preferuje LMWH pred warfarínom. Protiargumentom zostáva najmä nedostatočný TTR (time in therapeutic range) v spomínaných klinických štúdiách pri liečbe warfarínom (v štúdii CLOT len 46 % a v štúdii CATCH len 47 % pacientov) (11, 13), ktorý mohol ovplyvniť vyšší výskyt VTE.
Klinické štúdie s liekmi skupiny DOAK preto rešpektovali zmenu klinického správania a ako komparátor v kontrolnom ramene použili práve LMWH. Pre dabigatran sú k dispozícii zatiaľ len limitované dáta. Postupne pribúdali presvedčivé výsledky s edoxabánom (štúdia HOKUSAI VTE Cancer) (14), rivaroxabánom (štúdia SELECT – D) (15) a napokon aj apixabánom (štúdia CARAVAGGIO) (16). Pre vysoké riziko krvácania v týchto klinických štúdiách absentovali alebo boli veľmi málo zastúpení pacienti s hematologickými malignitami a pacienti s primárnym a metastatickým postihnutím mozgu. Výsledky potvrdili, že všetky spomínané lieky skupiny DOAK v porovnaní s dalteparínom preukázali rovnakú účinnosť v sekundárnej prevencii CAVTE, avšak apixabán sa javí ako bezpečnejší pri nepriamom porovnaní s rivaroxabánom a edoxabánom, a to najmä v populácii pacientov s nádormi hornej časti tráviaceho traktu (16).
Aj výsledky týchto štúdií sa odrazili v konsenze 2 pracovných skupín Európskej kardiologickej spoločnosti. Problematiku CAVTE možno z ich pohľadu zjednodušiť nasledovne (17):
• v úvode liečby sa majú uprednostniť preparáty LMWH pred nefrakcionovaným heparínom,
• v dlhodobej liečbe sa LMWH uprednostňuje pred antagonistami vitamínu K (warfarín),
• edoxabán a rivaroxabán sa majú zvážiť ako alternatíva ku LMWH v iniciálnej aj dlhodobej liečbe pacientov s CAVTE pri neprítomnosti malignity gastrointestinálneho alebo uropoetického systému. Potrebný je však dohľad nad možnými interakciami so systémovou liečbou,
• apixabán sa má zvážiť ako alternatíva ku LMWH v iniciálnej aj dlhodobej liečbe pacientov s CAVTE u pacientov bez primárneho a metastatického postihnutia mozgu a bez hematoonkologického ochorenia. Potrebný je dohľad nad možnými interakciami so systémovou liečbou,
• LMWH sa preferuje pred DOAK v iniciálnej aj pokračujúcej liečbe u pacientov s CAVTE a nestabilnou klinickou situáciou ako sú trombocytopénia, nauzea a vracanie, riziko predpokladanej liekovej interakcie so systémovou liečbou, alebo u pacientov po chirurgickom výkone na hornej časti gastrointestinálneho traktu (znížené vstrebávanie lieku).
Pri rešpektovaní všetkých dostupných výsledkov vrátane údajov z registrov (real life/world data) predkladáme niekoľko klinických scenárov s ilustračným výberom lieku (Tab. 5). Pri výbere konkrétneho lieku je potrebné rešpektovať aj preferenciu pacienta a poskytnúť mu dostatok informácií, aby sa mohol podieľať na procese výberu liečiva. Avšak pokračujúca liečba/sekundárna prevencia CAVTE preparátmi DOAK po 6 mesiacoch liečby v SR v čase tvorby tohto dokumentu podlieha pravidelnému schváleniu úhrady revíznym lekárom na základe platných indikačných obmedzení.
Table 5. CAVTE – klinické scenáre a výber liečiva 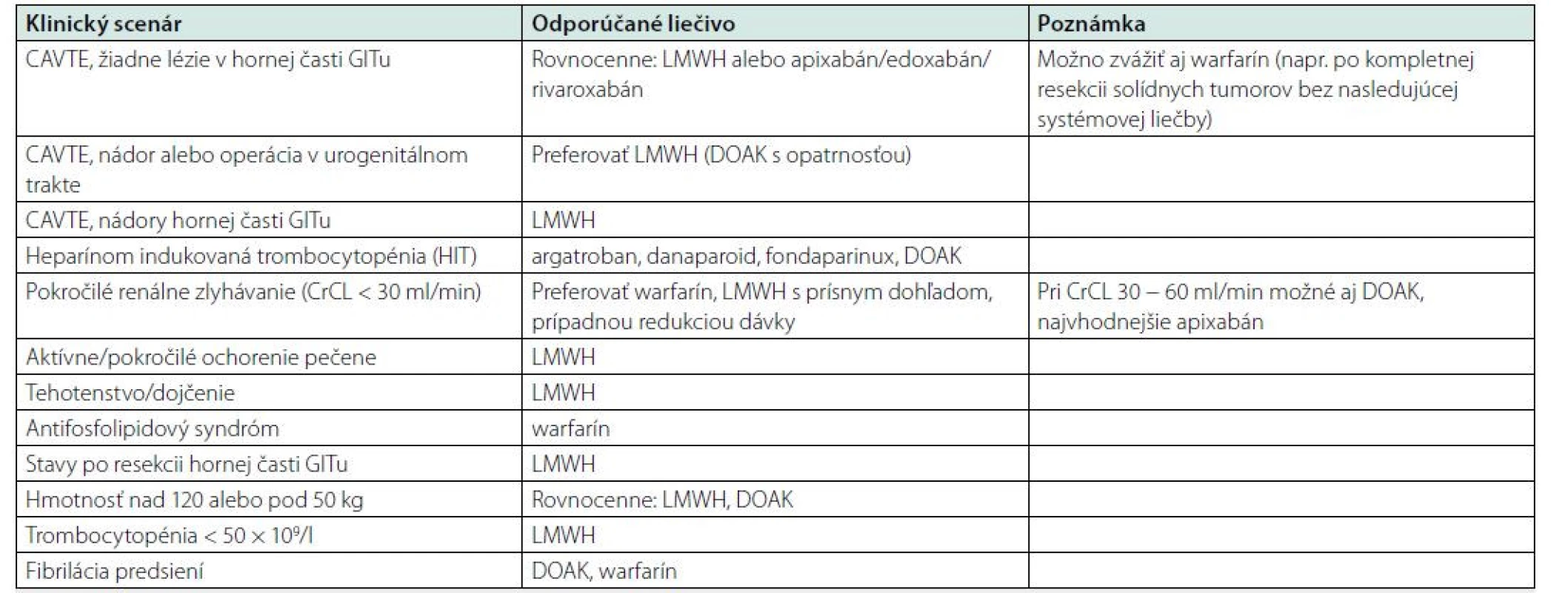
CAVTE – Cancer Associated Venous Thromboembolism, DOAK – direktné orálne antikoagulancium, GIT − gastro-intestinálny trakt, HIT – heparínom indukovaná trombocytopénia, LMWH – low molecular weight heparin Výber vhodného spôsobu antikoagulačnej liečby závisí aj od zhodnotenia potenciálne závažných liekových interakcií, ktoré sú uvedené v SPC jednotlivých liekov.
Trvanie antikoagulačnej liečby a sekundárnej profylaxie CAVTE
Aktívne onkologické ochorenie reprezentuje pretrvávajúce riziko recidívy CAVTE, a to si vyžaduje pokračovať v antikoagulačnej liečbe. Dôvodom ukončenia liečby CAVTE môže byť teda plné vyliečenie onkologického ochorenia pri neprítomnosti iných významných rizikových faktorov recidívy, alebo prevládnutie rizika krvácania. Zhodnotenie oboch vyžaduje spravidla interdisciplinárnu spoluprácu. Očakávajú sa výsledky klinických štúdií so zníženými dávkami DOAK v udržiavacej liečbe, ktoré môžu významne pomôcť v znížení rizika CAVTE pri súčasnom znížení rizika krvácania ako nežiaduceho účinku antikoagulačnej terapie.
Kompetencie v interdisciplinárnej starostlivosti o pacienta s CAVTE
Podozrenie na CAVTE epizódu počas aktívnej onkologickej liečby väčšinou vysloví onkológ, onkochirurg, onkohematológ prípadne iný ošetrujúci lekár. Diagnózu akútnej HŽT potvrdí angiológ resp. rádiológ kompresívnou ultrasonografiou čo najskôr od odoslania lekárom, ktorý suponoval diagnózu akútnej trombózy. Diagnózu pľúcnej embólie potvrdzuje rádiológ pomocou CT angiografie, výnimočne MR angiografie alebo ventilačno‑perfúzneho skenu. V prípade život ohrozujúcej PE je klinické vyšetrenie a transtorakálna echokardiografia často postačujúca na stanovenie diagnózy. Už samé podozrenie na HŽT a/alebo PE zakladá povinnosť začať liečbu. Do potvrdenia či vylúčenia diagnózy trombózy liečbu riadi väčšinou lekár, ktorý VTE zachytí. Pri aktívnom onkologickom ochorení (Tab. 6) je vhodné liečbu konzultovať s príslušným ošetrujúcim onkológom, onkohematológom alebo internistom. V SR nie je obmedzený predpis LMWH, ale v čase tvorby tohto dokumentu v širokom súbore špecialistov predpisujúcich lieky typu DOAK (chirurg, cievny chirurg, angiológ, internista, kardiológ, neurológ, hematológ, geriater) zatiaľ chýba odbornosť onkológa.
Table 6. Definícia aktívneho onkologického ochorenia (18) 
K pacientom s anamnézou onkologického ochorenia, ktorí sú v remisii a nevyžadujú systémovú terapiu, pristupujeme v diagnostike a liečbe VTE ako k neonkologickým pacientom. Liečbu VTE riadi angiológ, internista, kardiológ, hematológ, chirurg, prípadne iný ošetrujúci lekár.
Pri koincidencii nádorového ochorenia s onkohematologickým ochorením s trombocytopéniou alebo s hematologickým ochorením s poruchou hemostázy (koagulopatia, trombocytopatia) je potrebné antikoagulačnú liečbu alebo tromboprofylaxiu CAVTE konzultovať s hematológom.
Konsenzus schválený výbormi Slovenskej angiologickej spoločnosti, Slovenskej internistickej spoločnosti, Slovenskej onkologickej spoločnosti, Slovenskej spoločnosti hemostázy a trombózy, Slovenskej hematologickej a transfúziologickej spoločnosti.
KORESPONDENČNÍ ADRESA AUTORA:
MUDr. Ivar Vacula, PhD.
Angiologická-interná ambulancia Trnava
Halenárska 13/A, 917 01 Trnava
Cit. zkr: Vnitř Lék. 2022;68(4):221-226
Článek přijat redakcí: 11. 4. 2022
Článek přijat po recenzích: 11. 4. 2022
Sources
1. Khorana AA. Venous thromboembolism and prognosis in cancer. Thromb Res. 2010;125 : 490–493.
2. Schaefer JK, Elshoury A, Nachar VR, Streiff MB, Lim MY. How to Choose An Appropriate Anticoagulant for Cancer‑Associated Thrombosis. J Natl Compr Canc Netw. 2021 Oct 15;19(10):1203-1210. doi: 10.6004/jnccn.2021.7085. PMID: 34666314.
3. Lyman GH, Carrier M, Ay C, Di Nisio M, Hicks LK, Khorana AA, Leavitt AD, Lee AYY, Macbeth F, Morgan RL, Noble S, Sexton EA, Stenehjem D, Wiercioch W, Kahale LA, Alonso‑Coello P. American Society of Hematology 2021 guidelines for management of venous thromboembolism: prevention and treatment in patients with cancer. Blood Adv. 2021 Feb 23;5(4):927-974. doi: 10.1182/bloodadvances.2020003442. Erratum in: Blood Adv. 2021 Apr 13;5(7):1953. PMID: 33570602; PMCID: PMC7903232.
4. Streiff MB, Holmstrom B, Angelini D, Ashrani A, Elshoury A, Fanikos J, Fertrin KY, Fogerty AE, Gao S, Goldhaber SZ, Gundabolu K, Ibrahim I, Kraut E, Leavitt AD, Lee A, Lee JT, Lim M, Mann J, Martin K, McMahon B, Moriarty J, Morton C, Ortel TL, Paschal R, Schaefer J, Shattil S, Siddiqi T, Sudheendra D, Williams E, Hollinger L, Nguyen MQ. Cancer‑Associated Venous Thromboembolic Disease, Version 2.2021, NCCN Clinical Practice Guidelines in Oncology. J Natl Compr Canc Netw. 2021 Oct 15;19(10):1181-1201. doi: 10.6004/jnccn.2021.0047. PMID: 34666313.
5. Venclauskas, L, Maleckas A, Arcelus JI. European guidelines on perioperative venous thromboembolism prophylaxis. Surgery in the obese patients. Eur J Anaesthesiol 2018; 35 : 147-153.
6. Khorana AA, Kuderer NM, Culakova E, Lyman GH, Francis CW. Development and validation of a predictive model for chemotherapy‑associated thrombosis. Blood. 2008 May 15;111(10):4902-7. doi: 10.1182/blood-2007-10-116327. Epub 2008 Jan 23. PMID: 18216292; PMCID: PMC2384124.
7. Carrier M, Abou‑Nassar K, Mallick R, Tagalakis V, Shivakumar S, Schattner A, Kuruvilla P, Hill D, Spadafora S, Marquis K, Trinkaus M, Tomiak A, Lee AYY, Gross PL, Lazo‑Langner A, El‑Maraghi R, Goss G, Le Gal G, Stewart D, Ramsay T, Rodger M, Witham D, Wells PS; AVERT Investigators. Apixaban to Prevent Venous Thromboembolism in Patients with Cancer. N Engl J Med. 2019 Feb 21;380(8):711-719. doi: 10.1056/NEJMoa1814468. Epub 2018 Dec 4. PMID: 30511879.
8. Khorana AA, Soff GA, Kakkar AK, Vadhan‑Raj S, Riess H, Wun T, Streiff MB, Garcia DA, Liebman HA, Belani CP, O‘Reilly EM, Patel JN, Yimer HA, Wildgoose P, Burton P, Vijapurkar U, Kaul S, Eikelboom J, McBane R, Bauer KA, Kuderer NM, Lyman GH; CASSINI Investigators. Rivaroxaban for Thromboprophylaxis in High‑Risk Ambulatory Patients with Cancer. N Engl J Med. 2019 Feb 21;380(8):720-728. doi: 10.1056/NEJMoa1814630. PMID: 30786186.
9. Wang TF, Zwicker JI, Ay C, Pabinger I, Falanga A, Antic D, Noble S, Khorana AA, Carrier M, Meyer G. The use of direct oral anticoagulants for primary thromboprophylaxis in ambulatory cancer patients: Guidance from the SSC of the ISTH. J Thromb Haemost. 2019 Oct;17(10):1772-1778. doi: 10.1111/jth.14564. Epub 2019 Jul 28. PMID: 31353841; PMCID: PMC6773470.
10. Key NS, Khorana AA, Kuderer NM, Bohlke K, Lee AYY, Arcelus JI, Wong SL, Balaban EP, Flowers CR, Francis CW, Gates LE, Kakkar AK, Levine MN, Liebman HA, Tempero MA, Lyman GH, Falanga A. Venous Thromboembolism Prophylaxis and Treatment in Patients With Cancer: ASCO Clinical Practice Guideline Update. J Clin Oncol. 2020 Feb 10;38(5):496-520. doi: 10.1200/JCO.19.01461. Epub 2019 Aug 5. PMID: 31381464.
Další literatura u autorů a na www.casopisvnitrnilekarstvi.cz
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2022 Issue 4-
All articles in this issue
- Hlavní téma – Pneumologie
- Covid-19 a post‑ covid – Jekyll a Hyde moderní medicíny
- Antifibrotická terapie a její indikace u intersticiální plicní fibrózy
- Neo/adjuvantní imunoterapie v léčbě nemalobuněčného plicního karcinomu
- Prevencia a liečba venózneho tromboembolizmu spojeného s malignitou – interdisciplinárny konsenzus
- Akutní poškození ledvin vlivem antimikrobiální terapie
- Vývoj doporučení pro použití venofarmak v léčbě chronického žilního onemocnění – kde je jejich místo a kde jsou slabiny
- Kyselina acetylsalicylová v primární prevenci kardiovaskulárních onemocnění
- Zlepšili sme starostlivosť o pacientov s artériovou hypertenziou v roku 2021?
- Urapidil: neznámé / známé antihypertenzivum
- Hlavní teze směřování interny v příštích letech
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Vývoj doporučení pro použití venofarmak v léčbě chronického žilního onemocnění – kde je jejich místo a kde jsou slabiny
- Antifibrotická terapie a její indikace u intersticiální plicní fibrózy
- Urapidil: neznámé / známé antihypertenzivum
- Kyselina acetylsalicylová v primární prevenci kardiovaskulárních onemocnění
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

