-
Medical journals
- Career
Ovlivňuje doba od potíží do léčení průběh žilní trombózy dolních končetin?
Authors: Jiří Spáčil; Jaroslava Svobodová
Authors‘ workplace: Cévní ordinace Spamed, Praha
Published in: Vnitř Lék 2018; 64(10): 911-915
Category: Original Contributions
Overview
Úvod:
Není známo, po kolika dnech od začátku potíží je u nás zahájená antikoagulační léčba žilní trombózy (ŽT) dolních končetin a zda tato doba má vliv na průběh onemocnění.
Metodika:
Z pacientů, kteří byli u nás v posledních letech léčeni pro trombózu hlubokých žil na dolních končetinách, jsme vybrali 50 pacientů, u kterých byly známé požadované údaje. Diagnóza byla vždy potvrzena duplexní ultrasonografií. Průměrný věk pacientů byl 51 let, z nich bylo 31 mužů a 19 žen. Proximální ŽT byla diagnostikována u 72 % pacientů. Idiopatickou ŽT mělo 38 % pacientů. Nemocní byli sledováni 3–6 měsíců.
Výsledky:
Doba do zahájení léčby ŽT byla v průměru 10 dní, rozmezí 1–42 dny, medián 7 dní. Dvě třetiny pacientů bylo léčeno novými perorálními antikoagulačními léky. Reziduální ŽT (neúplná rekanalizace) byla přítomna po 1–2 měsících léčby u 40,9 % pacientů, po 3–6 měsících u 25 % pacientů. Byl významný pozitivní vztah mezi dobou do zahájení léčby a reziduální ŽT po 1–2 měsících léčení (p < 0,05) a reziduální ŽT po 3–6 měsících léčení (p < 0,01).
Závěr:
Doba do zahájení léčby ŽT je u nás zřetelně delší než v jiných zemích. Později zahájená léčba snižuje úspěšnost léčby posuzované zvýšeným rizikem reziduální trombózy v postižených žilách v následujících měsících.
Klíčová slova:
reziduální žilní trombóza – zpoždění v diagnóze žilní trombózy – žilní trombóza
Úvod
Všeobecně se soudí, že čím dříve začne léčba, tím příznivější je průběh onemocnění. Přesné údaje máme u ischemických příhod. Revaskularizace během několika málo hodin od začátku potíží zabrání vzniku infarktu myokardu, mozkové příhodě nebo gangréně končetiny nebo alespoň podstatně zmenší jejich rozsah. U většiny nemocí se léčba zahajuje až po několika dnech, týdnech nebo i měsících trvání potíží nebo zjištění patologického nálezu. U nemocných s primárním lymfedémem se léčba zahajuje dokonce až po několika letech.
Žilní trombóza (ŽT) ohrožuje nemocné na počátku onemocnění plicní embolií, která může být smrtelná. V dalším průběhu je pacient ohrožen recidivou žilní trombózy a vznikem chronické žilní insuficience. Předpokládá se, že včasná antikoagulační léčba tomu může snížit riziko těchto komplikací. Přesných údajů je však málo. V minulých desetiletích bylo prokázáno, že pokud dosáhneme po zahájení léčby účinnou koncentraci heparinu co nejdříve, sníží se riziko recidivy žilní trombózy [1,2]. Po zavedení nízkomolekulárních heparinů a nových antikoagulačních léků, jejichž efekt nastupuje rychle, tato starost odpadla. V některých lékových studiích je uvedena doba od začátku potíží do zařazení do studie. Ve studii Schulmana et al 2009 s dabigatranem byl medián 3 dny [3], ve studiích Bauersachse et al 2010 s rivaraxobanem a Agnelliho et al 2013 s apixabanem 5 dní [4,5]. Studie ukázaly, že tyto léky nejsou horší než tradiční léčba heparinem a následným warfarinem, posuzováno podle počtu recidiv trombóz, avšak jsou bezpečnější. Jen málo studií se zabývalo zpožděním při diagnostice a léčbě ŽT. Ve studii Elliota, Goldhabera et al 2005 [6] bylo zjištěno, že u 21 % pacientů (z 808) byla stanovena diagnóza ŽT později než 7 dnů od začátku potíží a u 5 % až po 3 týdnech. 80 % zpoždění je způsobeno pacienty. V italské studii Agena et al 2008 [7] s 1 505 pacienty s ŽT diagnóza byla stanovena až po 10 dnech u 22,6 %. Včasnější diagnóza byla stanovena, pokud měli nemocní více potíží, při bolesti a při recidivě ŽT. Ve studii z Iránu, Rahimi et al 2013, [8] byla léčba zahajovaná v průměru po 4,7 dne, a diagnóza potvrzena v průměru po 6,29 dne. V těchto studiích nebyl popsán vztah doby před léčením ŽT k průběhu choroby. Holandská studie Ticka et al 2008, která sledovala riziko recidivy ŽT u 1 668 nemocných s ŽT [9] uvádí dobu mezi vznikem potíží a diagnózou 4 dny (medián). Pacienti, u kterých byla léčba zahájena později než 2 týdny od začátku potíží ŽT, měli riziko recidivy ŽT zvýšené o 40 %, respektive o 20 % po adjustaci (podle věku, pohlaví, rizikových faktorů) oproti pacientům, u kterých byla zahájena léčba do 2 týdnů.
Není nám známo, za kolik dní je u nás zahajovaná léčba ŽT dolních končetin po začátku potíží. Klinická zkušenost ukazuje, při léčbě novými antikoagulanciem dochází rychle k zlepšení stavu i rekanalizaci. Proto jsme analyzovali malý soubor našich pacientů. Zabývali jsme se i tím, zda včas zahájená léčba vede k rychlejší a dokonalejší rekanalizaci postižených žil neboli rychlejšímu a většímu ústupu trombózy. Toto dosud, pokud je nám známo, nebylo publikováno.
Složení souboru pacientů a metodika
Z pacientů, léčených pro trombózu žil dolních končetin (DK) v naší cévní ordinaci v posledních letech, jsme vybrali 50 pacientů s první ŽT DK, u kterých bylo možno podle anamnézy anebo podle dokumentace určit počátek potíží, pro které vyhledali zdravotnické zařízení. Diagnóza byla vždy potvrzena duplexní ultrasonografií s barevným kódováním toku krve. Při přítomnosti rizikových faktorů ŽT jsme onemocnění označili jako provokovanou (sekundární) ŽT. Dva nemocné jsme s podezřením na plicní embolii (později potvrzenou) jsme nechali hospitalizovat. U 22 pacientů byla zahájena antikoagulační léčba (jednou subkutání dávkou nízkomolekulárního heparinu a předpisem receptu na rivaroxaban). U 28 nemocných byla diagnóza potvrzena a léčba zahájen v nemocnici a obvykle po několika dnech byli pacienti předáni do ambulantní péče: 13 pacientů (26 %) bylo léčeno warfarinem, 4 nadroparinem (Fraxiparine® inj), 5 apixabanem (Eliquis®) a 28 rivaroxabanem (Xarelto®). Nemocní byli sledováni podle klinického stavu. Duplexní ultrasonografii žil DK jsme provedli při zjištění diagnózy nebo při převzetí pacienta do péče a dále dle stavu po 1–2 měsících a po 3–6 měsících. Při ultrasonografickém vyšetření jsme vyšetřovali společné stehenní žíly, stehenní žíly a podkolenní žíly. Při pozitivním nálezu proximální ŽT jsme nehodnotili žíly bérce. Při negativním nálezu v proximálních žilách jsme vyšetřovali a hodnotili bércové žíly. Podle popisů jsme dodatečně odhadovali rozsah obliterací. Úplná obliterace (při nestlačitelnosti žíly a nepřítomnosti krevního toku) odpovídá číslu 100, trombózu postihující polovinu lumina žíly jsme vyjádřili číslem 50, zcela volné lumen žíly číslem 0. Rozsah trombózy v jednotlivých žilách jsme sčítali. Například postižení podkolenní a stehenní žíly jsme vyjádřili maximálně číslem 200, trombózu dosahující do v. femoralis communis jsme vyjádřili jako maximální číslo 300. Uzávěr bércových žil jsme vyjádřili jako 100. Rekanalizaci, přesněji rozsah reziduální trombózy, jsme vyjadřovali obdobně, číslem 100 nebo většinou menším. Výsledek jsme vztahovali k původnímu nálezu a vyjadřovali v procentech rozsahu žilní trombózy na počátku onemocnění. Retrospektivní hodnocení rozsahu žilní trombózy neumožnilo přesnější hodnocení rozsahu ŽT v různých segmentech hlubokých žil DK.
Výsledky
Složení souboru a výsledky jsou uvedeny v tab. 1. V souboru převažují muži a pacienti se sekundární trombózou. Nemocní s proximální žilní trombózou jsou starší než nemocní s trombózou bércových žil. Doba od začátku potíží do potvrzení diagnózy a zahájení léčby byl v průměru 10,2 dny, medián 7 dnů. U 24 % byla léčba zahájena až po 14 dnech!
Table 1. Složení souboru 50 nemocných s první žilní trombózou na dolních končetinách a výsledky 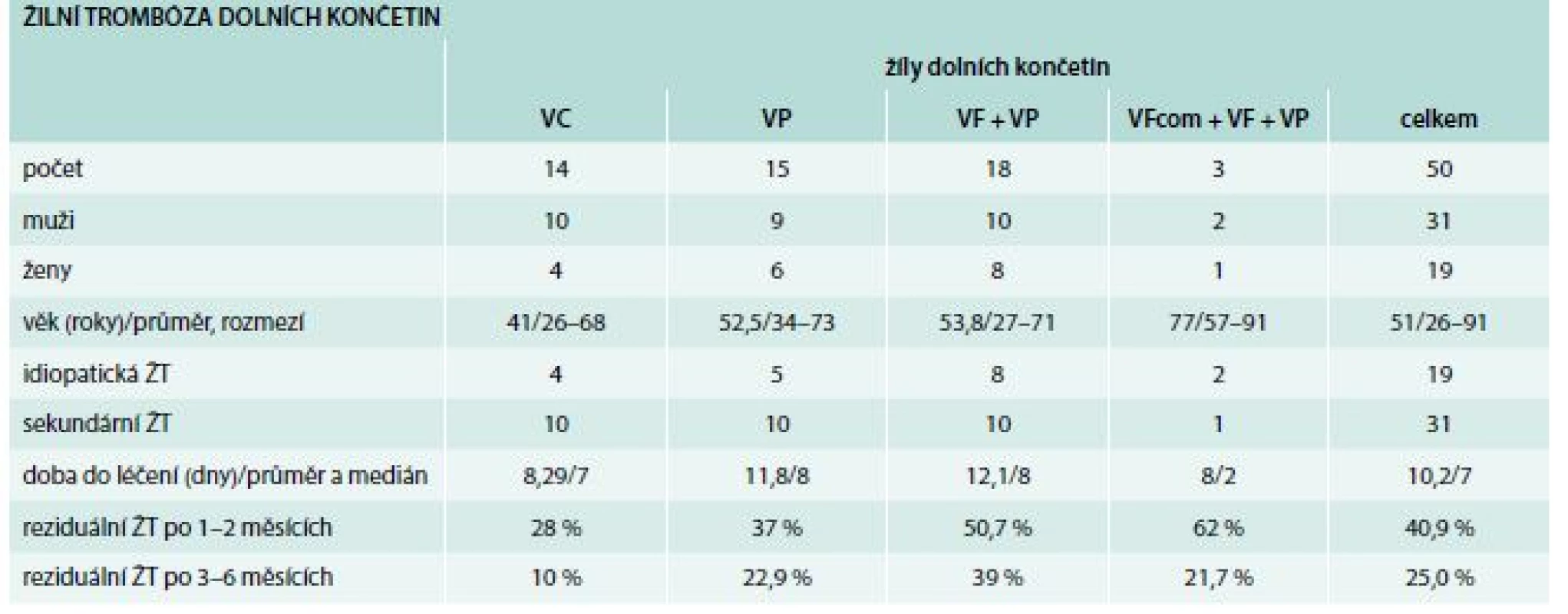
VC – venae crurales VF – vena femoralis VFcom – vena femoralis communis VP – vena poplitea ŽT – žilní trombóza Všichni nemocní byli ihned léčeni po potvrzení diagnózy ŽT. Neměli jsme nemocné s podezřením na ŽT, kteří by byli léčeni antikoagulancii před potvrzením diagnózy. Warfarinem bylo léčeno 26 % pacientů. Během sledování v naší ordinaci potíže většinou rychle ustupovaly. Nepozorovali jsme klinické známky plicní embolie ani progresi či recidivu ŽT. Také jsme nepozorovali žádné krvácivé komplikace.
Vztahy mezi základními ukazateli ukazuje tab. 2. Čím jsou pacienti starší, tím je pravděpodobnější větší rozsah ŽT a větší reziduální ŽT (neúplná rekanalizace) a častější idiopatická ŽT. Čím jsou pacienti léčeni později od začátku potíží, tím je rozsáhlejší reziduální ŽT, není však větší rozsah ŽT. Idiopatická (neprovokovaná) ŽT je častější u starších osob a u nich je větší rozsah reziduální ŽT po 3–6 měsících léčby. Rozsáhlejší ŽT má podle očekávání rozsáhlejší trombotické změny po 1–2 měsících léčby i po 3–6 měsících. Neprokázali jsme vliv pohlaví na sledované parametry.
Table 2. Vztah mezi vybranými ukazateli žilní trombózy. Spermanovské korelace (neparametrické) 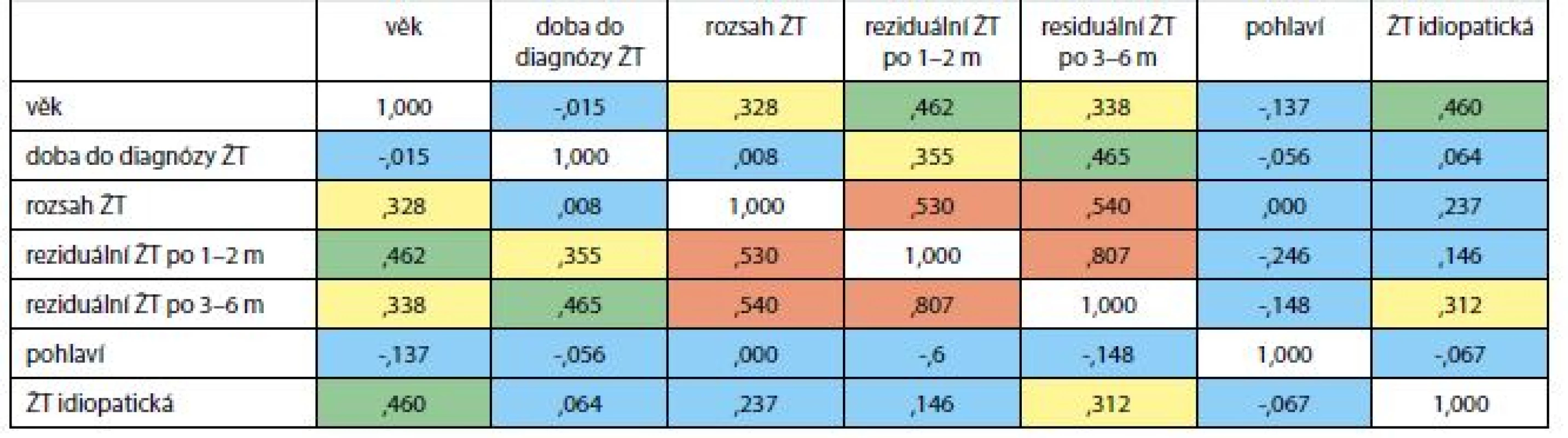
m – měsíc ŽT – žilní trombóza červená barva: korelace je významná (p < 0,001) modrá barva: korelace není významná. zelená barva: korelace je významná (p < 0,01) žlutá barva: korelace je významná (p < 0,05) Graf 1 ukazuje významný vztah mezi dobou do léčení a reziduální ŽT po 1–2 měsících léčení a graf 2 pak významný vztah mezi dobou do léčení ŽT a reziduální ŽT po 3–6 měsících léčení.
Graph 1. Vztah mezi dobou do léčení žilní trombózy (ŽT) a reziduální žilní trombózou po 1–2 měsících léčení: R = 0,355, p < 0,05 
Graph 2. Vztah mezi dobou do léčení žilní trombózy (ŽT) a reziduální žilní trombózou po 3–6 měsících léčení. R = 0,465, p < 0,01 
Diskuse
Výsledky různých prací, zabývající se ŽT, se obtížně srovnávají, protože složení souborů podle věku, pohlaví, rozsahu ŽT, podílu idiopatických ŽT, léčby, délky sledování a ultrasonografického hodnocení a dalších parametrů se velmi liší. Ve velkých lékových studiích [3–5] byli pacienti s proximálními ŽT průměrného věku asi 57 let, muži tvořili 58 % a idiopatická, neprovokovaná ŽT byla u 60–90 % pacientů. Lehce odlišné složení našeho souboru lze vysvětlit tím, v našem soboru bylo 28 % pacientů s ŽT bércových žil, kteří byli mladší a muži zřetelně převládali. Nemocní s idiopatickou (neprovokovanou) ŽT tvořili 38 %. Uvádí se, že tito nemocní tvoří 25–50 % [10].
Doba do zahájení léčby ŽT byla u nás v průměru 10,2 dny, medián 7 dní, přitom celých 24 % pacientů bylo léčeno až po 14 dnech! V literatuře se uvádí v případě ekonomicky vyspělých zemích doba kratší, medián 3–5 dní [3–5,9]. I v Iránu byla léčba zahajována v průměru po 4,7 dnech [8]. V severní Americe je 21 % pacientů léčeno až po 1 týdnu od vzniku potíží a na zpoždění se podílejí z 80 % pacienti [6]. V Itálii je diagnóza ŽT stanovena déle než 10 dní od začátku potíží u 22,6 % [7]. Práce týkající se žilní trombózy DK v České republice dobu do zahájení léčby neuvádějí [11–13]. Z klinické zkušenosti se zdá, že je i velká prodleva mezi první návštěvou lékaře a potvrzením diagnózy. Nedokážeme posoudit, zda je situace v jiných angiologických ordinacích lepší nebo horší. Nikdo však asi nebude pochybovat, že je třeba situaci zlepšit.
Je známo, že i při řádné léčbě nedochází vždy k úplné rekanalizaci žil. Z přehledné práce Carriera et al 2011 [14] vyplývá, že reziduální ŽT po 3–6měsících se vyskytuje u 10–80 % nemocných. Složení souborů se liší, je různý podíl distální a proximální ŽT i podíl idiopatické (neprovokované) a sekundární (provokované) ŽT a není jednotný způsob hodnocení ultrasonografických nálezů. Průměrně se reziduální ŽT vyskytuje u sekundárních (provokovaných) trombóz u 30,6 % a u 48 % u idiopatických ŽT. Přibližně 80 % pacientů mělo proximální ŽT. Podle dalšího přehledu Stephensona et al 2015 se reziduální žilní obstrukce po 3 měsíční léčbě ŽT vyskytuje u 38–80 % pacientů [15]. Naše výsledky nálezu reziduálních trombóz po 1–2 měsících u 40,9 % pacientů a po 3–6měsících u 25 % pacientů patří k lepším výsledkům. Nedostatkem naší studie je, že je malá a retrospektivní a ultrasonografické nálezy byly kvantifikovány dodatečně podle popisů. Naše studie tedy nedovoluje definitivní závěry. V našem souboru bylo 56 % pacientů léčeno novými perorálními antikoagulancii (NOAC – New Oral AntiCoagulants, v současnosti označované i jako Non-vitamin K Oral AntiCoagulants, případně DOAC – přímá perorální antikoagulancia/Direct Oral AntiCoagulants). Velmi podobné výsledky uvádí Prandoni et al 2017 [16] na souboru 352 pacientů, z nichž 41 % bylo léčeno NOAC. Reziduální trombóza byla zjištěna po 3 měsících u 41,2 % těchto pacientů a po 6 měsících u 21 %. U pacientů léčených warfarinem byly výsledky horší, reziduální ŽT byla zjištěna u 52 % a 54 %. Reziduální žilní trombóza se studuje se zaměřením na riziko recidivy ŽT i možnost řídit podle toho ukončení antikoagulační léčby. Předpokládáme, a uvádí to i literatura, že přítomnost reziduální žilní trombózy v době ukončení antikoagulační léčby zvyšuje riziko recidivy žilní trombózy [17]. Prandoni et al 2015 [18] uvádí zvýšení rizika na dvojnásobek. Jiní uvádějí kupodivu jen mírně zvýšené riziko nebo jen u některých skupin nemocných, případně že riziko není zvýšené [19]. Na základě výsledků naší studie se k tomuto nemůžeme vyjádřit.
Je překvapivé, že se velmi málo studuje vliv doby do zahájení léčby ŽT na její průběh. Nelze vyloučit, že tato možná závislost byla někým sledována, ale s negativními výsledky, které proto nebyly publikovány. Jak bylo uvedeno v úvodu, jen holandská práce Ticka et al 2008 [9] ukázala, že později zahájená léčba vedla k většímu riziku recidivy ŽT. My jsme prokázali volný, avšak statisticky významný vztah mezi dobou do zahájení léčby a nálezem reziduální ŽT. Je to možné tím, že v našem souboru byla doba do zahájení léčby ŽT delší než v jiných souborech. Při pozdějším zahájení léčby zůstává v postižených žilách více trombotických a fibrotických hmot po 1–2 měsících léčby i po 3–6 měsících léčby. Nebylo-li při pozdějším zahájení léčby, je rekanalizace méně úspěšná. Podle uvedených prací to zvyšuje riziko recidivy ŽT a rozvoj chronické žilní insuficience, alespoň u některých skupin pacientů. Z našeho malého souboru se nelze vyjádřit k tomu, zda včasná léčba ŽT snižuje výskyt a závažnost plicní embolie.
Pacienti, lékaři i organizátoři zdravotnictví oprávněně věnují velkou pozornost nejnovějším léčebným postupům jako je protonová nebo biologická léčba. Stejně důležité, nebo možná i důležitější je zabývat se dostupností moderní odborné péče.
Závěr
Z naší malé studie vyplývá, že léčba žilní trombózy je u nás zahajována zřetelně později než v jiných zemích. Při pozdějším zahájení léčby je rekanalizace méně dokonalá.
Za statistické zpracování dat děkujeme panu Mgr. Martinu Komarcovi z Ústavu biofyziky a informatiky 1. LF UK, Praha.
MUDr. Jiří Spáčil, CSc.
Cévní ordinace Spamed Praha
Doručeno do redakce 23. 1. 2018
Přijato po recenzi 25. 4. 2018
Sources
- Hull RD, Raskob GE, Brant RF et al. Relation between the time to achieve the Loir limit of the APTT therapeutic range and recurrent venous thromboembolism during heparin treatment for deep vein thrombosis. Arch Intern Med 1997; 157(22): 2562–2568.
- Anand SS, Bates S, Ginsberg JS et al. Recurrent venous thrombosis and heparin therapy: an evaluation of the importance of early activated parcel thromboplastin times. Arch Intern Med 1999; 159(1): 2029–2032.
- Schulman S, Kearon C, Kakkar AK et al. Dabigatran versus Warfarin in the Treatment of Acute Venous Thromboembolism. N Engl J Med 2009; 361(24): 2342–2352. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa0906598>.
- Bauersachs R, Berkowitz SD, Brenner B et al. Oral Rivaroxaban for symptomatic venous thromboembolism. N Engl J Med 2010; 363(26): 2499–2510. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1007903>.
- Agnelli G, Buller HR, Cohen A et al. Oral Apixaban for the treatment of Acute Venous Thromboembolism. N Engl J Med 2013; 369(9): 799–808. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1302507>.
- Elliot CG, Goldhaber SZ, Jensen RL. Delays in diagnosis of deep vein thrombosis and pulmonary embolism. Chest 2005; 128(5): 3372–3376. Dostupné z DOI: <http://dx.doi.org/10.1378/chest.128.5.3372>.
- Ageno W, Agnelli G, Imberti D et al. Factors associated with the timing of diagnosis of venous thromboembolis: results from MASTER registry. Thromb Res 2008; 121(6): 751–756. Dostupné z DOI: <http://dx.doi.org/10.1016/j.thromres.2007.08.009>.
- Rahimi-Rad MH, Rahimi-Rad S, Zarrin S. Delays in diagnosis and treatment of venous thromboembolism in a developing country petting. Tuberk Toraks 2013; 61(2): 96–102.
- Tick W, Kramer MHH, Rosendaal FR et al. Risk factors for post-thrombotic syndrome in patients with a first deep venous thrombosis. J Throm Haemost 2008; 6(12): 2075–2081. Dostupné z DOI: <http://dx.doi.org/10.1111/j.1538–7836.2008.03180.x>.
- Rajagopalan S, Dean SM, Mohler ER et al. Manual of Vascular Diseases. 2nd ed. Wolters Kluwer: Philadelphia 2012 : 415–438. ISBN 978–1609134228.
- Musil D. [Regression of deep venous thrombosis]. Vnitř Lék 2000; 46(1): 16–18.
- Vítovec M, Golán L, Roztočil K et al. The development of persistent thrombotic masses in patients with deep venous thrombosis randomized to long-term anticoagulation treatment. VASA 2009; 38(3): 238–244. Dostupné z DOI: <https://doi.org/10.1024/0301–1526.38.3.238>.
- Hirmerová J, Seidlerova JM, Filipovský J. Risk factors for residual thrombotic occlusion after proximal deep vein thrombosis of the legs. Int Angiol 2010; 29(4): 317–322.
- Carrier M, Rodger MA, Wells PS et al. Residual vein obstruction to predict the risk of recurrent venous thromboembolism in patients with deep vein thrombosis: a systematic review and meta-analysis. J Thromb Haemost 2011; 9(6): 1119–1132. Dostupné z DOI: <http://dx.doi.org/10.1111/j.1538–7836.2011.04254.x>.
- Stephenson EJ, Liem TK. Duplex imaging of residual venous obstruction to guide duration of therapy for lower extremity deep venous thrombosis. J Vasc Surg Venous Lymphat Disord 2015; 3(3): 326–332. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jvsv.2014.08.003>.
- Prandoni P, Ageno W, Mumoli N et al. Recanalization rate in patients with proximal vein thrombosis treated with the direct oral anticoagulants. Thromb Res 2017; 153 : 97–100. Dostupné z DOI: <http://dx.doi.org/10.1016/j.thromres.2017.03.022>.
- Karetová D, Chochola M et al. Vaskulární medicina. Maxdorf-Jesenius: Praha 2017 : 285–296. ISBN 978–80–7345–536–1
- Prandoni P, Lensing AW, Prins MH et al. The impact of residual thrombosis on the long-term outcome of patients with deep venous thrombosis treated with conventional anticoagulation. Semin Thromb Hemost 2015; 41(2): 133–140. Dostupné z DOI: <http://dx.doi.org/10.1055/s-0035–1544161>.
- Le Gal G, Carrier M, Kovacs MJ et al. Residual vein obstruction as a predictor for recurrent thromboembolic events after a firs unprovoked episode: data from the REVERSE cohort study. J Thromb Haemost 2011; 9(6): 1126–1132. Dostupné z DOI: <http://dx.doi.org/10.1111/j.1538–7836.2011.04240.x>.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2018 Issue 10-
All articles in this issue
- Je funkčná dyspepsia skutočne tak častá?
- Ovlivňuje doba od potíží do léčení průběh žilní trombózy dolních končetin?
- Tranzientní elastografie – přínos v hodnocení vývoje jaterního onemocnění
- Některé příčiny špatné adherence k dlouhodobé terapii statiny a jejich řešení
- Angioedém indukovaný inhibitory enzymu konvertujícího angiotenzin: epidemiologie, patogeneze a léčba
- Obštrukčné spánkové apnoe a dyslipidémia
- CD38 cílená léčba u mnohočetného myelomu
- Steatóza slinivky břišní: klinický význam
- Léčba pravé polycytemie
- Weberova-Christianova choroba: kazuistika
- Mnohočetné postižení tenkého střeva neuroendokrinním tumorem: kazuistika a přehled literatury
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Steatóza slinivky břišní: klinický význam
- Léčba pravé polycytemie
- Weberova-Christianova choroba: kazuistika
- Angioedém indukovaný inhibitory enzymu konvertujícího angiotenzin: epidemiologie, patogeneze a léčba
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

