-
Medical journals
- Career
Ultrasonografické vyšetření hrudníku v rukou lékaře klinika
Authors: Vratislav Sedlák 1; Vladimír Koblížek 1; Rastislav Šimek 2
Authors‘ workplace: Plicní klinika LF UK a FN Hradec Králové 1; Plicní oddělení Krajské nemocnice Tomáše Bati, a. s., Zlín 2
Published in: Vnitř Lék 2017; 63(11): 900-907
Category: Reviews
Overview
Ultrasonografie (USG) hrudníku proniká do klinické medicíny v řadě podoborů vnitřního lékařství. Velký rozvoj zažívá v oblasti nemocí hrudníku, které řeší pneumologie a intenzivní péče. V přehledovém článku přinášíme klinickým lékařům seznámení se základními principy a nomenklaturou nálezů v USG hrudníku. Je zmíněna diferenciálně diagnostická role u akutních příčin dušnosti. Ultrazvuk hrudníku by se měl stát standardní klinickou dovedností lékařů se specializací na nemoci hrudníku, srdce a plic nejen v intenzivní péči.
Klíčová slova:
hrudní drenáž – hrudní punkce – pleurální výpotek – pneumotorax – ultrasonografie hrudníkuÚvod
Do každodenního života klinických lékařů pronikají moderní diagnostické postupy, které byly v minulosti doménou specializovaných oborů. Příkladem je ultrasonografická (USG) diagnostika, která je dnes standardní metodou v řadě oborů vnitřního lékařství. V tomto souhrnném článku přinášíme základní přehled terminologie USG obrazů hrudníku v pneumologii a v intenzivní péči, mimo echokardiografii.
Ultrasonografie do hrudní medicíny pronikla koncem 80. let 20. století, kdy práce z oblasti intenzivní medicíny prokázaly USG specifické artefakty pro plicní onemocnění. Klinický lékař má oproti radiologovi velkou výhodu, zná totiž pacientovu anamnézu, fyzikální nález a dokáže USG obraz interpretovat v kontextu těchto informací. USG také zvyšuje přesnost a bezpečnost diagnostických intervenčních procedur v oblasti hrudníku (pleurální punkce a drenáže, kanylace velkých cév). Nevýhodou USG vyšetření je závislost interpretace výsledků na zkušenosti vyšetřujícího lékaře. Je doporučeno absolvovat některý vzdělávací program (e-learning, odborné společnosti) a ideálně se učit od zkušenějšího kolegy. Osvojení USG v praxi je zpravidla velmi rychlé zejména při diagnostice pleurálního syndromu. Systém postgraduálního vzdělávání v ultrasonografii není pro obor pneumologie dosud stanoven.
Základy ultrasonografie
Ultrasonografie používá princip různého odrazu USG vln vysílaných z USG sondy od tkání s různou impedancí (konzistencí) a tedy různými akustickými vlastnostmi. USG je metoda velmi vhodná pro zobrazování měkkých tkání. Na rozhraní měkkých tkání a kostí nebo tkání obsahujících plyn (dýchací cesty, vzdušná plíce, zažívací trakt, podkožní emfyzém a plyn obsahující abscesy) dochází k intenzivnímu odrazu mechanického vlnění, které pak obvykle zcela znemožňuje zobrazení tkání za tímto rozhraním. USG nelze dobře použít v situacích, v nichž naráží na fyzikální limitace (např. těžká obezita, těžký edém měkkých tkání, podkožní emfyzém atd). USG přístroj by měl být především jednoduše ovladatelný, kompaktní, mobilní a uživatelsky příjemný, podmínkou pohodlného užívání je start přístroje do 30 s (delší start přístroje spolehlivě odradí lékaře od rutinního používání). Přístroj lze pořídit i s vozíkem, na který je možné odložit bezpečně sondy, gel, dezinfekci a papírové ručníky na otření pacienta. USG přístroj by měl mít možnost záznamu obrazové informace (tiskárna, harddisk, USB disk). Pro potřeby běžného klinického USG vyšetření hrudníku je výhodné použití menší sondy umožňující pohodlné vyšetření mezižeberního prostoru (tzv. mikrokonvexní sonda), ideálně s frekvenčním rozhraním asi 5–7 MHz, dopplerovské zobrazení není nutné. Při použití přístroje je nutné dbát na dezinfekci sondy před a po použití u pacienta, sonda může být vektorem nozokomiální nákazy.
Z ovladačů přístroje začátečník použije jen několik nastavení – zesílení (gain) a přiblížení (zoom), zamrznutí obrazu (freeze) a jako nástroje pro hodnocení vzdáleností či rozměrů používáme měřič vzdálenosti (caliper) a jeho ovladač (trackball), obr. 1 – označeno bílými šipkami. Není doporučeno využívat softwarové algoritmy k vyhlazení šumu obraz, protože mohou znesnadnit zobrazení artefaktů nemocné plicní tkáně.
Image 1. Ovladací panel USG přístroje. 
Obr. 1–17 jsou z archivu autorů. Zahajujeme vyšetření
Pro správné provedení USG je nutné pacienta uložit do správné polohy pohodlné jak pro něj, tak pro vyšetřujícího. Polohu pacienta zvolíme podle očekávané patologie (u mobilních vsedě). USG sondu je vhodné držet mezi prsty podobně jako pero, podélná osa sondy směřuje nejprve v kraniokaudálním směru, marker (indikátor směru) sondy směřuje apikálně (obr. 2).
Image 2. Svislé držení sondy USG 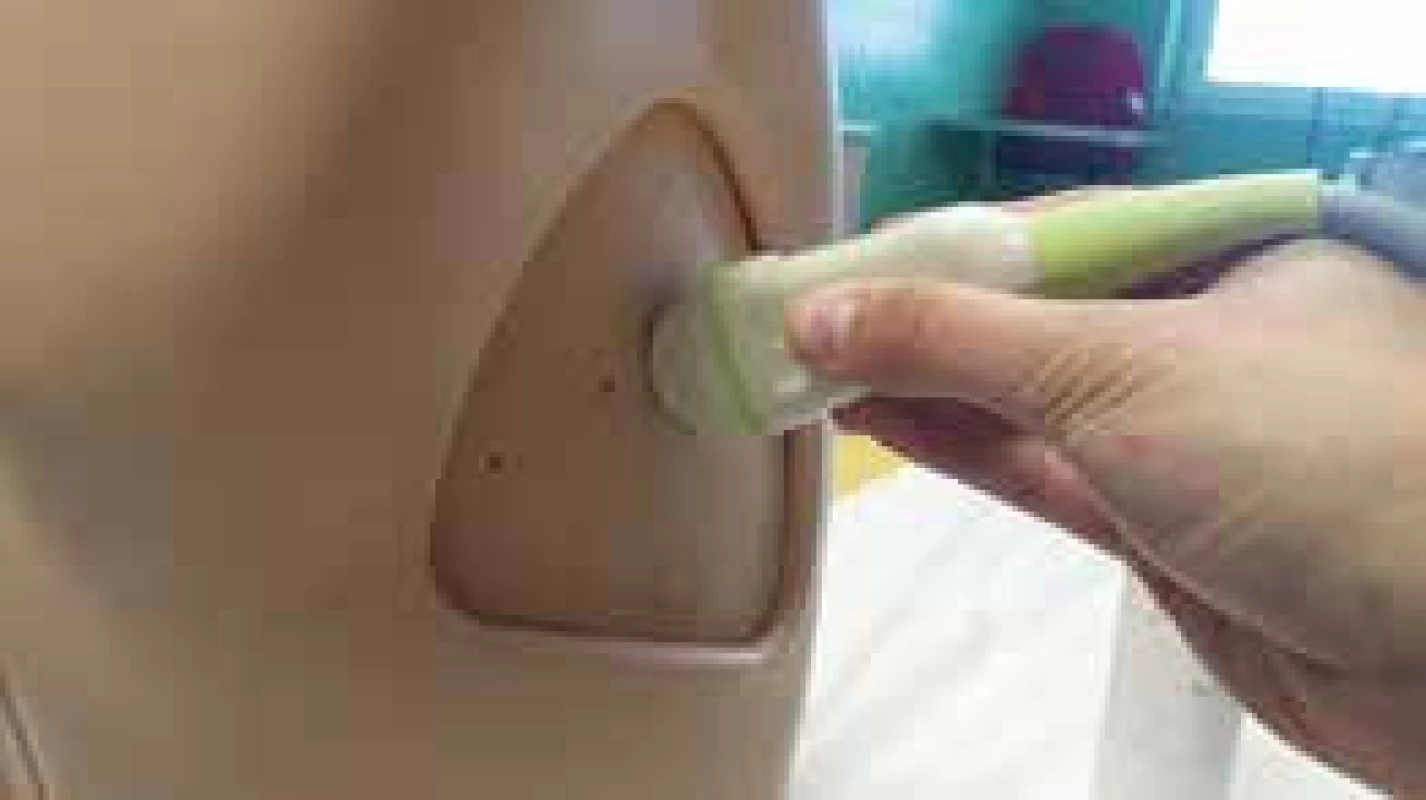
Indikátor směru sondy má korelát na obrazovce USG přístroje v levém horním rohu, tedy kraniální struktury jsou pak vlevo, kaudální struktury jsou vpravo. Vyšetřující tedy neustále kontroluje vztah USG obrazu k poloze sondy a jejího markeru. Většina patologických procesů plic, pohrudnice a srdce je v dosahu povrchového USG vyšetření. U sedícího pacienta nejprve identifikujeme subdiafragmatické struktury (slezinu a ledvinu vlevo, játra a ledvinu vpravo) a poté směrujeme sondu kraniálně. Vyšetření probíhá podobně jako při použití fonendoskopu, tj. porovnáváme nález na levé a pravé straně hrudníku v konkrétní lokalitě. Při nálezu abnormality sondou rotujeme o 90 a více stupňů tak, aby vymizely stíny žeber – získáme tak detailnější pohled na plicní parenchym a pleurální prostor. Rotací a výkyvem sondy dosáhneme zobrazení cílového orgánu ve více rovinách a můžeme si udělat prostorovou představu o cílovém orgánu či patologickém procesu. Důležité je nanesení dostatečné vrstvy gelu na sondu a vyvinutí takového tlaku sondy, aby byl ještě snesitelný pro pacienta a současně vznikal dostatečně kvalitní obraz. Druhou rukou vyšetřující ovládá panel USG s ovladači. Pokud přerušujeme kontakt sondy s pacientem, je vhodné zamrazit obraz (freeze), šetříme tak životnost sondy.
Echogenita nálezů
Pro popis intenzity odrazu USG vln od tkání používáme termín echogenita. USG obraz je generován v odstínech šedé barvy. Nejsilnější odraz USG vln je zobrazen jako velmi světlý odstín šedi až téměř bílá barva, naopak v případě nulového odrazu USG vln od orgánů je výsledný obraz velmi tmavě šedý až černý.
K porovnání echogenity lze použít jaterní parenchym (obr. 3), který u zdravého člověka lze označit za izoechogenní.
Image 3. Izoechogenní jaterní parenchym s hypoechogenním výpotkem 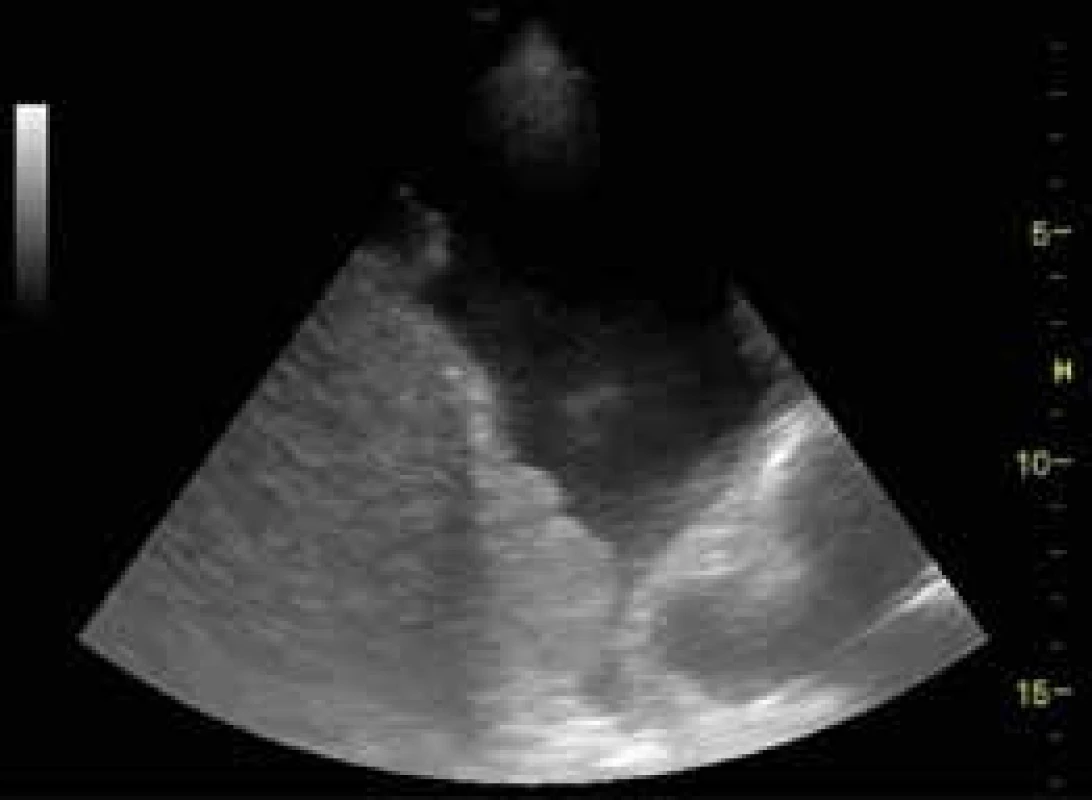
Sytější struktury než jaterní parenchym označujeme za hyperechogenní (empyém), naopak méně syté struktury za hypoechogenní (výpotek charakteru transsudátu). USG některými strukturami volně prostupuje (játra, slezina, tekutina) a umožňuje tak prohlédnutí hlubokých anatomických struktur – jde o obraz tzv. akustického okna. Naopak některá prostředí zcela absorbují USG vlny – vzniká tzv. USG akustický stín, např. za žebrem. Se změnou polohy dochází k přesunu vzduchu i tekutiny v hrudním prostoru, důležité je i posouzení změn USG obrazu při rotaci pacienta a změny obrazu při dýchání. USG obraz je složen také z artefaktů vznikajících lomem a odrazem USG vln na různých akustických rozhraních. I tyto artefakty jsou pro nás důležité.
Normální USG nález hrudníku
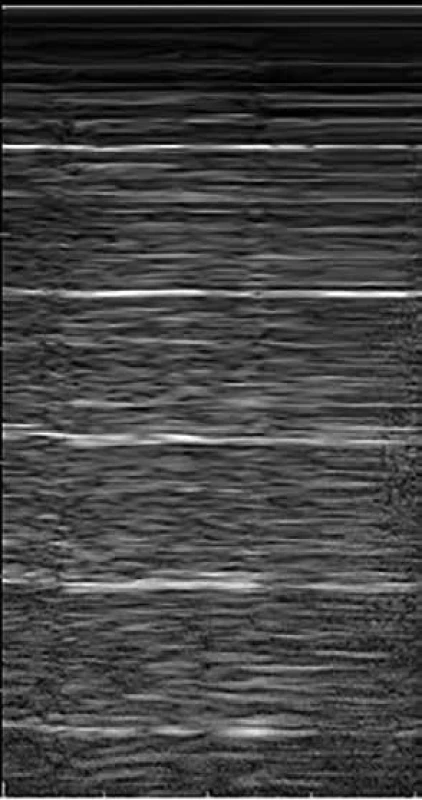
Při vyšetření hrudníku v sagitální rovině zobrazuje USG sonda akustický stín tvořený žebry a jen relativně malé části plicního parenchymu – tento obraz malé části viditelného plicního parenchymu mezi 2 akustickými stíny žeber je typický, anglická literatura jej zmiňuje jako tzv. bat-sign (obraz letícího netopýra), obr. 4.
Image 4. Normální nález USG plic – A-linie 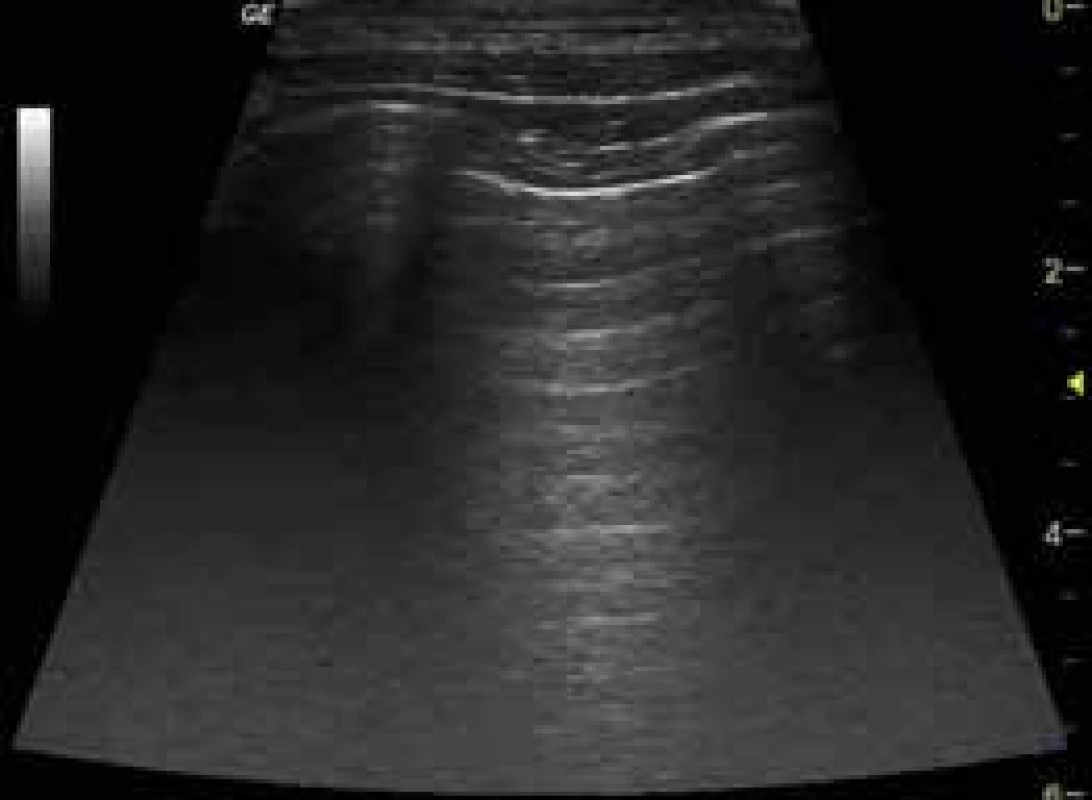
Viscerální a parietální pleura má na USG vzhled hyperechogenní nepřerušené linie do šíře 2 mm. Při dýchání dochází k pohybu plíce, která je v USG obraze popisována jako tzv. plicní klouzání. Přítomnost této známky má vysokou negativní prediktivní hodnotu pro pneumotorax, tedy chybění plicního klouzání může svědčit pro pneumotorax. U zdravé plíce tedy zobrazujeme v hypoechogenním parenchymu plicní tkáně reverbaci silného odrazu USG vln prostupujících hrudní stěnou k pleuře, v obrazu tedy vidíme zrcadlení ve formě několika horizontálních linií – tzv. A-linie a plicní klouzání (obr. 4). V dorzobazálních partiích plic je fyziologický výskyt 1–3 tzv. B-linií, jde o horizontální linie vycházející z pleurální linie a směřující radiálně distálně od sondy bez zeslabení (laser like), které se postupně vytrácejí. Jde o dynamický artefakt, který se pohybuje s dýcháním (obr. 5). Přítomnost četných B-linií svědčí pro náplň subpleurálních sept tekutinou nebo jiným patologickým obsahem v plicním intersticiu. Bránice má v USG obraze vzhled hyperechogenní linie silné 1–2 mm subpulmonálně, typický je souhyb s respirací, ideální zobrazení je přes echogenní okno jater či sleziny.
Image 5. B-linie u srdečního selhávání 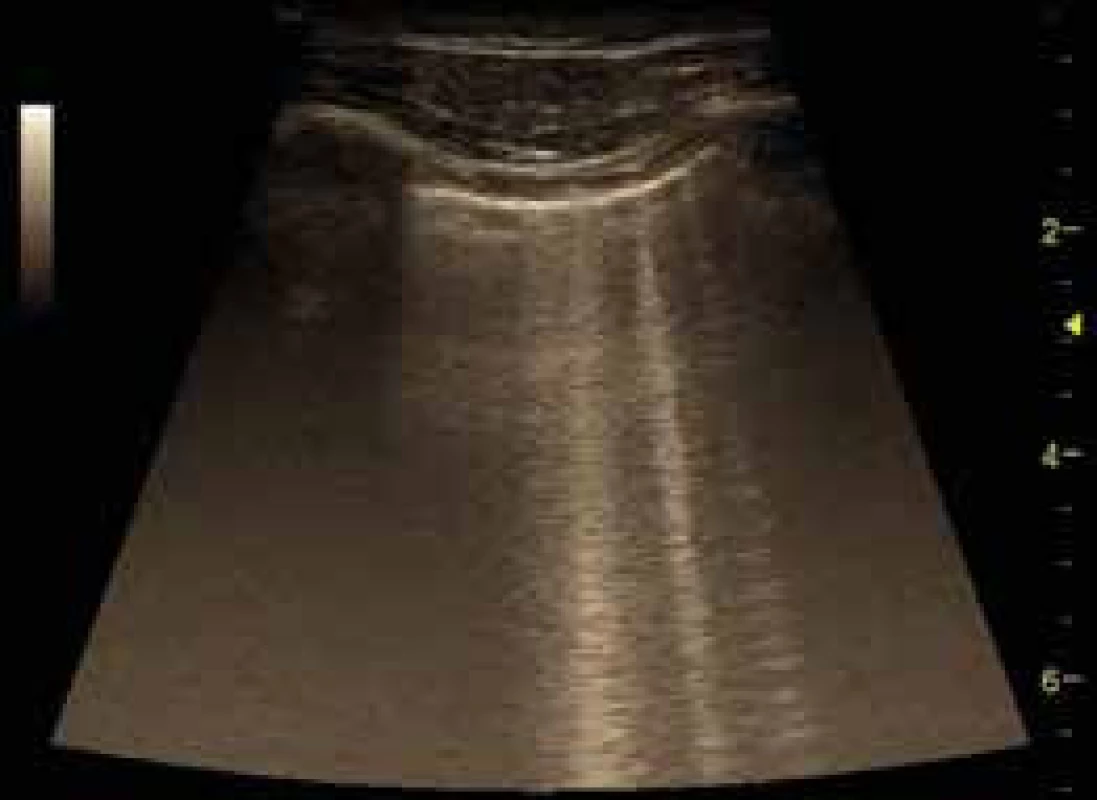
V oblasti hrudníku je možné také vyšetřit přiléhající uzliny a provést jejich biopsii jehlou pod přímou USG navigací. Maligní uzliny mívají splývavý charakter, nepravidelné okraje v případě extranodulárního růstu (obr. 6).
Image 6. USG obraz maligní uzliny 
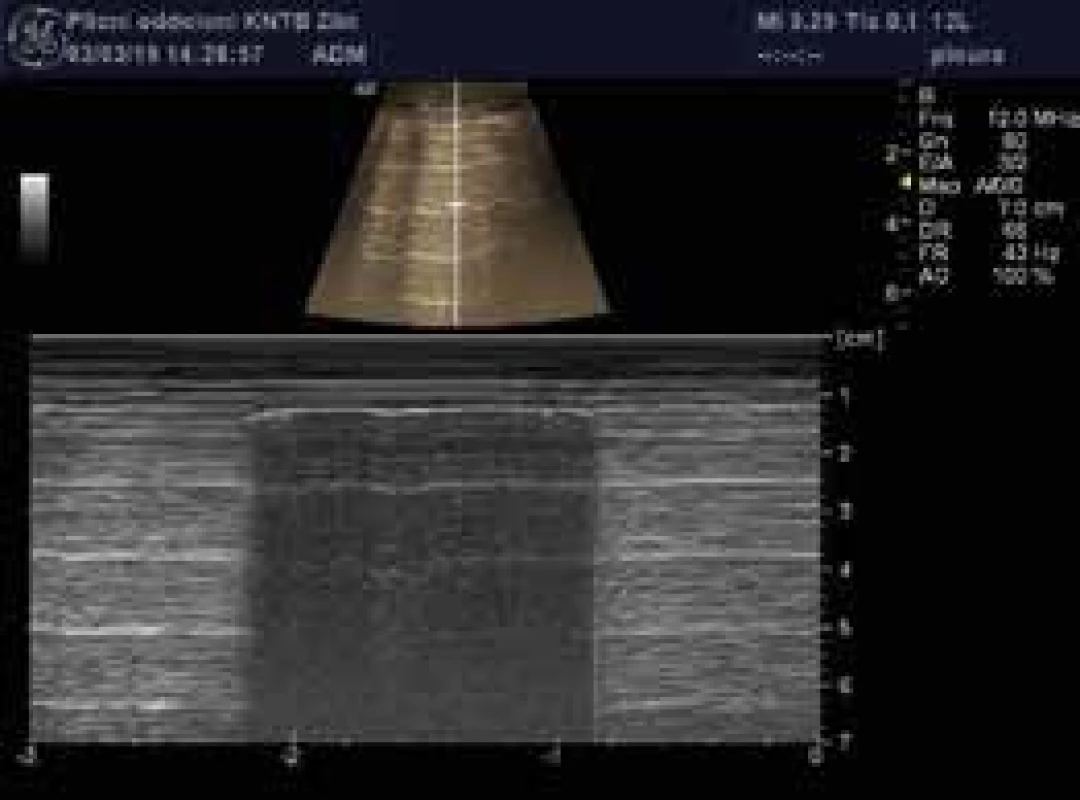
Patologie hrudní stěny
Patologii hrudní stěny je možné dobře posoudit pomocí sondy s frekvencí > 5 MHz. Většina oválných homogenně echogenních lézí v hrudní stěně bývá benigní etiologie (fibromy, lipomy atd), obr. 7. Na USG jsou dobře patrné zlomeniny žeber jako lomy v hyperechogenním obraze kortikalis žebra. Metastázy mají obraz setřelé struktury kosti s hypoechogenním nepravidelným postižením průběhu žebra.
Image 7. Komplexní septovaný výpotek 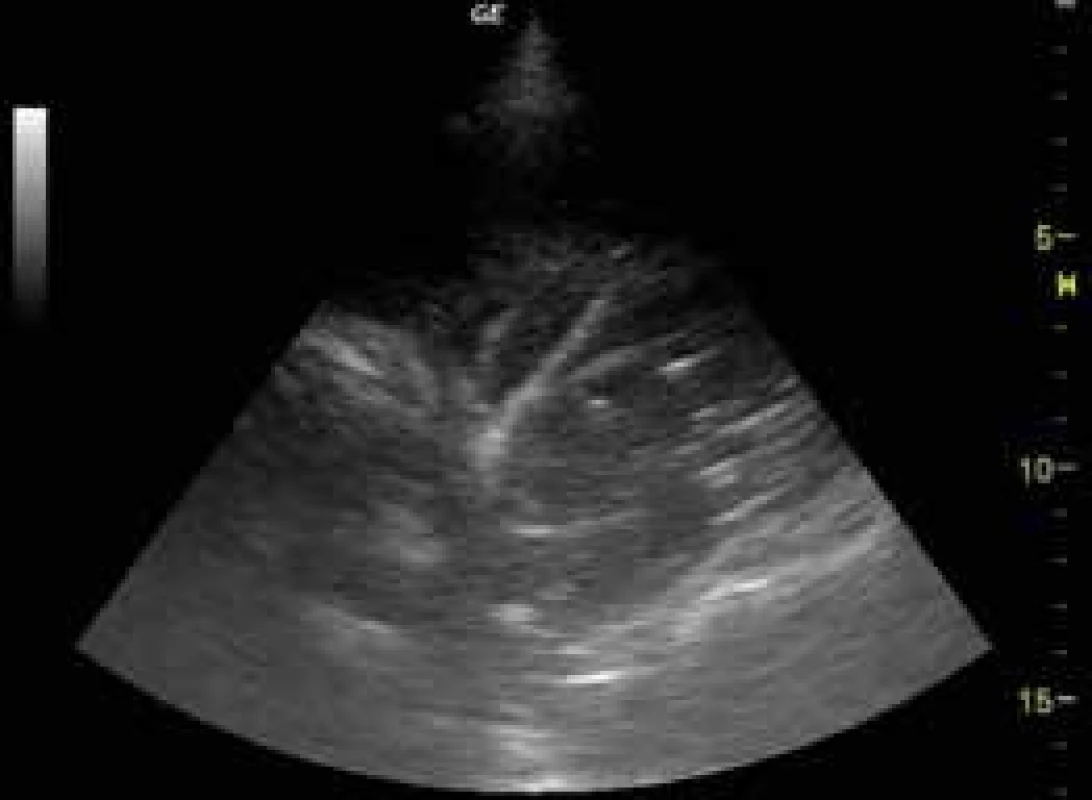
Pleurální výpotky
USG je ideálním nástrojem pro zhodnocení přítomnosti pleurálního výpotku, lze odhalit i stopové množství výpotku a také jeho charakter, objem a místo nejvhodnější k provedení pleurální punkce či drenáže, která je pod USG navigací bezpečněji proveditelná. Pleurální výpotek má typicky vzhled anechogenní či hypoechogenní kolekce roztlačující prostor mezi parietální a viscerální pleurou (obr. 3). Podle objemu a charakteru výpotku může být omezen pohyb plíce utlačené výpotkem, která může být i atelektatická (obr. 8).
Image 8. Atelektatická plíce se vzdušným bronchogramem 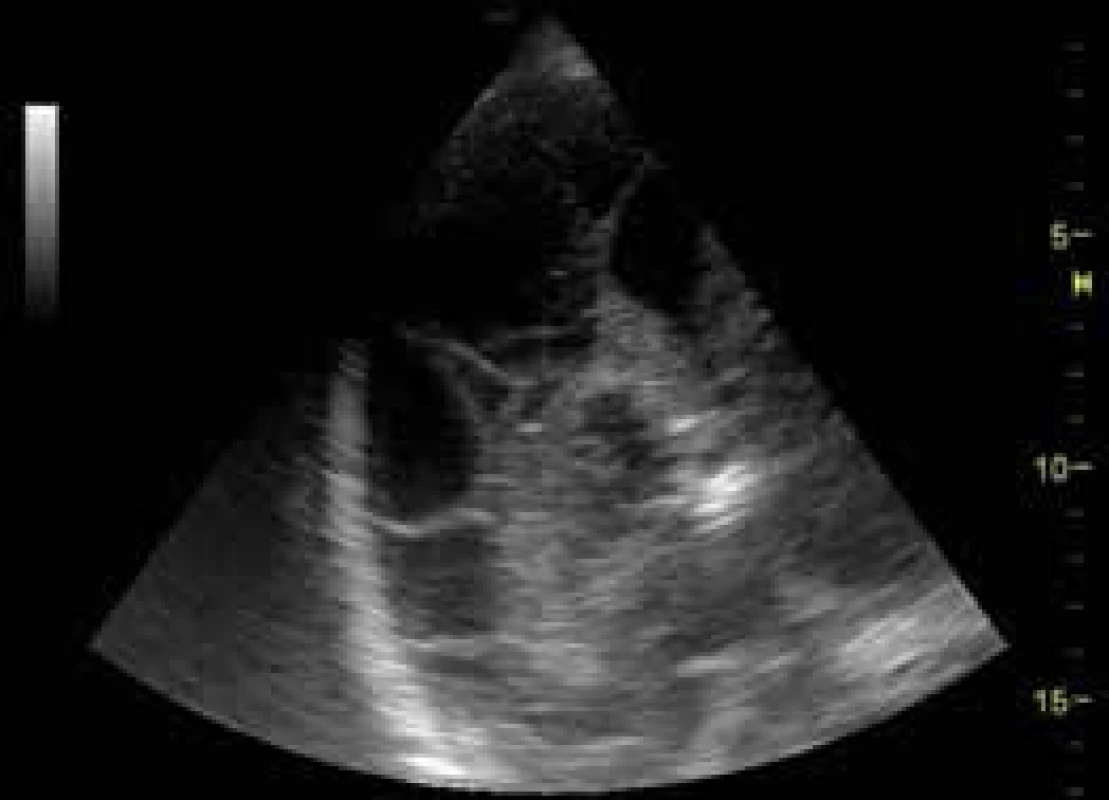
Rozlišujeme 4 základní druhy USG obrazu pleurálního výpotku – anechogenní výpotek (obr. 3), komplexní neseptovaný výpotek, komplexní septovaný výpotek (obr. 7), homogenně hyperechogení výpotek (obr. 9).
Image 9. Homogenně hyperechogenní empyém 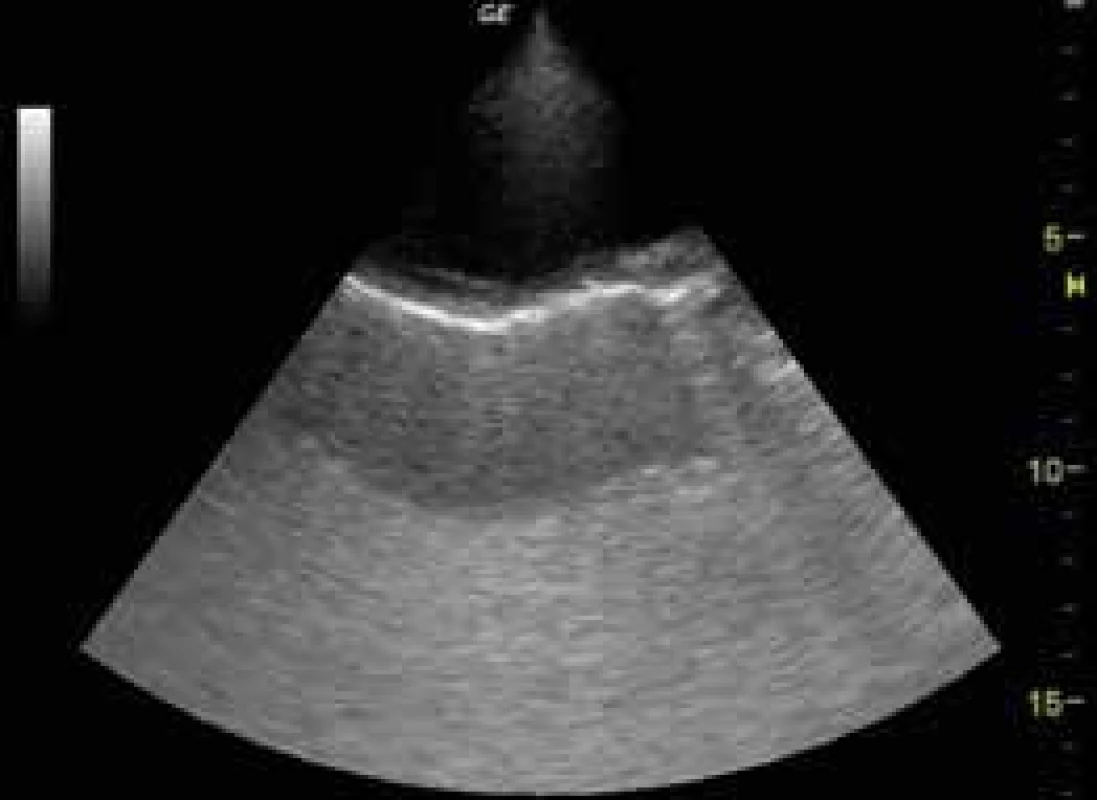
Anechogenní či hypoechogenní výpotky typicky odpovídají transsudátu, komplexní výpotky doprovázejí zánětlivé afekce pleury a plic, homogenně hyperechogenní výpotek nalézáme u empyému a hemotoraxu. Posouzení charakteru výpotku pomůže klinickému lékaři v rozhodnutí o dalším postupu. Např. hypoechogenní transsudáty u pacienta se srdečním selháváním obvykle nevyžadují pleurální punkci, protože dobře reagují na diuretickou léčbu. Přítomnost komplexního septovaného pleurálního výpotku je indikována primárně k hrudní drenáži a intrapleurální aplikaci fibrinolytika či chirurgické intervenci. Stejně tak hyperechogenní výpotek může svědčit pro empyém, anebo u pacienta po nedávné intervenci v oblasti hrudníku pro hemotorax. Objem výpotku je možné hodnotit různými způsoby, nejjednodušší je schéma dle Eibenbergera, podle nějž se u ležících pacientů interpleurální distance v mm výpotku násobí 20 a výsledek odpovídá objemu v ml. U separace listů pleury > 50 mm se vzdálenost násobí 30 a spolehlivost odhadu klesá.
Plicní patologie v USG obraze
Zdravá plicní tkáň je vzdušná a pro USG není viditelná. Zobrazujeme ji jako dominující A-linie s přítomným plicním klouzáním. Patologické procesy zejména v subpleurální oblasti plic mění absorpci a odraz USG vln a vytváří spektrum artefaktů, jejichž správnou interpretací můžeme dospět ke správné diagnóze nebo rozhodnutí o dalším postupu. Jako plicní konsolidace označujeme hypoechogenní formace subpleurálně umístěné s chybějícím odrazem pleury. Někdy mají přítomnou nehomogenně echogenní strukturu. USG obraz plicních konsolidací může být podmíněn celou řadou patologických změn (plicní tumor, plicní embolizace, pneumonie, atelektáza, absces). Odlišení jednotlivých příčin je pomocí USG možné, vyžaduje však hlubší znalosti a přesahuje rozsah tohoto přehledu. Plicní embolizace mívají klínovitý tvar a bývají uloženy nejčastěji dorzobazálně (obr. 10).
Image 10. Periferní plicní embolus – infarkt plic 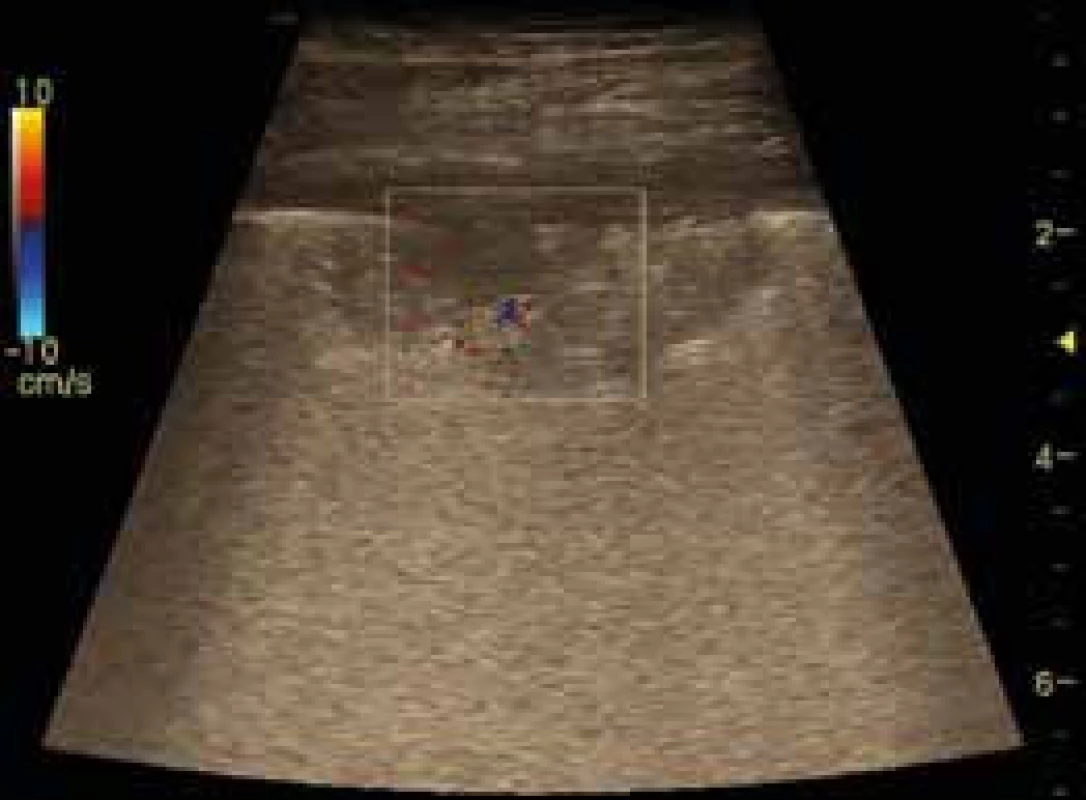
Plicní tumory mívají nepravidelný hypoechogenní tvar s akustickým zesílením zadní (distální) stěny léze, někdy je patrné vymizelé plicní klouzání a infiltrace hrudní stěny tumorem – zde má USG dokonce lepší diagnostickou výtěžnost než CT (obr. 11).
Image 11. Periferní plicní tumor 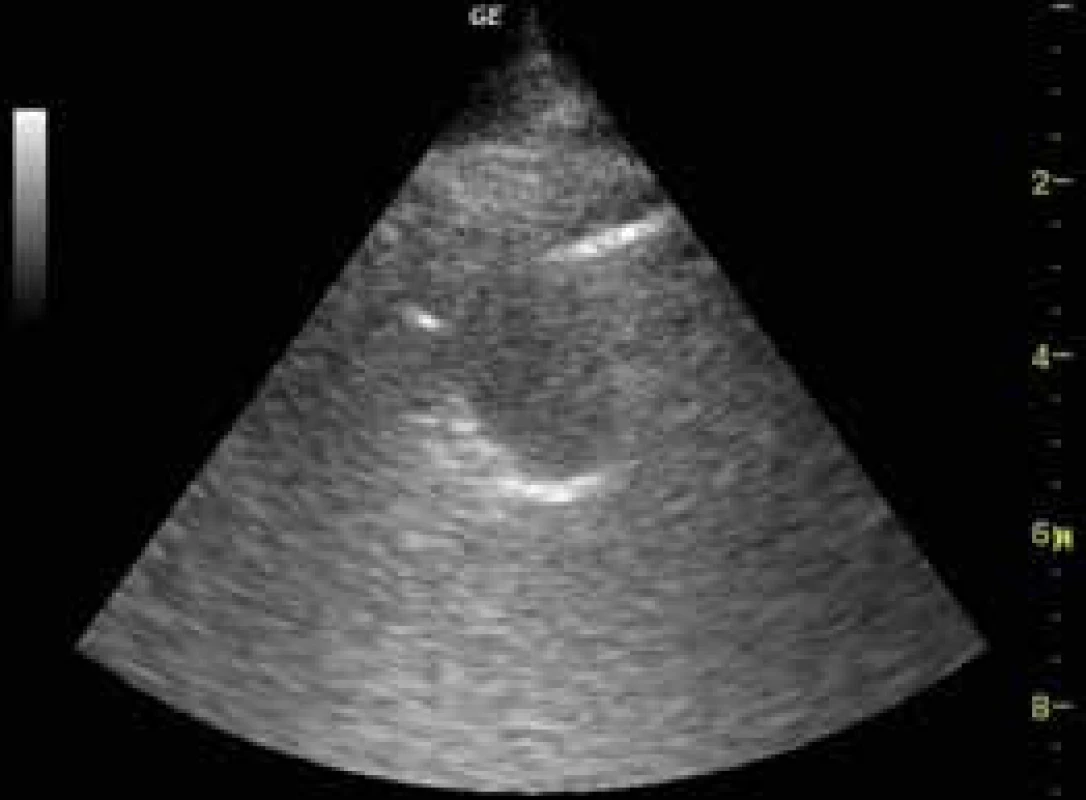
Kromě plicních konsolidací nalézáme velmi často obraz tzv. B-linií, jak je popsáno výše, u popisu normálního USG nálezu. B-linie vycházejí z pleury, vertikálně radiálně prostupují celým obrazem a jsou korelátem patologického obsahu plicního intersticia. Jejich velké množství (tzv. lung rockets) je typickým obrazem městnání tekutiny v plicním intersticiu např. u srdečního selhávání (obr. 5). U pacienta s akutní dušností lze tedy pomocí USG okamžitě rozpoznat, zda jde o srdeční selhání (bilaterálně četné jemné B-linie s plicním klouzáním, často s pleurálním výpotkem hypoechogenním) nebo o syndrom bronchiální obstrukce (typicky jen A-linie, bez pleurálního syndromu a s omezením plicního klouzání při hyperinflaci). Problém činí odlišení nálezu B-linií podmíněného retencí tekutiny v plicním intersticiu od fibrotických změn (ARDS, intersticiální plicní nemoci). V těchto případech bývají B-linie hrubšího charakteru a pleurální linie nebývá hladká, u ARDS bývá obraz B-linií nehomogenní, tedy v některých místech je méně výrazný, na rozdíl od plicního edému, u nějž jsou B-linie homogenně difuzně zobrazitelné.
Pneumotorax
Nejnáročnější technikou v USG hrudníku je pro klinického lékaře diagnostika pneumotoraxu. Pomocí USG jsme přitom schopni vyloučit pneumotorax až se 100% jistotou, což je důležité pro hodnocení ev. komplikací intervencí v oblasti hrudníku. Základem úspěchu je ovládnutí diagnostiky normálního USG obrazu, B-linií a plicního klouzání. Při pneumotoraxu buď plíce zkolabuje celá, pak ve srovnání se zdravou plící nevidíme nad postiženou stranou typické plicní klouzání, obraz A-linií je narušený, není patrný pohyb plíce při respiraci, což je zvláště patrné při změně USG obrazu do lineárního tzv. M-modu. Zdravá plíce se v M-modu zobrazuje jako měnící se obraz v místě pohybu plíce při dýchání vedle konstantního neměnného obrazu hrudní stěny připomínající vlny oplachující pláž (tzv. seashore sign – příznak mořského pobřeží), obr. 12.
Image 12. Příznak mořského pobřeží (seashore) – pohyb plíce v M-modu 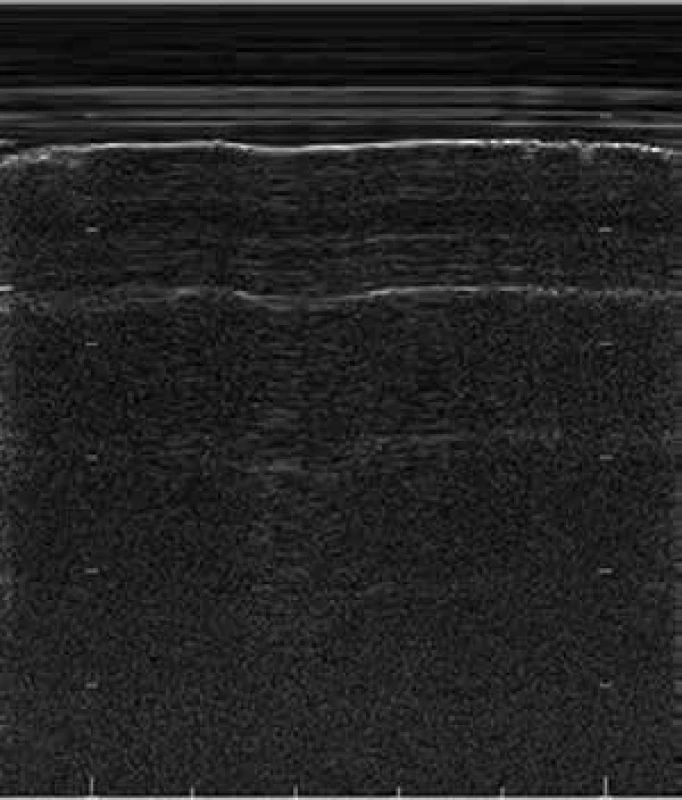
U pneumotoraxu je při respiraci neměnný obraz linií nehybné hrudní stěny i vzduchu v hrudním prostoru, který vytváří obraz podobný stratosférickým čarám nebo čárovému kódu na zboží (tzv. stratosphere nebo barcode sign), obr. 13.
Pokud došlo jen k parciálnímu kolapsu plíce, pak USG sondou můžeme nalézt místo, v němž je ještě patrný fyziologický pohyb vzdušné plíce s respirací a A-linie a současně v druhé polovině USG obrazovky vidíme tu část hrudníku, kde je plíce zkolabována od hrudní stěny. Toto místo se nazývá lung-point, tedy plicní bod, a jeho průkaz má vysokou specificitu pro pneumotorax (obr. 14). Současně nám pozice tohoto bodu sděluje informaci o rozsahu kolapsu plíce: čím dorzálněji je uložen, tím je pneumotorax významnější.
USG navigované hrudní punkce a drenáže, biopsie plic a hrudní stěny a kanylace velkých cév
Velké hrudní výpotky je možné punktovat jen s pomocí skiagramu hrudníku a fyzikálního vyšetření plic. V moderní medicíně hraje bezpečnost výkonu velmi významnou roli a použití USG při provádění pleurálních punkcí lze doporučit, protože zajišťuje větší komfort lékaře i pacienta a zvyšuje šanci na úspěšné a bezpečné provedení výkonu. S pomocí USG se lékař může rozhodnout, zda je indikována jen punkce či primárně hrudní drenáž pro komplexní charakter výpotku. Po výkonu pomocí USG ihned vyloučí komplikace (pneumotorax, hemotorax, krvácení do hrudní stěny). Při samotné USG navigaci je možné zvolit jak „handsfree“ postup, tj. zaměření vhodného místa k punkci v konkrétní poloze pacienta, poté lékař odloží sondu a samotnou punkci provede bez USG. U malých nebo lokulovaných výpotků je možné provést punkci pod přímou USG navigací a zobrazením pohybu jehly v reálném čase. Stejné postupy je možné aplikovat u hrudních drenáží.
Klinický lékař velmi rychle adoptuje USG do své každodenní praxe, jakmile získá základní zkušenosti s diagnostikou pleurálních syndromů a s USG navigovanými pleurálními punkcemi. S rostoucím počtem vyšetření pak roste klinická jistota a ochota lékaře používat USG v nových indikacích (biopsie periferních plicních tumorů, USG navigovaná kanylace velkých žil).
Biopsie pod USG navigací
Pomocí bioptické jehly je možné provádět bezpečné pleurální biopsie či biopsie subpleurálních plicních konsolidací, pokud naléhají na viscerální pleuru, případně prorůstají do hrudní stěny. Postup je bezpečný, provádí se pod přímou USG navigací v reálném čase, získaná aspirovaná cytologie je ihned zpracována natřením na sklo a tzv. ROSE (rapid-on-site cytology) okamžitým zhodnocením nálezu pod mikroskopem s možností ihned zopakovat biopsii u nevýtěžných vzorků. Pomocí tzv. bioptických děl je možné získat i velmi validní válečky tkání, ze kterých je možné odečíst histologii i imunohistochemii a genetické vyšetření vzorku (obr. 15). Výhodou USG je možnost okamžité kontroly hrudního prostoru po odběru vzorku s cílem vyloučit vznik komplikace (pneumotorax, krvácení). Výtěžnost USG navigovaných biopsií se pohybuje kolem 80–90 %.
Image 15. USG obraz bioptické jehly zavedené v uzlině 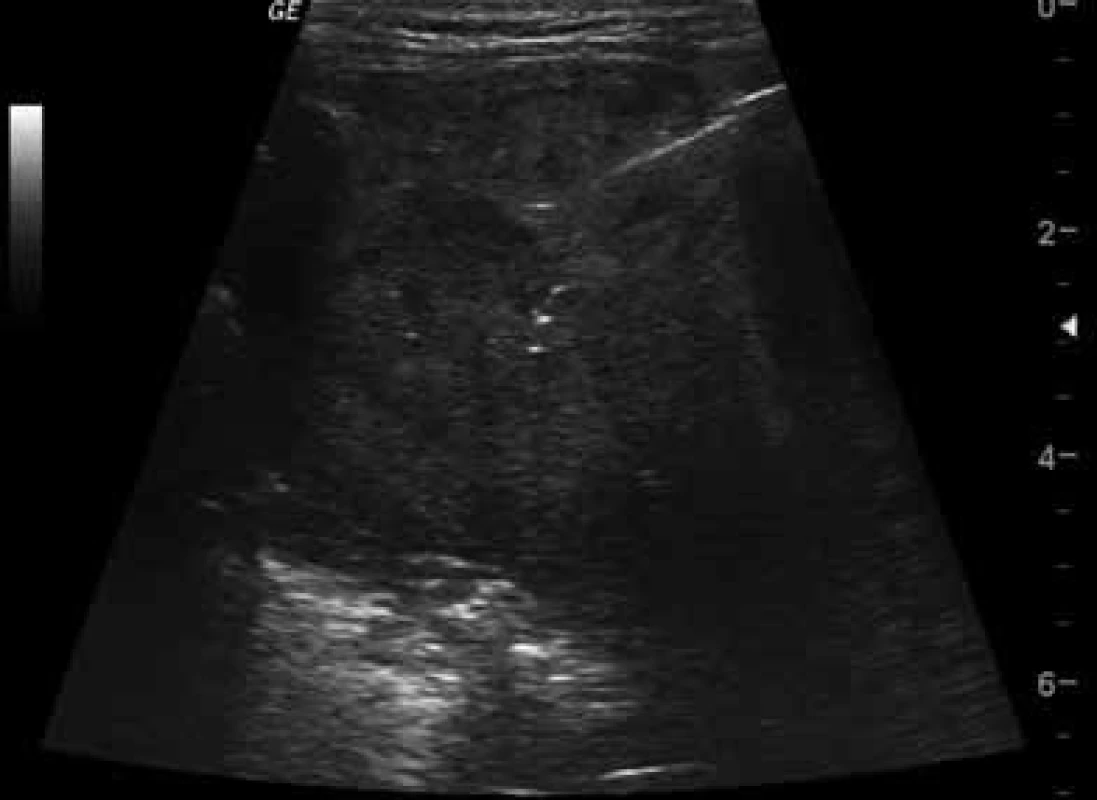
Kanylace velké žíly pod USG navigací
U pacientů v těžkém stavu a zejména s respirační insuficiencí podmíněnou těžkým strukturálním postižením plic je zavedení centrálního žilního katétru vždy riziková procedura. Pomocí USG lze zavést elegantně a bezpečně centrální žilní katétr do velkých kompresibilních žil na krku a v třísle. Kanylace v. jugularis (femoralis) se provádí pod přímou USG navigací. Lékař před dezinfekcí operačního pole zvolí pomocí USG nejvhodnější žilní přístup, samotná kanylace probíhá pod přímým zobrazením pohybu jehly v USG poli. Sonda je zakryta sterilním návlekem, do operačního pole je aplikován sterilní gel. Pohyb jehly v lumen žíly musí být po celou dobu zobrazen, po aspiraci krve lékař odloží sondu a dále dokončí kanylační manévr technikou dle Seldingera (zavedení vodiče, přetažení kanyly po vodiči do žíly), obr. 16 a obr. 17. Pomocí USG zkontroluje vznik ev. komplikací (vyloučení pneumotoraxu, lokálního krvácení, hematomu). Metoda USG navigované kanylace je tak bezpečná a jednoduchá, že lékaři reálně hrozí odklon od běžných kanylací bez USG navigace. Pro zachování erudice však doporučujeme střídat obě techniky kanylace, tj. s USG i bez USG asistence pro případ neočekávané nedostupnosti USG technologie.
Image 16. USG navidovaná kanylace v. jugularis 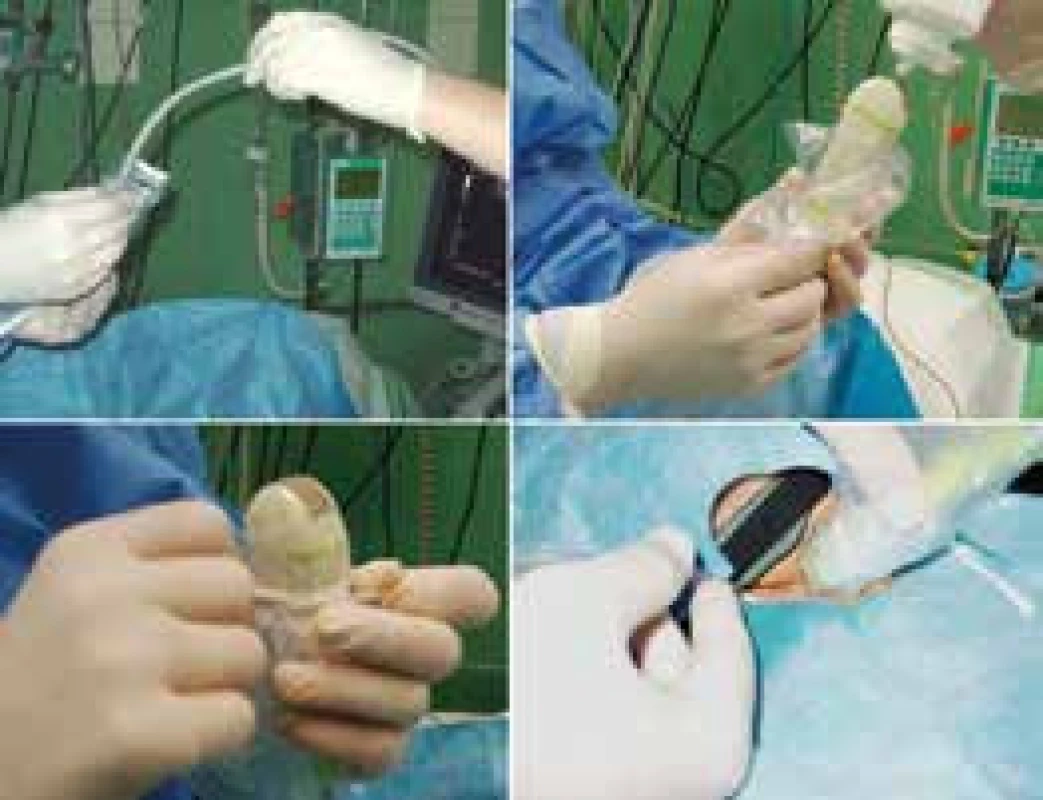
Image 17. USG obraz jehly ve v. jugularis 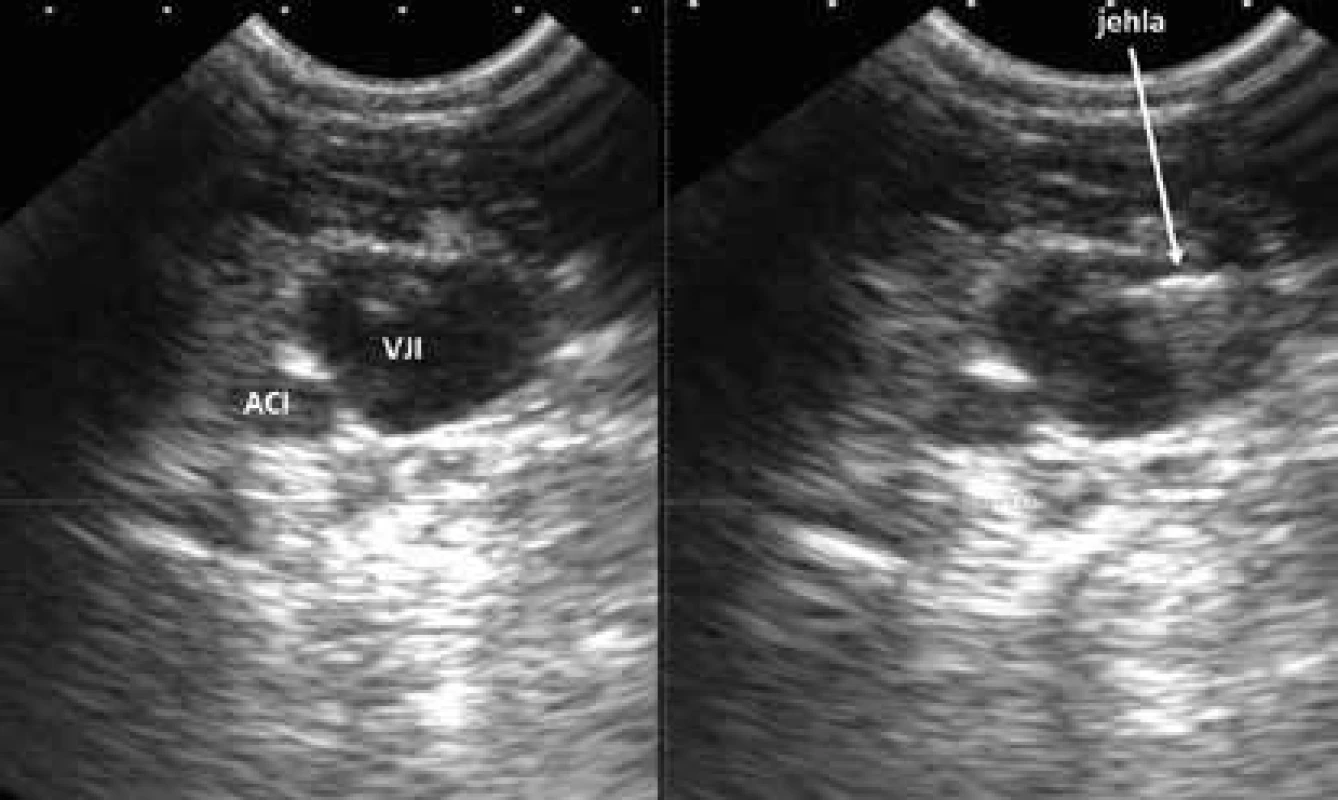
Diferenciální diagnostika příčin akutní dušnosti pomocí USG (BLUE protokol)
Akutní dušnost je pro pacienta i pro lékaře velmi stresující situace. Klinický lékař ovládající USG může spojit získané anamnestické údaje, fyzikální nález a EKG, případně laboratorní výsledky s USG obrazem a výrazně zpřesnit okruh pravděpodobných příčin dušnosti a ihned zahájí správnou léčbu. Jde o nákladově efektivní postup, bezpečný a klinicky ověřený v praxi. Autorem je prof. Lichtenstein, lékař intenzivní péče, který vytvořil algoritmus vyšetřování akutně dušného pacienta, tzv. BLUE protokol. S pomocí tohoto algoritmu lékař během 30 vteřin USG přístrojem vyloučí/potvrdí základní pravděpodobné příčiny dušnosti (pneumotorax, plicní edém, pleurální výpotek a bronchiální obstrukci) až u 90 % případů.
BLUE protokol nevyžaduje polohování pacienta, nemocný je vyšetřen vleže na zádech na přední, laterální a dorzobazální straně hrudníku vpravo i vlevo. Nejprve vyšetříme přítomnost plicního klouzání (použití i M-modu a průkazu příznaku pláže – pobřeží), které vyloučí pneumotorax. Poté se snažíme nalézt přítomnost B-linií (> 3 linie v USG obraze), ty svědčí pro srdeční selhávání, případně pro ARDS, u kterého je však obraz B-linií nehomogenní. USG nedokáže odlišit plicní edém od bilaterální intersticiální pneumonie, v diferenciální diagnostice nám však pomůže anamnéza a další komplementární vyšetření. Nález bilaterálního obrazu A-linií u dušného pacienta ve všech oblastech hrudníku nutí myslet na plicní embolizaci, pak je možné doplnit USG vyšetření femorálních a popliteálních žil – ztrombotizovaná žíla tlakem USG sondy nekolabuje. Pokud je žilní systém dolních končetin i horních končetin volně průchodný, pak pátráme v zóně 3 (laterodorzálně) po přítomnosti tzv. PLAPS (postero-laterální alveolární a/nebo pleurální syndrom). Jde o obraz alveolární konsolidace plíce (izoechogenní vzhled podobný slezině nebo jaterní tkáni) se vzdušným bronchogramem a přítomností pleurálního výpotku. Nález PLAPS při obrazu bilaterálních A-linií v předních zónách je typický pro pneumonii. Pokud nalezneme pouze A-linie v předních zónách bez PLAPS a bez nálezu trombů v žilním systému, je příčinou akutní dušnosti syndrom bronchiální obstrukce (akutní astma nebo akutní exacerbace chronické obstrukční plicní nemoci). Pokud unilaterálně neprokážeme plicní klouzání (příznak stratosféry v M-modu) a nalézáme jen A-linie nepohyblivé plíce, je třeba pátrat po přítomnosti plicního bodu k průkazu pneumotoraxu. Pokud se nám nepodaří nalézt plicní bod a prokazujeme jen A-linie bez plicního klouzání, je třeba provést jiné zobrazovací vyšetření, protože k diagnóze jen s pomocí USG nelze dospět. V těchto případech může být plicní klouzání omezeno např. těžkou hyperinflací plic při akutním astmatu nebo těžké exacerbaci chronické bronchitidy (schéma).
Schéma. Algoritmus použití USG u akutní dušnosti 
Závěr
USG je rychlá a relativně jednoduchá metoda, která vhodně doplňuje práci klinického lékaře u lůžka pacienta. Ve většině případů USG dokáže rychle a významně pomoci v další diagnostické rozvaze nemocí nitrohrudních orgánů a sníží potřebu RTG hrudníku a CT vyšetření. Klinický lékař má u lůžka pacienta při použití USG výhodu oproti radiologovi, protože může USG nález hodnotit v kontextu s anamnestickými daty, fyzikálním nálezem a svými předchozími klinickými zkušenostmi. USG tak může pomoci nejen při diferenciální diagnostice akutní dušnosti, ale i při diagnostice a léčbě pleurálního syndromu, plicních konsolidací, srdečního selhávání, s pomocí USG je možné bezpečně provádět řadu invazivních výkonů, jako jsou kanylace velkých cév, pleurální punkce a drenáže a USG navigované biopsie patologií hrudníku. Ovládnutí techniky USG hrudníku je pro klinického lékaře zpravidla jednoduché, lze využít postgraduálních praktických kurzů, které v pneumologii pořádáme např. v rámci konference Královéhradecké pneumologické dny (www.hradeckedny.cz). V brzké době se USG hrudníku stane povinnou součástí postgraduálních dovedností v pneumologii a tato technologie by se měla začlenit i do pregraduální výuky.
prim. MUDr. Vratislav Sedlák, Ph.D.
vratislav.sedlak@fnhk.cz
Plicní klinika LF UK a
FN Hradec Králové
www.fnhk.cz
Doručeno do redakce 8. 9. 2017
Přijato po recenzi 26. 9. 2017
Sources
1. Bolliger CT, Herth FJF, Mayo PH et al. Clinical Chest Ultrasound. From the ICU to the Bronchoscopy Suite. Karger: Basel 2009. ISBN 978–3–8055–8642–9.
2. Meuwly JY, Gudinchet F. Sonography of the thoracic and abdominal walls. J Clin Ultrasound 2004; 32(9): 500–510.
3. Muradali D, Gold WL, Phillips A et al. Can ultrasound probes and coupling gel be a source of nosocomiali infection in patients undergoing sonography? Am J Roentgenol 1995; 164(6): 1521–1524.
4. Mathis G, Spracher Z, Volpicelli G. EFSUMB – European Course Book. Dostupné z WWW: <http://www.efsumb.org >.
5. Lichtenstein D. General Ultrasound in the critically ill. Springer 2002. ISBN 978–3-540–20822–8.
6. Lichtenstein D. Ultrasound in the management of thoracic disease. Crit Care Med 2007; 35(5 Suppl): S520-S261.
7. Doelken P, Strange C. Chest ultrasound for dummies. Chest 2003; 123(2): 332–333.
8. Koh DM, Burke S, Davies N et al. Transthoracic ultrasound of the chest: clinical uses and applications. Radiographics 2002; 22(1): e1. Dostupné z DOI: <http://dx.doi.org/10.1148/radiographics.22.1.g02jae1e1>.
9. Sedlák V, Vaník P. Ultrazvuk hrudníku v klinické praxi. Maxdorf: Praha 2016. ISBN 978–80–7345–349–7.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2017 Issue 11-
All articles in this issue
- Cílené vyhledávání nemocných s chronickou obstrukční plicní nemocí: stručný přehled
- Asthma bronchiale v kontextu vnitřního lékařství
- Diagnostika a léčba komunitní pneumonie – v jednoduchosti je klíč k úspěchu
- Nozokomiální pneumonie
- Pneumonie u imunokompromitovaných
- Idiopatická plicní fibróza. Umíme ji vždy správně diagnostikovat a léčit?
- Exogenní alergické alveolitidy: minimum pro praxi
- Sarkoidóza – nadále záhadné onemocnění
- Současný přístup k diagnostice, léčbě a prevenci tuberkulózy
-
Non-CF bronchiektázie dospělých: stručný přehled pro praxi
Dokument Sekce chorob s bronchiální obstrukcí České pneumologické a ftizeologické společnosti České lékařské společnosti J. E. Purkyně - Cystická fibróza dospělých
- Kardiovaskulární riziko spánkové apnoe a kazuistika
- Komplikace po transplantaci plic
- Nemalobuněčný karcinom plic
- Malobuněčný karcinom plic: epidemiologie, diagnostika a léčba
- Maligní mezoteliom pleury – dosud nepokořený nádor
- Spirometrie – základní vyšetření funkce plic
- Postavení bronchologie v pneumologické diagnostice
- Ultrasonografické vyšetření hrudníku v rukou lékaře klinika
- Neinvazivní ventilace
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Spirometrie – základní vyšetření funkce plic
- Neinvazivní ventilace
- Pneumonie u imunokompromitovaných
- Malobuněčný karcinom plic: epidemiologie, diagnostika a léčba
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career