-
Medical journals
- Career
Diastolická dysfunkce levé komory ve vyšším věku. Nemoc, nebo fyziologický projev stárnutí?
Authors: J. Meluzín 1,2; H. Podroužková 1,2; Z. Gregorová 1,2; R. Panovský 1,2
Authors‘ workplace: I. interní kardio‑angiologická klinika Lékařské fakulty MU a FN u sv. Anny Brno, přednostka prof. MU Dr. Lenka Špinarová, Ph. D., FESC 1; Oddělení kardiovaskulárních chorob ICRC Brno, vedoucí programu MU Dr. Marek Orban 2
Published in: Vnitř Lék 2013; 59(5): 392-396
Category: Review
Overview
Cíl:
Cílem naší práce bylo rozebrat dosavadní znalosti o vlivu věku na diastolickou funkci levé komory.Literární data:
Dosud publikované práce jednoznačně dokazují významný vztah věku k diastolické funkci levé komory. Stárnutí je fyziologický děj doprovázený strukturálními změnami v myokardu a v systémovém tepenném řečišti spolu se zhoršením parametrů charakterizujících diastolickou funkci levé komory. Tato „fyziologická“ diastolická dysfunkce ve stáří je vysvětlitelná zhoršením pasivních plnících vlastností stěn levé komory i zpomalením rychlosti relaxace levé komory. Analýza dosud publikovaných prací na toto téma ukazuje na velké rezervy v odlišení „fyziologické“ diastolické dysfunkce, která je fyziologickým projevem stárnutí tkání, od „patologické“ diastolické dysfunkce, která je projevem nemoci a často progreduje až do obrazu srdečního selhání.Závěr:
Ke správné interpretaci parametrů hodnotících diastolickou funkci levé komory a ke správné diagnostice srdečního selhání primárně způsobeného poruchou diastolické funkce levé komory je třeba brát v úvahu věk vyšetřovaných. Další studie jsou nutné k přesnému odlišení „fyziologického“ zhoršení diastolické funkce levé komory spojeného s vyšším věkem od skutečně „patologické“ diastolické dysfunkce u starších jedinců.Klíčová slova:
stárnutí – echokardiografie – diastolická dysfunkce – diastolické srdeční selháníÚvod
Porucha diastolické funkce levé komory je základním faktorem vedoucím k rozvoji primárního diastolického srdečního selhání (častěji nyní uváděno jako srdeční selhání s normální ejekční frakcí levé komory – heart failure with normal ejection fraction – HFNEF). Základním projevem pokročilé diastolické dysfunkce levé komory (LK) je námahová dušnost a únavnost, vedoucí ke zhoršené toleranci zátěže. S progresí diastolické dysfunkce může dojít až ke klidové dušnosti v důsledku edému plic s nutností hospitalizace a intenzivní parenterální léčby. Uvádí se, že HFNEF odpovídá přibližně za 30 – 50 % hospitalizací nemocných se srdeční slabostí a jeho prognóza je srovnatelná nebo jen mírně lepší než u nemocných se srdečním selháním, kteří mají sníženou systolickou funkci LK [1 – 5]. Diagnostika HFNEF se opírá o 3 základní předpoklady [6,7], kterými jsou:
- a) přítomnost symptomů nebo příznaků srdeční slabosti,
- b) nález normální nebo jen lehce snížené systolické funkce LK (EF LK > 50 %) při nepřítomnosti významnější dilatace LK (index konečného diastolického objemu LK < 97 ml/ m2), a
- c) průkaz poruchy diastolické funkce LK.
Zatímco získání informací o prvních dvou bodech je poměrně snadné, průkaz diastolické dysfunkce může být spojen s řadou problémů a s obtížnou interpretací výsledků. Problémem je především obtížnost a snížená dostupnost invazivních vyšetření, které jsou v klinické praxi většinou nahrazeny nezatěžujícími neinvazivními metodami, a to především echokardiografií. Interpretace echokardiografických, ale i dalšími metodami získaných nálezů však není jednoduchá, a to zvláště u starších jedinců. Je totiž obecně známo, že stárnutí je fyziologicky spojeno se strukturálními změnami myokardu, které zhoršují diastolické vlastnosti LK a odlišení, co je ještě norma a co již patologie, může být u řady jedinců obtížné. Rovněž je třeba vždy vzít v úvahu, že většina parametrů užívaných k hodnocení diastolické funkce LK je ovlivněna i dalšími faktory, jako jsou např. srdeční frekvence, krevní tlak, tonus vegetativního nervstva, vlastnosti levé síně a perikardu apod.
Cílem naší práce bylo rozebrat dosavadní znalosti o vlivu věku na diastolickou funkci LK a poukázat na obtížnost v odlišení „fyziologického“ zhoršení diastolické funkce LK pravidelně přítomného ve vyšším věku od již „patologické“ diastolické dysfunkce, ohrožující nemocné progresí do srdečního selhání.
Základní neinvazivní parametry diastolické funkce LK
Základní komponenty určující diastolické vlastnosti LK jsou rychlost a úplnost její relaxace a pasivní plnící vlastnosti LK [8]. Kvalitu relaxace LK můžeme přímo invazivně měřit či na ni můžeme nepřímo usuzovat z neinvazivně echokardiograficky získaných parametrů diastolického plnění LK a pohybu mitrálního anulu v časné diastole. Porucha relaxace bez významnějšího vzestupu plnícího tlaku LK (left ventricular filling pressure – LVFP) je typická pro počáteční stadium diastolické dysfunkce [9,10]. Pro poruchu relaxace v tomto stadiu svědčí pokles vrcholné rychlosti plnění LK v časné diastole (E), vzestup vrcholné rychlosti plnění LK při síňovém stahu (A), pokles poměru E/ A, a prodloužení deceleračního času časného diastolického plnění LK (DT) a izovolumické relaxační periody (IVRT). Tyto parametry získáváme pulzní dopplerovskou echokardiografií kvantifikující transmitrální plnění LK [11 – 13]. Při využití tkáňové dopplerovské echokardiografie je pro počínající stadium diastolické dysfunkce s poruchou relaxace typický pokles vrcholné rychlosti pohybu mitrálního anulu v časné diastole (e‘), kterou se doporučuje určovat jako průměr časných diastolických rychlostí, změřených na septální a laterální části mitrálního anulu při záznamu apikální 4dutinové projekce.
Pasivní plnící vlastnosti LK jsou charakterizovány invazivně získanými parametry, jako jsou tuhost, respektive poddajnost LK, které vyžadující současné měření nitrokomorového tlaku, a objemu a posouzení jejich vztahu. Neinvazivně můžeme na zvýšenou tuhost LK usuzovat opět jen z nepřímých známek, např. ze vzestupu LVFP, který většinou odhadujeme z echokardiograficky naměřených parametrů a vypočítaných indexů. Typickou známkou vzestupu LVFP při normální EF LK (a tedy již známkou pokročilejšího stadia diastolické dysfunkce) je vzestup E/ e‘ ≥ 13 [10]. Hodnota E/ e‘ ≤ 8 je považována za normální nález [10]. Tab. 1 ukazuje echokardiografické parametry definující diastolickou dysfunkci v rámci diagnostiky HFNEF podle doporučení Evropské kardiologické společnosti [7]. Další echokardiografické parametry získané např. metodou speckle tracking a dalšími se zatím testují. Žádný z echokardiografických parametrů však zatím není dostatečně přesný, aby samotný s dostatečně vysokou senzitivitou a specificitou diagnostikoval diastolickou dysfunkci a HFNEF, a doporučuje se proto vždy analyzovat více parametrů [6,7,10]. Neinvazivní diagnostiku diastolické dysfunkce LK může v blízké budoucnosti zkvalitnit nukleární magnetická rezonance. Vzhledem k zásadní roli echokardiografie v klinické diagnostice diastolické dysfunkce a HFNEF bude v další části sdělení rozebírána především úloha a role parametrů získaných echokardiografií.
Table 1. Echokardiografické parametry doporučované Evropskou kardiologickou společností pro diagnostiku srdečního selhání s normální ejekční frakcí levé komory [7]. ![Echokardiografické parametry doporučované Evropskou kardiologickou společností pro diagnostiku srdečního selhání s normální ejekční frakcí levé komory [7].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/866ff460cec8d32dcc1ad8ffa7468537.png)
Parametry diastolické funkce LK u zdravých jedinců a jejich vztah k věku
Vztah mezi echokardiografickými parametry diastolické funkce LK a věkem u zdravých jedinců byl již analyzován v celé řadě studií [14 – 22]. Největší soubor 1 012 zdravých dobrovolníků ve věku 45 let a více vyšetřili Munagala et al [14]. Autoři při hodnocení transmitrálního plnění LK pulzní dopplerovskou echokardiografií nalezli s narůstajícím věkem významný pokles E a E/ A, vzestup A a prodloužení DT. Tkáňová dopplerovská echokardiografie odhalila významný pokles rychlostí e‘ na septálním (z 10 ± 3 cm/ s na 8 ± 7 cm/ s) i laterálním (z 13 ± 4 cm/ s na 9 ± 8 cm/ s) mitrálním anulu s narůstajícím věkem, což vedlo k vzestupu E/ e‘ (při e‘ měřeném na septální části mitrálního anulu) ze 7,2 ± 2,14 ve věkové kategorii 45 – 49 let až na 9,32 ± 3,32 u jedinců ve věku 70 let a výše. Při měření e‘ na laterální části mitrálního anulu byl obdobný vzestup E/ e‘ z 5,61 ± 1,38 na 8,32 ± 2,81. K dalším důležitým pracím patří studie De Suttera et al [15] zahrnující 174 jedinců bez kardiovaskulárního onemocnění rozdělených do věkových kategorií pod 45 let, 45 – 54 let, 55 – 64 let, 65 – 74 let a nad 74 let. Při hodnocení dopplerovských parametrů transmitrálního plnění LK s narůstajícím věkem E rychlost klesala, A rychlost stoupala s výsledným poklesem E/ A poměru z 1,44 na 0,98 a DT se prodlužoval. Při analýze tkáňové dopplerovské echokardiografie byl nalezen postupný pokles e‘ měřeném na septálním okraji mitrálního anulu z 10,1 ± 2,6 cm/ s až na 6,2 ± 1,7 cm/ s. Kategorie jedinců 55 – 64 let, 65 – 74 let a nad 74 let měly průměrné hodnoty e‘ měřené na septálním mitrálním annulu 7,6 ± 2,3 cm/ s, 7,0 ± 2,1 cm/ s a 6,2 ± 1,7 cm/ s; vypočítané E/ e‘ poměry narůstaly z 10,4 ± 3,3 na 11,5 ± 3,1 a 12,4 ± 3,3. Z nálezů vyplývá, že významná část starších zdravých jedinců se blížila echokardiografickým kritériím pro diagnostiku HFNEF nebo již tato kritéria dokonce splňovala. Progresivní pokles e‘ [16,17], E [17,20,22,23], E/ A [17,22,23], a vzestup E/ e‘ [17] s narůstajícím věkem byl potvrzen i na dalších souborech. Tab. 2 ukazuje základní echokardiografické parametry u zdravých jedinců různých věkových kategorií v nejdůležitějších studiích.
Table 2. Základní echokardiografické parametry u zdravých jedinců různých věkových kategorií v nejdůležitějších studiích. 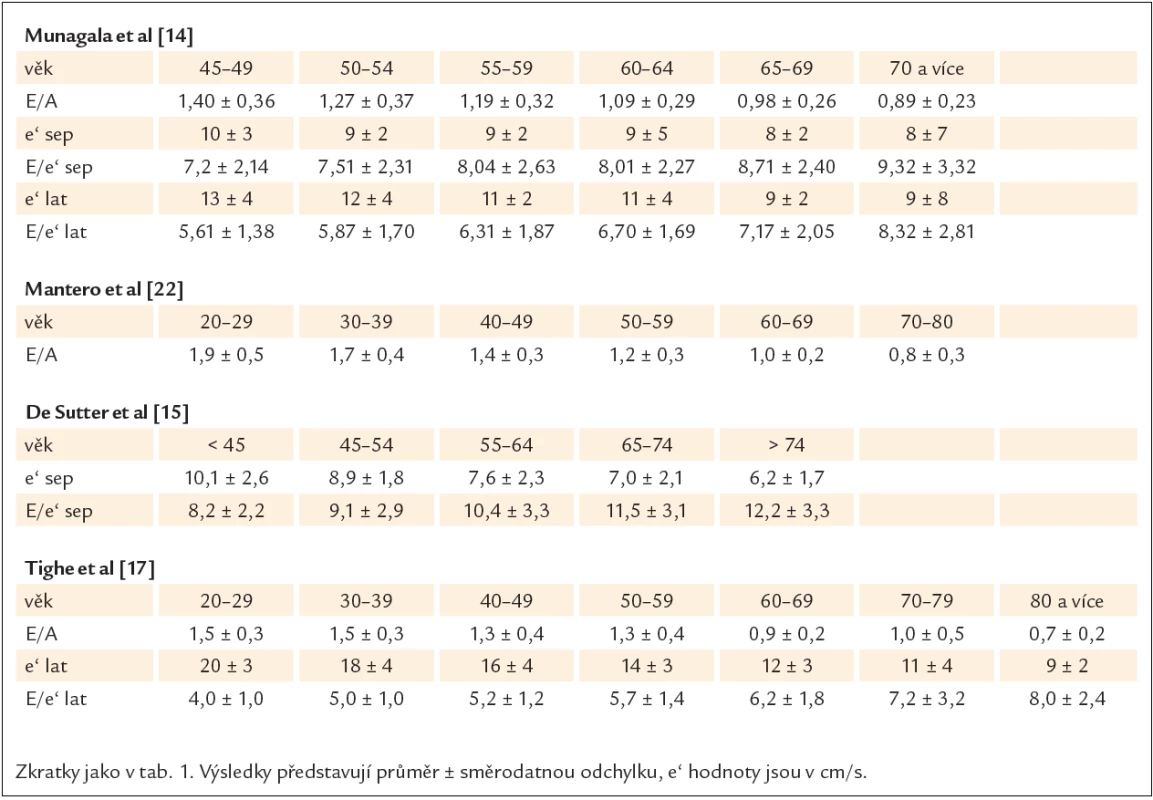
Nicméně vliv věku na diastolickou funkci LK byl prokázán i na invazivně získaných parametrech. Downes et al [18] srovnali katetrizačně získaná data 11 starších (průměr 68 ± 5 let) a 15 mladších (průměr 31 ± 7 let) jedinců katetrizovaných pro bolesti na hrudi. U všech byla vyloučena významná koronární nemoc, všichni měli normální EF LK a žádný netrpěl hypertenzní nemocí. Průměrný konečný diastolický tlak LK (LVEDP) u starších jedinců dosáhl 15 ± 7 mm Hg ve srovnání s hodnotou 11 ± 4 (p < 0,05) u mladších. I v tomto souboru měli někteří starší jedinci LVEDP > 16 mm Hg, což je hodnota diagnostická pro HFNEF [6]. Křivka charakterizující vztah LVEDP a LVEDVI (index konečného diastolického objemu LK) byla u starších jedinců posunuta vzhůru a doleva, což naznačuje snížení pasivní poddajnosti LK. Současný pokles E (61 ± 14 cm/ s vs 83 ± 8 cm/ s) a E/ A (0,81 ± 0,26 vs 1,88 ± 0,40) u starších jedinců však naznačuje i poruchu relaxace LK. Na věkově i počtem velmi podobných 2 souborech mladších a starších zdravých jedinců vyšetřených pravostrannou katetrizací a echokardiografií Prasad et al [19] ukázali, že pokles E a E/ A u starších jedinců není způsoben nízkým časně diastolickým tlakem v levé síni, ale patrně zhoršením relaxace LK (pro což svědčila i delší izovolumická relaxační perioda) a ev. i sníženou poddajností LK. Shrneme‑li dostupná data, je zřejmé, že u jedinců vyššího věku bez kardiovaskulárních onemocnění dochází fyziologicky jak ke zhoršení relaxace LK, tak i k nárůstu její tuhosti, resp. poklesu poddajnosti. Hranici, kdy je u asymptomatických, do doby vyšetření zdravých starších jedinců nález diastolické dysfunkce LK ještě normální a kdy je již patologický, je na základě současných znalostí velmi těžké přesně určit. Stejně tak je obtížné přesněji definovat „šedé zóny“ hraničních nálezů.
Strukturální změny myokardu u zdravých jedinců a jejich vztah k věku
Základní strukturální změnou myokardu ovlivňující diastolické vlastnosti LK ve vztahu k věku je nárůst množství vaziva. Procentuální nárůst množství vaziva v myokardu není jen záležitostí onemocnění myokardu. Řada autorů prokázala, že k nárůstu množství vaziva s věkem dochází „fyziologicky“ i u zdravých jedinců s jejich stárnutím [24,25]. Ling et al [24] prokázali pomocí nukleární magnetické rezonance, vybavené speciálním „softwarem“ pro kvantifikaci difuzní myokardiální fibrózy, významný lineární nárůst fibrózy myokardu s narůstajícím věkem u 23 zdravých dobrovolníků. V této práci byl věk jediným nezávislým prediktorem fibrotizace myokardu u zdravých jedinců. Rovněž histologická analýza srdcí bez dříve zjištěné patologie potvrdila významně vyšší obsah kolagenu (5,86 ± 0,81 %, p < 0,05) u srdcí jedinců mezi 67 – 87 lety ve srovnání s množstvím kolagenu (3,92 ± 0,8 %) získaných ze srdcí jedinců mezi 20 – 25 lety [25]. Ve stejné práci elektronová mikroskopie odhalila významně větší průměr fibril kolagenu u starších srdcí. Zvýšené hromadění kolagenu v myokardu s narůstajícím stářím srdcí bylo rovněž potvrzeno na zvířecích modelech [26]. Fibrotizace myokardu v důsledku nárůstu množství kolagenu v myokardu je typicky spojena s rozvojem diastolické dysfunkce a HFNEF [27,28]. U nemocných s HFNEF byla prokázána významná pozitivní korelace mezi množstvím kolagenu v myokardu a zhoršováním diastolické funkce LK [27,28]. Kasner et al [27] popsali významnou negativní korelaci mezi e‘ a procentuálním zastoupením kolagenu v myokardu (collagen volume fraction – CVF). S CVF ještě těsněji koreloval poměr E/ e‘, což je v současnosti hlavní neinvazivní echokardiografický prediktor zvýšeného LVFP [10]. Je zřejmé, že i vazivové změny myokardu, které se fyziologicky objevují se stárnutím organizmu, se budou odrážet ve zhoršení diastolických vlastností myokardu. Diastolickou funkci LK u zdravých jedinců vyššího věku však mohou negativně ovlivnit i další faktory, jako je nárůst objemů levé síně a komory [14], nárůst hmotnosti LK [14] a hlavně změny v systémovém tepenném řečišti. Je dobře známo, že nárůst tuhosti tepen (arterial stiffness), ke kterému dochází ve vyšším věku, je doprovázen zhoršením relaxace LK [29].
Kde je hranice, oddělující u starších jedinců „fyziologickou“ a „patologickou“ diastolickou dysfunkci?
Odpověď na tuto základní otázku je velmi těžká a autoři tohoto sdělení se domnívají, že na základě současných znalostí na tuto otázku nelze dát jasnou odpověď. Jeví se velmi pravděpodobné, že některé současné „cutoff“ hodnoty pro diagnostiku HFNEF nelze u starších jedinců spolehlivě použít. Problémy s interpretací „patologických“ parametrů diastolické funkce LK u „zdravých“ jedinců plynule narůstají s věkem a je třeba s nimi častěji počítat už po dosažení 65 let [14,18]. Jak bylo uvedeno v jedné z předchozích kapitol, lze i u zdravých asymptomatických starších jedinců naměřit hodnoty LVEDP nad 16 mm Hg [18], stejně jako klidový E/ e‘ poměr nad 8 [14]. Rovněž hodnota e‘ pod 9 cm/ s (průměr z hodnot na septálním a laterálním mitrálním anulu), uváděná podle nejnovějších doporučení Evropské kardiologické společnosti pro diagnostiku a léčbu srdeční slabosti jako patologická a diagnostická pro HFNEF [7], je u zdravých starších jedinců nacházena poměrně běžně [14]. Řešením těchto problémů a rozporů by bylo stanovení různých „cutoff“ hodnot pro diagnostiku diastolické dysfunkce u HFNEF podle věku vyšetřovaných.
Ještě obtížnější je definice normálních diastolických parametrů při zátěži. Přitom tato otázka je velmi důležitá, neboť nález izolovaného pouze zátěží navozeného HFNEF je velmi častou příčinou nejasné námahové dušnosti [30]. Zde chybí studie, které by primárně sledovaly vliv věku na zátěžové parametry diastolické funkce LK u zdravých jedinců. Různý věk vyšetřovaných může být i jednou z příčin velmi rozdílných zátěžových „normálních“ hodnot udávaných v literatuře [30 – 33]. Rozdílné hodnoty plicního kapilárního tlaku v zaklínění při zátěži vleže u zdravých jedinců ukazuje tab. 3. Při takto odlišných nálezech je potom velmi obtížné definovat normální zátěžovou hodnotu příslušného parametru pro zdravou populaci.
Table 3. Hodnoty plicního kapilárního tlaku při zátěži vleže u zdravých jedinců. Ukázka rozdílnosti výsledků v různých studiích. 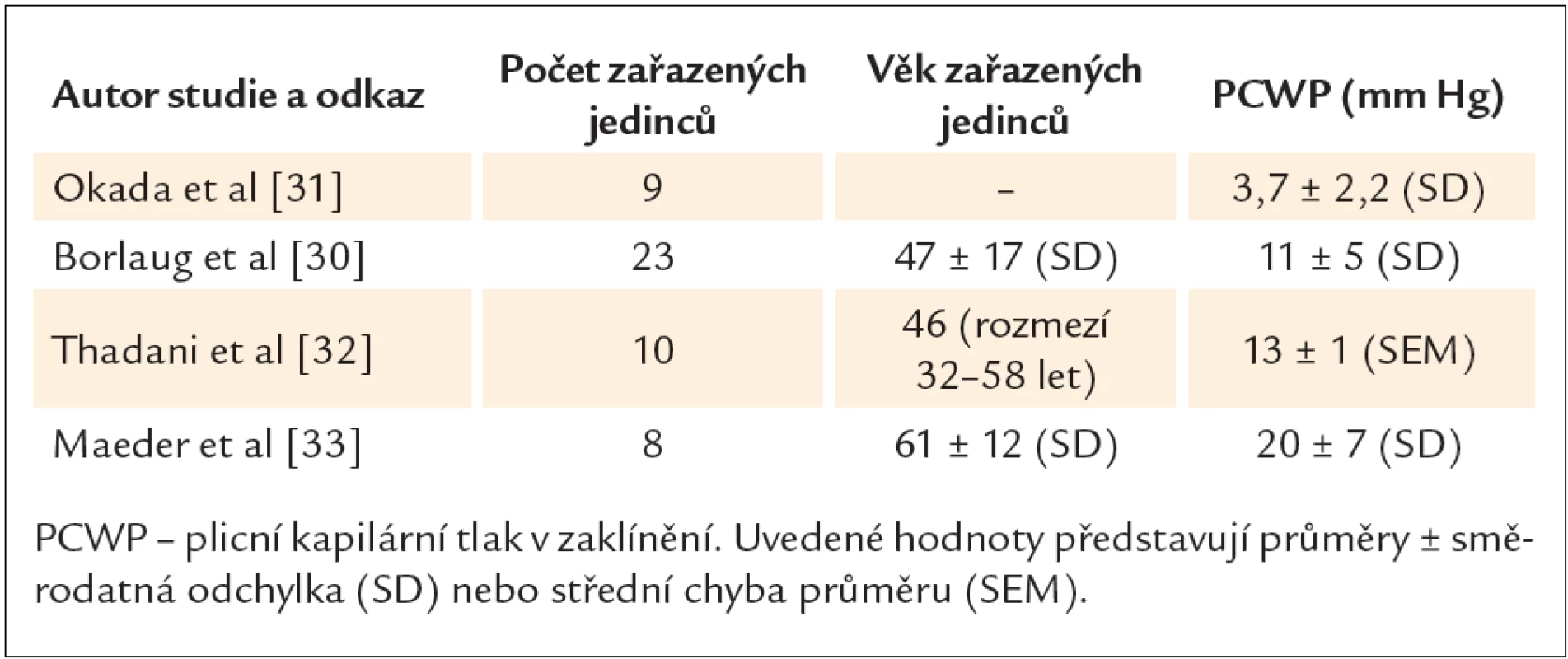
Závěr
Diagnostika diastolické dysfunkce LK a HFNEF je u starších jedinců obtížná a vyžaduje opatrnost v interpretaci nálezů. Získané parametry by měly být interpretovány s vědomím, že s narůstajícím věkem se fyziologicky mění struktura a vlastnost myokardu a tepenných stěn, což je doprovázeno „fyziologickým“ zhoršením diastolické funkce LK. Další studie jsou nutné k přesnému odlišení „fyziologického“ zhoršení diastolické funkce LK spojeného s vyšším věkem od skutečně „patologické“ diastolické dysfunkce u starších jedinců, která odráží nemoc organizmu.
Práce byla vypracována s podporou European Regional Development Fund – Project FNUSA ‑ ICRC (No.CZ.1.05/ 1.1.00/ 02.0123).
prof. MU Dr. Jaroslav Meluzín, CSc.
www.fnusa.cz
e‑mail: jaroslav.meluzin@fnusa.cz
Doručeno do redakce: 18. 2. 2013
Přijato po recenzi: 25. 3. 2013
Sources
1. Redfield MM, Jacobsen SJ, Burnett JC et al. Burden of systolic and diastolic ventricular dysfunction in the community. JAMA 2003; 289 : 194 – 202.
2. Owan TE, Hodge DO, Herges RM et al. Trends in prevalence and outcome of heart failure with preserved ejection fraction. N Engl J Med 2006; 355 : 251 – 259.
3. Bhatia RS, Tu JV, Lee DS et al. Outcome of heart failure with preserved ejection fraction in a population‑based study. N Engl J Med 2006; 355 : 260 – 269.
4. Steinberg BA, Zhao X, Heidenreich PA et al. Trends in patients hospitalized with heart failure and preserved left ventricular ejection fraction. Prevalence, therapies, and outcomes. Circulation 2012; 126 : 65 – 75.
5. Ho JE, Gona P, Pencina MJ et al. Discriminating clinical features of heart failure with preserved vs. reduced ejection fraction in the community. Eur Heart J 2012; 33 : 1734 – 1741.
6. Paulus WJ, Tschope C, Sanderson JE et al. How to diagnose diastolic heart failure: a consensus statement on the diagnosis of heart failure with normal left ventricular ejection fraction by the Heart Failure and Echocardiography Associations of the European Society of Cardiology. Eur Heart J 2007; 28 : 2539 – 2550.
7. McMurray JJV, Adamopoulos S, Anker SD et al. ESC guidelines for the diagnosis and treatment of acute and chronic heart failure 2012. Eur Heart J 2012; 33 : 1787 – 1847.
8. Zile MR, Baicu CF, Gaasch WH. Diastolic heart failure – abnormalities in active relaxation and passive stiffness of the left ventricle. N Engl J Med 2004; 350 : 1953 – 1959.
9. Yamamoto K, Redfield MM, Nishimura RA. Analysis of left ventricular diastolic function. Heart 1996; 75: (Suppl. 2): 27 – 35.
10. Nagueh SF, Appleton ChP, Gillebert TC et al. Recommendations for the evaluation of left ventricular diastolic function by echocardiography. Eur J Echocardiogr 2009; 10 : 165 – 193.
11. Hradec J. Srdeční selhání s normální ejekční frakcí. Kardiol Rev 2008; 10 : 111 – 116.
12. Hradec J. Diastolické srdeční selhání. Diagnostika, epidemiologie, prognóza. Kardiol Rev 2004; 4 : 156 – 160.
13. Paleček T, Linhart A. Echokardiografické hodnocení diastolické funkce levé komory: co dokážeme v roce 2009. Cor Vasa 2009; 51 : 789 – 804.
14. Munagala VK, Jacobsen SJ, Mahoney DW et al. Association of newer diastolic function parameters with age in healthy subjects: a population‑based study. J Am Soc Echocardiogr 2003; 16 : 1049 – 1056.
15. De Sutter J, De Backer J, Van de Veire N et al. Effects of age, gender, and left ventricular mass on septal mitral annulus velocity (E‘) and the ratio of transmitral early peak velocity to E‘ (E/ E‘). Am J Cardiol 2005; 95 : 1020 – 1023.
16. Peverill RE, Gelman JS, Mottram PM et al. Factors associated with mitral annular systolic and diastolic velocities in healthy adults. J Am Soc Echocardiogr 2004; 17 : 1146 – 1154.
17. Tighe DA, Vinch CS, Hill JC et al. Influence of age on assessment of diastolic function by Doppler tissue imaging. Am J Cardiol 2003; 91 : 254 – 257.
18. Downes TR, Nomeir AM, Smith KM et al. Mechanism of altered pattern of left ventricular filling with aging in subjects without cardiac disease. Am J Cardiol 1989; 64 : 523 – 527.
19. Prasad A, Okazaki K, Zadeh AA et al. Abnormalities of Doppler measures of diastolic function in the healthy elderly are not related to alterations of left atrial pressure. Circulation 2005; 111 : 1499 – 1503.
20. Bahl VK, Dave TH, Sundaram KR et al. Pulsed Doppler echocardiographic indices of left ventricular diastolic function in normal subjects. Clin Cardiol 1992; 15 : 504 – 512.
21. Henein M, Lindqvist P, Francis D et al. Tissue Doppler analysis of age ‑ dependency in diastolic ventricular behaviour and filling. Eur Heart J 2002; 23 : 162 – 171.
22. Mantero A, Gentile F, Qualtierotti C et al. Left ventricular diastolic parameters in 288 normal subjects from 20 to 80 years old. Eur Heart J 1995; 16 : 94 – 105.
23. Bryg RJ, Williams GA, Labovitz AJ. Effect of aging on left ventricular diastolic filling in normal subjects. Am J Cardiol 1987; 59 : 971 – 974.
24. Ling L, Kistler PM, Ellims AH et al. Diffuse ventricular fibrosis in atrial fibrillation. J Am Coll Cardiol 2012; 60 : 2402 – 2408.
25. Debessa CRG, Maifrino LBM, De Souza RR. Age related changes of the collagen network of the human heart. Mech Ageing Dev 2001; 122 : 1049 – 1058.
26. Eghbali M, Eghbali M, Robinson TF et al. Collagen accumulation in heart ventricles as a function of growth and aging. Cardiovasc Res 1989; 23 : 723 – 729.
27. Kasner M, Westermann D, Lopez B et al. Diastolic tissue Doppler indexes correlate with the degree of collagen expression and cross‑linking in heart failure and normal ejection fraction. J Am Coll Cardiol 2011; 57 : 977 – 985.
28. Martos R, Baugh J, Ledwidge M et al. Diastolic heart failure. Evidence of increased myocardial collagen turnover linked to diastolic dysfunction. Circulation 2007; 115 : 888 – 895.
29. Marti CN, Gheotghiade M, Kalogeropoulos AP et al. Endothelial dysfunction, arterial stiffness, and heart failure. J Am Coll Cardiol 2012; 60 : 1455 – 1469.
30. Borlaug BA, Nishimura RA, Sorajja P et al. Exercise hemodynamics enhance diagnosis of early heart failure with preserved ejection fraction. Circ Heart Fail 2010; 3 : 588 – 595.
31. Okada RD, Osbakken MD, Boucher ChA et al. Pulmonary blood volume ratio response to exercise: a noninvasive determination of exercise‑induced changes in pulmonary capillary wedge pressure. Circulation 1982; 65 : 126 – 133.
32. Thadani U, Parker JO. Hemodynamics at rest and during supine and sitting bicycle exercise in normal subjects. Am J Cardiol 1978; 41 : 52 – 59.
33. Maeder MT, Thompson BR, Brunner ‑ La Rocca HP et al. Hemodynamic basis of exercise limitation in patients with heart failure and normal ejection fraction. J Am Coll Cardiol 2010; 56 : 855 – 863.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2013 Issue 5-
All articles in this issue
- Spondyloartritidy: aktuální pohled na diagnostiku a klasifikaci
- Diastolická dysfunkce levé komory ve vyšším věku. Nemoc, nebo fyziologický projev stárnutí?
- Fixní kombinace telmisartanu a thiazidového diuretika v léčbě hypertenze
- Paraneoplastická hypoglykémia – popis prípadu a prehľad problematiky
- Malígnym melanómom imitovaný akútny koronárny syndróm alebo reálny akútny koronárny syndróm?
- Spondylodiscitida, epidurální empyém jako komplikace syndromu diabetické nohy
- Distribuce s lipoproteiny asociované fosfolipázy A2 v české populaci a její interakce s konvenčním kardiovaskulárním rizikem
- Možný vplyv génového polymorfizmu v oblasti GSTs génov na sérovú hladinu polychlorovaných bifenylov (PCB)
- Srovnání MRCP a ERCP v diagnostice choledocholitiázy
- Poruchy srdcového rytmu u pacientov s diabetes mellitus
- Kombinovaná terapie arteriální hypertenze
- Prevence náhlé srdeční smrti při sportu ve světle nových doporučení
- Choroby způsobené lepkem
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Diastolická dysfunkce levé komory ve vyšším věku. Nemoc, nebo fyziologický projev stárnutí?
- Spondyloartritidy: aktuální pohled na diagnostiku a klasifikaci
- Srovnání MRCP a ERCP v diagnostice choledocholitiázy
- Choroby způsobené lepkem
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

