-
Medical journals
- Career
Kazuistika získané hemofilie A
Authors: Z. Čermáková 1; R. Hrdličková 2; Š. Blahutová 2; A. Ligová 3
Authors‘ workplace: Lékařská fakulta OU Ostrava, děkan doc. MU Dr. Jaroslav Horáček, CSc. 1; Krevní centrum FN Ostrava, přednostka prim. MU Dr. Zuzana Čermáková, Ph. D. 2; Ústav klinické hematologie Lékařské fakulty OU a FN Ostrava, přednosta prim. MU Dr. Jaromír Gumulec 3
Published in: Vnitř Lék 2013; 59(4): 313-316
Category: Case Reports
Overview
Získaná hemofilie A je vzácná forma získané koagulopatie, vyvolaná protilátkami inhibujícími aktivitu koagulačního faktoru VIII. Je charakterizována závažným, mnohdy život ohrožujícím krvácením. Četnost onemocnění je asi 1 – 2 případy na 1 milion obyvatel ročně. Autoři představují kazuistiku získané hemofilie A u ženy ve věku 85 let. Krvácivé epizody byly efektivně zvládnuty preparáty s bypassovou aktivitou. Eradikace inhibitoru faktoru VIII byla úspěšná při použití 2. linie léčby rituximabem.
Klíčová slova:
získaná hemofilie A – inhibitor faktoru VIII – rituximabÚvod
Získaná hemofilie A je vzácné život ohrožující onemocnění způsobené autoprotilátkami inhibujícími aktivitu koagulačního faktoru VIII (F VIII). Četnost výskytu činí 1 – 2 případy na 1 milion obyvatel ročně; nejvíce případů onemocnění je popisováno u žen ve fertilním věku v souvislosti s graviditami a porody a u osob starších 68 let [1]. Ačkoliv je získaná hemofilie často asociována se základní diagnózou, nejčastěji autoimunitní chorobou, malignitou (solidní tumory, lymfoproliferace), graviditou, event. indukcí léky, téměř u 50 % nemocných se nepodaří příčinu odhalit [2]. Na rozdíl od vrozené hemofilie pacienti mnohem méně krvácejí do kloubů, v klinických projevech dominují rozsáhlé podkožní hematomy, krvácení do měkkých tkání, svalů a sliznic, hematurie, závažné krvácení do gastrointestinálního traktu a centrálního nervového systému. Výskyt těžkého a život ohrožujícího krvácení je častý (90 %), mortalita 3 – 33 %, resp. 8 – 22 % má v posledních letech se zlepšením diagnostiky a dostupnosti léčby klesající tendenci [3,4]. Přesto existuje skupina pacientů, podle různých údajů 6 – 33 %, kteří nekrvácejí, případně mají jen minimální příznaky, léčbu nevyžadují a jediným projevem tohoto onemocnění jsou patologické hodnoty výsledků laboratorních vyšetření [3,5].
V laboratorních výsledcích základních koagulačních testů je detekováno izolované prodloužení hodnoty aktivovaného parciálního tromboplastinového testu (aPTT), resp. jeho poměru aPTT - R na 2 – 3násobek při normálních hodnotách protrombinového času i trombinového času. Korekčním testem je možno odlišit deficit koagulačních faktorů tzv. vnitřní cesty od přítomnosti inhibitoru specifického i nespecifického (lupus antikoagulans). Principem testu je korekce koagulační odchylky přidáním normální „zdravé“ směsné plazmy v případě deficitu koagulačních faktorů a přetrvávání patologického výsledku v případě inhibitoru. Vyšetření je provedeno ihned a po 2hodinové inkubaci při 37 °C, jelikož specifický inhibitor F VIII je časově závislý. Dalším krokem je vyšetření aktivity F VIII. Při dostupnosti tohoto testu v místní laboratoři je vhodné (z důvodu časové úspory) u podezření na diagnózu získané hemofilie provést tento test souběžně s testem korekčním. Aktivita F VIII je v přítomnosti specifického inhibitoru nízká, většinou pod 1 %, nicméně ani méně významné snížení F VIII diagnózu nevylučuje. Nakonec je nutná kvantifikace inhibitoru F VIII. Titr se uvádí v Bethesda jednotkách (B.U.); 1 B.U. je množství inhibitoru, které během inkubace inaktivuje 50 % nabídnutého faktoru. Toto vyšetření bývá dostupné obvykle jen ve specializovaných koagulačních laboratořích. Aktivita F VIII a výše titru specifického inhibitoru často nekorelují se závažností a intenzitou klinických projevů [5,6].
V léčbě získané hemofilie je nutný komplexní přístup – zástava krvácení, eradikace inhibitoru a léčba případného vyvolávajícího onemocnění. K zvládnutí krvácivých komplikací jsou k dispozici 2 preparáty s bypassovou aktivitou – rekombinantní faktor VIIa (rF VIIa, NovoSeven®) v doporučené dávce 90 µg/ kg hmotnosti pacienta à 2 – 3 hod, nebo koncentrát aktivovaného protrombinového komplexu (aPCC, Feiba NF®) v dávce 50 – 100 IU/ kg hmotnosti pacienta à 6 – 12 hod s maximální dávkou 200 IU/ kg/ den [2,5]. Oba léky se podávají opakovaně do zástavy krvácení. Odpověď na hemostatickou terapii je sledována zejména klinicky, neexistuje specifický laboratorní test monitorující účinnost bypassové léčby. Výsledky obou preparátů jsou srovnatelné, a pokud se nedaří zvládnout krvácení jedním z nich, je možná jejich vzájemná výměna, případně i kombinace [3,5].
Zahájení eradikace inhibitoru je doporučeno ihned po stanovení diagnózy. V první linii se používají kortikoidy – prednison v dávce 1 mg/ kg hmotnosti pacienta na den samostatně nebo lépe v kombinaci s cyklofosfamidem 1 – 2 mg/ kg hmotnosti pacienta na den maximálně po dobu 3 týdnů [2,3,5]. Úspěšnost je udávána 60 – 70 % pro monoterapii kortikoidy a 70 – 80 % pro kombinovanou léčbu [6]. Medián doby dosažení remise představuje při použití tohoto způsobu léčby přibližně 5 týdnů [5]. Pokud po 4 – 6 týdnech imunosuprese nedochází k odpovědi, je doporučeno zvážit druhou linii léčby – rituximab (v dávce 375 mg/ m2 tělesného povrchu pacienta, 4 dávky v týdenních intervalech) samostatně nebo v kombinaci s kortikoidy [2,5]. Jinou alternativou jsou další cytotoxické léky – azathioprin, vinkristin, cyklosporin, mykofenolát.
Kazuistika
Prezentujeme kazuistiku 85leté polymorbidní pacientky hospitalizované na interním oddělení pro celkové zhoršení zdravotního stavu. Pro závažné krvácení do jazyka a spodiny dutiny ústní bylo vyžádáno hematologické konzilium (obr. 1). V osobní anamnéze je uvedena apendektomie v mládí, jeden porod, hysterektomie a parciální ovarektomie pro myom ve 44 letech a cholecystektomie v 50 letech, operace katarakty oboustranně, hypertenze III. stupně, ischemická choroba srdeční, stav po ischemické cévní mozkové příhodě bez neurologického deficitu, spondylartróza a spondylolistéza, kořenový iritační syndrom, hiátová hernie s ezofagitidou a glaukom. Pacientka v minulosti neudávala žádné krvácivé komplikace, rovněž rodinná anamnéza je negativní ve vztahu k vrozeným krvácivým chorobám. Při klinickém vyšetření byly dále nalezeny i poměrně rozsáhlé podkožní hematomy a trvale prosakující krev z drobné kožní exkoriace na krku. Z léků ovlivňujících hemostázu pacientka užívala pouze ticlopidin. Ostatní medikace: Fentanyl náplast, Lozap H, Concor COR, Betahistin Ratiofarm, Tanakan, Helicid, Vigantol gtt, Aricept, Betatopic gtt. Úvodní laboratorní výsledky (tab. 1) prokázaly mírnou normocytární normochromní anémii (Hgb 115 g/ l, Hct 0,35) a počet leukocytů a trombocytů bez nálezu patologických hodnot. V koagulačních testech bylo prodloužené aPTT - R na 4,1, protrombinový test, fibrinogen a antitrombin byly v normě. Při vyšetření korekčního testu nedošlo k úpravě hodnot aPTT po přidání normální plazmy. Trombinovým testem a vyšetřením anti‑Xa byla vyloučena event. přítomnost heparinu. Došetření koagulačních faktorů, ovlivňujících aPTT jednofázovou metodou pomocí aPTT reagencie středně citlivé na lupus antikoagulans (APTT - XL, Pacific hemostasis) a faktor deficitních plazem (DG - VIII, DG - IX, DG - XI a DG - XII, Grifols), odhalilo výrazně sníženou aktivitu F VIII (F VIII:C) – 0,9 %. Nižší byly i aktivity dalších faktorů: F IX:C 47,7 %, F XI:C 52,7 % a F XII:C 38,7 %. K vyloučení vlivu lupus antikoagulans byla stanovena F VIII:C i aPTT reagencií necitlivou k LA (Actin FS, Siemens) – 1,9 %. Nicméně paralelně byla potvrzena i přítomnost lupus antikoagulans konfirmačním testem (destičkový neutralizační test – PNP). Specifický inhibitor F VIII byl definován aktivitou 13,6 B.U. Na základě klinických projevů a výsledků provedených laboratorních vyšetření byla u pacientky stanovena diagnóza získané hemofilie A za současné přítomnosti lupus antikoagulans. Léčba pacientky byla zahájena podáním 3 dávek rFVIIa (NovoSeven®) v dávce 90 µg/ kg hmotnosti pacientky à 3 hod 1. den (celkem 3 dávky), 2. den bylo pokračováno dvěma aplikacemi koncentrátů faktorů aPCC (Feiba NF®) v dávce 85 IU/ kg hmotnosti v intervalu à 12 hod, což vedlo k zástavě krvácení a výrazné regresi otoku jazyka a sliznic dutiny ústní. Nové krvácivé projevy v 6., 11. a 17. dnu od stanovení diagnózy (2krát rozsáhlé podkožní hematomy na horních končetinách, 1krát na zádech a dolní končetině) byly řešeny podáním koncentrátů faktorů aPCC (Feiba NF®) v dávce 85 IU/ kg hmotnosti pacientky jednorázově, ve 2 případech s opakováním po 12 hod. Od 1. dne diagnózy byla zavedena kombinovaná imunosupresivní terapie s cílem eradikovat inhibitor F VIII: Solu - Medrol (metylprednisolon) 500 mg i.v. první 3 dny, dále pokračováno Prednisonem (prednison) 1 mg/ kg hmotnosti pacientky denně (50 mg/ den) p.o. a Cyclophosphamidem (cyklofosfamid) 1 mg/ kg hmotnosti pacientky denně (50 mg/ den) p.o. I když nedocházelo k poklesu titru inhibitoru, byla po úvodních 14 dnech zahájena pomalá redukce dávky Prednisonu o 5 – 10 mg za týden až na hodnotu 20 mg/ den s ohledem na věk pacientky a přidružené diagnózy (hypertenze, glaukom, osteoporóza, výrazná kožní atrofie). Pět týdnů od zahájení léčby se hodnoty inhibitoru faktoru VIII pohybovaly v hodnotách 10,4 – 13 B.U., pouze jednou zachycena hodnota titru 7,6 B.U. (graf 1). Vzhledem k neuspokojivým výsledkům první linie léčby bylo 35. den od jejího zahájení rozhodnuto zastavit podávání cyklofosfamidu a začít s aplikací 4 cyklů MabThery (rituximabu) 375 mg/ m2 tělesného povrchu pacientky v týdenních intervalech s pokračováním podávání Prednisonu 20 mg/ den. I během tohoto období ještě byly opakovaně podávány koncentráty faktorů aPCC pro 3 dny trvající hematurii (4 dávky faktorů aPCC v dávce 85 IU/ kg hmotnosti pacientky à 12 hod první 2 dny a následně v dávce 50 IU/ kg hmotnosti pacientky à 6 hod jeden den), dále pro nestavitelné krvácení z drobné ranky na prstu ruky (jednorázově 85 IU/ kg hmotnosti pacientky) a pro nové hematomy na dolních i horních končetinách (jednorázově 85 IU/ kg hmotnosti pacientky). Poslední krvácení se u pacientky objevilo následující den po aplikaci 4. dávky rituximabu. Během hospitalizace byla pacientka přeléčena pro infekci močových cest s febriliemi a bronchopneumonii s odpovídajícím nálezem na RTG plic kombinací širokospektrých antibiotik a antimykotik. Malignita nebyla prokázána. Z autoimunitních chorob byla nalezena pouze laboratorní přítomnost lupus antikoagulans bez orgánového postižení. Celkové remise s normalizací aktivity faktoru VIII (54,7 %), normalizací aPTT, poklesem inhibitoru F VIII na 0,1 B.U. i vymizením lupus antikoagulans bylo u naší pacientky dosaženo po 128 dnech od stanovení diagnózy (graf 1). Vzhledem k hodnotám aPTT jsme u pacientky již dále nekontrolovali v úvodu zřejmě jen in vitro snížené F IX:C, F XI:C, F XII:C.
Image 1. Krvácení do jazyka a spodiny dutiny ústní. 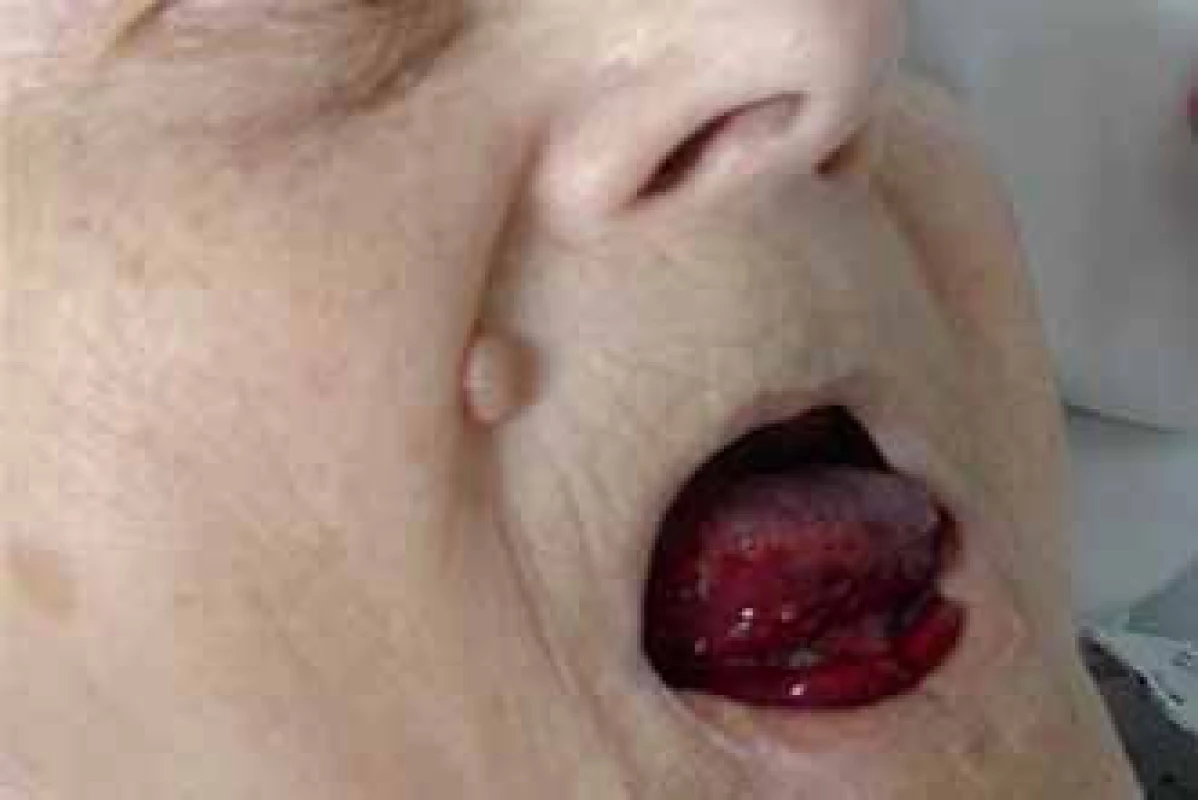
Table 1. Laboratorní výsledky při stanovení diagnózy získané hemofilie A, během léčby a po léčbě. 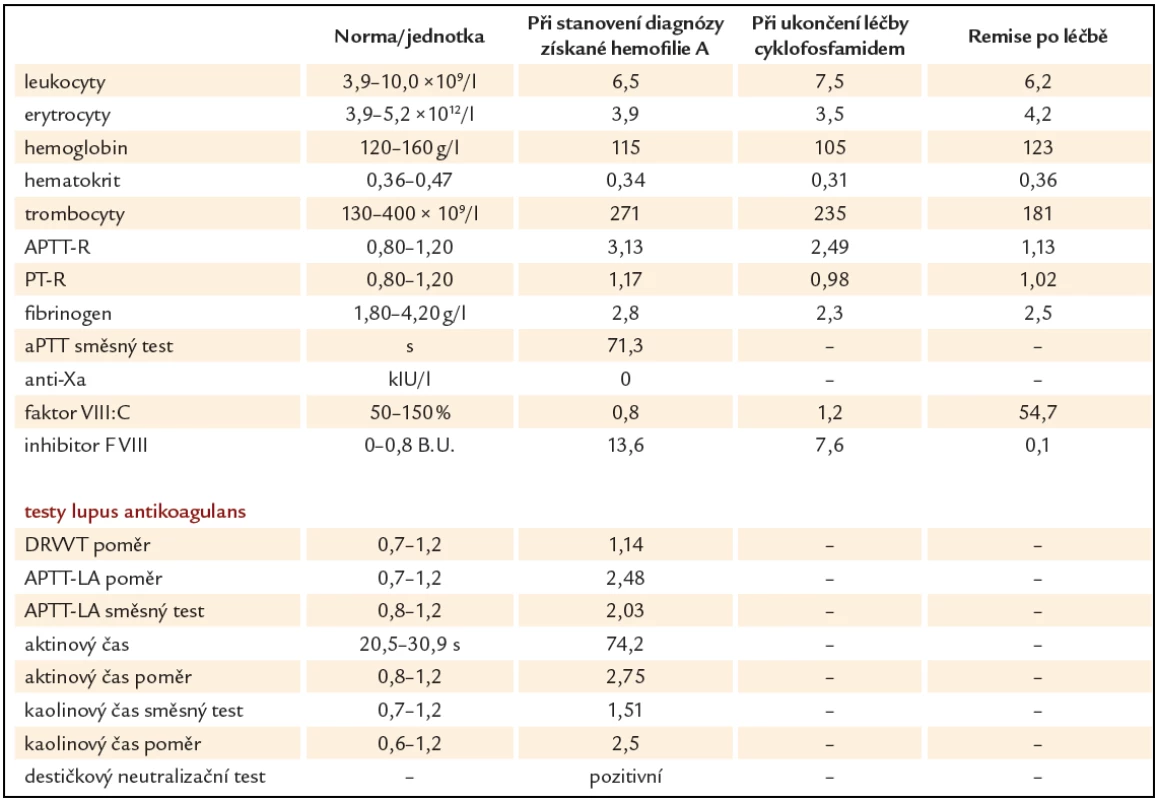
Graph 1. Časový průběh inhibitoru F VIII a F VIII. 
Diskuze
Získaná hemofilie A je relativně vzácné onemocnění vzniklé na autoimunitním podkladě. V patogenezi se uplatňuje vazba protilátky na některé z funkčních míst F VIII, následně znemožnění vazby F VIII na F IX a F X, interferenci s vazbou F VIII na von Willebrandovův faktor, případně interferenci s vazbou F VIII na fosfolipidy. Nejčastěji se jedná o imunoglobuliny třídy IgG, vzácně IgM nebo IgA [8]. Mechanizmus vzniku inhibitoru není plně objasněn. V klinickém obraze pacientů dominují závažné, často i život ohrožující krvácivé komplikace, které nemusejí korelovat s aktivitou faktoru VIII a titrem inhibitoru. Riziko zakrvácení trvá po celou dobu přítomnosti inhibitoru. U některých pacientů může být i klinicky asymptomatický průběh, případně mají jen minimální příznaky nevyžadující terapii. V laboratorních nálezech je přítomno prodloužené aPTT bez úpravy v korekčním testu po 2hodinové inkubaci s normální plazmou, diagnóza je určena stanovením F VIII:C a inhibitoru F VIII Bethesda metodou, v případě nízkého titru je přesnější jeho stanovení Nijmegen modifikací. V diferenciální diagnóze je nutno odlišit nespecifický inhibitor lupus antikoagulans, léčbu a případné předávkování heparinem, event. i jinými antikoagulačními léky. V terapii závažných krvácivých komplikací je doporučeno použití preparátů s bypassovou aktivitou rFVIIa nebo koncentrát aPCC, při nezvladatelných krváceních je možná i jejich kombinace. Součástí léčby je eradikace inhibitoru lépe kombinovanou imunosupresí kortikoidy s cyklofosfamidem v 1. linii léčby, v případě selhání po 5 – 6 týdnech je volena 2. line léčby – kortikoidy v kombinaci s jiným imunosupresivem (nejčastěji cyklosporinem A) nebo rituximabem (monoklonální protilátka anti‑CD20).
V uvedené kazuistice byl u pacientky kromě specifického inhibitoru F III prokázán i lupus antikoagulans, který se pravděpodobně spolu s reakcí inhibitoru F VIII s F VIII přítomným v použité faktor deficitní plazmě podílel na in vitro snížení F IX:C, F XI:C a F XII:C. Krvácivé komplikace byly dobře zvládnuty preparáty s bypassovou aktivitou rFVIIa použitým v úvodu léčby v dávce 90 µg/ kg hmotnosti pacientky à 3 hod 1. den i koncentrátem aPCC v dalším průběhu v dávce 85 IU/ kg hmotnosti 2krát denně, což je v souladu s mezinárodními doporučeními [3,5]. Na méně závažné krvácivé projevy byla použita také jednorázová aplikace. Pouze při hematurii jsme byli nuceni aplikovat koncentráty aPCC 3 dny za sebou a jako účinnější se nám jevil režim 50 IU/ kg hmotnosti pacientky à 6 hod než 85 IU/ kg hmotnosti 2krát denně. S eradikací inhibitoru faktoru VIII jsme byli úspěšní až v druhé linii léčby při použití rituximabu.
Závěr
V rámci diferenciální diagnostiky prodlouženého aPTT testu zejména u staršího pacienta s nově vzniklým krvácením je nutno uvažovat i o diagnóze získané hemofilie. Neodhalení problému může vést k fatálním krvácivým komplikacím. Naše pacientka dobře reagovala na přípravky s bypassovou aktivitou (rVIIa a faktory aPCC), s eradikací inhibitoru faktoru VIII jsme byli úspěšní až v 2. linii léčby. Použití rituximabu i v tak vysokém věku se kromě dobře zvládnutých febrilních infektů obešlo bez dalších komplikací.
prim. MU Dr. Zuzana Čermáková, Ph.D.
www.fno.cz
e‑mail: zuzana.cermakova@fno.cz
Doručeno do redakce: 16. 10. 2012
Přijato po recenzi: 12. 2. 2013
Sources
1. Hay CR, Brown S, Collins PW et al. The diagnosis and management of factor VIII and IX inhibitors: a guidline from the United Kingdom Haemophilia Centre Doctors’ Organization. Br J Haematol 2006; 133 : 591 – 605.
2. Huth-Kuhne A, Baudo F, Collins P et al. International recommendations on the diagnosis and treatment of patients with acquired hemophilia A. Haematologica 2009; 94 : 566 – 575.
3. Sborov DW, Rodgers GM. Acquired hemophilia A: a curent review of autoantibody disease. Clin Adv Hematol Oncol 2012; 10 : 19 – 27.
4. Holme PA, Brosstad F, Tjønnfjord GE. Acquired haemophilia: management of bleeds and immune therapy to eradicate autoantibodies. Haemophilia 2005; 11 : 510 – 515.
5. Collins P, Baudo F, Huth - Kuhne A et al. Consensus recommendations for the diagnosis and treatment of acquired hemophilia A. BMC Research Notes 2010; 3 : 161.
6. Smejkal P, Buliková A, Chlupová G et al. Získaná hemofilie A. Vnitř Lék 2012; 58 : 571 – 578.
7. Collins PW, Hirsch S, Baglin TP et al. Acquired hemophilia A in the United Kingdom: 2‑year national surveillance study by the United Kingdom Haemophilia Centre Doctors’ Organization. Blood 2007; 109 : 1870 – 1877.
8. Buliková A, Smejkal P, Zavřelová J et al. Získané inhibitory krevního srážení. Interní Med 2008; 10 : 336 – 339.
Labels
Diabetology Endocrinology Internal medicine Surgery Intensive Care Medicine Cardiology Clinical oncology Trauma surgery Laboratory
Article was published inInternal Medicine

2013 Issue 4-
All articles in this issue
- Perindopril v léčbě hypertenze a kardiovaskulárních chorob: evoluce pokračuje orodisperzní formou
- Oxidační stres u pacientů po transplantaci ledviny
- Metastázy do plic jako první projevy okultního medulárního mikrokarcinomu
- Kazuistika získané hemofilie A
- Využití vildagliptinu z pohledu interního lékaře
- PET-CT dokumentovaný rychlý nástup léčebné odpovědi cyklofosfamidu, thalidomidu a dexametazonu u multicentrické formy Castlemanovy nemoci. Popis případu a přehled informací o léčbě
- Změny hmotnosti a kompenzace diabetu (HbA1c) u nemocných s diabetes mellitus 2. typu po přidání exenatidu (Byetta) ke stávající léčbě ve 28 diabetologických ambulancích v ČR – studie BIBY‑II (sledování 24 měsíců)
- „Krátká baterie pro testování fyzické zdatnosti seniorů“ – pilotní studie a validizace testu u starších osob v České republice
- Kteří příbuzní prvního stupně nemocných s kolorektálními neoplaziemi jsou nejvíce ohroženi
- Přínos systému vzdáleného sledování v dlouhodobé péči o pacienty s implantabilními kardiovertery‑ defibrilátory
- Aortální stenóza
- Tuberkulóza v České republice. Současný stav. Diagnóza, léčba, prevence
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Aortální stenóza
- Metastázy do plic jako první projevy okultního medulárního mikrokarcinomu
- „Krátká baterie pro testování fyzické zdatnosti seniorů“ – pilotní studie a validizace testu u starších osob v České republice
- Perindopril v léčbě hypertenze a kardiovaskulárních chorob: evoluce pokračuje orodisperzní formou
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

