-
Medical journals
- Career
Přetížení železem – novinky v patogenezi a léčbě
Authors: J. Čermák 1,2
Authors‘ workplace: Ústav hematologi e a krevní transfuze Praha, zastupující ředitel prof. Ing. Jan E. Dyr, DrSc., 2Česká hematologická společnost České lékařské společnosti J. E. Purkyně, předseda doc. MUDr. Jaroslav Čermák, CSc. 1
Published in: Vnitř Lék 2009; 55(Suppl 1)(Supplementum 1): 59-63
Overview
Nadbytek železa v organizmu může vznikat v důsledku jeho nadměrného přívodu, při poruše transportu železa či při poruše jeho utilizace. V našich podmínkách jde nejčastěji o dědično u hemochromatózu či anémi e s vysokým stupněm inefektivní erytropoézy s nutností podávání opakovaných transfuzí erytrocytů (např. myelodysplastický syndrom). Klíčovým momentem v patofyzi ologii toxicity nadbytku železa je jeho zvýšený výdej do cirkulace. Při překročení saturace transferinu železem sto upá v plazmě množství tzv. netransferinového železa, jehož so učást, tzv. labilní plazmatické železo, je oxidačně aktivní a může inici ovat peroxidaci lipidů vedo ucí k zániku buněk. V laboratorní di agnostice nadbytku železa se uplatňuje vyšetření feritinu v séru a saturace transferinu, mezi neinvazivní metody slo užící ke kvantifikaci obsahu železa v tkáních patří NMR jater a srdce. V léčbě dědičné hemochromatózy se uplatňuje kombinace erytrocytoferéz a chelatační léčby. Ta je metodo u volby u anémi í s přetížením železem. V so učasné době jso u k dispozici 3 chelatační přípravky: desferi oxamine, deferiprone a deferasirox a cílem jejich podávání není jen odstranění již vzniklého přetížení železem, ale prevence jeho vzniku a toxického působení volného železa.
Klíčová slova:
železo – nadbytek železa v organizmu – dědičná hemochromatóza – saturace transferinu – labilní plazmatické železo – feritin v séru – chelatační léčbaÚvod
K přetížení železem dochází v důsledku jeho nadměrného hromadění v organizmu. Obdobně jako u nedostatku železa můžeme při rozvoji nadbytku železa rozlišovat z didaktického hlediska 3 fáze: prelatentní, kdy dochází k postupnému zvyšování obsahu železa v buňkách, latentní, kdy je již překročena zásobní kapacita buňky pro železo, ale ještě nedochází k jejímu poškození, a manifestní přetížení železem, které je spojeno s poškozením organizmu.
Příčiny nadbytku železa v organizmu
Nadbytek železa v organizmu může vznikat v důsledku jeho nadměrného přívodu, při poruše transportu železa či při poruše jeho utilizace. Základní příčiny nadbytku železa jso u shrnuty v tab. 1.
Table 1. Příčiny nadbytku železa. 
Nadměrný přívod železa může být důsledkem vrozeného defektu některého z mechanizmů, jež se uplatňují v regulaci příjmu a výdeje železa buňko u. Konečným důsledkem většiny těchto poruch je defektní stimulace tvorby hepcidinu, jenž představuje jeden z klíčových peptidů ovlivňujících metabolizmus železa v organizmu [1]. Hepcidin indukuje degradaci ferroportinu - 1, jenž je zodpovědný za transport železa přes buněčno u membránu extracelulárně. Nekontrolovaný výdej železa do cirkulace při deficitu hepcidinu vede na jedné straně k jeho nadbytečnému odsunu do zásobních tkání (hepatocytů, monocyto - makrofágového systému), na druhé straně vzniká jeho deficit zejména v buňkách střevní sliznice, což vede druhotně ke stimulaci resopce železa z trávicího traktu. Při překročení vazebné kapacity transferinu pro železo pak sto upá množství tzv. netransferinového železa v plazmě, jež může velmi dobře pronikat do tkání a jehož komponento u je tzv. labilní plazmatické železo, do značné míry zodpovědné za toxické účinky nadbytku železa v organizmu [2] (viz níže). Dnes se pod označení dědičná hemochromatóza vesměs zahrnuje řada defektů, jež vedo u k obdobnému klinickému obrazu a které se většino u liší především rychlostí vzniku a stupněm přetížení železem, ke kterému může dojít (tab. 2). Nejdéle je známa dědičná hemochromatóza vznikající jako důsledek deficitu tzv. proteinu dědičné hemochromatózy (tzv. HH či HFE proteinu) [3], v tab. 2 jso u uvedeny nejčastější mutace genu pro HH protein, přičemž zdaleka nejčastěji bývá přítomna záměna tyrosinu za cystein v pozici 282 (C282Y), jež v homozygotní formě vede k obrazu závažného stupně přetížení železem. HH protein vytváří spolu s transferinovým receptorem 2 a hemojuvelinem (HJV) tzv. transdukční komplex stimulující tvorbu mRNA pro hepcidin. Vzácně byly popsány mutace HJV, vedo ucí k obrazu těžké hemosiderózy v časném věku (tzv. juvenilní hemochromatóza) [4] a též mutace transferinového receptoru 2. Rovněž mutace samotného genu pro hepcidin může vést k obrazu juvenilní hemochromatózy, stejně tak jako mutace genu pro feroportin 1, které jso u spojeny se zvýšeno u stabilito u mRNA či se sníženo u citlivostí na hepcidin [5]. Obraz jaterní siderózy a mikrocytární anémi e je přítomen při defektu proteinu DMT - 1, zodpovědného za přestup železa ze střevního traktu do enterocytu a za uvolnění železa vázaného na transferin do cytoplazmy pro potřeby buňky.
Table 2. Jednotlivé typy dědičné hemochromatózy. 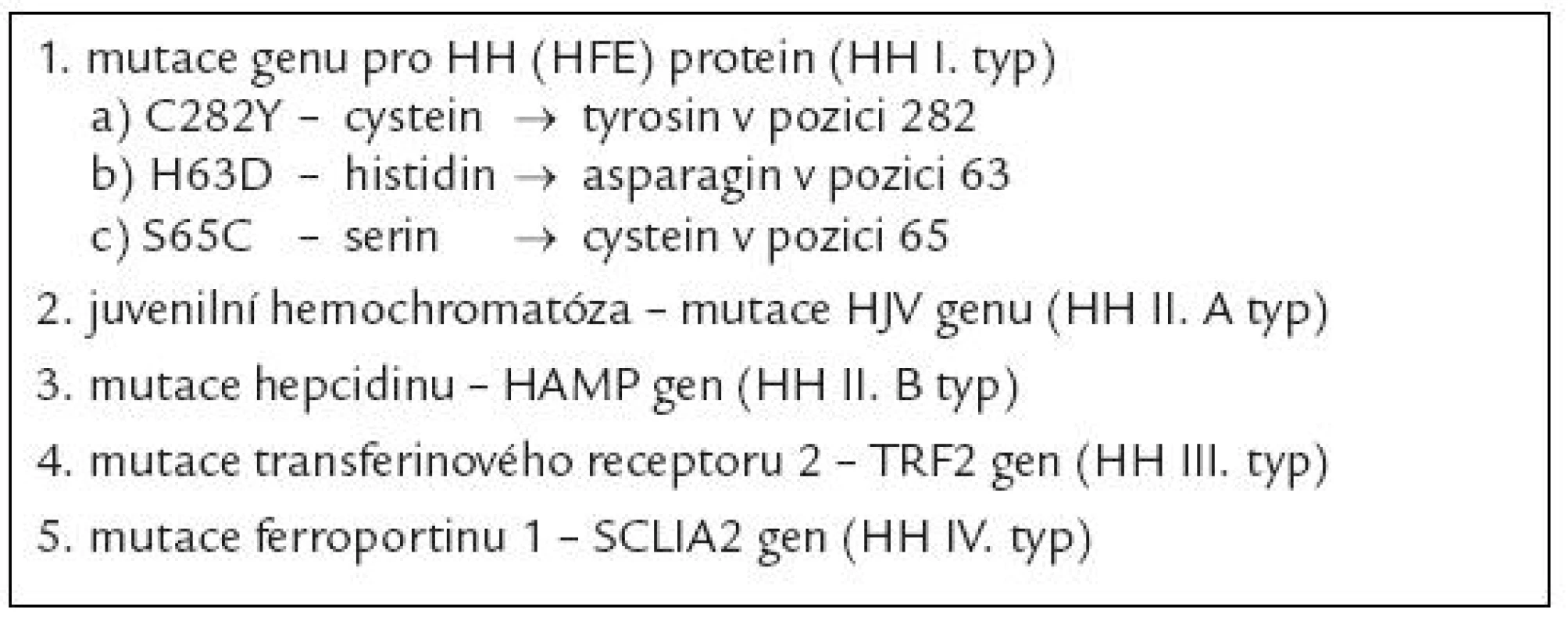
U nemocných s thalasemi a major a jinými dědičnými hemolytickými anémiemi a stejně tak zřejmě u nemocných s myelodysplastickým syndromem (MDS) se na vzniku přetížení do určité míry podílí rovněž zvýšená resorpce železa z trávicího traktu při vystupňovaných nárocích v důsledků přítomnosti hyperplastické inefektivní erytropoézy. V poslední době byly přineseny důkazy, že významnou roli v tomto procesu může opět hrát pokles syntézy hepcidinu, jenž je indukován inhibičním působením tzv. dřeňového faktoru GDF 15 [6]. Tvorba tohoto faktoru je pravděpodobně stimulována tkáňovo u hypoxií vznikající v důsledku anémie. U těchto onemocnění (a dále též např. u útlumu krvetvorby) se na vzniku přetížení železem většinou rovněž významně podílí dodávání železa do organizmu opakovanými krevními převody. Vezmeme‑li v úvahu, že 1 TU erytrocytární masy obsahuje 200 – 250 mg železa a že organizmus má velmi omezené možnosti, jak se zbavit dodaného železa (denní odpad Fe činí v průměru u mužů 1,3 mg, u žen 1,8 – 2,0 mg), může dojít k rozvoji latentního přetížení železem již po podání 20 – 25 TU erytrocytů [7]. V naší studii jsme pozorovali rozvoj závažného stupně přetížení železem u nemocných s časnými formami MDS, kteří dostávali více než 2 TU erytrocytů měsíčně po podání asi 60 TU v období 30 – 40 měsíců [8].
U tzv. africké nutriční hemochromatózy se zřejmě kromě nadbytečného příjmu železa uplatňují i určité genetické mechanizmy (polymorfizmus genu pro ferroportin?), poměrně vzácné defekty transportních proteinů železa (atransferinemi e) či proteinů s feroxidázovou aktivitou umožňujících vazbu Fe3+ na transferin (aceruloplazminemi e) mohou vést k těžkému stupni přetížení železem. K hromadění železa v organizmu dochází při poruše jeho utilizace pro tvorbu hemu při nedostatku protoporfyrinu v důsledku defektu ALA2 syntetázy u kongenitální sideroblastické anémi e. U získané sideroblastické anémie (ve většině případů jde o myelodysplastický syndrom typu refrakterní anémie s nadbytkem sideroblastů – RAS) je příčinou retence železa získaný defekt enzymatických systémů umožňujících jeho redukci na dvojmocno u formu, jež je poté utilizována v dýchacím řetězci mitochondri í [9]. Přetížení železem je popisováno i u porfyria cutanea tarda.
Patofyziologie toxicity nadbytku železa
Klíčovým momentem v patofyzi ologii toxicity nadbytku železa je jeho zvýšený výdej do cirkulace. Při překročení saturace transferinu železem stoupá v plazmě množství tzv. netransferinového železa, část tohoto železa je vázána na albumin, část může být přítomna ve formě komplexů s citrátem a fosfátem jako tzv. labilní plazmatické železo, jež velmi dobře proniká do tkání a je oxidačně aktivní. Výsledkem kaskády oxidačně‑redukčních reakcí inici ovaných „volným“ železem je tvorba volných hydroxylových radikálů uplatňujících se v peroxidativním štěpení lipidů, což ve svém důsledku vede k poškození řady buněčných struktur a v končeném stadi u k zániku buňky účinkem hydroláz uvolněných z poškozených lysozomů [10]. Současně dochází ke zvýšené syntéze kolagenu v důsledku indukce tvorby transformačního růstového faktoru β1 (TGFβ1). Hlavními cílovými orgány jso u při poškození nadbytkem železa játra, kde dochází k rozvoji cirhózy, srdce, kde se může rozvino ut kardiomyopatie vedoucí k srdečnímu selhání, a endokrinní orgány, postižení pankreatu vede k rozvoji diabetu, důsledkem poškození gonád je hypogonadizmus a neplodnost, poruchy růstu jso u důsledkem postižení epifýzy. Zvýšená pigmentace kůže vede k charakteristickému bronzovému zabarvení.
Diagnostika nadbytku železa
V di agnostice nadbytku železa se uplatňují laboratorní metody včetně molekulárně genetických vyšetření a dále řada invazivních či neinvazivních metod kvantifikujících obsah železa v tkáních, přehled diagnostických metod je uveden v tab. 3. Základními laboratorními vyšetřeními používanými k depistáži nemocných s nadbytkem železa jsou vyšetření hladiny feritinu v séru a saturace transferinu, jež je dána poměrem hladiny železa v séru a celkové vazebné kapacity transferinu pro železo. V tab. 4 jsou uvedeny hodnoty feritinu a saturace transferinu, které svědčí s velko u pravděpodobností pro přítomnost heterozygotní či homozygotní formy dědičné hemochromatózy a jejichž přítomnost je indikací pro molekulárně genetické vyšetření HH genu. V poslední době doporučuje Evropská pracovní skupina pro dědično u hemochromatózu jako dostačující screeningové vyšetření pro odhalení možné dědičné hemochromatózy vyšetření saturace transferinu, kdy při hodnotách vyšších než 50 – 55 % u mužů a 45 – 50 % u žen má být provedeno molekulárně genetické vyšetření HH genu [11]. U nemocných s thalasemií či MDS se orientujeme především podle výše hladiny feritinu v séru a neinvazivních metod kvantifikujících obsah železa v tkáních [12]. Vyšetření hladiny labilního plazmatického železa je stále do značné míry vázáno na klinické studi e.
Table 3. Metody uplatňující se v diagnostice nadbytku železa. 
Table 4. Screeningová diagnostika dědičné hemochromatózy. 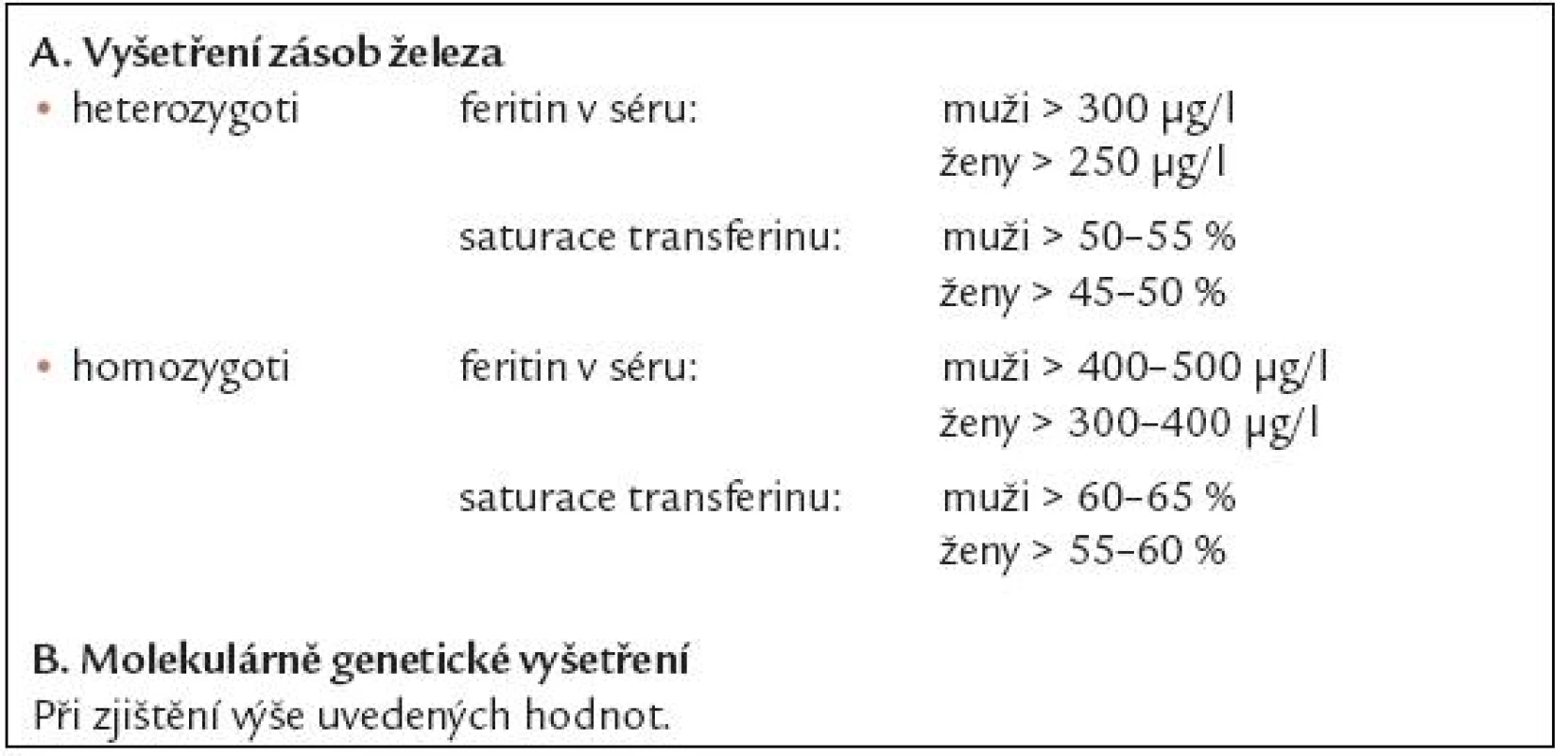
Pro kvantifikaci orgánových zásob železa je stále nejspolehlivější metodo u jaterní biopsi e se stanovením obsahu železa v sušině jaterní tkáně. Vyšetření železa v bioptickém vzorku kostní dřeně dává jen semikvantitativní obraz. Vzhledem k tomu, že jaterní biopsie je spojena s určitým rizikem zejména u nemocných s MDS a trombocytopeni í, byly hledány neinvazivní metody, jejichž výsledek by co nejpřesněji koreloval s výsledky jaterní bi opsi e. U nemocných s β thalasemi í a masivním přetížením železem byla popsána korelace obsahu železa v játrech s hladino u feritinu v séru [13], u nemocných s MDS nebyla tato korelace jednoznačně potvrzena. Nejcitlivější neinvazivní metodo u korelující s nálezy při jaterní bi opsii se ukázalo být vyšetření tzv. magnetické susceptibility jater. Vyšetření však vyžaduje velmi nákladné přístrojové vybavení, a je proto ve světě dostupné jen na několika pracovištích. V posledních letech se dává přednost měření nukle ární magnetické rezonance jater pomocí tzv. R2 metody využívající měření transverzálního relaxačního času jaterní tkáně, u thalasemických nemocných byla i u této metody prokázána dobrá korelace s nálezy získanými při jaterní bi opsii [14]. Vzhledem k tomu, že myokard je kritickým orgánem při rozvoji přetížení železem, byla i zde hledána optimální neinvazivní metoda, jež by spolehlivě odhalila rozvíjející se nadbytek železa v srdci. Na základě korelace s obsahem železa v myokardu při endomyokardi ální bi opsii bylo do praxe zavedeno vyšetření nukle ární magnetické rezonance myokardu pomocí tzv. T2* metody [15]. Zkrácení relaxačního času srdečných chlopní pod 20 ms může svědčit pro přetížení myokardu železem, zkrácení pod 10 ms bývá u thalasemických nemocných spojeno s významným poklesem ejekční frakce levé komory.
Léčba přetížení železem
V so učasné době se mění náhled na indikaci a cíle chelatační léčby. Namísto odstraňování již přítomného nadbytečného železa je kladen důraz na včasné zahájení chelatace a prevenci hromadění železa v tkáních a minimalizaci účinku potenci álně toxického volného železa. U dědičné hemochromatózy zůstává základní léčebno u metodo u provádění venepunkcí, resp. erytrocytoferéz. V počátečním stadi u jso u většino u prováděny 1krát týdně za účelem urychlené mobilizace nadbytečného železa pro erytropoézu, udržovací léčba je individu ální dle hodnot krevního obrazu a snášenlivosti opakovaných feréz, optimální léčba by měla vést k udržování hladiny feritinu v séru pod 50 µg/ l. Při nedostatečném efektu erytrocytoferéz je třeba tuto léčbu kombinovat s podáváním chelátorů.
U anemických nemocných se známkami přetížení železem nelze provádět erytrocytoferézy a základem léčby je podávání chelátorů. V so učasné době jso u na našem trhu dostupné 3 chelatační přípravky, jejich charakteristika je uvedena v tab. 5. Desferi oxamine (Desferal®, Novartis Pharma AG, Švýcarsko) je nejdéle užívaným chelátorem, ale vzhledem k jeho malé resorpci ze střeva a krátkému plazmatickému poločasu je nutné kontinu ální parenterální podávání, což je spojeno s řado u potenci álních nevýhod pro nemocné. Desferal je dnes podáván většino u v 12 – 16hodinové kontinu ální infuzi s.c. či i.v. pomocí přenosné pumpy, v preventivním podávání v dávkách od 2 g/ den, terape utická dávka je výrazně vyšší a dle inici ální hladiny feritinu činí 3 – 8 g/ denně. Desferi oxamine je stále indikován jako lék první řady k odstranění nadbytečného železa u nemocných s anémi í závislo u na podávání transfuzí [16]. Železo je při podávání Desferalu vylučováno močí a částečně i stolicí, k vedlejším účinkům patří především možný vznik anafylaktické re akce. Vzhledem k potížím spojeným s aplikací desferoxaminu jso u již po více než 30 let vyvíjeny perorální chelatační látky. Prvým komerčně dostupným perorálním chelátorem na našem trhu byl deferiprone (Ferriprox®, Apotex Europe Ltd, Velká Británi e). Dle charakteristiky přípravku udané výrobcem je Ferriprox indikován jako lék druhé řady k léčbě přetížení železem u nemocných s β thalasemi í, u nichž je léčba Desferalem kontraindikována či nedostatečná. Preventivní dávka přípravku činí 50 mg/ kg/ den, terape utická dávka je v rozmezí 75 – 100 mg/ kg/ den. Vzhledem k tomu, že poločas deferipronu je 3 – 4 hod, je nutno denní dávku rozdělit na 3 dílčí dávky, železo je při podávání deferipronu vylučováno močí. Deferiprone se ukázal být efektivní u nemocných s β thalasemi í, zejména byl prokázán jeho příznivý účinek na odstranění depot železa z myokardu, což bylo spojeno se signifikantním zlepšením ejekční frakce levé srdeční komory [17]. Nežádo ucím vedlejším účinkem bývají zažívací obtíže spojené s podáváním přípravku, což mnohdy limituje zvyšování dávek na efektivní hodnoty. Nejzávažnějším popsaným nepříznivým efektem při léčbě deferipronem je agranulocytóza, její incidence je 1 – 4 % a zpravidla je reverzibilní po vysazení léku a nasazení granulocytárního růstového faktoru. U thalasemických nemocných s těžkým stupněm přetížení železem se ukazuje jako výhodné so učasné podávání desferi oxaminu, jenž působí na extracelulárně lokalizované železo, a deferipronu, jenž velmi dobře proniká intracelulárně.
Table 5. Srovnání jednotlivých chelatačních přípravků. 
Deferasirox (Exjade®, Novartis PharmaAG, Švýcarsko) je nejnovějším perorálním chelátorem na trhu, dle udání výrobce je deferasirox indikován k léčbě chronického přetížení železem u nemocných s anémi í závislo u na podávání transfuzí u dospělých a dětí starších 2 let. Má poměrně dlo uhý poločas (8 – 16 hod), což umožňuje podávání v 1 denní dávce, železo je po podání deferasiroxu vylučováno stolicí. V našem regi onu jso u k léčbě indikováni zejména nemocní s časnými formami MDS bez nadbytku blastů, aplasticko u anémi í a paroxyzmální noční hemoglobinuri í, preventivní dávka činí 10 – 20 mg/ kg/ den, terape utická dávka je 30 mg/ den, dávky jso u modifikovány dle hladiny feritinu v séru a stupně dependence na transfuzích. Mezi nežádo ucí účinky patří gastro intestinální obtíže, jež moho u být limitující pro podávání léku, vzestup hladiny kre atininu, jenž se většino u stabilizuje po redukci dávky léku a alergické kožní re akce. U nemocných s MDS a těžkým stupněm přetížení železem vedlo ve studi ích dlo uhodobé podávání deferasiroxu k signifikantnímu poklesu hladiny feritinu v séru, k redukci orgánových zásob železa a k normalizaci hodnot labilního plazmatického železa [18]. Nejnovější výsledky ukazují, že u nemocných s MDS může včasná a řádná chelatační léčba ovlivnit i délku přežití nemocných a možná i incidenci transformace do le ukemi e [19]. Proto je u polytransfundovaných anemických nemocných dnes kladen velký důraz na prevenci rozvoje závažného stupně přetížení železem a je doporučováno začít s chelatací již při hodnotách feritinu v séru 1 000 – 1 200 µg/ l a po podání asi 20 – 25 TU erytrocytární masy [20].
doc. MUDr. Jaroslav Čermák, CSc.
www.uhkt.cz
e-mail: cermak@uhkt.czDoručeno do redakce: 4. 5. 2009
Sources
1. Ganz T. Hepcidin in iron metabolism. Curr Opin Hematol 2004; 11 : 251 – 254.
2. Cabantchik ZI, Bre uer W, Zanninelli G et al. LPI - labile plasma iron in iron overlo ad. Best Pract Res Clin Haematol 2005; 18 : 277 – 287.
3. Aji oka RS, Kushner JP. Hereditary hemochromatosis. Semin Hematol 2002; 39 : 235 – 241.
4. Camaschella C, Roetto A, De Gobbi M. Juvenile hemochromatosis. Semin Hematol 2002; 39 : 242 – 248.
5. Ponka P. Rare ca uses of hereditary iron overlo ad. Semin Hematol 2002; 39 : 249 – 262.
6. Nemeth E, Ganz T. Hepcidin and iron- - lo ading anemi as. He amatologica 2006; 91 : 727 – 732.
7. Porter JB. Practical management of iron overlo ad. Br J Haematol 2001; 115 : 239 – 252.
8. Čermák J, Kačírková P, Mikulenková D et al. A prognostic impact of transfusi on dependency on survival of pati ents with e arly myelodysplastic syndrome. Blo od Revi ews 2007; 21: S78.
9. Gattermann N. From sideroblastic anemi a to the role of mitochondri al DNA mutati ons in myelodysplastic syndromes. Lek Res 2000; 24 : 141 – 151.
10. Gutteridge JM, Halliwell B. Iron toxicity and oxygen radicals. Bailli eres Clin Haematol 1989; 2 : 195 – 256.
11. Robson KJH, Merrywe ather - Clarke AT, Po inton JJ et al. Di agnosis and management of haemochromatosis since the discovery of the HFE gene: a Europe an experi ence. Br J Haematol 2000; 108 : 31 – 39.
12. Piperno A. Classificati on and di agnosis of iron overlo ad. Haematologica 1998; 83 : 447 – 455.
13. Taher A, Nathan D, Porter J. Evalu ati on of iron levels to avo id the clinical sequelae of iron overlo ad. Semin Hematol 2007; 44: S2 – S6.
14. St Pi erre TG, Clark PR, Chu a - anusom W et al. Noninvasive me asurement and imaging of liver iron concentrati ons using proton magnetic resonance. Blo od 2005; 105 : 855 – 861.
15. Mavrogeni SI, Markussis V, Kaklamanis L et al. A comparison of magnetic resonance imaging and cardi ac bi opsy in the evalu ati on of he art iron overlo ad in pati ents with beta‑thalassemi a major. Eur J Haematol 2005; 75 : 241 – 247.
16. Hershko CM, Link GM, Konijn AM et al. Iron chelati on therapy. Curr Hematol Rep 2005; 4 : 110 – 116.
17. Olivi eri NF, Brittenham GM, McLaren CE et al. Long‑term safety and effectiveness of iron - chelati on therapy with deferiprone for thalassemi a major. N Engl J Med 1998; 339 : 417 – 423.
18. List AF, Baer MR, Steensma D et al. Iron chelati on with deferasirox (Exjade®) improves iron burden in pati ents with myelodysplastic syndromes (MDS). Blo od 2008; 112 : 236. Abstract 634.
19. Sanz G, Nomdede u B, Sach H et al. Independent impact of iron overlo ad and transfusi on dependency on survival and le ukemic evoluti on in pati ents with myelodysplastic syndrome. Blo od 2008; 112 : 238. Abstract 640.
20. Gattermann N. Overvi ew of guidelines on iron chelati on therapy in pati ents with myelodysplastic syndromes and transfusi onal iron overlo ad. Int J Hematol 2008; 88 : 24 – 29.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2009 Issue Supplementum 1-
All articles in this issue
- Léčba chronického srdečního selhání v interní ambulanci
- Léčba hypertenze u obezity
- Rozdíly mezi muži a ženami u akutního srdečního selhání
- Nová klasifikace Ph negativních chronických myeloproliferativních nemocí v přehledu
- Akutní krvácení z horní části gastro intestinálního traktu
- Přetížení železem – novinky v patogenezi a léčbě
- Léčba chronické myeloidní leukemie (CML) v éře imatinibu
- Maligní lymfomy trávicího traktu
- Současné možnosti diagnostiky a léčby systémové AL-amyloidózy
- Problematika porúch hemostázy pri metabolickom syndróme
- Protrombotický stav pri NAFLD a jeho dôsledky
- Liečba diabetika s ischemickou chorobou srdca
- Zmeny vo funkčnom renálnom náleze po maratónskom behu, po 100-kilometrovom behu a po 24-hodinovom dlhotrvajúcom behu
- Histiocytární choroby
- Diferenciální diagnostika eozinofilie
- Zahraniční styky Československé hematologické společnosti v letech 1951– 1989
- Di abetik, paci ent internisty
- Indikace k vyšetření rizikových faktorů žilní trombózy
- Hemofili e z pohledu vývoje zajištění péče o nemocné
- Dětské nádory metastazující do kostní dřeně a jejich hematologický obraz
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Diferenciální diagnostika eozinofilie
- Přetížení železem – novinky v patogenezi a léčbě
- Histiocytární choroby
- Akutní krvácení z horní části gastro intestinálního traktu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

