-
Medical journals
- Career
Výživa a hydratace u geriatrických pacientů v paliativní péči
Authors: Dana Hrnčiariková
Authors‘ workplace: III. interní gerontometabolická klinika LF UK a FN HK
Published in: Geriatrie a Gerontologie 2021, 10, č. 3: 149-155
Category: Review Article
Overview
Výživa a hydratace hrají v geriatrické paliativní péči klíčovou roli. Malnutrice je ve stáří velmi častá. Progredující kachexie je indikátorem vážné prognózy u geriatrických pacientů v paliativní péči. Včasné zavedení nutriční podpory a hydratace prodlužuje délku života, snižuje komplikace a zvyšuje kvalitu života nemocných v geriatrické paliativní péči. Nutriční podpora v geriatrické paliativní péči má své indikace i kontraindikace, a zejména v terminální péči je nutné postupovat individuálně s ohledem na přání pacienta.
Klíčová slova:
výživa – geriatrický pacient – paliativní péče – perkutánní endoskopická gastrostomie – hydratace – terminální péče – hypodermoklýza
Úvod
Geriatrická paliativní péče je logickým prolnutím dvou medicínských oborů – geriatrie a paliativní péče. Otázka výživy a hydratace je přitom klíčová pro oba obory, neboť poruchy výživy a hydratace mohou být spojeny s horší prognózou a častějším výskytem zdravotních komplikací jak u seniorů, tak u nemocných v paliativní péči. V geriatrii je hodnocení stavu výživy a včasná indikace nutriční podpory (vedle dostatečné fyzické aktivity a aktivizace seniorů) jedním ze zásadních pilířů prevence vzniku syndromu geriatrické křehkosti (frailty). V paliativní péči u onkologických i neonkologických onemocnění je malnutrice spojena s významným váhovým úbytkem a je rizikovým faktorem přechodu onemocnění do terminální fáze. Výživou (a v menší míře i hydratací) můžeme, stejně jako jakoukoli jinou léčbou, nemocnému pomáhat, ale i škodit. Podávání výživy a hydratace je v paliativní, a zejména terminální péči spojeno s mnoha etickými otázkami. Samostatnou kapitolou v geriatrické paliativní péči je otázka indikace a kontraindikace zavedení perkutánní gastrostomie a podávání výživy a hydratace u nemocných v terminálním stavu.
Geriatrická paliativní péče
Paliativní péče je komplexní péče orientovaná na kvalitu života u pacienta, který trpí onemocněním v pokročilém nebo konečném stadiu. Cílem paliativní péče je zmírnit bolest a další tělesná a duševní strádání, při tvorbě plánu péče respektovat pacientova přání a preference, chránit jeho důstojnost a poskytnout podporu jeho blízkým.(1) Významnou provázanost geriatrie a paliativní péče ukazuje mimo jiné i to, že více než 80 % úmrtí v České republice je u lidí v seniorském věku a v určité fázi života se paliativní péče dotýká téměř všech seniorů.(2) Přesto má geriatrická paliativní péče oproti paliativní péči u mladších dospělých nemocných, nebo dokonce dětí svá určitá specifika (tab. 1).
Table 1. Specifika geriatrické paliativní péče 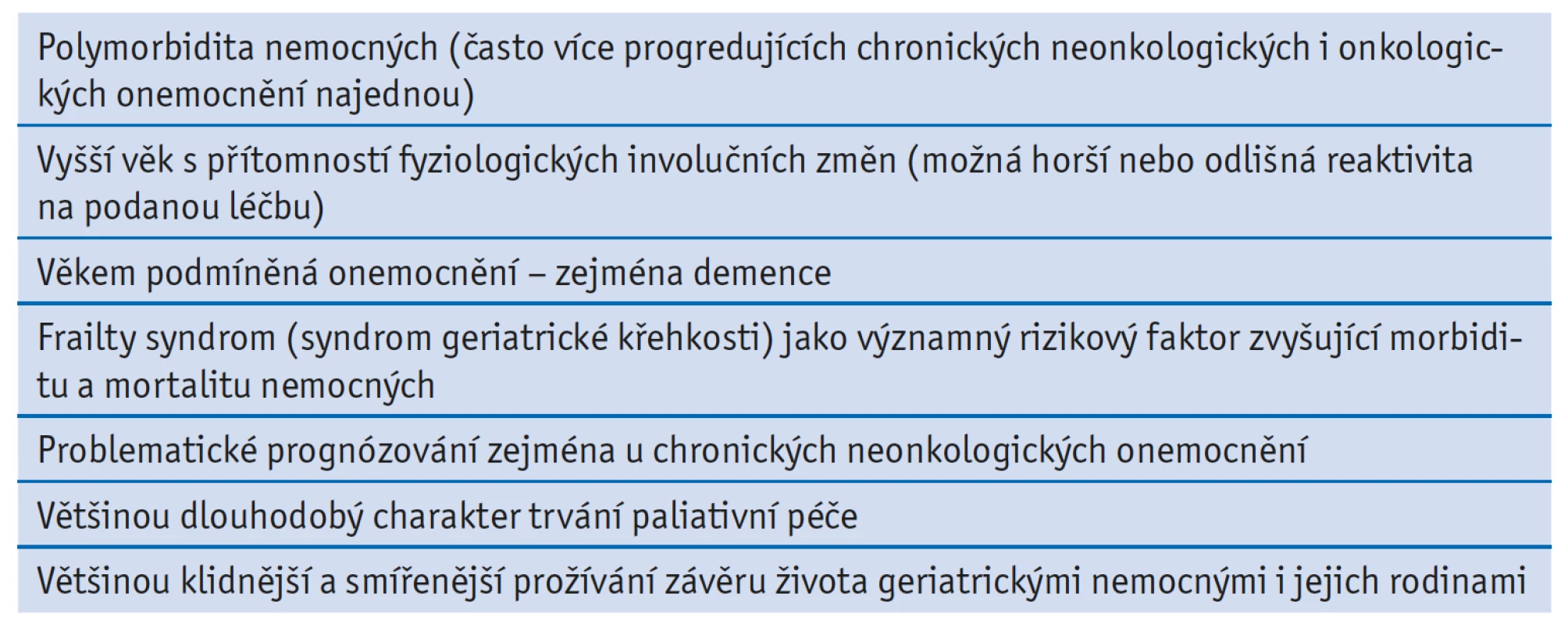
Dle trajektorie umírání lze geriatrické pacienty v paliativní péči rozdělit do 3 skupin: a) onkologicky nemocní, b) nemocní s chronicky progredujícím neonkologickým onemocněním/onemocněními (např. městnavé srdeční selhávání, chronická obstrukční plicní nemoc, renální selhání apod.) a c) nemocní s dlouhodobě nízkou kvalitou života (zejména pacienti s pokročilou demencí). Tyto skupiny se odlišují i délkou trvání paliativní péče – u onkologicky nemocných seniorů se většinou jedná o několik týdnů až měsíců, u nemocných s chronickým onemocněním měsíce až několik let a u seniorů s demencí se délka trvání paliativní péče počítá v řádu let. Vzhledem k polymorbiditě geriatrických pacientů se mohou jednotlivé skupiny vzájemně překrývat.
Indikátorem vážné prognózy u geriatrických pacientů v paliativní péči jsou recidivující delirantní stavy, syndrom terminální geriatrické deteriorace, progredující kachexie, u onkologických onemocnění opakované relapsy při paliativní systémové terapii a generalizace onemocnění.(1)
Etiologie malnutrice v geriatrické paliativní péči
Poruchy výživy jsou ve stáří velmi časté. Ve věku nad 80 let lze nalézt určité projevy podvýživy u téměř všech jedinců, pokročilejší forma malnutrice se ve stáří vyskytuje až v 50 %. Podvýživu lze prokázat u 50 % seniorů v ošetřovatelských ústavech, u 30 % geriatrických pacientů v nemocnicích, ale pouze u 10 % seniorů v domácí péči. Malnutrice ve stáří vzniká nejčastěji kombinací normálních na věku závislých involučních změn a faktorů sociálních, zdravotních (včetně lékových interakcí) a psychologických.(3)
U geriatrických pacientů v paliativní péči, kteří trpí chronickým progredujícím onemocněním často s přítomností interkurentně probíhajícího zánětu různé intenzity, se nejčastěji setkáváme s malnutricí typu kachexie.(4) Speciální subjednotkou této skupiny je syndrom nádorové anorexie a kachexie (CACS). Jedná se o komplexní syndrom charakterizovaný nechutenstvím a nedobrovolnou progresivní ztrátou hmotnosti. Vyskytuje se u více než 80 % pacientů s pokročilým nádorovým onemocněním a rovněž u nemocných s pokročilými formami městnavého srdečního selhání.(1,4)
Kachexie je charakterizovaná ztrátou svalové hmoty velmi často doprovázenou i ztrátou hmoty tukové. Hlavním projevem je váhový úbytek. Kachexie bývá často spojena s fyzickou i psychickou únavou, zhoršením výkonnosti, může vyústit až v apatii a depresi, což významně zvyšuje psychologický stres pacienta i rodiny. Díky poklesu sérových bílkovin dochází ke zhoršování odpovědi organismu na zánětlivé podněty a vyšší náchylnosti k infekcím (zejména respiračním). Progredující kachexie zvyšuje morbiditu a mortalitu geriatrických pacientů. U onkologicky nemocných snižuje možnost podstoupit paliativní onkologickou léčbu, zhoršuje odpověď a toleranci léčby.(1,4,5)
Vybrané parametry hodnocení nutričního stavu
Diagnostika a hodnocení nutričního stavu je součástí základního vyšetření v geriatrii i paliativní péči. Jedná se o komplexní vyšetření nutričního stavu skládající se z nutriční anamnézy, fyzikálního vyšetření s antropometrickým měřením, laboratorního vyšetření a následného zhodnocení tíže nutriční poruchy a rozpoznání příčin malnutrice a faktorů, které ji mohou ovlivňovat.(3,6)
Úkolem nutričního screeningu je včasné, rychlé a spolehlivé odlišení nemocných v riziku malnutrice nebo malnutričních a tvoří úvod do hodnocení nutričního stavu. Nejčastější dotazníky používané při screeningu malnutrice v nemocničním prostředí jsou Mini Nutritional Assessment (MNA), respektive jeho zkrácená verze Mini Nutritional Assessment – Short Form (MNA-SF), dále pak Malnutrition Universal Screening Tool (MUST) a Malnutrition Screening Tool (MST). Všechny mají vysokou senzitivitu i specificitu,(3,4,7) přičemž „zlatým standardem“ je MNA-SF, který lze s úspěchem používat ke screeningu malnutrice i v geriatrické paliativní péči, a to zejména ve fázi časné paliativní péče. U onkologicky nemocných geriatrických pacientů je ke screeningu malnutrice používán jednoduchý Dotazník hodnocení nutričního rizika vypracovaný Pracovní skupinou nutriční péče v onkologii (PSNPO) při České onkologické společnosti ČLS JEP, který lze volně stáhnout na webových stránkách této společnosti, anebo mezinárodní Nutriční rizikový screening 2002 (NRS 2002) v modifikaci pro onkologické pacienty.(1,8)
V nutriční anamnéze je (zejména u onkologicky nemocných) zásadním termínem tzv. významný váhový úbytek, označující neúmyslný pokles hmotnosti o více než 5 % za poslední 3 měsíce nebo o více než 10 % hmotnosti za posledních 6 měsíců (lépe zapamatovatelný je údaj o poklesu hmotnosti o více než 3 kg za poslední 3 měsíce nebo o více než 6 kg za posledních 6 měsíců).(1,4) Závažná je rovněž anamnéza poklesu příjmu potravy pod 50 % běžné porce za poslední týden nebo pod ²⁄³ běžné porce za posledních 14 dnů. U seniorů nelze zapomínat na lékovou a sociální anamnézu. V geriatrii je vhodné v závislosti na kognitivních funkcích nemocného nutriční anamnézu verifikovat od pečující osoby.(1,4,6) U onkologicky nemocných seniorů jsou samostatným indikátorem nutričního rizika tzv. nutričně riziková diagnóza (nádory hlavy, krku a horního GIT, nádory plic, generalizované nádory s celkovými příznaky) a/nebo nutričně riziková léčba (např. emetogenní chemoterapie, radioterapie oblasti dutiny ústní, krku a epigastria).(1) V rámci fyzikálního vyšetření je stále standardem (byť s výhradami, např. malnutriční hypoproteinemická obezita) výpočet a zhodnocení BMI – u seniorů nad 65 let se jako rizikový bere BMI pod 22 kg/m² a na těžkou malnutrici ukazuje BMI pod 20 kg/m².(1,4) Na množství svalové hmoty z běžně dostupných vyšetření lépe ukazuje měření obvodu lýtka nebo paže a na svalovou sílu měření stisku pomocí ručního dynamometru.(4,5) V rozpoznání nutričního rizika obecně platí, že úbytek hmotnosti hodnotí předchozí trend, hodnota BMI hodnotí aktuální stav a nízký příjem stravy předvídá budoucí trend vývoje malnutrice.(1) V laboratorním vyšetření je základem stanovení sérových bílkovin (albumin, prealbumin nebo transferin) v kombinaci s CRP, dobrým indikátorem stavu nutrice a prognostickým faktorem je hodnota celkového počtu lymfocytů.(4,5,6)
Terapie malnutrice v geriatrické paliativní péči
V geriatrické paliativní péči mají své místo všechny typy nutriční podpory (tab. 2). Při rozhodování o nutriční podpoře u geriatrických pacientů s pokročilým nevyléčitelným onemocněním je nutno zohlednit funkční a kognitivní stav nemocného, jeho prognózu, dostupnost aplikačních cest výživy, jejich invazivnost, toleranci pacientem a technické možnosti podávání jednotlivých typů nutriční podpory. Mimo medicínské indikace nutriční podpory je v geriatrické paliativní péči nezbytné zohlednit (a upřednostnit) i přání a preference pacienta a jeho rodiny.(9,10) Nutriční podpora u geriatrických pacientů v paliativní péči je jednoznačně indikována již u nemocných v riziku malnutrice, u onkologicky nemocných v některých případech i preventivně (např. před plánovanými zákroky na horní části GIT). Optimální příjem bílkovin ve stáří je 1,0–1,2 g/kg/den u zdravého seniora (oproti 0,8 g/kg/den u mladšího dospělého), u malnutrice nebo vážných onemocnění se však potřeba bílkovin zvyšuje nad 2 g/kg/den.(10) Problémem zůstává, jak takto vysoký příjem bílkovin zajistit ve stravě seniora v paliativní péči.
Table 2. Fáze vývoje nevyléčitelného onemocnění a indikace nutriční podpory a hydratace 
Základem nutriční podpory je úprava stravovacích návyků, dietní doporučení a nutriční doplňky ve formě sippingu. Enterální sondová a parenterální výživa jsou indikovány zejména v časnějších fázích geriatrické paliativní péče, u nemocných s delší prognózou, tam, kde podání výživy přináší klinický efekt ve smyslu zmírnění váhového úbytku, snížení obtěžující symptomatologie (např. neklid, stavy zmatenosti), zvýšení kvality života a psychického zklidnění nemocného.(9,11,12)
U geriatrických pacientů v onkologické paliativní péči tvoří zvláštní skupinu chuťová stimulancia vedoucí k farmakologickému ovlivnění malnutrice. Nejúčinnějším lékem této skupiny je megestrol acetát, syntetický gestagenní hormon s potvrzeným účinkem na zlepšení chuti k jídlu, zvýšení tělesné hmotnosti, zmírnění únavy a nevolnosti. Nebyl prokázán vliv na dobu přežití nemocných, ale zvyšuje kvalitu jejich života. Kortikosteroidy nebývají samy o sobě v geriatrické paliativní péči nasazovány k ovlivnění anorexie, ale mají příznivý vliv na chuť k jídlu jako vedlejší účinek při jejich indikaci k ovlivnění otoků, zvracení a bolesti.(1,8,11–14)
V geriatrické paliativní péči je třeba zvláštní péči věnovat úpravě medikace, která sama o sobě může mít jako vedlejší efekt zvýšení chuti k jídlu. Na jedné straně je důležitá redukce veškeré zbytné medikace (zejména v terminální péči), ale na straně druhé má zcela zásadní význam účinné medikamentózní tlumení všech nežádoucích negativních projevů základního onemocnění (terapie bolesti, dušnosti, deprese, nauzey a zvracení, zácpy, suchosti a zánětu v dutině ústní).(1,11) Rovněž udržení přiměřené fyzické aktivity během dne sekundárně pomáhá ke zlepšení chuti k jídlu a současně je prevencí ztráty svalové hmoty.(1,8)
Indikace nutriční podpory a hydratace
Indikace nebo omezení nutriční podpory a hydratace v geriatrické paliativní péči vychází z jednotlivých fází vývoje progredujícího chronického nevyléčitelného onemocnění a musí být pravidelně přehodnocována s postupným vývojem stavu onemocnění u konkrétního pacienta.(11) Jednotlivé fáze vývoje onemocnění ve vztahu k indikaci nutriční podpory a hydratace ukazuje tabulka 2.
Obecně pro indikaci nutriční podpory v paliativní péči platí, že je třeba volit individuální přístup ke každému pacientovi, přínos nutriční podpory musí převyšovat její rizika, podpůrná perorální léčba a edukace pacienta nepostačují k udržení nutričního stavu nebo se jedná o hrozící nebo již rozvinutou malnutrici a pacient s navrhovanou nutriční podporou souhlasí nebo si ji přeje. Cílem nutriční podpory v paliativní péči je zmírnění úbytku tělesné hmotnosti, zmírnění ztráty výkonnosti a zvýšení kvality života nemocného.
Problematika zavedení PEG
V případě úvah o zavedení perkutánní endoskopické gastrostomie (PEG) v geriatrické paliativní péči lze vycházet z doporučených postupů České gastroenterologické společnosti ČLS JEP z roku 2019.(15) Cílem zavedení PEG by mělo být zlepšení stavu výživy, kvality života a komfortu pacienta při tolerovatelné míře rizika komplikací spojených s výkonem. Obecně lze o zavedení PEG uvažovat při předpokládané době trvání poruchy příjmu potravy delší než 3–4 týdny, ale v geriatrické paliativní péči je zásadní zohlednit rovněž celkový zdravotní stav nemocného, základní diagnózu a zejména prognózu onemocnění (očekávaná doba přežití by měla být delší než 6 měsíců), vliv zavedení gastrostomie na kvalitu života nemocného a jeho přání, pokud je známo.(15) Indikace a kontraindikace zavedení PEG v geriatrické paliativní péči ukazuje tabulka 3.
Table 3. Indikace a kontraindikace zavedení PEG v geriatrické paliativní péči 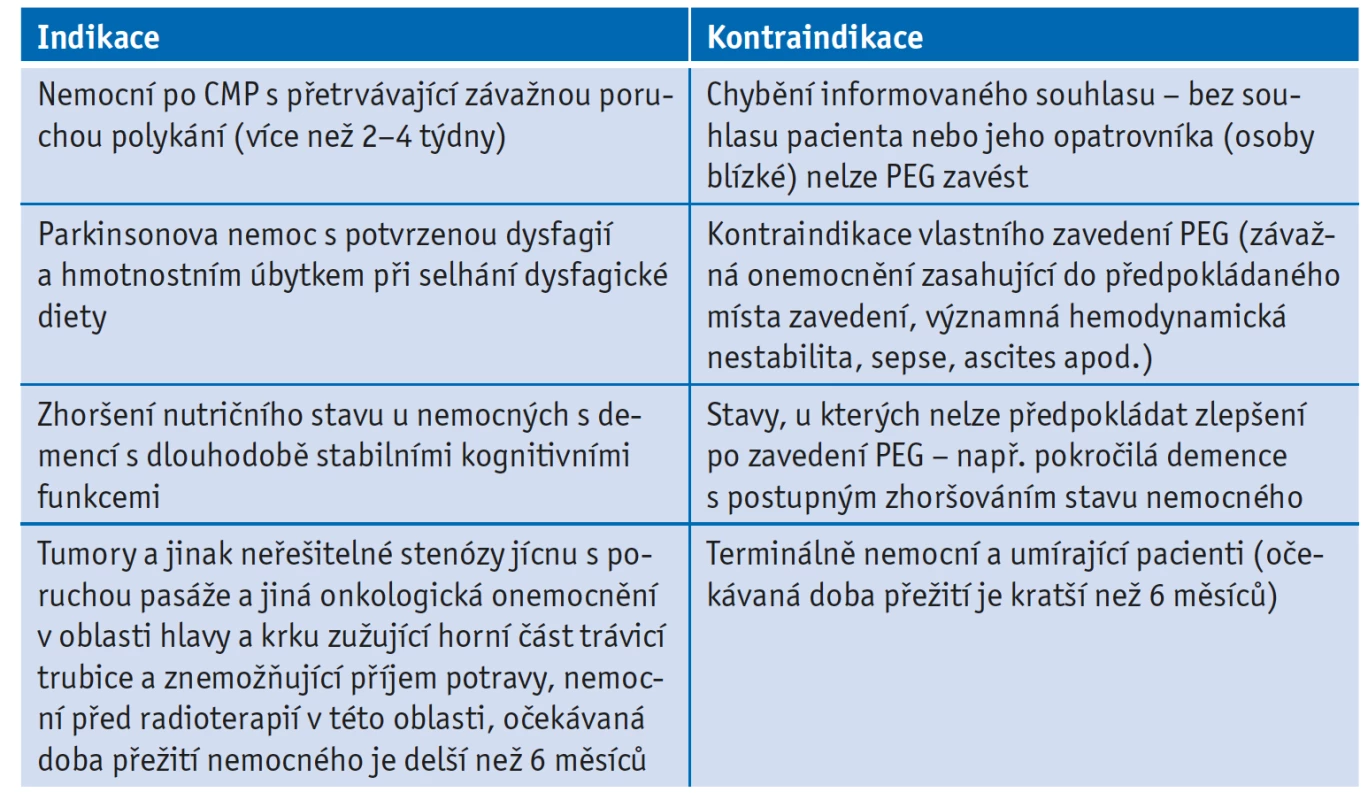
Nejčastější etický problém zavedení PEG v geriatrické paliativní péči je spojen s diagnózou demence. U pacientů s pokročilou demencí nebyl prokázán pozitivní efekt zavedení PEG na kvalitu jejich života a celkové přežití.(15–19) Faktory významně zhoršující přežití po zavedení PEG u geriatrických pacientů byly vyšší věk (nad 75 let), malignita a nízká hladina albuminu.(13,15) U těchto nemocných je k eventuálnímu zavedení PEG nutno postupovat přísně individuálně a spíše maximálně zdrženlivě. Vždy je potřeba brát v úvahu celkový funkční stav nemocného, vliv zavedení PEG na kvalitu jeho života, předpokládanou prognózu (délku přežití), a zejména přání nemocného a jeho rodiny.(10,11) V případě akutního zhoršení stavu nemocného s pokročilou demencí (např. při současně probíhajícím zánětlivém onemocnění) je nutné spolu s kauzální léčbou zajistit i dostatečný příjem živin – při nedostatečném příjmu per os je u těchto nemocných vhodnější parenterální výživa než enterální sondová výživa (invazivnější, hůře snášená, časté extrakce pacientem). O zavedení PEG lze uvažovat po odléčení akutního stavu, pokud při podávání výživy dochází k vylepšování celkového stavu, nutričních parametrů, kognitivních funkcí a trvá porucha příjmu potravy. V případě postupného zhoršování celkového stavu nemocného není zavedení PEG indikováno.(15)
Hydratace v geriatrické paliativní péči
Ve vyšším věku postupně klesá pocit žízně a obecně se snižuje perorální příjem tekutin, což zvyšuje riziko vzniku dehydratace. K dehydrataci u seniorů dochází vznikem nepoměru mezi příjmem tekutin a jejich výdejem. Nejčastějšími příčinami zhoršeného příjmu tekutin ve stáří jsou snížení pocitu žízně, nechutenství, nevolnost, polykací obtíže, pseudobulbární syndrom po proběhlé cévní mozkové příhodě, demence, deprese, zmatenost. Zvýšený výdej tekutin může být zapříčiněn zvracením, průjmy nebo vyšším užíváním diuretik. Dehydratace u geriatrických pacientů se nejčastěji projevuje ortostatickou hypotenzí až kolapsovými stavy, zvýšenou únavností a psychickým útlumem vedoucím až k poruše vědomí nebo naopak stavy zmatenosti a delirii.(3,6,11,21) Diagnostika dehydratace u seniorů může být problematická, kožní turgor bývá ovlivněn změněnou elasticitou kůže nebo vymizením podkoží u malnutrice, více vypovídající je sledování vlhkosti bukální sliznice (zde pozor na časté dýchání pacientů ústy a jeho vliv na osychání sliznic bez ohledu na stav hydratace), nejvíce vypovídající je údaj o nízkém příjmu tekutin (nejlépe objektivizovaný druhou osobou), na dehydrataci může upozornit také tmavší zbarvení moče, v laboratorním vyšetření pak vyšší osmolalita plazmy, zvýšení urey nebo natria.(3,6,10)
U seniorů v domácím prostředí s lehkou dehydratací lze stav vyřešit dohledem nad vyšším příjmem tekutin a jejich aktivním nabízením. Tekutiny je třeba nabízet častěji, v menším množství a střídat různé druhy nápojů.(9,10) U významnější dehydratace a při rozvoji klinických projevů spojených s dehydratací je metodou volby podání rehydratačních infuzí v domácím nebo nemocničním prostředí.(10) Hydratace ve formě podávání intravenózních anebo subkutánních infuzních roztoků má v geriatrické paliativní péči své nezastupitelné místo, ale jako léčebný prostředek má své indikace i omezení, a to zejména v terminální péči (tab. 2). Enterální sondové podání tekutin cestou nazogastrické, nazojejunální sondy nebo perkutánní gastrostomie je v paliativní péči minoritní pro svoji invazivnost, horší snášenlivost nemocnými a užívá se pouze tam, kde má nemocný již zavedenu sondu z jiné indikace.(11)
Subkutánní hydratace (hypodermoklýza)
Hypodermoklýza je podávání tekutin subkutánně při nemožnosti nebo nevhodnosti i.v. vstupu, kdy dochází k postupné resorpci tekutiny z podkoží. Tento způsob podávání infuzních roztoků a léků je velmi často používán v mobilní i lůžkové paliativní péči a na geriatrických odděleních u paliativních, a zejména terminálních pacientů, kde není možné zajistit periferní žilní vstup. Nejčastějšími lokalitami pro podání s.c. je přední strana hrudníku nebo břicha, eventuálně lze použít podkoží paží nebo stehen. Podkožní jehlu je možné ponechat 3–5 dní a místa vpichu je potřeba střídat.(11,20)
Hypodermoklýzou lze podat izotonické roztoky, F1/1, F1/2, kombinované roztoky NaCl a glukózy, G5%, KCl do koncentrace 20–40 mmol/l. Nejčastěji se používá kontinuální 24hodinová infuze (rychlost podání 40–60 ml/h), další obvyklé způsoby podání jsou 10hodinová infuze přes noc (rychlost podání 80 ml/h), dvouhodinová infuze 500 ml tekutiny 2–3× denně. Subkutánně se v paliativní péči podává obvykle 500–2000 ml tekutin/den, nejvyšší doporučená denní dávka s.c. je 3000 ml – 2× 1500 ml paralelně dvěma vstupy.(9,11,20,21)
Při aplikaci hypodermoklýzy je třeba se vyhýbat místům s poškozenou kůží, jizvením, otoky, oblastem po předchozí radioterapii, polovině hrudníku, kde byla provedena mastektomie nebo místům v okolí stomie. Komplikace subkutánního podání nejsou časté. V místě vpichu může dojít k lokální iritaci kůže, zánětu v okolí jehly nebo vytvoření hematomu. Kontraindikací podání hypodermoklýzy je těžká trombocytopenie (pod 30 × 109), těžké poruchy koagulace se spontánní tvorbou hematomů, extrémní kachexie nebo naopak generalizované edémy.(11,20)
Etické aspekty výživy a hydratace v terminální péči
V terminální péči je třeba odlišit pojem terminální stadium (fáze) postupně progredujícího chronického nevyléčitelného onemocnění a terminální stav (umírání). Terminální stadium onemocnění s sebou nese častější akutní dekompenzace onemocnění, postupné zhoršování jednotlivých symptomů a snižování terapeutických možností toto onemocnění ovlivnit. Prognóza nemocného může být i několik měsíců.(9) V terminálním stavu dochází k nevratnému selhání jednoho nebo více životně důležitých orgánů, které končí úmrtím pacienta během několika hodin nebo dnů.(1,8) Rozpoznání terminálního stadia onemocnění je jednodušší v případě onkologických onemocnění, v případě polymorbidních geriatrických pacientů trpících často současně několika postupně progredujícími chronickými nevyléčitelnými chorobami může být rozpoznání již nevratného orgánového selhání a určení prognózy nemocného složitější.(11)
Prioritou terminální péče je umožnit pacientovi klidný a důstojný závěr života. Cílem léčby a péče by mělo být mírnění tělesných a psychických obtíží a zachování co nejlepší možné kvality života.(1,4,8,11) Je třeba přehodnotit dosavadní diagnostické a terapeutické postupy a ukončit ty, které nepřispívají ke komfortu pacienta nebo uměle prodlužují proces umírání.
V případě nutriční podpory je potřeba postupovat přísně individuálně s ohledem na přání a preference pacienta. V posledních 2 měsících života pacienti chřadnou nezávisle na podávání výživy. Sondová enterální ani parenterální výživa nemá významný vliv na délku života pacienta. Nutriční podpora by měla zlepšit kvalitu života, přispět k emočnímu zklidnění pacienta, ale neprodlužovat utrpení a délku umírání. V terminálním stavu pacient obvykle nemá hlad ani žízeň a není zde indikována nutriční podpora ani sledování nutričního stavu, ale současně je potřeba bránit absolutnímu vyčerpání energetických substrátů a mučivé žízni způsobující silné nociceptivní podněty srovnatelné s bolestí či dušením.(1,13)
Ve spolupráci s pacientem a jeho rodinou je nutné se zohledněním indikací a kontraindikací nutriční podpory vybrat nejvhodnější formu, která by byla pro pacienta přínosem a ne zátěží. Perorální výživa je metodou volby. Pokud je nemocný schopen přijímat per os, je vhodné v tom pokračovat.(10,11) Základem nutriční podpory je úprava stravovacích doporučení, v terminální péči neplatí žádná dietní omezení.(1,9) Dle stavu pacienta se postupně přechází od pevné stravy přes kašovitou až k tekuté, v terminálním stavu postačí pouze svlažování dutiny ústní. Vhodnější jsou spíše chlazené potraviny než teplé a menší porce jídla s častější frekvencí. Je snaha omezit intenzivní vůně stravy. Úprava medikace s vysazením všech postradatelných léků a aktivní léčba symptomů (zejména bolesti, nevolnosti a zácpy) může rovněž přispět ke zvýšení perorálního příjmu.(1,13)
K enterální výživě v terminální péči je potřeba přistupovat velmi rezervovaně. Pacienti v terminálním stadiu onemocnění většinou dobře tolerují popíjení vychlazeného sippingu. Zavádění nazogastrické, nazojejunální sondy ani PEG není v terminální péči indikováno. V případě již zavedeného PEG je možné po dohodě s pacientem a jeho rodinou tento vstup využít k podávání léků a tekutin, podávání enterální výživy je vhodné postupně redukovat a v terminálním stavu vysadit. K zachování podávání výživy (v redukované dávce) přistupujeme pouze, pokud by její vynechání pacient nebo rodina vnímali jako omezení kvality života nemocného, který je na tento způsob výživy dlouhodobě zvyklý. Stejné pravidlo platí i pro parenterální výživu. V terminálním stavu není její podávání medicínsky odůvodněné s výjimkou toho, že její podání zlepšuje kvalitu života pacienta, přispívá ke zmírnění jeho obtíží nebo pokud by její odnětí nemocný vnímal negativně.(10,11,13)
Zvláštní kapitolou je podávání tekutin v terminální péči. I když nemocný v terminálním stavu většinou nechce nic jíst, může mít potřebu pít. Podávání tekutin per os je nutné zajistit způsobem, který pacient zvládne (slámkou, lahvičkou, po lžičkách), a pokud již není schopen polykat, pak k dobrému komfortu nemocného přispívá zvlhčování úst nebo cucání kostiček ledu. Podávání infuzních roztoků krystaloidů v terminálním stavu je velmi diskutované téma. Je potřeba postupovat přísně individuálně s ohledem na přání pacienta a s respektem k přání jeho rodiny. Podávání infuzí na rozdíl od zvlhčování dutiny ústní netlumí pocit žízně. Vhodná je postupná redukce již podávaných tekutin na 500–1000 ml krystaloidů za 24 hodin i.v. nebo s.c. Tato tzv. bazální hydratace se ve většině případů ponechává do úmrtí pacienta. Úplné vysazení parenterální hydratace je nutné, pokud podávané tekutiny zhoršují kvalitu života nemocného nadměrným zahleněním, zhoršením dušnosti nebo otoků při přetížení krevního oběhu.(1,13,21)
V terminální péči jsou otázky, zda podat, nebo nepodat nutriční podporu a hydrataci, pokračovat, nebo nepokračovat v již zavedené nutriční podpoře a hydrataci a kdy ji ukončit, velmi klíčové. V komunikaci s pacientem a jeho rodinou je třeba zvážit, zda přínos podávání výživy a hydratace je větší než zátěž s tím spojená, zda podávání nutriční podpory a hydratace zlepší kvalitu života terminálně nemocného pacienta a vede k jeho emočnímu zklidnění, nebo zvyšuje zatížení organismu a zhoršuje utrpení nemocného.(13)
Závěr
Výživa a hydratace hrají v geriatrické paliativní péči zásadní úlohu a jsou nedílnou součástí komplexní podpůrné péče geriatrických pacientů s chronickým nevyléčitelným onemocněním. Včasné zahájení nutriční podpory má pozitivní vliv na délku života, snižuje komplikace onemocnění a významně zvyšuje kvalitu života pacientů. Nutriční podpora a hydratace mají v geriatrické paliativní péči své indikace, ale také omezení, a to zejména v závěru života.
Korespondenční adresa:
MUDr. et Mgr. Dana Hrnčiariková, Ph.D.
III. interní gerontometabolická klinika LF UK
a FN HK
Sokolská 581, 500 05 Hradec Králové
e-mail: danahrnciarikova@seznam.cz
MUDr. et Mgr. Dana Hrnčiariková, Ph.D.
Studium na LF UK v Hradci Králové ukončila v roce 2001. Od promoce pracuje na III. interní gerontometabolické klinice FN HK. Získala atestace v oboru vnitřní lékařství, geriatrie a paliativní medicína. V roce 2014 absolvovala magisterské studium na katedře teologické etiky a spirituální teologie Katolické teologické fakulty Univerzity Karlovy v Praze. Je členkou výboru České gerontologické a geriatrické společnosti a vedoucí Sekce geriatrické paliativní péče České společnosti paliativní medicíny ČLS JEP. Je geriatrem zaměřeným na výživu a paliativní péči ve stáří.
Sources
- Kiss I, et al. Modrá kniha České onkologické společnosti. 27. vyd. Brno: KAPCZ 2021.
- Topinková E. Geriatrická paliativní péče a péče o umírající. Česká geriatrická revue 2004; 1 : 14–21.
- Kalvach Z, Zadák Z, Jirák R, et al. Geriatrie a gerontologie. Praha: Grada 2004.
- Vágnerová T a kol. Výživa v geriatrii a gerontologii. Praha: Karolinum 2020.
- Zadák Z. Výživa v intenzivní péči. 2.vyd. Praha: Grada 2008.
- Vágnerová T, Klímová E. Standard nutriční péče v geriatrii. Obecné principy nutriční péče. Geri a Gero 2020; 9 (1): 44–52.
- Vágnerová T, Kušniriková I. Standard nutriční péče v geriatrii. Nutriční screening a proces péče. Geri a Gero 2021; 10 (1): 41–51.
- Tomíška M. Výživa onkologických pacientů. Praha: Mladá fronta 2018.
- Kabelka L. Geriatrická paliativní péče a komunikace o nemoci. 2. vyd. Praha: Mladá fronta 2018.
- Volkert D, Beck AM, Cederholm T, et al. ESPEN guideline on clinical nutrition and hydration in geriatrics. Clin Nutr 2019; 38 : 10–47.
- Sláma O, Kabelka L, Vorlíček J, et al. Paliativní medicína pro praxi. Praha: Galén 2007.
- Šachtová M, Tomíška M, Sláma O. Doporučené postupy nutriční péče u pacientů v onkologické paliativní péči: Stanovisko pracovní skupiny pro výživu České společnosti paliativní medicíny ČLS JEP. Praha: Ambit Media 2012.
- Hrnčiariková D, Hrnčiarik M, Jurašková B, et al. Nutriční podpora v terminální péči. Klin Farmakol Farm 2007; 21(2): 62–66.
- Sochor M, Závadová I, Sláma O, et al. Paliativní péče v onkologii. Praha: Mladá fronta 2019.
- Kroupa R, Kohout P, Cyrany J, et al. Perkutánní endoskopická gastrostomie – doporučený postup České gastroenterologické společnosti ČLS JEP. Gastroent Hepatol 2019; 73(3): 195–207.
- Mitchell SL, Tetroe JM. Survival after percutaneous endoscopic gastrostomy placement in older persons. J Gerontol A Biol Sci Med Sci 2000; 55(12): M 735–739.
- Kianička B, Žák J, Bareš M. Využití perkutánní endoskopické gastrostomie – přehled indikací, popis techniky a současné trendy v neurologii. Cesk Slov Neurol N 2012; 75/108(2): 165–169.
- Candy B, Sampson EL, Jones L. Enteral tube feeding in older people with advanced dementia: findings from a Cochrane systematic review. Int J Palliat Nurs 2009; 15(8): 396–404
- Sampson EL, Candy B, Jones L. Enteral tube feeding for older people with advanced dementia. Cochrane Database Syst Rev 2009; 2: CD007209.
- Marková A, et al. Hospic do kapsy. Praha: Cesta domů 2009.
- Vorlíček J, Adam Z, Pospíšilová Y, et al. Paliativní medicína. 2. vyd. Praha: Grada 2004.
Labels
Geriatrics General practitioner for adults Orthopaedic prosthetics
Article was published inGeriatrics and Gerontology

2021 Issue 3-
All articles in this issue
- Editorial
- Očkování u seniorů – nejen SARS-CoV-2 vakcinace
- Antikoagulační terapie – známe její interakce?
- Efektivní řešení chronické bolesti může zlepšit kvalitu života i complianci starších nemocných
- Současné možnosti léčby klostridiové kolitidy a výhled do budoucnosti
- Výživa a hydratace u geriatrických pacientů v paliativní péči
- Point of Care Ultrasound (POCUS) v geriatrii se zaměřením na dehydrataci
- Sociální charakteristiky akutně hospitalizovaných seniorů a dynamika jejich změn během 25 let na geriatrii
- Analýza vývoje invalidity pro duševní onemocnění a kritérií invalidity
- Spolupráce lékaře a logopeda v komplexní péči o pacienty – naše zkušenosti z Centra následné péče FN Motol
- Představení nového pracoviště – Geriatrické interní kliniky 2. LF UK a FN Motol
- Zpráva o činnosti konziliárního týmu paliativní péče v dospělé části FN Motol
- Geriatrics and Gerontology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Současné možnosti léčby klostridiové kolitidy a výhled do budoucnosti
- Výživa a hydratace u geriatrických pacientů v paliativní péči
- Antikoagulační terapie – známe její interakce?
- Spolupráce lékaře a logopeda v komplexní péči o pacienty – naše zkušenosti z Centra následné péče FN Motol
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


