-
Medical journals
- Career
Akutní a pozdní komplikace diabetu – představují významný problém ve vyšším věku?
Authors: P. Weber; H. Meluzínová; D. Prudius; K. Bielaková
Published in: Geriatrie a Gerontologie 2016, 5, č. 4: 196-201
Category: Review Article
Overview
Diabetes mellitus (DM) představuje zásadní rizikový faktor pro vznik akutních i rozvoj pozdních diabetických komplikací. DM může být vnímán do určité míry i jako model stárnutí. Ve vyšším věku je často součástí polymorbidity a podílí se na mozaice současně se vyskytujících chorob. Terapie sama o sobě při užití inzulinů nebo inzulinových sekretagog (orální antidiabetika – sulfonylurea atp.) může pro seniory znamenat obzvláště významné riziko hypoglykemie, která může vést k rozvoji dalších akutních cévních komplikací (iktus, infarkt, arytmie apod.). Autoři nastiňují i další akutní a chronické pozdní komplikace, zejména pod zorným úhlem velké heterogenity seniorské populace.
Klíčová slova:
diabetes – stáří – akutní a pozdní komplikace – managementÚvod
Diabetes mellitus (DM) postihuje v 7. dekádě až 20 % osob a dalších 20 % má porušenou glukózovou toleranci(1, 2). Ve stáří (zejména pozdním) jde převážně o DM 2. typu (nad 70 roků až 95 %)(3, 4). Za vznik DM2 jsou zodpovědné zejména: 1. inzulinová rezistence (porucha účinku inzulinu při jeho relativním dostatku v oběhu); 2. porucha inzulinové sekrece (defekt B-buněk). DM2 ve stáří je důsledkem interakcí genetické predispozice a vlivů zevního prostředí(5). Podstatné pro vznik DM2 mohou být špatné stravovací návyky, převážně sedavý způsob života s nedostatkem pohybu, stres, úbytek svalové hmoty a nárůst abdominální obezity. Skupina starších diabetiků bude nesmírně heterogenní(6). Na jedné straně bude většinová skupina osob, kde DM2 bývá zjištěn až po 50. roce života (převážně jedinci v 6. až 8. dekádě bez odpovídajících orgánových komplikací), a na straně druhé budou diabetici 1. typu s trváním DM několika desítek roků a pokročilými orgánovými komplikacemi, LADA, jedinci s vyhaslou inzulinovou sekrecí nebo dokonce s T1DM vzniklým ve vysokém věku. Někteří budou plně kompliantní a schopní zvládat management své nemoci a nároky kladené na ně stran kompenzace se nebudou zásadně lišit od diabetiků středního věku(7). Jiní senioři kvůli kognitivní dysfunkci, zrakovému či jinému závažnému onemocnění nebo handicapu budou mít adherenci k dietním, režimovým i léčebným opatřením nízkou. Někteří mohou být těžce disabilní nebo ve finální fázi svého života(8). Přístup lékaře ke starším diabetikům musí chápat tuto extrémní heterogenitu seniorské diabetické populace a management choroby u nich musí být důsledně individualizován(9). Musí plně respektovat, a zejména umět interpretovat skutečnosti jako trvání diabetu, přítomnost komplikací a komorbidit, šanci dožití, pacientovy preference a funkční způsobilost(10). U seniorů ve srovnání s mladšími mohou vystupovat do popředí zřetelněji:
- nižší schopnost rozpoznání hypoglykemie a provádění self-monitoringu
- významné komorbidity, které omezují seniorovu nezávislost
- polyfarmakoterapie
- častý výskyt syndromu stařecké křehkosti a omezená délka života
- horší sociálně-ekonomická situace
- větší sociální izolace a osamělost
- vyšší potřeba dopomoci a závislost na rodině, pečovatelích atp.
Klinický obraz
DM2 může být dlouhou dobu zcela asymptomatický nebo se manifestovat projevy postupně se rozvíjející hyperglykemie (polydipsie, polyfagie, polyurie), hyperosmolárního neketoacidotického kómatu (HONK) nebo pozdními komplikacemi DM. Ve stáří se projevy hyperglykemie nejednou mohou skrývat pod obrazem deprese, kognitivních poruch (včetně demence), pádů, močové inkontinence, letargie, únavy, chronické bolesti nebo nevysvětlitelného hubnutí(2, 3).
I když bude glykemie vyšší, glukóza se v seniu nemusí dostat do moči, protože s věkem stoupá renální práh pro glukózu. Pitný režim se ve stáří obecně spíše zhoršuje a pocit žízně bývá naopak porušený až zcela vymizelý. Pokud je přítomna ve stáří u DM nějaká symptomatologie, bývá obvykle spíše atypická, mohou ji maskovat přítomné velké geriatrické syndromy (instabilita, imobilita, inkontinence, intelektové poruchy jako demence, deprese, delirium aj.).
Zjištění hyperglykemie a diabetu ve stáří může být nejednou náhodnou záležitostí, kdy je senior ambulantně vyšetřován nebo hospitalizován ze zcela jiných důvodů, než jsou symptomy případné hyperglykemie (stresová reakce v situacích, jako je úraz, operace, závažné akutní onemocnění – sepse, horečnatá onemocnění obecně, infarkt myokardu, iktus a jiné akutní stavy)(11).
Akutní komplikace
Z akutních komplikací DM se můžeme u starších diabetiků vedle méně častého diabetického ketoacidotického kómatu (DKK) setkat především s hyperosmolárním neketoacidotickým kómatem (HONK) a hypoglykemií. Postup léčby u nich bude obdobný jako u mladších jedinců, ale závažnost, důsledky a mortalita budou u starších diabetiků podstatně vyšší. Tyto tři možné komplikace představují život ohrožující poruchy glukózového metabolismu. Jejich možný vznik by měl být zvažován diferenciálnědiagnosticky u všech osob s mentální deteriorací, neurologickým deficitem a obecně v kritickém stavu. Hladiny glykemií u seniorů nediabetiků oscilují během dne okolo 5 mmol/l s tím, že nalačno neklesají pod 3 mmol/l a postprandiálně obvykle nepřesahují 9 mmol/l. Možná rizika rozvoje hypoglykemie v akutní i chronické situaci přehledně zachycuje tabulka 1.
Table 1. Příčiny zvýšeného rizika hypoglykemie ve stáří 
Naopak rizika rozvoje těžké hyperglykemie ve stáří až s možností postupného vzniku HONK uvádí přehledně tabulka 2.
Table 2. Příčiny těžké hyperglykemie až hyperosmolárního kómatu v seniu 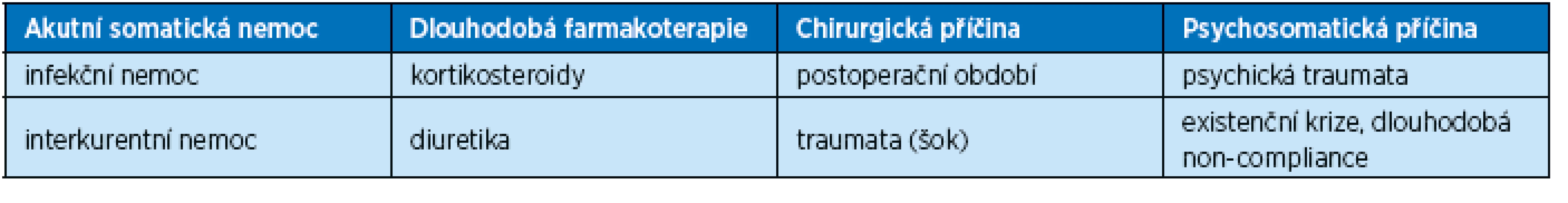
Hypoglykemie
Ačkoli hypoglykemie sama o sobě může být do určité míry průvodním jevem těsné kompenzace diabetu a důsledkem léčby inzulinem nebo perorálními antidiabetiky – PAD (sulfonylurea – SU, glinidy), jde o jakousi uměle navozenou dysbalanci mezi hladinou inzulinu a pro tkáně dostupnou glukózou (glykemií)(12, 13). Sako(14) poukazuje na potřebu důsledné individualizace terapie a pravidelných kontrol zejména při terapii velmi starých diabetiků. Sanchai(15) klade vysoký věk na první místo mezi rizikovými faktory těžké hypoglykemie u seniorů diabetiků léčených inzulinem. Ve stáří je pokles glykemie nebezpečný především pro mozkové buňky, neboť ty používají glukózu jako hlavní zdroj energie. Mozek neumí glukózu jako energetický zdroj skladovat, a proto spotřebuje více než polovinu glukózy vydané játry do cirkulace. Komplex neuroendokrinních změn, jež se mohou objevit, je velmi rizikový zejména ve vyšším věku.
Hypoglykemie jako taková je spíše termín biochemický než klinický. Obvykle je spojována s hodnotou glykemie pod 3,5–3,9 mmol/l. Snaha jakkoli ji definovat jen na biochemickém podkladě (hodnota glykemie) vyznívá nejednoznačně a kontroverzně. U starších jedinců (zejména nad 75–80 roků) se ovšem její příznaky mohou objevit i při vyšších hodnotách krevního cukru (5–6 mmol/l). Syndrom hypoglykemie(1, 2) představuje komplex neuroendokrinních změn, kdy dochází k aktivaci kontraregulačních hormonů a obvykle i požití glycidů (pocit hladu). Pro mnohé diabetiky, a především starší a osaměle žijící diabetiky patří hypoglykemie k velmi obávaným a závažným rizikům terapie diabetu. Cíl dosažení optimální euglykemie u dlouhodobě léčených seniorů by měl být vyhrazen skupině mladších seniorů a u starších jen těm, kteří jsou po ostatních stránkách ze skupiny tzv. „fit seniorů“. U ostatních, zejména polymorbidních a na polyfarmakoterapii s četnými riziky lékových interakcí, budeme více liberální na těsnou kompenzaci a hlavním cílem bude eliminace případných hypoglykemií. Tabulka 3 uvádí riziková farmaka, která mohou akcentovat cestou lékových interakcí velmi podstatně rozvoj hypoglykemie při terapii sulfonylureou.
Table 3. Sulfonylurea (SU) – lékové interakce způsobující hypoglykemii 
Klinický obraz hypoglykemie je dán Whippleovou triádou(3, 4). V zásadě může být symptomatická nebo asymptomatická. Jako mírná hypoglykemie bývá označována taková, kterou diabetik rozpozná a zvládne sám, aniž by to nějak narušilo jeho každodenní režim. Jako těžká hypoglykemie (podle Diabetes Control and Complications Trial – DCCT) bývá označována ta, kdy symptomy jsou takové, že jejich řešení již sám pacient nezvládne a vyžaduje pomoc jiné osoby nebo ambulantní ošetření či hospitalizaci.
Symptomy tvoří příznaky vyvolané aktivací autonomního nervového systému (pocení, palpitace, třes, hlad, bledost aj.) a příznaky z neuroglykopenie – nespecifické centrální příznaky (zmatenost, únava, slabost, poruchy řeči, zraku atp.).
Asymptomatickou hypoglykemii, která představuje laboratorní nález nižší glykemie bez průvodních příznaků, zjišťujeme především u nemocných léčených inzulinem (zejména na intenzifikovaném inzulinovém režimu) při terapii PAD (perorální antidiabetika – inzulinová sekretagoga). Přítomnost asymptomatické hypoglykemie by měl ošetřující lékař zvažovat u staršího diabetika na inzulinu nebo PAD vždy, pokud uvádí v anamnéze závratě, epizody zmatenosti, návalů, neurologické příznaky nebo má aktuálně nízký glykovaný hemoglobin. Ve stáří (především pozdním) vztah mezi symptomy a nízkou glykemií nebývá těsný. Málo specifické příznaky hypoglykemie mohou být mylně interpretovány jako delirium nebo TIA. Při každé ambulantní kontrole léčeného diabetika je třeba aktivně pátrat po hypoglykemii a při podezření na ni snížit či upravit dávkování perorálního antidiabetika nebo inzulinu.
Záludné bývají zvláště noční hypoglykemie, které potvrdí jen průběžné měření glykemií. Často nebývají vůbec rozpoznány, a lékař proto po nich musí cíleně pátrat při každé návštěvě pacienta. Při lékařem běžně položené otázce, zda byla v uplynulém období nějaká hypoglykemie, je obvyklá odpověď „ne“ s tím, že drobné poruchy vědomí, jež jsou jakýmisi hypoglykemickými ekvivalenty, nepokládají za významné.
Méně než jedna desetina hypoglykemických epizod je spojena se ztrátou vědomí – hypoglykemickým kómatem. Jeho vznik může navodit vedle aplikace vyšší dávky léku (inzulin, PAD) také nedostatečný příjem potravy a nadměrná fyzická aktivita. Za zvláště rizikové faktory těžké hypoglykemie ve stáří lze označit tyto faktory:
- léčba inzulinem (zejména intenzifikovaně), preparáty sulfonylurey, glinidy
- nízká hladina HbA1c
- dlouhá doba trvání DM
- alkohol
- nevhodný denní režim (načasování denních jídel a pohyb)
- fenomén nerozpoznání hypoglykemie
- stoupající věk
- komorbidity a zdravotní handicapy (demence, kognitivní poruchy, poruchy mobility, těžké zrakové nebo sluchové handicapy)
- sociální aspekty (osamělost)
- komplikace ohrožující starší pacienty při delším trvání jsou mozkové příhody, kardiální akutní epizody (infarkt, srdeční selhání, akutní dysrytmie) a možný je i pád s úrazem.
Hyperglykemické kóma
Oba akutní stavy hyperglykemie – DKK (diabetické ketoacidotické kóma) i HONK (hyperosmolární neketoacidotické kóma) bývají v počátečních stadiích svého vzniku (tj. prekómatu) často mylně zaměňovány, zejména u starších nemocných s nově zjištěným diabetem. Polyurie (hlavně noční) a hubnutí bývají při novém vzniku DM časté, i když senior – nový diabetik na ně nemusí sám upozornit. Tento fakt jen zdůrazňuje skutečnost, že každý nemocný v těžkém stavu nebo s neurologickými příznaky musí mít vyšetřenu glykemii, elektrolyty, osmolalitu a acidobazickou rovnováhu. Společným jmenovatelem obou stavů – DKK i HONK – je hyperglykemie a deficit vody a iontů. Na farmaka, která mají rizikový potenciál pro případné lékové interakce ve smyslu hyperglykemie při ambulantní léčbě SU, poukazuje tabulka 4.
Table 4. Sulfonylurea (SU) – lékové interakce způsobující hyperglykemii 
V léčbě obou hyperglykemických stavů obecně je hlavní rehydratace, malé dávky inzulinu podávané venózně kontinuálně, sledování kalia a acidobazické rovnováhy a jejich případná včasná korekce a suplementace.
Diabetické ketoacidotické kóma (DKK)
Jde o život ohrožující stav podmíněný absolutním nedostatkem inzulinu, spojeným s nadměrnou sekrecí glukagonu (primárně), katecholaminů, glukokortikoidů a růstového hormonu. Tyto hormony stimulují glykogenolýzu, glukoneogenezi a poruchu glukózové utilizace. Zvýšená je lipolýza s netlumenou beta-oxidací mastných kyselin a nadměrným vznikem acetyl-koenzymu A. Jeho spojením vzniká kyselina acetoctová, beta-hydroxymáslená a dekarboxylací aceton, který je vydýchán a vede k typickému pachu dechu nemocného po ovoci (Kusmaulovo dýchání). DKK může být projevem jak nově vzniklého DM1, tak non-compliance nebo ho může dokonce vyvolat jiné závažné horečnaté onemocnění či akutní nemoc, úraz, operace atp.
Hyperosmolární neketoacidotické kóma (HONK)
Vyskytuje se převážně u osob nad 50 let s DM2 s relativním deficitem inzulinu. Ten brání plnému rozvoji ketoacidózy ve smyslu DKK a je typický pro hyperosmolární stavy, které jsou právě ve stáří mnohem častější než u mladších jedinců. Glukóza se nalézá ve vysoké koncentraci v extracelulární tekutině a osmoticky stahuje vodu z buněčného kompartmentu. Osmotická diuréza podmíněná glykosurií vede k abnormálním ztrátám vody a elektrolytů. Neadekvátní příjem tekutin, dehydratace, hyperosmolalita a hypovolemie otevírají bludný kruh se vzestupem glykemie a prohloubením inzulinové rezistence. Chybění pocitu žízně, zhoršení pitného režimu při osamělosti nebo kognitivní poruše a osmotické diuréze.
Příčiny vzniku HONK (tab. 2) mohou být podobné jako u DKK: nově vzniklý DM, non-compliance, jiné závažné onemocnění (CMP, IM, srdeční selhání atp.), úraz, operace, zvracení, průjem, současná farmakoterapie (kortikosteroidy, diuretika atd.). Vysoké bude riziko cévních makrovaskulárních komplikací (ikty, infarkt myokardu, srdeční selhání), tromboembolických komplikací a dalších(16, 17). Mortalita u HONK je vysoká a stoupá s věkem – od 5 % v 7. decenniu ke 100 % v 9. dekádě.
Pozdní mikrovaskulární komplikace
Jsou zastoupeny retino-, nefro - a neuropatií a bývají označovány jako specifické. Ztluštění bazální membrány kapilár a prekapilár je společným jevem pro tyto specifické komplikace diabetu(1–4).
Diabetická retinopatie (DR)
Dělí se na neproliferativní formu/NPDR (mikroaneuryzmata, intraretinální hemoragie a exsudáty) a proliferativní formu/PDR (neovaskularizace sítnice). Její incidence i prevalence přímo koreluje s dobou trvání cukrovky, její dlouhodobou kompenzací, proteinurií i typem diabetu(18). Intenzivní léčba DM přitom příznivě ovlivňuje její rozvoj. Obě formy DR může komplikovat diabetická makulopatie, která se vyskytuje u seniorů diabetiků s NPDR v 65 % (u mladších diabetiků s NPDR jen ve 20 %). U těžší PDR se vyskytuje až v 71 % bez ohledu na věk. Přes všechny pokroky v diagnostice, terapii i prevenci je stále velmi nevypočitatelná, co se týká další progrese v čase. Neovaskularizace je pro diabetickou retinopatii zcela specifickou charakteristikou pro změny na sítnici.
Zejména PDR spojená s krvácením do sítnice a neovaskularizací povede k postupnému zhoršování vizu až ztrátě zraku, jež budou zvyšovat riziko pádů, sociální izolace a deprese. Představuje nejčastější riziko oslepnutí v průmyslově vyspělých zemích. Léčba proliferativní retinopatie laserovou fotokoagulací snižuje riziko oslepnutí o 50 % v průběhu 6 let. Navíc mají diabetici dvojnásobné riziko katarakty a trojnásobné glaukomu ve srovnání s nediabetiky.
Diabetická nefropatie
Diabetická nefropatie je chronické progresivní onemocnění ledvin s dominující proteinurií, hypertenzí a postupným zhoršováním renálních funkcí(17). Představuje život ohrožující komplikaci DM. Současně je i indikátorem kardiovaskulární (KV) patologie a je jednoznačně spojena s KV mortalitou. U starších diabetiků ve srovnání s mladšími je toto propojení méně těsné. O počínající nefropatii se jedná při mikroalbuminurii >30 mg/24 hodin (jde o cut-off). Nevýhodou při provádění tohoto vyšetření je častý neúplný sběr moče a nepohodlí pro staršího pacienta (i při užití kratšího osmihodinového sběru). Velmi problematický se stává sběr moče u inkontinentních seniorů a vůbec obecně polymorbidních geriatrických pacientů. Zde se pak nabízí možnost stanovení poměru albumin: kreatinin v prvním ranním vzorku moče nebo náhodném vzorku moče. Tento způsob testu doporučuje ve svých guidelines US National Kidney Foundation (2002) a American Diabetes Association (2005). Výhodou je snadnost provedení nezávisle na zdravotním stavu. Je nutné ovšem mít na mysli obecné nevýhody stanovení kreatininu v moči – vylučování se mění s klesající glomerulární filtrací a je závislé na svalové hmotě. Cut-off je podle České společnosti klinické biochemie a České diabetologické společnosti 2,8 mg/mmol pro muže i ženy (2003). K obrazu klinicky manifestní pokročilé nefropatie patří téměř vždy i diabetická retinopatie, neuropatie a hypertenze(19). Lékem volby, který vedle zpomalení progrese diabetické nefropatie také snižuje riziko KV epizod, jsou inhibitory ACE a AT2-blokátory.
Diabetická neuropatie
Diabetická neuropatie, kraniální neuropatie a mononeuropatie se objevují mnohem častěji u starších než mladších diabetiků a souvisí s nervovou ischemií(17). Radikulopatie nejčastěji postihuje nervové kořeny L2 až L4, vedoucí k bolestem, slabosti až atrofii dolních končetin (diabetická amyotrofie) nebo proximální kořeny Th4 až Th12 vedou k břišním bolestem. Kraniální neuropatie může vést k diplopii, ptóze a anizokorii při postižení NIII a okohybné problémy při postižení IV. a VI. hlavového nervu. Vůbec nejčastější je senzorická distální symetrická polyneuropatie. Běžné symptomy zahrnují trnutí a pálení nohou. Svým charakterem predisponuje pacienty k traumatu dolní končetiny a tím následně zvyšuje i riziko případné amputace. Autonomní neuropatii představují především diabetická gastroparéza, erektilní dysfunkce a neurogenní měchýř. Diabetická amyotrofie působí asymetrické bolestivé ochabnutí svalů pánevního pletence, stehna a obvykle spontánně odezní během několika měsíců. Častěji se objevuje u starších mužů. Diabetická neuropatická kachexie se objevuje u velmi starých diabetiků a projevuje se hubnutím, depresí a bolestivou periferní polyneuropatií.
Pozdní makrovaskulární komplikace diabetu
DM představuje významný rizikový faktor pro vznik i rozvoj pozdních diabetických komplikací jak mikro-, tak makroangiopatických. Prevence T2DM je možná právě úpravami životního stylu, jako jsou dietní opatření, redukce hmotnosti při obezitě a pravidelný pohyb.
Ateroskleróza (AS) velkých tepen souvisí s hyperinzulinemií, dyslipidemií a hyperglykemií. Platí, že diabetes je modelem urychlené aterogeneze. Oba typy cukrovky mohou vést po určité době trvání k podobným pozdním komplikacím(20, 21). Prognóza choroby není ani tolik určována typem DM jako spíše dobou trvání choroby, věkem, kdy se objeví, a dlouhodobým stupněm kompenzace.
Ateroskleróza postupuje u diabetiků několikanásobně rychleji(20). Z toho plyne dva - až pětkrát vyšší výskyt kardio - a cerebrovaskulárních příhod, včetně vyššího výskytu srdečního selhání, nebolestivého infarktu myokardu a cévních mozkových příhod. Endotelová dysfunkce tak vede ve svých důsledcích k významným změnám morbidity i mortality diabetiků.
U diabetiků 2. typu bude stejně významná jako terapie DM léčba hypertenze, dyslipidemie, obezity a dalších projevů Reavenova metabolického syndromu(16, 20, 21). Hyperglykemie sama o sobě nemusí sehrávat ústřední roli při rozvoji makrovaskulárních komplikací. Intenzivní kontrola hyperglykemie a pouhá optimální kompenzace DM nebude ani dostatečnou prevencí těchto cévních změn. Makrovaskulární pozdní aterosklerotické změny bývají označovány jako nespecifické komplikace, protože jejich morfologický a histologický korelát je identický s obrazem aterosklerotických změn na cévách u nediabetiků. Jen jejich vznik a rozvoj je poněkud dřívější a rychlejší ve srovnání s nediabetiky. Tyto komplikace jsou zastoupeny ischemickou chorobou srdeční (ICHS), anginou pectoris, infarktem myokardu, tranzitorní ischemickou atakou, ikty a ischemickou chorobou dolních končetin (ICHDKK). Riziko ICHS a mozkové příhody je více než dvojnásobné a riziko amputace na dolních končetinách více než 10násobné ve srovnání s nediabetiky.
Další komplikace
U starších diabetiků je vyšší riziko plísňových a bakteriálních infekcí (pneumonie) majících vztah ke zhoršené cévní mikrocirkulaci a hyperglykemie, která bývá spojena s poklesem celulární imunity. Slizniční a kožní plísňové infekce (např. ústní nebo vaginální kandidóza, tinea pedis) a bakteriální infekce nohou se vyskytují u nemocných s diabetem zcela běžně. Podobně časté u jedinců s delším trváním cukrovky jsou i plísňové infekce (mokvání, trhliny) a ulcerace, jež predisponují k sekundární bakteriální infekci(5, 8).
Další komplikace zahrnují depresi, kognitivní poruchy a poruchy pojivové tkáně (svalové infarkty, Dupuytrenova kontraktura atp.), hepatobiliární poruchy (jaterní steatóza) a steatohepatitidu, cirhózu, hepatitidu C, cholelitiázu, kožní infekce (tinea pedis, ulcerace nohou, necrobiosis lipoidica diabeticorum, vitiligo, granuloma annulare, acanthosis nigricans). Cukrovka může exacerbovat uroinfekci a ta může vést až k nekróze ledvinných papil.
U syndromu diabetické nohy stav akcentuje neuropatie a ischemická vaskulopatie. Syndrom diabetické nohy (SDN) zahrnuje kožní změny, ulcerace, infekce rány, gangrénu vznikající z ischemie, neuropatie a imunosuprese. Amputace jako terminální řešení u SDN je užita u 0,5 až 1 % všech diabetiků a u 1/8 (13 %) osob se SDN.
V seniu obecně se horší termoregulace a DM tak zvyšuje riziko nepředvídatelné hypotermie. Maligní externí otitida podmíněná Pseudomonas aeruginosa je nekrotizující infekce nejčastěji přítomná u starších diabetiků.
Závěr
Dlouhodobě dobrá kompenzace DM je schopná oddálit nebo zpomalit rozvoj pozdních komplikací(7). Na druhé straně je třeba stejnou měrou věnovat zvýšenou pozornost výskytu akutních komplikací, zejména riziku hypoglykemie s možností rozvoje makrovaskulárních komplikací. Zlepšená péče o diabetiky s pokročilými formami mikro - i makrovaskulárního postižení se rovněž jeví jako slibná do budoucna pro zlepšení kvality života starších diabetiků.
I ve vyšším věku si léčba DM vyžaduje značnou pozornost ošetřujícího lékaře(22), zejména pak diabetologa, který dlouhodobě staršího diabetika dispenzarizuje, aby bylo možno předejít nebo zpomalit progresi pozdních, zejména cévních komplikací, které se vyskytují u T2DM až 5krát častěji. Hlavním cílem léčby DM ve stáří je tedy zlepšení kvality života. Lze je shrnout do několika následujících bodů:
- optimální metabolická kompenzace
- prevence následujících příznaků: únava, hubnutí, polyurie, infekční komplikace
- vymezení požadavků na životní styl, zejména dietní návyky
- omezení užívaných léků – zejména s rizikem hypo - a hyperglykemie.
prof. MUDr. Pavel Weber, CSc.,
MUDr. Hana Meluzínová,
MUDr. Dana Prudius,
MUDr. Katarína Bielaková
Klinika interní, geriatrie a praktickéhoLF MU a FN Brno
prof. MUDr. Pavel Weber, CSc.
e-mail: p.weber@fnbrno.cz
Pracuje jako ambulantní lékař na Klinice interní, geriatrie a praktického lékařství LF MU a FN Brno a je vysokoškolským učitelem na dvou fakultách Masarykovy univerzity. Od 1999 je členem výboru v různých funkcích České gerontologické a geriatrické společnosti, dále členem 10 zahraničních odborných společností a jediným absolventem a členem EAMA z bývalého Československa. Stážoval na předních zahraničních pracovištích (Rakousko, Německo, Francie, Velká Británie, USA, Itálie). Od 2012 zastupuje Českou republiku v UEMS (European Union of Medical Specialists). Ve své klinické práci se orientuje na problematiku diabetu ve stáří, pádů a změn soběstačnosti. Je členem 8 redakčních rad, recenzentem našich i zahraničních lékařských periodik, autorem a spoluautorem mnoha odborných publikací
Sources
1. Hunter JA, Haslett C, Chilver AR, Boon NA, Colledge A (eds.). Principles & Practice of Medicine (Davidson’s). 22nd Edition. Edinburgh, UK. Churchill Livingstone 2014.
2. Wiener Ch, Fauci A, Braunwald E, Kasper D (eds.). Harrison’s Principles of Internal Medicine 18th Edition, New York, USA. McGraw-Hill Professional Publishing Division 2012.
3. Kvapil M (ed.). Diabetologie. Praha: Triton 2012.
4. Haluzík M a kol. Praktická léčba diabetu. 2. vyd. Praha: Mladá fronta 2013.
5. Kirkman MS, Briscoe VJ, Clark N, et al. Diabetes in older adults. Diabetes Care 2012; 35(12): 2650–2664.
6. Chiniwala N, Jabbour S. Management of diabetes mellitus in the elderly. Curr Opin Endocrinol Diabetes Obes 2011; 18(2): 148–152.
7. American Diabetes Association. Standards of Medical Care in Diabetes. Diabetes Care 2013; 36(Suppl.1): S11–S66.
8. Laubscher T, Regier L, Bareham J. Diabetes in the frail elderly: individualization of glycemic management. Can Fam Physician 2012; 58(5): 543–546.
9. Munshi MN, Maguchi M, Segal AR. Treatment of type 2 diabetes in the elderly. Curr Diab Rep 2012; 12(3): 239–245.
10. Yau CK, Eng C, Cenzer IS, et al. Glycosylated hemoglobin and functional decline in community-dwelling nursinghome-eligible elderly adults with diabetes mellitus. J Am Geriatr Soc 2012; 60(7): 1215–1221.
11. Inzucchi SE, Bergenstal RM, Buse JB. Management of hyperglycemia in type 2 diabetes: a patient-centered approach – position statement of the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care 2012; 35(6): 1364–1379.
12. Bramlage P, Gitt AK, Binz C, et al. Oral antidiabetic treatment in type-2 diabetes in the elderly: balancing the need for glucose control and the risk of hypoglycemia. Cardiovasc Diabetol 2012; 6(10): 111–122.
13. Greenway FL. Severe hypoglycemia in the Look AHEAD Trial. J Diabetes Complications 2016; 30(5): 935–943.
14. Sako A, Yasunaga H, Matsui H, et al. Hospitalization for hypoglycemia in Japanese diabetic patients: A retrospective study using a national inpatient database, 2008–2012. Medicine (Baltimore) 2015; 94(25): e1029.
15. Sanchai T, Patumanond J. Severe hypoglycemia in type II diabetes at Nakornping General Hospital: a study on clinical risk factors. J Med Assoc Thai 2011; 94(12): 1435–1440.
16. Eriksson M, Carlberg B, Eliasson M. The disparity in long-term survival after a first stroke in patients with and without diabetes persists: the Northern Sweden MONICA study. Cerebrovasc Dis 2012; 34(2): 153–60.
17. Basanta-Alario ML, Ferri J, Civera M, et al. Differences in clinical and biological characteristics and prevalence of chronic complications related to aging in patients with type 2 diabetes. Endocrinol Nutr 2016; 63(2): 79–86.
18. Tóth G, Szabó D, Sándor GL, et al. Diabetes and diabetic retinopathy in people aged 50 years and older in Hungary. Br J Ophthalmol 2016; pii: bjophthalmol-2016-309016. (Epub ahead of print).
19. Bailey CJ, Day C. Diabetes therapies in renal impairment. Br J Diabetes Vasc Dis 2012; 12(4): 167–171.
20. Williamson JD, Supiano MA, Applegate WB, et al; SPRINT research group. Intensive vs standard blood pressure control and cardiovascular disease outcomes in adults aged ≥75 years. JAMA 2016; 315(24): 2673–2682.
21. Paneni F, Beckman JA, Creager MA. Diabetes and vascular disease: pathophysiology, clinical consequences, and medical therapy: part I. Eur Heart J 2013; 34(31): 2436–2443.
22. Sinclair AJ, Paolisso G, Castro M, et al. European diabetes working party for older people 2011 clinical guidelines for type 2 diabetes mellitus. Executive summary. Diabetes Metab 2011; 37(Suppl. 3): S27–S38.
Labels
Geriatrics General practitioner for adults Orthopaedic prosthetics
Article was published inGeriatrics and Gerontology

2016 Issue 4-
All articles in this issue
- Můžeme předpovědět úmrtí geriatrických pacientů na klostridiovou infekci?
- Může sérová hladina vitaminu D ovlivnit délku hospitalizace seniora?
- Diabetes a demence – co je známo o jejich vztahu?
- Akutní a pozdní komplikace diabetu – představují významný problém ve vyšším věku?
- Specifika tuberkulózy u seniorů dnes
- Obstipace ve stáří
- Antikoagulační léčba ve stáří
- Kožní lymfomové onemocnění u geriatrického pacienta
- Geriatrics and Gerontology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Obstipace ve stáří
- Diabetes a demence – co je známo o jejich vztahu?
- Akutní a pozdní komplikace diabetu – představují významný problém ve vyšším věku?
- Kožní lymfomové onemocnění u geriatrického pacienta
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


