-
Medical journals
- Career
Profylaxe tromboembolické nemoci
Authors: M. Penka
Authors‘ workplace: Interní hematologická a onkologická klinika ; Společná pracoviště s FN Brno – pracoviště medicíny dospělého věku ; OKH FN Brno
Published in: Geriatrie a Gerontologie 2013, 2, č. 4: 206-209
Category: Review Article
Overview
Žilní tromboembolismus je vzdor značnému pokroku v diagnostice, profylaxi i léčbě stále závažným zdravotním i sociálním problémem. V současné době se klade velký důraz na širokou prevenci a profylaxi a vypracovávají se algoritmy zajištění péče ve specifických situacích. I přesto je tromboembolická žilní nemoc v Evropě příčinou úmrtí u více než 500 000 osob ročně.
Klíčová slova:
trombóza – embolie – profylaxe – heparin – warfarinÚvod
Hluboká žilní trombóza (deep venous thrombosis – DVT) se vyskytuje asi v 1 případě na 1000 osob. Má povětšinou multifaktoriální genezi a málo varovných známek. Její nejzávažnější komplikací je plicní embolie, a proto mluvíme raději o žilním tromboembolismu (venous thromboembolism – VTE). V 70 % se vyskytuje u hospitalizovaných nemocných a 75 % smrtících embolií se vyskytuje u nechirurgických pacientů(1). V Evropské unii umírá na VTE přes 500 000 obyvatel ročně, přičemž profylaxí VTE je zajištěno pouze 61 % nemocných(2, 3). Opožděná a neadekvátní léčba vede navíc ke vzniku insuficience chlopní a až v 80 % k chronické žilní insuficienci a posttrombotickému syndromu.
Asi 10 % recidivujících trombóz je zapříčiněno vrozeným defektem některého z inhibitorů koagulace, v 6–8 % populace zjišťujeme trombofilní genetickou odchylku – Leidenskou mutaci faktoru V (FVL) a asi ve 2 % mutaci protrombinu (PT20210A)(4). V 10 % případů primární trombózy je její příčinou okultní malignita(5). Je proto třeba se problematikou VTE zabývat, zvláště za zátěžových situací, které riziko vzniku tromboembolické nemoci (TEN) zvyšují. K nim bezesporu, vedle dalších,patří úrazy a operace.
Klinická manifestace žilního tromboembolismu
Trombóza hluboké žíly v typické lokalizaci postihuje buď systém dolních končetin, nebo pánve. V tomto případě dochází k otoku postižené končetiny, až cyanotickému zbarvení s event. napnutím kůže, bolestivosti na pohmat a v tahu (pozitivita tzv. napínacích manévrů).
V laboratorním nálezu koagulačních testů je přítomna pozitivita tzv. hyperkoagulačních markerů (fibrinové monomery – FM, trombin-antitrombinové komplexy – TAT, fragment 1+2 – F1+2, fibrinopeptid A – FpA a D-dimery – DD). Základní testy koagulace (protrombinový čas – PT a aktivovaný parciální tromboplastinový čas – APTT) se mohou pohybovat v normálním rozmezí(6).
Nejzávažnější komplikací hluboké žilní trombózy bývá plicní embolie (PE), kdy se skrze pravé srdce dostává (vmete – odtud český výraz vmetek) část trombu do plicnice a jejích větví (50–80% všech DVT). Dle rozsahu embolu může být důsledkem plicní infarkt, v nejtěžším případě i náhlá smrt(7).
Chronickou komplikací DVT je chronická žilní nedostatečnost a posttrombotický syndrom. Ten se může projevit přetrvávajícím otokem postižené končetiny, trofickými změnami kůže až ulceracemi (bércové vředy), bolestivým syndromem, poruchou chůze, lymfostázou až charakteru lymfedému.
V některých případech (zejm. v souvislosti s trombofilní dispozicí – vrozenou či získanou) se objevují trombózy i v méně obvyklých lokalizacích (v mezenteriálním či hepatolienálním povodí, žilách prstů, očního pozadí, mozku…) a recidivují.
Výskyt a závažnost vzniku tromboembolických komplikací se liší v závislosti na celé řadě faktorů a jedním z nich je charakter onemocnění či charakter poskytované péče (tab. 1).
Table 1. Tromboembolické komplikace u vybraných chorob 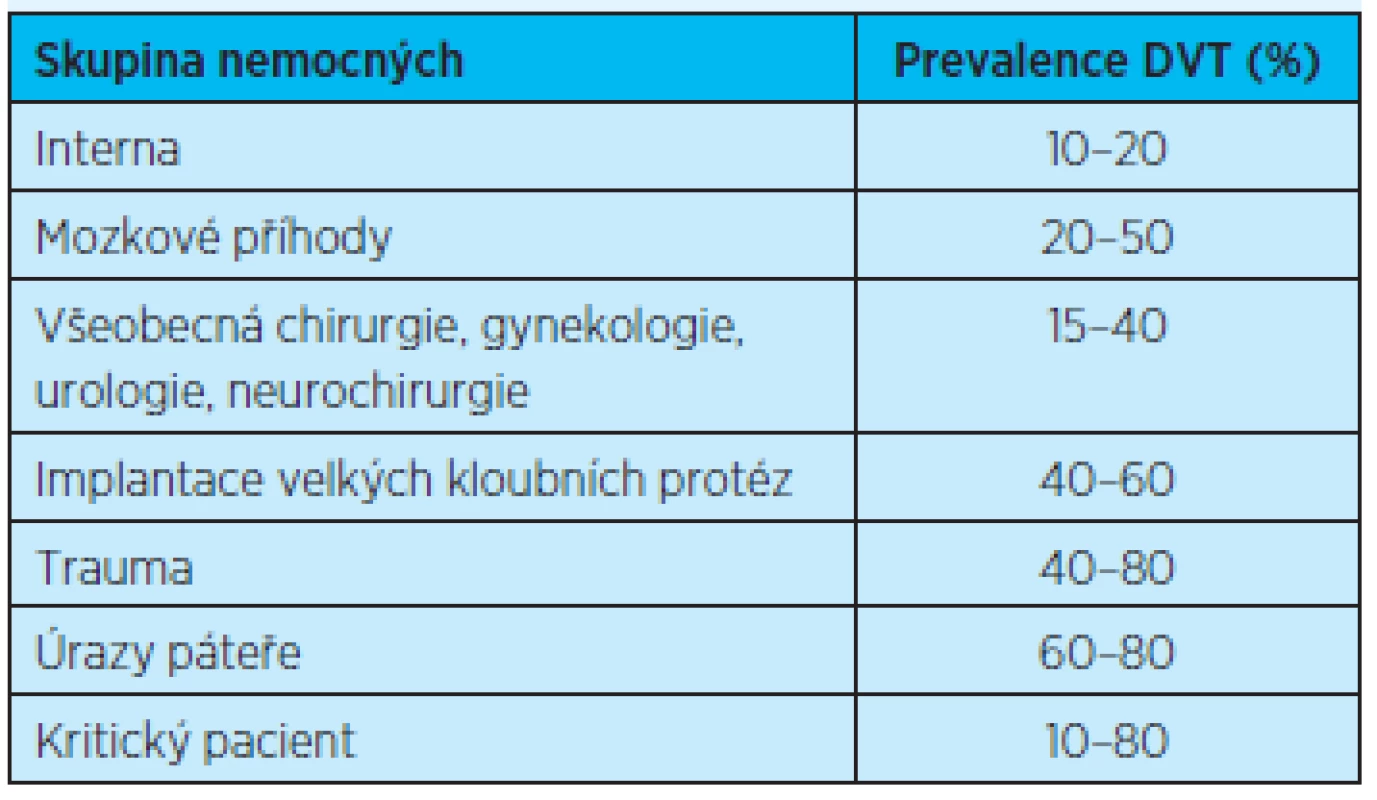
Profylaxe žilního trombembolismu
V rámci předcházení vzniku trombózy se uplatňuje řada profylaktických opatření v různých specifických situacích. Proto je vypracována řada schémat a skórovacích systémů k posouzení rizika vzniku tromboembolických komplikací – viz např. skóre podle Kuchera v tabulce 2(8).
Table 2. Riziko tromboembolických komplikací podle Kuchera 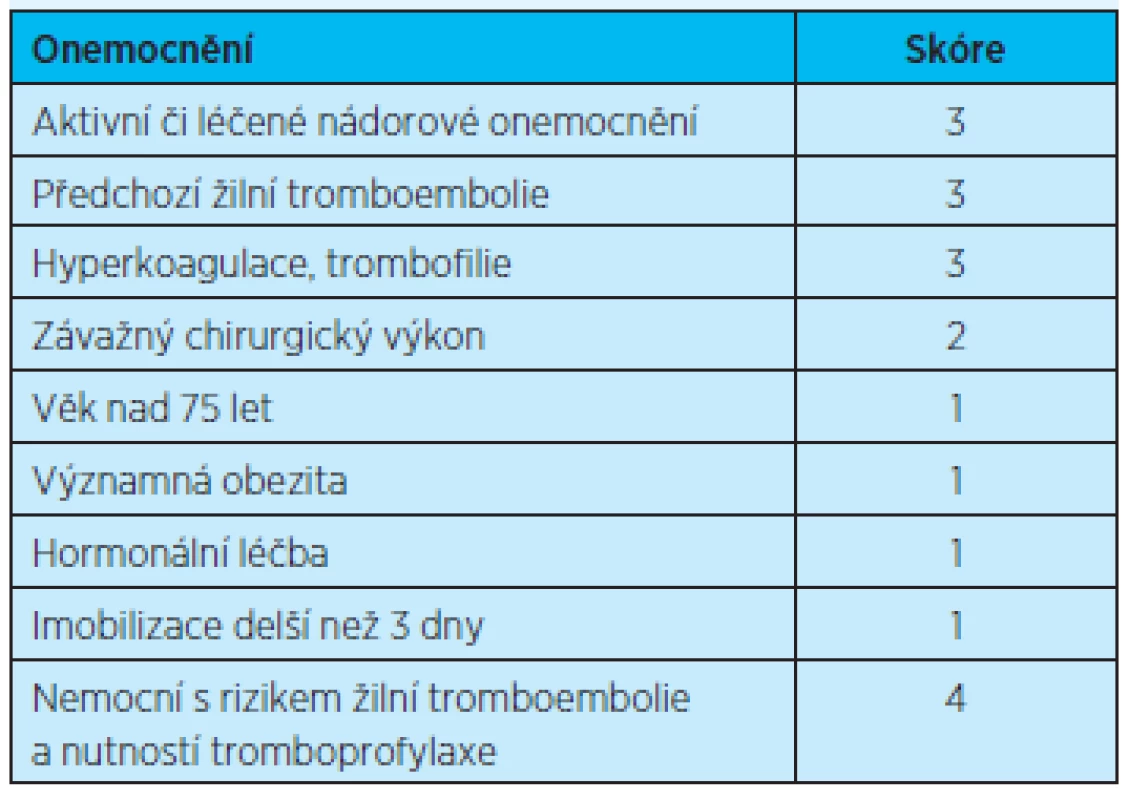
K profylaxi lze vedle nemedikamentózních užít medikamentózních opatření – hepariny (především LMWH), dále i pentasacharidy a pro domácí léčbu warfarin; z nových přípravků jsou to perorální preparáty z řady přímých inhibitorů trombinu – dabigatran etexilát, a přímých inhibitorů faktoru Xa – rivaroxaban a apixaban. Z nemedikamentozních možností jsou to časná vertikalizace a mobilizace, pružná obinadla a punčochy a pneumatické punčochy. Pro zajištění adekvátní profylaxe se využívají doporučení ACCP z roku 2012(9, 10, 11).
Profylaxe je indikována:
- v souvislosti s operací, či úrazem u nemocných s rizikem trombózy vyšším než 1 škály hodnocení trombotického rizika (tab. 3). Ke stupni nízkého rizika přináleží pouze zdravé osoby podstupující menší výkon bez souběžné medikace, perorální kontraceptiva nevyjímaje(12)
- v graviditě, šestinedělí či při hyperstimulačních režimech v souvislosti s prokázanou zátěží
- ve vnitřním lékařství v souvislosti se zvýšeným rizikem trombózy
- při výskytu trombofilních (vrozených či získaných) dispozic s klinickou symptomatologií opakovaných tromboembolických příhod.
Table 3. Stupeň rizika VTE podle Nicolaidese AN a spol., 1997<sup>(13)</sup> 
Profylaxi samotnou provádíme:
- a) aplikací nízkomolekulárních heparinů. Lze přitom volit buď alternativu paušální dávky, doporučené pro dané riziko a okolnosti výrobcem, nebo podávat adjustovanou dávku100 IU/kg tělesné hmotnosti a 24 hodin.
Ke sledování účinnosti LMWH lze použít vyšetření anti-Xa aktivity, která je doporučena u astenických či obézních pacientů, u dětí, v graviditě a u nemocných s renální insuficiencí. Účinná profylaxe by měla kolísat mezi hodnotami 0,2–0,6 IU/ml a odběr krve na vyšetření je nutné provést za 3–4 hodiny po aplikaci LMWH. Při profylaktickém podávání heparinu by nemělo docházet k prodlužování APTT.
- b) aplikací nízkodávkovaných schémat UFH – např. v dávce 2–3x 5000 j. za 24 hodin aplikovaných buď subkutánně nebo v kontinuální infúzi v celkové denní dávce 10 000–15 000 či 20 000 jednotek na 24 hodin. Ke kontinuálnímu podávání přistupujeme zejména tehdy, dochází-li k selhávání oběhu(14). Ke spektru monitorovaných testů patří také vyšetření počtu krevních destiček, protože i v souvislosti s preventivní heparinizací může dojít k výskytu heparinem indukované trombocytopenie s trombózou nebo bez trombózy – HIT/T. Alternativou profylaxe LMWH je pak v těchto případech podávání pentasacharidů v paušální profylaktické dávce (fondaparinux – Arixtra) 2,5 mg s.c. 1x denně(8).
U nemocných na dlouhodobé prevenci či profylaxi, zejména pooperační (po totálních náhradách kloubních), je možné přejít na kumariny (warfarin). Ukazuje se, že je u těchto nemocných (+ u nemocných po rozsáhlých břišních operacích pro nádor) výhodné prolongovat antitrombotickou profylaxi na 35–42 dní, protože výskyt až poloviny pooperačních trombóz se objevuje až po 14 dnech od operace(15). Na rozdíl od počátečních zkušeností, kdy se využívalo nízkodávkované warfarinizace, se ukazuje jako účinnější klasické dávkování s dosažením terapeutických hodnot INR. Zejména u starších osob se nabízela zmíněná nízkodávkovaná léčba, ale právě u nich docházelo k jejímu selhání, aniž by ubývalo komplikací(16). V případech, kdy se jedná o vrozenou nebo trvající získanou zátěž trombofilní dispozicí, je podávání warfarinu dlouhodobé nebo trvalé.
Kumariny jsou používány stále častěji v souvislosti se zajištěním profylaxe a prevence u nemocných s trombofilií, ať již v důsledku vrozených (např. defekty inhibitorů koagulace), nebo získaných (antifosfolipidový syndrom – APS) dispozic. Další velkou skupinou nemocných indikovaných k profylaxi VTE kumariny, resp. perorálními antikoagulancii – v tomto případě z důvodu prevence cévních mozkových příhod a systémových embolizací – jsou pacienti s fibrilací síní, a pacienti na dlouhodobé pooperační prevenci(17). Rovněž u žen v šestinedělí bývá kumarinová antikoagulační profylaxe častou alternativou zabezpečení. Současným trendem je i podávání kumarinů u těhotných s chlopňovou náhradou v době gravidity a dle některých autorů i po celou dobu. Tato doporučení vyplývají ze zpráv o nižší účinnosti heparinů ve zmíněných případech, které však nemusejí být zcela věrohodné, a to především z důvodu nedostatečné dávky heparinu, a tudíž i obtížného srovnávání efektivity léčby(18).
V případě, že je třeba zajistit operaci nebo úraz u nemocného užívajícího warfarin, pak při možnosti plánovaného postupu převádíme pacienta z warfarinu na LMWH a zpět, podle toho, jak je vyžaduje léčebný proces (obr. 1).
Image 1. Převedení nemocného z warfarinu na LMWH a zpět v případě elektivního výkonu 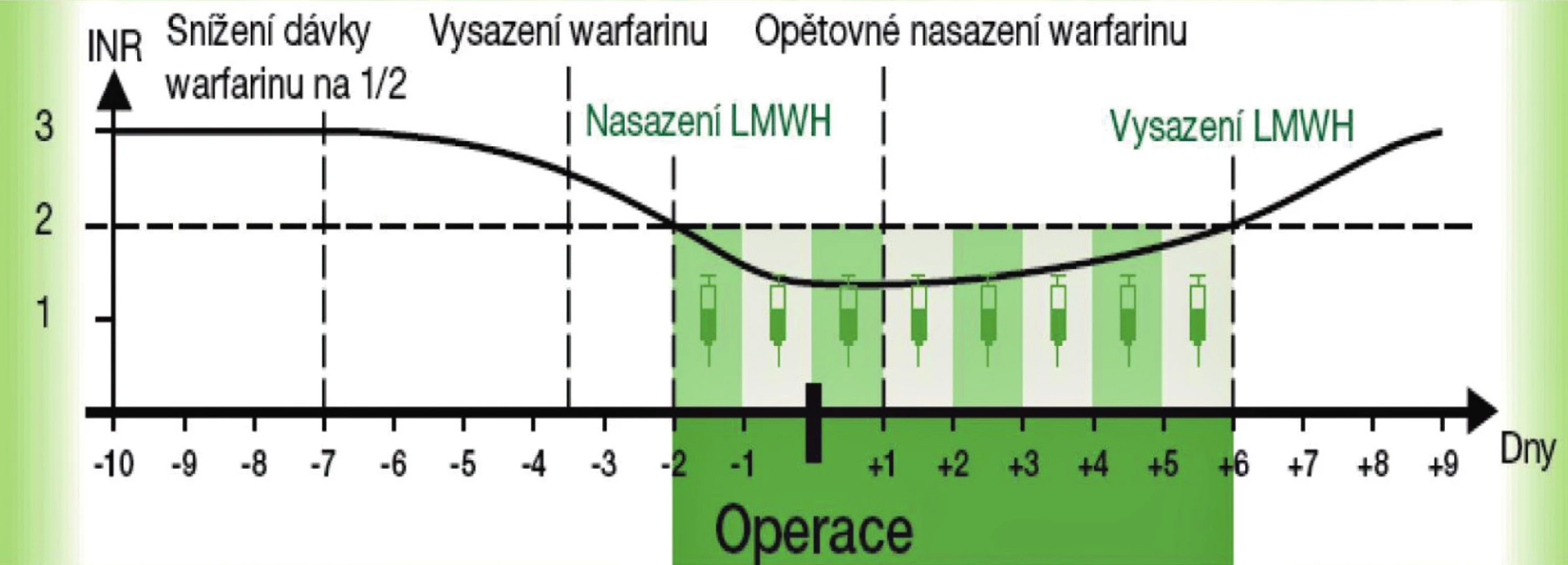
Vedle klasických perorálních preventivních režimů warfarinem jsou rozvíjeny snahy o zavedení podávání nových antitrombotických působků v perorální formě – až již přímých inhibitorů trombinu (dabigatran – Pradaxa) nebo přímých inhibitorů faktoru Xa (rivaroxaban – Xarelto, apixaban – Eliquis(19). Svoje významné místo si vydobyly právě k zajištění prevence u nemocných po implantacích totálních endoprotéz kyčle a kolene. Sledování účinku nových antitrombotik není běžně vyžadováno, ale i v těchto případech máme k dispozici dilutovaný trombinový čas pro sledování dabigatran etexilátu a anti-Xa aktivity u nemocných na rivaroxabanu či apixabanu.
Závěr
TEN je relativně častým a zároveň závažným medicínským problémem.
TEN může vést k smrtícím komplikacím – plicní embolie, cévní mozková příhoda.
TEN má ve vysokém procentu za následek chronické komplikace – posttrombotický syndrom, který může vést k invalidizaci nemocných.
TEN lze předcházet účinnými, nenáročnými, a to i v porovnání k řadě dalších smrtelných chorob, po finanční stránce hodnocenými režimy.
Jsou známy situace, za nichž dochází ke zvyšování rizika vzniku TEN a kdy by měla být zavedena specifická profylaktická opatření, ať již medikamentózní či nemedikamentózní. (O úspěšnosti antitrombotických opatření v chirurgii svědčí i obrázek 2).
Image 2. Výsledky antitrombotické profylaxe v chirurgii (upraveno podle J. Kvasničky<sup>6)</sup> 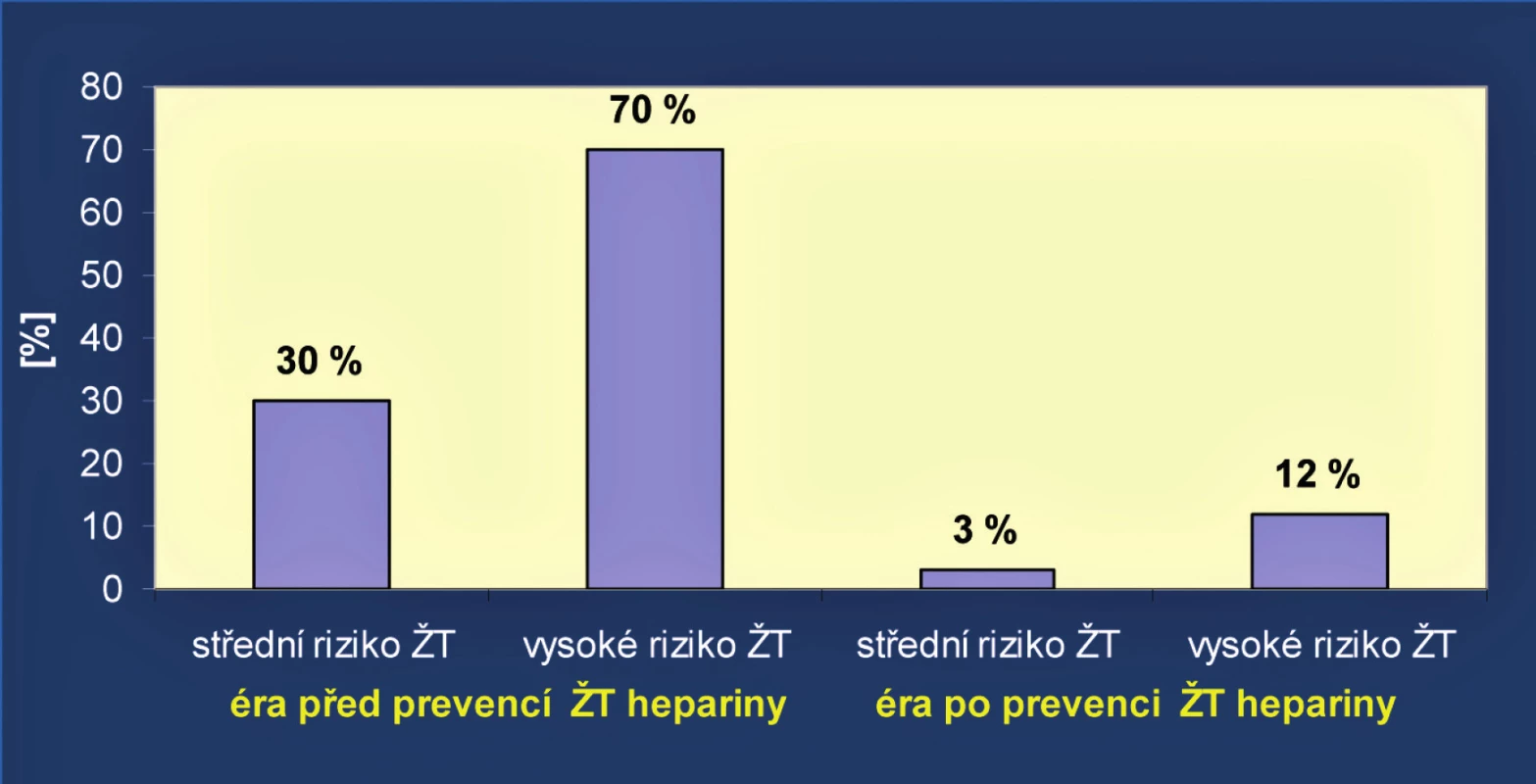
Každé pracoviště by mělo mít vypracovány standardní postupy profylaxe TEN.
TEN zasahuje do všech oblastí medicíny, a proto by s nimi měli být obeznámeni všichni kliničtí lékaři.
prof. MUDr. Miroslav Penka, CSc.
OKH FN Brno
Interní hematologická a onkologická klinika
Společná pracoviště s FN Brno – pracoviště medicíny dospělého věku
prof. MUDr. Miroslav Penka, CSc.
e-mail: m.penka@fnbrno.cz
Atestoval z vnitřního lékařství a z hematologie a krevní transfúze. V roce 1990 obhájil dizertační práci s názvem Klinický význam proteinu C, v roce 1993 se habilitoval. Téma habilitační práce – Koagulační změny u nemocných po transplantaci kostní dřeně, bylo zpracováno za studijního pobytu v Bruselu. Na Svobodné bruselské univerzitě získal „Licence speciále en cancerologie“ a v r. 1995 atestaci z klinické onkologie. V roce 1998 byl jmenován profesorem vnitřního lékařství. Působil nejprve na III. interní klinice a následně na Oddělení klinické hematologie ve FN u sv. Anny, a od roku 1989 ve FN Brno, nejprve na II. interní, později Interní hematoonkologické klinice a od r. 1998 na Oddělení klinické hematologie, které od zmíněného roku vede. Jeho odborným zájmem je problematika krevního srážení. Je autorem více než 220 prací a autorem či spoluautorem 10 monografií. Je t. č. místopředsedou České hematologické společnosti, byl zakládajícím koordinátorem Českého národního programu a členem řady dalších výborů, komisí a rad.
Sources
1. Geerts W: Prevention of venous thromboembolism: a key patient safety priority. JTH 2009; Suppl. 1 : 1–8.
2. Cohen AT, Tapson VF, Bergmann JF et al.: Venous thromboembolic risk and prophylaxis in the acute hospital care setting (ENDORSE study): a multinational cross-sectional study. Lancet 2008; 371 : 387–394.
3. http://epp.eurostat.cec.eu.int
4. Seligsohn U, Lubetsky A: Genetic Susceptibility to Venous Thrombosis. N Engl J Med 2001; 344 (16): 1222–1231.
5. Hettiarachchi, Lok J, Prins MH, Bueller HR, Prandoni P: Undiagnosed Malignancy in Patients with Deep Vein Thrombosis, Incidence, Risk factors, and Diagnosis. Cancer 1998; 83(1): 180–185.
6. Kvasnička J: Trombofilie a trombotické stavy v klinické praxi. Grada Publishing 2003 : 13–299.
7. Widimský J, Malý J a kol.: Akutní plicní embolie a žilní trombóza. Triton 2002 : 7–303.
8. Kucher N, Koo S, Quirit R et al: Electronic alerts to prevent venous thrombembolism among hospitalised patients. N Engl J Med 2005; 352 : 969–977.
9. Antithrombotic and thrombolytic therapy. American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (9th Edition), Chest, 2012; 141/2 : 7S–48S.
10. www.thrombosis.cz
11. www.hematology.cz
12. Krška Z: Trombembolická nemoc v chirurgii, Trendy soudobé chirurgie svazek 2, Galén Praha, 1998 : 1–165.
13. Kakkar VV, Lorenzo F: Prevention of venous thromboembolism in ge-neral surgery. Clinical Haematology 1998, 11(2): 605–619.
14. Jaenecke J: Indikationsgebiete fur Antikoagulantien. Post - und praeoperative Antikoagulantienprophylaxe Antikoagulanzien und Fibrinolzsetherapie. Georg Thieme Verlag. Stuttgart-New York 1996 : 142–175.
15. Hull RD, Pineo GF, Francis Ch et al.: Low-Molecular-Weight Heparin Prophylaxis Using Dalteparin Extended Out-of-Hospital vs In-Hospital Warfarin/Out-of-Hospital Placebo in Hip Arthroplasty Patients. Original Investigation. Arch. Intern. Med 2000; 160 : 2208–2215.
16. van Gorp ECM, Brandjes DPM, Cate J: Rational Antithrombotic Therapy and Prophylaxis in Elderly, Immobile Patients. Drugs & Aging 1998; 13(2): 145–157.
17. Kessler P: Léčba orálními antikoagulancii. Orion, Praha 2002 : 1–62.
18. Hirsh J, Fuster V, Ansell J, Halperin JL: American Heart Association/American College of Cardiology Foundation Guide to Warfarin therapy, Ciculation 2003; 107 : 1692–1711.
19. Berkowitz SD, Marder VJ, Kosutic G, Baugchman: Oral heparin administration with a novel drug delivery agent (SNAC) in healthy volunteers and patients undergoing elective total hip arthroplasty. Journal of Thrombosis and Haemostasis 2003; 1 : 1914–1919.
Labels
Geriatrics General practitioner for adults Orthopaedic prosthetics
Article was published inGeriatrics and Gerontology

2013 Issue 4-
All articles in this issue
- Alzheimerova demence – epidemie 21. století: můžeme a umíme jí předcházet?
- Genetika v terénní praxi
- Rizikové faktory trombózy
- Profylaxe tromboembolické nemoci
- Profylaxe posttraumatické epilepsie
- Prevence osteoporózya sarkopenie
- Sluneční záření a lidský organismus aneb „kam nechodí slunce, tam chodí lékař“
- Prevence infekcí očkováním jako celoživotní proces
- Diabetes mellitus – existují možnosti prevence?
- Geriatrics and Gerontology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Profylaxe tromboembolické nemoci
- Profylaxe posttraumatické epilepsie
- Rizikové faktory trombózy
- Alzheimerova demence – epidemie 21. století: můžeme a umíme jí předcházet?
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

