-
Medical journals
- Career
Zpráva o celorepublikovém mezilaboratorním porovnání vyšetření fekálního kalprotektinu
Authors: K. Malíčková
Authors‘ workplace: Klinická imunologie a alergologie – laboratoř, Ústav lékařské biochemie a laboratorní diagnostiky, 1. LF UK a VFN v Praze
Published in: Gastroent Hepatol 2014; 68(6): 532-534
Category: Various: Congress Report
Overview
Submitted:
18. 5. 2014Accepted:
16. 6. 2014Na jaře letošního roku proběhl již druhý ročník mezilaboratorního porovnání vyšetření fekálního kalprotektinu, jehož se letos zúčastnilo 26 klinických laboratoří z ČR. Ve srovnání s loňským rokem, kdy se porovnání zúčastnilo 13 pracovišť, jde o pozoruhodný nárůst počtu laboratoří, které vyšetření fekálního kalprotektinu provádějí a které mají zájem o kontrolu kvality svých vyšetřovacích postupů. Účast v mezilaboratorním porovnání byla bezplatná díky podpoře společnosti BioVendor – Laboratorní medicína, a. s., která se na organizaci akce spolupodílela.
Každá zúčastněná laboratoř obdržela po jednom alikvotu dvou fekálních eluátů (vzorky A a B) a jeden alikvot nativního vzorku stolice (vzorek C). Vyšetřované vzorky byly kódovány a nebyly označeny údaji o zdravotním stavu pacientů.
Vyšetřované vzorky
Vzorek A: dítě 12 let; diagnóza biopticky verifikované celiakie, před zahájením bezlepkové diety.
Vzorek B: muž 38 let; aktivní ulcerózní kolitida: enteroragie, bolesti břicha, průjmy, subfebrilie, elevace systémových zánětlivých parametrů, biopticky verifikovaná ulcerózní kolitida.
Vzorek C: žena 43 let; Crohnova nemoc v klinické remisi na biologické léčbě antiintegrinovými monoklonálními protilátkami. Bez subjektivních obtíží, dlouhodobě bez elevace systémových zánětlivých parametrů, histopatologicky prokázány chronické pozánětlivé změny v tenkém a tlustém střevě.
Příprava eluátů stolice
Vzorky A a B byly zpracovány s pomocí soupravy Faecal Sample Preparation Kit (Roche Diagnostics GmbH). Do komůrky zkumavky byl umístěn vzorek stolice o hmotnosti 85 mg, poté přidán diluční roztok tak, aby byl výsledný eluát naředěn v poměru 1 : 50. Po homogenizaci na vortexu po dobu 1 min byly vzorky centrifugovány 10 min při 3 000 g. Vzniklý supernatant byl rozdělen do alikvot a zamražen na –80 °C. Vzorek C byla nativní homogenizovaná stolice zamražená na –80 °C. Kódované vzorky byly distribuovány na ledu do příslušných laboratoří.
Přehled použitých diagnostických souprav
K vyšetření fekálního kalprotektinu byly použity výhradně diagnostické soupravy založené na principu enzymové imunoanalýzy (ELISA). Devatenáct laboratoří provedlo analýzy s pomocí jedné diagnostické soupravy. Sedm laboratoří uvedlo použití dvou různých diagnostických souprav, avšak pouze tři z nich zaslaly výsledky pro každou použitou diagnostickou soupravu zvlášť. Zbylé laboratoře uvedly do výsledku průměr měření, proto není možné přesněji vyhodnotit úspěšnost stanovení s ohledem na použitou dg. soupravu (tab. 1).
Table 1. Použité diagnostické soupravy. Tab. 1. Used diagnostic equipment. 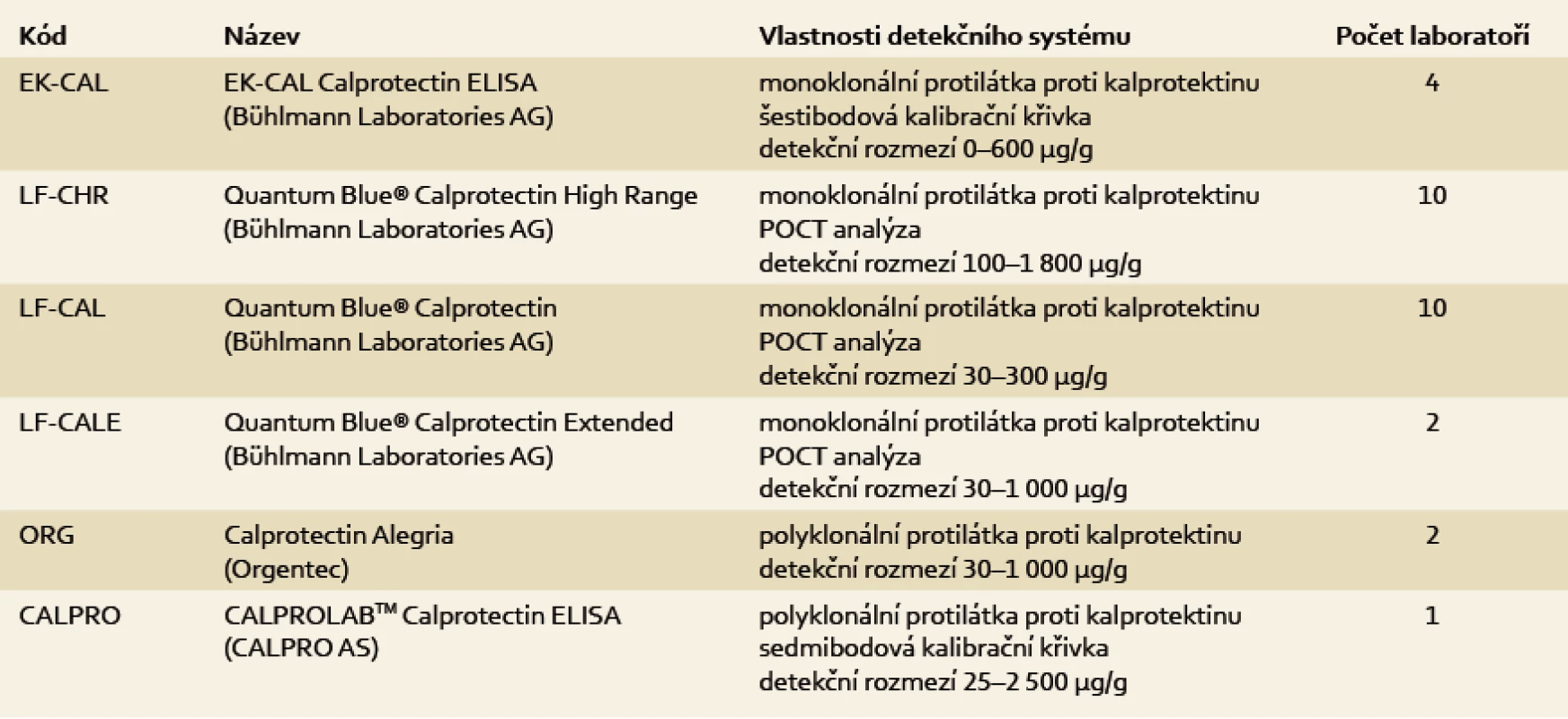
Výsledky
Kvalitativní hodnocení
Cílové hodnoty byly určeny konsenzuálním způsobem. Za konsenzus bylo označeno dosažení shody u alespoň 80 % všech účastníků, kteří uvedli platný výsledek (tab. 2).
Table 2. Kvalitativní hodnocení – souhrnné výsledky. Tab. 2. Qualitative assessment – the summary results. 
Vzorek A byl konsenzuálně označen jako negativní. Jedna laboratoř uvedla u vzorku A hraniční výsledek – v tomto případě musí být definitivní hodnocení učiněno s ohledem na interní referenční rozmezí laboratoře, nález rozhodně nelze označit za chybný. Dvě laboratoře uvedly chybně pozitivní výsledek.
Vzorek B byl konsenzuálně označen jako pozitivní, konsenzu bylo dosaženo ve 100 % případů.
Vzorek C označilo 80 % laboratoří jako hraniční. Tři laboratoře vykázaly negativní výsledek a tři laboratoře pozitivní výsledek. Jelikož se jednalo o nativní vzorek stolice, lze předpokládat možný problém v preanalytické fázi vyšetření při zhotovení eluátu.
Kvantitativní hodnocení
Statistická analýza byla provedena pomocí softwaru Statistica CZ 10.0 (Statsoft).
Pro kvantitativní výsledky, kde účastník uvedl výsledek v µg/g stolice, byla cílová hodnota definována jako aritmetický průměr výsledků všech účastníků (tab. 3 a 4).
Table 3. Kvantitativní hodnocení – souhrnné výsledky. Tab. 3. Quantitative assessment – the summary results. 
Table 4. Dosažené výsledky dle jednotlivých laboratoří. Tab. 4. The results achieved by individual laboratories. 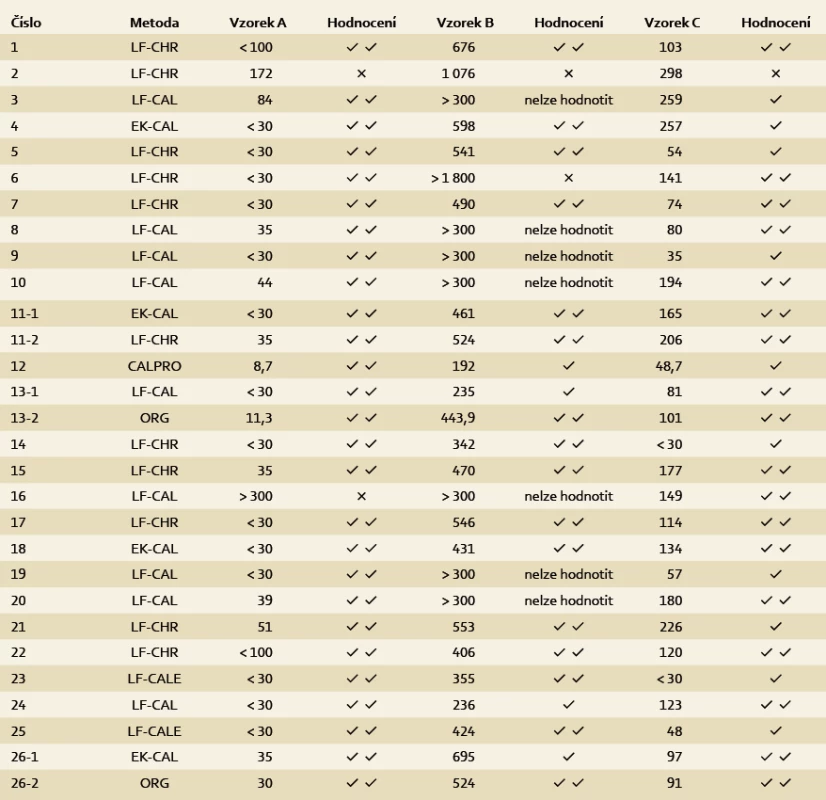
Hodnocení „velmi dobrý“ obdržela laboratoř při dosažení výsledku v rozmezí průměr ± 1 SD. Označení v tab.: ⌡.
Hodnocení „dobrý“ obdržela laboratoř při dosažení výsledku v rozmezí průměr ± 2 SD. Označení v tab.: ⌡.
Výsledky mimo rozmezí průměr ± ± 2 SD byly označeny jako neuspokojivé – v tab. 4 znázorněno jako x.
Co z uvedených výsledků vyplývá pro klinické gastroenterology? Především dobrá zpráva, že naprostá většina klinických laboratoří provádí vyšetření správně a že výsledky z různých laboratorních pracovišť jsou navzájem srovnatelné. Druhou důležitou informací pro kliniky je skutečnost, že detekční rozmezí používaných systémů se liší a že je na vzájemné domluvě klinického a laboratorního pracoviště, jak je pro klinika důležitá přesná kvantifikace pozitivních, negativních a hraničních vzorků.
Pro laboratorní pracoviště vyplývají z výsledků mezilaboratorního porovnání dvě důležité skutečnosti. Za prvé, ve srovnání s obvyklými imunoanalytickými metodami vyšetření krevního séra vyžaduje analýza fekálních vzorků mnohem větší pečlivost v preanalytické fázi vyšetření, při které hrozí zvýšené riziko preanalytické chyby – odběrem stolice počínaje přes správné uchovávání primárního vzorku až po přesné zhotovení eluátu. Na rozdíl od jiných biologických materiálů ovlivňuje složení vzorku stolice např. relativní poměr pevných a tekutých složek, který má vliv na nutné konstantní množství stolice pro testování, což rovněž může způsobit analytické chyby.Druhým poučením z letošního mezilaboratorního porovnání je situace s kvantifikací hladiny analytu u hraničního vzorku, ze které vyplývá doporučení retestovat vzorky ze „šedé zóny“ (s výsledky v rozmezí cca 40–150 µg/g) a vypracovat interní normy laboratoře.
Doručeno: 18. 5. 2014
Přijato: 16. 6. 2014
MUDr. Karin Malíčková
Klinická imunologie a alergologie – laboratoř
Ústav lékařské biochemie a laboratorní diagnostiky, 1. LF UK a VFN v Praze
Karlovo nám. 32, 121 11 Praha 2
kmali@lf1.cuni.cz
Labels
Paediatric gastroenterology Gastroenterology and hepatology Surgery
Article was published inGastroenterology and Hepatology
2014 Issue 6-
All articles in this issue
- Vedolizumab – nová antiintegrinová protilátka s vysokou gastrointestinální selektivitou
- OVESCO klip jako řešení komplikace ERCP
- Neobvyklý zdroj krvácení do gastrointestinálního traktu
- Problematika diferenciální diagnostiky autoimunitní formy pankreatitidy a pankreatického adenokarcinomu
- Standardní diagnostický a terapeutický postup chronické infekce virem hepatitidy C
- Doporučený postup diagnostiky a léčby chronické hepatitidy B
- Zpráva o celorepublikovém mezilaboratorním porovnání vyšetření fekálního kalprotektinu
- Podzimní pracovní den České hepatologické společnosti
- Karlovy Vary gastroenterologické – letos už potřinácté
- International professional competition Dr. Bares Award lived to see the 20th anniversary
- Poděkování recenzentům
- Zimní mix...
- Gastroenterology and Hepatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- OVESCO klip jako řešení komplikace ERCP
- Neobvyklý zdroj krvácení do gastrointestinálního traktu
- Vedolizumab – nová antiintegrinová protilátka s vysokou gastrointestinální selektivitou
- Karlovy Vary gastroenterologické – letos už potřinácté
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

