-
Medical journals
- Career
Prevalence protilátek proti SARS-CoV-2 u zaměstnanců Fakultní Thomayerovy nemocnice po první vlně covid-19
Authors: M. Ibrahimová 1; V. Jamriková 2; P. Sojka 1; Z. Khaznadar 1; K. Bořecká 2
Authors‘ workplace: Imunologická laboratoř, Fakultní Thomayerova nemocnice, Praha 1; Oddělení klinické biochemie, Fakultní Thomayerova nemocnice, Praha 2
Published in: Epidemiol. Mikrobiol. Imunol. 71, 2022, č. 1, s. 3-8
Category: Original Papers
Overview
Cíl práce: Zmapovat prevalenci protilátek proti SARS-CoV-2 u zaměstnanců Fakultní Thomayerovy nemocnice v Praze po první vlně nemoci covid-19. Právě ve Fakultní Thomayerově nemocnici bylo v první vlně ošetřeno a hospitalizováno velké množství osob s prokázanou infekcí covid-19.
Materiál a metody: Dobrovolná studie založená na dotazníkovém šetření a stanovení celkových protilátek (ECLIA, Roche) i jednotlivých tříd imunoglobulinů (ELISA IgG a IgA, Euroimmun).
Výsledky: Studie se zúčastnilo 808 zaměstnanců, z toho 2/3 z klinických pracovišť. U 15 účastníků, převážně zdravotních sester (n = 12), byly zjištěny pozitivní protilátky proti SARS-CoV-2 metodou ECLIA a pozitivní nebo hraniční protilátky ve třídě IgG metodou ELISA. Pozitivní nebo hraniční protilátky ve třídě IgA byly naměřeny u 12 osob. Většina osob s pozitivními protilátkami (n = 13) se nakazila virem SARS-CoV-2 na pracovišti po opakovaném kontaktu s pozitivními pacienty, u většiny (n = 12) byl těžší průběh nemoci, který však nevyžadoval hospitalizaci. Zaznamenali jsme pouze jednu asymptomatickou osobu s pozitivními protilátkami.
Závěry: Po první vlně covid-19 byly protilátky proti SARS-CoV-2 prokázány pouze u 1,9 % testovaných zaměstnanců Fakultní Thomayerovy nemocnice. Na klinických pracovištích byl podíl pozitivních zaměstnanců 2,3 % a na neklinických pouze 0,5 %. Nízká prevalence protilátek dokládá nízký počet nakažených zaměstnanců nemocnice a velmi dobrou úroveň všech hygienicko-epidemiologických opatření.
Klíčová slova:
zdravotníci – prevalence – protilátky – SARS-CoV-2 – COVID-19
ÚVOD
Pravděpodobně někdy v roce 2019 v provincii Chu-pej nastal bod nula celosvětové pandemie nového viru SARS-CoV-2. První člověk či menší skupina lidí se tímto virem nakazili minimálně o dva měsíce dříve, než bylo oficiálně oznámeno. Na konci roku 2019 už bylo pacientů s atypickou pneumonií ve Wu-chanu tolik, že bylo jasné, že se nejedná o žádné dosud známé infekční onemocnění. Začal závod s časem, tak jako např. v roce 2002 u příbuzného viru SARS-CoV. V tomto novém případě však bylo šíření viru mnohem rychlejší [1, 2]. Koncem ledna 2020 už WHO vyhlásila stav globální zdravotní nouze a v březnu celosvětovou pandemii [3].
Z epidemiologického hlediska je nejdůležitější znát způsob přenosu viru a mít možnost jeho jednoznačné detekce. Onemocnění covid-19 se snadno šíří vzdušnou cestou, rozhodující je koncentrace virových částic [4]. Samotná nákaza jedince pak záleží na hygieně rukou, izolační bariéře (zakrytí úst a nosu), na prostředí (vlhkost, teplota, uzavřený prostor, větrání) a na zdravotním stavu a imunitním systému příjemce. Je známo, že zakrytím úst a nosu se významně snižuje riziko přenosu, zato v uzavřené, nevětrané místnosti se riziko přenosu zvyšuje [5]. Hlavní příčinou hospitalizace při těžkém průběh covid-19 není mnohdy samotná nákaza virem SARS-CoV-2, ale jeho koexistence s dalšími chronickými onemocněními u nakažených osob [6].
V České republice (10,69 miliónů obyvatel) se virus SARS-CoV-2 poprvé objevil začátkem března 2020 a již 12. března byl vládou vyhlášen nouzový stav. První vlna epidemie zde vyvrcholila 11. dubna, kdy bylo za celé období zaznamenáno největší množství případů s prokázaným onemocněním, tj. 4 600. Po prvním přísném lockdownu se situace v červnu ustálila na hodnotě necelých 200 nových případů za den. Při této první vlně, která trvala přibližně od 1. března do 16. září, dosáhl celkový počet infikovaných osob v České republice hodnoty 41 034, což je 0,38 % všech obyvatel [7].
Předpokládá se, že z celkového počtu nakažených osob je téměř polovina bezpříznakových nebo s lehkým průběhem onemocnění a jen menšina má vážné příznaky vyžadující hospitalizaci [8]. Část asymptomatických osob vyvine protilátky v závislosti na indukční dávce viru [9]. Možnost, jak zpětně odhalit tuto část bezpříznakové skupiny, je existence jejich protilátkové odpovědi. Řada firem vyvinula různé testy na stanovení protilátek proti SARS-CoV-2 v krvi. Mezi prvními byla německá firma Euroimmun s ELISA testem stanovujícím protilátky ve třídě IgG nebo IgA proti S1 doméně spike proteinu viru. S dalším zajímavým a praktickým řešením přišla firma Roche, která v ECLIA testu použila sendvičovou metodu dvojitého nukleokapsidového antigenu vyvazující vysoce afinitní protilátky bez ohledu na třídu. Metoda byla plně automatizována pro rychlé zpracování do 18 minut.
První velká populační studie přítomnosti protilátek v české populaci PREVAL se konala v dubnu 2020, kde byly použity rychlotesty firmy Wantai [10]. Další menší studie následovaly [11, 12] a výzkum tvorby a dynamiky protilátek bude jistě dále pokračovat.
Naším cílem bylo zmapovat výskyt protilátek proti SARS-CoV-2 u všech zaměstnanců Fakultní Thomayerovy nemocnice (FTN) v Praze po první vlně nemoci covid-19. Hlavním důvodem bylo velké množství ošetřených, léčených a hospitalizovaných osob s RT-PCR prokázanou pozitivitou právě ve FTN.
MATERIÁL A METODY
Dobrovolné testování protilátek proti SARS-CoV-2 probíhalo ve FTN od 30. června do 7. září 2020. Každý účastník byl seznámen s cíli studie, podepsal informovaný souhlas a vyplnil dotazník, který obsahoval šest otázek. Jednalo se o informace o kontaktech s SARS-CoV-2 pozitivní osobou, suspektní osobou, používání osobních ochranných pracovních prostředků, existenci klinických symptomů a o případném testování pomocí RT-PCR a protilátkových Rapid testů. Projekt byl schválen Etickou komisí.
Účastníkům studie bylo odebráno standardním způsobem 5 ml srážlivé krve. Všechny vzorky byly následně změřeny pomocí soupravy Elecsys Anti-SARS-CoV-2 ECLIA (Roche) na analyzátoru Cobas 6000, modul e602. Jedná se o rychlé kvalitativní stanovení protilátek proti rekombinantnímu nukleokapsidovému antigenu. Pomocí elektrochemiluminiscenční koncovky jsou detekovány vyvázané protilátky všech imunoglobulinových tříd, především však vysoce afinitní IgG. Výsledek je vydán jako index COI (poměr signálu vzorku ku cut-off), COI ≥ 1,0 je považován za pozitivní. Senzitivita tohoto testu je podle výrobce po 14 dnech od pozitivního PCR testu 99,5% a specificita je 99,5% [13].
Všechny pozitivní výsledky byly dále konfirmovány Anti-SARS-CoV-2 ELISA testy IgG a IgA (Euroimmun). Jedná se o klasické sendvičové ELISA testy s navázanou rekombinantní S1 doménou spike proteinu. Vyvázané protilátky ze vzorku jsou detekovány pomocí sekundární protilátky proti IgG nebo IgA. Výsledek je vydáván jako poměr (R) mezi absorbancí vzorku a kalibrátoru. R ≥ 1,1 je považován za pozitivní, R ≥ 0,8 < 1,1 hraniční a R < 0,8 negativní. Senzitivita Anti-SARS-CoV-2 ELISA IgG je podle výrobce po 21 dnech od pozitivního PCR testu 93,8 % a specificita 99,6 %. Po 21 dnech od pozitivního PCR testu je senzitivita Anti-SARS-CoV-2 ELISA IgA 100 % a specificita 92,4 % [14, 15].
Statistická data byla zpracována na oddělení Lékařské statistiky IKEM, Praha. K vyhodnocení byly použity Fisherův exaktní test a McNemarův test.
Výsledky: Celkem bylo otestováno 808 osob, z toho 713 žen a 95 mužů jak z klinických, tak ostatních pracovišť FTN. Věkový medián účastníků byl 45 let (20 až 76 let), výrazně převažovaly ženy (713 žen = 88,2 % všech účastníků). Ze všech testovaných mělo pouze 15 osob pozitivní protilátky proti SARS-CoV-2, z toho 13 žen a 2 muži. Celkově byl tedy podíl pozitivních 1,9 % (tabulka 1).
Table 1. Vliv věku a pohlaví na pozitivitu anti-SARS-CoV-2 protilátek
Table 1. Effect of age and sex on the positivity for anti-SARS-CoV-2 antibodies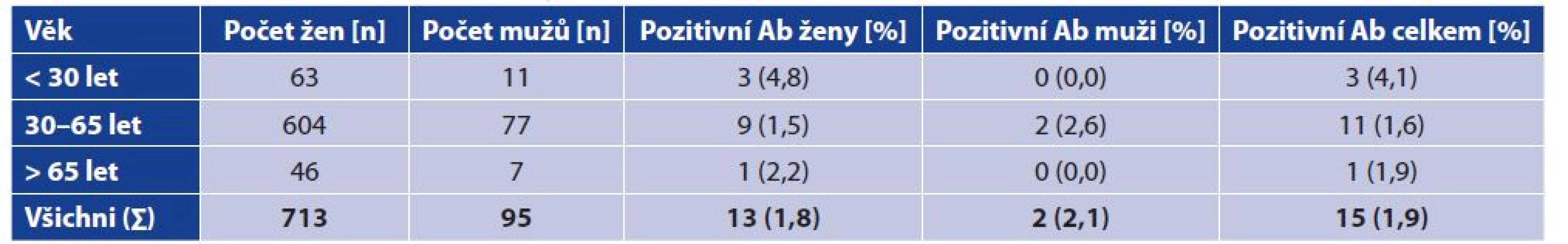
Fisherův exaktní test: p = 0,1475; vliv věku na pozitivitu Ab neprokázán
Fisherův exaktní test: p = 0,5490; vliv pohlaví na pozitivitu Ab neprokázán
Fisher’s exact test: p = 0.1475; effect of age on Ab positivity not shown
Fisher’s exact test: p = 0.5490; effect of sex on Ab positivity not shownVšichni pozitivně testovaní v dotazníku uvedli, že používali osobní ochranné pracovní prostředky podle aktuálně platných doporučení. Soubor pozitivních tvořili dva lékaři, dvanáct zdravotních sester ze tří klinických pracovišť a jedna sociální pracovnice uvedená v tabulce 2 v kategorii ostatní.
Table 2. Vliv profese na pozitivitu anti-SARS-CoV-2 protilátek
Table 2. Effect of staff category on the positivity for anti-SARS-CoV-2 antibodies
Fisherův exaktní test: p = 0,1329; vliv profese na pozitivitu Ab neprokázán
Fisher’s exact test: p = 0.1329; effect of staff category on Ab positivity not shownKromě jednoho lékaře a jedné sestry, kteří se nakazili pravděpodobně od rodinného příslušníka, se ostatní nakazili na pracovišti od pozitivních pacientů. Všichni uvedli opakovaný kontakt. Z celkového počtu 180 zaměstnanců, kteří se setkali se SARS-CoV-2 pozitivním člověkem (147 s pozitivním pacientem, 26 s pozitivním spolupracovníkem, 7 s pozitivním rodinným příslušníkem), se nakazilo jen 15 osob, tj. 8,3 % (tabulka 3).
Table 3. Vliv kontaktu na pozitivitu anti-SARS-CoV-2 protilátek
Table 3. Effect of contact on the positivity for anti-SARS-CoV-2 antibodies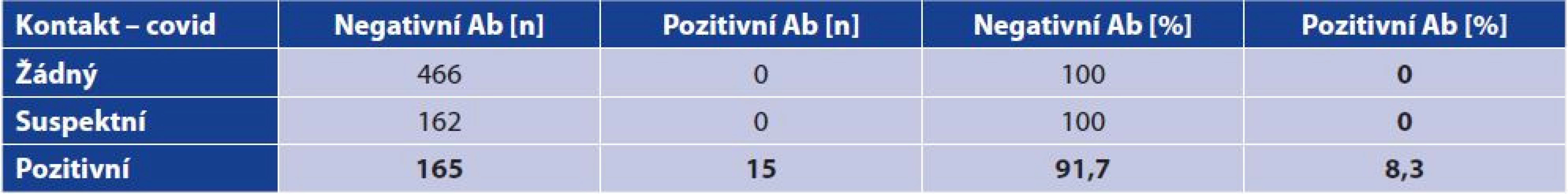
Fisherův exaktní test: p < 0,0001; vliv kontaktu na pozitivitu Ab prokázán
Fisher’s exact test: p < 0.0001; effect of contact on Ab positivity not shownJe zajímavé, že 131 respondentů (16,2 %) v dotazníku uvedlo, že během sledovaného období se u nich objevily některé symptomy onemocnění covid-19: kašel, teplota > 37,3 °C, zimnice, dušnost, bolest svalů a kloubů, ztráta chuti a čichu, průjem a zvracení. U 52 (6,4 %) byly symptomy těžší a byly důvodem pracovní neschopnosti a u 79 (9,8 %) byly lehčí, trvající kratší dobu. Protilátky však byly u většiny (n = 117) negativní, proto se pravděpodobně jednalo o jinou příčinu onemocnění. Pouze u 15 osob byly prokázány pozitivní protilátky anti-SARS-CoV-2. Ve skupině s těžšími symptomy mělo protilátky 12 osob (23,1 %) a ve skupině s lehčími příznaky jen 2 muži (2,5 %) s mírnou bolestí v krku a únavou. Zaznamenali jsme pouze jednu asymptomatickou osobu s prokázanými pozitivními protilátkami (tabulka 4).
Table 4. Vztah mezi symptomy a pozitivitou anti-SARS-CoV-2 protilátek
Table 4. Correlation between symptoms and the positivity for anti-SARS-CoV-2 antibodies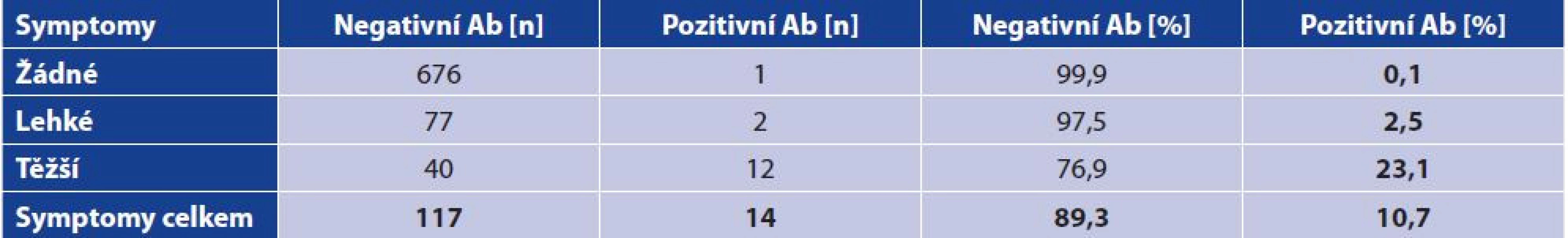
Fisherův exaktní test: p < 0,0001; vztah mezi symptomy a pozitivitou Ab prokázán
Fisher’s exact test: p < 0.0001; correlation between symptoms and Ab positivity shownPřímý průkaz viru pomocí RT-PCR je považován za jediný správný diagnostický nástroj pro potvrzení diagnózy covid-19. Ze začátku pandemie poptávka po testování převyšovala testovací kapacitu FTN, proto část vzorků byla testována v jiných laboratořích. Některé sporné výsledky byly konfirmovány v Národní referenční laboratoři. Informace o výsledcích RT-PCR byly součástí dotazníku. Celkem bylo pomocí RT-PCR otestováno 214 účastníků studie, tj. 26,5 % všech, 14 bylo pozitivních a 200 negativních. Z 15 osob, které měly pozitivní protilátky, uvedlo 12 pozitivní a 3 negativní RT-PCR test (tj. 1,5 % z PCR-negativních). Z těchto 3 osob měla jedna těžší, jedna lehčí a jedna žádné klinické symptomy. Na druhou stranu 2 osoby (1 se symptomy a 1 asymptomatická) uvedly pozitivní výsledek RT-PCR testu, ale protilátky byly negativní (tabulka 5 14,3 % z PCR-pozitivních). Celková shoda mezi RT-PCR testem a protilátkami stanovenými pomocí ECLIA testu byla vysoká (97,7 %).
Table 5. Vztah mezi RT-PCR SARS-CoV-2 a anti-SARS-CoV-2 protilátkami stanovených ECLIA
Table 5. Correlation between RT-PCR SARS-CoV-2 positivity and ECLIA anti-SARS-CoV-2 antibodies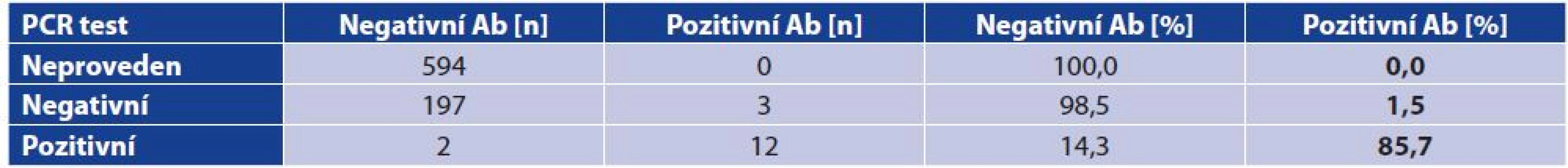
Fisherův exaktní test: p < 0,0001; vztah mezi PCR a pozitivitou Ab prokázán
Fisher’s exact test: p < 0.0001; correlation between RT-PCR positivity and Ab detection shownPatnáct vzorků, ve kterých byla zjištěna pozitivita anti - SARS-CoV-2 protilátek pomocí ECLIA, bylo následně konfirmováno ELISA testy, které stanovují separátně IgG a IgA anti-SARS-CoV-2 protilátky (tabulka 6). Bylo potvrzeno 13 pozitivních a 2 hraniční výsledky ve třídě IgG (celkem 100 %) a 9 pozitivních, 2 hraniční (celkem 73 %) a 4 negativní (27 %) ve třídě IgA. Vysoká shoda výsledků potvrzuje především vysoce afinitní IgG protilátky detekované v použitém screeningovém testu ECLIA a jeho vhodné použití pro séroprevalenční studie.
Table 6. Pozitivní protilátky stanovené pomocí ECLIA – vztah k jednotlivým třídám IgG a IgA v ELISA
Table 6. ECLIA positivity for antibodies – correlation with ELISA IgG and IgA antibodies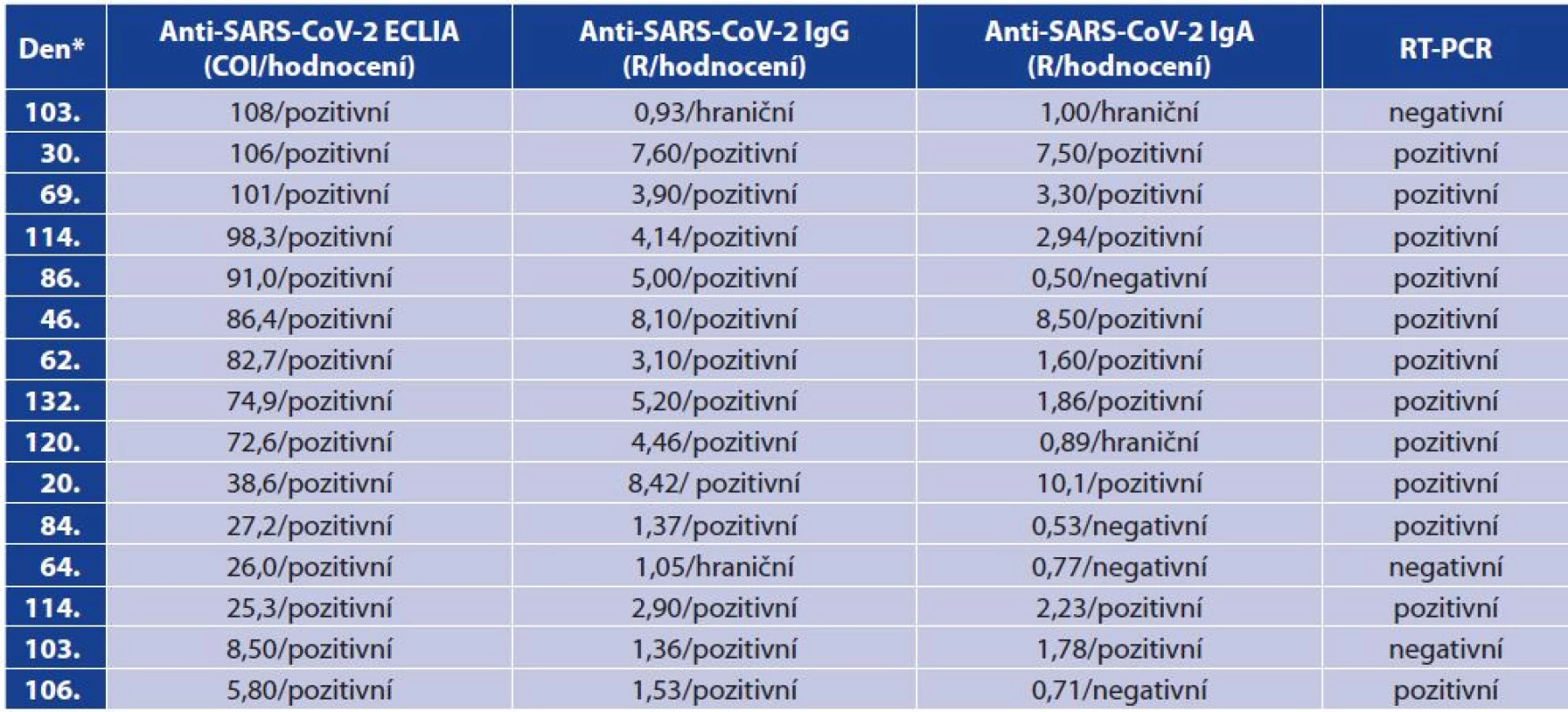
*Den odběru protilátek počítaný od RT-PCR testu
*Sampling day from RT-PCR assayU dvou vzorků s ECLIA negativními protilátkami bylo v dotazníku uvedeno pozitivní RT-PCR. První vzorek byl negativní ve všech třech protilátkových testech po 100 dnech od PCR testu a účastník neměl žádné klinické příznaky (tabulka 7, 1. vzorek). Druhý vzorek se při stanovení protilátek pomocí testu ECLIA pohyboval velmi těsně pod hranicí pozitivity, což odpovídalo hraničním protilátkám ve třídě IgG změřené v ELISA testu. Protilátky ve třídě IgA byly pozitivní. U tohoto účastníka byl opakován odběr po osmi dnech (38. den do PCR) se stejným výsledkem (tabulka 7, 2. vzorek). Jednalo se o účastníka s pozitivním rodinným kontaktem a klinickými symptomy (ztráta čichu).
Table 7. Sporné výsledky protilátek vzhledem k pozitivitě RT-PCR
Table 7. Contradictory antibody results vs RT-PCR positivity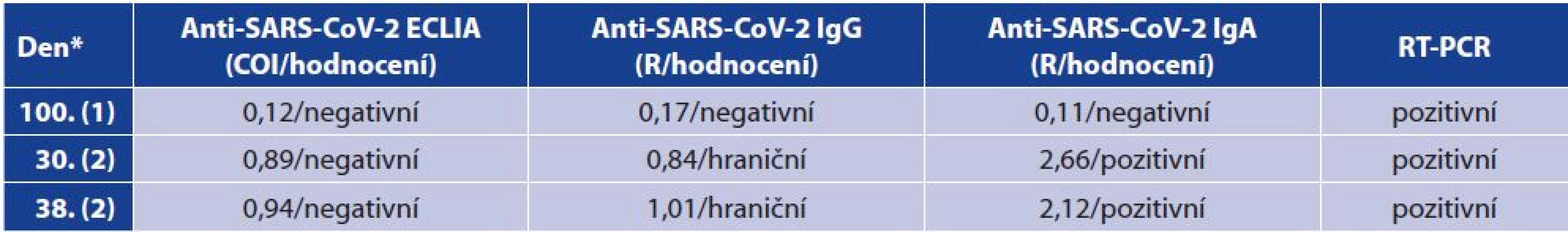
*Den odběru protilátek počítaný od RT-PCR testu, u vzorku (1) jeden odběr, u vzorku (2) dva odběry
*Sampling day from RT-PCR assay, sample (1) one collection, sample (2) two collectionsÚčastníci studie kromě RT-PCR uváděli také údaje o testování protilátek proti SARS-CoV-2 pomoci POCT Rapid testů. Jednalo se o testování na různých místech (FTN, IKEM, aj.), pravděpodobně i různými testy dostupnými v první vlně pandemie v ČR, podrobnější informace nebylo možné dohledat. Takto bylo celkem testováno 72 osob, což je 8,9 % všech účastníků studie. Výsledky potvrzují nižší senzitivitu těchto testů, resp. 70 % a vysokou specificitu dosahující 100 % (tabulka 8).
Table 8. Vztah mezi RT-PCR a pozitivitou anti-SARS-CoV-2 protilátek stanovených Rapid testem
Table 8. Correlation between RT-PCR positivity and rapid test positivity for anti-SARS-CoV-2 antibodies
McNemarův test: p = 0,0833; nezamítli jsme hypotézu, že testy dávají shodné výsledky.
McNemara’s test: p = 0.0833; we have not rejected the hypothesis that the tests yield concordant results.DISKUSE
Při první vlně onemocnění covid-19 bylo ve Fakultní Thomayerově nemocnici ošetřeno podstatné množství pacientů z Prahy a ze Středočeského kraje [7]. Do začátku září zde bylo hospitalizováno celkem 100 pacientů, 50 žen a 50 mužů. Personál nemocnice byl tedy jeden z prvních, který musel čelit nebezpečí souvisejícímu s dosud neznámým virovým onemocněním. FTN má celkem cca 2 500 zaměstnanců. Většina těch, kteří měli klinické příznaky anebo byli v přímém kontaktu s pozitivními pacienty, byla testována pomocí RT-PCR na SARS-CoV-2 (přibližně 1/4). Jednalo se především o lékaře, sestry a pomocný personál z klinických oddělení. Ze všech PCR testovaných bylo 31 pozitivních, což je 1,2 % všech zaměstnanců. Cílem této studie bylo zpětně zjistit celkový počet infikovaných zaměstnanců v prvních 6 měsících pandemie, včetně netestovaných PCR a asymptomatických.
Do dobrovolné prevalenční studie se přihlásila jedna třetina všech zaměstnanců. Počet pozitivních zaměstnanců ve FTN byl ve srovnání s ostatními nemocnicemi v ČR [16], ale i ve světě [17, 18] relativně nízký (1,9 %). Poněkud vyšší prevalence protilátek, již srovnatelná s obdobnými studiemi v ČR (12), je zachycena při hodnocení účastníků pouze z klinických pracovišť (2,3 %). Při ošetřování prvního pozitivního pacienta, u něhož z anamnézy nevyplývalo podezření na covid-19 a zaměstnanci měli pouze standardní osobní ochranné prostředky, došlo k první nákaze personálu. Poté byl zaveden přísný hygienicko-epidemiologický režim.
Všichni účastníci studie potvrdili používání osobních ochranných pracovních prostředků. Dva zdravotničtí pracovníci uvedli primární kontakt v rodině, 13 pracovníků uvedlo jako zdroj nákazy opakovaný kontakt s pozitivními pacienty nebo spolupracovníky. Nejvíce nakažených (12) bylo mezi zdravotními sestrami (10 žen a 2 muži) ve věku mezi 27 až 58 roky. Na neklinických pracovištích nebyla infekce prokázána, kromě jedné sociální pracovnice, která byla v opakovaném kontaktu s pozitivním pacientem. Nenakazil se nikdo z testovaných, kdo by o kontaktu nevěděl, ani nikdo, kdo byl v kontaktu se suspektní osobou. Potvrdili jsme stejně jako v jiných prevalenčních studiích, že není statisticky významný rozdíl mezi procentem nakažených žen a mužů [19].
Průběh onemocnění u pozitivně testovaných účastníků studie byl většinou těžší, spojený s pracovní neschopností. Nikdo však nebyl hospitalizován. Ze symptomů převažovaly subfebrilie, bolest hlavy, únava, ztráta čichu a chuti, u čtyř probandů také gastrointestinální symptomy (nevolnost, bolest žaludku, průjem). Pouze u dvou účastníků byl průběh velmi mírný, u jednoho zcela asymptomatický.
Stanovení protilátek anti-SARS-CoV-2 je v současnosti jediná cesta, jak zpětně potvrdit prodělanou infekci a detekovat protilátkovou odpověď organismu. Neméně důležitá buněčná imunitní odpověď zůstává ve stínu právě proto, že její vyšetření je obtížné a není dosud rutinně dostupné. Z protilátkových testů jsme vybrali ECLIA (Roche) jako rychlý screeningový test. Jeho výhody a možnost následné konfirmace pomocí IgG ELISA (Euroimmun) jsme prokázali v předcházejícím porovnání [20].
Podobně jako v jiných studiích byla IgG protilátková odpověď potvrzena u všech, kteří prodělali covid-19 nezávisle na tíži a délce onemocnění [21, 22]. U všech účastníků studie byly protilátky stanoveny minimálně po 20 dnech od provedeného PCR testu, maximálně pak po 132 dnech. V testovaných vzorcích byly protilátky po čtyřech měsících stále přítomny. Bylo publikováno, že již od 5.–14. dne dochází k poměrně rychlému nárustu protilátek ve všech imunoglobulinových třídách najednou [23]. Zatímco protilátky IgG dlouhodobě přetrvávají, odpověď ve třídě IgA je u některých jedinců krátkodobější, ale u jiných zůstává zachována. Zdali tato dynamika protilátek IgA v periferní krvi má nějaký význam, není zatím jasné. Pro základní diagnostiku prodělaného onemocnění covid-19 je zatím postačující stanovení protilátek IgG nebo specifických protilátek bez rozlišení tříd.
Studie potvrdila vysokou shodu mezi RT-PCR a stanovením protilátek proti SARS-CoV-2 (97,7 %). Tři účastníci s pozitivními protilátkami uvedli v dotazníku negativní RT-PCR test. Zde nelze vyloučit špatné provedení nebo načasování nazofaryngeálního stěru [24]. Pouze jeden účastník studie měl pozitivní přímý průkaz viru a negativní protilátky potvrzené všemi třemi testy. U asymptomatických osob mohou být detekovány negativní protilátky. Může se jednat o kontakt s malou virovou náloží nebo o vrozené genetické vybavení (vnímavost) jedince [25, 26].
Uvádíme také výsledky testování protilátek pomocí Rapid testů, jako připomínku dnes již známého faktu, že tyto testy používané v první fázi pandemie byly orientační a pro konečný průkaz prodělané infekce covid - 19 nejsou zcela vhodné [27].
ZÁVĚRY
Po sto letech od konce poslední velké celosvětové pandemie španělské chřipky se lidstvo setkává s novým onemocněním covid-19. Dnes je to již pandemie v globálním měřítku, což obnáší urychlenou snahu o její zastavení. Lidé pracující ve zdravotnictví se s touto nemocí setkávají jako první a jsou také nejvíce ohroženi. Tato studie ukázala poměrně nízký počet infikovaných zdravotníků FTN při první vlně covid-19. Je velmi důležité stanovit promořenost populace pomocí protilátek ještě před chystanou vakcinací, proto Fakultní Thomayerova nemocnice bude ve sledování zdravotníků dále pokračovat.
Poděkování
Děkujeme všem, kteří se do této studie zapojili, ale především těm, kteří se na zvládání pandemie covid-19 aktivně podíleli.
Studie byla podpořena MZ ČR – RVO („Thomayerova nemocnice – TN, 00064190“).
Do redakce došlo dne 27. 1. 2021.
Adresa pro korespondenci:
RNDr. Markéta Ibrahimová, Ph.D.
Imunologická laboratoř, Fakultní Thomayerova nemocnice
Vídeňská 800
140 59 Praha 4
e-mail: marketa.ibrahimova@ftn.cz
Sources
1. Liu YC, Kuo RL, Shih SR. COVID-19: The first documented coronavirus pandemic in history. Biomed J., 2020;43(4):328–333.
2. Li Q, Guan X, Wu P, et al. Early Transmission Dynamics in Wuhan, China, of Novel Coronavirus-Infected Pneumonia. N Engl J Med., 2020;382(13):1199–1207.
3. Bchetnia M, Girard C, Duchaine C, et al. The outbreak of the novel severe acute respiratory syndrome coronavirus 2 (SARS - -CoV-2): A review of the current global status. J Infect Public Health, 2020;13(11):1601–1610.
4. Sagnelli C, Celia B, Monari C, et al. Management of SARS-CoV-2 pneumonia [published online ahead of print, 2020 Aug 28]. J Med Virol., 2020;10.1002/jmv.26470.
5. Prather KA, Wang CC, Schooley RT. Reducing transmission of SARS-CoV-2. Science, 2020;368(6498):1422–1424.
6. Young BE, Ong SWX, Kalimuddin S, et al. Epidemiologic Features and Clinical Course of Patients Infected With SARS-CoV-2 in Singapore. JAMA, 2020;323(15):1488–1494.
7. Komenda M, Karolyi M, Bulhart V, et al. COVID‑19: Přehled aktuální situace v ČR. Onemocnění aktuálně [online]. Praha: Ministerstvo zdravotnictví ČR, 2020 [cit. 12.12.2020]. Dostupné na www:www:<https:// onemocneni-aktualne.mzcr.cz/covid-19. ISSN 2694-9423.
8. Oran DP, Topol EJ. Prevalence of Asymptomatic SARS-CoV-2 Infection: A Narrative Review. Ann Intern Med., 2020;173(5):362 – 367.
9. Nikolai LA, Meyer CG, Kremsner PG, et al. Asymptomatic SARS Coronavirus 2 infection: Invisible yet invincible. Int J Infect Dis., 2020;100 : 112–116.
10. Studie kolektivní imunity SARS-CoV-2-CZ-Preval [online]. Praha: ÚZIS ČR, 2020. Dostupné na www:<https://covid-imunita.uzis.cz/.
11. Malickova K, Kratka Z, Luxova S, et al. Anti-SARS-CoV-2 antibody testing in IBD healthcare professionals: are we currently able to provide COVID-free IBD clinics? Scand J Gastroenterol., 2020;55(8):917–919.
12. Krátká Z, Luxová Š, Malíčková K, et al. Testing for COVID-19: a few points to remember. Testování COVID-19 – co bychom měli mít na paměti. Cas Lek Cesk., 2020;159(2):72–77.
13. Elecsys Anti-SARS-CoV-2. Příbalová informace, 2020-11, V3.0; Material Numbers 09203095190.
14. EUROIMMUN Anti-SARS-CoV-2 ELISA IgG. Příbalová informace El_2606G_A_CZ_ C04.docx Verze: 2020-05-07.
15. EUROIMMUN Anti-SARS-CoV-2 ELISA IgA. Příbalová informace El_2606A_A_CZ_ C04.docx Verze: 2020-05-07.
16. Krátká Z, Fürst T. Světlo na konci tunelu? Počet lidí s protilátkami proti koronaviru v ČR rychle stoupá. ,Dostupné na www:<https://prolekare.cz/.
17. Steensels D, Oris E, Coninx L, et al. Hospital-Wide SARS-CoV-2 Antibody Screening in 3056 Staff in a Tertiary Center in Belgium. JAMA, 2020;324(2):195–197.
18. Jeremias A, Nguyen J, Levine J, et al. Prevalence of SARS-CoV-2 Infection Among Health Care Workers in a Tertiary Community ,Hospital [published online ahead of print, 2020 Aug 11]. JAMA ,Intern Med., 2020;e204214.
19. Plebani M, Padoan A, Fedeli U, et al. SARS-CoV-2 serosurvey in health care workers of the Veneto Region. Clin Chem Lab Med., 2020;58(12):2107–2111.
20. Bořecká K, Jamriková V, Sojka P, et al. Stanovení protilátek anti - SARS-CoV-2 nukleokapsid versus spike, ECLIA versus ELISA. Klin Biochem Metab., 2021;29(1):19–24.
21. Deeks JJ, Dinnes J, Takwoingi Y, et al. Antibody tests for identification of current and past infection with SARS-CoV-2. Cochrane Database Syst Rev., 2020;6(6):CD013652. Published 2020 Jun 25.
22. Wellinghausen N, Plonné D, Voss M, et al. SARS-CoV-2-IgG response is different in COVID-19 outpatients and asymptomatic contact persons. J Clin Virol., 2020;130 : 104542.
23. Isho B, Abe KT, Zuo M, et al. Persistence of serum and saliva antibody responses to SARS-CoV-2 spike antigens in COVID-19 patients. Sci Immunol., 2020;5(52):eabe5511. doi:10.1126/sciimmunol. abe5511.
24. Kucirka LM, Lauer SA, Laeyendecker O, et al. Variation in False-Negative Rate of Reverse Transcriptase Polymerase Chain Reaction-Based SARS-CoV-2 Tests by Time Since Exposure. Ann Intern Med., 2020;173(4):262–267.
25. Wang Y, Zhang L, Sang L, et al. Kinetics of viral load and antibody response in relation to COVID-19 severity. J Clin Invest., 2020;130(10):5235–5244.
26. Goetz L, Yang J, Greene W, et al. A COVID-19 Patient with Repeatedly Undetectable SARS-CoV-2 Antibodies. J Appl Lab Med., 2020;5(6):1401–1405.
27. Döhla M, Boesecke C, Schulte B, et al. Rapid point-of-care testing for SARS-CoV-2 in a community screening setting shows low sensitivity. Public Health, 2020;182 : 170–172.
Labels
Hygiene and epidemiology Medical virology Clinical microbiology
Article was published inEpidemiology, Microbiology, Immunology

2022 Issue 1-
All articles in this issue
- Prevalence protilátek proti SARS-CoV-2 u zaměstnanců Fakultní Thomayerovy nemocnice po první vlně covid-19
- Pokles hladiny neutralizačních protilátek proti SARS-CoV-2 po očkování u seniorů: výsledky observační studie v Jihomoravském kraji
- Charakteristiky bezdomovců hospitalizovaných ve zdravotnických zařízeních v České republice v letech 2006–2015
- Přehled základních epidemiologických charakteristik a deskriptivní analýza výskytu humánní yersiniózy v České republice v letech 2018–2020
- Epidemie spalniček 2017 až 2019 – začátek molekulární surveillance v České republice
- Probiotiká ďalšej generácie: prehľad najperspektívnejších kandidátov
- Detekce Borrelia miyamotoi v klíšťatech Ixodes ricinus na jižní Moravě – riziko pro veřejné zdraví
- Blahopřání k životnímu jubileu RNDr. Petra Petráše, CSc.
- Epidemiology, Microbiology, Immunology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Probiotiká ďalšej generácie: prehľad najperspektívnejších kandidátov
- Přehled základních epidemiologických charakteristik a deskriptivní analýza výskytu humánní yersiniózy v České republice v letech 2018–2020
- Charakteristiky bezdomovců hospitalizovaných ve zdravotnických zařízeních v České republice v letech 2006–2015
- Pokles hladiny neutralizačních protilátek proti SARS-CoV-2 po očkování u seniorů: výsledky observační studie v Jihomoravském kraji
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

