-
Medical journals
- Career
Incidentálna fokálna idiopatická sklerozujúca mezenteritída u 4-mesačného dieťaťa
Authors: Silvia Farkašová Iannaccone 1; Peter Švajdler 2; Dorota Sopková 1; Lucia Fröhlichová 2; Daniel Farkaš 3
Authors‘ workplace: Ústav súdneho lekárstva UPJŠ LF, Trieda SNP č. 1, Košice 1; Oddelenie patológie, Univerzitná nemocnica Louisa Pasteura, Košice 2; Úrad pre dohľad nad zdravotnou starostlivosťou, SLaPA pracovisko, Ipeľská 1, Košice 3
Published in: Čes.-slov. Patol., 55, 2019, No. 4, p. 235-238
Category: Original Articles
Overview
Sklerozujúca mezenteritída je zriedkavé nenádorové ochorenie postihujúce mezentérium tenkého čreva, vyskytujúce sa prevažne vo vyššom veku. Etiológia ochorenia nie je jednoznačne známa. Klinické príznaky sú veľmi variabilné a zahŕňajú bolesti brucha, distenziu brušnej steny, nauzeu, zvracanie. V článku popisujeme prípad 4-mesačného chlapca, ktorý náhle a neočakávane zomrel doma. Na základe vyšetrených okolností, výsledkov toxikologických a histologických vyšetrení bol prípad uzavretý ako syndróm náhleho úmrtia dojčaťa. Dieťa malo počas života opakované bolesti brucha sprevádzané jeho distenziou. Ako vedľajší nález bolo pri pitve zistené výrazné ložiskové zhrubnutie mezentéria terminálnej časti ilea v dĺžke 2,5 cm, pričom zhrubnutie dosahovalo až 1,5 cm a postihovalo takmer polovicu obvodu tenkého čreva. V práci popisujeme nález pravdepodobne najmladšieho jedinca postihnutého týmto ochorením spomenutého v dostupnej literatúre.
Klíčová slova:
sklerozujúca mezenteritída – fibrinoidná nekróza – SIDS
Sklerozujúca mezeneteritída (SM) je zriedkavé nenádorové ochorenie postihujúce mezentérium tenkého čreva, pričom priemerný vek postihnutia je 55 – 65 rokov (1,2). Zriedkavejšie sa táto chorobná jednotka vyskytuje aj v detskom veku (3). Ochorenie môže prebiehať asymptomaticky alebo sa prejavovať rôznymi symptómami, ako napríklad bolesťou brucha, distenziou brucha, nauzeou, zvracaním. Patofyziológia ochorenia ostáva neznáma. Napriek tomu, že ide o relatívne benígne ochorenie, až v 20 % prípadov môže mať vysilujúci priebeh končiaci smrťou, či už v dôsledku komplikácií SM, alebo jej liečby (2,4). V kazuistike popisujeme incidentálny nález pravdepodobne najmladšieho jedinca spomenutého v dostupnej literatúre.
OPIS PRÍPADU
Išlo o 4-mesačného chlapca (dĺžka 66 cm, hmotnosť 5,125 kg), ktorý sa narodil ako druhé dieťa 25-ročnej matky. Mal jednu staršiu 2,5-ročnú zdravú sestru. Podľa výpovede matky počas života horšie prijímal potravu. Pochádzal zo sociálne slabšieho prostredia, žil v chatrči s pieckou na drevo. Ako dvojmesačný bol pomocou ultrasonografie vyšetrený u pediatra pre pretrvávajúce bolesti brucha, opakované dávenie, avšak týmto vyšetrením v tom čase nebol zistený žiadny patologický proces. Deň pred smrťou malo dieťa vyklenuté brucho a veľa plakalo. Opakovanými návštevami lekára okrem konštatovania, že žije v nevyhovujúcich životných podmienkach, neboli zistené žiadne závažnejšie ochorenia, resp. prejavy zanedbávania, týrania alebo úrazového poškodenia.
Pitva bola vykonaná na druhý deň po smrti. Koža bola mierne znečistená, brucho distendované, ľahko sa vyklenovalo nad úroveň hrudníka a v dolnej tretine už malo svetlozelený odtieň. Na tele nebohého pri pitve neboli zistené žiadne čerstvé alebo hojace sa kožné odreniny, alebo krvné podliatiny, taktiež neboli zistené zjavné vrodené vývinové anomálie. Výsledky toxikologických vyšetrení na prítomnosť bežne užívaných skupín liekov, prchavých látok, methemoglobínu, ktoré by mohli spôsobiť smrť, boli negatívne. Vzhľadom na vyšetrené okolnosti úmrtia bolo realizované aj spektroskopické vyšetrenie množstva karboxyhemoglobínu s negatívnym výsledkom.
Pitvou a následným histologickým vyšetrením sme v pľúcach zistili recentné krvné výrony do pľúc, puzdra týmusu a epikardu, na mitrálnej chlopni izolované hemoragické Luschkove teliesko. Vzhľadom na vyšetrené okolnosti úmrtia dieťaťa výsledkom laboratórnych a histologických vyšetrení sme daný prípad uzavreli ako syndróm náhleho úmrtia dojčaťa.
V brušnej dutine bolo s výnimkou ileocekálnej oblasti prítomné rozšírenie tenkého a hrubého čreva. Ich slizničný povrch bol mierne autolyzovaný, avšak bez zjavného viditeľného patologického poškodenia. Tesne pred ileocekálnou chlopňou boli seróza a mezentérium terminálneho ilea na ploche 2 x 0,7 cm mapovito začervenané, pričom v dĺžke 2,5 cm boli výrazne tuhé, zhrubnuté od subserózy ilea až po radix mesenterii (obr. 1). Makroskopicky malo zhrubnutie na kolmých rezoch klinovitý, trojuholníkovitý tvar s bázou na seróze čreva a vrcholom smerujúcim k úponu radixu (obr. 2), malo sivastohnedú farbu a po fixácii vo formole dosahovalo zhrubnutie v oblasti serózy 1,2 – 1,5 cm. Zhrubnutie sa končilo vo vzdialenosti 1,5 cm pred Bauhinskou chlopňou. Ostatné časti závesného aparátu tenkého čreva boli jemné, blanovité. Histologickým vyšetrením série rezov zhrubnutej oblasti sme zistili výraznú fibrózu, pričom v centrálnej časti boli pôvodné súčasti mezentéria (cievy, nervy, tukové tkanivo). Fibrotické zhrubnutie subserózy postihovalo takmer polovicu obvodu čreva (obr. 3). Centrálna oblasť zhrubnutia bola tvorená hypocelulárnou, storiformnou, na kolagén bohatou fibroblastickou proliferáciou bez signifikantnejšieho zápalového infiltrátu (obr. 4). Periférne oblasti boli naopak tvorené relatívne celulárnou, na kolagén chudobnou fibroblastickou proliferáciou (obr. 5), ložiskovo s pomerne výraznou zmiešanou chronickou zápalovou celulizáciou s prevahou plazmatických buniek (obr. 6) a ojedinelými siderofágmi. Penovité makrofágy, nekróza tukového spojiva a ani obliteratívna flebitída neboli zachytené. Proliferácia bola bohatá na početné iregulárne distribuované tenkostenné cievy malého a stredného kalibru. Imunohistochemicky sme sa pomocou protilátok IgG4, MUM1 a CD138 pokúsili stanoviť absolútny počet IgG4 pozitívnych plazmocytov v jednom veľkom zornom poli, ako aj pomerné zastúpenie IgG4 pozitívnych plazmocytov k celkovému počtu všetkých plazmocytov, výsledok vyšetrenia však bol opakovane falošne negatívny, najskôr ako dôsledok autolýzy so stratou antigenicity tkaniva. Ďalším zaujímavým nálezom bol fokálny obraz fibrinoidnej nekrózy stien ciev malého kalibru (obr. 7) pozitívnych imunohistochemickým farbením pomocou protilátky CD34 s intramurálnymi depozitmi PAS-pozitívneho (obr. 8), diastáza rezistentného fibrinoidného materiálu a so sprievodnou leukocytokláziou v okolí. Na základe tohto obrazu sme nález uzavreli ako sklerozujúcu mezenteritídu, ktorá mohla byť u dieťaťa príčinou pretrvávajúcich bolestí brucha sprevádzaných jeho distenziou.
Image 1. Ileocekálna oblasť so zhrubnutím terminálneho mezentéria (šípky). 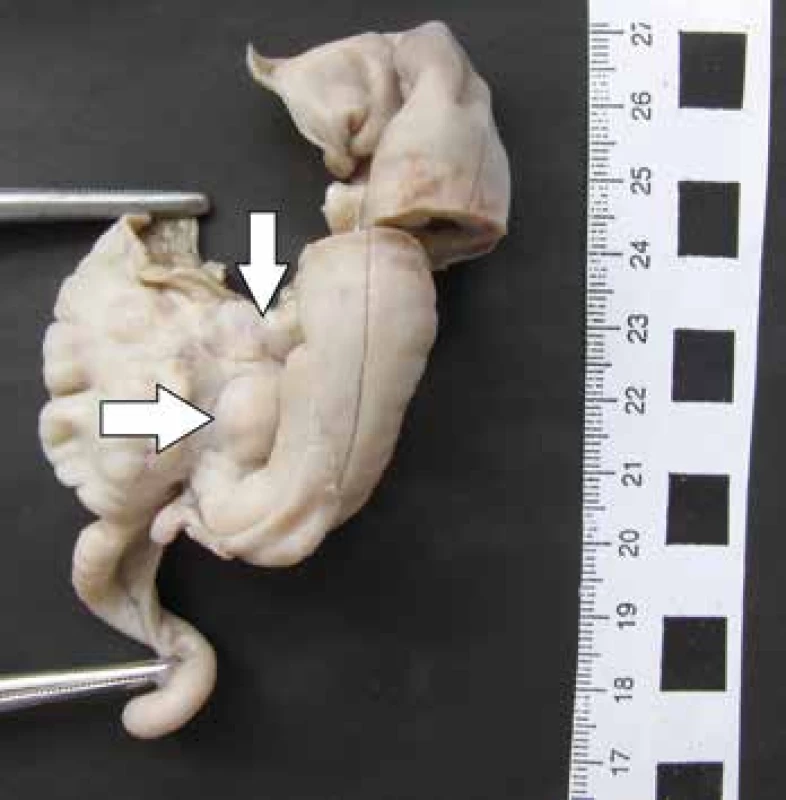
Image 2. Rezné plochy ileocekálnej oblasti so zhrubnutím terminálneho mezentéria (šípky). 
Image 3. Histotopogram fibrotického zhrubnutia terminálneho mezentéria s jeho pôvodnými štruktúrami (šípky). Farbenie hematoxylín-eozín. 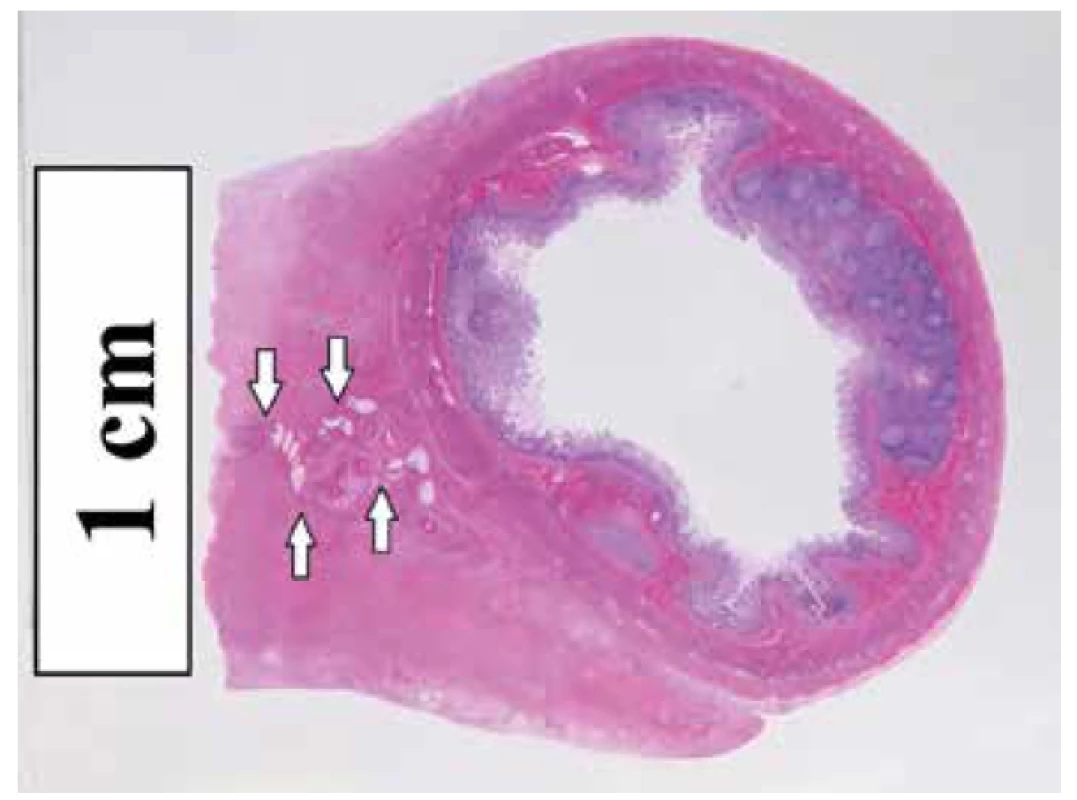
Image 4. Centrálna časť zhrubnutia s fibróznym tkanivom bohatým na kolagén. Farbenie van Gieson (zväčšenie 200x). 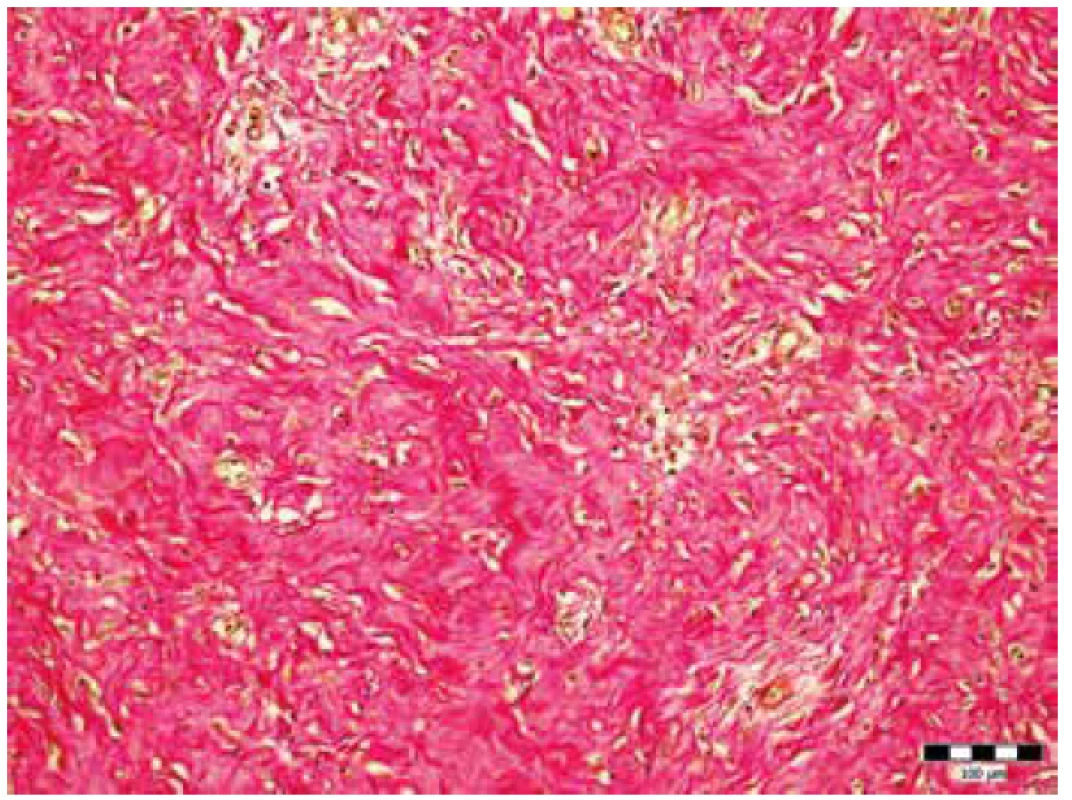
Image 5. Periférna časť zhrubnutia s fibróznym tkanivom bohatým na fibroblasty. Farbenie van Gieson (zväčšenie 200x). 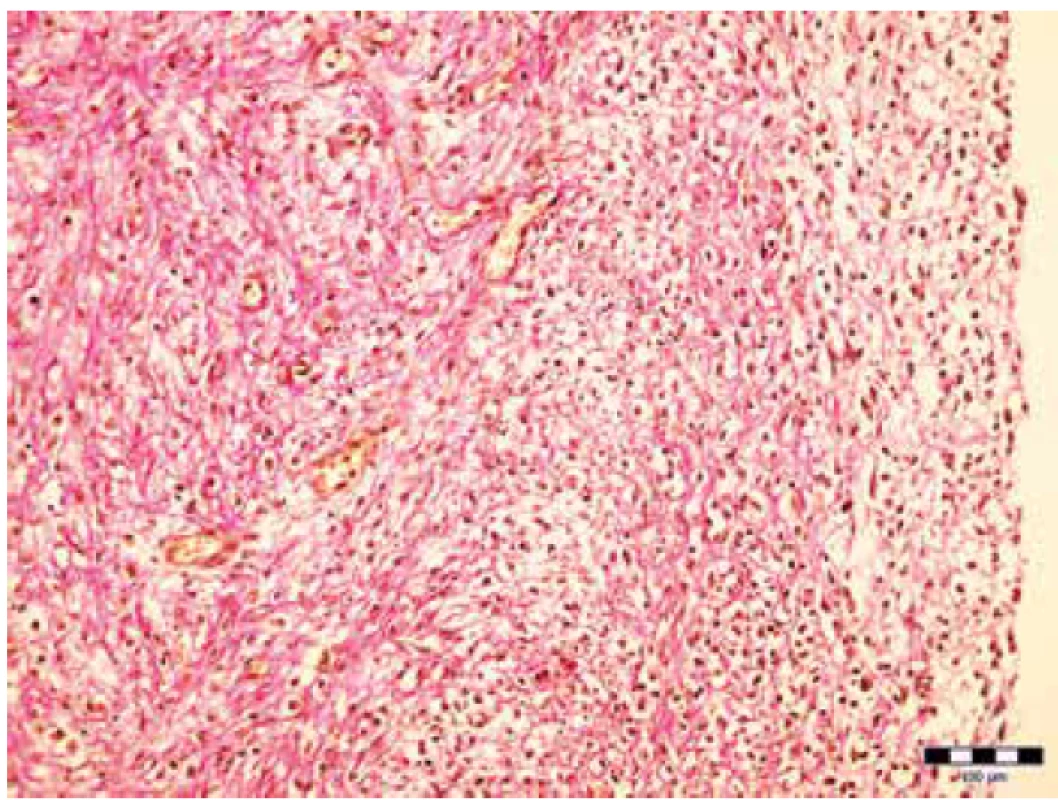
Image 6. Prítomnosť zvýšeného množstva plazmatických buniek v zhrubnutom mezentériu. Farbenie hematoxylín-eozín (zväčšenie 400x). 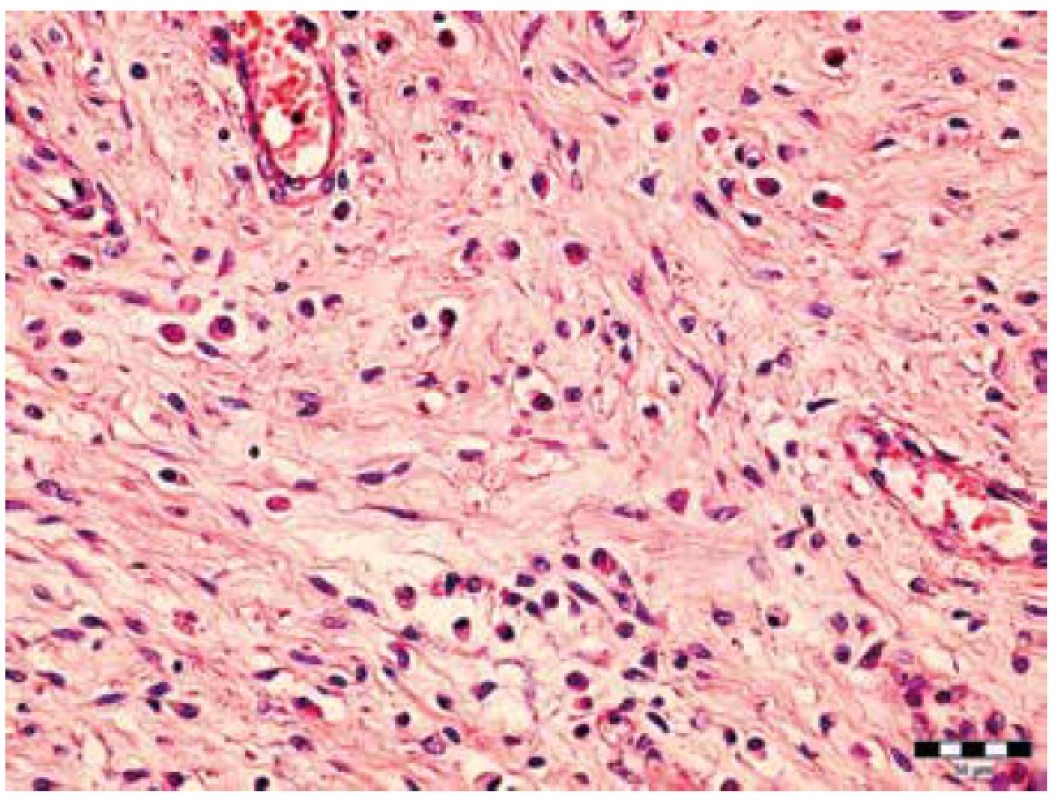
Image 7. Fibrinoidná nekróza stien ciev malého kalibru v mezentériu. Farbenie hematoxylín-eozín (zväčšenie 200x). Vložený obrázok imunohistochémia anti CD-34 (zväčšenie 200x). 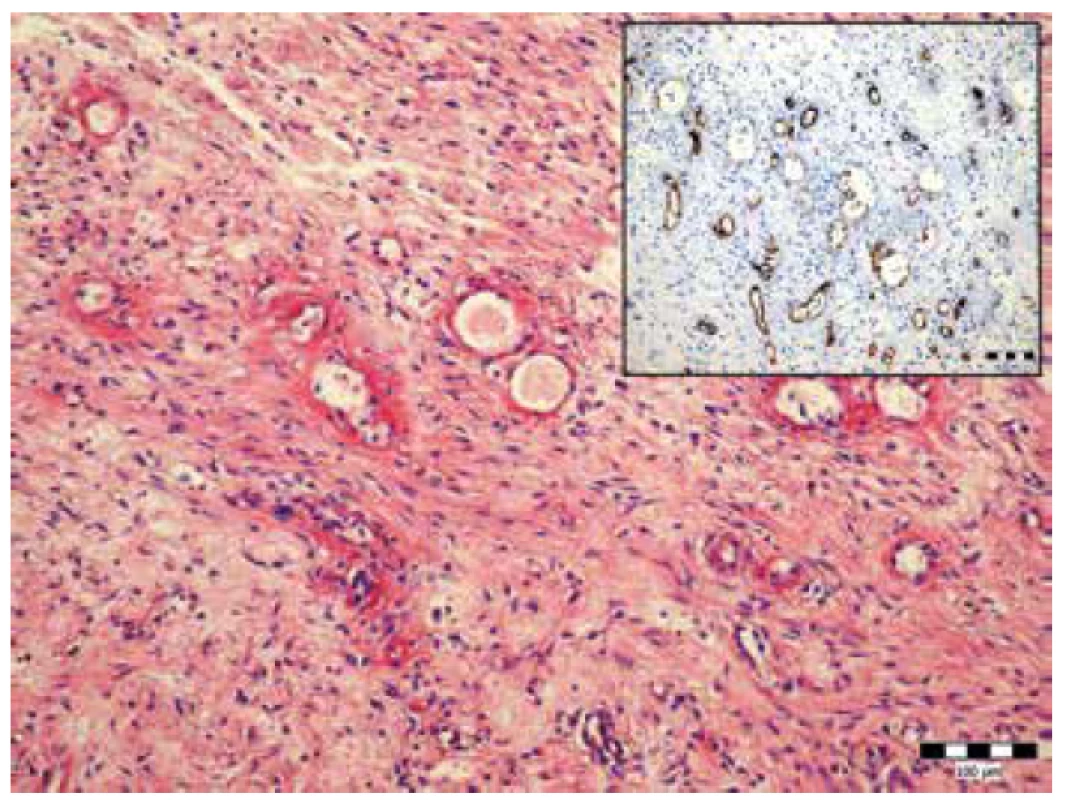
Image 8. Fibrinoidná nekróza stien ciev malého kalibru v mezentériu. Farbenie PAS (zväčšenie 400x). 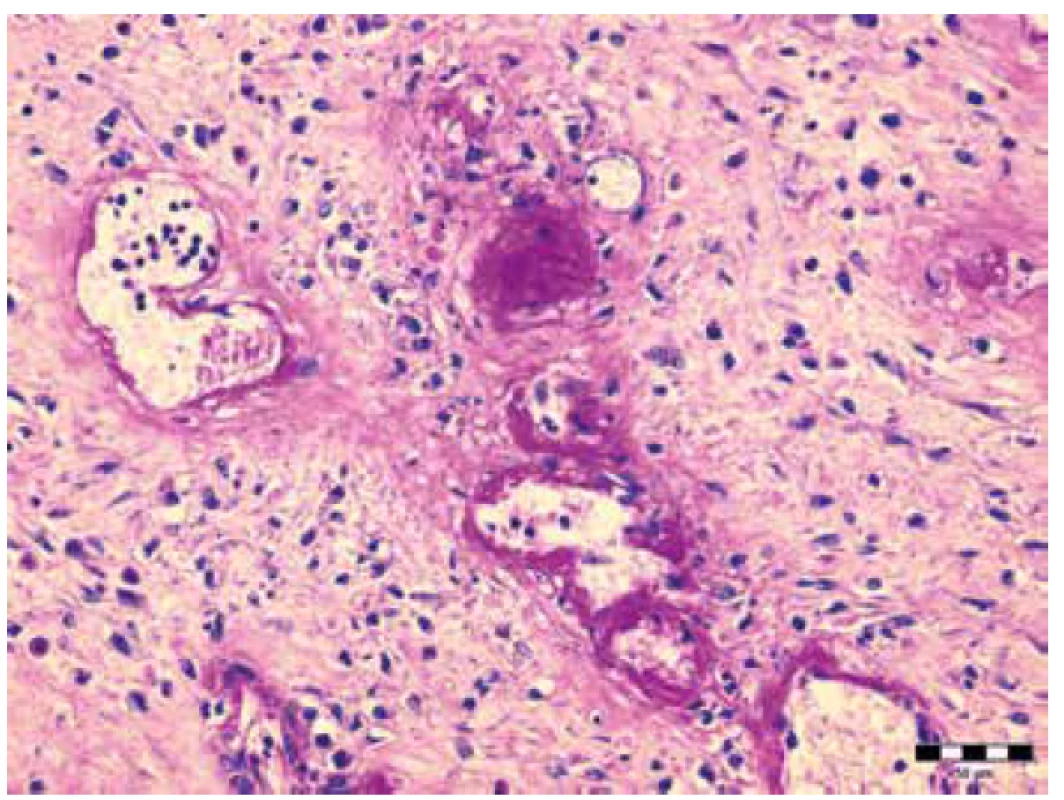
DISKUSIA
Sklerozujúca mezeneteritída (SM) je zriedkavé nenádorové ochorenie, ktoré postihuje mezentérium tenkého čreva s chronickým fibrotizujúcim zápalom (2). Popísaná bola pod mnohými názvami, ako napr. fibrozujúca, retraktilná, liposklerotická, xantogranulomatózna mezenteritída a systémová nodulárna panikulitída (3). Tieto názvy pravdepodobne odzrkadľovali obraz histologických variánt patologického poškodenia s lipodystrofickými zmenami mezentéria (predominantne degenerácia tukových buniek), mezenterická panikulitída (chronický zápal) a retraktilná mezenteritída (predominantná fibróza), pričom bolo akceptované, že tieto varianty predstavujú rôznorodé spektrum jedného chorobného procesu, ktorý by sa mohol nazývať idiopatická sklerozujúca mezenteritída (5). Dvakrát častejšie postihuje mužov (1,2,6,7), priemerný vek postihnutia je 55 – 65 rokov (1,2), ale popisovaná jednotka je spomenutá aj v prehľadovom článku (3) u 18-mesačného, ako aj v kazuistike 25-mesačného dieťaťa (8). V nami popisovanom prípade išlo, aspoň na základe dostupných literárnych údajov, o doteraz najmladšieho jedinca s diagnostikovaným ochorením. Histologicky sa SM vyznačuje variabilnou kombináciou fibrózy, chronického zápalu a nekrózy tukového tkaniva, pričom najčastejším nálezom je výrazná fibróza (2), tak ako to bolo aj v našom prípade. Zaujímavým nálezom bola aj prítomnosť fokálne fibrinoidnej nekrózy ciev mnalého kalibru, ktorá nepatrí do typického obrazu idiopatických fibrosklerozujúcich lézií. Mikroskopicky by diferenciálne diagnosticky do úvahy mohli spadať myofibroblastické ochorenia ako inflamatórny myofibroblastický tumor, dezmoidný typ fibromatózy, sklerozujúci variant dobre diferencovaného liposarkómu, retroperitoneálna fibróza (9), vaskulitídy a Crohnovej chorobe podobné ochorenia (10). Ochorenie môže prebiehať asymptomaticky. Klinické príznaky vyplývajú najčastejšie z priameho mechanického pôsobenia rastúcej hmoty na postihnuté tkanivo (črevo, cievy, lymfatické cievy) a okolité tkanivá (2). Ochorenie má zväčša pomalý priebeh (5,11), zriedkavo akútny (10). Medzi klinické symptómy patrí bolesť brucha, distenzia brucha, nauzea, zvracanie, hnačky, strata hmotnosti (2), anorexia, ascites, teploty (3). Okrem mezentéria môže byť postihnuté aj colon ascendens, transversum (3), flexura hepatica (10), sigmoideum (12,13). V popisovanom prípade boli anamnesticky zmienené opakované zvracanie a bolesti brucha. Patofyziológia SM zostáva neznáma, avšak jej vznik sa dáva do súvislosti s traumou (aj chirurgické zákroky ako napr. cholecystektómia a apendektómia) (2), hypoxickými, alergickými, infekčnými, autoimunitnými mechanizmami (12,14), nádormi (11) a zvýšenou hladinou sérového IgG4 (15). V nami opísanom prípade bolo možné vylúčiť traumu, chirurgický zákrok, nádor, neboli zistené prejavy sklerotického postihnutia iných orgánov, takže nebolo možné zistiť príčinu ochorenia a daný prípad predstavuje fokálnu idiopatickú sklerozujúcu mezenteritídu. V diagnostike lézie sa zo zobrazovacích metód najčastejšie využíva RTG, CT a USG vyšetrenie (1). Liečba ochorenia môže byť čisto medikamentózna (2,3), chirurgická alebo kombinovaná. V súčasnosti nie je jednoznačná zhoda v tom, ako dané ochorenie liečiť, avšak v niektorých prípadoch nebol vykonaný žiaden medicínsky zákrok (ani lieky) (13). Napriek tomu, že ide o relatívne benígne ochorenie, SM može mať až v 20 % prípadov vysilujúci priebeh končiaci sa smrťou, či už v dôsledku komplikácií SM, alebo jej liečby (2,4).
ZÁVER
V kazuistike sme prezentovali prípad 4-mesačného chlapca, ktorý náhle zomrel doma. Pitvou a ostatnými vyšetreniami nebola zistená bezprostredná príčina smrti, takže prípad bol uzavretý ako syndróm náhleho úmrtia dojčaťa. Ako zaujímavý vedľajší nález bolo zistené tumoriformné ložiskové zhrubnutie mesentéria v terminálnej časti ilea, ktoré bolo histologicky diagnostikované ako sklerozujúca mezeneteritída. Vzhľadom na tento nález predpokladáme, že počas života opakovaná výrazná citlivosť brucha sprevádzaná distenziou brušnej steny mohla byť podmienená touto chorobnou jednotkou. Prípad rozširuje spektrum najčastejších príčin brušných príhod o zriedkavú chorobnú jednotku nielen v detskom, ale aj v kojeneckom období.
PREHLÁSENIE
Autor práce prehlasuje, že v súvislosti s témou, vznikom a publikaciou tohto článku nie je v konflikte záujmov a vznik ani publikácia članku neboli podporené žiadnou farmaceutickou firmou. Toto prehlásenie sa týka všetkých spoluautorov.
MUDr. Daniel Farkaš, PhD.
Úrad pre dohľad nad zdravotnou starostlivosťou
SLaPA pracovisko Košice
Ipeľská 1, 043 74 Košice
tel.: +421552852660
fax: +421552852655
e-mail: farkas.dany@gmail.com
Sources
1. Sharma P, Yadav S, Needham CM, Feuerstadt P. Sclerosing mesenteritis: a systematic review of 192 cases. Clin J Gastroenterol 2017; 10(2): 103-111.
2. Akram S, Pardi DS, Schaffner JA, Smyrk TC. Sclerosing mesenteritis: clinical features, treatment, and outcome in ninety-two patients. Clin Gastroenterol Hepatol. 2007; 5(5): 589-596.
3. Viswanathan V, Murray KJ. Idiopathic sclerosing mesenteritis in paediatrics: Report of a successfully treated case and a review of literature. Pediatr Rheumatol Online J 2010; 8 : 5.
4. Kida T, Suzuki K, Matsuyama T, et al. Sclerosing mesenteritis presenting as protein-losing enteropathy: a fatal case. Intern Med 2011; 50(22): 2845-2849.
5. Emory TS, Monihan JM, Carr NJ. Sclerosing mesenteritis mesenteric panniculitis and mesenteric lipodystrophy: a single entity? Am J Surg Pathol 1997; 21 : 392–398.
6. Kipfer RE, Moertel CG, Dahlin DC. Mesenteric lipodystrophy. Ann Intern Med 1974; 80 : 582–588.
7. Durst AL, Freund H, Rosenmann E, Birnbaum D. Mesenteric panniculitis: review of the literature and presentation of cases. Surgery 1977; 81 : 203–211.
8. Parra-Buitrago A, Valencia-Zuluaga NA, Rivera-Echeverry JA, Contreras-Ramírez M, Vélez-Hoyos A. Idiopathic sclerosing mesenteritis in the pediatric patient: a case report. Rev Gastroenterol Mex 2013; 78(4): 255-257.
9. Kelly JK, Hwang WS. Idiopathic retractile (sclerosing) mesenteritis and its differential diagnosis Am J Surg Pathol 1989; 13(6): 513-521.
10. Ţarcă E, Trandafirescu MF, Cojocaru E, Mihăilă D, Savu B. Mesenteric panniculitis, rare cause of acute surgical abdomen in children. Case report and literature review. Rom J Morphol Embryol 2017; 58(4): 1597-1604.
11. Piessen G, Mariette C, Triboulet JP. Mesenteric panniculitis. Annal Chir. 2006; 131 : 85–90.
12. Parra-Davila E, McKenney MG, Sleeman D, et al. Mesenteric panniculitis: case report and literature review. Am Surg 1998; 64 : 768–771.
13. Seo M, Okada M, Okina S, Ohdera K, Nakashima R, Sakisaka S. Mesenteric panniculitis of the colon with obstruction of the inferior mesenteric vein: report of a case. Dis Colon Rectum 2001; 44(6): 885-889.
14. Schaffler A, Scholmerich J, Buchler C. Mechanisms of disease: adipocytokines and visceral adipose tissue–emerging role in intestinal and mesenteric diseases. Nat Clin Pract Gastroenterol Hepatol 2005; 2 : 103–111.
15. Vlachou PA, Khalili K, Jang HJ, Fischer S, Hirschfield GM, Kim TK. IgG4-related sclerosing disease: autoimmune pancreatitis and extrapancreatic manifestations. Radiographics 2011; 31(5): 1379-1402.
Labels
Anatomical pathology Forensic medical examiner Toxicology
Article was published inCzecho-Slovak Pathology

2019 Issue 4-
All articles in this issue
- Praktický přístup k pitvě srdce s vrozenou srdeční vadou
- Myokarditida a kardiomyopatie z pohledu kardiologa
- Histopatologická diagnostika myokarditid
- Nejnovější poznatky v mikroskopické diagnostice kardiomyopatií
- Lymfom z plášťové zóny diagnostikovaný z materiálu z radikální prostatektomie provedené pro adenokarcinom - kazuistika
- Incidentálna fokálna idiopatická sklerozujúca mezenteritída u 4-mesačného dieťaťa
- Inflamatorní myofibroblastický tumor dělohy – kazuistika
- Chondroidní melanom: kazuistika
- Novinky v kardiovaskulární patologii
- Nová učebnice PATOLOGIE je tady
- MONITOR, aneb nemělo by vám uniknout, že...
- MONITOR, aneb nemělo by vám uniknout, že...
- Spomienka na emeritného primára MUDr. Petra Kosseya, CSc.
- Dopis redakci
- Fumarát hydratáza deficientní karcinom z renálních buněk a jemu podobný karcinom z renálních buněk: Komparativní studie 23 geneticky testovaných případů
- Czecho-Slovak Pathology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Myokarditida a kardiomyopatie z pohledu kardiologa
- Fumarát hydratáza deficientní karcinom z renálních buněk a jemu podobný karcinom z renálních buněk: Komparativní studie 23 geneticky testovaných případů
- Inflamatorní myofibroblastický tumor dělohy – kazuistika
- Praktický přístup k pitvě srdce s vrozenou srdeční vadou
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

