-
Medical journals
- Career
VÝSKYT A ŘEŠENÍ UROLOGICKÝCH KOMPLIKACÍ PO TOTÁLNÍ PÁNEVNÍ EXENTERACI PROVEDENÉ PRO POKROČILÉ NÁDORY MALÉ PÁNVE
Authors: Jaroslav Jarabák 1; Roman Zachoval 1; Vladimír Visokai 2; Jaromír Šimša 2; Ludmila Lipská 2; Miroslav Levý 2
Authors‘ workplace: Urologické oddělení, Thomayerova nemocnice, Praha 1; Chirurgická klinika 1. lékařské fakulty Univerzity Karlovy a Thomayerovy nemocnice, Praha 2
Published in: Ces Urol 2016; 20(1): 39-47
Category: Original Articles
Overview
Hlavní stanovisko práce:
Totální pánevní exenterace je extenzivní výkon s vysokým výskytem urologických komplikací. Akutním řešením je derivace moči nefrostomií a poté u pacientů v remisi řešení stentem nebo reanastomózou.Cíl:
Vyhodnocení výskytu urologických komplikací u pacientů po totální pánevní exenteraci pro pokročilé nádory malé pánve.Materiál a metody:
Retrospektivně hodnocený soubor pacientů, kteří v letech 1999–2013 postoupili v naši nemocnici totální exenteraci pánve. Hodnoceny byly: onkologická charakteristika základního nádoru, předcházející operace, neoadjuvantní léčba, předcházející související urologické onemocnění a operace, délka operačního výkonu, krevní ztráty, druh a doba vzniku urologické komplikace a její řešení.Výsledky:
Soubor 42 pacientů, 28 mužů (67 %) a 14 žen (33 %), průměrného věku 58 let (rozmezí 43–71). Derivace moči byla u 41 pacientů provedena ureteroileostomií, v jednom případě pomocí kožní ureterostomie. Urologické komplikace jsme zaznamenali u dvanácti pacientů (29 %), časné u čtyř a pozdní u osmi pacientů. Časnou komplikaci představoval u tří pacientů urinózní leak z ureteroileální anastomózy, u jednoho pacienta septický stav na podkladě izolované infekce močových cest. Pozdní komplikace byly zjištěné v průměru 24 měsíců po operaci (rozmezí 4–60 měsíců). U sedmi pacientů se jednalo o strikturu močovodů v ureterointestinální anastomóze. U jednoho pacienta se vyskytla striktura kožní ureterostomie. Stadium nádorového onemocnění, předchozí chirurgické výkony a urologické onemocnění, délka operačního výkonu a velikost krevních ztrát výskyt komplikací neovlivňovaly. Všichni pacienti s výskytem urologických komplikací absolvovali neoadjuvantní léčbu.Závěr:
Urologické komplikace po totální pánevní exenteraci se vyskytují přibližně u třetiny pacientů. Bezpečným akutním řešením bylo provedení derivace moči pomocí punkční nefrostomie. U pacientů s pozdními komplikacemi ve druhé době výměna nefrostomie za transureterální stent. U pacientů v dlouhodobé remisi nádorového onemocnění následně otevřená revize s reanastomózou ureteroileálního spojení.KLÍČOVÁ SLOVA:
Nádory malé pánve, striktura močovodu, TPE – totální pánevní exenterace, ureteroileostomie, urinózní leak.ÚVOD
Pánevní exenterace je základem komplexní léčby pokročilých nádorů malé pánve, které nelze radikálně odstranit méně rozsáhlým, byť multiviscerálním resekčním výkonem. K pánevní exenteraci jsou indikováni nemocní s lokálně pokročilým, primárním nebo recidivujícím nádorem kolorektálního původu, dále pak nemocní s některými typy nádorů původu gynekologického a urologického. Jedná se zejména o nádory T4, které prorůstají do okolních struktur a orgánů v malé pánvi. Typy, rozsah a indikace pánevních exenterací jsou znázorněny v tabulce 1, kontraindikace v tabulce 2 a ilustrační fotografie na obrázku 1.
Table 1. Základní typy pánevní exenterace, její indikace a rozsah Tab. 1. Basic types of pelvic exenteration, its indications and scope 
Table 2. Kontraindikace pánevní exenterace Tab. 2. Contraindications of pelvic exenteration 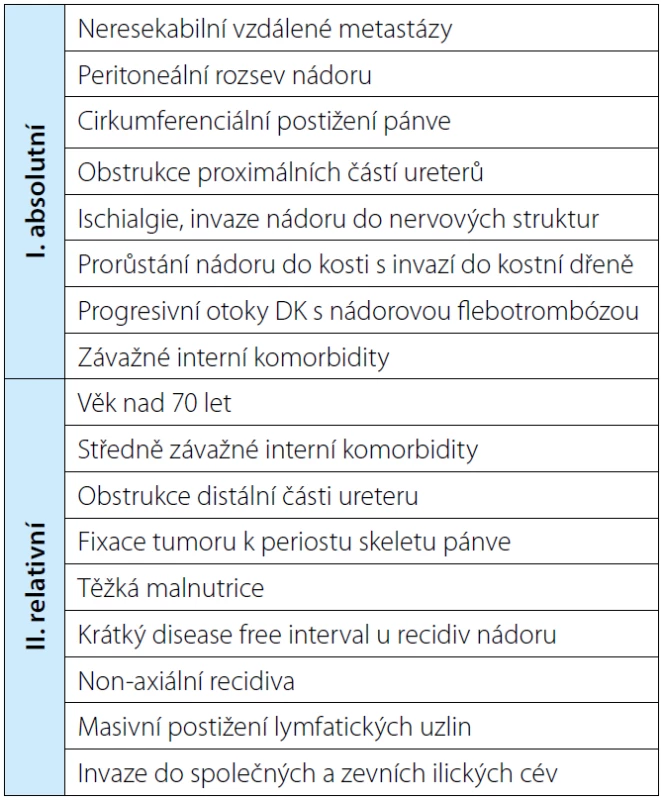
Image 1. Operační nález: úvodní fáze pelvické exenterace s paraaortální a perikavální lymfadenektomií; žluté závěsy jsou na ureterech, červený na arteria ilica communis sinistra Fig. 1. Operative findings: the initial phase of pelvic exenteration with para-aortic and percaval lymphadenectomy; yellow loops on the ureter, red on the artery iliaca communis sinistra 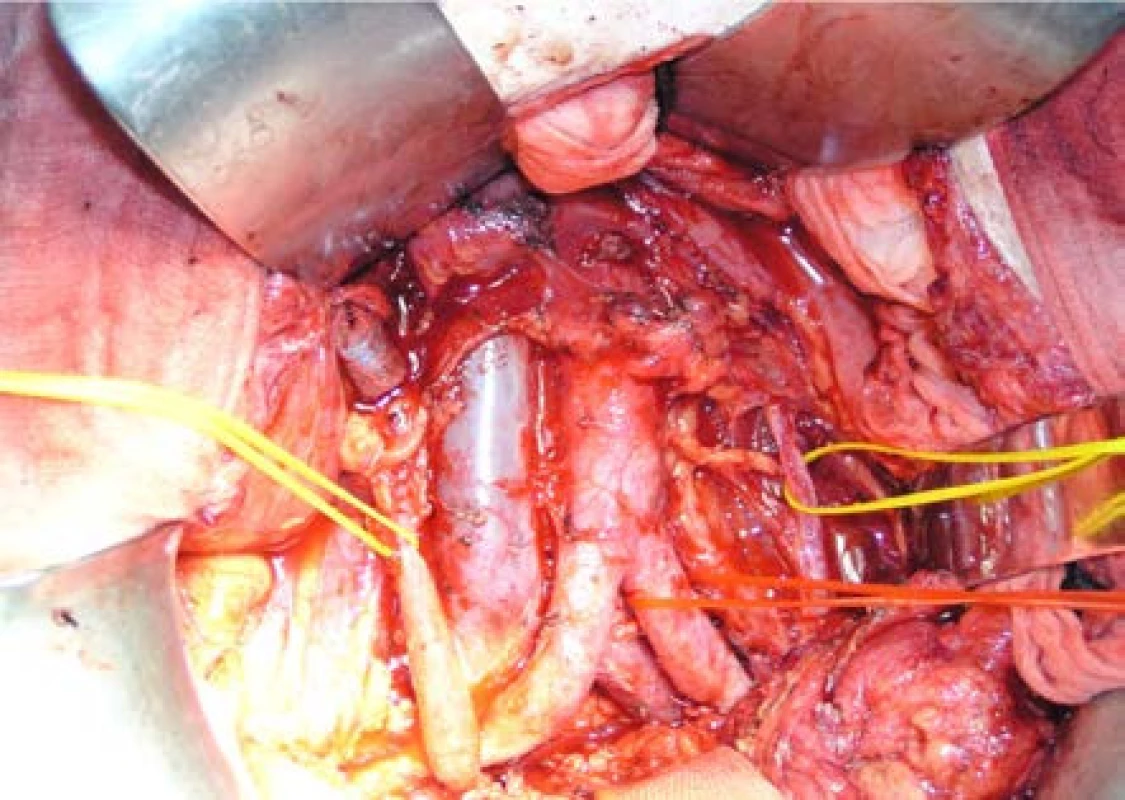
Exenterační výkony mají tři fáze: explorativní, ablativní a rekonstrukční. Rekonstrukční část výkonu zajištuje rekonstrukci pánevního dna a derivaci moči a stolice. Urolog je součástí operačního týmu a rozhoduje o typu močové derivace. Výběr vhodného typu derivace závisí na faktorech nemocného (věk, pohlaví, komorbidity) a jeho onemocnění. Při rozhodování o typu derivace je také nutné zohlednit přání pacienta s cílem dosažení co nejvyšší kvality života po operaci. Ve většině případů je vzhledem k nejisté onkologické prognóze pacienta volena derivace jednodušší, tj. pomocí ureteroileostomie nebo kožní ureterostomie. Operační tým musí byt schopen podle aktuálního nálezu vyhodnotit situaci a případně naplánovaný typ derivace změnit.
Cílem této práce je vyhodnocení výskytu urologických komplikací u pacientů po totální pánevní exenteraci pro pokročilé nádory malé pánve s nutností následné derivaci moči.
MATERIÁL A METODY
Do retrospektivní analýzy byli zařazeni všichni pacienti, kteří v letech 1999–2013 podstoupili totální pánevní exenteraci (TPE) v našem zdravotnickém zařízení.
Hodnoceny byly následující parametry:
- charakteristika základního nádorového onemocnění
- předcházející operační výkony
- neoadjuvantní léčba
- předcházející související urologické onemocnění, resp. operační výkony
- délka operačního výkonu
- krevní ztráty
- druh a doba vzniku časných (do tří měsíců od primárního operačního výkonu) a pozdních urologických komplikací a jejich řešení
VÝSLEDKY
Soubor tvoří 42 pacientů, z toho 28 mužů (67 %) a 14 žen (33 %), průměrného věku 58 let (rozmezí 43–71). Derivace moči byla u 41 pacientů provedena pomocí ureteroileostomie a v jednom případě kožní ureterostomií. U šesti pacientů (14 %) byla derivace moči z důvodů extrémní extenzitivity primárního operačního výkonu provedena až ve druhé době (2.–5. pooperační den). Nejčastějšími diagnózami, které vedly k indikaci TPE, byl zhoubný nádor konečníku u 23 pacientů (55 %) a rektosigmoideálního spojení u 13 pacientů (30 %). Tabulka 3 znázorňuje zastoupení jednotlivých typů nádoru v souboru, malignita prostaty nebyla indikací k TPE (jednalo se již o diagnostikovanou tumorovou duplicitu při recidivujícím nádoru konečníku). U 98 % operovaných pacientů bylo nádorové postižení ve stadiu cT3–4 dle TNM klasifikace. Čtyři pacienti absolvovaly TPE jako primární výkon, u zbylých pacientů byla TPE indikována po předcházejícím chirurgickém výkonu v dutině břišní. Nejčastěji se jednalo o paliativní založení střevní stomie u 23 pacientů. Spektrum předcházejících chirurgických výkonů zobrazuje graf 1.
Table 3. Zastoupení jednotlivých typů nádoru v souboru pacientů Tab. 3. Representation of each type of cancer in the group of patients 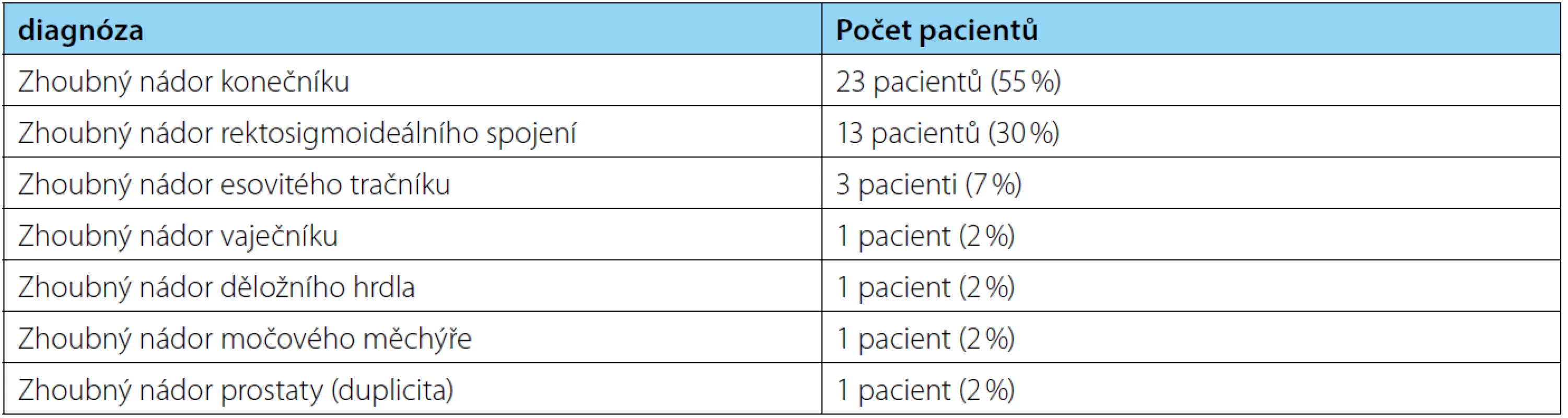
Graph 1. Chirurgické zákroky předcházející TPE Graph 1. Surgery preceeding total pervic exentereation 
Neoadjuvantní onkologickou léčbu absolvovalo 36 pacientů (86 %), z toho 18 pacientů v kombinaci chemoterapie a radioterapie. Průměrná délka TPE byla 10 : 30 hodiny (rozmezí 7 : 05–12 : 40), krevní ztráta 5 740 ml (rozmezí 750–13 000). U 13 pacientů (31 %) byl zjištěn předcházející urologický výkon v souvislosti se základním nádorovým onemocněním (osm pacientů s dilatací horních močových cest: 1x řešeno zavedením stentů a 7x punkční nefrostomií; pět pacientů absolvovalo transuretrální resekci pro nádorovou infiltraci močového měchýře tumorem střeva).
Výskyt urologických komplikací po TPE jsme zaznamenali u dvanácti pacientů (29 %), z toho časné u čtyř a pozdní u osmi pacientů. Časnou komplikaci představoval urinózní leak z ureteroileální anastomózy, u tří pacientů s derivací moči ureteroilestomií dle Brickera (obrázek 2), u jednoho pacienta septický stav na podkladě izolované infekce močových cest. Charakteristika a řešení časných komplikací viz tabulka 4.
Image 2. Urinózní leak v místě ureteroileální anastomózy (znázorněn šipkou) Fig. 2. Urinary leakage at the site of the ureteroileal anastomosis (indicated by arrow) 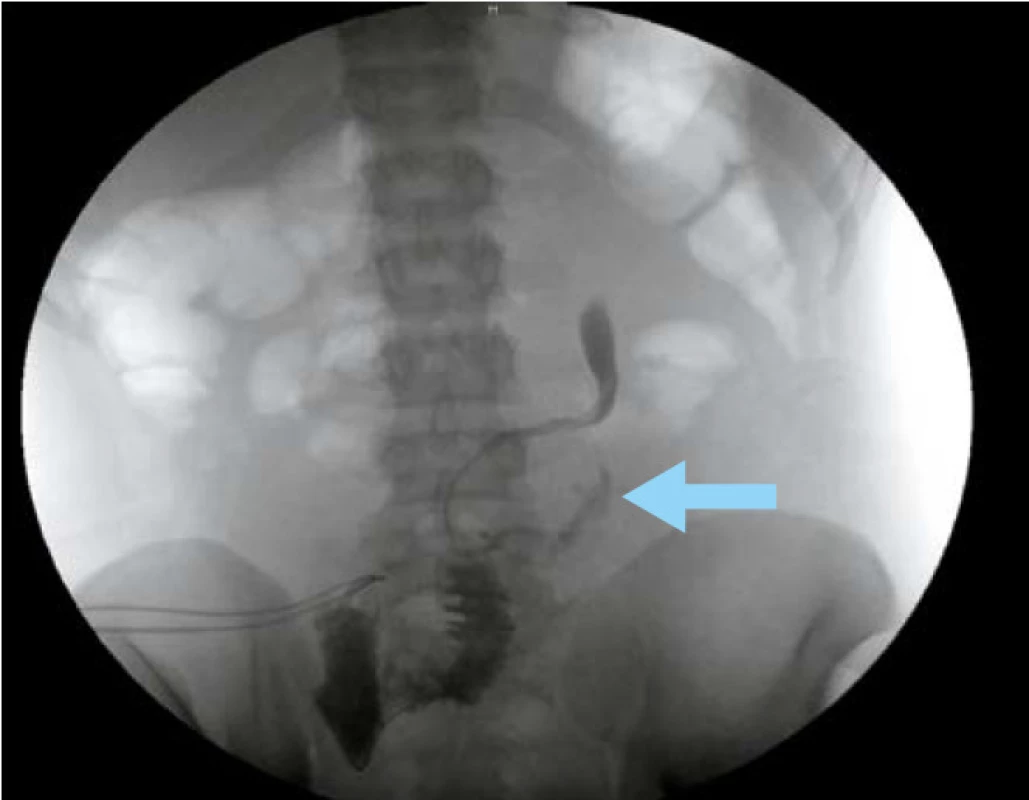
Table 4. Časné komplikace – počet pacientů, doba vzniku komplikace, řešení Tab. 4. Early complications – the number of patients, age of onset of complications, solutions 
Pozdní komplikace byly zjištěné v průměru 24 měsíců po TPE (4.–60. měsíc), jednalo se o striktury močovodů v ureterointestinální anastomóze se vznikem sekundární hydronefrózy u sedmi pacientů (derivace moči ureteroileostomií dle Brickera), z toho u tří pacientů oboustranné a u šesti pacientů symptomatické. U jednoho pacienta byla zjištěna striktura kožní ureterostomie (derivace moči kožní uretereostomií).
Ve skupině pacientů s výskytem urologických komplikací jsme nezaznamenali podstatný rozdíl v délce operačního výkonu ve srovnání se zbytkem souboru (průměrný čas 10 : 45 vs. 10 : 30 hod), totéž platí o krevních ztrátách (průměr 5 585 vs. 5 740 ml). Všichni pacienti s výskytem urologických komplikací byli ve stadiu cT3–4 nádorového onemocnění, dva z těchto pacientů absolvovali TPE jako primární výkon. Jeden pacient měl před TPE založenou pravostrannou punkční nefrotomii a jeden absolvoval transuretrální resekci močového měchýře. U dvou pacientů byla ureteroileoanastomóza realizována ve druhé době (2. resp. 5. den po TPE), u obou dvou těchto pacientů došlo ke vzniku časné urologické komplikace (urinózní leak). Všichni pacienti s výskytem urologických komplikací absolvovali neoadjuvantní onkologickou léčbu – kombinaci chemoterapie a radioterapie. U žádného pacienta s výskytem časné komplikace jsme nezaznamenali výskyt pozdní urologické komplikace.
ŘEŠENÍ POZDNÍCH KOMPLIKACÍ
Pacientka s asymptomatickou jednostrannou hydronefrózou, zjištěnou šest měsíců po TPE, je pouze pravidelně sledována (ultrasonografické kontroly, funkční vyšetření ledvin, monitorace renálních funkcí, iontogramu a zánětlivých parametrů). U šesti pacientů se symptomatickou hydronefrózou byl stav řešen dočasně založenou punkční nefrostomií na postižené straně, resp. stranách. U dvou pacientů v dlouhodobé remisi následovala operační revize s reanastomózou v místě ureteroileálního spojení (dva roky resp. pět let po TPE), u zbylých čtyř pacientů byl stav řešen antegrádním zavedením transuretrálních stentů přes stávající punkční nefrostomií pod skiaskopickou kontrolou, s plánem operační revize při dlouhodobější remisi základního onemocnění. Z těchto pacientů tři zemřeli v důsledku generalizace základního nádorového onemocnění, u čtvrtého pacienta jsou prováděny pravidelné výměny transuretrálních stentů trvalým řešením vzhledem k potvrzené generalizaci. U pacientů s kožní ureterostomií jsou pravidelně měněny ureterální stenty v důsledku striktury v místě jejího kožního vyústění.
DISKUZE
Totální pánevní exenterace představuje jeden z nejrozsáhlejších výkonů v abdominální onkochirurgii, s rizikem velkých perioperačních krevních ztrát, zatížený vysokou pooperační morbiditou (30−45 %) i mortalitou (5−10 %). Někteří autoři uvádějí ve svých souborech dokonce i hodnoty daleko vyšší, v případě morbidity 30−100 % a mortality 3−25 % (1).
Indikace k těmto extrémním a rizikovým výkonům musí být velmi precizní. Měla by vždy vycházet z rozhodnutí mezioborového indikačního týmu pracoviště, které má s uvedenou problematikou dostatečné zkušenosti a je schopné řešit často se vyskytující pooperační komplikace. Nejlepší výsledky jsou dnes dosahovány v centrech s úzce spolupracujícím týmem chirurgů, urologů, gynekologů, anesteziologů a onkologů (1).
Exenterace pánevních orgánů byla poprvé provedena v roce 1940 v Ellis Fishel State Cancer Center pod vedením Brunschwiga. Ten jako první v roce 1948 publikoval sestavu 22 nemocných po pánevní exenteraci. Výkony indikoval jako paliativní, močovody implantoval do tlustého střeva nad zhotovenou kolostomií (2). Velký vývoj následně zaznamenaly operace umožňující derivaci moči po cystektomii. Zlomovým bodem popsání techniky konduitu z pasáže exkludované kličky ilea s ureteroileoanastomózou, publikované Brickerem v roce 1950 (3).
Původně paliativní historický záměr exenterací jako záchranné „salvage“ operace u nemocných v beznadějném stavu se v posledních letech zásadně změnil. Zlepšující se výsledky a klesající morbidita tak vedly k situaci dnešní, kdy je naprostá většina nemocných indikována k pánevní exenteraci se záměrem kurativním. Podle různých autorů a povahy primárního nádoru lze po kompletním odstranění nádoru s dosažením resekce do negativní spodiny dosáhnout pětiletého přežití v rozmezí 30−60 % (1). V našem publikovaném soboru pacientů jsme výskyt urologických komplikací po TPE zaznamenali u 12 pacientů (29 %), časné u čtyř pacientů, pozdní u osmi pacientů. Srovnání výskytu urologických komplikací v jiných publikovaných souborech pacientů po TPE je uvedeno v tabulce 5.
Table 5. Výskyt urologických komplikací v souborech pacientů po TPE Tab. 5. The incidence of urological complications in patients’ files after TPE 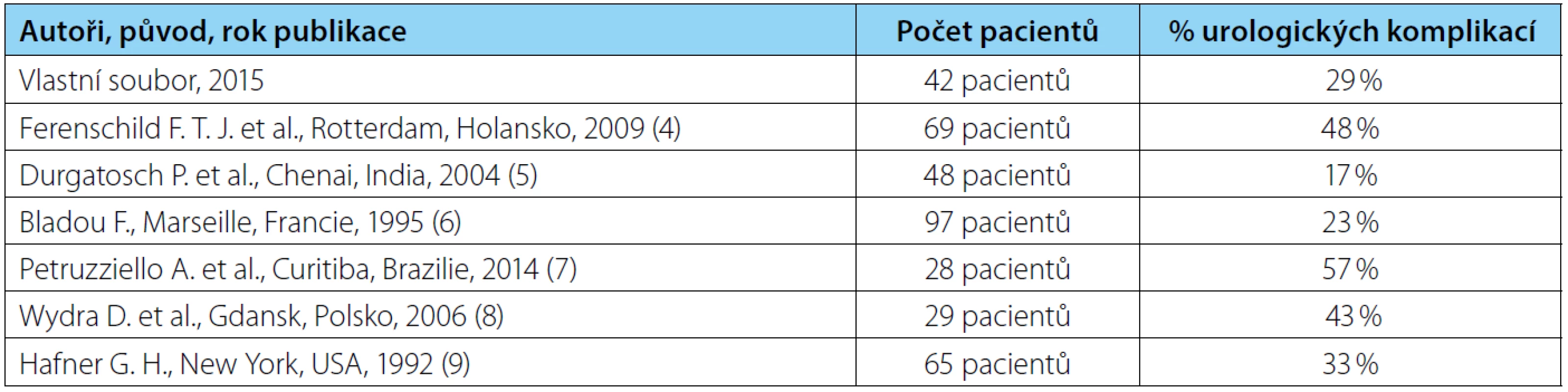
Výskyt urologických komplikací je různými autory uváděn v širokém rozmezí od 17–57 % (4 ,5, 6, 7, 8, 9). U 41 pacientů jsme použili derivaci moči ureteroileostomií, u jednoho pacienta kožní ureterostomií (močová derivace provedena ve druhé době a zvolená vzhledem k lokálnímu peroperčnímu nálezu jako paliativní forma derivace). U pacientů s ureteroileostomií se všechny vzniklé komplikace týkaly ureteroileální anastomózy. Komplikace v místě vyšití aborálního konce exkludované kličky ilea do kůže (stenózy, dehiscence, krvácení, ischemii resp. nekrózu) jsme nezaznamenali. Urinózní únik v místě ureterointestinálního spojení jako časná komplikace (tří pacienti) byl vyřešen u všech pacientů dočasným zavedením oboustranných punkčních nefrostomií, bez nutností operační revize. Pravidelně byla kontrolována dobrá funkčnost nefrostomických drénů a močová kultivace.
Nefrostomie byly odstraněny 12 týdnů po jejich založení po provedení kontrolního nefrostomogramu. U pacientů s výskytem časných komplikací jsme nezaznamenali výskyt pozdních urologických komplikací (striktury močovodů, urinózní fistuly).
Pozdní komplikaci tvořily striktury – u sedmi pacientů s ureteroileostomií se jednalo o zúženiny močovodů v místě ureterointestinálního spojení, u jednoho pacienta s kožní ureterostomií o strikturu kožní stomie. U symtomatických pacientů (bolesti, teploty, progrese renálního selhání s oligurií až anurií) jsme stav řešili akutním založením punkční nefrostomie. Po stabilizaci stavu pacienta a reparaci renálních funkcí následovalo onkologické vyšetření (restaging základního nádorového onemocnění – CT, PET/CT, MR). U dvou pacientů v dlouhodobé remisi na základě multidisciplinárního konzilia (chirurg, urolog, onkolog) byla provedena úspěšná operační revize s reanastomózou ureteroileálního spojení. Stadium nádorového onemocnění, předchozí chirurgické výkony a výskyt urologických onemocnění v předchorobí výskyt urologických komplikací neovlivňovaly. Všichni pacienti s výskytem urologických komplikací absolvovali neoadjuvantní léčbu. Délka operačního výkonu a velikost krevních ztrát vznik urologických komplikací neovlivňovaly.
Na vznik močových komplikací u pacientů po TPE má vliv více faktorů (věk, komorbidity a celkový stav pacienta, předcházející chirurgické zákroky, neoadjuvantní onkologická léčba, zvolený typ močové derivace aj.). Řada autorů za hlavní příčinu vzniku močových komplikací považuje předcházející radioterapii, event. v kombinaci s chemoterapií (6, 7, 8, 10). Ozáření malé pánve je rizikovým faktorem chronické alterace cév tenkého střeva a močovodů, způsobující zejména fibrózu a sklerózu drobných cév (11). Dalším rizikovým faktorem poškozující vaskularizaci tkání v průběhu TPE je velmi extenzivní preparace struktur v malé pánvi, včetně močovodů, s nebezpečím jejich ischemizace a denervace. Poškozená vaskularizace tkáně představuje u každého typu derivace rizikový faktor vzniku komplikací.
Typ močové derivace také signifikantně souvisí s rozvojem komplikací (8). Za nejčastěji používanou derivaci moči po TPE je v literatuře uváděna Brickerova urostomie (4). Jako alternativy této derivace se můžou použít techniky využívající jiný, radioterapií nepoškozený segment střeva např. jejunum nebo tlusté střev o, mají však také své nevýhody. Použití jejuna může vést k závažným metabolickým komplikacím (tzv. syndrom jejunálního konduitu – hyponatremie, hyperchloremie, těžká acidóza), v současné době v praxi se tato derivace téměř nepoužívá (12, 13). Užití rezervoáru z tlustého střeva (používá se exkludovaná klička transverza nebo sigmatu) limitují jeho předcházející resekce v minulosti. Použití kontinentních derivací je také možné (10). Ve srovnání s kutánní ureterostomií nebo Brickerovou derivací může dobrá funkce kontinentní derivace zlepšit kvalitu života, Karsenty et al. (14) ale uvádějí až 46% výskyt komplikací po jejich použití ve svém souboru pacientů, Chang et al. (15) uvádějí zejména zvýšený výskyt časných komplikací v ráně. Kožní ureterostomie je poměrně jednoduchá metoda, bez nutnosti manipulace se střevem. Vzhledem k vysoké frekvenci pozdních komplikací (vznik striktur v oblasti stomie, uroinfekce a tvorba litiázy) je používána u pacientů po TPE výjimečně, nejčastěji jako forma paliativní derivace. Alternativou dvou vývodů po TPE (močového a střevního) je vyšití pouze jedné stomie – tzv. dvouhlavňové vlhké kolostomie. Tento operační výkon je technicky odlišný od nedoporučované, tradiční vlhké kolostomie. Golda et al. ve své publikaci uvádějí srovnatelné a uspokojivé výsledky s výskytem urologických komplikací po použití této formy derivace ve srovnání s použitím dvou oddělených stomií (16).
ZÁVĚR
Výskyt urologických komplikací po TPE je vysoký, vyskytuje se přibližně u třetiny pacientů. Jejich vznik a výskyt souvisí s absolvováním neoadjuvantní léčby.
Bezpečným akutním řešením urologických komplikací v našem souboru bylo provedení derivace moči pomocí punkční nefrostomie. U pacientů s pozdními komplikacemi ve druhé době je možná výměna nefrostomie za transureterální stent a u pacientů s dobrou prognózou, v dlouhodobé remisi základního nádorového onemocnění, následně provedení otevřené revize s reanastomózou ureteroileálního spojení.
Pečlivé zhodnocení celkového stavu nemocného i rozsahu a lokální pokročilosti nádoru je vždy zásadní. Stanovení optimálního léčebného postupu by dnes mělo vždy vycházet z rozhodnutí mezioborového indikačního týmu.
Došlo: 5. 11. 2015
Přijato: 7. 1. 2016
Střet zájmů: žádný
Prohlášení o podpoře: Jedná se o nezávislý článek – zpracování tohoto článku nebylo podpořeno žádnou společností.
Kontaktní adresa:
MUDr. Jaroslav Jarabák
Urologické oddělení, Thomayerova nemocnice
Vídeňská 800, 140 59 Praha 4 – Krč
e-mail: jaroslav.jarabak@ftn.cz
Sources
1. Šimša J, Visokai V, Lipská L, Levý M. Pánevní exenterace v léčbě pokročilých nádorů malé pánve. Rohl. Chir 2014; 93(1): 34–37.
2. Brunschwig A. Complete excision of pelvic viscera for advanced carcinoma. A one-stage abdominoperineal operation with end colostomy and bilateral ureteral implantation into the colon above the colostomy. Cancer 1948; 1 : 177−183.
3. Bricker EM. Bladder substitution after pelvic evisceration. Surg Clin North Am 1950; 30 : 1511−1521.
4. Ferenschild FTJ, Vermaas M, Verhoef C, et al. Total pelvic exenteration for primary and recurrent malignancies. Word J Surg 2009; 33 : 1502–1508.
5. Durgatosh P, Shuaib Z, Vikas M, Ravi K. Pelvix exenteration: a perspective from a regional cancer center in India. Indian J Cancer 2004; 41(3): 109–114.
6. Bladou F, Houvenaeghel G, Delpero JR, Guerinel G. Incidence and management of major urinary complications after pelvic exenteration for gynecological malignancies. J Surg Oncol 1995; 58(2): 91–96.
7. Petruzziello A, Kondo W, Hatschback SN, et al. Surgical results of pelvic exenteration in treatment of gynecological cancer. W Jour Surg Oncol 2014; 12 : 279–284.
8. Wydra D, Emerich J, Sawicki S, Ciach K, Marciniak A. Major complications following exenteration in cases of pelvic malignancy: a 10-year experience. World J Gastroenterol 2006; 12(7): 1115–1119.
9. Hafner GH, Herrera L, Petrelli NJ. Morbidity and mortality after pelvic exenteration for colorectal adenocarcinoma. Ann Surg 1992; 215(1): 63–67.
10. Pawlik TM, Skibber JM, Rodrigues-Bigas MA. Pelvic exenteration for advanced pelvic malignancies. Ann Surg Oncol 2006; 13(5): 612–623.
11. Jadon R, Pembroke CA, Hanna CL, et al. A systematic review of organ motion ang image-guided strategies in external beam radioterapy for cervical cancer. Cin Oncol 2014; 26 : 185–196.
12. Seifert L. Die darm-siphonbalse. Arch Klin Chir 1935; 183 : 569–574.
13. Mansson W, Lindstedt E. Elektrolyte disturbances after jejunal condiut urinary diversion. Scan J Urol Nephrol 1978; 12 : 17−21.
14. Karsenty G, Moutardier V, Lelong B, et al. Long-term follow-up of continent urinary diversion after pelvic exenteration for gynecological malignancies. Gynecol Oncol 2005; 97 : 524–528.
15. Chang HK, Lo KY, Chiang AS. Complications of urinary diversion after pelvic exenteration for gynecologycal malignancy. Int Urogynecol J pelvic Floor Dysfunct 2000; 11 : 358–360.
16. Golda T, Biondo S, Kresisler E, et al. Follow-up of double-barreled wet colostomy after pelvic exenteration at a single institution. Dis Colon Rectum 2010; 53 : 822–829.
Labels
Paediatric urologist Nephrology Urology
Article was published inCzech Urology
2016 Issue 1-
All articles in this issue
- 31ST ANNUAL CONFERENCE EAUIN MUNICH
- SOUTĚŽ ČUS O NEJLEPŠÍ VĚDECKOU PUBLIKACI ZA ROK 2015
- DOCENT MUDR. RADIM KOČVARA, CSC. OSLAVIL 65. NAROZENINY
- JEDNOPORTOVÁ LAPAROSKOPICKÁ (LESS) ADRENALEKTOMIE
- ROBOTICKY ASISTOVANÁ RESEKCE LEDVINY PRO TUMOR
- VYUŽITÍ RÁZOVÉ VLNY PŘI LÉČBĚ PORUCH EREKCE
- NEUROSTIMULACE A NEUROMODULACE V DĚTSKÉM VĚKU
- JAK PŘIPRAVIT ABSTRAKT NA VÝROČNÍ KONFERENCI ČUS
- VÝSKYT A ŘEŠENÍ UROLOGICKÝCH KOMPLIKACÍ PO TOTÁLNÍ PÁNEVNÍ EXENTERACI PROVEDENÉ PRO POKROČILÉ NÁDORY MALÉ PÁNVE
- 18-F CHOLIN PET CT V PRIMODIAGNOSTICE KARCINOMU PROSTATY
- KARCINOSARKOM MOČOVÉHO MĚCHÝŘE
- TRAUMA PODKOVOVITÉ LEDVINY
- 61. PRACOVNÍ KONFERENCE ČUS V OLOMOUCI 2015
- DESET LET ROBOTICKÉ CHIRURGIE V ČESKÉ REPUBLICE
- KOREKCIA BIPLANÁRNYCH ZAKRIVENÍ PENISU U PACIENTOV S PEYRONEHO CHOROBOU. POPIS MODIFIKÁCIE EGYDIOVEJ TECHNIKY S NALOŽENÍM SUTÚRY PRIAMO NA MATERIÁL BOVÍNNEHO PERIKARDU
- Czech Urology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- VYUŽITÍ RÁZOVÉ VLNY PŘI LÉČBĚ PORUCH EREKCE
- TRAUMA PODKOVOVITÉ LEDVINY
- 18-F CHOLIN PET CT V PRIMODIAGNOSTICE KARCINOMU PROSTATY
- NEUROSTIMULACE A NEUROMODULACE V DĚTSKÉM VĚKU
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

