-
Medical journals
- Career
Pacient s Williamsovým–Beurenovým syndromem v ordinaci dětského lékaře
Authors: Urbanová Wanda 1,2; Kubíková Hana 1; Dubovská Ivana 1,3; Chramosta Petr 1,4,5; Pelánová Jana 1,6,7
Authors‘ workplace: Spolek pro Williamsův syndrom, z. s. – Willík 1; Oddělení ortodoncie a rozštěpových vad, Stomatologická klinika, 3. lékařská fakulta Univerzity Karlovy a FN Královské Vinohrady, Praha 3 Ortodontické oddělení, Klinika zubního lékařství, Univerzita Palackého a FN Olomouc 2; Stomatologická klinika, Lékařská fakulta Univerzity Karlovy v Plzni a FN Plzeň 4; Oddělení ústní, čelistní a obličejové chirurgie, Masarykova nemocnice, Ústí nad Labem 5; Ordinace PLDD – MUDr. Jana Pelánová 6; Oddělení neurofyziologie sluchu, Ústav experimentální medicíny, Akademie věd ČR 7
Published in: Čes-slov Pediat 2022; 77 (4): 232-235.
Category:
doi: https://doi.org/10.55095/CSPediatrie2022/038Overview
Williamsův–Beurenův syndrom je multisystémové postižení způsobené mikrodelecí v místě dlouhého raménka chromozomu 7. Mezi příznaky tohoto syndromu patří charakteristická dysmorfie obličeje, postižení kardiovaskulárního systému, menší vzrůst, opožděný psychomotorický vývoj a lehká až střední mentální retardace. Časná diagnostika tohoto onemocnění je zásadní pro cílenou dispenzarizaci. Péče o pacienta s Williamsovým–Beurenovým syndromem vyžaduje interdisciplinární přístup týmu lékařů specialistů v čele s praktickým lékařem pro děti a dorost.
Klíčová slova:
Williamsův–Beurenův syndrom – mikrodelece – chromozom 7 – elfí obličej – supravalvulární stenóza aorty
Úvod
Williamsův–Beurenův syndrom (také známý jako Williamsův syndrom, dále jen WBS, OMIM 194050) je multisystémové postižení patřící mezi mikrodeleční syndromy. Je způsoben delecí 1,5–1,8 milionu párů bází obsahujících 26–28 genů dlouhého raménka chromozomu 7 (oblast 7q11.23).(1) Mezi chybějící geny v postižené oblasti patří především gen pro syntézu elastinu. Příznaky syndromu zahrnují typický vzhled obličeje, vrozené vady kardiovaskulárního systému, opoždění psychomotorického vývoje a lehký až střední stupeň mentální retardace. U některých pacientů způsobuje v raném dětství obtíže vysoká hladina kalcia. Lidé s WBS mají charakteristické zvláštnosti chování: společenskou osobnost, verbalismus, stereotypní, obsesivní až úzkostné chování.(1) Časná diagnóza je důležitá pro cílenou dispenzarizaci pacienta, jelikož některé zdravotní problémy mohou progredovat či se objevit až během růstu dítěte.
Prevalence
Williamsův–Beurenův syndrom patří mezi vzácná onemocnění, jehož výskyt je u europoidní rasy mezi 1 : 7500 a 1 : 20 000 živě narozených dětí. Vyskytuje se stejně u chlapců i dívek.(1,2) Prakticky ve všech případech se jedná o nově vzniklou mutaci, familiární výskyt je ojedinělý. Výskyt v ČR je obtížné stanovit – česká pacientská organizace Willík, spolek pro Williamsův syndrom, z. s., v současné době spolupracuje s cca 85 osobami s WBS různého věku (0,5–48 let) a jejich rodinami.(3)
Klinické projevy
V projevech WBS existují mezi jednotlivými pacienty značné rozdíly. U konkrétního dítěte se zpravidla nemanifestuje celé spektrum potíží. Ačkoli různé zdravotní komplikace nemusí dosahovat vysokého stupně závažnosti, systémový charakter postižení způsobuje, že některé děti vyžadují opakované hospitalizace a časté ambulantní kontroly u různých odborníků.
Pacienti s WBS jsou dobře identifikovatelní díky charakteristickému vzhledu obličeje (100 %) – široké čelo; nos se sedlovitým kořenem a kulatou špičkou; boubelaté tváře; jakoby opuchlá oční víčka; velká ústa s plnými rty, drobnými zuby a prodlouženým filtrem (často též nazýván „elfí obličej“) (obr. 1).(1) Na duhovkách většiny z nich nalézáme charakteristický hvězdicovitý vzor – iris stellatae (obr. 2).
Image 1. Fotografie jedinců s WBS ve věku: A – 1,5 roku; B – 4 roky; C – 5 let; D – 8 let; E – 10 let; F – 12 let; G – 13 let; H – 13,5 roku; CH – 23 let; I – 32 let. Typické rysy „elfího“ obličeje zahrnují široké čelo, nos se sedlovitým kořenem a kulatou špičkou, boubelaté tváře, jakoby opuchlá oční víčka, velká ústa s plnými rty, drobnými zuby a prodlouženým filtrem. 
Publikováno s písemným souhlasem zákonných zástupců. Image 2. Hvězdicovitý vzor na duhovkách u dvouletého chlapce s diagnostikovaným WBS – iris stellatae 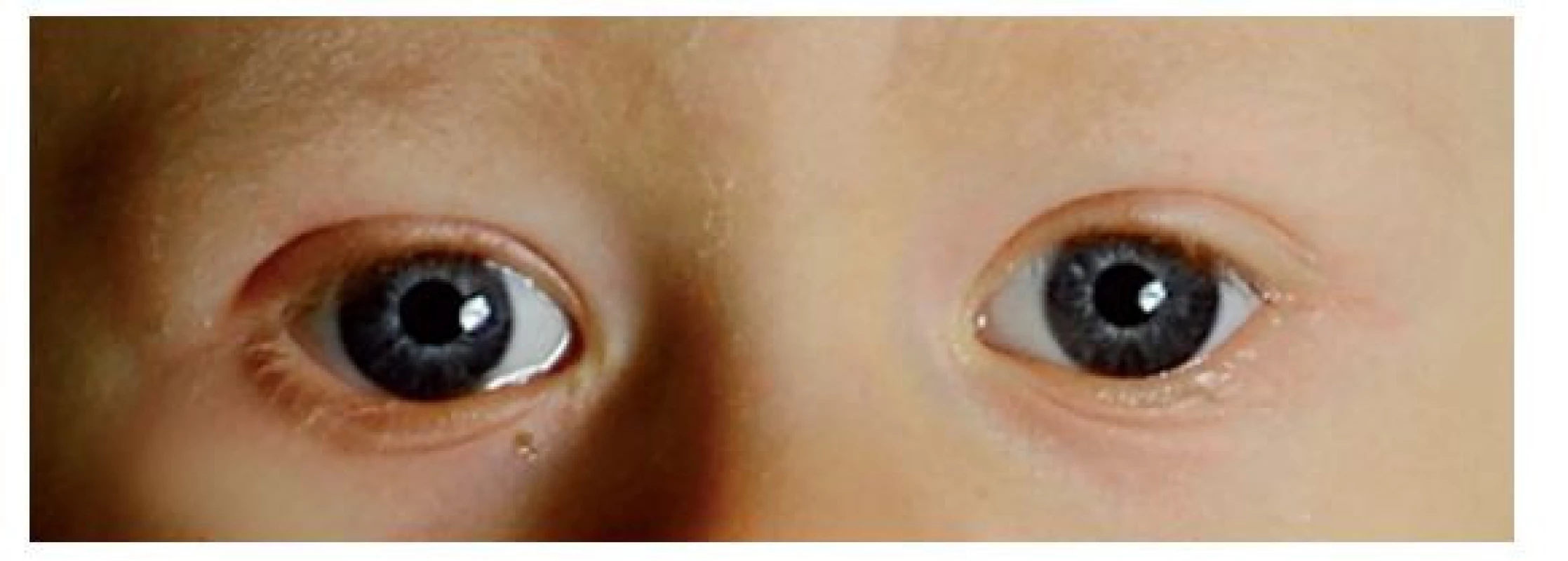
Až 80 % pacientů s WBS má postižení kardiovaskulárního systému (KVS) – vrozené vady velkých cév a srdce spolu s elastinovou arteriopatií. Nejčastěji nalézáme supravalvulární stenózu aorty, stenózu plicnice a/nebo renálních tepen a mitrální regurgitaci. Symptomatická stenóza či obstrukce se však může vyvinout na jakékoliv arterii a rizikem je její postupné zhoršování, proto je nutné celoživotní sledování na kardiologii.(4) WBS může být spojen i s jinými vadami velkých cév a srdce – například Fallotovou tetralogií či koarktací aorty.(5) Zvláštní pozornost u pacientů s WBS je třeba věnovat výkonům v celkové anestezii, protože vlivem postižení kardiovaskulárního systému jsou více rizikové.(6) Byly popsány i případy náhlého úmrtí během celkové anestezie a jako možná příčina se uvádějí abnormity v repolarizaci srdce (prodloužení QT intervalu na EKG).(7) Zvýšený krevní tlak se vyskytuje přibližně u 50 % pacientů, často je diagnostikován již v předškolním věku a vyžaduje medikaci.(1)
U pacientů s WBS lze již od narození pozorovat poruchu růstu – většina dětí se rodí s nízkou porodní hmotností a v raném věku neprospívá, i v dospělosti bývají menšího vzrůstu. V porovnání se zdravou populací zůstávají tyto děti při vyznačení výsledků vážení a měření do růstového grafu pod 10. percentilem, proto pro ně byly stanoveny specifické růstové grafy.(8) Mikrocefalii nalézáme až u třetiny postižených jedinců.(9)
V literatuře často uváděná rekurentní infantilní hyperkalcemie se vyskytuje přibližně u čtvrtiny kojenců s WBS.(10) Projevuje se zvýšením hladiny vápníku v krvi spolu s dehydratací, zvýšenou dráždivostí a nechutenstvím. Během prvních roků života se všem dětem s WBS doporučuje nepodávat preparáty obsahující vitamin D (např. Vigantol).(1) Během puberty a v dospělosti se hyperkalcemie vyskytuje spíše jako sekundární nález daný například hyperparatyreózou, avšak ve všech věkových skupinách pacientů s WBS byly prokázány zvýšené hladiny kalcia oproti zdravým vrstevníkům.(10) V dospělosti se pak u poloviny z nich setkáváme s osteopenií či osteoporózou. Příčina těchto abnormalit v metabolismu kalcia zůstává neobjasněna. Mezi další endokrinní odchylky patří u WBS častý výskyt diabetes mellitus již v pubertálním věku, hypotyreóza, předčasná puberta a předčasné stárnutí.(11)
Psychomotorický vývoj je opožděn – dětem s WBS trvá déle, než se naučí lézt, stát, chodit i mluvit. V pozdějším věku se projeví různý stupeň mentálního postižení (95 %), nejčastěji v rozmezí lehké až středně těžké mentální retardace, ovšem s velmi nevyrovnanými výkony v různých složkách a s velkými interindividuálními rozdíly.(1) Verbální schopnosti jedinců s WBS jsou většinou velmi dobré, ale mívají obtíže se zpracováním zrakově-prostorových informací a s orientací, což jim způsobuje problémy v běžném životě – chybný odhad vzdálenosti, potíže s chůzí na nerovném terénu či po schodech, strach z výšek a problémy s koordinací jemné i hrubé motoriky. Často mají poruchy pozornosti s hyperaktivitou typu ADHD (v 65 %).(12) Děti i dospělí s WBS mají excesivně sociální povahu – postrádají sociální zábrany a jsou velmi důvěřiví a přátelští vůči cizím lidem. Během dospívání a v dospělosti však mohou trpět úzkostmi, depresemi, fobiemi, případně obsedantně-kompulzivní poruchou.(13) Tyto obtíže jsou často dávány do souvislosti i s hyperakuzí – zvýšenou citlivostí na hluk a určité zvuky.(14) Děti si již od časného dětství často zakrývají uši, některé z nich musí dlouhodobě používat sluchátka s rušivým efektem, tzv. hluchátka. Většina jedinců s WBS má nezvykle vyvinutou muzikalitu a pozitivně reagují na melodické zvuky.
Neurologické obtíže zahrnují centrální hypotonii, hyperreflexii a cerebelární dysfunkci (ataxii a tremor).(15) Vyšetření magnetickou rezonancí prokázala celkově menší velikost mozku (bílé i šedé hmoty) a jeho strukturální abnormality – například redukovanou hloubku intraparietální rýhy či Chiariho malformaci I. stupně. V mozkové tkáni byly nalezeny abnormality integrity axonů a tenčí myelinové pochvy.
Velmi časté u WBS jsou ortodontické anomálie – odchylky ve velikosti a počtu zubů, vady skusu a anomálie ve velikosti čelistí (u 94 %). Častěji se vyskytuje zubní kaz a onemocnění parodontu, především z důvodu nedostatečné dentální hygieny.(16)
Postižení zraku zahrnuje strabismus (v polovině případů), typický hvězdicovitý vzor na duhovce nalézáme u 74 % pacientů s WBS.(17) Nefrologické nálezy (u 18 %) se pohybují od málo významných (divertikly močového měchýře) až po aplazii, hypoplazii či duplikaci ledviny.(18) U pacientů s výskytem hyperkalcemie v dětství je možné diagnostikovat nefrokalcinózu. Mezi další zdravotní komplikace mohou patřit poruchy příjmu potravy, trávicí potíže (v raném věku reflux, koliky, tolerance jen kašovité stravy a pouze určitých chutí, zácpa, divertikulóza střev, prolaps konečníku),(19) vícečetné kýly (umbilikální, inguinální a další), opakované nebo chronické záněty středního ucha, skolióza (ve 34 %) a hypermobilita či progredující ztuhlost kloubů.(20) Většina odborných pramenů udává i zvýšený výskyt celiakie.(21)
Genetický profil
Podezření na diagnózu WBS většinou vychází z typického vzhledu pacienta v kombinaci s postižením kardiovaskulárního systému, celkovým neprospíváním a psychomotorickou retardací. Diagnózu potvrdí genetik vyšetřením krevního vzorku metodou FISH (fluorescent in situ hybridization). Novější diagnostickou metodou je array CGH (comparative genomic hybridization), díky které je možné přesně určit úsek delece a chybějící geny.
Mikrodelece obecně vznikají v důsledku nerovnoměrného crossing-over mezi homologními chromozomy nebo nerovnoměrnou výměnou mezi sesterskými chromatidami při profázi během prvního meiotického dělení. V současné době jsou v kritickém regionu 7q11.23, jehož delece vede k WBS, považovány za důležité především geny ELN, STX1A, LIMK1, RFC2, NCF1, FKBP6, CYLN2, TBL2 a genová rodina GTF.(22) Elastinový gen (ELN) reguluje syntézu elastinu – proteinu důležitého pro správnou funkci kontraktilních tkání. Projevy jeho nedostatku jsou především kardiovaskulární poruchy a anomálie pojivových tkání (kýly, divertikly močového měchýře/střev, jemná pokožka atd.). Syntaxin 1A (STX1A) je hojně exprimovaný v neuronech. Také LIM kináza 1 (LIMK1) je důležitá pro vývoj centrálního nervového systému a maturaci nervových synapsí. RFC2 je podjednotkou replikačního faktoru C a jeho nepřítomnost způsobí nedostatek faktoru zodpovědného za replikaci a reparaci DNA, což následně vede k růstové retardaci a poruchám vývoje. Neutrofilní cytosolický faktor 1 (NCF1) se podílí na reakci oxidačního stresu v buňkách. Podle posledních výzkumů jeho přítomnost přispívá ke vzniku hypertenze – paradoxně chybění tohoto genu působí protektivně proti vzniku vysokého krevního tlaku.(23) Genová rodina všeobecných transkripčních faktorů GTF (GTF2I, GTF2IRD1 a GTF2IRD2) se ponejvíce exprimuje v mozku. GTF2I spolu s GTF2IRD1 jsou zapojeny do patogeneze kognitivních a behaviorálních fenotypů spojených s WBS(24) a GTF2I může narušovat funkci oligodendrocytů.(25) Této genové rodině se přisuzuje i zodpovědnost za dysmorfii obličeje a za zubní i čelistní anomálie. Chybění dalších genů v místě delece je zřejmě zodpovědné za ostatní klinické projevy WBS.
Dispenzarizace pacienta
WBS je multisystémová porucha, proto je třeba u těchto pacientů provádět pravidelný screening. Základem péče jsou pravidelné návštěvy u praktického lékaře pro děti a dorost (PLDD) s důrazem na kontroly výšky, váhy a obvodu hlavy, měření krevního tlaku na všech čtyřech končetinách, funkce ledvin, včasný záchyt skoliózy, kloubních obtíží a v neposlední řadě i krevní testy s monitorováním hladiny Ca, TSH a glykemie.(8) U dětí se srdečními anomáliemi a rizikem infekční endokarditidy je nutné, aby PLDD zajištoval antibiotickou profylaxi při chirurgických a stomatochirurgických ošetřeních.
Mezi další specialisty, kteří pravidelně monitorují pacienty s WBS, patří kardiolog, neurolog, rehabilitační lékař, endokrinolog, zubní lékař spolu s ortodontistou a dentální hygienistkou. Dále podle individuálních obtíží konkrétního pacienta mohou být součástí multidisciplinárního týmu i gastroenterolog a nutriční specialista, ortoped, oční lékař, nefrolog, foniatr, dětský psycholog, při výrazných poruchách chování i psychiatr. Většina pacientů s WBS navštěvuje od útlého dětství fyzioterapeuta, v indikovaných případech mohou být přínosné pobyty v lázních. Při potížích s příjmem tuhé stravy a s nácvikem mluvy pomůže klinický logoped – vhodné jsou různé formy orofaciální stimulace.
V rámci podpůrné péče o rodiny s dítětem s WBS se v prvních letech života uplatňuje terénní sociální služba rané péče. Děti s WBS patří mezi žáky se speciálními vzdělávacími potřebami, vhodnou podporu pro jejich vzdělávání stanovuje školské poradenské zařízení (speciálně pedagogické centrum). Zařazení dětí do běžných školek a škol s asistentem závisí na míře zdravotních obtíží dítěte a jeho sociálních dovednostech. Kontakt se zdravými vrstevníky je každopádně velmi žádoucí a motivační, ať už v rámci širší rodiny, ve škole, či během volnočasových aktivit.
Závěr
Péče o pacienta s Williamsovým–Beurenovým syndromem z pohledu praktického lékaře pro děti a dorost je náročnější a obsáhlejší než u zdravých vrstevníků. Vyžaduje pravidelné kontroly a posouzení plánu návštěv u dalších odborníků. Problematika WBS je přehledně zpracována v brožuře „Klinický management Williamsova syndromu“, dostupné na webových stránkách spolku Willík.(8)
Korespondenční adresa:
MUDr. Wanda Urbanová, Ph.D.
Oddělení ortodoncie a rozštěpových vad
Stomatologická klinika 3. LF UK a FNKV Praha
Sources
1. Morris CA, Braddock SR; Council On Genetics Health Care. Supervision for Children with Williams Syndrome. Pediatrics 2020; 145(2): e20193761.
2. Strømme P, Bjørnstad PG, Ramstad K. Prevalence estimation of Williams syndrome. J Child Neurol 2002; 17(4): 269–71.
3. Neuschlová N, Kubíková H. Willík – spolek pro Williamsův syndrom. https:// www.spolek-willik.cz
4. Wessel A, Pankau R, Kececioglu D, et al. Three decades of follow-up of aortic and pulmonary vascular lesions in the Williams-Beuren syndrome. Am J Med Genet 1994; 52(3): 297–301.
5. Huarte NM, García-Guereta L, Lapunzina P. Williams-Beuren syndrome: Usual face, unusual heart. Open J of Genet 2013; 3(1): 79–81.
6. Nosková P. Anesteziologická problematika u dětí s Williamsovým syndromem. Anest Intenziv Med 2018; 29(3): 148–150.
7. Collins RT 2nd, Aziz PF, Gleason MM, et al. Abnormalities of cardiac repolarization in Williams syndrome. Am J Cardiol 2010; 106(7): 1029–33.
8. Williams syndrome foundation. Klinický management Williamsova syndromu – doporučené postupy. Praha: Spolek Willík 2017. Dostupné na: https:// www.spolek-willik.cz/prakticke-informace/informace-pro-lekare/
9. Pankau R, Partsch CJ, Neblung A, et al. Head circumference of children with Williams-Beuren syndrome. Am J Med Genet 1994; 52(3): 285–290.
10. Sindhar S, Lugo M, Levin MD, et al. Hypercalcemia in patients with Williams - Beuren syndrome. J Pediatr 2016; 178 : 254–260.e4.
11. Levy-Shraga Y, Gothelf D, Pinchevski-Kadir S, et al. Endocrine manifestations in children with Williams-Beuren syndrome. Acta Paediatr 2018; 107(4): 678–684.
12. Leyfer OT, Woodruff-Borden J, Klein-Tasman BP, et al. Prevalence of psychiatric disorders in 4 to 16-year-olds with Williams syndrome. Am J Med Genet B Neuropsychiatr Genet 2006; 141B(6): 615–22.
13. Riby D, Hanley M, Rodgers J. Úzkost u Williamsova syndromu: Příručka pro podporu dospělých s Williamsovým syndromem. Český překlad. Paha: Spolek Willík 2020.
14. Johnson LB, Comeau M, Clarke KD. Hyperacusis in Williams syndrome. J Otolaryngol 2001; 30(2): 9092.
15. Chapman CA, du Plessis A, Pober BR. Neurologic findings in children and adults with Williams syndrome. J Child Neurol 1996; 11(1): 63–65.
16. Patil PM, Patil SP. Williams-Beuren syndrome: a complete guide for oral healthcare. J Oral Med Oral Surg 2021, 27 : 21.
17. Winter M, Pankau R, Amm M, et al. The spectrum of ocular features in the Williams-Beuren syndrome. Clin Genet 1996; 49(1): 28–31.
18. Pankau R, Partsch CJ, Winter M, et al. Incidence and spectrum of renal abnormalities in Williams-Beuren syndrome. Am J Med Genet 1996; 63(1): 301–304.
19. O ‘Reilly MF, Lancioni GE. Treating food refusal in a child with Williams syndrome using the parent as therapist in the home setting. J Intellect Disabil Res 2001; 45(Pt 1): 41–46.
20. Damasceno ML, Cristante AF, Marcon RM, Barros Filho TE. Prevalence of scoliosis in Williams-Beuren syndrome patients treated at a regional reference center. Clinics (Sao Paulo) 2014; 69(7): 452–456.
21. Simşek-Kiper PO, Sahin Y, Arslan U, et al. Celiac disease in Williams-Beuren syndrome. Turk J Pediatr 2014; 56(2): 154–9.
22. Merla G, Brunetti-Pierri N, Micale L, Fusco C. Copy number variants at Williams - Beuren syndrome 7q11.23 region. Hum Genet 2010; 128(1): 3–26.
23. Del Campo M, Antonell A, Magano LF, et al. Hemizygosity at the NCF1 gene in patients with Williams-Beuren syndrome decreases their risk of hypertension. Am J Hum Genet 2006; 78(4): 533–542.
24. Porter MA, Dobson-Stone C, Kwok JB, et al. A role for transcription factor GTF2IRD2 in executive function in Williams-Beuren syndrome. PLoS One 2012; 7(10): e47457.
25. Barak B, Zhang Z, Liu Y, et al. Neuronal deletion of Gtf2i, associated with Williams syndrome, causes behavioral and myelin alterations rescuable by a remyelinating drug [published correction appears in Nat Neurosci 2019; 22(7): 1197]. Nat Neurosci 2019; 22(5): 700–708.
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2022 Issue 4-
All articles in this issue
- Co jsme psali
- Purkyňova cena za rok 2022 byla udělena prof. MUDr. Otto Hrodkovi, DrSc.
- Editorial
- Gregor Mendel slaví 200 let: ze zahrad augustiniánského kláštera v Brně až ke kauzální léčbě monogenně podmíněných chorob
- Dystrofinopatie
- Gregor Mendel a řízení růstu dítěte: geny, molekuly a pediatrická klinická praxe
- Syndrom intelektuálního postižení související s DYRK1A
- Fabryho choroba v dětském věku – přehled a kazuistika
- Klinický fenotyp a genetická diagnostika raritného syndrómu cutis laxa u polystigmatizovaného novorodenca
- Pacient s Williamsovým–Beurenovým syndromem v ordinaci dětského lékaře
- Diferenciální diagnostika mikroskopické hematurie
- Hypertermie, její příčiny a rizika z pohledu patofyziologa
- Sepse u dětí
- Za MUDr. Janem Škovránkem, CSc.
- Pediatrická poezie
- Ze sbírky moderního českého a slovenského umění
- Genetická různorodost monogenního diabetu na Ukrajině
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Sepse u dětí
- Diferenciální diagnostika mikroskopické hematurie
- Hypertermie, její příčiny a rizika z pohledu patofyziologa
- Dystrofinopatie
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

