-
Medical journals
- Career
Diferenciální diagnostika mikroskopické hematurie
Authors: Konopásek Patrik; Krejčová Vlasta; Zieg Jakub
Authors‘ workplace: Pediatrická klinika 2. LF UK a FN v Motole, Praha
Published in: Čes-slov Pediat 2022; 77 (4): 236-240.
Category: Pediatric Protocols in Praxis
doi: https://doi.org/10.55095/CSPediatrie2022/039Overview
Mikroskopická hematurie je poměrně častá diagnóza v ambulanci dětského nefrologa a zpravidla bývá prvně diagnostikována praktickým dětským lékařem. Příčinou jsou většinou benigní diagnózy, v rámci diagnostického postupu je ale třeba vyloučit závažnější stavy, jako jsou glomerulonefritidy či systémová onemocnění, pro které bývá charakteristická přítomnost proteinurie, hypertenze nebo zhoršená funkce ledvin. Obsahem našeho sdělení je základní diferenciální diagnostika mikroskopické hematurie spolu se stručným popisem jednotlivých diagnóz a návrhem jednotlivých vyšetření jako návod pro praktické lékaře pro děti a dorost a ambulantní specialisty.
Klíčová slova:
diferenciální diagnostika – mikroskopická hematurie – vyšetření moči
Úvod
Mikroskopická hematurie je definovaná jako přítomnost zvýšeného množství erytrocytů v moči, které však nevede k viditelné změně jejího zabarvení (na rozdíl od makroskopické hematurie). Jedná se o poměrně běžnou diagnózu v ambulanci pediatra či dětského nefrologa. Prevalence nálezu hematurie v 1 vzorku moči je 3–4 %, perzistující hematurii, definovanou jako přetrvávající pozitivní nález v moči po dobu 6 měsíců, nacházíme ale vzácněji. Současná přítomnost hematurie a proteinurie s prevalencí pod 0,7 % je většinou spojená se závažnější diagnózou.(1–4)
Stanovení diagnózy
Mikroskopická hematurie bývá často prvně diagnostikována náhodně pomocí testačního proužku při běžné preventivní prohlídce či při cíleném vyšetření moči u febrilních stavů v ambulanci dětského lékaře. Pozitivní reakce testačního proužku (pseudoperoxidázová reakce) odráží přítomnost hemoglobinu, který se vyskytuje i v moči pacientů s hemoglobinurií doprovázející rabdomyolýzu či hemolytickou anemii. Proto je diagnózu hematurie nutno následně potvrdit vyšetřením močového sedimentu stanovením počtu erytrocytů. Ten se dnes již většinou provádí v laboratořích pomocí automatických analyzátorů, kde považujeme za patologické hodnoty více než 10 erytrocytů v 1 μl necentrifugované moči (ev. více než 5 erytrocytů v zorném poli z centrifugované moči).(5,6)
V tomto článku stručně shrnujeme základní diferenciální diagnostiku mikroskopické hematurie včetně souhrnu jednotlivých vyšetření, která standardně provádíme při pátrání po diagnóze. Kompletní výčet etiologie s dělením na prerenální (zdroj hematurie je mimo urotrakt), renální a postrenální (zdroj je ve vývodných cestách močových) shrnuje tabulka 1.
Table 1. Dělení příčin hematurie dle zdroje erytrocytů 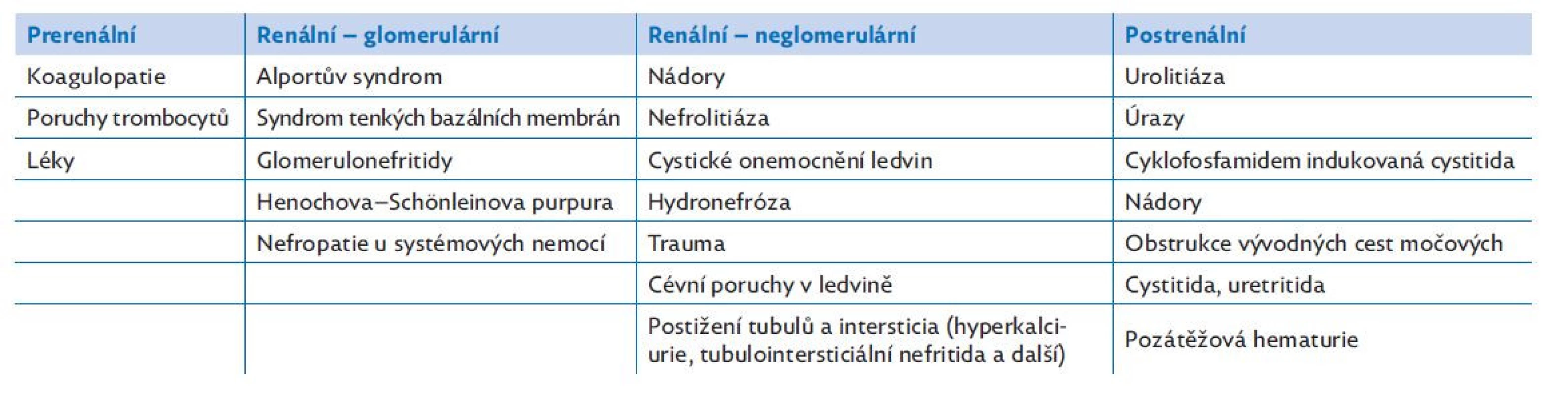
(zdroj: Dětská nefrologie, Seeman et al. 2021) Diferenciální diagnostika
Při nálezu mikroskopické hematurie je nutné odebrat podrobnou osobní a rodinnou anamnézu. V rámci diferenciální diagnostiky je důležité zjistit, zda pacient neměl v nedávné době úraz břicha nebo zad. Dále se dotazujeme na příznaky doprovázející infekci močových cest (dysurie, urgence, lumbalgie), obstrukci výhodných cest močových (kolikovitá bolest v bedrech iradikující do třísel). Virová respirační nebo gastrointestinální infekce či bakteriální tonzilitida v předchorobí jsou dalším důležitým anamnestickým údajem. Stejně tak nás zajímá medikace užívaná v předchorobí, jelikož řada léků je spojena se vznikem tubulointersticiální nefritidy. Pozitivní rodinná anamnéza na přítomnost hematurie, nefrolitiázy, percepční poruchy sluchu, závažné koagulační poruchy, chronického renálního onemocnění či nejasného selhání ledvin nám může významně pomoci v diferenciálně diagnostické rozvaze.
Při provádění fyzikálního vyšetření se soustřeďujeme na známky poruchy vodní rovnováhy (otoky) a hodnocení vitálních funkcí, kde speciální pozornost věnujeme správnému změření krevního tlaku. Některá onemocnění postihující ledviny mají i charakteristické extrarenální projevy – kožní eflorescence, kloubní změny a další. Jednotlivá komplementární vyšetření shrnuje tabulka 2, stručnou diferenciální diagnostiku dle anamnézy a klinického nálezu shrnuje tabulka 3.
Table 2. Seznam vhodných vyšetření u pacientů s mikroskopickou hematurií 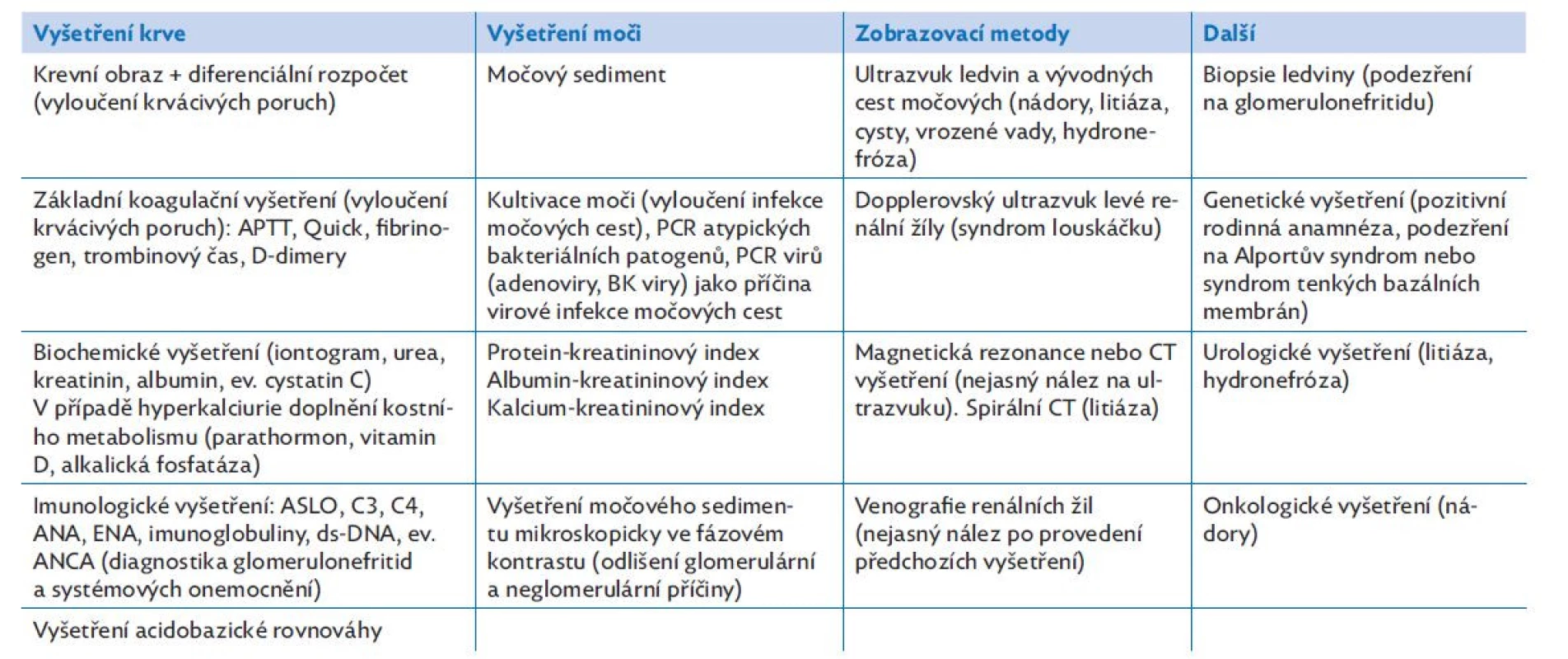
Table 3. Stručná diferenciální diagnostika dle anamnézy a fyzikálního vyšetření 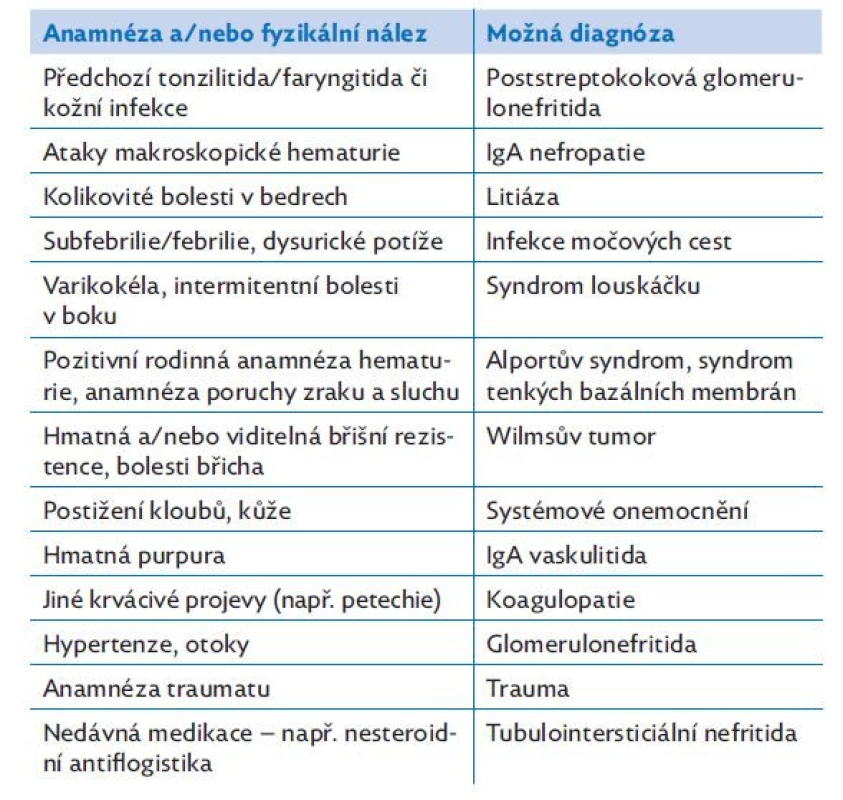
Dalším krokem v rámci diagnostické rozvahy je zhodnocení, zda se jedná o jednorázový nález hematurie (tranzientní hematurie), nebo zda je hematurie diagnostikovaná opakovaným vyšetřením moči (perzistující hematurie).
Tranzientní hematurie se běžně vyskytuje u infekcí močových cest a traumat urogenitálního traktu. Může se však objevit i v souvislosti s nadměrnou fyzickou zátěží a horečkou. Tyto nálezy nemají klinický význam, mohou však vést k diagnostickým rozpakům.
Perzistující mikroskopická hematurie se nejčastěji vyskytuje u glomerulopatií, hyperkalciurie a syndromu louskáčku (tzv. nutcracker syndrome).
Následně je zapotřebí posoudit, zda se jedná o izolovanou hematurii, nebo jestli v moči nacházíme zároveň proteinurii, jež může být projevem závažnějšího onemocnění, jako jsou akutní nebo chronické glomerulonefritidy. Přítomnost hypertenze či zhoršené funkce ledvin (zvýšený sérový kreatinin) jsou dalšími varovnými známkami, jež vedou k podezření na nefropatii vyžadující širší diagnostiku.
V neposlední řadě nám může v diferenciálně diagnostické rozvaze pomoci vyšetření moči za pomoci mikroskopu s fázovým kontrastem k rozlišení glomerulární a neglomerulární hematurie dle morfologie erytrocytů v závislosti na zdroji přítomnosti erytrocytů v moči. Přítomnost více než 30–40 % dysmorfních erytrocytů a více než 5 % akantocytů (prstenčité formy erytrocytů) obvykle svědčí pro glomerulární původ erytrocytů v moči (tabulka 1).(1,7)
Nejčastější příčiny perzistující mikroskopické hematurie
Hyperkalciurie je definovaná jako odpad vápníku do moči > 0,1 mmol/kg ve 24h sběru moči. Je možné ji prokázat u 11 až 35 % dětí s mikroskopickou hematurií. U malých dětí se v diagnostice běžně používá močový kalcium-kreatininový index, normy dle věku jsou shrnuty v tabulce 4. Nejčastěji se setkáváme s idiopatickou hyperkalciurií, tu lze však diagnostikovat pouze vyloučením jiných možných příčin, jako jsou stavy s vyšší resorpcí kalcia (z gastrointestinálního traktu či osteoresorpcí), případně nižší renální reabsorpcí v tubulech ledvin (u některých tubulopatií). Proto je nález hyperkalciurie vždy indikací k podrobnějšímu vyšetření pacienta.( 8–11)
Table 4. Normální hodnoty kalcium kreatininového indexu vzhledem k věku, upraveno dle (8) 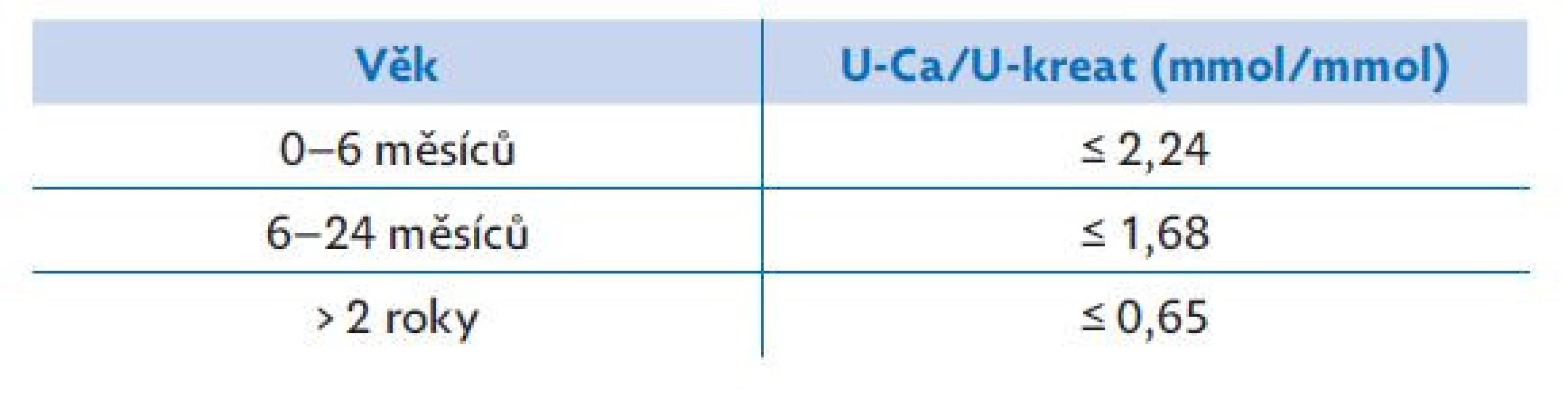
Vzácně se může mikroskopickou hematurií bez jiných příznaků projevit urolitiáza a nefrokalcinóza. Většinou jsou ale příznaky u obou diagnóz více alarmující (renální kolika s vegetativními projevy, makroskopická hematurie a další).(1,8)
Syndrom louskáčku (nutcracker syndrome) vzniká při kompresi levé renální žíly mezi aortou a horní mezenterickou arterií. Předpokládá se, že při tomto útlaku dochází k retrográdnímu toku krve s rozvojem venózní hypertenze a varikózní přestavbou mezi ureterem a ledvinnou pánvičkou. Prevalence je neznámá jednak kvůli nejasným diagnostickým kritériím a dále pro značně variabilní symptomatologii. Tento syndrom se typicky začne projevovat v adolescenci a v mladším dospělém věku v důsledku rychlého růstu v pubertálním období, kdy dojde ke zúžení úhlu mezi aortou a horní mezenterickou arterií. Dvě třetiny pacientů jsou asymptomatické, mezi klinické projevy patří kromě hematurie ortostatická proteinurie, bolest v pánvi a v boku a rozvoj gonadálních varixů. Vyšetřením první volby je dopplerovský ultrazvuk levé renální žíly, výsledek však značně závisí na zkušenosti radiologa. Vyšetření by mělo být provedeno u každého dítěte s nevysvětlitelnou mikroskopickou hematurií, obzvláště u pacientů s ortostatickou proteinurií či typickými klinickými příznaky. Při nejasném závěru dopplerovského ultrazvuku je vhodné doplnit CT nebo MR angiografii, v poslední řadě pak flebografii renálních žil.(12,13)
Postinfekční glomerulonefritida je akutní glomerulonefritida, jež se manifestuje v návaznosti na proběhlou (nejčastěji streptokokovou) infekci. Pacienti se mohou projevovat širokou škálou symptomatologie, někteří mají pouze mikroskopickou hematurii, u jiných se rozvine nefritický syndrom s hypertenzí a poruchou funkce ledvin, výjimečně probíhá tato glomerulonefritida pod obrazem rychle progredující glomerulonefritidy. V laboratoři typicky nacházíme vysoké ASLO a nízkou C3 složku komplementu, jež by se měla znormalizovat do 8 týdnů od manifestace onemocnění. Nález mikroskopické hematurie však může přetrvávat i po dobu několika let.(1,8,14)
IgA nefropatie (Bergerova choroba) je nejčastější chronickou glomerulonefritidou dětského a dospělého věku. 30 % dospělých pacientů progreduje do konečného stadia chronického onemocnění ledvin (ESRD – end-stage renal disease) do 20 let od manifestace onemocnění. Typickým projevem nemoci jsou ataky makroskopické hematurie obvykle v souvislosti s infektem, v mezidobí může být moč bez patologického nálezu, ev. s mikroskopickou hematurií. Také příznaky IgA nefropatie jsou značně variabilní. Onemocnění se může manifestovat mikroskopickou hematurií s lehkou proteinurií nebo bez ní, nefrotickým syndromem nebo jako rychle progredující glomerulonefritida. IgA nefropatii lze definitivně diagnostikovat pouze renální biopsií.(8,15)
Alportův syndrom (AS) je onemocnění charakterizované postižením ledvin, sluchu a očními abnormalitami. Dědičnost je ve většině případů X-vázaná, může být ale i autozomálně recesivní (15 %) či dominantní (5 %). Recentně byla popsána i digenní dědičnost. Příčinou nemoci jsou mutace genů kódujících α řetězce kolagenu typu IV. Fenotyp AS může být různě závažný. Zatímco u některých nemocných nacházíme pouze mikroskopickou hematurii, u jiných pozorujeme progresivní onemocnění ledvin spojené s výrazným extrarenálním postižením. U X-vázané formy AS jsou významněji postižení muži, k rozvoji ESRD dochází do 40 let u 90 % jedinců. Mikroskopická hematurie se objevuje u všech pacientů mužského pohlaví, nacházíme ji i u 95–98 % žen, u kterých probíhá onemocnění mírněji. Navzdory tomu rozvine ESRD do 40 let věku 12 % z nich. Percepční porucha sluchu se objevuje u chlapců v pozdním dětství, u žen pak v dospělosti. Mezi oční postižení v rámci AS řadíme přední lentikonus (protruze čočky) a změny na sítnici či rohovce. Anamnéza mikroskopické hematurie a poruch zraku a sluchu v rodině by měly vyvolat podezření na toto onemocnění a vést ošetřujícího lékaře k provedení genetického vyšetření. Je třeba ale také zdůraznit, že 15 % mutací vzniká de novo, negativní rodinná anamnéza tedy nemoc nevylučuje. Pacienti s autozomálně recesivní formou AS mají obvykle obdobné symptomy jako jedinci s X-vázaným AS, je pro ně ale typická negativní rodinná anamnéza a časná progrese chronického onemocnění ledvin s mediánem nástupu ESRD ve 21 letech. Naproti tomu u pacientů s autozomálně dominantní formou AS vidíme extrarenální příznaky spíše výjimečně a k rozvoji ESRD u nich dochází až v pokročilém věku. V diagnostice AS se využívá biopsie kůže, ledviny a molekulárně genetické vyšetření, jež představuje pro svou neinvazivitu a možnost přesné klasifikace v současné době hlavní diagnostickou modalitu.(8,16,17)
Nemoc tenkých bazálních membrán, nazývaná též benigní familiární hematurie, je autozomálně dominantní onemocnění s rodinným výskytem. Postihuje kolem 1 % populace. Většina pacientů má pouze hematurii bez proteinurie s normální funkcí ledvin a bez hypertenze. Onemocnění však může mít i závažnější průběh, proto je název benigní familiární hematurie poněkud zavádějící vzhledem k riziku progrese chronického onemocnění ledvin do ESRD u malé části pacientů. Charakteristické pro nemocné je geneticky podmíněné ztenčení glomerulární bazální membrány zjištěné při vyšetření elektronovým mikroskopem. U nemocných byly nalezeny četné heterozygotní varianty řetězců α3 a α4 kolagenu IV. Někteří experti řadí pacienty s hematurií, tenkými bazálními membránami a výše zmíněnými variantami α řetězců kolagenu IV do skupiny autozomálně dominantního AS. Tím diagnózu nemoci tenkých bazálních membrán vyřazují z klasifikace onemocnění ledvin. Správné zařazení této diagnostické jednotky je však stále předmětem diskuse odborníků.(1,8,17,18)
Henochova–Schönleinova purpura (IgA vaskulitida) je nejčastější vaskulitidou dětského věku. Diagnóza se stanovuje na základě nálezu hmatné purpury a alespoň jednoho z následujících kritérií: difuzní břišní bolest, artritida nebo artralgie, bioptický kožní nález leukocytoklastické vaskulitidy s predominantním zastoupením IgA depozit nebo nález proliferativní glomerulonefritidy s predominantním zastoupením IgA depozit v renální tkáni a postižení ledvin (hematurie a/nebo proteinurie). Renální postižení se vyskytuje u 20–80 % dětí, v případě nálezu pouze mikroskopické hematurie bez dalších projevů postižení ledvin nevyžaduje medikamentózní terapii a obvykle se spontánně upraví v čase. U části dětí však může být průběh glomerulonefritidy závažný s nutností provedení renální biopsie. Vzhledem k typickému nálezu hmatné purpury nečiní obvykle stanovení diagnózy větší problém.(19,20)
Mikroskopická hematurie je zpravidla součástí močových nálezů u dalších glomerulonefritid a systémových onemocnění. Je třeba na ně pomýšlet především při rozvoji hypertenze, zhoršení renálních funkcí nebo v případě významné proteinurie, ev. při abnormálních imunologických nálezech (např. nízká C3 a/nebo C4 složka komplementu při lupusové nefritidě, membranoproliferativní glomerulonefritidě a dalších).(8)
Nesmíme ovšem opomenout, že hematurie může být také příznakem Wilmsova tumoru.(21)
Závěr
Mikroskopická hematurie je u dětí poměrně častým nálezem, pro který jsou obvykle sledované v ambulanci dětského nefrologa. I když se u těchto pacientů většinou jedná o benigní diagnózy, je třeba vždy pomýšlet i na závažnější stavy, jako jsou glomerulonefritidy nebo systémová onemocnění. Rozvoj molekulárně genetických metod významně zlepšil diagnostiku hereditárních nefropatií s hematurií. Znalost základní diferenciální diagnostiky je zcela zásadní pro správný diagnosticko-terapeutický postup.
Korespondenční adresa:
MUDr. Patrik Konopásek
Pediatrická klinika 2. LF UK a FN v Motole
V Úvalu 84
150 06 Praha 5
Sources
1. Boyer OG. Evaluation of microscopic hematuria in children. In: uptodate. com. [online]. [cit. 6-12-2021] Dostupné na: https: //www.uptodate. com/contents/evaluation-of-microscopic-hematuria-in-children. Path: Homepage; Contents; Topics by Specialty; Pediatrics; Pediatric Nephrology; Evaluation of microscopic hematuria in children.
2. Chen MC, Wang JH, Chen JS, et al. Socio-demographic factors affect the prevalence of hematuria and proteinuria among school children in Hualien, Taiwan: A longitudinal localization–based cohort study. Front Pediatr 2020; 8 : 600907.
3. Vehaskari VM, Rapola J, Koskimies O, et al. Microscopic hematuria in school children: epidemiology and clinicopathologic evaluation. J Pediatr 1979; 95(5): 676–84.
4. Iitaka K, Igarashi S, Sakai T. Hypocomplementaemia and membranoproliferative glomerulonephritis in school urinary screening in Japan. Pediatr Nephrol 1994; 8(4): 420–2.
5. David J, Šibíková M, Fencl F. Rabdomyolýza u dětí. Pediatr Praxi 2020; 21(1): 17–21.
6. Gut J. Hematurie jako příznak. Pediatr Praxi 2016; 17(6): 353–356.
7. Fogazzi GB, Edefonti A, Garigali G, et al. Urine erythrocyte morphology in patients with microscopic haematuria caused by a glomerulopathy. Pediatr Nephrol 2008; 23(7): 1093–100.
8. Zieg J, Skálová S. Dětská nefrologie do kapsy. Praha: Mladá fronta 2019.
9. Stapleton FB, Roy S 3rd, Noe HN, Jerkins G. Hypercalciuria in children with hematuria. N Engl J Med 1984; 310(21): 1345–8.
10. Stapleton FB. Idiopathic hypercalciuria: association with isolated hematuria and risk for urolithiasis in children. The Southwest Pediatric Nephrology Study Group. Kidney Int 1990; 37(2): 807–11.
11. Feld LG, Meyers KE, Kaplan BS, Stapleton FB. Limited evaluation of microscopic hematuria in pediatrics. Pediatrics 1998; 102(4): E42.
12. Ananthan K, Onida S, Davies AH. Nutcracker syndrome: an update on current diagnostic criteria and management guidelines. Eur J Vasc Endovasc Surg 2017; 53 : 886–894.
13. Vianello FA, Mazzoni MB, Peeters GG, et al. Micro - and macroscopic hematuria caused by renal vein entrapment: systematic review of the literature. Pediatr Nephrol 2016; 31(2): 175–84.
14. Sagel I, Treser G, Ty A, et al. Occurrence and nature of glomerular lesions after group A streptococci infections in children. Ann Intern Med 1973; 79(4): 492–9.
15. KDI GO 2021 Clinical practice guideline for the management of glomerular disease. Kidney Int 2021; 100 : 1–276.
16. Nozu K, Nakanishi K, Abe Y, et al. A review of clinical characteristics and genetic backgrounds in Alport syndrome. Clin Exp Nephrol 2019; 23(2): 158–168.
17. Kashtan CE. Alport syndrome: achieving early diagnosis and treatment. Am J Kidney Dis 2021; 77(2): 272–279.
18. Savige J, Gregory M, Gross O, et al. Expert guidelines for the management of Alport syndrome and thin basement membrane nephropathy. J Am Soc Nephrol 2013; 24(3): 364–75.
19. Ozen S, Pistorio A, Iusan SM, et al. Paediatric Rheumatology International Trials Organisation (PRINTO). EULAR/PRINTO/PRES criteria for Henoch-Schönlein purpura, childhood polyarteritis nodosa, childhood Wegener granulomatosis and childhood Takayasu arteritis: Ankara 2008. Part II: Final classification criteria. Ann Rheum Dis 2010; 69(5): 798–806.
20. Ozen S, Marks SD, Brogan P, et al. European consensus-based recommendations for diagnosis and treatment of immunoglobulin A vasculitis – the SHARE initiative. Rheumatology (Oxford) 2019; 58(9): 1607–1616.
21. Varan A. Wilms’ tumor in children: an overview. Nephron Clin Pract 2008; 108(2): c83–90.
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2022 Issue 4-
All articles in this issue
- Co jsme psali
- Purkyňova cena za rok 2022 byla udělena prof. MUDr. Otto Hrodkovi, DrSc.
- Editorial
- Gregor Mendel celebrates 200 years: from the gardens of the Augustinian monastery in Brno to the causal treatment of monogenic diseases
- Dystrophinopathies
- Gregor Mendel and regulation of child’s growth: genes, molecules, and paediatric clinical routine
- DYRK1A-related intellectual disability syndrome
- Fabry disease in childhood – overview and a case report
- The clinical phenotype and genetic diagnosis of a rare cutis laxa syndrome in a newborn with multiple anomalies
- Patient with Williams-Beuren syndrome in paediatrician’s office
- Differential diagnosis of microscopic hematuria
- Hyperthermia, its causes and risks from the pathophysiologist’s perspective
- Sepsis in children
- Za MUDr. Janem Škovránkem, CSc.
- Pediatrická poezie
- Ze sbírky moderního českého a slovenského umění
- Genetic diversity of monogenic diabetes in Ukraine
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Sepsis in children
- Differential diagnosis of microscopic hematuria
- Hyperthermia, its causes and risks from the pathophysiologist’s perspective
- Dystrophinopathies
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

