-
Medical journals
- Career
Porucha růstu u 11leté dívky s diabetem
Authors: R. Pomahačová 1; T. Pomahačová 2; K. Fiklík 1; P. Paterová 1; J. Sýkora 1
Authors‘ workplace: Dětská klinika FN Plzeň, Univerzita Karlova v Praze, Lékařská fakulta v Plzni 1; Neonatologické oddělení FN a LF UK Plzeň 2
Published in: Čes-slov Pediat 2020; 75 (4): 256-261.
Category:
Overview
Syndrom přerušené stopky hypofýzy (PSIS, pituitary stalk interruption syndrome) je jednou z příčin vrozeného hypopituitarismu. Vzniká na genetickém podkladě v důsledku poruchy morfogeneze hypofýzy. Typickým nálezem na magnetické rezonanci mozku (MR) je hypoplazie nebo aplazie adenohypofýzy, ektopicky uložená neurohypofýza a chybění nebo ztenčení stopky hypofýzy. Vzácnou příčinou získaného hypopituitarismu může být v dětském věku autoimunitní hypofyzitida.
Prezentujeme případ 11leté dívky, u které byl při záchytu iniciální fáze diabetes mellitus 1. typu (DM) současně zjištěn kombinovaný pituitární deficit růstového hormonu, centrální hypotyreóza a centrální hypokortikalismus. K diagnóze hypopituitarismu vedla růstová porucha s progresivní růstovou retardací přítomnou od 7 let věku dítěte. V diferenciální diagnóze bylo primárně pomýšleno na autoimunitní hypofyzitidu, nález na MR mozku však svědčil pro PSIS. Deficit kortisolu a růstového hormonu ovlivnil manifestaci DM a iniciální potřebu inzulinu před zahájením substituční hormonální terapie hydrocortisonem a růstovým hormonem.
Klíčová slova:
porucha růstu – hypopituitarismus – syndrom přerušené stopky hypofýzy – diabetes mellitus 1. typu – autoimunitní hypofyzitida
ÚVOD
Růst dítěte je za fyziologických okolností zákonitým procesem. Do dvou let věku dítě zaujme v růstové percentilové síti místo, které mu je geneticky predikované a v tomto percentilovém pásmu by mělo růst plynule po celé dětské růstové období. Zpomalení nebo urychlení růstu po 2. roce života může signalizovat závažné onemocnění dítěte. Při hodnocení růstu dítěte je třeba současně posuzovat jeho růst v geneticky predikovaném pásmu daném výškami rodičů [1‒3]. V odhalení příčiny zpomalování růstu dítěte nám může pomoci zhodnocení vývoje BMI (Body Mass Index), například progredující BMI u těžké primární hypotyreózy nebo u Cushingova syndromu, naopak klesající BMI u celiakie nebo Crohnovy choroby. K diagnóze nás může přiblížit vlastní klinické vyšetření pacienta, například disproporcionální růst se zkrácením dolního tělesného segmentu a svalovou hypertrofií u hypochondroplazie, Turnerova syndromu nebo Lériho-Weillova syndromu [1‒3]. Zkušenosti ukazují, že porucha růstu se zpomalováním růstového tempa může předcházet i několik let vlastní klinické manifestaci onemocnění. Typickým příkladem je získaný deficit růstového hormonu u pacientů s kraniofaryngeomem, nádorem vycházejícím ze zbytků Rathkeho výchlipky [2, 3].
Vyšetření dítěte s poruchou růstu je tedy vždy komplexní. Vedle endokrinní poruchy, jako je především hypotyreóza a deficit růstového hormonu, vylučujeme chronické onemocnění systémové povahy (tab. 1).
Table 1. Některé patofyziologické mechanismy vedoucí k růstové retardaci u dětí s chronickým onemocněním. (Upraveno dle Lebl J, Al Taji E, Koloušková S, et al. Dětská endokrinologie a diabetologie. Praha: Galén, 2016, s. 68) 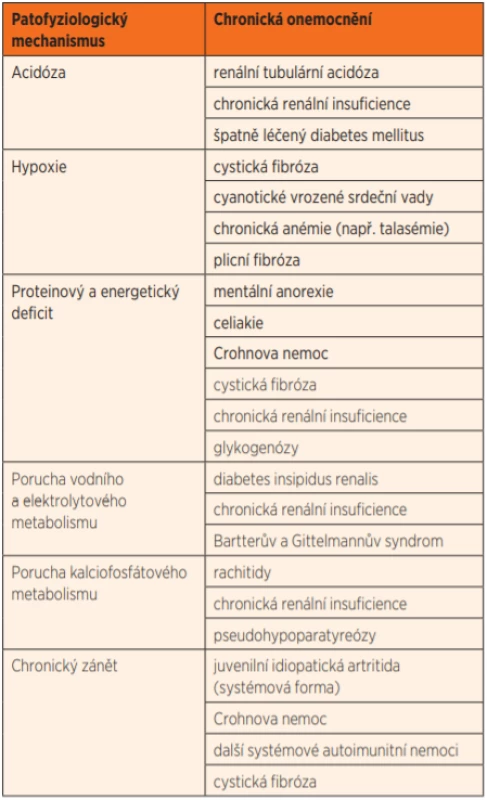
Hypopituitarismus je porucha funkce adenohypofýzy s deficitem jednoho nebo více hypofyzárních hormonů. Nejčastěji se jedná o deficit růstového hormonu, který může být izolovaný nebo kombinovaný s deficity dalších hypofyzárních hormonů. Z hlediska etiologie je hypopituitarismus vrozený nebo získaný. Příčinou vrozeného hypopituitarismu může být porucha morfogeneze hypofýzy (např. holoprosencefalie, septooptická dysplazie, syndrom přerušené stopky hypofýzy) nebo porucha diferenciace hypofýzy (např. mutace PROP1 genu, POU1F1 genu). Vrozený hypopituitarismus se může projevit již u novorozence těžkými hypoglykémiemi v důsledku deficitu růstového hormonu a kortisolu, žloutenkou a u chlapců hypogenitalismem (mikropenis, retence testes) v důsledku prenatálního deficitu gonadotropinů. Nejzávažnější získanou postnatální organickou příčinou deficitu růstového hormonu jsou nádory hypotalamo-hypofyzární oblasti, především kraniofaryngeom, dále germinom, gliom optiku a histiocytóza z Langerhansových buněk. Další postnatální příčinou deficitu růstového hormonu může být zánětlivé onemocnění CNS (meningitida, encefalitida), radioterapie pro jiné tumory CNS, úrazy mozku nebo autoimunitní hypofyzitida [1‒3]. Deficit růstového hormonu je jednou z indikací k léčbě růstovým hormonem do ukončení růstu. U těžkého deficitu pak pokračujeme v léčbě sníženou dávkou růstového hormonu z tzv. metabolické indikace, kdy se uplatňuje jeho pozitivní proteoanabolický, lipolytický a hyperglykemizující efekt [2, 3].
KAZUISTIKA
Dívka se narodila z první fyziologické gravidity rodičům z nepříbuzenského vztahu v termínu, sekcí pro hrozící hypoxii plodu, s porodní hmotností 3400 g a délkou 50 cm. Poporodní adaptace byla fyziologická, na hmotnosti prospívala a její psychomotorický vývoj byl v normě. Nikdy vážněji nestonala. Měla negativní alergickou anamnézu. Ve škole se učila výborně, aktivně nesportovala. Rodinná anamnéza byla z hlediska výskytu diabetes mellitus 1. typu (DM) a obecně autoimunitních onemocnění negativní. Výška otce byla 175 cm a matky 165 cm.
V 11 letech věku byla odeslána praktickým lékařem k vyšetření pro náhodně zachycenou glykosurii s podezřením na DM. Osmotické symptomy manifestního DM nebyly přítomny. Tomu odpovídala fyziologická ranní lačná glykémie 4,8 mmol/l (norma <5,6 mmol/l). Výškou při našem prvovyšetření 122 cm (-3,8 SDS; výška vyjádřená pomocí skóre směrodatné odchylky) byla hluboko pod 3. percentilem, podle BMI 15,5 kg/m² byla v dolním pásmu normální výživy. Doplněná růstová křivka ukazovala do 7 let věku plynulý růst těsně pod 3. percentilem, od 7 let věku bylo patrné progresivní růstové opožďování s poklesem v růstové křivce hluboko pod 3. percentil (obr. 1). Fenotypicky měla proporcionální postavu, nebyla stigmatizovaná a byla prepubertální.
Image 1. Růstová křivka ukazuje do 7 let věku plynulý růst těsně pod 3. percentilem, od 7 let věku progresivní růstové opožďování s poklesem výšky hluboko pod 3. percentil. Po zahájení kombinované substituční hormonální terapie v 11 letech věku je patrná růstová akcelerace. V 12,5 letech věku nastupuje spontánní puberta. Růst ukončen v 16 letech věku. Výška při stanovení diagnózy hypopituitarismu 122 cm. Finální výška 161 cm. 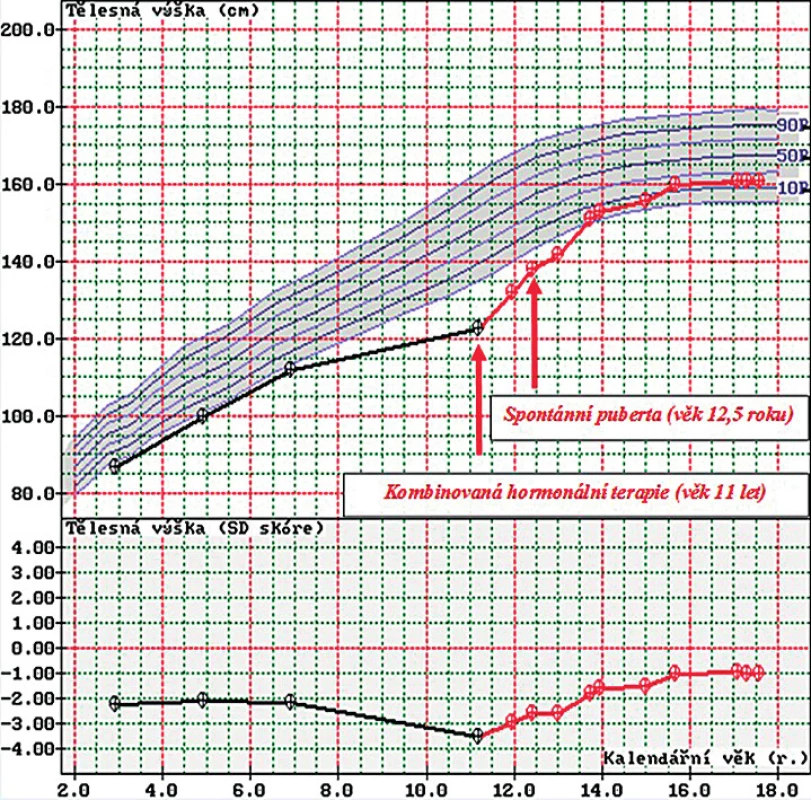
Před sebou jsme měli pacientku se suspektní poruchou sacharidového metabolismu a současně přítomnou těžkou růstovou poruchou. V tomto směru byla provedena komplexní vyšetření.
Při vyšetření sacharidového metabolismu potvrdil orální glukózový toleranční test (oGTT) poruchu glukózové tolerance. Glykémie před perorálním podáním glukózy 1,75 g/kg byla 4,2 mmol/l a za 2 hodiny po podání glukózy byla glykémie 9,9 mmol/l (pro normální glukózovou toleranci svědčí glykémie za 2 hodiny po podání glukózy pod 7,8 mmol/l; pro DM glykémie nad 11,1 mmol/l a pro poruchu glukózové tolerance glykémie mezi 7,8 a 11,1 mmol/l). Pro diagnózu DM ale svědčily monitorované postprandiální glykémie opakovaně přesahující hodnotu 11,1 mmol/l. Diagnóze DM současně odpovídala vysoká hodnota glykovaného hemoglobinu (HbA1c 68 mmol/mol, norma: <42). Podle zvýšených pankreatických protilátek proti tyrosinfosfatáze (aIA2 28,1 U/ml, norma: <1) byla potvrzena autoimunitní etiologie DM, v tomto případě tedy iniciální fáze DM.
Při vyšetření poruchy růstu jsme u pacientky vyloučili chronické onemocnění systémové povahy, včetně systémové autoimunitní choroby s ohledem na DM 1. typu. Farmakologická stimulace produkce růstového hormonu (pyridostigmin-clonidinový test po primingu pohlavním hormonem) potvrdila těžký nedostatek růstového hormonu. Při testu došlo k maximálnímu vzestupu v hladině růstového hormonu (RH) na 1,22 mIU/l (požadovaný vzestup je nad 20 mIU/l). Těžkému nedostatku RH odpovídala extrémně nízká hladina inzulinu podobného růstového faktoru 1 (IGF-1) 6 ng/ml (-4 SD). Snížené hladiny tyreotropního hormonu (TSH) 0,2 mIU/l (norma: 0,3‒4) a volného tyroxinu (fT4) 8 pmol/l (norma: 11,5‒23) potvrdily současně centrální hypotyreózu. Nízké hladiny ranního sérového kortisolu 81,6 nmol/l (norma: 200‒650) a odpoledního sérového kortisolu 20,2 (norma: 50‒350) ukazovaly na hypokortikalismus, podle normální hladiny adrenokortikotropního hormonu (ACTH) 14 μg/l (norma: 10‒60) centrální etiologie. Vyšetření magnetickou rezonancí mozku (MR) odhalilo PSIS („pituitary stalk interruption syndrome“) s nálezem hypoplastické hypofýzy, ektopicky uložené neurohypofýzy a chyběním stopky hypofýzy (obr. 2). Biologický věk dítěte byl opožděný o 3 roky a odpovídal věku 8 let (hodnoceno podle Greulicha a Pyleové).
Image 2. Magnetická rezonance mozku. PSIS („pituitary stalk interruption syndrome“) s nálezem hypoplastické hypofýzy (A), ektopicky uložené neurohypofýzy (B) a chyběním stopky hypofýzy. (Vlastní fotodokumentace)
Fig. 2. Magnetic resonance imaging of the brain. PSIS („pituitary stalk interruption syndrome„) with pituitary hypoplasia (A), ectopic posterior pituitary (B) and absence of pituitary stalk.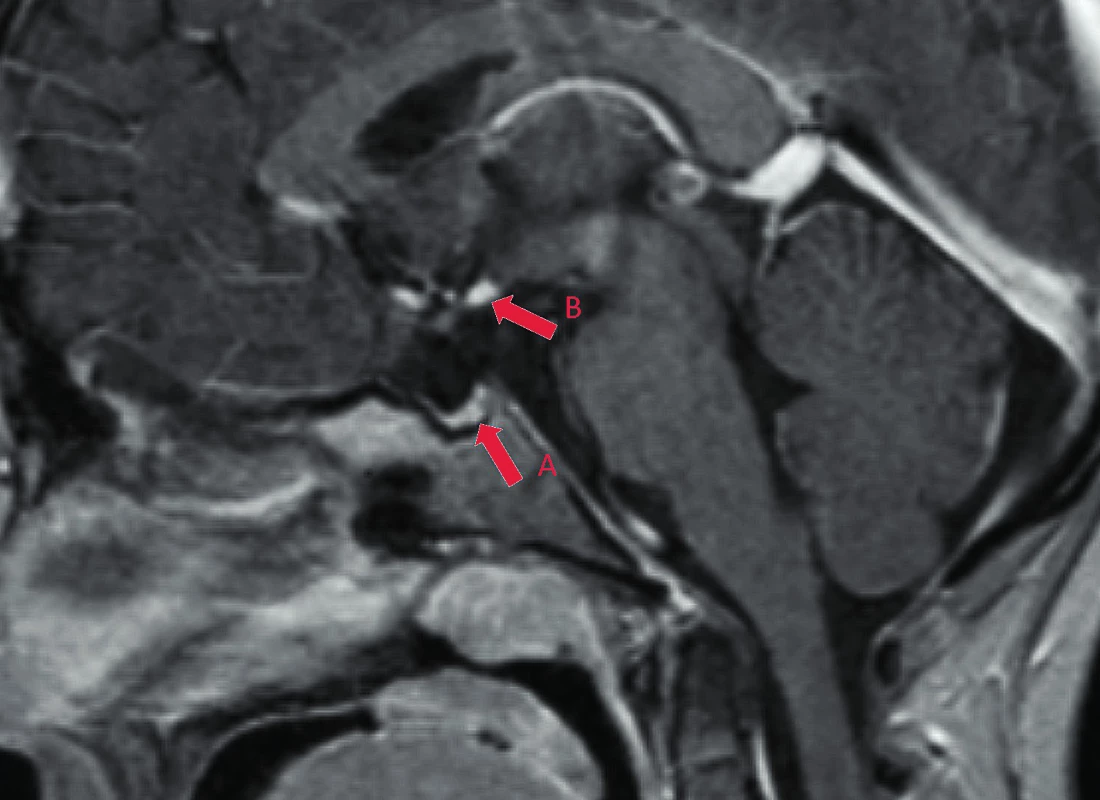
Vyšetření potvrdila diabetes mellitus 1. typu a kombinovaný pituitární deficit růstového hormonu, centrální hypotyreózu a centrální hypokortikalismus při syndromu přerušené stopky hypofýzy.
Po stanovení diagnózy DM byl u pacientky zahájen intenzifikovaný inzulinový režim s aplikací rychle působícího inzulinu k hlavním jídlům a střednědobého inzulinu na noc. Přes nízkou potřebu inzulinu (0,2 j/kg/den) měla pacientka tendenci k hypoglykémiím. Po nasazení substituční terapie hydrokortisonem a růstovým hormonem pro potvrzený hypopituitarismus došlo ke vzestupu inzulinové rezistence, tím ke vzestupu glykémií a potřeby inzulinu na 0,5 j/kg/den. Při této komplexní hormonální substituční terapii vidíme na růstové křivce příznivou růstovou akceleraci (obr. 1).
Ve 12,5 letech věku nastoupila spontánní centrální izosexuální puberta. Pacientka dosáhla v 16 letech věku, ve shodě s rodičovsku predikcí, finální výšky 161 cm. Pro potvrzený těžký nedostatek růstového hormonu při retestaci po 2měsíčním přerušení léčby RH jsme pokračovali po ukončení růstu v léčbě RH z metabolické indikace. Z hlediska DM je pacientka v současné době léčena inzulinovou pumpou s výbornou kompenzací diabetu. Zůstává na kombinované substituční hormonální terapii, její gonadální funkce je fyziologická.
DISKUSE
Prezentujeme případ pacientky, u které v 11 letech věku byl při záchytu iniciální fáze diabetes mellitus 1. typu současně zjištěn kombinovaný pituitární deficit růstového hormonu, centrální hypotyreóza a centrální hypokortikalismus. K diagnóze hypopituitarismu vedla růstová porucha s progresivní růstovou retardací přítomnou od 7 let věku dítěte (obr. 1). Předpokládanou příčinou hypopituitarismu byla, s ohledem na přítomnost diabetes mellitus 1. typu, autoimunitní hypofyzitida (AH). MR mozku překvapivě odhalila syndrom přerušené stopky hypofýzy. U pacientky se z hlediska etiologie tedy jedná o dvě nesouvisející endokrinopatie, vzájemně se ale ovlivňující s ohledem na účinky jednotlivých hormonů. V případě naší pacientky hypopituitarismus (deficit kortisolu a růstového hormonu) ovlivnil manifestaci diabetes mellitus, výsledek oGTT a potřebu inzulinu. V diskusi se proto zaměříme na problematiku syndromu přerušené stopky hypofýzy, autoimunitní hypofyzitidy a na úlohu kontraregulačních hormonů (kortisol, růstový hormon) v regulaci sacharidového metabolismu.
Syndrom přerušené stopky hypofýzy (PSIS, pituitary stalk interruption syndrome) je jednou z častých příčin vrozeného hypopituitarismu, který vzniká v důsledku poruchy morfogeneze hypofýzy. Je charakterizován typickým nálezem na MR mozku zahrnujícím hypoplazii nebo aplazii adenohypofýzy (obraz „empty sella“), ektopickou neurohypofýzu a chybění nebo ztenčení stopky hypofýzy [1, 4, 5]. Může se pojit s dalšími malformacemi mozku, s kardiálními, očními, zubními, kraniofaciálními vadami a s vadami gastrointestinálního systému [4]. PSIS byl dříve dáván do souvislosti s perinatálním traumatem při porodu koncem pánevním s poškozením stopky hypofýzy a přerušením komunikace mezi hypotalamem a hypofýzou. Proti teorii perinatálního traumatu stojí v některých případech zjištěná mutace genů, které kódují transkripční faktory klíčové pro fyziologický vývoj hypofýzy a středočárových struktur (HESX1, LHX4, OTX2, SOX3, PROKR2, GPR161) [1, 4, 6, 7]. Dnes se naopak soudí, že fetální poloha koncem pánevním je důsledkem PSIS [1]. Diagnóza PSIS je většinou stanovena v dětství při vyšetření dítěte pro poruchu růstu. Ve studii Céline Bar et al. byl medián věku stanovení diagnózy PSIS 4 roky. Jeden pacient byl v této studii diagnostikován ve věku 16 let v souvislosti s malým vzrůstem a opožděnou pubertou [4]. Méně často je diagnóza stanovena již v novorozeneckém období v souvislosti s hypoglykémiemi (deficit RH a kortisolu), žloutenkou a mikropenisem/kryptorchismem u chlapců (prenatální deficit gonadotropinů) [4, 8‒10]. Tyto symptomy u novorozence jsou tedy důsledkem těžkého kombinovaného deficitu hypofyzárních hormonů a měly by být indikací k zobrazení hypofýzy [4]. Pozdější diagnózu PSIS, na podkladě růstové poruchy v průběhu dětství, lze vysvětlit méně těžkou endokrinní poruchou. Pro tuto domněnku svědčí fakt, že 66 % těchto dětí má v době stanovení diagnózy pouze izolovaný deficit RH. U většiny těchto dětí se ale postupně vyvine kombinovaný deficit hypofyzárních hormonů, proto musí být v tomto směru pravidelně sledovány [4].
Jak uvádíme v úvodu diskuse, primární předpokládanou příčinou hypopituitarismu u naší pacientky byla autoimunitní hypofyzitida, která je vzácnou příčinou získaného hypopituitarismu u dětí. Přesný údaj o incidenci v této věkové skupině není znám [11]. Častěji se toto onemocnění vyskytuje u dospělých pacientů, predominantně u gravidních žen v konečné fázi těhotenství nebo v časném postpartálním období [12‒14]. U dětských pacientů jsou obě pohlaví postižena stejně [11, 15]. U většiny pacientů je popisována přidružená autoimunitní choroba (např. Hashimotova tyroiditida, DM 1. typu, Addisonova choroba, systémový lupus erythematodes) [12]. Přesný mechanismus rozvoje autoimunitní reakce je předmětem studií. Rozvoj AH byl například popsán u pacientů s anamnézou neuroinfekce či kraniotraumatu. U geneticky predisponovaného jedince dochází vlivem iniciálního spouštěcího faktoru k expozici neoantigenů hypofýzy s rozvojem autoimunitního zánětu [11, 16]. Nejčastějším klinickým projevem u dětí je v 85 % centrální diabetes insipidus (CDI) a v 76 % deficit růstového hormonu. Pacienti mohou být panhypopituitární. Klinickým projevem AH může být také porucha vizu v důsledku útlaku chiasma opticum a známky nitrolební hypertenze [11]. Typickým nálezem na MR mozku je zvětšená hypofýza homogenní hyperintenzity po podání kontrastní látky, tzv. „dural tail sign“ (ztluštění tvrdé pleny vyčnívající ze zvětšené hypofýzy) a ztluštělá stopka hypofýzy (obr. 3). V pozdní fázi onemocnění může dojít k involuci hypofýzy [11, 12].
Image 3. Magnetická rezonance mozku. Autoimunitní hypofyzitida. Zvětšená hypofýza homogenní hyperintenzity. (Zdroj: Lymphocytic hypophysitis | Radiology Reference Article | Radiopaedia.org. Radiopaedia.org, the wiki-based collaborative Radiology resource [online]. Copyright© 2005 [cit. 27.03.2020]. Dostupné z: https://radiopaedia.org/articles/ /lymphocytic-hypophysitis)
Fig. 3. Magnetic resonance imaging of the brain. Autoimmune hypophysitis. Enlarged pituitary gland of homogeneous hyperintensity![Magnetická rezonance mozku. Autoimunitní hypofyzitida. Zvětšená hypofýza homogenní hyperintenzity.
(Zdroj: Lymphocytic hypophysitis | Radiology Reference Article | Radiopaedia.org.
Radiopaedia.org, the wiki-based collaborative Radiology resource [online].
Copyright© 2005 [cit. 27.03.2020]. Dostupné z: https://radiopaedia.org/articles/
/lymphocytic-hypophysitis)<br>
Fig. 3. Magnetic resonance imaging of the brain. Autoimmune hypophysitis. Enlarged pituitary gland of homogeneous hyperintensity](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/173b207fdd06aaa4bdc075aa13ee6d68.jpeg)
Biopsie, definitivně potvrzující diagnózu AH, je indikována u nejzávažnějších pacientů (např. hrozící porucha vizu), kdy je zvažována resekce hypofýzy. Literární zdroje uvádějí, že klinický význam detekce hypofyzárních autoprotilátek v rutinní diagnostice je limitován nízkou diagnostickou senzitivitou a specificitou [11]. Léčba AH spočívá v hormonální substituci, případně v neurochirurgické intervenci u nejtěžších případů. U většiny pacientů je volen konzervativní postup. Je popisován příznivý efekt kortikosteroidů i jiných imunosupresiv (azathioprin, metotrexát) ve smyslu potlačení zánětlivé reakce, redukce velikosti hypofýzy a úpravy endokrinní dysfunkce [11, 17]. Byly publikovány případy spontánní remise onemocnění s kompletní úpravou klinických projevů včetně normalizace hladin hypofyzárních hormonů. Většina pacientů však vyžaduje trvalou substituční hormonální léčbu [11].
V případě naší pacientky byla diagnóza hypopituitarismu v 11 letech věku pozdní. Růstová křivka jednoznačně ukazovala zpomalování růstu již od 7 let věku. Magnetická rezonance mozku vyloučila možnost původně předpokládané autoimunitní hypofyzitidy, pro kterou je typický výše uvedený radiologický nález. Naopak odhalila syndrom přerušené stopky hypofýzy s hypoplastickou adenohypofýzou, ektopicky uloženou neurohypofýzou a chyběním stopky hypofýzy.
V době stanovení diagnózy hypopituitarismu měla pacientka kombinovaný pituitární deficit růstového hormonu, centrální hypotyreózu a centrální hypokortikalismus. Proti deficitu gonadotropinů svědčil spontánní nástup puberty. Podle průběhu růstové křivky a ve shodě s literárními údaji se lze domnívat, že u pacientky v průběhu dětství došlo k postupnému selhání hypofyzární funkce [4].
V diagnostice DM a v následné léčbě inzulinem hrála roli úloha kontraregulačních hormonů (kortisol, růstový hormon) v regulaci sacharidového metabolismu. Těžký deficit těchto hormonů vedl, v důsledku nízké inzulinové rezistence, k poruše glukózové tolerance při oGTT a současně způsobil iniciální nízkou potřebu inzulinu se sklonem k hypoglykémiím. Naopak zahájení substituční léčby hydrocortisonem a růstovým hormonem vedlo, v důsledku vzestupu inzulinové rezistence a glukoneogeneze, k hyperglykémiím se vzestupem potřeby inzulinu.
ZÁVĚR
Syndrom přerušené stopky hypofýzy, který byl dříve dáván do souvislosti s perinatálním traumatem při porodu koncem pánevním, je dnes považován za jednu z příčin vrozeného hypopituitarismu v důsledku geneticky podmíněné poruchy morfogeneze hypofýzy. Méně často je tato diagnóza stanovena již v novorozeneckém období v souvislosti s hypoglykémiemi, žloutenkou a mikropenisem/kryptorchismem u chlapců. Tito pacienti mají těžký kombinovaný pituitární deficit. Častěji je syndrom diagnostikován později v dětství na podkladě růstové poruchy. V tomto případě mohou mít pacienti v době stanovení diagnózy pouze izolovaný deficit růstového hormonu. U většiny z nich se postupně vyvíjí kombinovaný pituitární deficit, v tomto směru proto vyžadují pravidelné sledování vývoje hypofyzární funkce.
Autoimunitní hypofyzitida je u dětí vzácná forma získaného hypopituitarismu. Pro diagnózu svědčí typický nález zvětšené hypofýzy se ztluštělou stopkou na MR mozku. Hypofyzární autoprotilátky v rutinní diagnostice nemají, pro jejich nízkou senzitivitu a specificitu, význam. Kromě hypopituitarismu je pro tyto pacienty typický vývoj centrálního diabetes insipidus.
Kontraregulační hormony, kortisol a růstový hormon, ovlivňují sacharidový metabolismus prostřednictvím inzulinové rezistence a glukoneogeneze.
Hlavním cílem našeho sdělení je zdůraznění správné monitorace růstu dítěte s cílem časného odhalení růstové poruchy a odstranění její příčiny. Vyšetření příčiny poruchy růstu dítěte je vždy komplexní.
Doc. MUDr. Renata Pomahačová, Ph.D.
Dětská klinika FN Plzeň
Univerzita Karlova v Praze,
Lékařská fakulta v Plzni
Alej Svobody 80
304 60 Plzeň
e-mail: pomahacova@fnplzen.cz
Sources
1. Lebl J, Krásničanová H. Růst dětí a jeho poruchy. Praha: Galén, 1996.
2. Lebl J, Al Taji E, Koloušková S, et al. Dětská endokrinologie a diabetologie. Praha: Galén, 2016.
3. Pomahačová R, Kalvachová B. Dětská endokrinologie do kapsy. Praha: Mladá fronta, 2013.
4. Bar C, Zadro C, Diene G, et al. Pituitary stalk interruption syndrome from infancy to adulthood: Clinical, hormonal and radiological assessment according to the initial presentation. PLoS One 2015; 10 (11): e0142354. doi: 10.1371/journal.pone.0142354.
5. Fujisawa I, Kikuchi K, Nishimura K, et al. Transection of the pituitary stalk: development of an ectopic posterior lobe assessed with MR imaging. Radiology 1987; 165 (2): 487–489. PMID: 3659371.
6. Reynaud R, Albarel F, Saveanu A, et al. Pituitary stalk interruption syndrome in 83 patients: novel HESX1 mutation and severe hormonal prognosis in malformative forms. Eur J Endocrinol 2011; 164 (4): 457–465. doi: 10.1530/EJE-10-0892. PMID: 21270112.
7. Melo ME, Marui S, Carvalho LR, et al. Hormonal, pituitary magnetic resonance, LHX4 and HESX1 evaluation in patients with hypopituitarism and ectopic posterior pituitary lobe. Clin Endocrinol (Oxf) 2007; 66 (1): 95–102.
8. Pinto G, Netchine I, Sobrier ML, et al. Pituitary stalk interruption syndrome: a clinical-biological-genetic assessment of its pathogenesis. J Clin Endocrinol Metab 1997; 82 (10): 3450–3454. PMID: 9329385.
9. Tauber M, Chevrel J, Diene G, et al. Long-term evolution of endocrine disorders and effect of GH therapy in 35 patients with pituitary stalk interruption syndrome. Horm Res 2005; 64 (6): 266–73. PMID: 16260897.
10. Guo Q, Yang Y, Mu Y, et al. Pituitary stalk interruption syndrome in Chinese people: clinical characteristic analysis of 55 cases. PLoS One 2013; 8 (1): e53579. PMID: 23341953. doi: 10.1371/journal.pone.0053579.
11. Romano A, Rigante D, Cipolla C. Autoimmune phenomena involving the pituitary gland in children: New developing data about diagnosis and treatment. Autoimmun Rev 2019; 18 (10): 102363.
12. Kalra AA, Riel-Romero RM, Gonzalez-Toledo E. Lymphocytic hypophysitis in children: A novel presentation and literature review. J Child Neurol 2011; 26 (1): 87–94.
13. Molitch ME, Gillam M. Lymphocytic hypophysitis. Horm Res 2007; 68 (5): 145–150.
14. Rivera JA. Lymphocytic hypophysitis: disease spectrum and approach to diagnosis and therapy. Pituitary 2006; 9 : 35–45.
15. Kalra AA, Riel-Romero RM, Gonzalez-Toledo E. Lymphocytic hypophysitis in children: A novel presentation and literature review. J Child Neurol 2011; 26 (1): 87–94.
16. Lupi I, Broman KW, Tzou SC, et al. Novel autoantigens in autoimmune hypophysitis. Clin Endocrinol 2008; 69 : 269–278.
17. Falorni A, Minarelli V, Bartoloni E, et al. Diagnosis and classification of autoimmune hypophysitis. Autoimmun Rev 2014; 13 : 412–6.
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2020 Issue 4-
All articles in this issue
- Dětský růst v zrcadle času – a věčný třetí percentil
- Analýza dat z celostátního registru pacientů léčených růstovým hormonem REPAR
- Význam acidolabilní podjednotky (ALS) v etiologii a v diagnostice malého vzrůstu
- Syndrom Noonanové a další RASopatie: Etiologie, diagnostika a terapie
- Syndrom Noonanové z pohledu dětského kardiologa
- Prenatální fenotyp RASopatií
- Etiologie a diagnostika poruchy růstu u dětí, které se narodily malé na svůj gestační věk (SGA) s přetrvávající malou výškou v dětství (SGA-SS)
- Růstové databáze a registry – cesta k poznání fyziologických účinků růstového hormonu
- Porucha růstu u 11leté dívky s diabetem
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Syndrom Noonanové a další RASopatie: Etiologie, diagnostika a terapie
- Etiologie a diagnostika poruchy růstu u dětí, které se narodily malé na svůj gestační věk (SGA) s přetrvávající malou výškou v dětství (SGA-SS)
- Syndrom Noonanové z pohledu dětského kardiologa
- Prenatální fenotyp RASopatií
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

