-
Medical journals
- Career
Manažment pacientov s rizikom náhlej kardiálnej smrti
Authors: V. Illíková 1; M. Bjeloševič 1; P. Olejník 1; R. Hatala 2; M. Chalúpka 1
Authors‘ workplace: Detské kardiocentrum NÚSCH a. s a Lekárska fakulta Univerzity Komenského, Bratislava 1; NÚSCH a. s. a Lekárska fakulta Slovenskej zdravotníckej univerzity, Bratislava 2
Published in: Čes-slov Pediat 2018; 73 (5): 296-303.
Category:
Overview
Náhla kardiálna smrť u dieťaťa a mladého dospelého je zriedkavou, ale veľmi tragickou udalosťou s hlbokým dopadom na rodinu, zdravotnícku komunitu aj laickú verejnosť. Cieľom článku je poskytnúť odbornej pediatrickej obci v prehľadnej forme súčasné poznatky o manažmente detských pacientov s rizikom arytmicky podmienenej NKS.
Práca analyzuje možnosti primárnej aj sekundárnej prevencie NKS všeobecne aj pri konkrétnych etiologických jednotkách, ako sú štrukturálne ochorenia srdca alebo primárne arytmické syndrómy.
Klúčové slova:
náhla kardiálna smrť, arytmie, deti a mladí dospelí, kardiopulmonálna resuscitácia, prevencia, manažment
ÚVOD
Náhla kardiálna smrť (NKS) je podľa definície WHO neočakávaná nevysvetliteľná prirodzená (nenásilná) smrť z kardiálnej príčiny, ku ktorej dochádza do 1 hodiny od začiatku akútnych symptómov. Rozhodujúcim kritériom nie je prítomnosť alebo absencia preexistu-júceho ochorenia srdca, ale neočakávaná doba a spôsob smrti [1]. Z praktického klinického pohľadu za najlep-šiu považujeme nasledovnú pragmatickú definíciu [2, 3]:
Náhla kardiálna smrť je definovaná ako istá v prípade, ak
- ide o neočakávané nenásilné úmrtie bez zrejmej extrakardiálnej príčiny, ku ktorému dochádza v prítomnosti svedkov do 1 hodiny po rýchlom kolapse,
alebo ako pravdepodobná, ak
- ide o neočakávané nenásilné úmrtie v priebehu 24 hodín od momentu, keď bola obeť posledný krát videná v dobrom stave nažive.
Odvrátená NKS je termín používaný v situácii, pri ktorej dôjde k obnoveniu normálnej srdcovej činnosti po jej prechodnom zastavení, a tým k reverzii procesov, ktoré by inak spôsobili smrť. Z tohto pohľadu môžeme používať aj termíny náhle zastavenie srdca (ekvivalent anglického „cardiac arrest“) a NKS. Zastavenie srdca je definované ako náhle zastavenie elektrickej a mechanickej aktivity srdca, vedúce ku takmer okamžitej strate vedomia a kolapsu [4].
NKS u dieťaťa a mladého dospelého (0–20 r. veku) je zriedkavou, ale veľmi tragickou udalosťou s hlbokým dopadom na rodinu, zdravotnícku komunitu aj laickú verejnosť.
Cieľom článku je poskytnúť odbornej pediatrickej obci v prehľadnej forme súčasné poznatky o manažmente detských pacientov s rizikom arytmicky podmienenej NKS (nearytmické príčiny NKS presahujú obsahový rámec práce).
INCIDENCIA NKS
Väčšina krajín nedisponuje centrálnymi registrami obetí NKS. Incidencia NKS v pediatrickej populácii sa odhaduje z rôznych zdrojov a pohybuje sa podľa týchto odhadov v pásme 0,8–2,8 alebo 1,3–8,5/100 000 pac. rokov, či napr. v USA 0,6–6,2/100 000 detí [5–9]. V jednotlivých podskupinách na základe etiológie je incidencia NKS rôzna. Napr. u detí s hypertrofickou kardiomyopatiou (HKMP) je výskyt 1 : 500 [10] či u syndrómu dlhého QT intervalu (LQTS) 1 : 2000 [11]. Významný posun poznania o výskyte NKS u detí a mladých dospelých s vrodenými srdcovými chybami (VCHS) priniesli čerstvo publikované údaje z dánskeho registra [12], kde je výskyt NKS u osôb s VCHS vo veku 0–35 rokov 0,4/100 000 osobo-rokov, čo je 10-násobne viac ako u zdravej populácie rovnakého veku. Náhle zomierajúce osoby v tejto vekovej kategórii mali v 59 % pred úmrtím diagnostikovanú VCHS. Prekvapujúce je zistenie, že NKS pri fyzickej aktivite je u osôb s VCHS zriedkavá. U dospe-lých sa incidencia NKS odhaduje v počte cca 135//100 000 [8].
Na Slovensku v súčasnosti neexistuje register NKS, takže reálny výskyt NKS u detí ani u dospelých nepoznáme.
ETIOLÓGIA NKS
Ochorenia s rizikom NKS v detskom a adolescentnom veku sa vo väčšine prác delia na 3 skupiny (tab. 1) [8, 13, 14]:
- Štrukturálne ochorenia: kardiomyopatie (KMP)//myokarditídy, koronárne anomálie, vrodené chyby srdca, Marfanov syndróm s ruptúrou aorty.
- Primárne arytmické príčiny: vrodené primárne arytmické syndrómy, tzv. kanálopatie, a poruchy prevodu impulzu pri Wolf-Parkinson-White (WPW) syndróme a kompletnej átrioventrikulárnej blokáde.
- Iné: pľúcna hypertenzia, užívanie návykových látok či niektorých liekov, komócia srdca a i.
Table 1. Ochorenia s rizikom NKS u detí a mladých dospelých (0–35 r.). 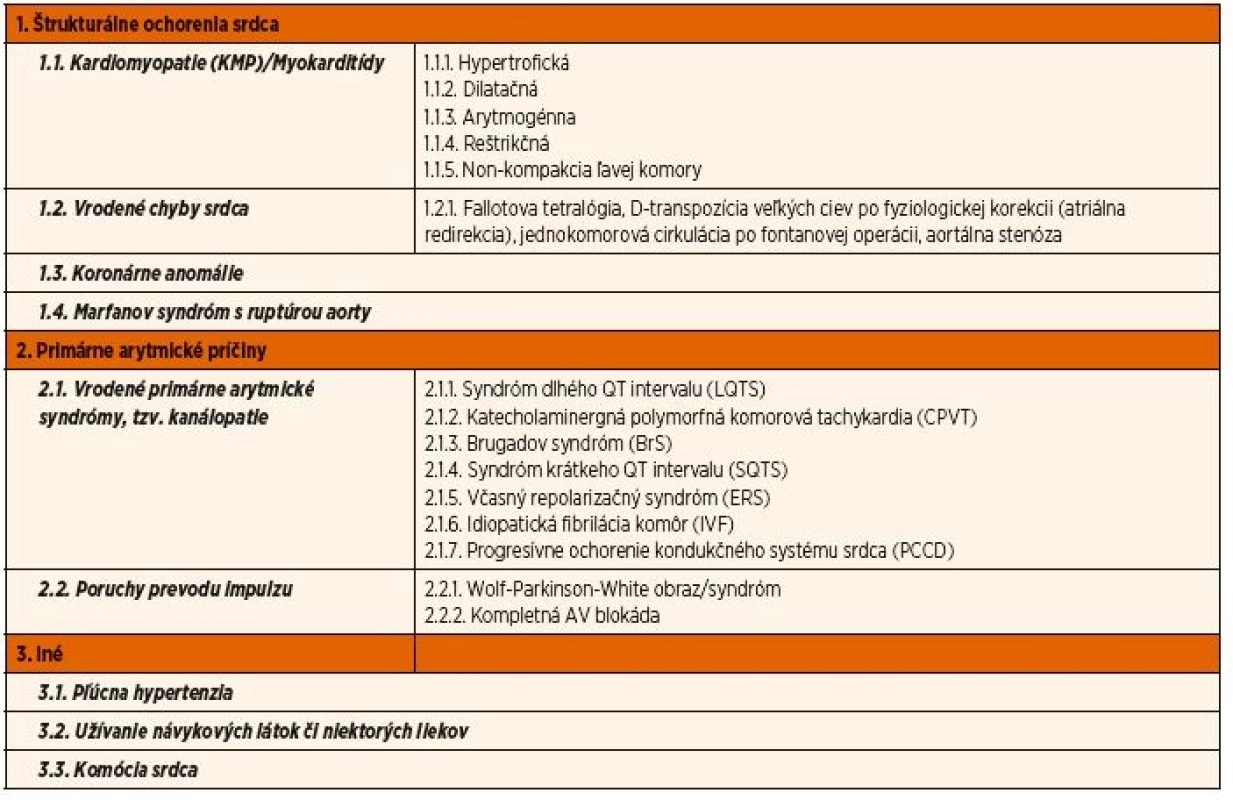
MANAŽMENT DETÍ S RIZIKOM NKS
Pravdepodobnosť prežitia malígnej komorovej tachy-arytmie je vo všeobecnosti veľmi nízka a pohybuje sa v našich podmienkach na úrovni 5 %. Cieľom terapeutického zásahu musí byť teda predovšetkým prevencia takejto pravdepodobne fatálnej príhody – v tomto prípade hovoríme o primárnej prevencii NKS. Problémom je skutočnosť, že každá farmakologická i nefarmakologická preventívna intervencia je spojená aj s rizikom nežiadúcich účinkov a komplikácií. Aby bola primárna prevencia zmysluplná, musí byť jej riziko mnohokrát nižšie ako riziko NKS. K tomu je potrebné poznať individuálne riziko malígnej komorovej tachyarytmie, ktorého odhad je však osobitne v pediatrickej populácii veľmi zložitý. Vzhľadom k chýbaniu exaktných epidemiologických údajov o riziku NKS pre rôzne syndrómy, považujeme za pragmatické extrapolovať a aproximovať poznatky z epidemiológie NKS u pacientov s HKMP aj na iné etiológie. V tomto zmysle môžeme 5-ročné riziko arytmickej NKS >5 % považovať za vysoké, čo oprávňuje použiť aj agresívnejšie preventívne opatrenia.
Cieľom primárnej prevencie je v prvom rade identifikácia detí s rizikom NKS a ich následná liečba zameraná na prevenciu vzniku resuscitačnej príhody. Významná časť obetí NKS má varovné symptómy predchádzajúce zastaveniu srdca, ale často sú dezinterpretované alebo podceňované obeťou aj rodinnými príslušníkmi. Závraty, bolesť na hrudníku, palpitácie, synkopa, dušnosť alebo rodinná anamnéza predčasného náhleho neočakávaného úmrtia sú prítomné v 8–33 % prípadov [9, 16] a treba im venovať náležitú pozornosť s ďalšími potrebnými vyšetreniami. Varovnými rizikovými symptómami sú najmä synkopa a bolesť na hrudníku pri záťaži. Časť detí s NKS má známe ochorenie srdca už pred resuscitačnou príhodou [13]. Prítomnosť symptómov pomáha identifikovať populáciu s vyšším rizikom NKS.
Riziková stratifikácia NKS je limitovaná na ochorenia s častým výskytom a dostatočnými dlhodobými skúsenosťami, ako aj s klinickými štúdiami porovnávajúcimi viaceré preventívne stratégie. To sa podarilo dosiahnuť viac-menej len u hypertrofickej KMP a u niektorých kanálopatií ako LQTS [13]. V roku 2012 bola riziková stratifikácia NKS publikovaná aj u asymptomatických detí s EKG obrazom komorovej preexcitácie [17]. Celkovo sa dá povedať, že riziková stratifikácia NKS u detí je podstatne menej preskúmaná ako v dospelej kardiológii a treba ju používať opatrne s individualizovaným ohodnotením a posúdením rizika.
Asymptomatických jedincov s rizikom NKS je možné identifikovať prostredníctvom skríningových programov zameraných na určité skupiny s vyšším rizikom NKS (napr. športovcov). Keďže mnohé ochorenia s rizikom NKS majú kongenitálny/genetický podklad, treba ich študovať v kontexte rodiny, kde má významné miesto genetický skríning rodinných príslušníkov obete NKS [13, 18, 19]. Skríning, jeho rozsah, cieľové skupiny a iná problematika týkajúca sa skríningu sú predmetom rozsiahlej stále prebiehajúcej diskusie a presahujú cieľ tejto práce
KLINICKÉ PRÍZNAKY A DIFERENCIÁLNA DIAGNOSTIKA
Okamžitou príčinou zastavenia srdca pri NKS je obvykle malígna komorová tachyarytmia (fibrilácia komôr alebo bezpulzová komorová tachykardia). Keď je krátka a spontánne terminuje, vedie ku presynkope alebo synkope s následným návratom vedomia po terminácii tachykardie, ale prejavom mozgovej hypoperfúzie počas straty vedomia môžu byť svalové tonicko-klonické kŕče. Táto symptomatológia vedie nezriedka primárne chybne k neurologickému diagnostickému záveru epilepsie s následnou dlhodobou liečbou antiepileptikami. V prípade, že stavy s poruchou vedomia pretrvávajú aj pri tejto liečbe, treba vždy v prvom rade spochybniť diagnózu epilepsie a až po vylúčení kardiálnej príčiny ďalej eskalovať antiepileptickú liečbu.
Treba však myslieť i na to, že epileptický záchvat môže byť samotný príčinou náhlej smrti, pravdepodobne v dôsledku masívnej sympatikovej aktivácie. Bolesť na hrudníku ako symptóm je výnimočná u arytmických príčin NKS, ale môže sprevádzať KMP, koronárne anomálie, alebo ochorenia aorty (ruptúra aorty pri Marfanovom syndróme). Iné netypické príznaky tiež môžu odviesť pozornosť od kardiálnej príčiny, napríklad záťažou indukovaný bronchospazmus pri KMP (následok zníženej compliance/poddajnosti ľavej komory, pľúcnej venóznej hypertenzie s pľúcnym edémom, mitrálnej regurgitácie). Malígna komorová arytmia spustená náhlym ponorením do vody pri syndróme dlhého QT intervalu alebo katecholaminergnej polymorfnej komorovej tachykardii môže imponovať ako prosté topenie alebo utopenie. Kongenitálna hluchota môže byť súčasťou LQTS. Febrilné kŕče môžu byť aj prejavom Brugadovho syndrómu, pretože aktivita kanálopatie sa zvýrazňuje so stúpajúcou telesnou teplotou [14].
Primárna prevencia NKS závisí od konkrétnej diagnózy, etiológie a špecifickej liečby pre konkrétne ochorenie. Možnosti liečby všeobecne zahŕňajú:
- farmakologickú liečbu,
- intervenčnú liečbu,
- modifikáciu životného štýlu.
Základom farmakologickej liečby sú vzhľadom k vysokej bezpečnosti betablokátory a v špecifických indikáciách aj iné antiarytmiká (flekainid, mexiletín, amiodaron a i.).
Z nefarmakologických terapeutických možností pripadajú do úvahy:
- implantácia kardiostimulátora pri závažných bradyarytmiách (najmä pokročilé AV blokády);
- implantácia kardiovertera-defibrilátora (ICD) pri vysokom riziku potenciálne fatálnych tachyarytmií;
- katétrová ablácia komorovej tachykardie (KT) vo vybraných indikáciách (KT z výtokového traktu komôr, hemodynamicky tolerovaná monomorfná KT na podklade lokalizovaného arytmogénneho substrátu – napr. jazva po operácii defektu komorového septa, idiopatické KT u chorých bez štrukturálneho ochorenia srdca a v poslednom čase aj epikardiálna ablácia pri Brugadovom syndróme);
- ľavostranná kardiálna sympatiková denervácia pri zriedkavých primárnych arytmických syndrómoch za určitých okolností.
Optimálne indikácie k primárne preventívnej implantácii ICD sú menej známe ako u dospelých, hlavné indikácie sú však extrapolované z indikácií pre dospelých [20, 21]. V porovnaní s dospelou populáciou je totiž pomer riziko/benefit podstatne horšie kvantifikovateľný. Implantácia ICD u detí je spojená s viacerými dodatočnými technickými problémami: deti rastú a majú odlišnú fyziologickú srdcovú frekvenciu a pri VCHS majú odlišné anatomické pomery. Vzhľadom na očakávaný počet rokov, či skôr desaťročí života po implantácii ICD v detskom veku ich očakáva množstvo výmen impulzogenerátora, čo je spojené s rizikom infekčných komplikácií. Deti majú vyšší výskyt neadekvátnych výbojov, potrebujú časté modifikácie programovania ICD, majú vyššie kumulatívne riziko malfunkcie elektród a vaskulárnych komplikácií. Na druhej strane z pohľadu potenciálneho benefitu ICD je riziko NKS pri VCHS a kardiomyopatiách v detskom veku nižšie ako v dospelosti [13, 22].
Všetky tieto faktory v reálnej praxi znamenajú, že rozhodnutie o implantácii ICD v primárnej prevencii NKS patrí v detskej kardiológii k tým najťažším. Nie je preto prekvapujúce, že odporúčania pre implantáciu ICD v pediatrickej populácii sa vždy významne oneskorujú v porovnaní s odporúčaniami pre dospelých [23].
Dôležitú súčasť prevencie NKS predstavuje modifikácia životného štýlu, ako je limitácia športovej aktivity, minimalizácia spúšťačov arytmických príhod, eliminácia niektorých potenciálne proarytmogénnych liekov – to všetko špecificky pre jednotlivé ochorenia. U primárnych vrodených arytmických syndrómov, tzv. kanálopatií, má úprava životosprávy najvyššiu triedu I odporúčaní v dokumente Európskej kardiologickej spoločnosti na manažment komorových arytmií a prevenciu NKS z r. 2015 [15, 24].
Významnú časť primárnej prevencie tvorí edukácia a príprava rodiny na urgentné situácie a kardiopulmonálnu resuscitáciu.
SEKUNDÁRNA PREVENCIA NKS
Keď zlyhá primárna prevencia a u dieťaťa príde k náhlemu zastaveniu srdca, nastáva fáza sekundárnej prevencie. V prvom rade ide o rýchlu a účinnú kardiopulmonálnu resuscitáciu – pri komorovej tachyarytmii najmä rýchlu elektrickú defibriláciu. Tu zohrávajú úlohu mnohé faktory. Americká kardiologická asociácia (AHA) navrhla tzv. „reťaz života“ („chain of survival“) [25]. Ide o kaskádu činností kľúčových pre prežitie pa-cienta: začína včasným rozpoznaním príznakov svedkami príhody, pokračuje okamžitým zavolaním špecializovanej záchrannej zdravotníckej služby (v krajinách EU na telefonickom čísle 112), kardiopulmonálnou resuscitáciou (KPR) najskôr laickou a potom profesionálnou so skorou defibriláciou, transportom do nemocnice a definitívnou liečbou v zdravotníckom zariadení.
Rytmus prítomný u dieťaťa pri mimonemocničnom zastavení srdca môže byť v zásade trojaký: asystólia, bezpulzová elektrická aktivita a komorová fibrilácia. V epidemiologických štúdiách mimonemocničných resuscitácií je u detí častejšia asystólia ako komorové arytmie, ale v týchto štúdiách boli aj deti s komorbiditami, topiace alebo dusiace sa. U detí s kardiálnou etiológiou náhlej smrti je primárnou arytmiou často fibrilácia komôr [13].
Prežívanie detí po KPR mimo nemocnice je veľmi nízke, obvykle menej ako 5 %, pričom mnohé prežívajúce deti majú ťažké poškodenie mozgu. Ide o ireverzibilné dôsledky dlhej periódy bez srdcového výdaja. Nezriedka totiž k zastaveniu srdca dochádza bez svedkov, takže „reťaz prežívania“ nemá kto včas aktivovať. Údaje z registrov ukazujú, že iba cca 30 % obetí je resuscitovaných svedkom udalosti, pričom práve laická KPR svedkom udalosti viac ako dvojnásobne zvyšuje pravdepodobnosť prežívania.
Prvých 15 minút po zastavení srdca rozhoduje o prežití: v priebehu 5 minút asystólie a apnoe odumierajú mozgové bunky. Zastavenie srdca má tri fázy, odlíšiteľné srdcovým rytmom a metabolickými následkami nízkeho prietoku a hypoxie. Tieto fázy definujú adekvátnu liečbu a predikujú pravdepodobnosť prežitia a ireverezibilného neurologického poškodenia:
- Prvá elektrická fáza trvá asi 4 minúty a je reprezentovaná tzv. šokovateľným rytmom, kedy srdce reaguje na defibriláciu. Pri okamžitom začatí KPR a defibrilácii do 3–5 minút má postihnutý pravdepodobnosť prežitia 50–75 %, každá minúta oneskorenia znižuje pravdepodobnosť prepustenia z nemocnice (teda vlastne prežitia) o 10–15 %.
- V nasledujúcej cirkulačnej fáze nastáva tkanivová hypoxémia a asystólia. V tejto fáze je nevyhnutná KPR s dodávkou kyslíka, defibrilácia je už menej účinná, ale môže byť podporená podaním adrenalínu a pokračujúcou resuscitáciou.
- Metabolická fáza nastáva asi po 10 minútach od zastavenia srdca, pretrváva asystólia, zhoršuje sa hypoxia a cirkulujúce metabolické faktory vedú ku bunkovej smrti a multiorgánovému zlyhaniu. Prežitie tejto fázy je nepravdepodobné a ak nastane, je spojené s ťažkým trvalým postihnutím.
KPR má 4 komponenty rovnaké u detí aj dospelých:
- kompresie hrudníka s frekvenciou cca 100/minútu (externá masáž srdca),
- defibrilácia,
- ventilácia,
- farmakologická liečba.
Všetky tieto časti sú dôležité, ale efektívna masáž srdca a skorá defibrilácia sú najjasnejšie spojené so zlepšeným prežívaním [13].
Práve preto môže mať v reťazi prežívania významnú úlohu dostupnosť automatických externých defibrilátorov (AED). Použitie AED sa odporúča aj u detí mladších ako 8 rokov veku, neexistuje však jasné stanovisko pre ich použitie u detí mladších ako 1 rok. O použití AED v domácnosti nemáme dostatok informácií [14].
Odporúčania Európskej kardiologickej spoločnosti na manažment komorových arytmií a prevenciu NKS z r. 2015 [15] kladú dôraz na umiestnenie verejne dostupných defibrilátorov na miestach, kde je vysoká koncentrácia ľudí (napríklad dopravné uzly, školy, športové štadióny a i.), alebo na miestach, kde nie je možný iný prístup k defibrilácii (napríklad v dopravných prostriedkoch – vlaky, lode, lietadlá). Okrem toho sa odporúča, aby napríklad aj zamestnanci športovísk boli zaškolení v správnej KPR a vedeli adekvátne používať AED [15, 24].
Dôležitou súčasťou sekundárnej prevencie NKS je genetické vyšetrenie u mladých ľudí po NKS, vytvorenie štandardov pre pitvu obetí NKS a vytvorenie národných registrov NKS [13].
V nemocničnej a ponemocničnej fáze po odvrátenej NKS je potrebné cielené kardiologické a genetické vyšetrenie (po získaní výsledkov aj genetické vyšetrenie rodinných príslušníkov podľa odporučenia genetika) na identifikáciu konkrétneho ochorenia vedúceho ku vzniku NKS. Po odvrátenej NKS v dôsledku malígnej komorovej tachyarytmie, kde sa nenašla žiadna reverzibilná príčina život-ohrozujúcej príhody, je v sekundárnej prevencii NKS indikovaná implantácia ICD v triede I odporúčaní, zahŕňajúc pacientov so štrukturálne normálnym srdcom, VCHS, KMP aj kanálopatiami [7].
ŠTRUKTURÁLNE OCHORENIA SRDCA S RIZIKOM ARYTMICKEJ NKS
Kardiomyopatie (KMP)
KMP sú ochorenia charakterizované štrukturálnymi a funkčnými abnormalitami komorového myokardu, často autozomálne dominantne dedičné, takmer všetky asociované s komorovými arytmiami a zvýšeným rizikom NKS. Do skupiny KMP sú zahrnuté hypertrofická – HKMP, dilatačná – DKMP, reštrikčná – RKMP, arytmogénna – AKMP (pôvodne arytmogénna dysplázia pravej komory) a non-kompakcia ľavej komory – NKĽK (z anglického výrazu „non-compation left ventricle“ – NCLV).
V primárnej prevencii NKS sú u detí najpresnejšie vytvorené odporúčania pre HKMP. Rizikové faktory pre NKS zahŕňajú: hrúbka septa ≥30 mm alebo ≥6 štandardných odchýlok priemernej hrúbky septa v danej vekovej kategórii (Z-skóre ≥6), rodinná anamnéza NKS v mladom veku, nepretrvávajúca komorová tachykardia, synkopa a hypotenzná reakcia na záťaž [21, 23, 26].
Dospelí aj detskí pacienti ≥8 r. veku s ≥2 rizikovými faktormi majú vysoké riziko NKS a v týchto prípadoch treba zvážiť implantáciu ICD v primárnej prevencii NKS [15, 26]. U detí mladších ako 8 rokov veku nie je dostatok údajov týkajúcich sa stratifikácie rizika NKS na indikáciu implantácie ICD.
Čo sa týka farmakologickej profylaxie NKS pri HKMP, nie sú žiadne randomizované štúdie podporujúce jej účinnosť. Výskyt NKS podľa niektorých štúdií znižoval amiodaron. Betablokátory a disopyramide sa síce používajú na liečbu obštrukcie výtoku ľavej komory, ale nemali signifikantný efekt na výskyt NKS [15]. Betablokátory a amiodaron sa môžu použiť u malých detí v prechodnom období, kým sa implantuje ICD [22]. Chirurgickú septektómiu alebo alkoholovú abláciu ako prevenciu NKS súčasné odporúčania Európskej kardiologickej spoločnosti (ESC) neodporúčajú [15]. Ku primárnej prevencii NKS pri HKMP patrí aj manažment akcesórnych dráh (asociácia WPW syndrómu a HKMP pri PRKAG2 mutácii), fibrilácie predsiení a ischémie myokardu (posledné dve prevažne až v dospelosti) [22].
Z ďalších opatrení je u pacientov s rizikovými faktormi pre NKS a/alebo s obštrukciou výtoku ľavej komory odporú-čaná eliminácia kompetitívneho športu a intenzívnej športovej aktivity v triede I odporúčaní ESC [15].
Pre AKMP je v primárnej prevencii NKS podľa ESC odporúčaní na prvých miestach taktiež reštrikcia športovej aktivity (trieda I) a vo farmakologickej profylaxii liečba betablokátormi (trieda I). Pri neúčinnosti betablokátorov je odporúčané zváženie amiodaronu. Katétrová ablácia môže byť úspešná najmä u chorých s menším rozsahom dysplastických oblastí myokardu, nezriedka si však vyžaduje epikardiálny prístup [15].
Pre ostatné typy KMP (dilatačná, reštrikčná a non-kompakcia) sú odporúčania ešte menej presné. V pediatrickej populácii neexistujú veľké randomizované štúdie ako u dospelých, kde bol dokázaný klinický benefit ICD v primárnej prevencii NKS pri DKMP a z týchto štúdií vychádzajú ESC odporúčania [15] pre dospelú populáciu: ICD je odporúčaný pri hemodynamicky netolerovanej komorovej tachykardii a pri funkčnej triede II–III s ejekčnou frakciou ľavej komory <35 % napriek viac ako 3 mesiace trvajúcej optimálnej farmakologickej liečbe (trieda I). Implantácia ICD sa môže zvážiť pri LMNA mutácii (lamin A/C) s klinickými rizikovými známkami. Vo farmakologickej profylaxii sú odporúčané betablokátory a identifikácia a eliminácia proarytmogénnych faktorov (hypokalémia, proarytmogénne lieky, ochorenie štítnej žľazy). V určitých indikáciách je odporúčaná resynchronizačná liečba.
V sekundárnej prevencii po odvrátenej NKS a po život-ohrozujúcej pretrvávajúcej komorovej tachykardii je pri všetkých typoch KMP u detí aj dospelých indikovaná implantácia ICD v triede I ESC odporúčaní [15].
VRODENÉ CHYBY SRDCA (VCHS)
Výskyt NKS u detí s VCHS je v absolútnach hodnotách nízky, ale podstatne vyšší ako v bežnej populácii. Podľa dánskej štúdie z r. 2018 je u 0–35-ročných ľudí s VCHS až 9,6-krát vyšší ako v bežnej populácii rovnakého veku, s výskytom 0,4/100 000 pac. rokov [12].
NKS sa najčastejšie vyskytuje u cyanotických a ľavostranných obštrukčných VCHS. Kombinácia dysfunkcie myokardu, jaziev po kardiochirurgickej operácii, hypertrofie a fibrózy zvyšujú riziko NKS hlavne u detí s komplexnými VCHS, ako je Fallotova tetralógia, D-transpozícia veľkých ciev po fyziologickej korekcii (Senningova alebo Mustardova operácia), alebo jednokomorovej cirkulácie po Fontanovej operácii. Riziko NKS rastie s vekom a časom od operácie. NKS tvorí 15–20 % úmrtí v tejto skupine pacientov [13]. Príčinou NKS môže byť okrem arytmie aj embólia, alebo cirkulačný kolaps. Rizikové faktory NKS u VCHS sú podobné ako pri ischemickej chorobe srdca: supraventrikulárne tachykardie, dysfunkcia myokardu systémovej alebo pľúcnej komory a predĺžený interval QRS. Najviac štúdií sa venovalo rizikovým faktorom NKS pri Fallotovej tetralógii. Mechanizmom NKS pri VCHS sú vo všeobecnosti buď rýchle atriálne tachykardie s 1 : 1 AV prevodom s dete-rioráciou do fibrilácie komôr, alebo primárne komorové arytmie [15].
Efektívnou liečbou na zníženie rizika NKS môže byť pri supraventrikulárnej aj ventrikulárnej tachykardii katétrová ablácia. Takisto adekvátna chirurgická liečba niektorých VCHS znižuje riziko NKS (aortálna stenóza). Keďže dysfunkcia myokardu je rizikovým faktorom NKS, chirurgická korekcia reziduálnych defektov a optimalizácia farmakologickej liečby srdcového zlyhávania tiež znižuje riziko NKS. Implantácia ICD je u detí odporúčaná v sekundárnej prevencii po odvrátenej NKS po vylúčení iných reverzibilných príčin a po prekonaní symptomatickej pretrvávajúcej komorovej tachykardie [15]. Antiarytmická liečba liekmi s nízkym proarytmogénnym rizikom je indikovaná pri recidívach tachykardií po ablácii alebo ako prídavná liečba k ICD [22].
PRIMÁRNE ARYTMICKÉ OCHORENIA S RIZIKOM NKS
Primárne genetické arytmické syndrómy, tzv. kanálopatie
Kanálopatie sú autozomálne dedičné ochorenia podmienené mutáciami génov kódujúcich proteíny tvoriace alebo reagujúce s iónovými kanálmi v membránach myokardiálnych buniek. Následné zmeny funkcie iónových kanálov predstavujú arytmogénny substrát predisponu-júci pacienta so štrukturálne zdravým srdcom k náhlej kardiálnej smrti na podklade komorovej tachykardie alebo fibrilácie [27].
Medzi najčastejšie sa vyskytujúce kanálopatie v detskom veku patrí syndróm dlhého QT intervalu (LQTS) a katecholaminergná polymorfná komorová tachykardia (CPVT), menej Brugadov syndróm (BrS) a syndróm krátkeho QT intervalu (SQTS). NKS je niekedy prvým prejavom ochorenia, ale častejšie sú prvým prejavom menej malígne symptómy (synkopy) a pacient má často abnormálne EKG.
Dôležitú súčasť manažmentu kanálopatií hrajú modifikácie životného štýlu, ktoré majú najvyššiu, t.j. triedu I odporúčaní Európskej kardiolgickej spoločnosti z r. 2015 [15]. Pri syndróme dlhého QT intervalu to znamená vyhýbanie sa liekom potenciálne predlžujúcim QT interval a vyhýbanie sa genotypovo špecifickým spúšťačom malígnych arytmií (napríklad namáhavé plávanie pri LQT1, expozícia hlasným zvukom pri LQT2 [28]). Pri Brugadovom syndróme ide najmä o vyhýbanie sa liekom potenciálne indukujúcim elevácie ST segmentu v pravých prekordiálnych zvodoch, nadmernému príjmu alkoholu a veľkých porcií jedál a promptnú liečbu akejkoľvek horúčky antipyretikami. U pacientov s CPVT je odporúčaný zákaz kompetitívneho a vrcholového športu. Vo farmakologickom manažmente kanálopatií sú základom liečby betablokátory. U pacientov s LQT3 nie sú betablokátory dostatočne účinné a môže sa zvážiť ich kombinácia s blokátormi sodíkového kanála (mexiletín, flekainid alebo ranolazín) s cieľom skrátenia intervalu QT.
Do podobnej kategórie odporúčaní patrí zváženie sotalolu alebo chinidínu u pacientov s SQTS. Takisto sa môže zvážiť pridanie flekainidu do liečby u pacientov s CPVT, ktorí majú rekurentné synkopy alebo polymorfné//bidirekčné KT pri liečbe betablokátorom. Pri BrS je pri elektrickej búrke odporúčané zváženie liečby chinidínom a izoprenalínom.
Z nefarmakologických terapeutických možností pri primárnych arytmických syndrómoch pripadá do úvahy implantácia ICD, odporúčaná vždy v sekundárnej prevencii po odvrátenej NKS spolu s liečbou betablokátormi, pri dokumentovanej spontánnej pretrvávajúcej komorovej tachykardii u SQTS a BrS a pri opakovaných synkopách napriek liečbe adekvátnymi dávkami betablokátorov pri LQTS. Implantácia ICD sa môže zvážiť aj pri spontánnom diagnostickom EKG type I BrS a pozitívnej anamnéze synkôp. Inou nefarmakologickou možnosťou je ľavostranná kardiálna sympatiková denervácia u symptomatických pacientov s LQTS, u ktorých sú betablokátory neefektívne, netolerované alebo sú kontraindikované, liečba pomocou ICD je kontraindikovaná alebo ju pacient odmietne, alebo u pacientov s implantovaným ICD, ktorí majú opakované výboje napriek liečbe betablokátormi. Podobná úvaha je potrebná u pacientov s CPVT, ak nedosiahneme dostatočný efekt pridaním flekainidu ku liečbe betablokátormi [15, 24].
WPW OBRAZ A SYNDRÓM
Termín WPW obraz označuje prítomnosť známok komorovej preexcitácie na EKG u asymptomatických detí, termín WPW syndróm označuje prítomnosť symptomatickej tachykardie u detí so známkami komorovej preexcitácie na EKG. Mechanizmom NKS u pacientov s komorovou preexcitáciou je veľmi rýchle vedenie fibrilácie alebo flutteru predsiení na komoru cez akcesórnu dráhu, čo vyprovokuje komorovú fibriláciu [28, 29]. Hoci väčšina pacientov resuscitovaných z NKS mala predchádzajúce symptómy, hlavne u detí môže byť komorová fibrilácia prvým prejavom WPW syndrómu. U malých detí je riziko NKS pri komorovej preexcitácii takmer nulové, po dosiahnutí veku 8‒10 rokov veku jej výskyt stúpa u detí s asymptomatickým WPW obrazom na odhadovaných 0,1 % na pacientský rok sledovania [29].
Medzi anamnestické faktory svedčiace pre vyššie riziko život ohrozujúcej arytmie patrí mužské pohlavie, anamnéza flutteru/fibrilácie predsiení, synkopa, rýchle antegrádne vodivé vlastnosti akcesórnej dráhy, viacpočetné akcesórne dráhy, Ebsteinova anomália trikuspidálnej chlopne a i. Čo sa týka posudzovania rizika NKS u asymptomatických pacientov s WPW obrazom, v r. 2012 boli publikované odporúčania pre manažment 8‒21-ročných asymptomatických detí s ekg obrazom komorovej preexcitácie [17]. Pri pretrvávaní preexcitácie pri maximálnej dosiahnutej frekvencii počas ergometrie je odporúčané invazívne elektrofyziologické vyšetrenie so zmeraním kondukčných vlastností akcesórnej dráhy a event. katétrovou abláciou. Intermitentná preexcitácia odzrkadľuje nízku rizikovosť akcesórnej dráhy z hľadiska NKS, novšie štúdie ale ukazujú možnosť zvýšenia rizikovosti akcesórnej dráhy vplyvom prudkého vyplavenia adrenalínu s následným vzostupom rizika NKS aj pri bazálne nízkorizikovej akcesórnej dráhe. V niektorých prácach sa odporúča invazívne elektrofyziologické vyšetrenie ako preventívna stratégia pri posudzovaní rizika NKS, keďže neinvazívna stratifikácia rizika nie je dostatočne presná [30].
Za prediktory malígnej arytmie sa považuje indukovateľná AV reentry tachykardia alebo elektrofyziologické vlastnosti akcesórnej dráhy svedčiace o schopnosti rýchleho antegrádneho prevodu (najkratší preexcitovaný RR interval pri fibrilácii predsiení alebo efektívna refraktérna perióda akcesórnej dráhy <250 ms) [29‒32]. Ovšem v nedávno publikovanej práci [31] sa referovalo o výsledkoch elektrofyziologických vyšetrení u detí po život-ohrozujúcej príhode (rýchla preexcitovaná fibrilácia predsiení, odvrátená NKS a NKS) na podklade komorovej preexcitácie, pričom u viac ako 50 % detí neboli prítomné rizikové charakteristiky akcesórnej dráhy pri vyšetrení. Toto pozorovanie spolu so zdokonalením ablačných techník (vrátane eliminácie radiačnej záťaže) podporuje stanovisko, že neinvazívna riziková stratifikácia nie je dostatočne spoľahlivá a každý detský pacient (vo veku 8 a viac rokov) s komorovou preexcitáciou by mal podstúpiť invazívne vyšetrenie a väčšina aj kauzálnu liečbu katétrovou abláciou s elimináciou rizika NKS [32].
ZÁVER
Manažment detí a mladých dospelých s rizikom NKS spočíva v primárnej a sekundárnej prevencii NKS. Zmysluplná primárna prevencia sa musí opierať o spoľahlivú identifikáciu a rizikovú stratifikáciu ohrozenej populácie, na základe ktorej je potrebné idnividuálne zvoliť optimálnu formu prevencie resp. ich kombináciu: modifikácia životného štýlu s cieľom eliminácie spúšťačov arytmických príhod, farmakologická prevencia a intervenčná prevencia. Obzvlášť v oblasti rizikovej stratifikácie a intervenčnej profylaxie sú odporúčania u detí podstatne menej presné ako u dospelých, pretože zväčša postrádame randomizované klinické štúdie a postupy pre deti musíme extrapolovať zo štúdií na dospelej populácii.
V práci sme sa pokúsili poskytnúť prehľadný manažment detí s rizikom NKS v súčasnosti. V ostatnom čase sa do popredia stále viac dostáva katétrová ablácia, ktorá má potenciál kauzálne alebo paliatívne eliminovať arytmogénny substrát. Technické zdokonaľovanie intervenčnej liečby ju robí stále viac využiteľnou aj u zraniteľnej detskej populácie, za predpokladu jej realizácie v skúsených špecializovaných centrách.
MUDr. Viera Illíková, PhD.
vedúca lekárka Odd. arytmií a kardiostimulácie
Detské kardiocentrum NÚSCH a.s.
a Lekárska fakulta Univerzity Komenského
Limbová 1
833 51 Bratislava
Slovenská republika
e-mail: illikvie@gmail.com
Sources
1. Kumar V, Abbas AK, Aster JC. Robbins and Cotran Pathologic Basis of Disease. 9th ed. Philadelphia PA: Elsevier Saunders, 2015 : 1–551. ISBN: 9780808924500.
2. Myerburg RJ, Castellanos A. Cardiac arrest and sudden cardiac death. In: Zipes DP, Libby P, Bonow RO. Braunwald’s Heart Disease. A Textbook of Cardiovascular Medicine. 8th ed. Elsevier Saunders, 2007 : 933–974.
3. Fishman GI, Chugh SS, Dimarco JP, et al. Sudden cardiac death prediction and prevention: report from a National Heart, Lung, and Blood Institute and Heart Rhythm Society Workshop. Circulation 2010 Nov 30; 122 (22): 2335–2348. doi: 10.1161/circulationaha.110.976092.
4. Graham R, Eisenberg M, Atkins D, et al. Strategies to improve cardiac arrest survival: a time to act. Institute of Medicine, Committee on the treatment of cardiac arrest: Current status and future directions, Board on health sciences policy. Washington (DC):National Academies Press, 2015 Sept. ISBN-13 : 978-0-309-37199-5.
5. Berger S, Campbell R. Sudden cardiac death in children and adolescence: introduction and overview. PACE 2009 July; 32: S2–S5. doi:10.1111/j.1540-8159.2009.02378.
6. Wren C. Sudden death in children and adolescents. Heart 2002; 88 : 426–431.
7. Brugada J, Blom N, Sarquella-Brugada G, et al. Pharmacological and non-pharmacological therapy for arrhythmias in the pediatric population: EHRA and AEPC-Arrhythmia Working Group joint consensus statement. Europace 2013 Sep; 15 (9): 1337–1338. doi: 10.1093/europace/eut082.
8. Gajewski KK, Saul PJ. Sudden cardiac death in children and adolescents (excluding Sudden Infant Death Syndrome). Ann Pediatr Card 2010, 3 (2):107–112. doi:10.4103/0974-2069.74035.
9. Liberthson RR. Sudden death from cardiac causes in children and young adults. N Engl J Med 1996; 334 : 1039–1044. doi:10.1056/nejm199604183341607.
10. Maron BJ, Gardin JM, Flack JM, et al. Prevalence of hypertrophic cardiomyopathy in a general population of young adults. Echocardiographic analysis of 4111 subjects in the cardia study. Coronary artery risk development in (young) adults. Circulation 1995; 92 : 785–789.
11. Schwartz PJ, Stramba-Badiale M, Crotti L, et al. Prevalence of the congenital long QT syndrome. Circulation 2009; 120 : 761–767.
12. Lynge THE, Jeppesen AG, Winkel BG, et al. Nationwide study of sudden cardiac death in people with congenital heart defects aged 0 to 35 years. Circ. Arrhythm Electrophysiol 2018; 11: e005757. doi: 10.1161/ circep. 117. 005757.
13. Ackerman MJ, Atkins DL, Triedman JK. Sudden cardiac death in the young. Cirulation 2016 March 8; 133 (10) :1006–1026. doi:10.1161/circulationaha. 115.020254.
14. Campbell R, Berger S, Ackerman MJ. Pediatric sudden cardiac arrest. Pediatrics 2012;129;e1094; Section on cardiology and cardiac surgery. doi: 10.1542/peds.2012-0144.
15. Priori SG, Blomstrom-Lundqvist C, Mazantti A. 2015 ESC Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death: The Task Force for the Management of Patients with Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death of the European Society of Cardiology (ESC). Endorsed by: Association for European Paediatric and Congenital Cardiology (AEPC). Eur Heart J 2015 Nov 1; 36 (41): 2793–2867. doi:10.1093/eurheartj/ehv316.
16. Wisten A, Messner T. Symptoms preceding sudden cardiac death in the young are common but often misinterpreted. Scand Cardiovasc J 2005; 39 (3):143–149.
17. Cohen M. PACES/HRS Expert Consensus Statement on the Management of the Asymptomatic Young Patient with a Wolff-Parkinson-White (WPW, Ventricular Preexcitation) Electrocardiographic Pattern. Heart Rhythm 2012; 9 (6): 1006–1024. doi:10.1016/j.hrthm.2012.03.050.
18. Kubuš P, Janoušek J. Sudden cardiac death in the young – epidemiology and prevention. Cor Vasa 2012; 54: e223–e226.
19. Tester DJ, Ackerman MJ. Postmortem long QT syndrome genetic testing for sudden unexplained death in the young. J Am Coll Cardiol 2007; 49 (2): 240–246.
20. Zipes DP, Camm AJ, Borggrefe M, et al. ACC/AHA/ESC 2006 guidelines for management of patients with ventricular arrhythmias and the prevention of sudden cardiac death: a report of the American College of Cardiology/American Heart Association Task Force and the European Society of Cardiology Committee for Practice Guidelines (Writing Committee to Develop guidelines for management of patients with ventricular arrhythmias and the prevention of sudden cardiac death) developed in collaboration with the European Heart Rhythm Association and the Heart Rhythm Society. Europace 2006; 8 : 746–837.
21. Epstein AE, Dimarco JP, Ellenbogen KA, et al. ACC/AHA/HRS 2008 Guidelines for Device-Based Therapy of Cardiac Rhythm Abnormalities: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the ACC/AHA/NASPE 2002 Guideline Update for Implantation of Cardiac Pacemakers and Antiarrhythmia Devices) developed in collaboration with the American Association for Thoracic Surgery and Society of Thoracic Surgeons. J Am Coll Cardiol 2008; 51: e1–62.
22. Epstein AE, DiMarco JP, Ellenbogen KA, et al. 2012 accf/aha/hrs focused update incorporated into the accf/aha/hrs 2008 guidelines for device-based therapy of cardiac rhythm abnormalities: A report of the american college of cardiology foundation/american heart association task force on practice guidelines and the heart rhythm society. Circulation 2013; 127: e283–352. PubMed:2325546.
23. Hatala R, Hlivák P. Comment on 2015 ESC Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death. Cardiology Lett 2016; 25 (3): 157–162.
24. Cummins RO, Ornato JP, Thies WH, Pepe PE. Improving survival from sudden cardiac arrest: the „chain of survival“ concept. A statement for health professionals from the Advanced Cardiac Life Support Subcommittee and the Emergency Cardiac Care Committee, American Heart Association. Circulation 1991; 83 (5): 1832–1847.
25. Elliott PM, Anastasakis A, Borger MA, et al. 2014 ESC Guidelines on diagnosis and management of hypertrophic cardiomyopathy. The Task Force for the Diagnosis and Management of Hypertrophic Cardiomyopathy of the European Society of Cardiology (ESC). Eur Heart J 2014; (35): 2733–2779. doi:10.1093/eurheartj/ehu284.
26. Marban E. Cardiac channelopathies. Nature 2002, Jan 10; 415 (6868): 213–218.
27. Schwartz PJ, Priori SG, Spazzolini C, et al. Genotype-phenotype correlation in the long-QT syndrome: Gene-specific triggers for lifethreatening arrhythmias. Circulation 2001; 103 : 89–95.
28. Obeyesekere M. Risk of sudden death in Wolff-Parkinson-White syndrome: How high is the risk? Circulation 2012; 125 (5): 659–660.
29. Gebauer R, Janoušek J. Supraventrikulárne tachykardie. In: Janoušek J, a kol. EKG a dysrytmie v dětském věku. 3. vyd. Praha: Grada Publishing, a.s., 2014 : 117–148. ISBN 978-80-247-5006-4.
30. Etheridge SP, Escudero CA, Blaufox AD, et al. Life threatening event risk in patients with Wolf-Parkinson-White syndrome. A multicenter international study. J Am Coll Cardiol EP 2018; 4 : 433–444. doi:10.1016/j.jacep.2017.10.009.
31. Kubuš P, Vít P, Gebauer RA, et al. Electrophysiologic profile and results of invasive risk stratification in asymptomatic children and adolescents with Wolf-Parkinson-White electrocardiographic pattern. Circ Arrhythm Electrophysiol 2014; 7 : 218–223. doi: 10.1161/circep.113.000930.
32. Pappone C, Santinelli V. Asymptomatic Wolff-Parkinson-White syndrome should be ablated. Electrophysiol Clin 2012; 4 : 281–2855. doi:10.1016/ j.ccep. 2012.06.006.
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2018 Issue 5-
All articles in this issue
- Prenatální detekce srdečních vad a její důsledky
- Screening rizika náhlé srdeční smrti v dětském věku – mýtus nebo realita?
- Manažment pacientov s rizikom náhlej kardiálnej smrti
- Výskyt vrozených srdečních vad – dopad prenatální diagnostiky
- Nespokojenost žen s vlastním tělem v třetím trimestru těhotenství
- Mentální anorexie s raným začátkem, diagnostika a terapie
- Turnerův syndrom a anomálie aortálního oblouku čtyřikrát jinak
- Lokálne reakcie po uhryznutí hadom – klinické skúsenosti
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Mentální anorexie s raným začátkem, diagnostika a terapie
- Výskyt vrozených srdečních vad – dopad prenatální diagnostiky
- Prenatální detekce srdečních vad a její důsledky
- Lokálne reakcie po uhryznutí hadom – klinické skúsenosti
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

