-
Medical journals
- Career
Současné možnosti prenatální diagnostiky kongenitální diafragmatické hernie
Authors: Z. Straňák 1,4; I. Kučerová 1; I. Urbánková 1,4; B. Goldová 2; Vítková I.. 2; M. Rygl 3; K. Pýcha 3; L. Krofta 1
Authors‘ workplace: Ústav pro péči o matku a dítě, ředitel doc. MUDr. J. Feyereisl, CSc. 1; Ústav patologie VFN a 1. LF UK, přednosta prof. MUDr. C. Povýšil, DrSc. 2; Klinika dětské chirurgie FN Motol a 2. LF UK, přednosta prof. MUDr. J. Šnajdauf, DrSc. 3; Katedra gynekologie a porodnictví 3. LF UK, přednosta doc. MUDr. B. Svoboda, CSc. 4
Published in: Ceska Gynekol 2009; 74(3): 183-187
Overview
Cíl studie:
Cílem článku je poskytnout přehled o současných možnostech prenatální diagnostiky u plodů s vrozenou brániční kýlou (congenital diaphragmatic hernia, CDH).Typ práce:
Souhrnný přehled.Název a sídlo pracoviště:
Ústav pro péči o matku a dítě, 3. LF UK Praha.Metodika:
Literární přehled recentních prací.Výsledky:
Základní diagnostickou metodou (CDH) je 2D ultrasonografie: měření lung to head ratio (LHR), měření očekávané a naměřené hodnoty LHR (observed to expected LHR – O/E LHR), lokalizace defektu, stanovení polohy jater a přítomnost sdružených vývojových vad (negativní prognostické faktory). Prenatální diagnostika může být doplněna 3D ultrazvukovým vyšetřením a magnetickou rezonancí (zobrazovací metody pro validní měření objemu plicního parenchymu plodu a/nebo potvrzení přítomnosti sdružených vývojových vad). Reaktivitu plicního řečiště hodnotíme hyperoxygenačním testem matky a měřením dopplerovských parametrů v arteria pulmonalis. Invazivní prenatální diagnostika není indikována u izolované levostranné CDH. Koncentrace případů do specializovaného centra je elementární podmínkou úspěšné diagnostiky a terapie CDH.Klíčová slova:
kongenitální diafragmatická hernie, hypoplazie plic, prenatální diagnostika.ÚVOD
Kongenitalní diafragmatická hernie (congenital diaphragmatic hernia – CDH) je závažná vrozená vývojová vada. Incidence CDH v ČR se udává 2,31 na 10 000 živě narozených dětí [19]. Vada se častěji vyskytuje u chlapců (v poměru 2 : 1). Rozlišujeme několik morfologických forem CDH: posterolaterální, retrosternální, paraezofageální a diafragmatickou eventeraci. Levostranný defekt bránice se vyskytuje u 80 % případů, pravostranný u 10 – 20 % a u 1 – 2 % případů je defekt bilaterální. U většiny pacientů s CDH přechází peritoneum ve viscerální pleuru a herniované orgány nejsou kryty kýlním vakem – jde o nepravou kýlu. Z hlediska morfologie a lateralizace je nejčastějším typem nepravá posterolaterální levostranná kongenitální diafragmatická hernie (seu Bochdaleki) [15, 18].
Prognosticky důležitým parametrem je, který z orgánů dutiny břišní proniká do dutiny hrudní. Nejčastěji dochází k herniaci střev, žaludku a jater, méně často pankreatu, sleziny a ledvin. Prognosticky nepříznivým faktorem je herniace jater [6].
Sdružené vývojové vady jsou přítomny u 30 – 40 % případů CDH. Strukturální a numerické chromozomální aberace jsou vzácné (trizomie 18, trizomie 13, Frynsův syndrom, syndrom Ehrlesův-Danlosův) [18, 20]. Nejčastěji jsou sdruženy vývojové poruchy centrálního nervového systému, uropoetického ústrojí a srdeční vady. Přítomnost a závažnost srdeční vady bývá limitující pro přežití novorozence. Vzácně se může CDH vyskytovat familiárně [15].
Přežívání novorozenců s CDH se v posledních letech mírně zlepšilo (50 – 70 % v případě izolovaného výskytu). Vysoká mortalita zůstává u pacientů se sdruženými vývojovými vadami (přežívá přibližně 15 % pacientů) [4]. Z publikovaných studií vyplývá, že lepších výsledků se dosahuje v centrech s vyšším počtem pacientů (v centrech s více než 12 případy za 22 měsíců je přežívání o 13 % vyšší) [11].
Limitujícími faktory mortality a závažné dlouhodobé morbidity u pacientů s CDH jsou: hypoplazie plic, perzistující plicní hypertenze a přítomnost sdružených vývojových vad (viz obr. 1 a 2).
Image 1. Makroskopický průkaz těžké hypoplazie plic u levostranné CDH: celková hmotnost plic 26,1 gramů (norma 60,1±16,6 gramů), poměr hmotnost plic/hmotnost pacienta 0,007 (dolní hranice normy: 0,012). Publikováno se souhlasem Ústavu patologie VFN a 1. LF UK 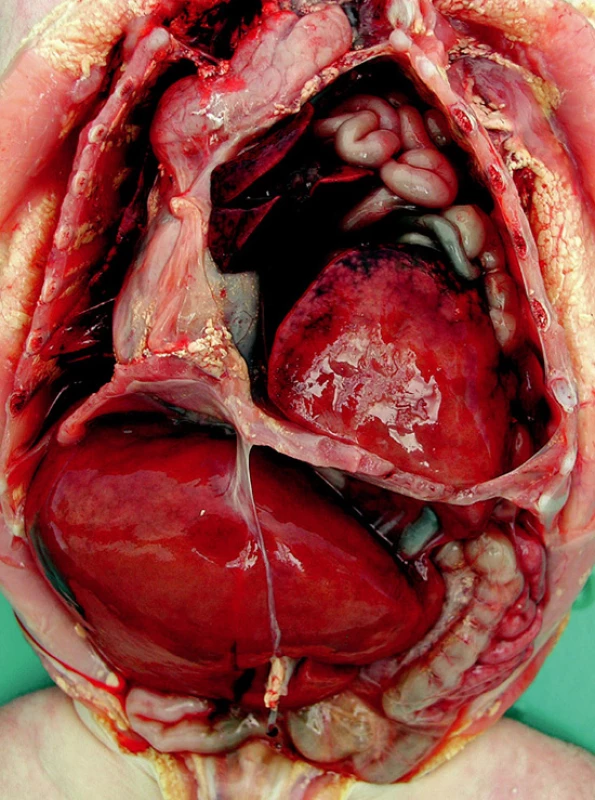
Image 2. Histologický průkaz závažné hypoplazie plic: redukce počtu bronchů a bronchiolů, snížený radial count (terminální bronchioly se nacházejí těsně pod pleurou a nejsou odděleny řadou 4-5 alveolů), zmnožení mezenchymálních tkání (chrupavka, vazivo) kolem bronchiolů, intersticiální zmnoženi vaziva (barvení na vazivo - modrý trichrom, publikováno se souhlasem Ústavu patologie VFN a 1. LF UK) 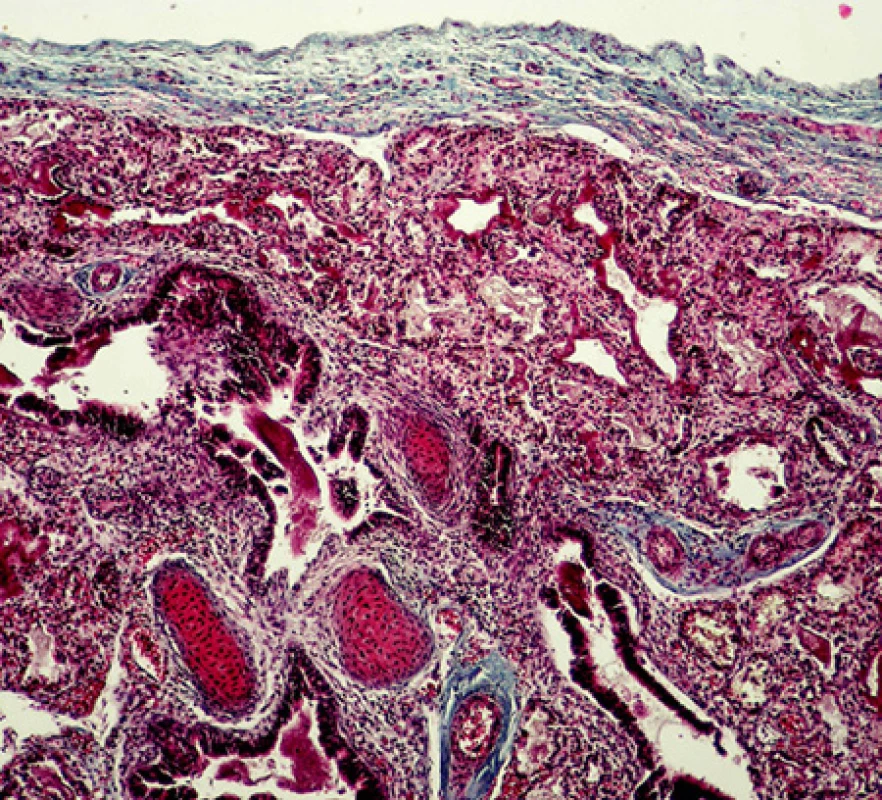
Cílem prenatální diagnostiky je validní zhodnocení závažnosti hypoplazie plic, detekce asociovaných vrozených vývojových vad, eventuálně zhodnocení reaktivity plicní cirkulace u plodu.
MOŽNOSTI PRENATÁLNÍ DIAGNOSTIKY KONGENITÁLNÍ DIAFRAGMATICKÉ HERNIE
Ultrazvuková diagnostika
Při ultrasonografickém 2D vyšetření se bránice zobrazuje jako tenká anechogenní linie oddělující orgány dutiny hrudní a břišní. Bránici lze spolehlivě zobrazit ve dvou projekcích (v rovině sagitální a frontální).
Ultrazvukovou diagnostiku diafragmatické hernie (CDH) je možné provádět v transverzální rovině hrudníku při zobrazení čtyřdutinové srdeční projekce. První ultrazvukovou známkou je přesun srdce ze střední čáry. Levostranná brániční kýla, která je nejčastější, se při ultrazvukovém vyšetření typicky projeví posunem srdce a mediastina doprava. Hrot srdeční směřuje vlevo (dextropozice srdce). Pokud je současně i hrot srdeční otočen vpravo, je nutné pomýšlet na přítomnost srdeční vady. V dutině hrudní se nejčastěji nachází žaludek a střevní kličky. Žaludek se zobrazuje jako anechogenní struktura, protože je vyplněn tekutinou. Střeva se odlišují jednak svojí vyšší echogenitou a zejména přítomností peristaltiky. Součástí herniovaných orgánů mohou být i játra (nejčastěji levý lalok), jejich odlišení od plicního parenchymu je často obtížné, protože oba orgány mají velmi podobnou echogenitu. Vzhledem k této skutečnosti je diagnostika pravostranné brániční kýly složitější. Pravý jaterní lalok může způsobit přesun mediastina doleva, častěji dochází ke kompresi pravých srdečních oddílů. Přesnější lokalizaci jater usnadní barevné dopplerovské zobrazení deviované umbilikální žíly nebo hepatálních žil a zobrazení žlučníku.
Nepřímou ultrazvukovou známkou CDH je přítomnost polyhydramnia, které se ale obvykle rozvíjí až na začátku třetího trimestru těhotenství.
Diferenciálně diagnosticky je nutné vyloučit další patologické cystické útvary v hrudníku (např. bronchogenní cysty, mediastinální teratom, cysty thymu a další), bronchopulmonální atrézii nebo plicní sekvestraci. Ve všech těchto případech není změněna pozice nitrobřišních orgánů [4].
Přidružené malformace jsou přítomny ve 30 – 40 % případů CDH. Nejčastěji se vyskytují vrozené vady centrálního nervového systému, uropoetického ústrojí a srdeční vady. V případě nálezu těchto a/nebo jiných sdružených vad je nutné indikovat metody invazivní prenatální diagnostiky (amniocentéza, kordocentéza).
Strukturální i numerické chromozomální aberace jsou vzácné (výskyt aneuploidií do 2 %), a proto v případě izolovaného nálezu CDH není nutné karyotypizaci plodu provádět [20].
Ultrasonografické prediktivní faktory mortality a morbidity novorozenců s CDH
Limitujícím faktorem pro přežívání novorozenců s izolovanou CDH je stupeň plicní hypoplazie a případný rozvoj perzistující plicní hypertenze novorozenců (persistent pulmonary hypertension, PPHN). Hodnocení závažnosti hypoplazie plic prenatálně je nejpřesnější v období mezi 18. – 33. týdnem těhotenství. Velikost plicní tkáně se nejčastěji měří pomocí 2D ultrazvuku. Zjišťováním poměru plochy kontralaterální plíce a obvodu hlavičky získáváme hodnotu lung-to-head ratio (LHR), která je považována za vysoce validní prediktivní faktor [6, 8, 12]. K měření LHR se používá metoda popsaná Metkusem [14], podle které měříme plochu kontralaterální plíce při čtyřdutinové projekci srdce. Vynásobením dvou největších na sebe kolmých průměrů plíce získáme její plochu, tuto hodnotu následně dáme do poměru s velikostí obvodu hlavičky změřené v transtalamické rovině. Výsledkem je hodnota LHR (viz obr. 3). Pokud je tato hodnota nižší než 1,0, není prognóza ani při využití mimotělní membránové oxygenace (ECMO – extra corporeal membrane oxygenation) dobrá, při hodnotě mezi 1,0 – 1,5 je prognóza nejistá, přežívání se pohybuje od 30 do 60 % a je nejčastěji spojena s nutností použití ECMO, při hodnotách nad 1,4 je prognóza většinou dobrá (viz tab. 1) [4, 7, 12, 15].
Image 3. Měření plochy kontralaterální plíce při čtyřdutinové projekci srdce pro získání hodnoty lung-to-head ratio (LHR) podle Metkuse [16] ![Měření plochy kontralaterální plíce při čtyřdutinové projekci srdce pro získání hodnoty lung-to-head ratio (LHR) podle Metkuse [16]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/2fdd4e5e52dbaf419b689f5fe88bef33.jpeg)
Table 1. Předpokládaná mortalita novorozenců s CDH ve vztahu k LHR a O/E LHR [4] ![Předpokládaná mortalita novorozenců s CDH ve vztahu k LHR a O/E LHR [4]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/b24361f4bce5151bfbe65fe128cb66f9.png)
V období mezi 12. – 32. gestačním týdnem se u normálního plodu plocha plicní tkáně zvětší čtyřikrát více než obvod hlavičky, a proto se v průběhu gestace velikost LHR mění. Vytvoření normativů pro toto období [8] nám umožňuje porovnat očekávanou a naměřenou velikost LHR (observed to expected LHR – O/E LHR) v jednotlivých týdnech gravidity. Hodnocení plodů s izolovanou vadou mezi 18. a 38. gestačním týdnem prokázalo, že průměrná hodnota O/E LHR u plodů s CDH je 39 % (u více než 90 % případů se hodnota pohybovala pod 5. percentilem normy) [8]. O/E LHR se ukázal jako nezávislý parametr pro predikci přežívání [10]. Na základě O/E LHR byla vytvořena čtyřstupňová klasifikace závažnosti plicní hypoplazie [5].
- O/E LHR 15 %: extrémní plicní hypoplazie neslučitelná se životem.
- O/E LHR 15-25 %: těžká plicní hypoplazie, přežívání okolo 15 %.
- O/E LHR 26-45 %: středně závažná plicní hypoplazie, přežívání 30-60 %.
- O/E LHR 45 %: mírná plicní hypoplazie.
Pro každou z kategorií je třeba dále brát v úvahu pozici jater, protože novorozenci s herniací jater mají horší prognózu [6]. Výrazný vliv na přežívání novorozenců má samozřejmě i gestační stáří při porodu (viz tab. 2) [8].
Table 2. Předpokládaná mortalita novorozenců s CDH ve vztahu k O/E LHR a pozici jater [4] ![Předpokládaná mortalita novorozenců s CDH ve vztahu k O/E LHR a pozici jater [4]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/7561338e8d552b8c183400657531e597.png)
Za další nezávislý faktor v predikci vývoje onemocnění je považována strana bráničního defektu – novorozenci s pravostrannou CDH mají horší prognózu, protože levá plíce je vždy menší než pravá (v těchto případech je možné využít hodnot LHR a O/E LHR pro levou plíci) [8].
Nepřímé a méně validní parametry závažnosti CDH jsou: měření relativní velikosti srdečních komor k posouzení ventrikulární komprese, stupeň mediastinálního přesunu, celkové množství amniální tekutiny a/nebo pozice žaludku [4].
Predikce závažnosti perzistující plicní hypertenze u novorozenců
Závažným klinickým problémem u CDH je perzistující plicní hypertenze novorozenců (PPHN), jejíž příčina je ve strukturálních změnách cév. Existují různé metody prenatální detekce závažnosti PPHN. Nejčastěji používaným diagnostickým parametrem je měření průměru hlavní větve ipsilaterální plicní arterie. Pro průměr hlavní větve plicní arterie plodů byly vytvořeny normativní tabulky, které umožňují zhodnocení závažnosti PPHN [16].
Další možností pro zlepšení přesnosti predikce vývoje onemocnění je měření reaktivity plicní cirkulace při hyperoxygenaci matky. Při hyperoxygenačním testu zjišťujeme reaktivitu plicní cirkulace u plodu (pokles plicní vaskulární rezistence plodu). V případě pozitivní odpovědi můžeme očekávat identickou reakci u novorozence po porodu (tzn. nižší stupeň PPHN). Test probíhá v pozdním období těhotenství (po 30. týdnu těhotenství). Před aplikací a po aplikaci 60% koncentrace kyslíku matce měříme pomocí dopplerovského zobrazení index pulzatility (PI) v hlavní větvi plicní arterie kontralaterální plíce. Pokud je zjištěn pokles PI o 20 % a více, je výsledek testu označen jako reaktivní a je pozitivním prediktorem dobrého poporodního vývoje. V případě negativního výsledku je vyšší riziko rozvoje těžké formy PPHN a neonatálního úmrtí [1, 4].
Dopplerovské zobrazení průtokových parametrů plicních cév poskytuje další hodnoty, které mohou být využity v predikci závažnosti CDH: peak early-diastolic reversed flow (PEDRF), peak systolic velocity (PSV) a time averaged velocity (TAV). Význam a validitu uvedených parametrů je však třeba ještě ověřit dalšími studiemi [16].
Postavení 3D ultrazvuku v prenatální diagnostice CDH
U CDH je možné pomocí 3D ultrazvuku měřit velikost obou plic a celkový objem plicní tkáně. Stejně jako u 2D ultrazvuku můžeme využít normativních tabulek a porovnat naměřené a očekávané hodnoty podle příslušného gestačního věku. Nevýhodou vyšetření je, že až ve 40 % není ipsilaterální plíce optimálně měřitelná a vyšetření je nesmírně náročné vzhledem k četným pohybům plodu [7, 9].
Při měření objemu plicní tkáně se využívá rotační technika VOCAL (virtual organ computer-aided analysis). Základem pro měření je ruční označení kontury plicní tkáně ve třech na sebe kolmých rovinách (transverzální, sagitální a koronární) [7, 9, 17].
U zdravých plodů se hodnota LHR zvyšuje úměrně s narůstajícím objemem plicní tkáně. Plody s CDH mají tento proces narušený, LHR i plicní objem jsou při srovnání s hodnotami získanými u stejně starých zdravých plodů signifikantně nižší. Objem se pohybuje pod 2,5 percentilem normy pro daný gestační věk. Měření parametrů plic plodů prokázala, že délka (vzdálenost apex plíce – vrchol brániční klenby) je u CDH o 13 % větší a objem plicní tkáně je naopak o 44 % nižší než u zdravých plodů. Z toho vyplývá, že hodnota LHR mírně podhodnocuje skutečný stupeň plicní hypoplazie. Důvodem nepřesnosti LHR je skutečnost, že herniované orgány způsobují větší útlak v horizontálním směru než ve směru vertikálním [7].
K přesnějšímu posouzení stupně plicní hypoplazie se používá poměr změřeného a očekávaného objemu plicní tkáně, buď celkového (observed to expected total fetal lung volume ratio, O/E TotFLVR), nebo jen pro kontralaterální plíci (observed to expected contralateral fetal lung volume ratio, O/E ContFLVR). S rizikem neonatálního úmrtí nejlépe koreluje hodnota O/E TotFLVR [17].
O skutečném přínosu 3D ultrazvukové diagnostiky se stále diskutuje a průběžně se hodnotí. Porovnáním O/E LHR a O/E TotFLVR se zjistilo, že v predikci přežívání plodů s brániční kýlou jsou výsledky objemového měření 3D ultrazvukem horší. Zlatým standardem prenatální diagnostiky CDH zůstává 2D ultrazvuk.
Využití magnetické rezonance (magnetic resonance imaging, MRI) v diagnostice CDH
Princip MRI je odlišný od ultrazvuku, protože zobrazení je založeno na rozdílném obsahu vody v jednotlivých tkáních. Díky MRI získáme při zobrazení plic signál o vysoké intenzitě, který nám umožní morfologické i volumometrické hodnocení plicní tkáně. K měření objemu plicní tkáně se používají data z T2-vážených zobrazení, kde jsou plíce velmi dobře diferencovatelné. T1-vážená zobrazení jsou používána k přesnému zobrazení pozice jater. Zjištěné výsledky je možné porovnat s normativními tabulkami [3].
Pro posouzení stupně plicní hypoplazie se používá poměr naměřeného a očekávaného plicního objemu (observed-to-expected fetal lung ratio), poměr celkového objemu plic k celkovému tělesnému objemu a/nebo poměr celkového objemu plic k objemu jater [2]. U plodů s CDH se hodnoty observed-to-expected fetal lung ratio pohybují v průměru okolo 0,31 a pozitivně korelují s LHR [13].
Mezi nesporné výhody MRI patří bezproblémové zobrazení a změření objemu obou plic, snadnější vyhledávání asociovaných vad a možnost vizualizace plodu při obezitě matky [4, 9].
ZÁVĚR
Kongenitální diafragmatická hernie je závažná a velmi variabilní vrozená vývojová vada. Primárně je postižena bránice, ale nejzávažnějším a limitujícím faktorem mortality i morbidity je porucha vývoje plic. Plíce u novorozenců s CDH jsou hypoplastické: množství plicní tkáně je snížené, stěny alveolů jsou zúžené, snížené je i množství intersticiální tkáně a zároveň lze prokázat změny na úrovni alveolokapilární membrány. Dochází ke změnám ve stěně cév, svalová vrstva je rozšířená do perifernějších intraacinárních arteriol a medie je hyperplastická. Postiženy jsou obě plíce, ipsilaterální více. Všechny tyto změny se plně projeví až po narození různě těžkým stupněm respiračního selhávání a rozvojem perzistující plicní hypertenze.
Včasná a validní prenatální diagnostika je důležitá:
- pro posouzení prognózy plodů s CDH,
- pro eventuální zahájení prenatální terapie a/nebo pro předčasné ukončení těhotenství,
- pro odeslání matky do specializovaného centra, které koncentruje pacienty s CDH a disponuje všemi dostupnými metodami pro řešení nejtěžších forem akutního respiračního selhání u novorozenců.
V současnosti je optimální stanovení prognózy prenatálně diagnostikované CDH na základě kombinace ultrazvukových nálezů – vyloučení přidružených VVV, stanovení typu CDH, zhodnocení pozice jater, výpočet LHR, O/E LHR, zhodnocení výsledků magnetické rezonance (validní stanovení přítomnosti sdružených vývojových vad a plicní hypoplazie) a výsledků invazivní prenatální diagnostiky (vyloučení aneuploidií).
Simplexní izolované CDH mají velmi dobrou prognózu (přežívání izolované levostranné CDH bez těžké hypolazie plic je téměř 100%) na rozdíl od CDH se sdruženými vývojovými vadami a těžkou plicní hypoplazií.
Doc. MUDr. Zbyněk Straňák, CSc., MBA
Ústav pro péči o matku a dítě
Podolské nábřeží 157
147 00 Praha 4
e-mail: z.stranak@seznam.cz
Sources
1. Broth, RE., Wood, DC., Tasanem, J., et al. Prenatel prediction of lehal pulmonary hypoplasia: The hyperoxygenation test for pulmonary Artery reaktivity. Am J Obstet Gynecol, 2002, 187, p. 940-945.
2. Cannie, M., Jani, JC., De Keyzer, F., et al. Fetal Body Volume: Use at MR imaging to quantify relative lung volume in fetuses suspected of having pulmonary hypoplasia. Radiology, 2006, 241, p. 847-853.
3. Coakley, FV., Lopoo, JB., Lu, Y., et al. Normal and hypoplastic fetal lungs: volumetric assessment with prenatal single – shot rapid acquisition with relaxation enhancement MR imaging. Radiology, 2000, 216, p. 107-111.
4. Doné, E., Gucciardo, L., Van Mieghem, T., et al. Prenatal diagnosis, prediction of outcome and in utero therapy of isolated congenital diaphragmatic hernia. Prenatal Diagnosis, 2008, 28, p. 581-591.
5. Gucciardo, L., Deprest, J., Doné, E., et al. Prediction of outcome in isolated congenital diaphragmatic hernia and its consequences for fetal therapy. Best Pract Res Clin Obstet Gynaecol, 2008, 22, 1, p. 123-138.
6. Jani, J., Keller, RL., Benachi, A., et al. Prenatal prediction of survival in isolated left-sided diaphragmatic hernia. 2006, 27, 1, p. 18-22.
7. Jani, J., Peralta, CFA., Van Schoubroeck, D., et al. Relationship between lung-to-head ratio and lung volume in normal fetuses with diaphragmatic hernia. Ultrasound Obstet Gynecol, 2006, 27, p. 545-550.
8. Jani, J., Nicolaides, KH., Keller, RL., et al. Observed to expected lung area to head circumference ratio in the prediction of survival in fetuses with isolated diaphragmatic hernia. Ultrasound Obstet Gynecol, 2007, 30, 1, p. 67-71.
9. Jani, J., Cannie, M., Peralta, CFA., et al. Lung volumes in fetuses with congenital diaphragmatic hernia: comparison of 3D US and MR imaging assessments. Radiology, 2007, 244, p. 575-582.
10. Jani, J., Nicolaides, KH., Benachi, A., et al. Timing of lung size assessment in the prediction of survival in fetuses with diaphragmatic hernia. Ultrasound Obstet Gynecol, 2008, 31, 1, p. 37-40.
11. Javid, PJ., Jaksic, T., Skarsgard, ED., et al. Survival rate in congenital diaphragmatic hernia: the experience of the Canadian Neonatal Network. 2004, 39, 5, p. 657-660.
12. Laudy, JAM., Van Gucht, M., Van Dooren, MF., et al. Congenital diaphragmatic hernia: an evaluation of the prognostic value of the lung-to-head ratio and other prenatal parameters. Prenat Diagnosis, 2003, 23, p. 634-639.
13. Mahieu-Caputo, D., Sonigo, P., Dommergues, M., et al. Fetal lung volume measurement by magnetic resonance imaging in congenital diaphragmatic hernia. Brit J Obstet Gynek, 2001, 108, p. 863-868.
14. Metkus, AP., Filly, RA., Stringer, MD., et al. Sonographic predictors of survival in fetal diaphragmatic hernia. J Pediatr Surg, 1996, 31, p. 148-153.
15. Mikic, NA., Quintero, R. Diaphragmatic hernia. Diaphragmatic hernia in www.TheFetus.net.
16. Moreno-Alvarez, O., Hernandez-Andrade, E., Oros, D. et al. Association between intrapulmonary arterial Doppler parametrs and degree of lung growth as measured by lung-to-head ratio in fetuses with congenital diaphragmatic hernia. Ultrasound Obstet Gynecol, 2008, 31, p. 164-170.
17. Ruano, R., Aubry, MC., Bartle, B., et al. Three – dimesional sonographic measurement of contralateral lung volume in fetuses with isolated congenital diaphragmatic hernia. J Clin Ultrasound, 2008, 36, 5, p. 273-278.
18. Straňák, Z. Kongenitální diafragmatická hernie - nové poznatky v patofyziologii, diagnostice a léčbě. Kandidátská disertační práce, 1999.
19. Šípek, A., Gregor, V., et al. Výskyt diafragmatické hernie v ČR v období 1961-1996. Čs Gynek, 1998, 63, p. 22-26.
20. Witters, I., Legius, E., Moerman, P., et al. Associated malformations and chromosomal anomalies in 42 casese of prenataly diagnose diaphragmatic hernia. Amer J Med Genetics, 2001, 103, p. 278-282.
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicine
Article was published inCzech Gynaecology

2009 Issue 3-
All articles in this issue
- Proteomika a biomarkery karcinomu ovaria
- Paraneoplastické syndromy v onkogynekologii
- Nové diagnostické přístupy k různým typům hydatidózních mol, hydropickým abortům a příslušné klinické postupy
- Současné možnosti prenatální diagnostiky kongenitální diafragmatické hernie
- IgG protilátky namířené proti lamininu-1 v séru a v peritoneální tekutině u pacientek se sníženou plodností
- Poruchy sexuální diferenciace s chybným vývojem gonád: dosud známé zodpovědné geny a výsledný fenotype
- Běžný variabilní imunodeficit v těhotenství (soubor kazuistik)
- Izolace a imunologická identifikace spermaglutinační protilátky z lidského séra
- Praxe v používání kontracepčních metod u žen v období před porodem a po porodu
- Hyperviskozita ejakulátu v kooperácii (asociácii) s niektorými fyzikálno-morfologickými a mikrobiologickými parametrami
- Komparace prenatálního ultrazvukového vyšetření, post mortem magnetické rezonance a patologicko – anatomické pitvy (kazuistika – schizencefalie)
- Nechtěné děti
- Torze těhotné dělohy – neobvyklá porodnická komplikace
- Cystická duplikatura rekta – kazuistika
- Informovanost českých a rumunských žen o problematice pohlavně přenosných nemocí:Výsledky reprezentativních výzkumů
- Czech Gynaecology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Nechtěné děti
- Torze těhotné dělohy – neobvyklá porodnická komplikace
- Nové diagnostické přístupy k různým typům hydatidózních mol, hydropickým abortům a příslušné klinické postupy
- Paraneoplastické syndromy v onkogynekologii
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

