-
Medical journals
- Career
MOLÁROVÁ A ŘEZÁKOVÁ HYPOMINERALIZACE
Authors: M. Hepová; M. Miklasová; T. Kovalský; E. Míšová
Authors‘ workplace: Klinika zubního lékařství, Lékařská fakulta Univerzity Palackého a Fakultní nemocnice, Olomouc
Published in: Česká stomatologie / Praktické zubní lékařství, ročník 122, 2022, 2, s. 43-49
Category: Review Article
doi: https://doi.org/10.51479/cspzl.2022.004Overview
Úvod a cíl: V posledních letech přibývá v ordinacích zubních lékařů pacientů s vývojovým postižením skloviny u molárů a řezáků. Jedná se o onemocnění systémového původu postihující jeden až čtyři první stálé moláry, které je často spojené s poškozením stálých řezáků. Toto onemocnění nemá zcela objasněnou etiologii. V literatuře jsou zmíněny vlivy vnějšího prostředí, v úvahu je třeba brát i vlivy genetické. U těchto pacientů nahrazujeme ztracené tvrdé zubní tkáně molárů, ale také zlepšujeme estetiku řezáků, na kterých se mohou nacházet opacity pokrývající téměř celou vestibulární plošku. Při volbě terapie se rozhodujeme na základě stavu chrupu, spolupráce a věku pacienta. Ke každému pacientovi musíme přistupovat individuálně a zvolit pro něj vhodnou terapii. Cílem tohoto článku je shrnout dostupné informace o etiopatogenezi, klasifikaci, histologických změnách, klinickém obrazu, prevenci a terapii molárové a řezákové hypomineralizace.
Metodika: Pro tento přehledový článek byly využity odborné publikace z databází PubMed a Web of Science. Publikace byly vyhledávány v anglickém jazyce za pomoci klíčových slov: MIH, molár, řezák, molárová a řezáková hypomineralizace, DDE, hypomineralizace, opacita. Jako zdroje pro tento přehled byly využity články publikované mezi lety 2006 a 2021.
Závěr: U molárové a řezákové hypomineralizace je důležitá včasná diagnostika a zavedení preventivních postupů tak, abychom zamezili možným komplikacím souvisejícím s tímto onemocněním. Navíc prevalence tohoto onemocnění v populaci narůstá a s pacienty postiženými molárovou a řezákovou hypomineralizací se setkáváme stále častěji.
Klíčová slova:
MIH – molár – řezák – molárová a řezáková hypomineralizace – DDE – hypomineralizace – opacita
ÚVOD
Molárová a řezáková hypomineralizace (MIH) byla definována v roce 2001 jako kvalitativní porucha skloviny systémového původu, která postihuje jeden až čtyři první stálé moláry a bývá často spojená s postižením stálých řezáků [1, 2]. Moláry a řezáky jsou postiženy opacitami. Častěji se opacity vyskytují na horních řezácích (obr. 1). S opacitami se však mohou prořezat i řezáky dolní [1, 2]. Pokud jsou postiženy pouze moláry, hovoříme o molárové hypomineralizaci (MH). Dříve se MIH označovala i jinými názvy, jako idiopatická hypomineralizace skloviny, sýrové moláry (na podkladě podobnosti s vyzrálým holandským sýrem). Tyto pojmy se dnes již nepoužívají [3, 4]. Epidemiologické studie přicházejí s velkým rozptylem dat týkajících se prevalence MIH, která se pohybuje od 2,8 % do 40,2 % [3, 5]. Vyšší výskyt MIH byl zjištěn u dívek než u chlapců, tento rozdíl však není signifikantní [6]. Porovnání výsledků jednotlivých studií je obtížné, jelikož studie využívají odlišná kritéria, jiné metody vyšetření i metody záznamu výsledků a sledují odlišné věkové skupiny [7].
Image 1. Bílé opacity na zubech 12, 11, 21 a hnědá opacita na zubu 32
Fig. 1 White opacities on the teeth 12, 11, 21, and a brown opacity on the tooth 32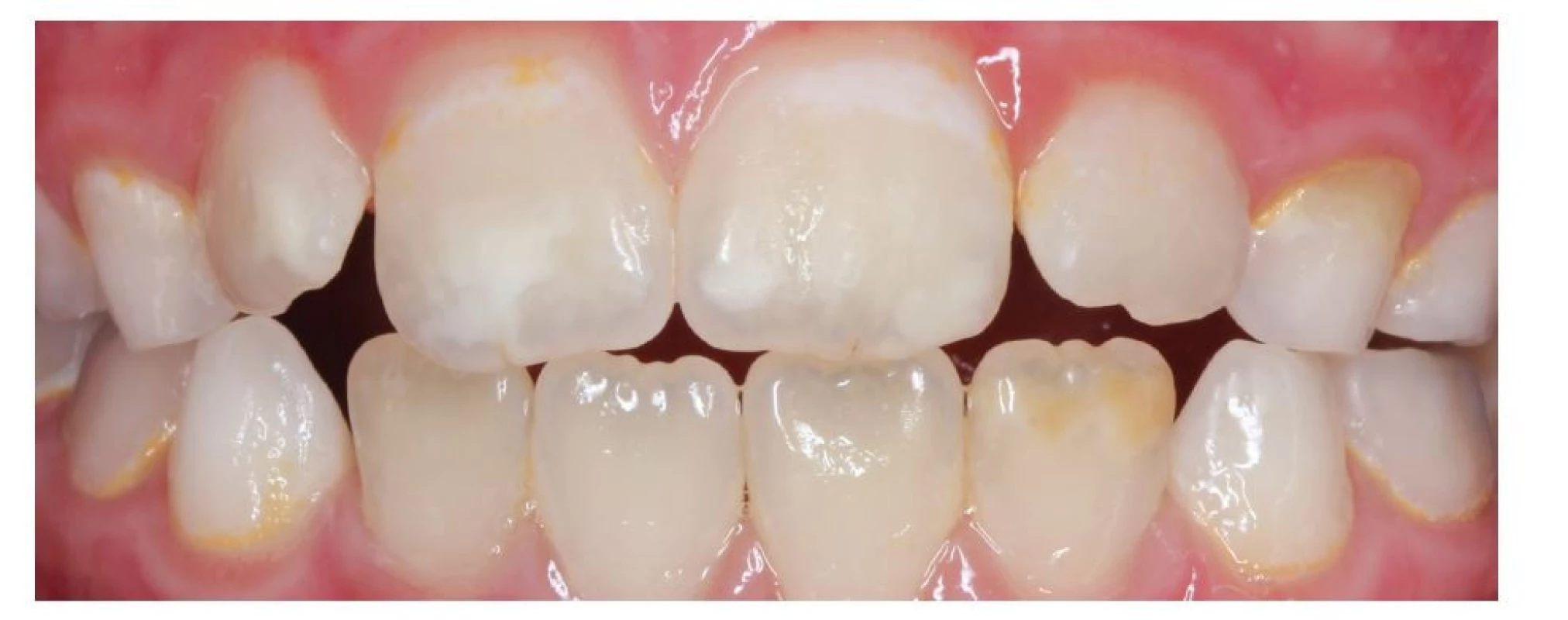
Vývojové defekty skloviny (developmental defects of enamel, DDE) jsou viditelné odchylky od normálního vzhledu skloviny, často viditelné v dočasné i stálé dentici. Tyto defekty lze rozdělit do dvou skupin: hypoplazie a hypomineralizace (opacity) [8]. Hypoplazie je kvantitativní defekt skloviny, který se na povrchu zubu projevuje jamkami a rýhami. Dokonce v některých místech může sklovina zcela chybět [9]. Opacity jsou kvalitativní poruchou tvorby skloviny [8, 10]. Rozdělujeme je na ohraničené a difuzní. Zuby mají po prořezání do dutiny ústní normální tvar a velikost [9]. Moláry jsou opacitami postiženy na bukálních, orálních a okluzních ploškách korunky (obr. 2), řezáky pak na labiálních ploškách korunky [1, 11]. Ohraničené opacity totožné s opacitami u MIH se nacházejí i v dočasném chrupu na druhých dočasných molárech (hypomineralizated second primary molar, HSPM). Prevalenci HSPM uvádí Elfrink et al. 4,9 %, podle dalších autorů se může pohybovat od 0 % do 21,8 % [12, 13]. Vedle druhého dočasného moláru se opacity vyskytují také na hrotech špičáků, na druhých stálých molárech a premolárech [7].
Image 2. Hypomineralizovaný horní molár s posteruptivní frakturou
Fig. 2 Hypominezalized upper molar with posteruptive fracture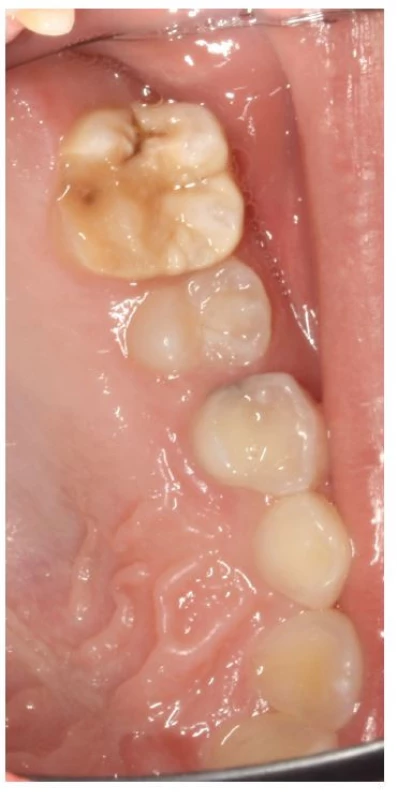
METODIKA
Pro tento přehledový článek byly využity odborné publikace z databází PubMed a Web of Science. Publikace byly vyhledávány v anglickém jazyce za pomoci klíčových slov: MIH, molár, řezák, molárová a řezáková hypomineralizace, DDE, hypomineralizace, opacita. Jako zdroje byly využity články publikované mezi lety 2006 a 2021.
ETIOPATOGENEZE ONEMOCNĚNÍ
Dříve se předpokládalo, že jsou opacity způsobeny vlivem změn lokálních, systémových nebo na základě dědičnosti, při nichž dochází k ovlivnění ameloblastů při počáteční fázi tvorby skloviny [8, 10]. Ameloblasty jsou primárně zodpovědné za tvorbu a mineralizaci skloviny. Vlivy prostředí nebo genetické změny během období amelogeneze mohou vést k hypomineralizaci [14, 15]. Podle nejnovější studie je však za vznik opacit u MH zodpovědná přítomnost albuminu. Nejedná se tedy o poruchu ameloblastů. Bylo dokázáno, že se albumin v neporušené opacitě skloviny vyskytuje v hojném množství, naopak v normální sklovině zachycen nebyl. Albumin proniká do sklovinné matrix, váže se na krystaly hydroxyapatitu a blokuje jejich růst. Dochází k inhibici mineralizace a vzniká porézní křídovitá sklovina [16]. Etiologie tohoto onemocnění není objasněna.
Vznik hypomineralizací ovlivňují vnější faktory i faktory genetické. Vnější vlivy mohou působit v období prenatálním, perinatálním i postnatálním [14]. Mineralizace skloviny začíná během pozdní fáze těhotenství a pokračuje během prvních tří let života dítěte [14]. Během těhotenství mohou mít vliv nemoci matky, stres, konzumace alkoholu nebo kouření cigaret [14]. Podle některých studií se však vliv těchto faktorů nepotvrdil [17]. Mezi perinatální faktory patří předčasný porod, nízká porodní hmotnost, porod císařským řezem, hypoxie při porodu nebo jiné komplikace při porodu [14]. K postnatálním faktorům řadíme dětská onemocnění (záněty středního ucha, plané neštovice, asthma bronchiale, respirační onemocnění během prvního roku života, infekce močových cest), užívání léků (antibiotika, antiastmatika) nebo vystavení znečišťujícím látkám v životním prostředí (dioxiny, bisfenol A) [11, 14, 17]. Některé studie naznačovaly vliv dioxinů z mateřského mléka na vznik MIH, tato hypotéza však zatím nebyla potvrzena [17]. Při léčbě některých z uvedených dětských onemocnění jsou předepisována antibiotika; podle studií je pravděpodobné, že ke vzniku MIH přispívají spíše jednotlivá onemocnění než antibiotická terapie předepsaná k léčbě onemocnění [17]. Podle nejnovějších poznatků se naopak nepotvrdila souvislost mezi sinusitidou, zarděnkami, rinitidou, malnutricí nebo mezi alergiemi a vznikem MIH [17]. Mezi onemocnění, u kterých se může MIH častěji projevit, patří také celiakie. Ve studii [18] pacientů s diagnostikovanou celiakií byly hodnoceny projevy MIH jako častější než u pacientů bez této diagnózy.
KLASIFIKACE
Jednou z možností, jak lze hodnotit míru poškození zubů, je MIH severity scoring system (MIH-SSS). Systém pracuje na základě kódů od 0 do 9, kdy 0 znamená zdravou sklovinu bez opacit a 9 znamená extrahovaný molár [5]. Mathu-Muju a Wright klasifikují MIH do tří skupin, na mírnou, střední a těžkou formu [3]. Mírná forma MIH zahrnuje ohraničené opacity na prvních stálých molárech. Nedochází ke ztrátám skloviny v místě opacit. Pacienti s touto formou MIH si nestěžují na zvýšenou citlivost. U střední formy MIH jsou přítomny ohraničené opacity na molárech i řezácích. Posteruptivní fraktury se nacházejí na jedné nebo dvou ploškách, nedochází k poškození hrbolků molárů, zuby jsou bez zvýšené citlivosti. Těžká forma MIH postihuje moláry posteruptivními frakturami skloviny, korunky jsou destruované, dochází k sekundární kazivé lézi, moláry jsou zvýšeně citlivé [3, 19].
DIFERENCIÁLNÍ DIAGNOSTIKA
Hypomineralizovaná sklovina má oproti normální sklovině histologicky odlišnou strukturu. Sklovinná prizmata jsou neorganizovaná, oddělená masivním množstvím interprizmatické matrix, která je bohatá na proteiny [10, 20]. Oproti zdravé sklovině obsahuje hypomineralizovaná sklovina jiný poměr vápníku, fosforu, kyslíku a uhlíku [21].
Při diagnostice MIH využíváme diagnostických kritérií opacit na molárech a řezácích, popřípadě špičácích a druhých dočasných molárech [12]. Mezi tato kritéria řadíme poškození molárů a řezáků, ohraničené opacity, odlomení skloviny, atypické výplně, citlivost zubů, extrahovaný jeden nebo více molárů s opacitami na zbylých molárech nebo řezácích v ústní dutině [7]. Postiženy jsou jeden až čtyři první stálé moláry, k tomu je často přidruženo poškození stálých řezáků. Tyto defekty jsou dobře ohraničené od zdravé skloviny, bílé, krémové, žluté nebo hnědé barvy [1]. Hodnotíme pouze opacity větší než jeden milimetr, nezaznamenáváme barevné změny do jednoho milimetru [11]. Sklovina je porézní a často dochází k jejímu odlamování. Na molárech i řezácích můžeme při vyšetření zaznamenat atypické výplně. Pokud mají rozsah hypomineralizací, je vhodné tyto zuby zaznamenat jako zuby postižené MIH. Extrahovaný molár můžeme považovat za diagnostické kritérium pouze při výskytu hypomineralizací na ostatních prvních stálých molárech. Při absenci opacit na ostatních prvních stálých molárech stav nehodnotíme jako MIH.
MIH je třeba odlišit od jiných vývojových anomálií skloviny, fluorózy či amelogenesis imperfecta. U pacientů s fluorózou je v anamnéze nadměrný příjem fluoridů. Klinické projevy fluorózy závisí na koncentraci a délce časového úseku, kdy byly fluoridy přijímány. U mírné formy se projevují jako bělavé linie a drobné opacity. Rozsáhlé difuzní opacity se nacházejí u střední formy. U těžké formy fluorózy může docházet k hnědému zbarvení skloviny, kromě opacit se na zubech mohou nacházet hypoplastické změny [3]. Na rozdíl od MIH je poškození zubů u fluorózy oboustranně symetrické. Amelogenesis imperfecta (AI) je geneticky podmíněná vývojová vada skloviny, která se může vyskytovat ve třech typech: hypoplastická, hypokalcifikační a hypomaturační. U hypoplastického typu je vrstva skloviny ztenčená. Zuby jsou menší a prosvítáním dentinu mají žlutavou barvu. Zuby s hypomaturační formou AI prořezávají s normální tloušťkou skloviny, ta je však měkká a dochází k jejímu odlamování [3]. U hypokalcifikační formy AI prořezávají zuby také s normální tloušťkou skloviny, je však natolik křehká, že se odlamuje záhy po erupci zubu do ústní dutiny. Dochází k odhalení dentinu a pacienti si stěžují na citlivost zubů [3, 22]. Ještě před prořezáním prvních stálých molárů můžeme předpokládat vznik MIH při přítomnosti hypomineralizací na druhých dočasných molárech. V období mineralizace korunek prvního stálého moláru a druhého dočasného moláru mohou být při působení některých faktorů během prenatálního a perinatálního období postiženy hypomineralizací i druhé dočasné moláry [23]. Tyto hypomineralizace lze posuzovat jako predilekční faktor vzniku MIH ve stálé dentici [23].
KOMPLIKACE
Sklovina je u MIH porézní, a tedy méně odolná než zdravá sklovina. Dochází k odlamování prizmat, což vede k odhalení dentinu a možnosti vzniku zubního kazu nebo k selhání výplňové terapie [20]. Působením žvýkacích sil dochází k odlamování skloviny, k posteruptivním frakturám. Ty byly pozorovány u 14 % bílých opacit a u 27,5 % žlutých opacit [12]. U molárů je často velmi složité dosáhnout účinku lokální anestezie, ošetření tedy může být pro pacienta bolestivé. Selhání účinku lokální anestezie se udává až u 50 % pacientů [20, 24]. Pacienti s MIH mají často potíže se zvýšenou citlivostí zubů na termické nebo mechanické podněty. Mechanismus vzniku hypersenzitivity není stále objasněn. Předpokládá se, že je za ni odpovědna vysoká poréznost, která umožňuje penetraci bakterií do dentinových tubulů, což vede k subklinickému zánětu zubní dřeně [25]. Děti cítí vystřelující bolest při konzumaci zmrzliny a studených nápojů nebo při nadechování studeného vzduchu [20]. Zvýšená citlivost zubů se může projevovat od mírné reakce na vnější stimuly až po spontánní hypersenzitivitu [17]. Bylo zjištěno, že za bolestivost zubů u pacientů s MIH je odpovědná zvýšená exprese tepelného receptoru TRPV1 v zubní dřeni [24]. Hypersenzitivita vede k odmítání čištění zubů v místech posterupčních fraktur a dochází k zvýšené retenci zubního plaku [14, 20] Při dlouhodobém odhalení dentinu a absenci orální hygieny může docházet ke vzniku kazivé léze [7]. Na základě porozity skloviny a obnažení dentinu mohou bakterie pronikat do dentinu, což může vést k chronickému zánětu zubní dřeně nebo častějšímu selhávání lokální anestezie [7].
PREVENCE
Důležitá je včasná diagnostika tohoto onemocnění a vysvětlení problematiky dětskému pacientovi a jeho rodičům. Nastavíme odpovídající preventivní a dietetický plán (omezení konzumace sladkých a kyselých nápojů i pokrmů) [26]. Je vhodné začít hygienickou instruktáží, pacientům doporučíme zubní pasty s 1450 ppm fluoridů, zubní pěny s obsahem kasein fosfopeptidu a amorfního kalciumfosfátu (CPP-ACP), u kterého byly prokázány remineralizační vlastnosti. Zároveň se CPP-ACP používá u pacientů se zvýšenou citlivostí molárů [17, 27]. V rámci prevence zubního kazu můžeme ošetřit fi -sury molárů pečetidlem. Pečetíme pouze moláry s mírnou formou MIH [28]. Pro pacienty trpící hypersenzitivitou se doporučují zubní pasty s 1450 ppm fluoridů a pasty obsahující desenzitizační látky. Na zuby aplikujeme fluoridový gel v ordinaci nebo jej doporučíme na domácí použití. Další možností léčby u pacientů s hypersenzitivitou je aplikace fluoridového laku [17, 29].
TERAPIE
U dětí s MIH bývá často zhoršená spolupráce. Tito pacienti vyžadují komplexní péči a jsou náchylnější ke vzniku zubního kazu [12, 30]. Při ošetřování pacienta je vhodné řídit se rozsahem poškození zubů a věkem a mírou spolupráce pacienta [24]. K ošetření molárů využíváme výplňové materiály, jako skloionomerní cementy (SIC) a kompozitní pryskyřice nebo prefabrikované či individuálně zhotovené korunkové náhrady (tab. 1). Podle klinických zkušeností a literatury je nejvhodnějším výplňovým materiálem k ošetření zubů postižených MIH kompozitní pryskyřice [24]. Často kladenou otázkou je, zda postupovat minimálně invazivně, nebo odstranit všechnu hypomineralizovanou sklovinu před aplikací kompozitního výplňového materiálu do kavity [24]. Všechny laboratorní studie zdůraznily, že za slabší pevnost vazby mezi kompozitní pryskyřicí a postiženou sklovinou je odpovědna nedostatečná schopnost kyseliny vytvořit stejný povrch jako u zdravé skloviny [17, 31]. Před aplikací fotokompozitní výplně je podle výsledků výzkumů vhodné odstranit veškerou postiženou sklovinu kolem kavity, protože adheze na porézní sklovinu je omezená a dochází ke vzniku sekundárního kazu [15, 32]. Někteří autoři doporučují použití 5% chlornanu sodného za účelem odstranění proteinů. Chlornan sodný v této koncentraci odstraňuje zbytky bílkovin z hypomineralizovaného povrchu skloviny, a tím zlepšuje vazbu [33]. K dispozici jsou studie, které ukazují zlepšení vazby při použití 5% chlornanu sodného po leptání, jiné však jeho účinek nepotvrdily [34].
Table 1. Shrnutí terapie MIH u molárů a řezáků
Tab. 1 Summary of MIH treatment of molars and incisors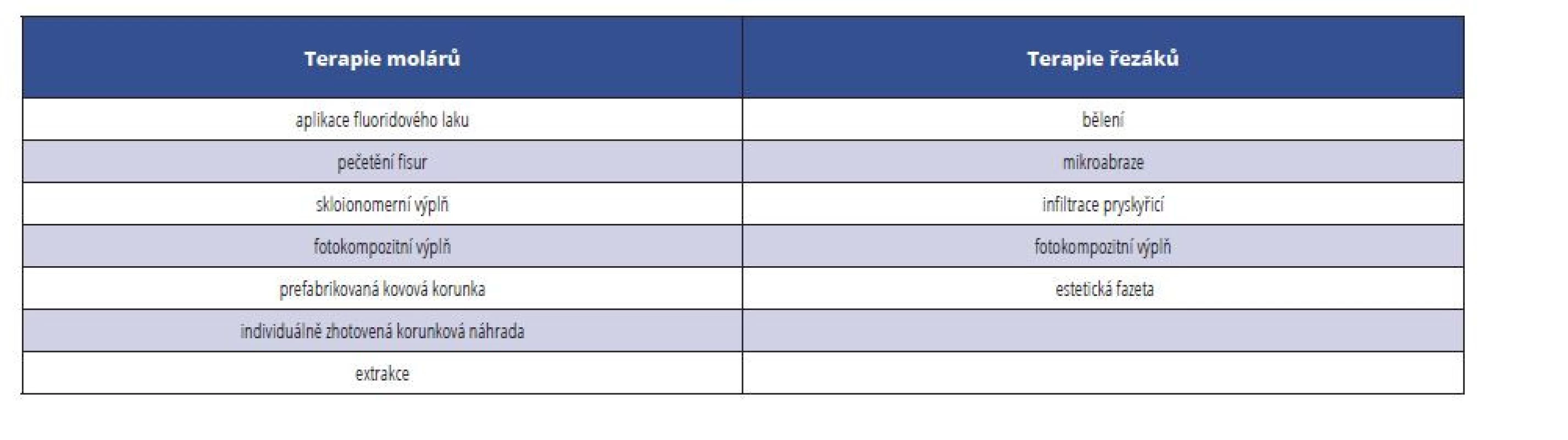
Skloionomerními cementy (SIC) nebo skloionomerními cementy modifikovanými pryskyřicí sanujeme postižené zuby zejména pacientů se zhoršenou spoluprací. Pomocí SIC můžeme sanovat i pacienty spolupracující, využíváme vlastností, jako je uvolňování fluoridů a relativně nižší nároky na suché pracovní pole při aplikaci materiálu do kavity [32]. Tyto výplně je vhodné časem revidovat; zhotovíme sendvičovou výplň nebo novou kompozitní výplň u již spolupracujících pacientů [32]. Při výrazné ztrátě tvrdých zubních tkání rekonstruujeme zuby prefabrikovanými nebo individuálně zhotovenými korunkovými náhradami. Prefabrikované kovové korunky používáme jako dočasné ošetření molárů, dokud pacient není schopný spolupráce. Tímto způsobem se ošetřují moláry se střední a těžkou formou MIH [32, 35]. Korunky zabraňují dalším ztrátám skloviny, snižují hypersenzitivitu molárů a vytvářejí správné okluzní kontakty [34]. Jiní autoři doporučují provedení 3D scanu pomocí intraorálního scaneru a následné zhotovení frézované lithium disilikátové korunkové náhrady pomocí technologie CAD-CAM. Toto ošetření však není běžné a ani vhodné v pedostomatologii [32]. Zcela nevhodným materiálem k sanaci hypomineralizovaných molárů se ukázal být amalgám, který nemá adhezi a retenci k tvarově atypickým kavitám molárů. Kromě toho je podle evropských směrnic, nařízení Evropského parlamentu a rady Evropské unie 2017/852 používání amalgámových výplní u dětí mladších než patnáct let zakázáno [36].
U molárů postižených pulpitidou nebo apikální periodontitidou lze za předpokladu spolupráce pacienta provést endodontické ošetření u zubů s dokončeným vývojem kořene. U zubů s nedokončeným vývojem kořene je možné provést endodontické ošetření koronární pulpotomií. MTA (mineral trioxide aggregate) zátkou nebo maturogenezí můžeme ošetřit řezáky s neukončeným vývojem kořene. Vždy se řídíme stadiem vývoje kořene, mírou spolupráce rodičů a pacienta i názorem ortodontisty, zda zuby se špatným biologickým faktorem zachovat, nebo upravit dlouhodobý léčebný plán a nevitální zuby extrahovat [37]. U rozsáhlého poškození tvrdých zubních tkání, špatné prognózy zubu nebo poškození zubní dřeně je možné se rozhodnout pro extrakci. Je však třeba vzít v úvahu i spolupráci a věk pacienta, ortodontické hledisko, výskyt dalších dentálních anomálií, přítomnost zárodků třetích molárů i finanční možnosti rodičů [26, 34, 38]. Pokud se rozhodneme pro extrakci molárů, je třeba extrakci naplánovat ve spolupráci s ortodontistou, plán musíme doplnit o rentgenové vyšetření. Ideální období pro extrakci moláru je dentální věk odpovídající rozmezí 8,5 až 9 let věku pacienta. Spontánní meziální erupce druhého stálého moláru (tzv. bodily posun) pravděpodobně nastane, pokud je jeho zárodek zcela v kosti [3, 26, 38]. K tomu, aby prořezal druhý stálý molár do kontaktu s druhým premolárem, je důležité extrakci načasovat tak, že druhý stálý molár má kompletně vytvořenou korunku a současně dochází k počáteční kalcifikaci bifurkace. Ke kontaktu zubů dojde zvláště tehdy, když je přítomno stěsnání zubů [26]. Pokud je stěsnání malé nebo se nevyskytuje vůbec, zůstane mezi druhým premolárem a druhým stálým molárem mezera, kterou je možné ošetřit fixním ortodontickým aparátem. Řezáky ošetřujeme miniinvazivními metodami, mezi které patří infiltrace pryskyřicí, mikroabraze a bělení, popřípadě u rozsáhlých opacit volíme fotokompozitní výplně nebo estetické fazety (tab. 1) [32]. Při infiltraci pryskyřicí (ICON, DMG Chemisch-Pharmazeutische Fabrik GmbH, Hamburk, Německo) aplikujeme na očištěný a izolovaný řezák 15% gel kyseliny chlorovodíkové (ICON ETCH) na 120 sekund, poté zub 30 sekund oplachujeme, pro kontrolu dostatečného naleptání naneseme 100% ethanol (ICON DRY), který změní matný naleptaný vzhled skloviny zpět na transparentní. Následuje infiltrace pryskyřicí (ICON INFILTRANT) nebo při neuspokojivém výsledku po aplikaci 100% ethanolu zopakujeme předchozí kroky. Pryskyřici aplikujeme na zub a necháme působit tři minuty, poté polymerujeme světlem [39]. Tuto techniku nelze využít za účelem odstranění rozsáhlých opacit řezáků a u zubů s neukončeným vývojem kořene [34, 38, 39]. Bělicí prostředky považujeme za kosmetické, proto podle nařízení Evropského parlamentu mohou být tyto prostředky s obsahem karbaminu vodíku použity jen u pacientů ve věku vyšším než 18 let. Odstranění lézí mikroabrazí je účinné pouze u mírného poškození řezáků a její použití je omezené na mělké defekty skloviny, konkrétně na hypomineralizace do hloubky 100 μm [38]. Na trhu jsou dostupné mikroabrazivní pasty s 18% kyselinou chlorovodíkovou obohacenou o abrazivní částice. [11, 34]. Potom je doporučeno zuby ošetřit remineralizační pastou s CPP-ACP [8].
ZÁVĚR
MIH lze považovat za onemocnění vyžadující komplexní stomatologickou péči zahrnující prevenci, sanace, endodontické ošetření nebo extrakce, doplněné i o ortodontickou léčbu [12]. U pacientů s MIH je nutná včasná diagnostika tohoto onemocnění pro stanovení odpovídajícího preventivního programu a terapeutického plánu. Jako nejlepší materiál k sanaci pacientů se ukazuje kompozitní pryskyřice. Při použití tohoto materiálu musíme zajistit absolutně suché pole a je nutná spolupráce dětského pacienta. Pokud je to možné, vždy se snažíme o zachování molárů v ústní dutině a k extrakci přistupujeme pouze při rozsáhlé destrukci, a to vždy po pečlivém naplánování. U řezáků se snažíme o zlepšení estetiky. Můžeme využít více druhů terapie v závislosti na věku pacienta a stadiu vývoje kořene. Podle nejnovějších studií bylo zjištěno, že za vznik MIH je zodpovědná infiltrace sklovinné matrix albuminem, který blokuje růst krystalů hydroxyapatitu. Tento objev je průlomový a v budoucnu by mohl vést ke zlepšení stavu chrupu u MIH [16].
Tento článek vznikl za podpory grantu IGA_LF_2021_007.
MDDr. Monika Hepová
Klinika zubního lékařství LF UP a FN
Palackého 12
779 00 Olomouc
e-mail: monika.hepova01@upol.cz
Sources
1. Tourino LF, Corrêa-Faria P, Ferreira RC, Bendo CB, Zarzar PM, Vale MP. Association between molar incisor hypomineralization in schoolchildren and both prenatal and postnatal factors: A populationbased study. PLoS One. 2016; 11(6).
2. Giuca MR, Lardani L, Pasini M, Beretta M, Gallusi G, Campanella V. State-of-the-art on MIH. Part. 1 Definition and aepidemiology. Eur J Paediatr Dent. 2020; 21(1): 80–82.
3. Almuallem Z, Busuttil-Naudi A. Molar incisor hypomineralisation (MIH) – an overview. Br Dent J. 2018; 225 : 601–609.
4. Koruyucu M, Özel S, Tuna EB. Prevalence and etiology of molar-incisor hypomineralization (MIH) in the city of Istanbul. J Dent Sci. 2018; 13(4): 318–328.
5. Cabral RN, Nyvad B, Soviero VLVM, Freitas E, Leal SC. Reliability and validity of a new classification of MIH based on severity. Clin Oral Investig. 2020; 24(2): 727–734.
6. Mishra A, Pandey RK. Molar incisor hypomineralization: An epidemiological study with prevalence and etiological factors in Indian pediatric population. Int J Clin Pediatr Dent. 2016; 9(2): 167–71.
7. Lygidakis NA, Wong F, Jälevik B, Vierrou AM, Alaluusua S, Espelid I. Best clinical practice guidance for clinicians dealing with children presenting with molarincisor - hypomineralisation (MIH): An EAPD policy document. Eur Arch Paediatr Dent. 2010; 11(2): 75–81
8. Xie ZH, Mahoney EK, Kilpatrick NM, Swain MV, Hoffman M. On the structure-property relationship of sound and hypomineralized enamel. Acta Biomater. 2007; 3(6): 865–872.
9. Patel A, Aghababaie S, Parekh S. Hypomineralisation or hypoplasia? Br Dent J. 2019; 227(8): 683–686.
10. Marouane O, Douki N. The use of transillumination in detecting subclinical extensions of enamel opacities. J Esthet Restor Dent. 2019; 31(6): 595–600.
11. Zhao D, Dong B, Yu D, Ren Q, Sun Y. The prevalence of molar incisor hypomineralization: evidence from 70 studies. Int J Paediatr Dent. 2018; 28(2): 170–179.
12. Reyes MRT, Fatturi AL, Menezes JVNB, Fraiz FC, Assunção LRDS, Souza JF. Demarcated opacity in primary teeth increases the prevalence of molar incisor hypomineralization. Braz Oral Res. 2019; 33: e048.
13. Elfrink ME, Schuller AA, Weerheijm KL, Veerkamp JS. Hypomineralized second primary molars: prevalence data in Dutch 5-year-olds. Caries Res. 2008; 42(4): 282–285.
14. Elzein R, Chouery E, Abdel-Sater F, Bacho R, Ayoub F. Molar-incisor hypomineralisation in Lebanon: association with prenatal, natal and postnatal factors. Eur Arch Paediatr Dent. 2021; 22(2): 283–290.
15. Krämer N, Bui Khac NN, Lücker S, Stachniss V, Frankenberger R. Bonding strategies for MIH-affected enamel and dentin. Dent Mater. 2018; 34(2): 331–340.
16. Hubbard MJ, Mangum JE, Perez VA, Williams R. A breakthrough in understanding the pathogenesis of molar hypomineralisation: the mineralisation-poisoning model. Front Physiol. 2021; 12 : 802833.
17. Lygidakis NA, Garot E, Somani C, Taylor GD, Rouas P, Wong FSL. Best clinical practice guidance for clinicians dealing with children presenting with molarincisor - hypomineralisation (MIH): an updated European Academy of Paediatric Dentistry policy document. Eur Arch Paediatr Dent. 2021. doi: 10.1007/s40368-021-00668-5
18. Kuklik HH, Cruz ITSA, Celli A, Fraiz FC, Assunção LRDS. Molar incisor hypomineralization and celiac disease. Arq Gastroenterol. 2020; 57(2): 167–171.
19. Mathu-Muju K, Wright JT. Diagnosis and treatment of molar incisor hypomineralization. Compend Contin Educ Dent. 2006; 27 : 604–610.
20. de Souza JF, Fragelli CB, Jeremias F, Paschoal MAB, Santos-Pinto L, de Cássia Loiola Cordeiro R. Eighteen-month clinical performance of composite resin restorations with two different adhesive systems for molars affected by molar incisor hypomineralization. Clin Oral Investig. 2017; 21(5): 1725–1733.
21. Alifakioti E, Arhakis A, Oikonomidis S, Kotsanos N. Structural and chemical enamel characteristics of hypomineralised second primary molars. Eur Arch Paediatr Dent. 2021; 2(3): 361–366.
22. Jälevik B, Szigyarto-Matei A, Robertson A. The prevalence of developmental defects of enamel, a prospective cohort study of adolescents in Western Sweden: a Barn I TAnadvarden (BITA, children in dental care) study. Eur Arch Paediatr Dent. 2018; 19(3): 187–195.
23. Negre-Barber A, Montiel-Company JM, Boronat-Catalá M, Catalá-Pizarro M, Almerich-Silla JM. Hypomineralized second primary molars as predictor of molar incisor hypomineralization. Sci Rep. 2016; 6 : 31929.
24. Kopperud SE, Pedersen CG, Espelid I. Treatment decisions on Molar-Incisor Hypomineralization (MIH) by Norwegian dentists – a questionnaire study. BMC Oral Health. 2016; 17(1): 3.
25. Raposo F, de Carvalho Rodrigues AC, Lia ÉN, Leal SC. Prevalence of hypersensitivity in teeth affected by Molar-Incisor Hypomineralization (MIH). Caries Res. 2019; 53(4): 424–430.
26. Lygidakis NA. Treatment modalities in children with teeth affected by molar-incisor enamel hypomineralisation (MIH): A systematic review. Eur Arch Paediatr Dent. 2010; 11(2): 65–74.
27. Toumba KJ, Twetman S, Splieth C, Parnell C, van Loveren C, Lygidakis NΑ. Guidelines on the use of fluoride for caries prevention in children: an updated EAPD policy document. Eur Arch Paediatr Dent. 2019; 20(6): 507–516.
28. Fragelli CMB, Souza JF, Bussaneli DG, Jeremias F, Santos-Pinto LD, Cordeiro RCL. Survival of sealants in molars affected by molar-incisor hypomineralization: 18-month follow-up. Braz Oral Res. 2017; 31: e30.
29. Davari A, Ataei E, Assarzadeh H. Dentin hypersensitivity: etiology, diagnosis and treatment; a literature review. J Dent (Shiraz). 2013; 14(3): 136–145.
30. Negre-Barber A, Montiel-Company JM, Catalá-Pizarro M, Almerich-Silla JM. Degree of severity of molar incisor hypomineralization and its relation to dental caries. Sci Rep. 2018; 8(1): 1248.
31. Lagarde M, Vennat E, Attal JP, Dursun E. Strategies to optimize bonding of adhesive materials to molar-incisor hypomineralizationaffected enamel: A systematic review. Int J Paediatr Dent. 2020; 30(4): 405–420.
32. Davidovich E, Dagon S, Tamari I, Etinger M, Mijiritsky E. An innovative treatment approach using digital workflow and CAD-CAM Part 2: The restoration of molar incisor hypomineralization in children. Int J Environ Res Public Health. 2020; 17(5): 1499.
33. Ekambaram M, Anthonappa RP, Govindool SR, Yiu CKY. Comparison of deproteinization agents on bonding to developmentally hypomineralized enamel. J Dent. 2017; 67 : 94–101.
34. Bandeira Lopes L, Machado V, Botelho J, Haubek D. Molar-incisor hypomineralization: an umbrella review. Acta Odontol Scand. 2021; 79(5): 359–369.
35. Wuollet E, Tseveenjav B, Furuholm J, Waltimo-Sirén J, Valen H, Mulic A, Ansteinsson V, Uhlen MM. Restorative material choices for extensive carious lesions and hypomineralisation defects in children: a questionnaire survey among Finnish dentists. Eur J Paediatr Dent. 2020; 21(1): 29–34.
36. Somani C, Taylor GD, Garot E, Rouas P, Lygidakis NA, Wong FSL. An update incisor hypomineralisation (MIH): a systematic review. Eur Arch Paediatr Dent. 2021. doi: 10.1007/s40368-021-00635-0
37. Žižka R, Šedý J, Voborná I. Retreatment of failed revascularization/ revitalization of immature permanent tooth – a case report. J Clin Exp Dent. 2018; 10(2): e185–e188.
38. Saitoh M, Shintani S. Molar incisor hypomineralization: A review and prevalence in Japan. Jpn Dent Sci Rev. 2021; 57 : 71–77.
39. Bhandari R, Thakur S, Singhal P, Chauhan D, Jayam C, Jain T. Concealment effect of resin infiltration on incisor of Grade I molar incisor hypomineralization patients: An in vivo study. J Conserv Dent. 2018; 21(4): 450–454.
Labels
Maxillofacial surgery Orthodontics Dental medicine
Article was published inCzech Dental Journal

2022 Issue 2-
All articles in this issue
- Editorial
- SVĚTOVÝ DEN ÚSTNÍHO ZDRAVÍ 2022 NAPŘÍČ ČESKEM
- PRAŽSKÉ DENTÁLNÍ DNY 2022 SE ZAMĚŘÍ NA SNÍMATELNOU PROTETIKU
- HISTORIE ORL – 100 LET
- ATTITUDES OF CZECH DENTAL CHAMBER MEMBERS TO THE COVID-19 PANDEMIC MEASURES IMPLEMENTED IN DENTAL PRACTICES
- MOLAR INCISOR HYPOMINERALIZATION
- FATIGUE FAILURE OF NICKEL-TITANIUM INSTRUMENTS IN ENDODONTICS AND ITS INFLUENCING FACTORS
- SBORNÍK ABSTRAKTŮ KONFERENCE ÚSMĚV 022
- PREVENCE NEÚSPĚCHŮ PŘI PROTETICKÉ REHABILITACI CHRUPU
- SPECIFIKA PROTETICKÉHO OŠETŘENÍ U PSYCHICKY NEMOCNÝCH A SOCIÁLNĚ ČI FYZICKY ZNEVÝHODNĚNÝCH PACIENTŮ
- MIKROBIÓM SNÍMATEĽNÝCH NÁHRAD A POMÔCOK A NAJNOVŠIE METÓDY STAROSTLIVOSTI
- POUŽITIE TERMOKAMERY PRI DIAGNOSTIKE A SLEDOVANÍ OCHORENÍ OROMAXILOFACIÁLNEJ OBLASTI
- NEOPTERIN, KYNURENIN A TRYPTOFAN JAKO MARKERY AKTIVACE IMUNITNÍHO SYSTÉMU U PARODONTITIDY
- VPLYV PAROPATOGÉNNYCH BAKTÉRIÍ NA SPONTÁNNE POTRATY
- PREVALENCE KAZU RANÉHO DĚTSTVÍ V ČESKÉ REPUBLICE
- MOLÁROVÁ A ŘEZÁKOVÁ HYPOMINERALIZACE
- HYDRODYNAMICKÝ VÝPLACH A KALCIUMSILIKÁTOVÉ MATERIÁLY V ENDODONCII
- KRÁTKODOBÁ ANTIBAKTERIÁLNA AKTIVITA TROCH VYBRANÝCH ENDODONTICKÝCH SEALEROV PROTI ENTEROCOCCUS FAECALIS
- HYPERODONCIE
- PALATINÁNĚ DISLOKOVANÝ ŠPIČÁK A ASOCIOVANÉ DENTÁLNÍ ANOMÁLIE
- Czech Dental Journal
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- MOLAR INCISOR HYPOMINERALIZATION
- HYPERODONCIE
- NEOPTERIN, KYNURENIN A TRYPTOFAN JAKO MARKERY AKTIVACE IMUNITNÍHO SYSTÉMU U PARODONTITIDY
- MOLÁROVÁ A ŘEZÁKOVÁ HYPOMINERALIZACE
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

