-
Medical journals
- Career
Postavení milnacipranu v klinické praxi
: E. Češková
: Psychiatrická klinika LF MU a FN, Brno přednostka prof. MUDr. E. Češková, CSc.
: Čes. a slov. Psychiat., 104, 2008, No. 8, pp. 420-425.
: Comprehensive Reports
Duálně působící antidepresiva jsou relativně novou skupinou. Hlavními zástupci jsou inhibitoři zpětného vychytávání serotoninu a noradrenalinu (SNRI), mezi které patří venlafaxin, milnacipran a duloxetin. Sdělení se zabývá milnacipranem. Detailněji je rozebírána nová indikace fibromyalgie. V současně době je zdůrazňována individualizovaná léčba. Určité drobné rozdíly ve farmakokinetice a farmakodynamice SNRI mohou být důležité při individualizované léčbě. Jsou uvedeny kazuistiky nemocných úspěšně léčených milnacipranem..
Klíčová slova:
milnacipran, antidepresiva, fibromyalgie, farmakokinetika, farmakodynamika.ÚVOD
Dnes máme k dispozici kolem čtyř desítek antidepresiv (AD) rozdělených do několika skupin. Do popředí zájmu se dostávají tzv. duální AD. Hlavními zástupci jsou SNRI (serotonin and noradrenalin reuptake inhibitors, tj. inhibitory zpětného vychytávání serotoninu a noradrenalinu).
SNRI
Venlafaxin je první z této skupiny a je na našem trhu nejdéle. Dále je u nás k dispozici pro léčbu depresivní poruchy milnacipran. Duloxetin je v ČR registrován pro léčbu depresivní poruchy (i generalizované úzkostné poruchy), nemá však sjednánu úhradu od systému zdravotního pojištění. Venlafaxin má vysokou afinitu k serotoninovému (5-HT) transportéru a v nízkých dávkách účinkuje jako SSRI. Duloxetin má také vyšší afinitu k serotoninovému než noradrenalinovému (NA) transportéru (10 : 1). Milnacipran je v tomto ohledu nejvyrovnanější, s relativní vyšší afinitou k NA systému (1,6 : 1). Venlafaxin a duloxetin mají také nízkou afinitu k dopaminovému transportéru, což může být ve vyšších dávkách klinicky významné [27].
SNRI jsou rychle absorbována po perorálním podání, mají relativně krátký vylučovací poločas. Venlafaxin a duloxetin jsou metabolizovány izoenzymem CYP 2D6 a mají slabý inhibiční vliv na CYP 2D6. Pouze milnacipran je minimálně metabolizován a neinterferuje s cytochomem P450 enzymů [27].
SNRI jsou stejně účinná jako tricyklická antidepresiva (TCA) a minimálně stejně účinná nebo lepší než specifické zpětné inhibitory serotoninu (SSRI), včetně dosažených odpovědí a remisí. Nedávno publikovaná metaanalýza srovnávala výskyt remisí v kontrolovaných klinických studiích se SNRI (venlafaxin, milnacipran, duloxetin), SSRI (citalopram, escitalopram, fluoxetin, paroxetin, sertralin) a TCA (amitriptylin, klomipramin, imipramin). SNRI vykazovala nejvyšší účinnost vyjádřenou výskytem remisí (u hospitalizovaných i ambulantních pacientů) a nejnižší počet vysazení [14]. Přímé srovnání jednotlivých duálních AD provedeno nebylo. Obecně jsou SNRI lépe snášena než TCA (méně anticholinergních vedlejších účinků) a s výjimkou venlafaxinu mají méně sexuálních vedlejších účinků než SSRI. Venlafaxin je považován za relativně nejméně tolerované SNRI.
Kromě depresivní poruchy jsou SNRI úspěšná u celého spektra úzkostných poruch. V této indikaci je nejvíce údajů s venlafaxinem [4]. Vzhledem k tomu, že noradrenergní složka hraje v léčbě bolesti roli, stávají se SNRI významnou léčbou bolesti (včetně bolesti spojené s depresí) [1, 4, 27].
MILNACIPRAN – POSTAVENÍ V RÁMCI SNRI
O milnacipranu (f.o. Ixel, Dalcipran) byla v naší odborné literatuře publikována dvě souhrnná sdělení, jedno poměrně nedávno [1, 29]. Od té doby byly publikovány některé nové práce s milnacipranem a naši psychiatři postupně získávají vlastní zkušenosti s jeho podáváním.
Farmakodynamika
Jeho vysoká afinita k oběma transportérům předpokládá, že účinkuje podobně jako imipramin, ale bez jeho vedlejších účinků. V této souvislosti je zajímavé, že japonští autoři zjistili, že reaktivita na milnacipran byla predikována polymorfismem NA transportéru [37].
Farmakokinetika
Po perorálním podání je milnacipran výborně absorbován a jeho absorpce není ovlivněna jídlem. Vazba na proteiny je nízká (13%), distribuční objem vysoký, což vše vede k vysoké biologické dostupnosti a nízké interindividuální variabilitě. Milnacipran není metabolizován jaterním enzymatickým systémem CYP 450, je metabolizován konjugací s kyselinou glukuronidovou a N-dealkylací. Nemá aktivní metabolity, nemá vliv na žádný z enzymatických systémů CYP 450, z čehož vyplývá, že není nutné upravovat dávku u nemocných s narušenými jaterními funkcemi, např. u alkoholiků a starších lidí [20]. Byl zjištěn lineární vztah mezi dávkou a plazmatickými hladinami, takže se snadno dávka přizpůsobuje. Metabolismus současně podávané medikace zřejmě není ovlivněn léčbou milnacipranem. Naproti tomu současné podávání karbamazepinu, lithia a lorazepamu může mírně zvyšovat hladiny milnacipranu, avšak ne klinicky relevantně [22]. Stabilních plazmatických hladin je dosaženo v průměru po 2 dnech. Má relativně krátký vylučovací poločas (8 hod.). Celkem 90 % je vyloučeno močí, < 5 % stolicí. Protože vyloučení závisí na aktivitě ledvin, je třeba upravit dávku v případě ledvinné nedostačivosti [21].
ÚČINNOST, SNÁŠENLIVOST, BEZPEČNOST
Antidepresivní účinnost milnacipranu byla prokázána v řadě randomizovaných, kontrolovaných studií. V komparativních studiích byla prokázána srovnatelná účinnost s TCA a lepší než SSRI, konkrétně fluoxetinu a fluvoxaminu [1, 2]. Z klinického hlediska je důležité, že milnacipran prokázal dobrou účinnost v léčbě závažné deprese. Ve velké otevřené japonské studii u těžkých, středně těžkých a mírných depresí byla pozorována odpověď u 72 %, 70 % a 44 % léčených. Rozdíl mezi dosaženými remisemi byla mezi skupinou těžkých a středně těžkých a skupinou mírných depresí statisticky signifikantní [28]. Odpověď u mírné deprese se blížila účinnosti SSRI v léčbě standardního nemocného s velkou depresí. S tímto do určité míry korespondují výsledky nedávno publikované meta-analýzy. Tato zahrnovala 6 dvojitě slepých, randomizovaných klinických studií srovnávajících milnacipran se SSRI v léčbě velké deprese u 1082 ambulantních nemocných a nezaznamenala rozdíl v lékové odpovědi mezi SSRI a milnacipranem (58,9 % odpovědí na milnacipranu a 58,3 % na SSRI). Také nebyl zjištěn významný rozdíl ve vysazení léčby [17]. Tato studie tehdy hodnotila lékovou odpověď (ne remisi) u ambulantních nemocných bez diferenciace, podle tíže deprese. Lze předpokládat, že se jednalo spíše o méně závažné deprese. Milnacipran může mít o něco více noradrenergních (sucho v ústech, bolesti hlavy, pocení, dysurie) a méně serotonergních nežádoucích účinků (nauzea, sexuální dysfunkce) ve srovnání s duloxetinem nebo venlafaxinem [27]. Milnacipran neovlivňuje napěťově závislé kalciové, káliové nebo sodíkové iontové kanály a není tedy pravděpodobné, že by ovlivnil srdeční funkce [24]. Milnacipran je spojen s minimálním vlivem na TK, pulz a minimálně ovlivňuje QT interval [19]. U malého procenta pacientů bylo náhlé vysazení milnacipranu spojeno s úzkostí a sporadicky s nauzeou a insomnií [34]. Proto je vhodná postupná redukce dávky. Příznaky z vysazení jsou méně časté než u převážně serotonergních látek (některá SSRI a venlafaxin). Předávkování až do množství 2,8 g milnacipranu nemělo významné důsledky a nebyly popsány žádné fatality [15]. V poslední době se u depresivní poruchy dostávají do popředí zájmu kognitivní dysfunkce. Ve dvojitě slepé placebem kontrolované studii u 12 zdravých neměly dobrovolné dávky 100 mg milnacipranu [23] vliv na řízení motorového vozidla a opakované podání milnacipranu nemělo ve srovnání s placebem žádný vliv na kognitivní funkce dobrovolníků [18]. Klinicky relevantní údaje o jednotlivých SNRI jsou shrnuty v tabulce 1.
1. Klinicky relevantní charakteristiky jednotlivých SNRI. 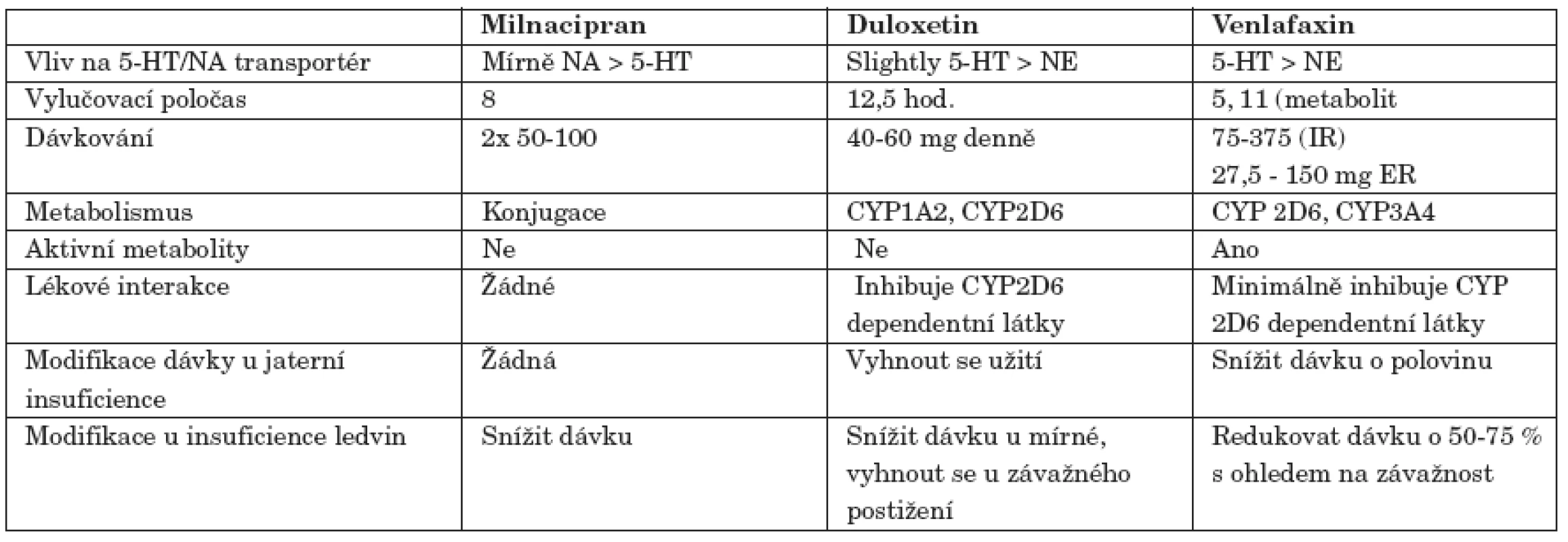
V jedné studii byl zkoumán vliv paroxetinu a milnacipranu na sérové hladiny brain-derived neurotrophic factor (BDNF) u depresivních nemocných. BDNF patří do skupiny neurotropních růstových faktorů. V řadě studií jsou nacházeny nižší hladiny BDNF u neléčených depresivních nemocných ve srovnání se zdravými kontrolami. Tato skutečnost může u deprese odrážet selhání neuronalní plasticity. Autoři sledovali kromě jiného sérové hladiny BDNF před a po léčbě milnacipranem a paroxetinem. Došlo ke zvýšení jeho hladiny, které byly významně vyšší u respondérů na obě aktivní látky [38].
MILNACIPRAN A BOLEST
Ukazuje se, že analgetický efekt AD je nezávislý na jejich vlivu na depresivní náladu, nastupuje dříve než efekt antidepresivní, často v nižších dávkách, a byl prokázán u pacientů s chronickou bolestí bez deprese [7, 13]. Kazuistiky a malé otevřené studie prokázaly zmírnění bolesti při podávání milnacipranu u osteoartritidy a degenerativní spondylózy [11, 30], glossodynie [31], postherpetické neuralgie [26, 33], temporomandibulární bolesti [32] a fibromyalgie [8, 16].
Fibromyalgie
Problematika fibromyalgie se v posledních několika letech objevuje na různých psychiatrických kongresech. V ČR zůstává doménou revmatologů. Fibromyalgie je chronický generalizovaný nezánětlivý muskuloskeletální syndrom. Prevalence je 5 % klientely rodinných /praktických lékařů a až 20 % klientely revmatologů. Základním znakem je plošná bolest se ztuhlostí a přítomnost bodů se zvýšenou citlivostí na tlak. Průběh je mnohaletý, nevede ale k deformitám, pohybové invaliditě nebo kosmetické újmě a nezkracuje život. Příznačné je kolísání v čase, a to jak dlouhodobě tak diurnálně (polední okénko). Z projevů mimo pohybový aparát je nápadný pocit chronické únavy až vyčerpanosti, poruchy spánku, úzkost, deprese, často i bolest hlavy, včetně migrenózní, závratě, poruchy paměti, parestézie, může být přítomen syndrom dráždivého střeva a další funkční orgánové syndromy. Část nemocných s fibromyalgií splňuje i kritéria chronického únavového syndromu [9, 10]. Pro diagnózu je nutné splnění obou kritérií ACR 1990 (American College of Rheumatology): 1. plošná bolest trvající minimálně 3 měsíce (v pravé i levé polovině, pod pasem i nad pasem), 2. tlaková bolest u 11 nebo více z 18 párových bodů [36]. Odpověď testujeme tlakem nebo algometrem. Podstatou je kvalitativně změněná percepce nociceptivních podnětů, práh pro vnímání bolesti je snížen. Zobrazovacími metodami bylo prokázáno snížení krevního průtoku oblastmi, které kontrolují percepci bolesti, po indukci bolesti větší aktivace korových oblastí a biochemické abnormity – nízké hladiny biogenních aminů, včetně serotoninu a jeho metabolitů, zvýšené hodnoty substance P a některé další.
V nejnovějších českých revmatologických učebnicích je v rámci nefarmakologické léčby zdůrazňováno získání vzájemné důvěry, edukace a psychologické vedení. V kontrolovaných studiích byl prokázán efekt redukce stresu, kinezioterapie (aerobní cvičení), hypnoterapie a elektroakupunktury. U farmakologické léčby jsou základem psychofarmaka, nejčastěji malé dávky TCA (amitriptylin), dále analgetika (paracetamol). Efekt nesteroidních antirevmatik nebyl prokázán (nejde o zánět), mohou však povýšit efekt analgetik. Nejčastěji jsou podávána externě. SNRI zmiňována nejsou [9, 10]. Již z tohoto popisu vyplývají analogie s depresivními stavy.
Milnacipran u fibromyalgie
Kromě již zmíněných malých studií byly nedávno publikovány minimálně dvě dvojitě slepé, placebem kontrolované úspěšné studie. První studie byla 12týdenní a milnacipran byl podáván v dávce 200 mg denně [35]. Významně více léčených milnacipranem vykazovalo zmírnění bolesti a únavy (75 %) ve srovnání s placebem (38 %). Cunningham [6] referuje o 6měsíční dvojitě slepé, placebem kontrolované studii. V této relativně velké studii (224 nemocných léčeno milnacipranem 100 mg pro die, 441 dávkou 200 mg denně a dále bylo zařazeno 223 kontrol) signifikantně více pacientů na milnacipranu udávalo zmírnění bolesti, nástup účinku byl pozorován do jednoho týdne a efekt přetrvával.
Ve srovnání se zdravými kontrolami je u fibromylagie častější genotyp serotoninového transportéru se zkrácenou alelou, což ukazuje na možnost alterace serotoninového metabolismu. Tito nemocní také vykazují vyšší úroveň deprese a psychologické nepohody [5]. V této souvislosti se nabízí analogie se zásadní epidemiologickou studií Caspiho. Tato prokazuje, že genetický polymorfismus serotoninového transportéru může ovlivnit rozvoj depresivní symptomatologie u rizikových jedinců, kteří prožili v minulosti závažné stresující životní události [3]. Nepochybně v budoucnosti může farmakogenetika přispět k individualizované léčbě fibromyalgie.
Individualizovaná léčba deprese milnacipranem ve světle současných algoritmů
Dostupnost řady AD je opodstatněná individuální reaktivitou a snášenlivostí nemocných s depresivní poruchou. Zatím vycházíme při individuální volbě ze znalostí o dostupných AD a detailní znalosti nemocného. Nabízí se otázka, pro jaké nemocné je milnacipran vhodný. Nedávno byl vydán sborníku kazuistik, které upozorňují na klinické charakteristiky deprese spojené s úspěšným podáváním milnacipranu. Je prezentována úspěšná aplikace při převažující únavě a inhibici, ať již v rámci první volby nebo při snaze zvládnout reziduální příznaky. Toto má své opodstatnění na základě studie srovnávající milnacipran a paroxetin, kdy na milnacipran reagovali signifikantně lépe pacienti s výraznou motorickou retardací bazálně [25]. Několik kazuistik dokumentuje úspěšnost záměny AD za antidepresivum s jiným mechanismem, resp. širším mechanismem účinku (milnacipran) při známkách farmakorezistence. Další skupinu, která může profitovat z milnacipranu, tvoří nemocní, kteří mají na stávající antidepresivní léčbě sexuální vedlejší účinky a nemocní s postižením jater jakékoliv etiologie [12].
Z brněnského pracoviště uvádím dvě krátké kazuistiky poukazující na možnost indikace u organické depresivní poruchy a sekundárního alkoholismu.
Muž, 63 roků, hospitalizován na psychiatrické klinice (PK) březen - květen 2008.
Matka pacienta trpěla Huntingtonovou chorobou, u pacienta se první projevy Huntingtonovy choroby objevily asi před 5 lety. Pacient je vdovec, manželka alkoholička před 2 lety suicidovala. Má 2 dospělé, výdělečně činné děti, aktuálně žije se synem. V poslední době pracoval jako zámečník, od r. 2006 je v částečném invalidním důchodu. V únoru 2008 byl hospitalizován v léčebně pro paranoidně-halucinatorní symptomatologii a suicidální pokus z psychotických důvodů. Na PK přijat po opětném suicidálním pokusu. Při přijetí orientován s výjimkou mírné časové dezorientace, snaha o spolupráci, myšlení chudé, odpovědi po latencích, výrazně depresivní, autoakuzace (ohledně manželky). Nasazen escitalopram. Pro rozvoj paranoidní symtomatologie převeden na olanzapin. Po ústupu paranoidity návrat výrazné depresivní symtomatologie, přidán escitalopram, kombinace nebyla úspěšná. Proto escitalopram zaměněn za milnacipran, po ústupu depresivní symptomatologie olanzapin postupně vysazen, pacient odchází pouze s milnacipranem v dávce 100 mg. V srpnu telefonický dotaz ohledně stavu nemocného u příslušného ambulantního lékaře – pacient je nadále v relativně dobrém stavu, pokračuje v aplikaci milnacipranu. K volbě léčby nás vedla přítomnost závažné deprese s psychotickými rysy.
Muž, 49 roků, hospitalizován na PK v době říjen - prosinec 2007.
Otec a syn nemocného inklinují k abúzu návykových látek. Pacient je ženatý, 2 děti, manželství harmonické. Od r. 2004 léčen pro depresivní stavy ambulantně, nasazen nejprve escitalopram, na tomto zlepšení, které trvalo až do března 2006, kdy došlo k návratu depresivní symptomatologie. Navýšení dávky bylo neúspěšné, proto převeden na venlafaxin, na kterém zlepšen do března 2007. Opět návrat deprese, přechodné zlepšení na sertralinu a poté mirtazapinu. V září 2007 zvýraznění deprese, doporučena hospitalizace na PK. Pacient popisuje obavy, zhoršení nálady, nespavost, stavy úzkosti, únavu, zpomalení, sklon k abúzu alkoholu. Objektivně v popředí apatie, hypobulie, depresivní nálada, insomnie, hypoorexie, přítomna i úzkostná komponenta. Ze somatické komorbidity léčen pro hypertenzi a hypercholesterolémii, diagnostikována hepatopatie. Po nasazení milnacipranu zlepšen (přechodné zhoršení zvládnuto navýšením milnacipranu), posléze propuštěn. Srpen 2008 - telefonický dotaz u příslušného ambulantního psychiatra – dobrý psychický stav nemocného trvá, nadále bere milnacipran. Volbu ovlivnila komorbidita a neúspěšnost předchozí terapie (změna na jiný mechanismus účinku).
ZÁVĚRY
Inhibitory zpětného vychytávní serotoninu a noradrenalinu jsou v některých aspektech lepší než AD ovlivňující jeden neurotransmitérový systém díky komplementaritě serotonergního a noradrenergního systému. Milnacipran, na rozdíl od venlafaxinu a duloxetinu, je nejvíce vybalancované SNRI z hlediska podílu zpětného vychytávání serotoninu k zpětnému vychytávání noradrenalinu. Tento farmakologický profil a výhodné farmakokinetické parametry (není metabolizován jaterním enzymatickýmn systémem CYP 450) určují jeho postavení v rámci SNRI a umožňují individualizovanou antidepresivní léčbu. Perspektivní se jeví i indikce u chronické bolesti, hlavně fibromyalgie.
Finanční podpora Výzkumným záměrem MSM0021622404.
Prof. MUDr. Eva Češková, CSc.
Psychiatrická klinika LF MU a FN Brno
Jihlavská 20
625 00 Brno
e-mail: eceska@med.muni.cz
Sources
1. Anders, M., Doležal, T.: Současné postavení milnacipranu mezi antidepresivy. Farmakoterapie, 2, 2006, s. 676-679.
2. Bisserbe, J. C.: Clinical utility of milnacipran in comparison with other antidepressants. Int. Clin. Psychopharmacol., 17, 2002, Suppl. 1, S43-S50.
3. Caspi, A., Sugden, K., Moffitt, T. E. et al.: Influence of life stress on depression: moderation by a polymorphism in the 5-HTT gene. Science, 18, 2003, pp.291-293.
4. Češková E.: Duálně působící antidepresiva. Remedia, 16, 2006, s. 594-597.
5. Cohen, H., Buskila, D., Neumann, L., Ebstein, R. P.: Confirmation of an association between fibromyalgia and serotonin transporter promoter region (5-HTTLPR) polymorphism, and relationship to anxiety-related personality traits. Arthritis Rheum., 46, 2002, pp. 845-847.
6. Cunningham, J.: Milnacipran is a safe and effective treatment for fibromyalgia. CNS Spect., 13, 2008, pp. 465-466.
7. Fishbain, D.: Evidence-based data on pain relief with antidepressants. Ann. Med., 32, 2000, pp. 305-316.
8. Gendreau, R. M., Mease, P. J., Rao, S. R. et al.: Milnacipran: A potential new treatment of fibromyalgia. Arthritis Rheum., 48, 2003, Suppl. 9, S616.
9. Hrnčíř, Z.: Terapie fibromyalgie. In: Pavelka, K. et al.: Farmakoterapie revmatických onemocnění. Galén, 2005, Praha, s. 413-415.
10. Hrnčíř, Z., Dvořák, Z.: Fibromyalgie a chronický únavový syndrom. In: Pavelka, K, Rovenský, J. et al.: Klinická revmatologie. Galén, 2003, Praha, s. 679-683.
11. Kamata, M., Naito, S., Takahashi, H., Higuchi, H.: Milnacipran for the treatment of chronic pain. Hum. Psychopharmacol., 18, 2003, pp. 575-576.
12. Kolektiv autorů: Léčba deprese duálním antidepresivem Ixel. Sborník kazuistik, 2008, Janssen-Cilag.
13. Leo, R. J.: Chronic pain and comorbid depression. Curr. Treat. Options Neurol., 7, 2005, pp. 403-412.
14. Machado, M., Iskedjian, M., Ruin, I., Einarson, T. R.: Remission, dropouts, and adverse drug reaction rates in major depressive disordeer. A meta-analysis of head - to-head trials. Current Medicine Research and Opinions, 22, 2006, pp. 1825-1837.
15. Montgomery, S. A., Prost, J. F., Solles, A., Briket, M.: Efficacy and tolerability of milnacipran: An overview. Int. Clin. Psychopharmacol., 11, 1996, Suppl. 4, pp. 47-51.
16. Nagaoka, S., Ohno, M., Sekiguchi, A.: An open-label clinical trial of milnacipran in fibromyalgia syndrome with comorbid depressive symptoms. Int. J. Psychiatry Clin. Practice, 8, 2004, pp. 47-51.
17. Papakostas, G. I., Fava, M.: A meta-analysis of clinical trials comparing milnacipran, a serotonin-norpinephrine reuptake inhibitor, with a selective serotonin reuptake inhibitor for the treatment of major depressive disorder. Eur. Neuropsychopharmacol., 17, 2007, pp. 32-36.
18. Poirier, M. F., Galinowski, A., Amado, I. et al.: Double-blind comparative study of the action of repeated administration of milnacipran versus placebo on cognitive functions in healthy volunteers. Hum. Psychopharmacol. Clin. Exp,. 19, 2004, pp. 1-7.
19. Puech, A., Montgomery, S. A., Prost, J. F. et al.: Milnacipran, a new serotonin and noradrenaline reuptake inhibitor: An overview of its antidepressant activity and clinical tolerability. Int. Clin. Psychopharmacol., 12, 1997, pp. 99-108.
20. Puozzo, C., Albin, H., Vincon, G. et al.: Pharmacokinetics of milnacipran in liver impairment. Eur. J. Drug Metab. Pharmacokinet., 23, 1998, pp. 273-279.
21. Puozzo, C., Pozet, N., Deprez, D. et al.: Pharmacokinetics of milnacipran in renal impairment. Eur. J. Drug Metab. Pharmacokinet., 23, 1998, pp. 280-286.
22. Puozzo, C., Lens, S., Reh, C. et al.: Lack of interaction of milnacipran with the cytochrome P450 isoenzymes frequently involved in the metabolism of antidepressants. Clin. Pharmacokinet., 44, 2005, pp. 977-988.
23. Rochet, F., Marais, J., Serre, C., Pandini, E.: Effects of milnacipran on driving vigilance. Int. J. Psych. Clin. Practice, 8, 2004, pp. 109-115.
24. Rouet, R. H., Tisne-Versailles, J., Adamantidis, M. M. et al.: Comparative in vivo and in vitro study of the cardiac effects of milnacipran and imipramine. Fundam. Clin. Pharmacol., 3, 1989, pp. 237-244.
25. Sechter, D., Vandel, P., Weiller, E. et al.: A comparative study of milnacipran and paroxetine in outpatients with major depression. J. Affect. Disord., 83, 2005, pp. 233-236.
26. Shimamoto, E., Doi, N., Suwa, H. et al.: A case of postherpetic neuralgia improved by milnacipran. Jpn. J. Clin. Psychopharmacol., 5, 2002, pp. 197-200.
27. Stahl, S. M., Grady, M., Moret, Ch., Briket, M.: SNRIs: The pharmacology, clinical efficacy, and tolerability in comparison with other classes of antidepressants. CNS Spectr., 10, 2005, pp. 732-747.
28. Sugawara, Y., Higuchi, H., Yoshida K. et al.: Response rate obtained using milnacipran depending on the severity of depression in the treatment of major depressive patiens. Clin. Neuropharmacol., 29, 2006, pp. 6-9.
29. Švestka, J.: Nová psychofarmaka. Milnacipran-antidepresivum s prvním označením příslušnosti ke čtvrté generaci. Psychiatrie, 4, 2000, s. 46-56.
30. Tanikawa, H.: Efficacy of milnacipran in patients with chronic orthopedic pain including degenerative spondylosis and osteoarthritis. Int. J. Psychiatry Clin. Practice, 6, 2002, p. 255.
31. Toyofuku, A.: Efficacy of milnacipran for glossodynia patients. Int. J. Psychiatry Clin. Praktice, 7, 2003, Suppl. 1, pp. 23-24.
32. Toyofuku, A., Miyako, H.: A case of temporo-mandibular disorder with fibromyalgia treated with the antidepressant, milnacipran. Hum. Psychopharmacol., 19, 2004, pp. 357-358.
33. Utsunomiya, K., Ukita, T., Sirota, S.: A case of postherpetic neuralgia treated with milnacipran. Jpn. J. Clin. Psychopharmacol., 5, 2002, pp. 190-196.
34. Vandel, P., Sechter, D., Weiller, E. et al.: A comparative study of milnacipran and paroxetine in outpatients with major depression. Hum. Psychopharmacol., 19, 2004, pp. 585-586.
35. Vitton, O., Gendreau, M., Gendreau, J. et al.: A double-blind placebo controlled trial of milnacipran in the treatment of fibromyalgia. Hum. Psychopharmacol., 19, 2004, Suppl. 1, S27-S35.
36. Wolfe, F., Smythe, H. A., Yunus, M. B. et al.: The American College of Rheumatology 1990 criteria for the classification of fibromyalgia. Report of the multicenter criteria committee. Arthritis Rheum., 33, 1990, pp. 160-172.
37. Yoshida, K., Takahashi, H., Higuchi, H. et al.: Prediction of antidepressant response to milnacipran by norepinephrine transporter gene polymorphisms. Am. J. Psychiatry, 161, 2004, pp. 1575-1580.
38. Yoshimura, R., Mitoma, M., Sugita, A. et al.: Effects of paroxetine or milnacipran on serum brain-derived neurotrophic factor in depressed patients. Prog. Neuropsychopharmacol. Biol. Psychiatry, 31, 2007, pp. 1034-1037.
Labels
Addictology Paediatric psychiatry Psychiatry
Article was published inCzech and Slovak Psychiatry

2008 Issue 8-
All articles in this issue
- Satisfaction of Patients and their Relatives with Therapy in Psychiatry within the Framework of the EUNOMIA Project – Final Results in the Czech Republic
- Application of Standardized Evaluating Scales in the Nursing Process in Psychiatry
- Possibilities of Evaluation and Scaling Aggressiveness in Psychiatric Patients by Means of Personality Questionnaires
- Disorders of Perception in Anxiety Conditions
- Effect of Medication on Anthropometric Characteristic of ADHD Children
- The Position of Milnacipran in Clinical Practice
- Borna Disease Virus (BDV) and Psychical Disorders
- Czech and Slovak Psychiatry
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Application of Standardized Evaluating Scales in the Nursing Process in Psychiatry
- Borna Disease Virus (BDV) and Psychical Disorders
- The Position of Milnacipran in Clinical Practice
- Possibilities of Evaluation and Scaling Aggressiveness in Psychiatric Patients by Means of Personality Questionnaires
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

