-
Medical journals
- Career
Diazotační titrace v lékopisné kontrole jakosti léčiv a návrhy pro jejich revizi v Evropském lékopisu*
Authors: Jan Šubert; Jozef Kolář; Jozef Čižmárik
Authors‘ workplace: Katedra farmaceutickej chémie FaF Univerzita Komenského v Bratislave, Slovenská republika ; Ústav aplikované farmacie Farmaceutická fakulta, Masarykova univerzita
Published in: Čes. slov. Farm., 2023; 72, 165-171
Category: Review Articles
doi: https://doi.org/10.5817/CSF2023-4-165Overview
Na základě údajů v Ph. Eur., v některých dalších nověj - ších lékopisech a v publikovaných experimentálních pracích je navrženo revidovat text Ph. Eur. 2.5.8. V první řadě je třeba specifikovat, která z elektrometrických metod má být k instrumentální indikaci konečného bodu diazotačních titrací v Ph. Eur. použita (nejlépe potenciometrie s platinovou indikační elektrodou). Množství bromidu draselného v roztoku k titraci lze snížit na 1 g, chlazení roztoku před titrací z rámcového postupu vypustit a uvést až v jednotlivých monografiích, pokud bude u některých léčiv k získání přesných a správných výsledků potřebné. Diazotační titraci lze v Ph. Eur. využít ke stanovení obsahu i u některých dalších léčiv.
*Věnováno vzpomínce autorů na doc. RNDr. PhMr. Bohuslava Melichara, CSc. (1906–1989), vysokoškolského učitele a farmaceutického chemika se širokým rozhledem.
Úvod
Stanovení obsahu léčiv s primární aromatickou aminoskupinou titrací odměrným roztokem dusitanu sodného patří ke klasickým metodám lékopisné kontroly jakosti léčiv. Přechod od původně vizuální indikace k indikaci instrumentální je však v některých lékopisech, včetně Evropského lékopisu1) (dále Ph. Eur.), doprovázen nejasnostmi, která z elektrometrických metod má být ke stanovení konečného bodu titrace použita, a někdy i nesprávným označením těchto metod. Nejednotný je také přístup lékopisů k otázce koncentrace kyseliny chlorovodíkové, která je nejčastěji používána k okyselení roztoku k titraci a k přídavku bromidu jako katalyzátoru diazotační reakce. Nejasná je potřebnost chlazení roztoku stanovovaného léčiva před titrací a v jejím průběhu. Záměrem našeho příspěvku je na základě srovnání Ph. Eur.1 s některými novějšími lékopisy zemí mimo EU a s údaji v odborném tisku diskutovat tyto problémy a navrhnout změny pro revizi textu části 2.5.8. Ph. Eur.1 a revizi monografií léčiv, u nichž je stanovení obsahu titrací roztokem dusitanu sodného v Ph. Eur.1 za instrumentální indikace konečného bodu předepsáno.
Indikace konečného bodu diazotačních titrací elektrometrickými metodami
V lékopisech jsou rámcovými postupy anebo v jednotlivých článcích předepsány k indikaci konečného bodu titrace diazotačních titrací léčiv různé metody založené na měření elektrických veličin. V Ph. Eur.1 je v rámcovém postupu 2.5.8. uvedena indikace elektrometrická. Není tedy specifikováno, která z elektrometrických metod má být k instrumentální indikaci konečného bodu titrace použita. Z metod uvedených v tomto lékopisu může jít o indikaci potenciometrickou (2.2.20.), amperometrickou (2.2.19.) nebo voltametrickou (2.2.65.). Na postup podle 2.5.8. příslušné články Ph. Eur.1 odkazují s výjimkou článku na natrium-aminosalicylát dihydrát, ve kterém je předepsána potenciometrická indikace konečného bodu titrace. Z jiných nadnárodních lékopisů Mezinárodní lékopis WHO (dále Ph. Int.)2 označuje v rámcovém postupu 2.7 indikaci rovněž jako elektrometrickou, z popisu potřebného přístroje a elektrod ale vyplývá, že jde o indikaci biamperometrickou (50–100 mV). V článcích na léčivé přípravky s obsahem sulfamethoxazolu je však předepsána indikace potenciometrická. Z národních lékopisů Britský lékopis (dále BP)3 uplatňuje v zásadě stejný přístup k problematice jako Ph. Eur.1 V části 2.5.8 instrumentální indikaci konečného bodu diazotačních titrací označuje jako elektrometrickou a v článku na natrium-aminosalicylát dihydrát požaduje indikaci potenciometrickou. Lékopis Spojených států amerických (dále USP)4 v části <451> Nitrite titration předepisuje stanovení konečného bodu elektrometricky za použití vhodných elektrod, a to platinové a kalomelové, nebo dvou platinových elektrod. Z dalšího popisu je zřejmé, že vedle indikace potenciometrické by při použití dvou platinových elektrod mělo jít o indikaci biamperometrickou bez vkládaného napětí podobně, jako tomu bylo v československých lékopisech5. V článcích na některé lékové formy sulfonamidů předepisuje USP4 potenciometrickou indikaci za použití platinové a kalomelové elektrody, nebo za použití vhodných elektrod bez jejich bližší specifikace. Japonský lékopis (dále JP)6 rámcový postup neuvádí a v článcích příslušných léčiv u diazotační titrace předepisuje potenciometrickou nebo amperometrickou indikaci konečného bodu, přičemž podle popisu v JP jde spíše o indikaci biamperometrickou. Indický lékopis (dále IP)7 předepisuje rámcový postup, metodu indikace konečného bodu titrace neoznačuje; z popisu v části 2.3.31. je však zřejmé, že jde o indikaci biamperometrickou (50 mV). Na tuto část články příslušných léčiv odkazují, v článku na prokain-hydrochlorid předepisuje ale IP indikaci potenciometrickou. Brazilský lékopis (dále FB)8 v části 5.3.3.1. rovněž předepisuje rámcový postup a instrumentální variantu stanovení konečného bodu titrace označuje jako indikaci potenciometrickou, podle specifikace elektrod (platinová a kalomelová nebo dvě platinové elektrody s adekvátním rozdílem potenciálu) může jít vedle potenciometrické indikace také o indikaci biamperometrickou. Z uvedeného přehledu je zřejmé, že přístup lékopisů k instrumentální indikaci diazotačních titrací léčiv roztokem dusitanu sodného je nejednotný a v některých je označení metody k indikaci konečného bodu titrace nepřesné či dokonce nesprávné. Náhled do starších experimentálních prací zabývajících se diazotační titrací primárních aromatických aminů, včetně léčiv za instrumentální indikace, ukazuje, že původně byla používána potenciometrická indikace konečného bodu titrace 9–17, která se z navržených metod osvědčila nejlépe18 a byla nejčastější i v dalších letech (např.19–25). Z jiných elektrometrických metod byla ověřována amperometrická a biamperometrická indikace za konstantního napětí 16, 20, 21, 26, 27. Ve sdělení16 je ale hodnocena jako výhodnější než biamperometrická indikace potenciometrická. Bipotenciometrická indikace diazotačních titrací za konstantního proudu (v Ph. Eur.1 voltametrická indikace) byla dosud v souvislosti s diazotačními titracemi publikována jen zřídka (např.28). Byla ale předepsána v rámcovém postupu pro stanovení primárních aromatických aminů lékopisu bývalé NDR29). Indikace konečného bodu diazotačních titrací za použití platinové a tuhové elektrody bez vkládaného napětí běžná v laboratorní praxi ve druhé polovině 20. století má dnes spíš už jen historický význam. Ve své době umožňovala s jednoduchým a levným přístrojovým vybavením získávat objektivní výsledky odměrného stanovení obsahu léčiv s primární aromatickou aminoskupinou. Příkladem jejího využití může být vedle původních prací30, 31 také poslední Československý lékopis (dále ČsL)5. Jsou s ní spojeny nomenklaturní nejasnosti v původních pracích 30, 31 i v monografiích a učebnicích 32–34. Autoři30 popisují indikaci jako elektrometrickou, přičemž z kontextu je zřejmé, že sledovali změny proudu, autoři31 ji ale při citování30 označují jako indikaci potenciometrickou. Označení elektrometrická titrace lze nalézt i ve starší knižní literatuře, např.32 a z faktu, že v následujícím odstavci na stejné úrovni je zmíněna potenciometrická indikace s platinovou a kalomelovou elektrodou jako jiná možnost, je zřejmé, že nejde o označení zastřešující různé možné elektrometrické metody, ale důsledek rozpaků jak indikaci založenou na sledování proudu mezi elektrodami bez vkládaného napětí označit. Autoři33 ji pokládají za potenciometrickou indikaci s bimetalickým systémem elektrod a autorka34) ve shodě s ČsL5 za biamperometrickou indikaci bez vkládaného napětí. Z tohoto přehledu je zřejmé, že uplatnění jednotlivých elektrometrických metod při instrumentální indikaci konečného bodu diazotačních titrací v lékopisech, včetně Ph. Eur.1, neodpovídá poznatkům z experimentálních prací, v nichž samotných ale jsou v některých případech nepřesnosti. I když lze vzhledem k přístupu
některých sledovaných lékopisů (zejména JP)6 předpokládat, že potenciometrická a biamperometrická indikace poskytují v předmětné aplikaci shodné výsledky, jsou autoři příspěvku názoru, že vhodnější než skupinové či alternativní označení indikační metody by bylo označení specifické. Jako řešení pro Ph. Eur.1 se z pohledu správné laboratorní praxe a vzhledem k rozsahu stávajícího využití jednotlivých elektrometrických metod v lékopisné kontroly jakosti léčiv nabízí jednotné využití potenciometrické indikace konečného bodu diazotačních titrací s platinovou indikační elektrodou9, 11–17, 20–25 a kalomelovou nebo jinou vhodnou porovnávací elektrodou. Potenciometrická indikace diazotační titrace již je v Ph. Eur.1 předepsána v článku na natrium-aminosalicylát dihydrát (a v monografiích dalších lékopisů ji lze nalézt i u jiných léčiv) a potenciometrická indikace konečného bodu titrace je v Ph. Eur.1 využívána v obecné rovině v míře podstatně větší než indikace biamperometrická či amperometrická.
Složení reakčního prostředí
Diazotační titrace primárních aromatických aminů roztokem dusitanu sodného (výjimečně dusitanu draselného)10 probíhají v kyselém prostředí, k jehož zajištění je používána obvykle kyselina chlorovodíková (dále HCl). Podle 35, 36 není nitrosačním činidlem kyselina dusitá, ale reaktivnější nitrosoniový iont NO+, resp. ve vodném roztoku nitrosylchlorid NOCl. Přepočet údajů o obsahu a přídavku HCl (popř. kyseliny octové) v roztoku před diazotační titrací ve sledovaných lékopisech a v původních experimentálních pracích na jejich koncentrace vedl ve více případech ke zjištění významných rozdílů. V rámcovém postupu Ph. Eur.1 (2.5.8.) je předepsáno prostředí zředěné kyseliny chlorovodíkové, kterému odpovídá koncentrace HCl 2 mol/l. Tak tomu je ve většině článků léčiv stanovovaných diazotační titrací v Ph. Eur.1 s odchylkami u některých léčiv v širším rozmezí. V článku na natrium-aminosalicylát dihydrát je pro titraci předepsáno prostředí kyseliny octové 8 mol/l, což může souviset s chováním tohoto léčiva v prostředí kyseliny chlorovodíkové22. Ph. Int.2 v rámcovém postupu pro diazotační titraci předepisuje rovněž prostředí HCl 2 mol/l s odchylkami v některých článcích na léčiva a léčivé přípravky. V nich se koncentrace HCl pohybuje častěji v hodnotách nižších, počínaje 0,4 mol/l HCl v článku na sulfamethoxazol a 0,5 mol/l HCl v článku na paracetamol (kdy se titruje po hydrolýze léčiva p-aminofenol). V článku na sulfamethoxazol je součástí roztoku k titraci mimo kyselinu chlorovodíkovou i kyselina octová, v článcích na léčivé přípravky s obsahem tohoto léčiva tomu tak ale není. Koncentrace HCl 2 mol/l je předepsána také u roztoku k titraci v rámcovém postupu BP3 a je předepsána ve většině článků, v nichž je použita diazotační titrace za instrumentální indikace. V článku na natrium-aminosalicylát dihydrát je podobně jako v Ph. Eur.1 předepsána místo HCl kyselina octová 8 mol/l. USP4 v rámcovém postupu předepisuje koncentraci HCl v roztoku k titraci téměř 4 mol/l,
v některých článcích je však koncentrace HCl v roztoku k titraci nižší, u prokain-hydrochloridu dokonce jen 0,6 mol/l. V některých článcích požaduje USP4 jako součást titračního prostředí vedle kyseliny chlorovodíkové jistý podíl kyseliny octové, a to u acetylsulfisoxazolu a přípravku s jeho obsahem a dále u přípravků obsahujících sulfamethoxazol. V článcích JP6, který pro diazotační titrace nemá rámcový postup, se koncentrace HCl v roztoku k diazotačním titracím pohybují v rozmezí 0,7–0,9 mol/l, tedy v nižších hodnotách s výjimkou článku na aflochalon, kde je koncentrace HCl v roztoku k titraci téměř 2 mol/l. IP7) v rámcovém postupu požaduje koncentraci HCl v roztoku k titraci vyšší než 3 mol/l. Ještě vyšší koncentraci HCl, než je v rámcovém postupu, předepisuje IP7 v článcích na benzokain a na léčivé přípravky s obsahem prokainamid-hydrochloridu. V dalších článcích IP se koncentrace HCl v roztoku k titraci pohybuje v rozmezí 0,6 mol/l (sulfacetamid sodná sůl, sulfadiazin) do 2 mol/l. FB8 v rámcovém postupu předepisuje koncentraci HCl v roztoku k titraci 2 mol/l, tedy stejnou jako Ph. Eur.1, Ph. Int.2 a BP3.
Obsah sledovaných lékopisů 1–4, 6, 7 ukazuje a tabulka 1 dokládá, že řadu léčiv lze úspěšně titrovat dusitanem sodným při různé koncentraci HCl, přičemž u lékopisných postupů by mělo jít o postupy validované. Také v experimentálních pracích zabývajících se zčásti či výhradně léčivy lze nalézt či z údajů v nich vyčíslit pro koncentraci HCl v roztoku k titraci různé údaje. Autoři některých starších prací13, 19, 30, 32) titrovali řadu léčiv při výchozí koncentraci HCl 6 mol/l, pro stanovení mesalazinu volili autoři koncentraci HCl v roztoku k titraci vyšší než 4 mol/l24), běžnější jsou však koncentrace nižší. Autorům1 5, 17 stačila při titraci p-fenetidinu po hydrolýze fenacetinu 3 mol/l a k titraci sulfonamidů 2,5 mol/l HCl37). Koncentraci HCl 4 mol/l volili autoři21 při titraci metoklopramid-hydrochloridu, současně však prokázali sledováním v rozmezí 0,2–9 mol/l, že koncentrace HCl v širokém rozmezí při navážce 300 mg léčiva neovlivňuje výsledky stanovení. Při navážce 10 mg byla optimální koncentrace HCl v rozmezí 3,7–4,7 mol/l. Autoři23 ale úspěšně stanovili malá množství téhož léčiva 0,006 mol/l odměrným roztokem dusitanu sodného při koncentraci HCl v roztoku k titraci nižší než 2 mol/l. Koncentrace HCl v rozmezí 1–9 mol/l neměla průkazný vliv na výsledky diazotační titrace bromhexin-hydrochloridu z navážek 100 mg (v mikroměřítku tomu bylo jinak)28. Přesto autor publikace volil koncentraci HCl v roztoku k titraci 5 mol/l, tedy zbytečně vysokou. Kyselina octová, která je součástí titračního prostředí v několika článcích v lékopisech, např. u natrium-aminosalicylátu dihydrátu Ph. Eur.1 a BP3, se při diazotační titraci bromhexin-hydrochloridu neosvědčila28. Autorům 26, 36 při titraci kyseliny p-aminobenzoové stačila koncentrace HCl 1 mol/l a srovnatelně nízká koncentrace HCl vyhověla i při mikrotitraci řady sulfonamidů20. Optimalizační experimenty prováděné se sulfadimidinem za přítomnosti KBr a ověřené s dalšími léčivy vedly ke koncentraci HCl 0,6 mol/l22. Tyto údaje spolu s obsahem sledovaných lékopisů ukazují, že diazotační
Table 1. Koncentrace HCl v prostředí pro stanovení obsahu některých léčiv diazotační titrací v různých lékopisech 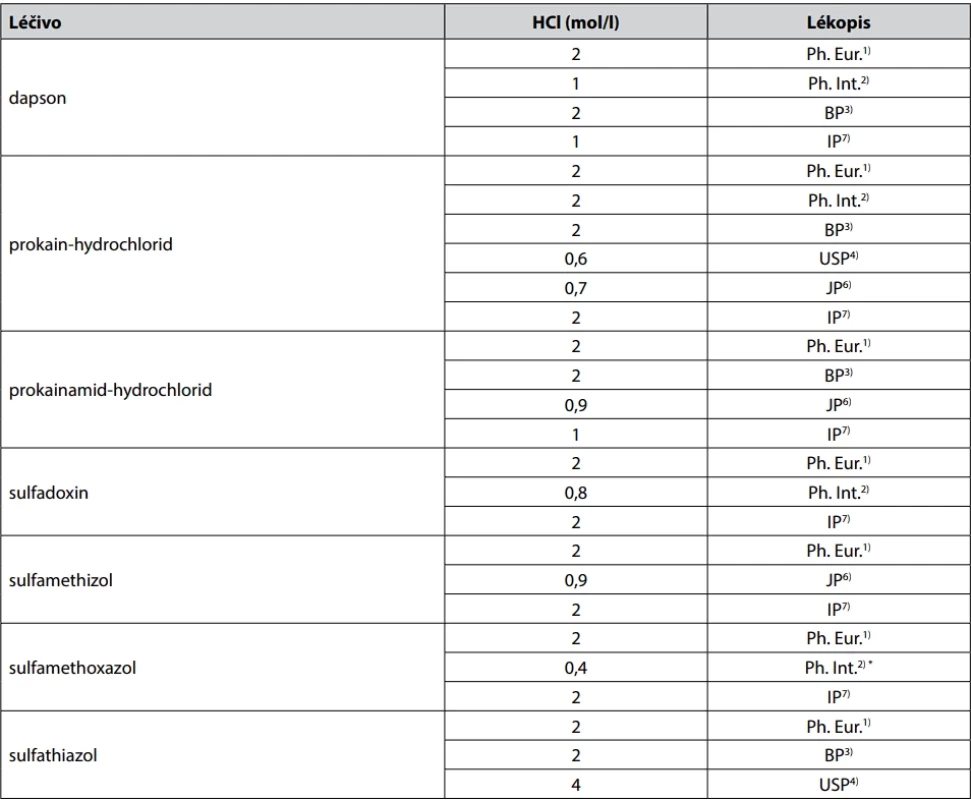
* Mimo HCl je v roztoku k titraci kyselina octová v koncentraci 4,5 mol/l. titrace léčiv probíhají v řadě případů úspěšně v širokém rozmezí koncentrace HCl, přičemž vysoké koncentrace HCl obvykle nejsou potřebné. Dalším důležitým faktorem při diazotačních titracích léčiv roztokem dusitanu sodného je přítomnost alkalického bromidu. Za přítomnosti alkalického bromidu vzniká nitrosylbromid NOBr, který je efektivnějším nitrosačním činidlem než NOCl 20, 35, 36. Urychluje průběh N-nitrosace a tím zkracuje čas potřebný k provedení titrace. Lékopisy tuto skutečnost dosud plně nevyužívají, přestože na ni upozorňuje řada experimentálních prací, např.12, 16, 17, 20, 26. Používá se bromid draselný, výjimečně byl použit nebo je předepsán bromid sodný (např.16) a články na natrium-aminosalicylát dihydrát v Ph. Eur.1 a BP3). Některé lékopisy předepisují přídavek bromidu draselného již v rámcovém postupu1, 3 a pravidelně je KBr jako součást titračního prostředí předepsán v článcích JP6. Koncentrace KBr v rámcovém postupu Ph. Eur.1 a BP3 je 0,5 mol/l, v článcích Ph. Eur., které se rámcovým postupem v plném rozsahu neřídí v rozmezí 0,3–0,4 mol/l, v BP3 0,3–0,8 mol/l. V obou těchto lékopisech u natrium-aminosalicylátu dihydrátu je koncentrace NaBr 0,9 mol/l. V JP6 se pohybuje koncentrace KBr v roztoku k titraci v rozmezí 0,3–0,4 mol/l, v článcích IP7 0,3–0,8 mol/l, v článcích dalších lékopisů od nepřítomnosti KBr ve většině dotčených článků USP4 přes 0,008 mol/l (prokain-hydrochlorid v USP4) či 0,02 mol/l (prokain-hydrochlorid v Ph. Int.2) až po koncentrace řádově vyšší. Rovněž v publikovaných experimentálních pracích zabývajících se zčásti či výhradně diazotační titrací léčiv lze nalézt koncentrace KBr v roztoku k titraci řádově rozdílné. Ve starších pracích, např.11, 13–15, 30 podobně jako v některých novějších 21, 23, 24, 27, 28, KBr součástí reakčního prostředí nebyl, autoři12 při titraci sulfanilamidu použili ke katalýze jen několik krystalů KBr, v práci26 byla koncentrace KBr 0,03 mol/l, autoři16 použili koncentraci NaBr v roztoku k titraci 0,4 mol/l. Při titraci p-fenetidinu po hydrolýze fenacetinu se osvědčil přídavek KBr 0,4 mol/l a bez použití katalýzy KBr nebylo možné vyhodnotit konečný bod potenciometrické titrace17. Pro mikrotitrace sulfonamidů používali autoři20 KBr v koncentraci okolo 2 mol/l. Optimalizační experimenty22 při analýze v běžném měřítku ukázaly, že pro titraci sulfonamidů postačí při koncentraci HCl 0,6 mol/l koncentrace KBr 0,2 mol/l (1 g/50 ml). Se zohledněním výše uvedených skutečností se jeví koncentrace HCl v roztoku k titraci podle Ph. Eur.1 2 mol/l jako hodnota, kterou v rámcovém postupu není nutné měnit. Z obsahu lékopisů a experimentálních prací lze současně předpokládat, že ve většině případů, zejména při současném použití bromidu, by stačila koncentrace HCl poloviční, tedy 1 mol/l. Přídavek bromidu by měl v rámcovém postupu Ph. Eur. a v jeho článcích určitě zůstat, mohl by však být snížen na 1 g s tím, že účinnost přídavku 0,1 g KBr podle některých článků sledovaných lékopisů (Ph. Int., USP) by stála za ověření u dalších léčiv. Obsah některých článků sledovaných lékopisů (např. JP)6 naznačuje, že katalýza KBr umožňuje snížit koncentraci HCl v roztoku k titraci a v nepřítomnosti KBr jsou používané koncentrace HCl násobně vyšší (řada článků v USP)4. Tento předpoklad by zasluhoval ověření vzhledem k tomu, že i v publikovaných experimentálních pracích byly vysoké koncentrace HCl v roztoku k titraci zejména v případech, kdy KBr součástí pracovního postupu nebyl 13, 19, 24, 30, 32. Z ekonomického a ekologického pohledu není výhodné používat v analytických postupech větší množství chemikálií, než je prokazatelně nutné.
Teplota roztoku před titrací a v jejím průběhu
Pravděpodobně první významná analyticky zaměřená experimentální práce se zabývala stanovením jednoduchých aromatických aminů, jako je anilin, m-xylidin a tolidin, se závěrem, že titrace při teplotě 60 °C vede k chybě až 3%, při 30 °C, 0,5% a při 20 °C, resp. při pokojové teplotě, jsou výsledky přesné9. Tato práce byla pravděpodobně důvodem k chlazení roztoku před titrací či i v jejím průběhu autory některých dalších publikací, včetně prací zabývajících se částečně nebo výhradně léčivy bez ověření, zda je chlazení potřebné. Autoři těchto prací před titrací a někdy i v průběhu titrace chladili roztok na teplotu ≤ 10 °C11, 13, 27 nebo dokonce na ≤ 5 °C12, 19, 24. Jiní16, 30–32 prováděli titraci při 15–20 °C, tedy s chlazením jen mírným, přestože nejde o přípravu diazoniové soli rozkládající se vyššími teplotami, ale o zjištění nadbytku dusitanu30, 32, přičemž vyšší teplota zvyšuje reakční rychlost a tím zkracuje dobu analýzy26, 36. Práce požadující chlazení roztoku ale v odborném písemnictví nepřevažují. Většina autorů zabývajících se problematikou diazotačních titrací léčiv chlazení roztoku před titrací k získání adekvátních výsledků nepotřebovala 14, 15, 17, 20–23, 26, 28, 36, 37. Autoři30 při zjišťování optimálních podmínek stanovení potvrdili názor, že chlazení titrovaného roztoku ledem, doporučované jinými autory, je zbytečné; totéž soudí32. Autoři14 konstatují, že jejich výsledky nepotvrdily potřebu ledu v titrační směsi. Práce porovnávající výsledky stanovení léčiv diazotační titrací bez chlazení a s chlazením ale nejsou k dispozici a existují dokonce publikace upozorňující na výhodnost vyšší teploty titrovaného roztoku (např.15, 36). Tradičně konzervativní lékopisy ale zjevně přikládají větší váhu první skupině prací. Ze sledovaných lékopisů všechny, které mají rámcový postup, požadují chlazení roztoku před titrací už
v nich, a to na asi 15 °C 2, 4, 7, 8, nebo ve vodě s ledem, tedy ještě důraznější 1, 3. Požadavek Ph. Eur.1 na chlazení ve vodě s ledem byl nastolen v rámcové stati už v prvním vydání Evropského lékopisu z roku 196938, v jeho dalším vydání z roku 198039 byl nahrazen požadavkem na chlazení v případě potřeby, není-li v monografii předepsáno jinak, ale od třetího vydání 40 je znovu požadováno už v rámcovém postupu, tedy plošně chlazení ve vodě s ledem. Chlazení je požadováno odkazem na rámcovou stať nebo údajem přímo v monografii téměř ve všech dotčených monografiích sledovaných lékopisů. Vzhledem k poznatkům z publikovaných experimentálních prací a v rámci snahy o zjednodušení analytického postupu lze přesto považovat za výhodné řešení vrátit se v novém Ph. Eur. k přístupu Ph. Eur. 239 a požadavek na chlazení ve vodě s ledem z rámcové stati vypustit s tím, že se pracuje při běžné laboratorní teplotě, pokud není v monografii uvedeno jinak. Toto řešení bylo předepsáno také v lékopisu bývalé NDR29 a je pojistkou pro případ, že zvýšená teplota při titraci některého léčiva vyvolá nežádoucí reakci ovlivňující průběh a výsledek analýzy. Autoři36 zmiňují v této souvislosti jako příklad dekarboxylaci kyseliny p-aminosalicylové. Podle znění monografií na natrium-aminosalicylát dihydrát v Ph. Eur.1 a v BP3, které chlazení při analýze tohoto léčiva nepožadují, by však nemělo jít o příklad aktuální. Struktura analyzovaného aminu je však při diazotačních titracích jedním z významných faktorů, se kterým souvisí mimo jiné poměrně velké rozdíly v reakčních rychlostech nitrosace36. Proto by bylo vhodné při revizi monografií Ph. Eur., v nichž se diazotační titrace uplatňuje, porovnávat průběh titrace a výsledky stanovení získané za běžné laboratorní teploty a při teplotě snížené. Do doby revize monografií lze nahradit v rámci předběžné opatrnosti požadavek na chlazení ve vodě s ledem požadavkem na titraci při teplotě nepřevyšující 25 °C, což je teplota uvedená ve studii36 jako bezpečná.
Závěr
Stanovení obsahu léčiv s aromatickou aminoskupinou titrací roztokem dusitanu sodného za instrumentální indikace konečného bodu není v Ph. Eur.1 využíváno tak často jako některé jiné odměrné metody. Přesto zasluhuje text 2.5.8. Ph. Eur. 111, který se obsahem shoduje s textem v Ph. Eur. 1 z roku 196938, revizi. V první řadě je třeba specifikovat, která z elektrometrických metod má být k indikaci konečného bodu diazotačních titrací v Ph. Eur. použita. Měla by to být potenciometrie s platinovou indikační elektrodou a kalomelovou nebo jinou vhodnou porovnávací elektrodou. Množství bromidu v roztoku k titraci je možné snížit na 1,0 g. Ochlazení roztoku před titrací, na jehož potřebnost není v publikovaných experimentálních pracích jednotný názor, z rámcového postupu vypustit a předepsat až v jednotlivých článcích, pokud bude u některých léčiv k získání výsledků stanovení jejich obsahu v požadované kvalitě průkazně potřebné. Lze také zvážit využití diazotační titrace ke stanovení obsahu dalších léčiv s primární aromatickou aminoskupinou uvedených v Ph. Eur.1), jako jsou bromhexin-hydrochlorid, metoklopramid a metoklopramid-hydrochlorid. Publikace41) naznačuje, že diazotační titrace mohou být v lékopisné kontrole jakosti léčiv aplikovány i mimo oblast jejich původního využití. V případě budoucího uplatnění této či jiné obdobné možnosti v Ph. Eur. by bylo nutné název stati 2.5.8. změnit.
Střet zájmů: žádný.
Sources
- Ph. Eur. 11th ed. 2022. https://www.edqm.eu/en/ european-pharmacopoeia-ph.-eur.-11th-edition#%7B%22468819%22 (24. 2. 2023).
- The International Pharmacopoeia, 11th ed. Geneva: WHO 2022. https://digicollections.net/phint/2022/index.html#p/home (2.4.2023).
- British Pharmacopoeia 2022, Vol. I–V. London: The Stationery Office. https://www.webofpharma.com/2022/06/ british-pharmacopoeia-2022-bp-2022-pdf.html (28. 1.2023).
- The United States Pharmacopeia 43 – The National Formulary 38, Volume 1–5, Baltimore: United Book Press, 2020. https://www.webofpharma.com/2022/01/usp-2021-united-state-pharmacopeia-44.html (28. 1. 2023).
- Československý lékopis, 4. vydání, svazek I. Praha: Avicenum 1987; 78.
- The Japanese Pharmacopoeia, 18th ed., English Version, The Ministry of Health, Labour and Welfare, 2021. https:// www.mhlw.go.jp › content (28. 1. 2023).
- Indian Pharmacopoeia, 8th ed., Volume I–III, Ghaziabad: The Indian Pharmacopoeia Commission 2018. https:// www.webofpharma.com/2022/04/indian-pharmacopo eia-2018-ip-2018-pdf.html (28. 1. 2023).
- Brazilian Pharmacopoeia, 6th ed., Volume I, MG5.3.3-00, Brasilia: Anvisa 2019. http://portal.anvisa.gov.br (28. 1.2023).
- Müller E., Dachselt E. Die potentiometrische Indikation der Diazotierung und quantitative Bestimmung von Aminen. Z. Elektrochem. 1925; 31, 662–666.
- Atanasiu J. A., Velculescu A. I. Potentiometrische Bestimmung von Benzidin durch Diazotierung. Ber. 1932; 65, 1080–1082.
- Singh B., Ahmed G. Potentiometric studies in diazotisation determination of aromatic amines. J. Indian Chem. Soc. 1938; 15, 416–420.
- Towne R. W., Hitchens R. M. Method of analysis for sulfanilamide. J. Am. Pharm. Assoc. 1939; 28, 585–588. https://doi.org/10.1002/jps.3080280904 (3. 2. 2023).
- Saeki T. Studies on quantitative analysis of aromatic amines by potentiometric titration. Yakugaku Zasshi 1950; 70, 660–668. https://doi.org/10.1248/yakushi1947.70.11_660 (27. 1. 2023).
- Larocca J. P., Waters, K. L. The potentiometric titration of the sulfa drugs. J. Am. Pharm. Assoc. Sci. Ed. 1950; 39, 521–523.
- Dušinský G. Potenciometrické stanovenie fenacetínu. Chem. Zvesti 1952; 6, 201–208.
- Butt L. T., Stagg H. E. The automatic titration of primary aromatic amines with nitrous acid. Anal. Chim. Acta 1958; 19, 208–215. https://doi.org/10.1016/S0003-2670(00)88144-1 (28. 1. 2023).
- Baldinus J. G., Rothberg I. The determination of acetophenetidin in tablet mixtures: A potentiometric method. J. Am. Pharm. Assoc. Sci. Ed. 1959; 48, 318–319. https://doi.org/10.1002/jps.3030480606 (7. 2. 2023).
- Čihalík J. Potenciometrie. Praha: Nakladatelství Československé akademie věd 1961; 683.
- Ueno K., Tachikawa T. Potentiometric titration of sulfanylamide with sodium nitrite. Japan Analyst 1962; 11, 554–558.
- Coenegracht P. M. J., Franke J. P., Metting, H. J. The automatic amperometric and potentiometric microtitration of pharmaceutically important sulfanilamide derivatives by diazotization with nitrite. Anal. Chim. Acta 1973; 65, 375–384.
- Badwan A. A., Jawan O. A., Owais L. Metoclopramide determination by amperometric and potentiometric titrations – application to some pharmaceutical preparations. Int. J. Pharm. 1986; 28, 41–46. https://doi.org/10.1016/0378-5173(86)90145-6 (7. 2. 2023).
- Šubert J. Příspěvky k analytice léčiv. VI. Studium podmínek pro diazotační titrace léčiv za potenciometrické indikace a standardizaci odměrného dusitanu sodného. Farm. Obzor 1981; 50, 273–278.
- Devi O. Z., Basavaiah K., Vinay K. B., Revanasiddappa H. D. Determination of metoclopramide hydrochloride in pharmaceuticals and spiked human urine through diazotization reaction. J. Food Drug Anal. 2012; 20, 4. https://doi.org/10.6227/jfda.2012200204 (7. 2. 2023).
- Zawada E., Pirianowicz-Chaber E., Somogi A., Pawinski T. Development and validation of bromatometric, diazotization and VIS-spectrophotometric methods for the determination of mesalazine in pharmaceutical formulation. Acta Pol. Pharm. 2017; 74, 401–404.
- Metrohm A. G.; Herisau. Nitrite titration according to USP general chapter <451>. Titration Application Note T-194 (2018). https://www.metrohm.com/en/applications/appli-cation-notes/aa-t-001-100/an-t-194.html (7. 2. 2023).
- Scholten H. G., Stone K. G. Determination of primary aromatic amines by diazotization using the dead-stop end point. Anal. Chem. 1952; 24, 749–750.
- Mohamed M. E., Abounassif M. A., Kandil H. A., Aboul-Enein H. Y. Biamperometric and differential pulse polarographic methods for the assay of nomifensine maleate. Anal. Lett. 1988; 21, 241–251.
- Arafat T. Bromhexine determination by diazotization using potentiometric titration: application to content uniformity. Anal. Lett. 1990; 23, 311–326.
- Arzneibuch der Deutschen Demokratischen Republik: AB-DDR 87. Berlin: Akademie-Verlag 1975–1987; VII,12.0.1. http://www.digibib.tu-bs.de/?docid=00000955(24. 2. 2019).
- Kucharský J., Erben J., Mikule V. Elektrometrická titrace sulfonamidů. Českoslov. Farm. 1954; 3, 284–285.
- Špinková V., Černý J. Jednoduché stanovení některých méně běžných sulfonamidů – 4-aminobenzensulfothiocarbamidu 4-aminomethylbenzensulfonamidu (Marbadal-Bayer) a směsi s 2-(4´-aminobenzensulfon amido)-4-methylpyrimidinem (Supronal-Bayer). Českoslov. Farm. 1958; 7, 591–593.
- Hrdý O., Jindra A., Jung Z., Šlouf A., Zýka J. Kvantitativní analysa léčiv. Praha: Státní zdravotnické nakladatelství 1957; 477.
- Portych J., Děťák J., Mareček Š., Lehký M. Základy farmaceutickej analýzy. Martin: Vydavateľstvo Osveta 1978, 181, 488.
- Bezáková Ž. Analýza chemických liečiv. Nitra: VA Print 2000; 128, 129.
- Connors K. A. Reaction Mechanisms in Organic Analytical Chemistry. New York: John Wiley 1973; 236–238.
- Matrka M., Pípalová J. K problematice potenciometrických titrací aromatických aminů dusitanem. Chem. Prům. 1973; 23, 149–152.
- Ågren A. Halbestämning av sulfonamider. Svensk Farm. Tidskr. 1951; 55, 229–238.
- Ph. Eur. 1st ed. 1969. Online: https://pheur.edqm.eu/app/ arch/content/arch-0/1969_1st_Edition_Volume_I_E.pdf (27. 3. 2023).
- Ph. Eur. 2nd ed. 1980. Online: https://pheur.edqm.eu/app/ arch/content/arch-0/1980_2nd_Edition_Part_I_E.pdf (27. 3. 2023).
- Ph. Eur. 3rd ed. 1996. Online: https://pheur.edqm.eu/app/ arch/content/arch-0/1997_3rd_Edition_E.pdf (27. 3.2023).
- Kumara A., Singhb V., Kumarc P. Quantitative estimation of eflornithine by nitrite (diazotization) titration. Int. J. Pharm. Sci. 2016; 2, 12–14. https://www.metfop.edu.in/wp-content/uploads/2023/02/76836-paper-3.pdf (16. 3. 2023).
Labels
Pharmacy Clinical pharmacology
Article was published inCzech and Slovak Pharmacy

2023 Issue 4-
All articles in this issue
- Celkové intravenózne anestetiká – farmakodynamika, farmakokinetika a chirálne vlastnosti
- Diazotační titrace v lékopisné kontrole jakosti léčiv a návrhy pro jejich revizi v Evropském lékopisu*
- Vliv digoxinu, valproátu sodného a celekoxibu na mozkovou cyklooxygenázovou dráhu a neuron-specifickou enolázu při pentylenetetrazolem podnícené záchvaty u myší
- Studium protizánětlivých vlastností hustého extraktu Tribulus terrestris L.
- Syntéza, charakterizace, studie molekulárního dokování nových alkylových derivátů 5-(2-brom-4-fluorfenyl)-4-ethyl- 4H-1,2,4-triazol-3-thiolu
- Czech and Slovak Pharmacy
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Celkové intravenózne anestetiká – farmakodynamika, farmakokinetika a chirálne vlastnosti
- Studium protizánětlivých vlastností hustého extraktu Tribulus terrestris L.
- Vliv digoxinu, valproátu sodného a celekoxibu na mozkovou cyklooxygenázovou dráhu a neuron-specifickou enolázu při pentylenetetrazolem podnícené záchvaty u myší
- Diazotační titrace v lékopisné kontrole jakosti léčiv a návrhy pro jejich revizi v Evropském lékopisu*
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

