-
Medical journals
- Career
Dvoudobý nízkoprůtokový a vysokoprůtokový EC-IC bypass v prevenci ischemie při obětování vnitřní karotidy u intrakavernózního aneuryzmatu
Authors: V. Přibáň; J. Dostál; I. Holečková; J. Mraček
Authors‘ workplace: Neurochirurgická klinika LF UK a FN Plzeň
Published in: Cesk Slov Neurol N 2020; 83/116(5): 563-565
Category: Letter to Editor
doi: https://doi.org/10.14735/amcsnn2020563Vážená redakce,
mozková aneuryzmata (AN) jsou dominantně ošetřována mikrochirurgicky klipem nebo endovaskulárně pomocí koilů. S nárůstem velikosti a komplexnosti tvaru se ošetření aneuryzmatu stává výzvou. U těchto mnohdy gigantických výdutí v povodí vnitřní karotidy (internal carotid artery; ICA) je metodou volby ošetření flowdiverterem. Není-li použití z technických důvodů možné, přichází v úvahu obětování ICA. Tato technika, nazývaná Hunterská ligatura, je však spojena s riziky. Nebezpečí následné teritoriální ischemie v povodí uzavřené ICA je vysoké a dosahuje až 49 % [1]. Významná je i změna hemodynamických poměrů s rizikem de novo vzniku aneuryzmat, popřípadě růstu již existujících.
K vyloučení těchto rizik vedou dvě cesty, obě s využitím bypassu: univerzální revaskularizace a selektivní revaskularizace. Při univerzálním přístupu se před obětováním ICA našije bypass vždy. Riziko perioperačních komplikací, vč. ischemických, není zanedbatelné. Při selektivním přístupu se provádí balon okluzní test (BTO). Ten posoudí riziko ischemie v důsledku okluze tepny. Nabízí se široké portfolio vyšetřovacích technik: vyšetření v normotenzi s následnou hypotenzí, navazující SPECT nebo perfuzní CT, posouzení zpoždění venózní fáze na DSA, určení tlaků ve střední mozkové tepně (middle cerebral artery; MCA) peroperačně atp. Senzitivita vyšetření dosahuje 80 % [2]. Invazivita BTO může ale přinášet komplikace, např. disekci ICA. Na naší klinice využíváme BTO v normotenzi a hypotenzi s hodnocením klinického stavu pacienta. Vyšetření trvá 2× 20 min a hypotenze značí dvě třetiny tlaku v normotenzi [1].
Pacientka (59 let) byla přijata pro 3 dny trvající bolesti hlavy a dezorientaci. CT prokázala subarachnoidální krvácení. Klinický stav a grafický nález subarachnoidálního krvácení byl příznivý: Hunt-Hess skóre 2, Fisher 3. CTA a následná DSA zobrazila gigantické intrakavernózní karotické aneuryzma vpravo. Další neprasklé aneuryzma velikosti 3 mm bylo na přední komunikující tepně (A-comm) (obr. 1).
Image 1. DSA 3D snímek gigantického intrakavernózního aneuryzmatu pravé karotidy.
Fig. 1. 3D DSA of right giant intracavernous internal carotid artery aneurysm. Arrow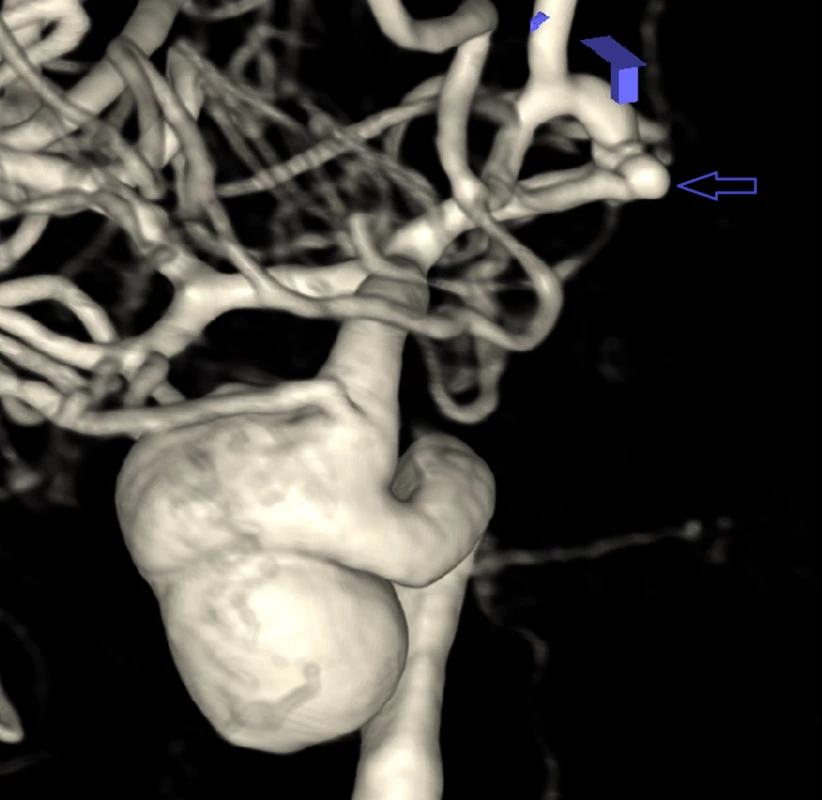
Modrá značka ukazuje incidentální aneuryzma přední komunikanty.
Arrow show concomitant incidental A-comm aneurysm.Intervenční radiologové kontraindikovali po diskuzi na národní i mezinárodní úrovni použití stentu/flowdiverteru. Důvodem byl významně rozdílný průsvit ICA ve vtoku a výtoku z výdutě. Pro posouzení bezpečné možnosti obětování ICA byl proveden balon okluzní test, který však pacientka netolerovala. Po 2 min uzávěru v normotenzi došlo k plegii levé horní končetiny.
Byl proto indikován high-flow bypass pomocí štěpu radiální arterie mezi zevní karotidou a dolní větví M2 střední mozkové tepny (ECA-M2t). Z důvodu zajištění bazální perfuze po dobu uzávěru MCA byl nejprve našit low-flow bypass mezi větví a. temporalis superficialis a kortikální větví MCA (STA-M4) (obr. 2).
Image 2. Low-flow bypass mezi větví a. temporalis superficialis a kortikální větví střední mozkové tepny v teritoriu pravé karotidy.
a) peroperační foto – donorem je parietální větev a. temporalis superficialis, recipientem korová, temporálně uložená a. angularis (M4)
b) průkaz průtoku bypassem na DSA
c) kapilární fáze průtoku bypassem
Fig. 2. Low-flow superficial temporal artery to middle cerebral artery bypass in right internal carotid artery territory.
a) superficial temporal artery parietal branch as donor and cortical temporally located angular artery (M4) as recipient are in intraoperative photo
b) bypass flow on DSA
c) bypass flow in capillary phase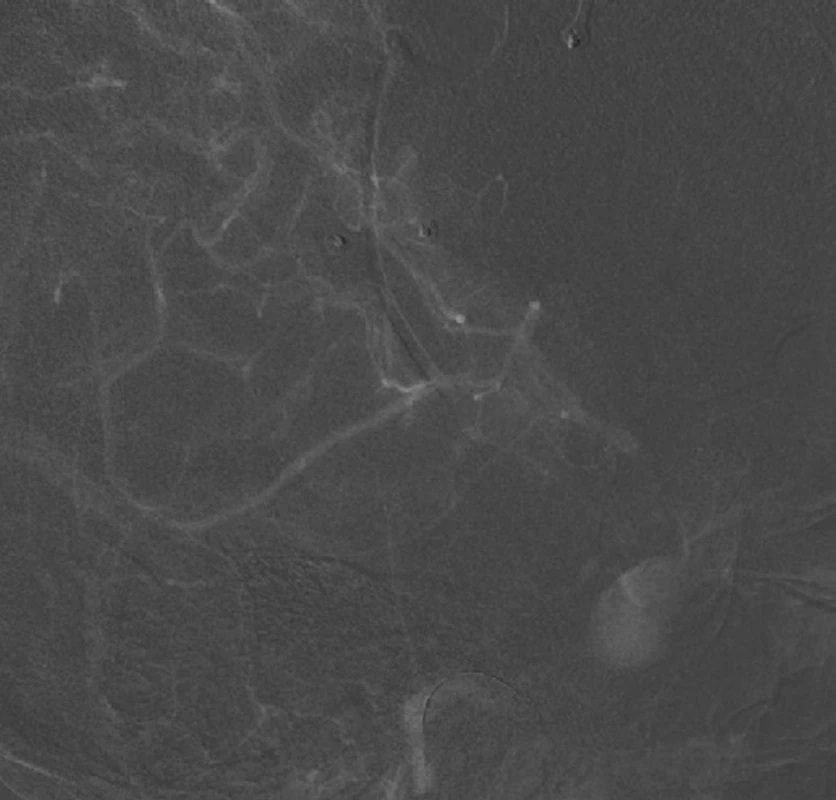
Den po operaci byl opakován BTO, který byl negativní. V odstupu 2 dní proběhla další operace: zaklipování aneuryzmatu A-com a high-flow ECA-M2(t) bypass vpravo s radiálním štěpem. Po ověření průchodnosti štěpu flowmetrem (průtok krevní 77 ml/min) byla uzavřena ICA na krku a za odstupem a. ophthalmica.
Došlo tím k vyřazení výdutě z cirkulace (trapping) a zároveň k zajištění perfuze ipsilaterální hemisféry vysokoprůtokovým štěpem. Pacientka byla před výkonem upozorněna na riziko slepoty v důsledku uzavření průtoku v a. ophthalmica. To se literárně pohybuje v jednotkách procent. Pacientka riziko akceptovala. Ke zhoršení vizu po operaci však nedošlo. Během operace byla indukována mírná hypotermie a farmakologicky snížena metabolická potřeba mozku (burst supression). Po dobu operace probíhala monitorace evokovaných potenciálů (obr. 3).
Image 3. (a) High-flow bypass ECA-M2(t) na DSA. (b). Kapilární fáze průtoků bypassem.
Fig. 3. (a) High-flow ECA-M2(t) bypass on DSA. (b) Bypass flow in capillary phase on DSA.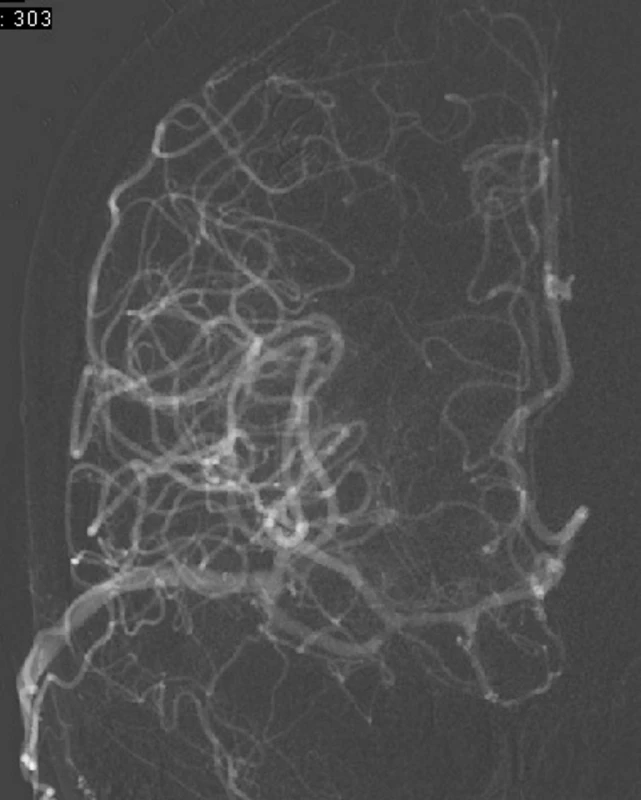
Pooperační průběh byl nekomplikovaný. Průtok bypassem na DSA byl dobrý, CT perfuze bez patologie. Na časné MR nebyla přítomna ischemie v teritoriu MCA. Průtok štěpem na MRA v odstupu týdne dosáhl 180 ml/min, tedy více než dvojnásobek peroperačního nálezu. Příznivý klinický stav trvá 6 měsíců po operaci.
Logika protektivního STA-M4 bypassu před našitím high-flow bypassu je zřejmá: zajistit bazální perfuzi hemisféry po kritickou dobu okluze velké recipientní tepny (obvykle M2 nebo M1) a snížit riziko teritoriální iatrogenní ischemie. Přesto je užití této techniky výjimečné [2,3]. Na rozdíl od obou autorů jsme bypassy provedli ve dvou separátních výkonech. Nabízí se otázka, zda při negativním BTO nebyl low-flow bypass dostačující, a tudíž následný výkon rizikem pro pacientku. Věk pacientky s potenciálem dožití nad 20 let a obava z možného pozdního ischemického deficitu nás vedla k radikální augmentaci průtoku a našití vysokoprůtokového bypassu. Jasné doporučení postupu v technice revaskularizace při obětování ICA neexistuje. Sia et al upozorňují na riziko deficitu při dočasném uzávěru magistrální tepny. Zdůrazňují vyšší pravděpodobnost rizika ischemie s nárůstem délky trvání sutury anastomózy [4]. Nussbaum et al jsou zastánci selektivní revaskularizace. BTO hodnotí klinicky a graficky (perfuzní CT/SPECT). Pacienti s pozitivním klinickým BTO postupují paušální high-flow bypass stejně tak jako pacienti s pozitivním grafickým testem do 40 let. U starších a polymorbidních se pak spokojí s low-flow bypassem. Ten provádí i u pacientů s negativním BTO do 65 let. Dosáhl tak morbidity/mortality u high-flow bypassu 9,6 % a u low-flow bypassu 2,4 % [5]. Matsukawa et al užívají low-flow bypass před našitím high-flow bypassu jako protekci ischemie a dále k monitoraci tlaku v MCA během výkonu. Tím dosahují snížení peroperačních ischemických komplikací a zároveň volby adekvátního graftu [6]. Cherian et al doporučují techniku využití obou větví STA (tzv. double barrel bypass). Tvrdí, že tak lze dosáhnout významného a mnohdy dostatečného navýšení průtoku [7]. Významnou pomoc při rozhodování o typu bypassu může přinést flowmetrie. Pokud rozdíl průtoku před uzávěrem a po uzávěru ICA v MCA odpovídá průtoku v STA a není zásadně vyšší, pak je potenciálně „low-flow“ STA-M4 bypass suficientní při náhradě toku obětovanou ICA a lze jej využít [8]. Přínosem v této rozvaze by jistě bylo předoperační vyšetření hemodynamiky pomocí MR NOVA. Vzhledem k akutnímu stavu pacientky však nebylo provedeno. Technickou odpovědí na rizika dočasného uzávěru magistrálních tepen po dobu šití anastomózy se zdála po určitou dobu být neokluzivní technika pomocí excimer-laseru ELANA (Utrecht, Nizozemsko). Nicméně morbidita/mortalita a četnost ischemických komplikací se neliší od vysokoprůtokových bypassů provedených konvenční technikou [9].
Potenciální rizika námi zvolené techniky jsou dvojího rázu. Za prvé je provedení protektivního bypassu spojeno s prodloužením celkové doby anestezie [10]. S délkou operace se zvyšuje riziko komplikací spojených s anestezií. Za druhé je riziko uzávěru nízkoprůtokového bypassu při kompetici toku s dosud otevřeným průtokem v ICA. U naší pacientky byl low-flow bypass průchodný a splnil svůj „úkol“ protektivní perfuze hemisféry po dobu uzávěru magistrální tepny M2 při šití high-flow bypassu. Domníváme se, že výhody protektivního low-flow bypassu převažují nad výše zmíněnými riziky. V případě selhání high-flow bypassu může být jeho význam pro pooperační klinický stav klíčový. Autoři prezentují první publikaci kombinovaného low-flow a high-flow bypassu při obětování vnitřní karotidy v českém písemnictví.
Grantová podpora
Práce byla podpořena MZ ČR – RVO (Fakultní nemocnice Plzeň – FNPl, 00669806).
Konflikt zájmů
Autoři deklarují, že v souvislosti s předmětem studie nemají žádný konflikt zájmů.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manu script met the ICMJE “uniform requirements” for biomedical papers.
doc. MUDr. Vladimír Přibáň, Ph.D.
Neurochirurgická klinika LF UK a FN Plzeň
alej Svobody 80
304 60 Plzeň
e-mail: pribanv@fnplzen.cz
Přijato k recenzi: 11. 9. 2019
Přijato do tisku: 27. 8. 2020
Sources
1. Standard SC, Ahuja A, Guterman LF et al. Balloon test occlusion of the internal carotid artery with hypotensive challenge. AJNR Am J Neuroradiol 1995; 16 (7): 1453–1458.
2. Matsukawa H, Miyata S, Toshiyuki T et al. Rationale for graft selection in patients with complex internal carotid aneurysms treated with extracranial to intracranial high-flow bypass and therapeutic internal carotid artery occlusion. J Neurosurg 2018; 128 (6): 1753–1761. doi: 10.3171/2016.11.JNS161986.
3. Abouakais R, Verbraeken B, Leclerc X et al. Protective STA-MCA bypass to prevent brain ischemia during high-flow bypass surgery: case series of 10 patients. Acta Neurochir 2019; 161 (6): 1207–1214. doi: 10.1007/s00 701-019-03906-4.
4. Sia SF, Lai L, Morgan MK. Measuring competence development for performing high flow extracranial-to-intracranial bypass. J Clin Neurosci 2013; 20 (8): 1083–1088. doi: 10.1016/j.jocn.2012.10.019.
5. Nussbaum ES, Kallmes MA, Lassig JP et al. Cerebral revascularization for the management of complex intracranial aneurysms: a single-center experience. J Neurosurg 2018; 1 : 1–11. doi: 10.3171/2018.4.JNS172752.
6.Matsukawa K, Tanikawa R, Kamiyama H et al. Risk factors for low-flow related ischemic complications and neurological worsening in patients with complex internal carotid artery aneurysms treated by EC-IC high-flow bypass. World Neurosurg 2016; 85 : 49–55. doi: 10.1016/j.wneu.2015.09.095.
7. Cherian J, Srinivasan V, Kan P et al. Double-barrel superficial temporal artery bypass: ca nit be considered „high-flow?“ Oper Neurosurg 2018; 18 : 288–294. doi: 10.1093/ons/opx119.
8. Amin-Hanjani S, Alaraj A, Charbel FT. Flow replacement bypass for aneurysms: decision-making using intraoperative blood flow measurement. Acta neurochir 2010; 152 (6): 1021–1032. doi: 10.1007/s00701-010-0635-
9. Vajkoczy P, Korja M, Czabanka M et al. Experience in using the excimer laser-assisted nonocclusive anastomosis bypass technique for high-flow revascularization: Mannheim-Helsinki series of 64 patients. Neurosurgery 2012; 70 (1): 49–54. doi: 10.1227/NEU.0b013e31822cb979.
10. Kim BD, Ver Halen JP, Grant DW et al. Anesthesia duration as an independent risk factor for postoperative complications in free flap surgery: a review of 1,305 surgical cases. J Reconstr Microsurg 2014; 30 (4): 217–226. doi: 10.1055/s-0033-1358382.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2020 Issue 5-
All articles in this issue
- Difuzní nízkostupňové gliomy
- Dechová rehabilitace u pacientů s amyotrofickou laterální sklerózou
- Socioekonomické dopady bolestí hlavy – příčiny a možnosti ovlivnění
- Neurorehabilitácia u pacientov s amyotrofickou laterálnou sklerózou
- Chirurgická liečba degeneratívnej skoliózy
- Funkční a strukturální změny na kortikální úrovni u pacientů s nespecifickými bolestmi zad v bederním úseku páteře
- Kognitivně-motorická interference po cévní mozkové příhodě
- Sonografické hodnocení nervus ischiadicus u jedinců s radikulární symptomatikou S1
- Taste strips – metoda samovyšetření chuti
- Účinnost mikrovaskulární dekomprese v porovnání s mikrovaskulární dekompresí s parciální senzorickou rhizotomií při klasické neuralgii trojklanného nervu – retrospektivní analýza 58 pacientů
- Pacient s Parkinsonovou nemocí v datových zdrojích Národního zdravotnického informačního systému
- Léčba intravenózní trombolýzou mimo iktové centrum
- Dekompresivní kraniektomie u maligního hemisferálního infarktu – monoinstitucionální retrospektivní analýza souboru 33 pacientů
- Dvoudobý nízkoprůtokový a vysokoprůtokový EC-IC bypass v prevenci ischemie při obětování vnitřní karotidy u intrakavernózního aneuryzmatu
- Stentování durálních splavů u idiopatické intrakraniální hypertenze
- Syndrom reverzibilní encefalopatie v zadní cirkulaci ve spojitosti s meningitidou vyvolanou Neisseria elongata
- Hyperbarická oxygenoterapie & mozek; přehled z výroční konference EUBS 2019
- Test Amnesia Light and Brief Assessment (ALBA) – druhá verze a opakovaná vyšetření
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Difuzní nízkostupňové gliomy
- Dechová rehabilitace u pacientů s amyotrofickou laterální sklerózou
- Test Amnesia Light and Brief Assessment (ALBA) – druhá verze a opakovaná vyšetření
- Neurorehabilitácia u pacientov s amyotrofickou laterálnou sklerózou
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career




