-
Medical journals
- Career
Posturálna instabilita, poruchy chôdze a pády pri Parkinsonovej chorobe
Authors: P. Valkovič1ihash2 ,2 ,3
Authors‘ workplace: II. neurologická klinika LF UK a UN Bratislava, Nemocnica akad. L. Dérera 1; Laboratórium regulácie motoriky, Ústav normálnej a patologickej fyziológie SAV, Bratislava 2; Oddelenie fyziatrie a liečebnej rehabilitácie, Falck Healthcare, a. s., Bratislava 3
Published in: Cesk Slov Neurol N 2012; 75/108(2): 141-151
Category: Minimonography
Overview
Posturálna instabilita (PI) je kardinálnym príznakom Parkinsonovej choroby (PCH) a stúpa na význame s progresiou ochorenia. Najvážnejším následkom PI sú rekurentné pády, ktoré extrémne zhoršujú kvalitu života pacientov a svojimi komplikáciami zaťažujú zdravotnícky systém. Väčšina pádov u pacientov s PCH vzniká v domácom prostredí a v stave dobrej pohyblivosti. Na detekciu začínajúcej a monitoring signifikantnej PI je potrebná cielená anamnéza a špecifické klinické neurologické vyšetrenie. Farmakoterapia má len obmedzený účinok, sľubné sa ukazujú najmä preparáty pôsobiace na noradrenergný a cholínergný neurotransmiterový systém. V liečbe PI a prevencii pádov u PCH má najdôležitejšie postavenie kontinuálna a „na mieru ušitá“ fyzioterapia.
Kľúčové slová:
posturálna instabilita – Parkinsonova choroba – poruchy chôdze – pády – liečbaÚvod
Posturálna instabilita (PI) je kardinálnym príznakom v diagnostike parkinsonského syndrómu a Parkinsonovej choroby (PCH) [1]. Už v prvej monografii „o trasľavej obrne” James Parkinson zdôrazňoval, že pacient musí byť nadmerne opatrný, ak sa chce vyhnúť pádom („...the utmost care is necessary to prevent falls...“) [2]. Termín PI zahŕňa z klinického hľadiska nielen poruchu udržiavania postoja, ale aj problémy s chôdzou a následné pády, tiež poruchy otáčania sa (v ľahu, v sede, v stoji a pri chôdzi), ako aj poruchu zmeny jednotlivých pozícií (z ľahu do sedu, zo sedu do stoja, a naopak) [3]. Najvážnejším následkom PI je pád, resp. rekurentné (opakované) pády. Výskyt pádov je u pacientov s PCH najvyšší spomedzi najčastejších neurologických ochorení [4]. Z prospektívnych štúdií je známe, že takmer 70 % pacientov s PCH spadne aspoň raz počas jedného roka. Viac ako 50 % parkinsonikov padá za rok opakovane [5].
PI a pády patria medzi najviac negatívne faktory, ktoré znižujú celkovú kvalitu života pacientov s PCH [6,7]. Absolútny počet pádov nie je u pacientov s PCH korelátom PI. Pády sú najčastejšie v 3. štádiu podľa Hoehnovej a Yahra [8], teda v čase ešte pomerne dobre zachovanej mobility [5,9–11]. Závažnosť PI a pádov výstižne charakterizuje model „bludného kruhu“ (obr. 1) [10]. Spúšťačom sú mierne poruchy chôdze a pády. U pacientov s PCH vedú pády až v 35 % k zlomenine. Strach z ďalších pádov môže byť príčinou straty sebadôvery, čo môže viesť k obmedzeniu mobility. Dochádza k eliminácii aktivít mimo domácnosť, nasleduje redukcia presunov aj v rámci domácnosti a neúprosne sa vyvinie imobilizačný syndróm, ktorý prehlbuje osteoporózu, zhoršuje svalovú slabosť, kardiovaskulárnu kondíciu, komorbiditu (ktoré spätne ďalej zhoršujú posturálnu stabilitu) a sociálne izoluje pacienta. Pacient sa dostane do štádia tzv. malígnej PCH, ktorú charakterizuje progresívna redukcia kvality života, vysoké náklady na ošetrovateľskú starostlivosť, liečbu komplikácií pádov a zvýšená mortalita [3].
Image 1. Bludný kruh posturálnej instability. 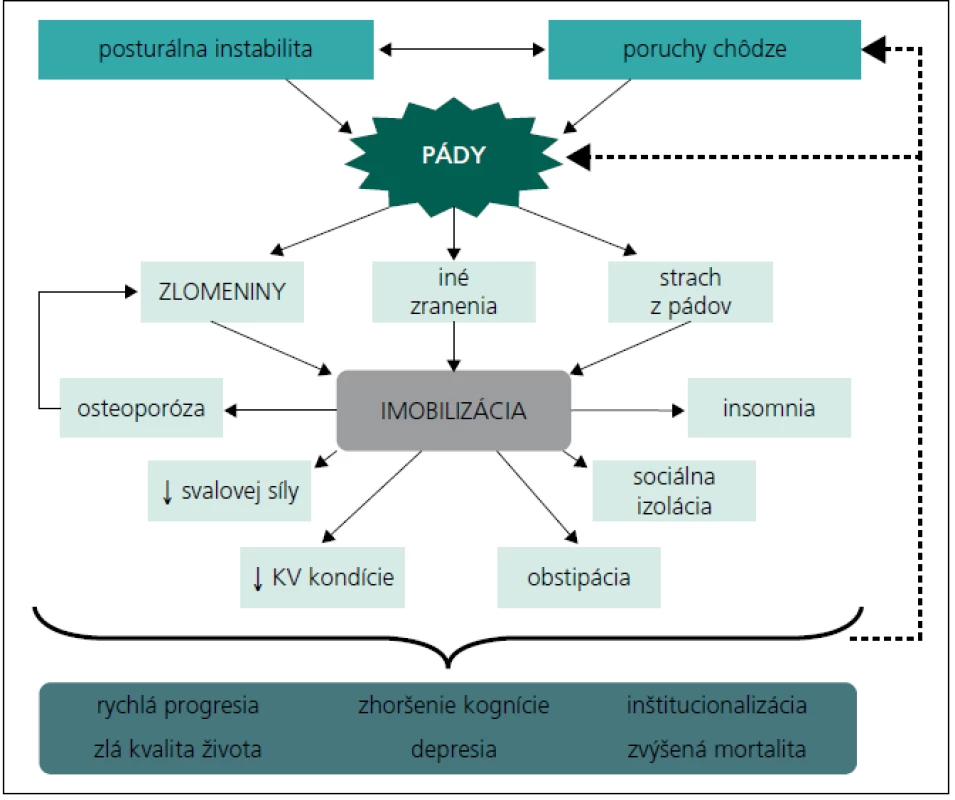
Komentár viď v texte. Upravené podľa [2,10]. Klinický obraz
Výrazná PI charakterizovaná jasnými poruchami chôdze, rovnováhy a rekurentnými pádmi postihuje pacientov s PCH až v pokročilom štádiu ochorenia (štádiá podľa Hoehnovej a Yahra 3–5). Rekurentné pády sa u PCH v priemere vyskytujú až po 7–10 rokoch ochorenia [2]. Včasný výskyt závažných porúch rovnováhy a pádov je indikátorom inej príčiny parkinsonizmu [12], v poradí:
- progresívna supranukleárna obrna (PSP),
- multisystémová atrofia (MSA),
- demencia s Lewyho telieskami (DLT) alebo vaskulárny parkinsonizmus (VP),
- kortikobazálna degenerácia (KBD).
Z klinického hľadiska je ale potrebné mať na zreteli, že existuje samostatný fenotyp idiopatickej PCH, najčastejšie u pacientov s neskorým začiatkom PCH (po 70. roku života), kde prevládajú v klinickej symptomatike akinéza a rigidita, je spravidla rýchlejšia progresia, takmer istý vývin kognitívnej dysfunkcie (až demencie) a ťažkosti s posturálnou instabilitou (tzv. Postural Instability-Gait Disorder – PIGD – subtype) [13].
Postoj
Na začiatku motorickej manifestácie PCH majú pacienti vo vzpriamenom postoji tendenciu k miernemu presunu ťažiska dozadu (ktorý nie je pre klinika markantný), čo sa s progresiou ochorenia systematicky mení. Postupne sa mimovoľne ťažisko tela presúva dopredu a dáva typický obraz zhrbeného parkinsonského postoja s flexiou krku, trupu, v lakťových kĺboch a kolenách [14]. Je zaujímavé, že ak sú títo pacienti požiadaní, aby zatvorili oči, možno pozorovať mierny presun váhy tela späť dozadu. Možno predpokladať, že aktívne využívajú zrakovú spätnú väzbu na udržiavanie postoja (v predklone), podobne ako zápasníci sumo, ktorý zaručuje prevenciu proti pádom dozadu [15]. Extrémny predklon hlavy (anterocollis), v porovnaní s ostatnými časťami tela, upozorňuje na možnosť alternatívnej diagnózy MSA. Retroflexia krku (retrocollis) sa v porovnaní s PCH zasa častejšie vyskytuje u pacientov s PSP. Laterálna deviácia trupu so skoliózou je typická pre pokročilé štádiá PCH, ale ťažká perzistujúca lateroflexia (tiež nazývaná Pisa syndróm alebo pleurothotonus), zvyčajne poukazujú na dystóniu pri užívaní neuroleptík, prítomnosť MSA alebo postencefalitický parkinsonizmus. Ako kamptokormia (z gréčtiny „kamptos“ = zhrbený, zohnutý a „kormos“ = trup) sa označuje výrazná anteflexia hrudno-driekovej chrbtice (30 a viac stupňov). Môže sa vyskytovať samostatne ako idiopatická, ale častejšie je asociovaná s inými príčinami, ako napr. užívaním liekov (napr. valproátu, neuroleptík), fokálnou myozitídou paraspinálneho svalstva, dystóniou a u viac ako 60 % prípadov práve s PCH [16]. Typické pre kamptokormiu ako takú je, že napriek extrémnemu predklonu trupu (ale nie krku) v stoji, alebo počas chôdze, tento úplne vymizne v ležiacej polohe. To odlišuje kamptokormiu od fixovanej kyfoskoliózy, ktorá sa takisto môže vyskytovať u pacientov s PCH [15].
Chôdza
Spočiatku sú poruchy chôdze spravidla diskrétne. Takáto chôdza je charakteristická asymetrickou redukciou súhybov (synkinéz) horných končatín a miernym predklonom. S progresiou sa chôdza stáva pomalšou, kroky sú kratšie, šúchavé, oporná báza sa zužuje. Synkinézy horných končatín obojstranne vymiznú, zmeny smeru napr. pri otáčaní (obchádzaní prekážok) pacient realizuje „en bloc“ [15]. Tento termín charakterizuje strnulé, kompaktné, vzájomné správanie sa segmentov tela pri obrátke (zmene smeru) – ako robot alebo človek v sadrovom korzete. Za fyziologických okolností sa u človeka pohybujú v smere predpokladanej zmeny chôdze najprv oči, nasleduje hlava, potom horná časť trupu a nakoniec panva [17]. V stave dobrej hybnosti je aj v tomto štádiu chôdza často relatívne istá, najmä vďaka spomaleniu a anteflexii. Avšak prítomnosť výrazných dyskinéz (vyvolaných dopaminergnou liečbou) môže pacienta veľmi destabilizovať a nezriedka viesť k pádu [15].
Porucha chôdze u pacientov s PCH môže taktiež vykazovať dva epizodické fenomény, ktoré sú čiastočne opozitami. Prvým je kinesia paradoxa. Ide o veľmi zriedkavý jav, charakterizovaný ako náhla, tranzientná, výborná pohyblivosť vrátane chôdze a behu u dovtedy veľmi zle mobilného pacienta, ktorá je spustená extrémnym emočným stresom v súvislosti s ohrozením samého pacienta alebo jeho blízkej osoby, prípadne silným pozitívnym emočným podnetom [18].
Druhým, oveľa častejším fenoménom je tzv. zamrznutie chôdze – freezing (alebo motorický blok), pri ktorom pacient nie je schopný začať lokomóciu, alebo v nej pokračovať. Freezing veľmi ohrozuje rovnováhu a je jedným z najčastejších mechanizmov pádov pri PCH [19]. Klinicky je freezing definovaný ako „epizodická neschopnosť (trvajúca rádovo sekundy) produkcie efektívnych krokov, pri neprítomnosti inej príčiny okrem parkinsonizmu alebo tzv. high-level poruchy chôdze. Najčastejšie sa objavuje počas otáčania a iniciácie chôdze, ale tiež v situáciách sprevádzaných obmedzeniami v priestore, stresom alebo rozptýlením pozornosti. Upriamenie pozornosti a externé podnety môžu pomôcť prekonať epizódu“ [20]. Pri freezingu má pacient subjektívny pocit, akoby mal nohy primrznuté alebo prilepené k podložke. Nie je špecifický pre PCH, ale vyskytuje sa aj samostatne (gait ignition failure, pure freezing of gait syndrome, primary progressive freezing), alebo ako súčasť iných extrapyramídových ochorení, napr. PSP (53 % pacientov), MSA (54 %), DLT (54 %), VP (50 %), KBD (25 %) [21]. Aj keď je freezing doménou pokročilého štádia PCH (53% výskyt) [22], jedna štúdia zistila freezing až u 26 % pacientov, ktorí neboli ešte liečení levodopou [23], čo sa nám zdá mierne nadhodnotené. V praxi je možné rozlišovať nasledovné tri podtypy freezingu:
- akinéza chôdze – pacient bez jasnej príčiny prestane kráčať dopredu, alebo nevie naštartovať chôdzu,
- prestupovanie na mieste – je viditeľná snaha prekonať blok „cupkaním“ z jednej nohy na druhú,
- pošuchovanie sa dopredu malými krokmi [24].
Takéto delenie môže mať význam z hľadiska rizika pádov, pretože pacient, ktorý akceptuje freezing a ostane nehybne stáť až do spontánneho ústupu, môže byť v menšom riziku pádu ako ten, čo presúva ťažisko tela dopredu, kým nohy zaostávajú [10]. Typickými situáciami, v ktorých sa objavuje freezing, sú prechody cez úzky priestor (dvere, úzka ulička, medzi stromami), alebo tesne pred dosiahnutím cieľa (tzv. cieľová hezitácia). Obmedzený čas na vykročenie (napr. na prechode pre chodcov, vstup na eskalátor) taktiež potencuje freezing. Kritickými sú aj zmeny smeru a obrátky, resp. potreba prekročenia alebo obchádzania prekážky na podlahe, alebo situácie, v ktorých má pacient počas chôdze zmysluplne konverzovať, či riešiť matematické úlohy. Na druhej strane, horizontálna čiara alebo pruhovanie na podlahe, pochodová hudba alebo dotykový podnet môžu pomôcť prekonať freezing a naštartovať lokomóciu. Tento jav má spoločné črty s kinesia paradoxa a využíva sa aj terapeuticky (viď ďalej). Väčšina epizód freezingu trvá do 10 sekúnd a len málokedy dlhšie ako 30 sekúnd [24]. Freezing sa častejšie (v 70–90 %) vyskytuje pri poklese účinku dopaminergnej medikácie s ústupom po užití liekov – „OFF freezing“, ale bohužiaľ môže byť prítomný aj v stave dobrej kompenzácie – „ON freezing“ [25].
Pády
Väčšina pádov u pacientov s PCH sa deje v interiéri, zvyčajne v prostredí, ktoré je pre pacienta dobre známe. V ich genéze prevažujú vnútorné príčiny, to znamená, že ich spôsobuje najmä porucha rovnováhy ako taká a nie nejaká kolízia alebo nestabilita podlahy (náraz, zakopnutie, pošmyknutie) [9]. Mnohé pády vznikajú pri presunoch (postavenie sa zo stoličky alebo postele) a náhlej zmene postoja, najmä pri otáčaní trupu, alebo pri pokuse o realizáciu ešte nejakej inej aktivity okrem chôdze (alebo udržiavania rovnováhy). Pacienti s PCH väčšinou dokážu počas chôdze plynule konverzovať, ale pri simultánnej motorickej alebo kognitívnej činnosti (nosenie podnosu, vyhýbanie sa prekážkam, matematická úloha atď.) sa môže objaviť freezing či dokonca pád. Parkinsonici majú ťažkosti stanoviť si prioritu. Tou by v tomto prípade malo byť udržanie rovnováhy, resp. plynulej chôdze. Namiesto toho sa snažia urobiť všetky činnosti naraz a rovnako dobre, čo si vyberá daň vo forme nestability a pádov (tzv. posture second strategy) [26].
Pády pri PCH sú najčastejšie smerované dopredu (46 % zo všetkých pádov), pády dozadu sú menej časté (21 %), podobne, ako aj pády do strany (19 %). Tento pomer je asi zapríčinený zhrbeným predkloneným postojom. U pacientov s PSP prevažujú pády dozadu, pravdepodobne kvôli vzpriamenému postoju (často s retrocollis) [3,15]. Synkopálne pády spôsobené ortostatickou hypotenziou sú, napriek všeobecnému odbornému povedomiu a vysokej prevalencii ortostatickej hypotenzie, u pacientov s PCH zriedkavé [9,27]. U pacientov s parkinsonizmom a synkopálnymi pádmi je namieste skôr uvažovať o diagnóze MSA alebo DLT.
Klinické vyšetrenie posturálnej instability
Anamnéza
Mnohí parkinsonici neverbalizujú svoje ťažkosti s rovnováhou, lebo majú pocit, že je to normálna súčasť starnutia. Iní zasa nechcú zaťažovať lekára problémami, o ktorých sú presvedčení, že sa aj tak nedajú zlepšiť. Taktiež treba mať na pamäti, že pacienti jednoducho zabúdajú na to, aby sa posťažovali na poruchu rovnováhy, alebo na to, že spadli. Opačným javom je agravácia ťažkostí a hlásanie počtu pádov vyššieho ako je realita. Preto je veľmi prínosné konfrontovať stav s partnerom alebo inými blízkymi. Kritickým prvkom anamnézy je informácia ohľadne sebaistoty so zreteľom na rovnováhu pri vykonávaní bežných činností. Strach z pádov je významným faktorom pre imobilizáciu. Na druhej strane, strata úsudku a riskantné správanie sa (precenenie schopností) zvyšujú riziko pádov a zranení. Tento druhý prípad je typický pre pacientov s PSP a je známkou subkortikálnej frontálnej deliberácie. V anglosaskej literatúre sa zvykne označovať ako „motor recklessness“.
Fyzikálne vyšetrenie
V praxi je okrem štandardného klinického neurologického vyšetrenia vhodné použiť batériu testov zameraných na rôzne aspekty udržiavania rovnováhy. Je potrebné štandardne vyšetrovať oba komponenty rovnováhy, statický aj dynamický. Statický komponent sa posudzuje inšpekciou pacienta v pokoji (sediaceho, stojaceho, spredu, zozadu aj zo strany). Dynamické riadenie rovnováhy je zabezpečené viacerými prvkami. Vzpriamovacie reakcie sú potrebné na zmenu postúry (napr. vstávanie zo stoličky alebo z postele). Oporné reakcie sa využívajú na udržiavanie dosiahnutej pozície. Anticipačné reakcie predstavujú automatické a prediktívne adaptácie, ktoré sú prevenciou instability pri pohyboch iniciovaných z vnútorného popudu, ako napr. pri dvíhaní ťažkého predmetu. Reaktívne posturálne odpovede (nazývané klinikmi aj posturálne reflexy ako také) chránia proti narušeniu rovnováhy vonkajšími silami (napr. proti úderu do pleca inou osobou). Takzvané obranné reakcie, ktoré sa uplatňujú pri bezprostrednej hrozbe pádu, zahŕňajú korekčný úkrok (alebo viac krokov) a protektívne pohyby horných končatín. Sú azda najdôležitejšími prvkami, ale je ich ťažké testovať počas bežného ambulantného vyšetrenia [15].
Všeobecným problémom klinického vyšetrenia postoja a chôdze je malý priestor ambulancie alebo vyšetrovne. Ak sa obmedzíme na „štandardné vyšetrenie“ s Rombergovým testom, mnohé kľúčové aspekty PI môžu ostať neodhalené. Preto je vhodné zaradiť do repertoáru klinického vyšetrenia parkinsonika aj štandardizované vyšetrenie napr. pomocou „Get-Up and Go“ testu na čas (viď ďalej) na chodbe pred ambulanciou. Dnes je k dispozícii mnoho štandardizovaných klinických manévrov a testov, ktoré majú rôznu diagnostickú „silu“ v detekcii PI a rizika pádov pri PCH. Tu predstavujeme tie z nich, ktoré sa nám najviac osvedčili z hľadiska spoľahlivosti a časovej nenáročnosti.
Pull test (retropulzný test). Spočíva v náhlom prudšom potiahnutí pacienta zozadu stojacim vyšetrujúcim za obe plecia. Kvantifikuje sa schopnosť adaptácie na takéto narušenie rovnováhy korigujúcim pohybom trupu, resp. počtom krokov vzad. Je implementovaný aj v najnovšej revidovanej verzii hodnotiacej škály pre PCH – the Movement Disorders Society Unified Parkinson’s Disease rating scale (položka 3.12) [28].
„Push and Release” (P&R) test. Tento test hodnotí posturálnu odpoveď na náhle uvoľnenie rúk vyšetrujúceho, opretých o chrbát vyšetrovaného, ktorý na ne tlačí [29].
„Get-up and Go” test na čas (voľný preklad: „postav sa a choď“ test). Test je vhodný pre rutinné hodnotenie viacerých aspektov mobility, ale umožňuje aj longitudinálne sledovanie [15]. Spočíva v stopovaní a observácii výkonu pacienta. Ten v prvej pozícii sedí pohodlne na stoličke, na slovo štart (po predchádzajúcom vysvetlení a možnosti odskúšania) sa postaví, prejde dopredu pohodlnou, resp. preferovanou rýchlosťou k značke na dlážke, ktorá je vzdialená 5 metrov, otočí sa a vráti sa späť k stoličke, na ktorú si sadne. Toto je moment, kedy vyšetrujúci vypne stopky. Ako je zrejmé, možno posúdiť vzpriamovaciu synergiu, chôdzu, prípadne objavenie sa freezingu, stratégiu obrátky aj „pristávaciu“ reakciu. Na vedecké účely sa používa vzdialenosť 3 metre [30], ale pre lepšiu inšpekciu pacientovej lokomócie sa nám osvedčila väčšia vzdialenosť.
„Mini-BESTest“. Tento test je skrátenou verziou BESTestu (Balance Evaluation Systems Test), ktorý vyvinula skupina okolo Fay B. Horak. Mini-BESTest je 14-položkový test zameraný na dynamickú rovnováhu, najmä anticipačné presuny, posturálne odpovede, senzorickú orientáciu a dynamiku chôdze [31]. Každá položka sa skóruje od 0 do 2, skóre 0 indikuje, že pacient nedokáže úlohu vykonať, skóre 2 sa priradí normálnemu výkonu.
„Test desiatich krokov“ – (Bloemov test). Poslúži najmä v diferenciálnej diagnostike PCH. Úlohou pacienta je prejsť ľubovoľnou rýchlosťou desať krokov systémom päta-špička (tandemová chôdza) s otvorenými očami po čiare vyznačenej na podlahe. Väčšina (92 %) pacientov s PCH, aj napriek pokročilému štádiu ochorenia, prejde bezchybne bez úkroku (lateropulzie) desať krokov. Avšak len menšina (18 %) pacientov s atypickým parkinsonizmom podá bezchybný výkon [32]. Charakteristickou črtou týchto syndrómov je porucha medio-laterálnej stability, ktorá sa pri tandemovej chôdzi prejavuje lateropulziami až pádmi do strany.
Patofyziológia
S pokročilosťou PCH, kedy si pacient viac uvedomuje svoje ťažkosti s rovnováhou, podvedome sa vyvíjajú kompenzačné stratégie, ktoré pomáhajú znížiť frekvenciu pádov, ale majú aj negatívne konzekvencie (tab. 1). Keďže obraz posturálnych anomálií a rizikových faktorov pádov pri PCH je mnoho, patofyziológia PI je veľmi komplexná (tab. 2). V nasledujúcom texte bližšie charakterizujeme najdôležitejšie patofyziologické aspekty PI.
Table 1. Niektoré kompenzačné stratégie, ktoré používajú parkinsonici, aby znížili riziko pádov. Upravené podľa [14]. ![Niektoré kompenzačné stratégie, ktoré používajú parkinsonici, aby znížili riziko pádov. Upravené podľa [14].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/5dbc01f6f360d22f9e09399ead30c097.png)
Table 2. Významné faktory v patofyziológii posturálnej instability a pádov u pacientov s Parkinsonovou chorobou. 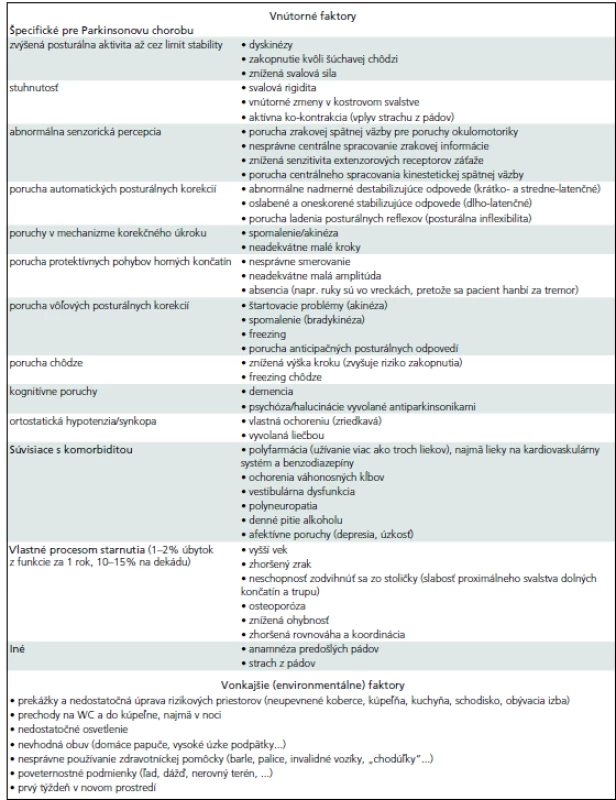
Statická posturografia
Statická posturografia (stabilometria) zaznamenáva postojovú aktivitu tela registráciou presunov centra oporných síl (COS, ktoré závisí od polohy ťažiska tela) vyvinutých na podložku. V začiatočnom štádiu PCH sa posturálna aktivita podstatne nelíši od vekovo primeraného súboru seniorov [33]. V pokročilých štádiách PCH posturálna aktivita signifikantne narastá, čo je príznakom destabilizácie postoja. Všeobecne nie je tento jav priamo závislý na tom, či sú pacienti v stave „ON“, alebo „OFF“. S progresiou PCH sa mení aj stratégia posturálnej stabilizácie (obr. 2). Kým u zdravých osôb a u pacientov v skorom štádiu PCH, pri pokojnom státí s očami otvorenými alebo zatvorenými a nohami vedľa seba, prevažuje antero-posteriórna (AP) aktivita nad medio-laterálnou (ML), u pacientov v pokročilom štádiu (väčšinou s anamnézou pádov) prevažuje ML aktivita (až 3-násobne viac) [33]. Pri postoji s nohami vedľa seba sú ML náklony riadené v bedrových kĺboch činnosťou abduktorov a adduktorov. AP aktivita je však od ML aktivity nezávislá a je riadená v členkoch (aktivitou flexorov a extenzorov nohy). V zmysle zvýšeného rizika pádov je nárast aktivity v ML smere dôležitejším nálezom ako v AP. V AP smere máme možnosť použiť najmenej tri stratégie, aby sme sa vyhli pádom: členkovú (korekcie v členkových kĺboch), bedrovú (pohyby v bedrách) a krokovú (úkrok, vykročenie) [34]. Zmenu stratégie posturálnej stabilizácie u pacientov v pokročilej PCH v prospech ML aktivity, možno interpretovať viacerými spôsobmi. Keďže je riadenie ML posturálnej aktivity spriahnuté s pohybmi v bedrových kĺboch, progresia PCH viac postihuje posturálne riadenie v bedrových, ako členkových kĺboch. Podobne môže ísť o tendenciu k relatívne stereotypnému preferovaniu bedrovej stratégie, čo dokázali viaceré práce [35]. Nemožno vylúčiť ani fenomén rozpojenia (decoupling) medzi riadením posturálnej orientácie trupu a dolných končatín, čo súvisí s poruchou axiálnych synergií [36].
Image 2. Originálne krivky posturálnej aktivity v medio-laterálnom (ML) a antero-posteriórnom (AP) smere. 
RMS – stredná kvadratická odchýlka statokineziogramu (Root Mean Square). Senzori-motorická integrácia a automatické posturálne odpovede
Viacerí experimentátori s posturálnou senzorickou manipuláciou alebo s posturálnym narúšaním (dynamická posturografia) publikovali, že vzorec (synergie) a časovanie (latencie) posturálnych odpovedí nie sú u parkinsonikov postihnuté. Pacienti s PCH teda nemajú podstatný problém s časovaním posturálnych odpovedí, bez ohľadu na štádium ochorenia alebo testovanú zmyslovú modalitu. Avšak posturálne odpovede (amplitúdy) pri manipulácii zrakového systému [37,38], vestibulárneho systému [39], ako aj krčnej alebo lýtkovej propriocepcie [40,41] nie sú oslabené, čo by sa dalo predpokladať z typickej parkinsonskej hypokinézy. Naopak, sú zvýšené, a to najmä v pokročilých štádiách PCH, čo indikuje progresívnu poruchu kvantitatívneho „váženia“ posturálnych reakcií s progresiou PCH.
Dynamická posturografia pracuje na princípe náhlych posunov podložky v zmysle translácie (podtrhnutie dopredu a dozadu) alebo rotácie okolo členkových kĺbov (dorziflexia a plantárna flexia). Aj experimenty s dynamickou posturografiou dokázali, že niektoré automatické reakcie, ktoré sa podieľajú na udržiavaní rovnováhy sú porušené pri PCH. Výlučne u pacientov s pokročilou a dlhotrvajúcou chorobou sú amplitúdy „destabilizujúcich” stredne-latenčných posturálnych odpovedí zvýšené, zatiaľ čo amplitúdy dlho-latenčných „stabilizujúcich” odpovedí sú znížené [2,26]. U parkinsonikov v pokročilých štádiách sú tieto posturálne odpovede ešte aj neflexibilné, pretože bez ohľadu na kontext, potreby a podmienky narušenia rovnováhy, odpovede týchto pacientov majú fixovaný amplitúdový rozsah [14,26]. Čiže s progresiou PCH dochádza k poruche váženia posturálnych reakcií pri rýchlej zmene senzorických podmienok bez ohľadu na to, či je testované (manipulované) aferentné rameno propriocepčne-, vestibulo-, alebo vizuo-posturálneho okruhu. Braak et al [42] imunohistochemickým farbením α-synukleínu zistili významné postihnutie niektorých kmeňových jadier, najmä locus coeruleus. Toto jadro (resp. komplex jadier) sa vyznačuje bohatými aferentnými spojeniami s krčnou miechou a recipročne tiež projikuje k cervikálnym inter - a motoneurónom [43]. Je aj kľúčovou štruktúrou v centrálnom noradrenalínovom neuromediátorovom systéme a práve ona by mohla byť zodpovedná za poruchy váženia (gain-setting) automatických reakcií v pokročilej PCH.
Vôľové posturálne korekcie
Vôľové alebo centrálne spúšťané posturálne korekcie tvoria taktiež dôležitú obrannú líniu proti narušeniu rovnováhy vonkajšími silami. Porucha recipročného programovania a nedostatočná koordinácia pohybu, vzhľadom na akinézu a bradykinézu, sú príčinou oneskorených, neadekvátnych, alebo dokonca chýbajúcich vôľových posturálnych odpovedí. Taktiež nadmerné stuhnutie pre rigiditu a ko-kontrakciu (pre strach z pádov) môže spôsobovať biomechanické oneskorenie týchto reakcií [2]. Na rozdiel od automatických reakcií, ktoré sú neekonomicky zvýšené (viď vyššie), vôľové posturálne reakcie sú hypometrické [26]. Okrem nedostatočnej kompenzácie výkyvov ťažiska sa môže tento deficit podieľať aj na vzniku freezingu.
Mechanizmus korekčného úkroku a protektívne pohyby horných končatín
V prípade významného ohrozenia rovnováhy sú k dispozícii dve kľúčové stratégie, ktoré dokážu zabrániť pádu, alebo zmierniť jeho následky: vystretie horných končatín a ukročenie. Pacienti s PCH majú problémy s iniciáciou kompenzačného úkroku. Predpokladá sa, že zodpovedným mechanizmom je porucha anticipačných posturálnych nastavení (na uvoľnenie jednej dolnej končatiny pred krokom je potrebné preniesť váhu tela na druhú stranu). Nielen z hľadiska patofyziológie, ale aj terapie je podstatný nález, že poruchu možno preklenúť vonkajším podnetom. Napríklad ak je krok spúšťaný dotykovým, zrakovým alebo akustickým signálom, je oveľa rýchlejší a dlhší [44,45].
Funkciou automatických protektívnych pohybov horných končatín je jednak vybalansovanie a vyhnutie sa pádu (ako u povrazolezca), ale aj zmiernenie pádu dopadnutím na horné končatiny (chráni sa hlava, najmä tvár). Pacienti s PCH majú poruchu týchto automatických pohybov, ktoré nastupujú síce rýchlejšie ako u zdravých osôb, ale ich amplitúda, ako aj distribúcia na tele je relatívne stereotypná a nezávislá od kontextu [46]. Táto porucha môže byť príčinou nižšej frekvencie fraktúr horných končatín u pacientov s PCH, bohužiaľ na úkor zlomenín bedrovej kosti (viď vyššie).
Freezing chôdze
Pacienti s freezingom majú zvýšenú variabilitu chôdze (kroky sú rôzne dlhé) aj v čase mimo epizódy. To znamená, že u týchto pacientov sú neustále prítomné subtílne poruchy rytmickosti chôdze [47,48]. Preto sa predpokladá, že by v patogenéze freezingu mohli zohrávať úlohu lézie štruktúr, ktoré majú úlohu jedného alebo viacerých generátorov centrálneho vzorca chôdze [48]. Inšpirujúcou je kazuistika pacienta s výrazným freezingom. Autopsiou sa u neho potvrdili obojstranné infarkty v oblasti horného mozgového kmeňa, ktorá sa dáva do súvislosti s lokomotorickou funkciou, nucleus pedunculopontinus [49]. Autori predpokladajú, že práve táto oblasť je priamo zodpovedná za freezing. Anatomická porucha bude pravdepodobne komplexnejšia, keďže freezing sa manifestuje často v situáciách s emočným, vôľovým alebo kognitívnym kontextom, čo predpokladá zapojenie kôrových štruktúr mozgu. Zo štúdií, ktoré použili PET a MR zobrazovacie techniky, sa dá usudzovať, že korelátom freezingu je neuronálna dysfunkcia na dvoch hlavných úrovniach:
- v pravostranných parietálnych laterálnych premotorických okruhoch, tieto za fyziologických podmienok priraďujú senzorické informácie do procesov riadenia chôdze a
- vo fronto-striatálnych okruhoch, ktoré zapracúvajú kognitívny kontext, podieľajú sa na zacielení pozornosti.
Záujemcov o komplexný pohľad na fenomén freezingu odkazujeme na recentnú publikáciu [48].
Liečba posturálnej instability
Keďže mnohé aspekty PI sú spôsobené non-dopaminergnými léziami, liečba PI nie je jednoduchá a právom sa považuje za „crux medicorum“. Taktiež je potrebné si uvedomiť, že prejavy PI sa zhoršujú s progresiou ochorenia, ktorá so sebou nesie zmeny takmer všetkých domén fyzického a psychického bytia (kognitívne poruchy, afektívne poruchy, únava, vegetatívna dysfunkcia, muskuloskeletálna involúcia a deformity, zhoršená kardiovaskulárna výkonnosť atď.). To znamená, že sú výrazne obmedzené funkčné rezervné a substitučné mechanizmy, ktoré by defektné posturálne funkcie mohli preklenúť. Avšak jednoznačne nie je namieste nihilistický postoj k terapii PI.
Farmakoterapia
Prvým krokom by malo byť určenie dopaminergnej responzivity problematických aspektov. V prípade symptómov viazaných na OFF stav, je potrebné citlivo zvýšiť dávku dopaminergnej liečby (levodopy alebo agonistov dopamínových receptorov – DA agonistov). Takýmto symptómom môže byť častejší variant freezingu, ktorý je viazaný na OFF stav, alebo hypokinéza chôdze pri ťažkej globálnej rigidite a bradykinéze. Väčšina posturálnych abnormít bohužiaľ na dopaminergnú liečbu nezaberá, resp. ich táto liečba zhoršuje [2]. V prípade zhoršenia stavu kvôli dopaminergnej stimulácii (zvýšenie rizika pádov pre dyskinézy, prehĺbenie ortostatických ťažkostí, halucinácie, nebezpečne zvýšená mobilita pri demencii), je potrebné takúto liečbu citlivo redukovať. L-threo-DOPS (droxidopa) je syntetický prekurzor noradrenalínu, u ktorého bolo v menších štúdiách dokázané zlepšenie freezingu, rôznych aspektov chôdze a automatických posturálnych reakcií. Avšak v zaslepenej, placebom kontrolovanej štúdii, sa tento efekt nepotvrdil [15]. Ani posledné európske guidelines použitie tejto látky u parkinsonikov neodporúčajú [50]. Novšie práce naznačujú taktiež možnosti inhibítorov cholínesterázy (napr. galantamínu) v liečbe posturálnej instability u parkinsonikov s kognitívnou dysfunkciou [51], čo sa odôvodňuje hypotézou, že mnohé axiálne problémy rezultujú z nerovnováhy medzi centrálnym dopamínergným a cholinergným systémom [52]. Konzistentnejšie dôkazy sú k dispozícii s dvomi látkami, rasagilínom a metylfenidátom. Rasagilín je inhibítor monoaminooxidázy B. Je dodnes jedinou látkou testovanou v prospektívnej, dvojito-zaslepenej, placebom a aktívnou látkou kontrolovanej štúdii kvôli efektu na freezing chôdze. Tento bol hodnotený dotazníkom na podskupine 454 pacientov zo štúdie LARGO [53], ktorí užívali buď rasagilín, alebo entakapon (inhibítor COMT). Po 10 týždňoch došlo u rasagilínu k zlepšeniu freezingu, podobne ako u entakaponu. Obe látky však ukázali vysoko signifikantné zlepšenie freezingu v porovnaní s placebom [54]. Zaujímavá je kazuistika 84-ročného muža so 4-ročnou anamnézou freezingu (v rámci diagnózy primárneho progresívneho freezingu). Nasadenie rasagilínu viedlo k rýchlemu, dramatickému a trvalému zlepšeniu frekvencie a trvania epizód free-zingu. Pri liečbe rasagilínom bolo navyše dokumentované zlepšenie perfúzie frontálnych lalokov na SPECT vyšetrení, čo môže jednak osvetľovať patofyziológiu freezingu, ako aj mechanizmus pôsobenia rasagilínu na freezing [55]. Metylfenidát, tradične podávaný na liečbu poruchy pozornosti sprevádzanej hyperaktivitou (ADHD, Attention Deficit Hyperactivity Dis-order), môže znížiť riziko pádov u seniorov v komunite, pravdepodobne zvýšením dostupnosti striatálneho dopamínu, alebo zlepšením pozornosti [56]. Napriek tomu, že v nekontrolovanej štúdii bol metylfenidát (3 mg/kg/deň) efektívny na vzorke 17 pacientov v pokročilom štádiu PCH v zlepšení viacerých parametrov motoriky vrátane špecifických testov chôdze [57], v randomizovanej, placebom kontrolovanej štúdii sa tento výsledok nepotvrdil [58].
V kontexte farmakoterapie PI a prevencie pádov je potrebné pamätať na skutočnosť, že niektoré skupiny liekov (najmä sedatíva a neuroleptiká) alebo polyfarmácia majú dokázateľne negatívny efekt a je vhodné sa im v liečbe pacientov s PCH vystríhať.
Stereotaktická neurochirurgia
Hlboká mozgová stimulácia (Deep Brain Stimulation, DBS) dokáže u vybraných pacientov v pokročilom štádiu PCH efektívne redukovať dyskinézy, zlepšiť motorické príznaky na končatinách a celkovú kvalitu života [59]. Avšak neodporúča sa realizovať DBS ncl. subthalamicus (STN) ani globus pallidus internus (GPi) u pacientov s výraznou PI a poruchami chôdze vrátane freezingu, ktoré sú rezistentné na dopaminergnú liečbu. Jedná sa prakticky o exklúzne kritérium pre DBS u pacientov s PCH v týchto anatomických cieľoch [60]. Sľubnou sa zdá byť možnosť ovplyvnenia axiálnych príznakov pomocou stimulácie ncl. pedunculopontinus (PPN). Táto súčasť lokomotorického regiónu mezencefalickej retikulárnej formácie je spomínaná vyššie v súvislosti s pravdepodobnou úlohou v patogenéze freezingu. Stimulácia PPN zlepšuje hlavne levodopa-rezistentnú poruchu postoja a chôdze [61]. Aj keď je dodnes implantovaných už niekoľko stovák pacientov, na stanovisko k dlhodobému efektu DBS PPN (prípadne „duálnej“ bilaterálnej stimulácie PPN + STN) je potrebné ešte počkať.
Fyzioterapia
Fyzioterapia (FT) má kľúčový význam v liečbe PI a prevencii pádov u PCH [50,62]. Najefektívnejším prístupom v ovplyvnení porúch rovnováhy, mobility a rizika pádov je každodenné cvičenie, ktoré pozostáva z pestrej zostavy cvikov. Keďže PCH predstavuje syndróm s rozsiahlou fenotypovou variáciou, FT musí byť „ušitá na mieru“ pre konkrétneho pacienta, so zreteľom na prevahu symptómov a štádium ochorenia [63].
V začiatočnom štádiu PCH je dôležité stimulovať pacientovu mobilitu aj podporou činností a športových aktivít, ktoré vykonával pred diagnostikovaním ochorenia (ako plávanie, loptové športy, bicyklovanie, kondičný beh alebo jogging – pomalý beh kombinovaný s chôdzou). Pravidelné pestovanie takýchto činností podporuje udržanie krokového vzorca, rovnováhy, koordinácie a rýchlosti pohybov. V strednom štádiu je výhodné, ak sa pacient zúčastňuje na FT v skupinách alebo individuálne so zameraním na problémy, ktoré sa týkajú chôdze, udržiavania rovnováhy, správneho postoja a presunov, akým je napríklad otáčanie sa na posteli. Aj v neskorých štádiách PCH je dokázaný efekt FT, ktorá má byť častejšie realizovaná v domácom prostredí pacienta ako v priestoroch kliniky. Zameraním FT sú problémy spojené s denným fungovaním, ako napr. chôdza, freezing a presuny v ich vlastnom kontextuálnom prostredí. Takýto prístup dokázateľne zlepšuje nezávislosť pacienta v bežných denných činnostiach a pomáha významne oddialiť potrebu inštitucionalizácie pacienta [64].
Kognitívne pohybové stratégie
Využívajú sa na zlepšenie presunov (transferov). Princípom je to, že komplexné (automatické) činnosti sa rozdelia do separátnych úkonov, ktoré pozostávajú z relatívne jednoduchých komponentov, a tie sa vykonávajú postupne [65]. Takýto prístup núti pacienta vedome myslieť na každý pohyb, čo umožňuje vyhnúť sa realizácii viacerých činností naraz (multiple tasking) počas komplexných činností v dennom živote. Okrem toho takýto pohyb alebo činnosť možno správne nacvičiť a zafixovať v motorickej pamäti.
Navádzajúce (cueing) stratégie
Akinéza a freezing sú výsledkom deficitu, tzv. vnútorného riadenia pohybu. Podstatou je porucha realizácie adekvátnych motorických odpovedí z vnútorného popudu u pacientov s PCH. Navádzajúcimi prvkami (cues) sú podnety z vonkajšieho prostredia alebo zriedkavejšie aj podnety generované pacientom, ktoré zvyšujú pozornosť pacienta a facilitujú automatické pohyby. Predpokladá sa, že tieto podnety umožňujú riadenie pohybu priamo mozgovou kôrou, s minimálnou alebo žiadnou participáciou bazálnych ganglií [66]. Najčastejšie využívané navádzajúce podnety podáva tab. 3.
Table 3. Navádzajúce (cueing) podnety, ktoré sa využívajú vo fyzioterapii freezingu chôdze. Upravené podľa [3]. ![Navádzajúce (cueing) podnety, ktoré sa využívajú vo fyzioterapii freezingu chôdze. Upravené podľa [3].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/bc6510ef078e727b85a0687940b0d54e.png)
Zdravotnícke pomôcky
S progresiou PCH postupne vzniká potreba využívania špeciálnych zdravotníckych pomôcok (tab. 4). Je potrebné si ale uvedomiť, že ak sa používajú nesprávnym spôsobom, môžu byť rizikovým faktorom pre komplikáciu PCH, najčastejšie mechanizmom pádu. Úlohou rehabilitačného lekára a fyzioterapeuta (spolu s ergoterapeutom) je okrem iného aj výber vhodnej zdravotníckej pomôcky a zabezpečenie správneho tréningu v jej používaní. Pacient by mal byť navyše informovaný, kde a akým spôsobom možno pomôcku v prípade jej poruchy opraviť. V prípade potreby by mal byť pacient taktiež odoslaný za ergoterapeutom, ktorý dokáže poradiť pri potrebných úpravách domácnosti [3].
Table 4. Najčastejšie používané zdravotnícke pomôcky pri Parkinsonovej chorobe. 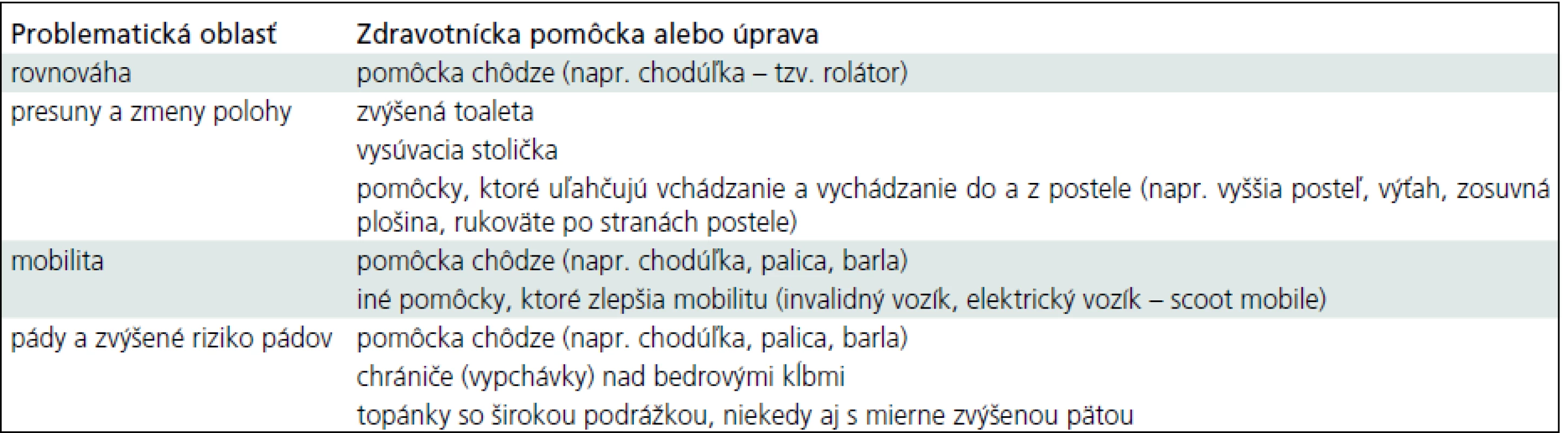
Záver
Posturálna instabilita, poruchy chôdze a pády patria medzi najviac negatívne faktory, ktoré znižujú celkovú kvalitu života pacientov s PCH. Patofyziológia týchto symptómov je komplexná a reflektuje komplexnosť súčasnej patofyziologickej koncepcie idiopatickej PCH. Napriek tomu má skúsený klinik pri citlivom vyšetrení, komunikácii s pacientom a jeho príbuznými a poznaní variability klinického obrazu tohto ochorenia viaceré nástroje, ktorými možno pozitívne zasiahnuť. Sú nimi najmä úprava antiparkinsonskej medikácie a vysadenie alebo zníženie dávky rizikovej komedikácie (napr. psychofarmaká, antihypertenzíva), pozitívna motivácia pacienta a jeho okolia a najmä na mieru „ušitá“ fyzioterapia naprieč celým priebehom PCH.
Práca vznikla s podporou grantu VEGA 1/0070/11.
Prijaté k recenzii: 13. 1. 2012
Prijaté do tlače: 22. 3. 2012
doc. MUDr. Peter Valkovič, PhD.
II. neurologická klinika
LF UK a UN Bratislava
Nemocnica akad. L. Dérera
Limbová 5
833 05 Bratislava
e-mail: peter.valkovic@gmail.com
Recenzenti:
doc. MUDr. Ján Benetin, PhD.
prof. MUDr. Petr Kaňovský, CSc.
prof. MUDr. Evžen Růžička, DrSc.
doc. MUDr. Peter Valkovič, PhD. (1976)
Docent Valkovič promoval na Lekárskej fakulte Univerzity Komenského v Bratislave v roku 2000. Od promócie bol doktorandom postgraduálneho štúdia na II. neurologickej klinike LF UK v Bratislave. Dizertačnú prácu na tému Posturálna instabilita pri Parkinsonovej chorobe obhájil v roku 2005. V rokoch 2004–2010 pôsobil ako odborný asistent a od roku 2011 je docentom neurológie na II. neurologickej klinike LF UK v Bratislave. Od roku 2007 tiež pôsobí na Ústave normálnej a patologickej fyziológie Slovenskej akadémie vied v Bratislave. V rokoch 2003–2004 (štipendium EÚ Marie-Curie Training Program Fellowship) a v roku 2005 (European Neurological Society Fellowship) absolvoval dva ročné výskumné pobyty na Neurologickej klinike Ludwig-Maximilians-Universität v Mníchove. Je členom redakcie časopisu Česká a slovenská neurologie a neurochirurgie, členom širšej redakčnej rady časopisu Neurológia pre prax a od roku 2011 je členom medzinárodnej redakčnej rady World Journal of Neurology. Okrem toho je od roku 2010 zástupcom Slovenskej neurologickej spoločnosti v EFNS/MDS-ES Panel on Movement disorders a od roku 2011 vedeckým sekretárom Slovenskej neuropsychiatrickej spoločnosti. Doc. Valkovič je držiteľom Guothovej ceny prezídia Slovenskej lekárskej spoločnosti (2008), ceny Arnolda Picka za najlepšiu slovenskú prácu publikovanú v časopise Neurológia pre prax (2007), prémie Literárneho fondu za knihu Parkinsonova choroba (HERBA 2009, autori Benetin a Valkovič) a ďakovného listu rektora Univerzity Komenského pri príležitosti osláv Medzinárodného dňa študentstva (2011). V klinickej, vedeckej a publikačnej práci sa sústreďuje na oblasť neurodegeneratívnych ochorení a na poruchy rovnováhy. Na svoje publikácie má aktuálne 94 citácií (bez autocitácií) podľa SCI, h-index 6.
Vědomostní test
1. Posturálna instabilita pri Parkinsonovej chorobe:
- a) je základným diagnostickým príznakom, ktorý sa vyskytuje u všetkých pacientov od samého začiatku ochorenia
- b) je súčasťou tetrády kardinálnych klinických príznakov
- c) ako termín zahŕňa z klinického hľadiska nielen poruchu udržiavania postoja, ale aj problémy s chôdzou a pády
- d) je vo väčšine prípadov zapríčinená dopaminergnými léziami CNS
2. Ktoré tvrdenie o pádoch u pacientov s Parkinsonovou chorobou je správne:
- a) Pády sú najčastejšie v 1. štádiu podľa Hoehnovej a Yahra, resp. pred stanovením dg. PCH.
- b) U pacientov s PCH zohrávajú v mechanizme pádov významnejšiu úlohu vonkajšie rizikové faktory (nebezpečenstvo z prostredia, ktoré predurčuje k pošmyknutiu alebo zakopnutiu).
- c) Pády sú najčastejšie v 3. štádiu podľa Hoehnovej a Yahra, teda v čase ešte pomerne dobre zachovanej mobility.
- d) Absolútny počet pádov nie je u pacientov s PCH korelátom závažnosti posturálnej instability, pretože imobilný pacient nepadá.
3. Ktoré tvrdenie o pádoch u pacientov s Parkinsonovou chorobou je správne:
- a) Výskyt pádov je u pacientov s PCH najvyšší spomedzi najčastejších neurologických ochorení.
- b) Viac pádov sa vyskytuje v štádiu obmedzenej pohyblivosti (OFF) v porovnaní so stavom dobrej motoriky (ON).
- c) Z prospektívnych štúdií je známe, že 17 % pacientov s PCH spadne aspoň raz počas jedného roka a 15 % padá opakovane.
- d) Z prospektívnych štúdií je známe, že takmer 70 % pacientov s PCH spadne aspoň raz počas jedného roka.
4. Označte správne tvrdenie:
- a) Pri „bludnom“ vývoji po páde môže byť strach z ďalších pádov príčinou straty sebadôvery, čo môže viesť k obmedzeniu mobility.
- b) U pacientov s PCH zohrávajú v mechanizme pádov významnejšiu úlohu vnútorné (intrinsické) rizikové faktory, ktoré priamo postihujú schopnosť udržiavania rovnováhy.
- c) Imobilizačný syndróm zhoršuje osteoporózu, svalovú slabosť a kardiovaskulárnu kondíciu.
- d) Rekurentné pády sú samolimitujúcim faktorom posturálnej instability a po zmene medikácie z dopamínových agonistov na agonistu NMDA spontánne vymiznú.
5. Označte správne tvrdenie:
- a) Včasný výskyt závažných porúch rovnováhy a pádov upozorňuje skôr na inú príčinu parkinsonizmu (napr. progresívnu supranukleárnu obrnu alebo vaskulárny parkinsonizmus).
- b) Termínom kamptokormia označujeme typickú fixovanú kyfoskoliózu, ktorá je prítomná u väčšiny pacientovs PCH.
- c) Rekurentné pády sú indikátorom prechodu pacienta z latentného do manifestného štádia PCH.
- d) Výrazná PI charakterizovaná jasnými poruchami chôdze, rovnováhy a rekurentnými pádmi postihuje pacientov s PCH až v pokročilom štádiu ochorenia (štádiá podľa Hoehnovej a Yahra 3–5).
6. Chôdza pri Parkinsonovej chorobe:
- a) nie je výrazne postihnutá v priebehu celého ochorenia
- b) je výrazne postihnutá od začiatku klinickej manifestácie
- c) je v skorom štádiu ochorenia charakterizovaná najmä asymetrickou redukciou synkinéz horných končatín a miernym predklonom
- d) sa s progresiou stáva pomalšou, kroky sú kratšie, šúchavé, oporná báza sa zužuje, synkinézy horných končatín obojstranne vymiznú a zmeny smeru napr. pri otáčaní (obchádzaní prekážok) pacient realizuje „en bloc“
7. Freezing chôdze:
- a) nie je špecifický pre PCH, ale vyskytuje sa aj samostatne, alebo ako súčasť iných extrapyramídových ochorení, napr. pri progresívnej supranukleárnej obrne alebo vaskulárnom parkinsonizme
- b) je na rozdiel od iných príčin parkinsonizmu výlučne prítomný u pacientov s idiopatickou PCH
- c) veľmi ohrozuje rovnováhu a je jedným z najčastejších mechanizmov pádov pri PCH
- d) nikdy sa nezlepší po úprave liečby levodopu
8) Freezing chôdze:
- a) eliminuje ho zaťaženie pozornosti pacienta počas chôdze mentálnou úlohou
- b) väčšina epizód trvá 20–40 sekúnd
- c) ako termín zahŕňa z klinického hľadiska nielen poruchu udržiavania postoja, ale aj problémy s chôdzou a pády
- d) sa najčastejšie objavuje počas otáčania a iniciácie chôdze, ale tiež v situáciách sprevádzaných obmedzeniami v priestore, stresom alebo rozptýlením pozornosti
9. Ktoré tvrdenie o pádoch pri Parkinsonovej chorobe je správne:
- a) Väčšina pádov u pacientov s PCH sa deje v interiéri, zvyčajne v prostredí, ktoré je pre pacienta dobre známe.
- b) U pacientov s PCH sú pády naj-častejšie smerované dozadu, kým u progresívnej supranukleárnej obrny najmä dopredu.
- c) Najčastejšou príčinou sú synkopálne pády.
- d) Simultánna motorická alebo kognitívna činnosť počas chôdze eliminuje riziko pádu.
10. Označte správne tvrdenie:
- a) Najcitlivejším prediktorom budúcich pádov u pacienta s PCH je Rombergov test.
- b) Fenomén strachu z pádov je významným rizikovým faktorom pre ďalšie pády.
- c) Pull test (retropulzný test) spočíva v náhlom prudšom potiahnutí pacienta zozadu stojacim vyšetrujúcim za obe plecia.
- d) Test desiatich krokov po čiare môže byť nápomocný v diferenciálnej diagnostike PCH (kde je väčšinou normálny) a atypického parkinsonizmu (kde je spravidla patologický).
11. Patofyziológia posturálnej instability (označte správne tvrdenie):
- a) Posturálna aktivita registrovaná pomocou statickej posturografie (postoj s očami zatvorenými) nedokáže odlíšiť skupinu vekovo primeraných zdravých seniorov od parkinsonikov v pokročilom štádiu PCH.
- b) Pacienti s PCH nemajú podstatný problém s časovaním posturálnych odpovedí, bez ohľadu na štádium ochorenia alebo testovanú zmyslovú modalitu.
- c) S progresiou PCH dochádza k poruche škálovania posturálnych reakcií.
- d) Je to paradoxné, ale pacienti v pokročilých štádiách PCH nemajú na rozdiel od skorých štádií problémy s iniciáciou kompenzačného úkroku.
12. Označte správne tvrdenie:
- a) Zaujatie predklonenej postúry znižuje riziko pádov dopredu.
- b) Postoj na užšej opornej báze zlepšuje medio-laterálnu a antero-posteriórnu stabilitu.
- c) Zaujatie predklonenej postúry znižuje riziko pádov dozadu.
- d) Zaujatie predklonenej postúry môže spôsobiť zvýšenú strnulosť a festinácie.
13. Liečba posturálnej instability (označte správne tvrdenie):
- a) V prípade symptómov viazaných na OFF stav je potrebné zvýšiť dávku dopaminergnej liečby.
- b) Nie je jednoduchá a právom sa považuje za „crux medicorum“.
- c) Niektoré skupiny liekov (najmä sedatíva a neuroleptiká) majú negatívny vplyv.
- d) Všetky vyššie uvedené tvrdenia sú správne.
14. Liečba posturálnej instability (označte správne tvrdenie):
- a) V prípade zhoršenia stavu kvôli dopaminergnej stimulácii je potrebné zvýšiť dávku levodopy.
- b) Prvým krokom by malo byť určenie dopaminergnej responzivity problematických aspektov.
- c) Podľa medicíny založenej na dôkazoch je takmer ideálnym postupom pridanie inhibítora COMT k rasagilínu.
- d) OFF freezing je indikáciou pre nasadenie metylfenidátu.
15. Hlboká mozgová stimulácia (DBS) v liečbe posturálnej instability pri PCH:
- a) Neodporúča sa realizovať DBS ncl. subthalamicus ani globus pallidus internus u pacientov s výraznou posturálnou instabilitou a poruchami chôdze.
- b) Posturálna instabilita je indikáciou pre DBS ncl. subthalamicus.
- c) Stimulácia ncl. pedunculopontinus zlepšuje hlavne levodopa-rezistentnú poruchu postoja a chôdze.
- d) Stimulácia ncl. pedunculopontinus je rutínne implantovanou štruktúrou pri OFF freezingu.
16. Fyzioterapia (označte správne tvrdenie):
- a) Dokázateľne zlepšuje nezávislosť pacienta v bežných denných činnostiach a pomáha významne oddialiť potrebu inštitucionalizácie pacienta.
- b) Kľúčom k prevencii imobilizačného syndrómu je každodenné skupinové cvičenie.
- c) Má byť v neskorom štádiu realizovaná výlučne na rehabilitačnej klinike.
- d) Má byť „ušitá na mieru“ pre konkrétneho pacienta, so zreteľom na prevahu symptómov a štádium ochorenia.
17. Navádzajúce (cueing) stratégie:
- a) využívajú Uhthoffov fenomén
- b) využívajú aj rytmicky sa opakujúce zmyslové podnety
- c) sú efektívne aj pri synkopálnych pádoch
- d) sú efektívnejšie ak sa asynchrónne v tom istom čase stimulujú viaceré zmyslové modality
18. Zdravotnícke pomôcky (označte správne tvrdenie):
- a) Freezing možno eliminovať používaním dvoch francúzskych bariel.
- b) Úlohou rehabilitačného lekára a fyzioterapeuta (spolu s ergoterapeutom) je aj výber vhodnej zdravotníckej pomôcky a zabezpečenie správneho tréningu v jej používaní.
- c) Ak sa používajú nesprávnym spôsobom, môžu byť rizikovým faktorom pádov.
- d) V prípade objavenia sa freezingu je namieste predpis invalidného vozíka.
19. Posturálna instabilita a rekurentné pády sú možnou príčinou:
- a) imobilizačného syndrómu
- b) inštitucionalizácie pacienta
- c) zvýšenej mortality parkinsonikov
- d) všetky odpovede sú správne
20. Označte časté „vonkajšie“ rizikové faktory pádov pri Parkinsonovej chorobe:
- a) vestibulárna a zraková dysfunkcia
- b) alkoholická alebo benzodiazepínová polyneuropatia
- c) nevhodná obuv a nedostatočné osvetlenie vnútorných priestorov
- d) nesprávne používanie zdravotníckej pomôcky
Správně jsou jedna nebo více odpovědí.
Test můžete vyplnit na:
www.csnn.eu
Sources
1. Hughes AJ, Daniel SE, Kilford L, Lees AJ. Accuracy of clinical diagnosis of idiopathic Parkinson’s disease: a clinico-pathological study of 100 cases. J Neurol Neurosurg Psychiatry 1992; 55(3): 181–184.
2. Bloem BR, van Vugt JP, Beckley DJ. Postural instability and falls in Parkinson’s disease. Adv Neurol 2001; 87 : 209–223.
3. Valkovič P. Posturálna instabilita u pacientov s Parkinsonovou chorobou a jej liečba. Neurol Prax 2009; 10(6): 348–353.
4. Stolze H, Klebe S, Zechlin C, Baecker C, Friege L, Deuschl G. Falls in frequent neurological diseases-prevalence, risk factors and aetiology. J Neurol 2004; 251(1): 79–84.
5. Pickering RM, Grimbergen YA, Rigney U, Ashburn A, Mazibrada G, Wood B et al. A meta-analysis of six prospective studies of falling in Parkinson’s disease. Mov Disord 2007; 22(13): 1892–1900.
6. Schrag A, Selai C, Jahanshahi M, Quinn NP. The EQ-5D a generic quality of life measure-is a useful instrument to measure quality of life in patients with Parkinson’s disease. J Neurol Neurosurg Psychiatry 2000; 69(1): 67–73.
7. Rahman S, Griffin HJ, Quinn NP, Jahanshahi M. Quality of life in Parkinson’s disease: the relative importance of the symptoms. Mov Disord 2008; 23(10): 1428–1434.
8. Jankovic J, McDermott M, Carter J, Gauthier S, Goetz C, Golbe L et al. Variable expression of Parkinson’s disease: a base-line analysis of the DATATOP cohort. The Parkinson Study Group. Neurology 1990; 40(10): 1529–1534.
9. Bloem BR, Grimbergen YA, Cramer M, Willemsen M, Zwinderman AH. Prospective assessment of falls in Parkinson’s disease. J Neurol 2001; 248(11): 950–958.
10. Bloem BR, Hausdorff JM, Visser JE, Giladi N. Falls and freezing of gait in Parkinson’s disease: a review of two interconnected, episodic phenomena. Mov Disord 2004; 19(8): 871–884.
11. Ashburn A, Stack E, Pickering RM, Ward CD. Predicting fallers in a community-based sample of people with Parkinson’s disease. Gerontology 2001; 47(5): 277–281.
12. Farníková K, Bareš M, Nestrašil I, Kaňovský P. Parkinsonské fenotypy – na cestě k nové nozologii atypických parkinsonských syndromů. Cesk Slov Neurol N 2011; 74/107(6): 641–653.
13. Schrag A, Quinn NP, Ben-Shlomo Y. Heterogeneity of Parkinson’s disease. J Neurol Neurosurg Psychiatry 2006; 77(2): 275–276.
14. Schieppati M, Nardone A. Free and supported stance in Parkinson’s disease. The effect of posture and ‚postural set‘ on leg muscle responses to perturbation, and its relation to the severity of the disease. Brain 1991; 114(Pt 3): 1227–1244.
15. Bloem BR, Bhatia KP. Gait and balance in basal ganglia disorders. In: Bronstein AM, Brandt T, Woollacott MH et al (eds). Clinical disorders of balance, posture and gait. London: Arnold 2004 : 173–206.
16. Azher SN, Jankovic J. Camptocormia: pathogenesis, classification, and response to therapy. Neurology 2005; 65(3): 355–359.
17. Anastasopoulos D, Ziavra N, Savvidou E, Bain P, Bronstein AM. Altered eye-to-foot coordination in standing parkinsonian patients during large gaze and whole-body reorientations. Mov Disord. 2011; 26(12): 2201–2211.
18. Schlesinger I, Erikh I, Yarnitsky D. Paradoxical kinesia at war. Mov Disord 2007; 22(16): 2394–2397.
19. Giladi N, Balash Y. The clinical approach to gait disturbances in Parkinson’s disease; maintaining independent mobility. J Neural Transm Suppl 2006; 70 : 327–332.
20. Giladi N, Nieuwboer A. Understanding and treating freezing of gait in parkinsonism, proposed working definition, and setting the stage. Mov Disord 2008; 23 (Suppl 2): S423–S425.
21. Factor SA. The clinical spectrum of freezing of gait in atypical parkinsonism. Mov Disord 2008; 23 (Suppl 2): S431–S438.
22. Giladi N, Treves TA, Simon ES, Shabtai H, Orlov Y, Kandinov B et al. Freezing of gait in patients with advanced Parkinson’s disease. J Neural Transm 2001; 108(1): 53–61.
23. Giladi N, McDermott MP, Fahn S, Przedborski S, Jankovic J, Stern M et al. Freezing of gait in PD: prospective assessment in the DATATOP cohort. Neurology 2001; 56(12): 1712–1721.
24. Schaafsma JD, Balash Y, Gurevich T, Bartels AL, Hausdorff JM, Giladi N. Characterization of freezing of gait subtypes and the response of each to levodopa in Parkinson’s disease. Eur J Neurol 2003; 10(4): 391–398.
25. Snijders AH, Nijkrake MJ, Bakker M, Munneke M, Wind C, Bloem BR. Clinimetrics of freezing of gait. Mov Disord 2008; 23 (Suppl 2): S468–S474.
26. Bloem BR, Grimbergen YA, van Dijk JG, Munneke M. The „posture second“ strategy: a review of wrong priorities in Parkinson’s disease. J Neurol Sci 2006; 248(1–2): 196–204.
27. Matinolli M, Korpelainen JT, Korpelainen R, Sotaniemi KA, Myllylä VV. Orthostatic hypotension, balance and falls in Parkinson’s disease. Mov Disord 2009; 24(5): 745–751.
28. Goetz CG, Tilley BC, Shaftman SR, Stebbins GT, Fahn S, Martinez-Martin P et al. Movement Disorder Society-sponsored revision of the Unified Parkinson’s Disease Rating Scale (MDS-UPDRS): scale presentation and clinimetric testing results. Mov Disord 2008; 23(15): 2129–2170.
29. Valkovič P, Brožová H, Bötzel K, Růžička E, Benetin J. Push-and-release test predicts Parkinson fallers and nonfallers better than the pull test: comparison in OFF and ON medication states. Mov Disord 2008; 23(10): 1453–1457.
30. Morris S, Morris ME, Iansek R. Reliability of measurements obtained with the Timed „Up & Go“ test in people with Parkinson disease. Phys Ther 2001; 81(2): 810–818.
31. Franchignoni F, Horak F, Godi M, Nardone A, Giordano A. Using psychometric techniques to improve the Balance Evaluation Systems Test: the mini-BESTest. J Rehabil Med 2010; 42(4): 323–331.
32. Abdo WF, Borm GF, Munneke M, Verbeek MM, Esselink RA, Bloem BR. Ten steps to identify atypical parkinsonism. J Neurol Neurosurg Psychiatry 2006; 77(12): 1367–1369.
33. Valkovič P, Krafczyk S, Benetin J, Šaling M, Bötzel K. Deteriorácia posturálnej stability v progresii Parkinsonovej choroby: posturografická štúdia. Cesk Slov Neurol N 2004; 67/100(5): 347–353.
34. Horak FB, MacPherson JM. Postural orientation and equilibrium. In: Rowell LB, Shepard JT (eds). Handbook of Physiology. Section 12: Exercise: Regulation and Integration of Multiple Systems. New York: Oxford University Press 1996 : 255–292.
35. Horak FB, Dimitrova D, Nutt JG. Direction-specific postural instability in subjects with Parkinson’s disease. Exp Neurol 2005; 193(2): 504–521.
36. Alexandrov A, Aurenty R, Massion J, Mesure S, Viallet F. Axial synergies in parkinsonian patients during voluntary trunk bending. Gait Posture 1998; 8(2): 124–135.
37. Bronstein AM, Hood JD, Gresty MA, Panagi C. Visual control of balance in cerebellar and parkinsonian syndromes. Brain 1990; 113(Pt 3): 767–779.
38. Bronstein AM, Yardley L, Moore AP, Cleeves L. Visually and posturally mediated tilt illusion in Parkinson’s disease and in labyrinthine defective subjects. Neurology 1996; 47(3): 651–656.
39. Pastor MA, Day BL, Marsden CD. Vestibular induced postural responses in Parkinson’s disease. Brain 1993; 116(Pt 5): 1177–1190.
40. Valkovič P, Krafczyk S, Bötzel K. Postural reactions to soleus muscle vibration in Parkinson’s disease: scaling deteriorates as disease progresses. Neurosci Lett 2006; 401(1–2): 92–96.
41. Valkovič P, Krafczyk S, Šaling M, Benetin J, Bötzel K. Postural reactions to neck vibration in Parkinson’s disease. Mov Disord 2006; 21(1): 59–65.
42. Braak H, Del Tredici K, Rüb U, de Vos RA, Jansen Steur EN, Braak E. Staging of brain pathology related to sporadic Parkinson’s disease. Neurobiol Aging 2003; 24(2): 197–211.
43. Gdowski GT, McCrea RA. Neck proprioceptive inputs to primate vestibular nucleus neurons. Exp Brain Res 2000; 135(4): 511–526.
44. Jacobs JV, Horak FB. Abnormal proprioceptive-motor integration contributes to hypometric postural responses of subjects with Parkinson’s disease. Neuroscience 2006; 141(2): 999–1009.
45. Mille ML, Johnson Hilliard M, Martinez KM, Simuni T, Rogers MW. Acute effects of a lateral postural assist on voluntary step initiation in patients with Parkinson’s disease. Mov Disord 2007; 22(1): 20–27.
46. Carpenter MG, Allum JH, Honegger F, Adkin AL, Bloem BR. Postural abnormalities to multidirectional stance perturbations in Parkinson’s disease. J Neurol Neurosurg Psychiatry 2004; 75(9): 1245–1254.
47. Hausdorff JM, Schaafsma JD, Balash Y, Bartels AL, Gurevich T, Giladi N. Impaired regulation of stride variability in Parkinson’s disease subjects with freezing of gait. Exp Brain Res 2003; 149(2): 187–194.
48. Nutt JG, Bloem BR, Giladi N, Hallett M, Horak FB, Nieuwboer A. Freezing of gait: moving forward on a mysterious clinical phenomenon. Lancet Neurol 2011; 10(8): 734–744.
49. Kuo SH, Kenney C, Jankovic J. Bilateral pedunculopontine nuclei strokes presenting as freezing of gait. Mov Disord 2008; 23(4): 616–619.
50. Oertel WH, Berardelli A, Bloem BR, Bonuccelli U, Burn D, Deuschl G et al. Joint EFNS/MDS-ES Guidelines on late (complicated) Parkinson’s disease. In: Gilhus NE, Barnes MP, Brainin M (eds). European Handbook of Neurological Management: Volume 1. 2nd ed. Chichester, UK: Blackwell Publishing Ltd. 2011 : 237–267.
51. Litvinenko IV, Odinak MM, Mogiľnaya VI, Emelin AY. Efficacy and safety of galantamine (reminyl) for dementia in patients with Parkinson’s disease (an open controlled trial). Neurosci Behav Physiol 2008; 38(9): 937–945.
52. Bohnen NI, Albin RL. The cholinergic system and Parkinson disease. Behav Brain Res 2011; 221(2): 564–573.
53. Rascol O, Brooks DJ, Melamed E, Oertel W, Poewe W, Stocchi F et al. Rasagiline as an adjunct to levodopa in patients with Parkinson’s disease and motor fluctuations (LARGO, Lasting effect in Adjunct therapy with Rasagiline Given Once daily, study): a randomised, double-blind, parallel-group trial. Lancet 2005; 365(9463): 947–954.
54. Giladi N, Rascol O, Melamed E, Oertel W, Poewe W, Stocchi F et al. Rasagiline treatment can improve freezing of gait in advanced Parkinson’s disease: A prospective randomized, double blind, placebo and entacapone controlled study. Mov Disord 2004; 19 (Suppl): S191–S192.
55. Coria F, Cozar-Santiago Mdel P. Rasagiline improves freezing in a patient with primary progressive freezing gait. Mov Disord 2008; 23(3): 449–451.
56. Boonstra TA, van der Kooij H, Munneke M, Bloem BR. Gait disorders and balance disturbances in Parkinson’s disease: clinical update and pathophysiology. Curr Opin Neurol 2008; 21(4): 461–471.
57. Devos D, Krystkowiak P, Clement F, Dujardin K, Cottencin O, Waucquier N et al. Improvement of gait by chronic, high doses of methylphenidate in patients with advanced Parkinson’s disease. J Neurol Neurosurg Psychiatry 2007; 78(5): 470–475.
58. Espay AJ, Dwivedi AK, Payne M, Gaines L, Vaughan JE, Maddux BN et al. Methylphenidate for gait impairment in Parkinson disease: a randomized clinical trial. Neurology 2011; 76(14): 1256–1262.
59. Baláž M, Bočková M, Bareš M, Rektorová I, Dírerová V, Rektor I. Kvalita života po hluboké mozkové stimulaci u pacientů s pokročilou Parkinsonovou nemocí. Cesk Slov Neurol N 2011; 74/107(5): 564–568.
60. Snijders AH, Nonnekes J, Bloem BR. Recent advances in the assessment and treatment of falls in Parkinson’s disease. F1000 Med Rep 2010; 2 : 76.
61. Ferraye MU, Debû B, Fraix V, Goetz L, Ardouin C, Yelnik J et al. Effects of pedunculopontine nucleus area stimulation on gait disorders in Parkinson’s disease. Brain 2010; 133(Pt 1): 205–214.
62. Oertel WH, Berardelli A, Bloem BR, Bonuccelli U, Burn D, Deuschl G et al. Joint EFNS/MDS-ES Guidelines on early (uncomplicated) Parkinson’s disease. In: Gilhus NE, Barnes MP, Brainin M (eds). European Handbook of Neurological Management: Volume 1. 2nd ed. Chichester: Blackwell Publishing Ltd. 2011 : 217–236.
63. Keus SH, Bloem BR, Hendriks EJ, Bredero-Cohen AB, Munneke M. Evidence-based analysis of physical therapy in Parkinson’s disease with recommendations for practice and research. Mov Disord 2007; 22(4): 451–460.
64. Valkovič P, Schmidt F. Princípy liečebnej rehabilitácie. In: Benetin J, Valkovič P (eds). Parkinsonova choroba. Herba 2009 : 204–212.
65. Morris ME, Perry A, Bilney B, Curran A, Dodd K, Wittwer JE et al. Outcomes of physical therapy, speech pathology, and occupational therapy for people with motor neuron disease: a systematic review. Neurorehabil Neural Repair 2006; 20(3): 424–434.
66. Nieuwboer A. Cueing for freezing of gait in patients with Parkinson’s disease: a rehabilitation perspective. Mov Disord 2008; 23 (Suppl 2): S475–S481.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2012 Issue 2-
All articles in this issue
- Posturálna instabilita, poruchy chôdze a pády pri Parkinsonovej chorobe
- Sulcus temporalis superior a jeho funkční význam
- Algoritmus vyšetření likvoru v návaznosti na doporučení Sekce neuroimunologie a likvorologie České neurologické společnosti JEP
- Využití perkutánní endoskopické gastrostomie – přehled indikací, popis techniky a současné trendy v neurologii
- Diagnostické možnosti zobrazovacích metod v hodnocení morfologického korelátu kognitivních změn u pacientů s roztroušenou sklerózou
- Poruchy výživy a metabolizmu u Parkinsonovy nemoci
- Měření kognitivního deficitu u pacientů po ošetření mozkových aneuryzmat
- Polysomnografické nálezy u dětí s poruchou pozornosti a hyperaktivitou (ADHD) vyšetřovaných pro poruchu spánku
- Léčba neurogenního hyperaktivního detruzoru po spinálním poranění aplikací botulinumtoxinu A. Porovnání endoskopické subslizniční a intramuskulární aplikace
- Naše zkušenosti s laterálním supraorbitálním přístupem při operacích mozkových aneuryzmat
- Zrakové funkce nedonošených dětí s perinatálním mozkovým postižením
- Obstrukční spánková apnoe a CPAP – má význam řešit nosní průchodnost?
- Terapeutické možnosti prevence cévní mozkové příhody u pacientů s karotickým stump syndromem – kazuistiky
- Oligosymptomatické formy myotonické dystrofie typu 2
- Odeznění traumatické pentaplegie u pacienta po kombinované zlomenině C1–C2
- Klinický standard pro diagnostiku a léčbu myasthenia gravis
- Diagnostika a léčba demence českými neurology a psychiatry
- Endoskopická ventrikulostomie III. komory v léčbě hydrocefalu u dětí s mozkovými tumory – zkušenosti jednoho centra
- Detekcia anaplastických ložísk v kontrastnou látkou sa nevýrazne farbiacich infiltratívnych gliómoch pomocou 5-aminolevulovej kyseliny – správa o piatich prípadoch
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Využití perkutánní endoskopické gastrostomie – přehled indikací, popis techniky a současné trendy v neurologii
- Posturálna instabilita, poruchy chôdze a pády pri Parkinsonovej chorobe
- Algoritmus vyšetření likvoru v návaznosti na doporučení Sekce neuroimunologie a likvorologie České neurologické společnosti JEP
- Obstrukční spánková apnoe a CPAP – má význam řešit nosní průchodnost?
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


