-
Medical journals
- Career
Thunderclap headache
Authors: D. Doležil 1; T. Peisker 1; V. Doležilová 2; S. Obermannová 1; V. Janík 3
Authors‘ workplace: Univerzita Karlova v Praze, 3. LF, Neurologická klinikaa FN Královské Vinohrady, Praha 1; RTG oddělení, MEDICON, a. s. 2; Univerzita Karlova v Praze, 3. LF, Radiodiagnostická klinika a FN Královské Vinohrady, Praha 3
Published in: Cesk Slov Neurol N 2010; 73/106(3): 231-236
Category: Review Article
Overview
Thunderclap headache je silná, explozivní bolest hlavy s maximem intenzity během 60 sekund od počátku vzniku bolesti. Primární thunderclap headache má trvání od 1 hodiny do 10 dnů a může být diagnostikována pouze po vyloučení jiných příčin. Nejprve musí být každá thunderclap headache považována za symptomatickou bolest hlavy, jako je např. subarachnoidální krvácení, trombóza mozkových splavů nebo disekce mozkových arterií. Syndrom reverzibilní mozkové vazokonstrikce je rovněž charakterizován obrazem thunderclap headache s výskytem anebo bez přítomnosti neurologických symptomů a s vazokonstrikcí mozkových arterií, která odezní během tří měsíců a je bez průkazu subarachnoidálního krvácení.
Klíčová slova:
thunderclap headache – subarachnoidální krvácení – výstražná bolest hlavy – syndrom reverzibilní mozkové vazokonstrikceÚvod
Thunderclap headache (TCH), v českém překladu „prudce nastupující (blesková) bolest hlavy“, je definována dle Mezinárodní klasifikace bolestí hlavy International Headache Society z roku 2004 (ICHD ‑ II) [1,2] jako těžká, explozivní bolest hlavy s rychlým začátkem a dosažením maxima intenzity během 60 s. Může se jednat o primární anebo sekundární bolest hlavy. Doporučujeme užívat anglický termín thunderclap headache, který nejlépe vystihuje tuto jednotku, analogicky jako užíváme termín cluster headache. Český překlad pojmu thunderclap headache nebo jeho opis se nejeví dostatečně výstižný. Každá TCH by však měla být posuzována při svém vzniku jako sekundární, symptomatická bolest hlavy a pacient s obrazem TCH by měl být neprodleně podroben neurologickému vyšetření. Lokalizace a typ bolesti hlavy (tlaková, ostrá, bodavá atd.) není v tomto případě specifická pro žádný typ příčiny, délka TCH (minuty až dny) však může s charakterem primární příčiny souviset. TCH může mít charakter ojedinělé, izolované ataky anebo může být rekurentní. TCH může vzniknout spontánně nebo může být vyvolán spouštěčem, např. fyzickou aktivitou, pohlavním stykem či Valsalvovým manévrem. Klasifikaci a charakteristiku primární TCH ukazuje tab. 1, sekundární příčiny vzniku TCH (vaskulární a nevaskulární) zobrazuje tab. 2. Primární TCH je klasifikována ICHD - II [1,2] pod kódem 4.6. Tento kód můžeme použít jen pro primární TCH a nemá být aplikován pro obraz TCH splňující kritéria pro tyto jiné primární bolesti hlavy:
- primární bolest hlavy v souvislosti s kašlem (ICHD ‑ II, kód 4.2),
- ponámahová primární bolest hlavy (ICHD ‑ II, kód 4.3),
- bolest hlavy asociovaná se sexuální aktivitou (ICHD ‑ II, kód 4.4) [1,2].
Table 1. ICHD-II klasifikace – 4.6. Primární thunderclap headache. 
Nejčastější a patrně nejzávažnější sekundární příčinou TCH je subarachnoidální krvácení (SAH), velice zajímavou a patrně poddiagnostikovanou příčinou TCH je syndrom reverzibilní mozkové vazokonstrikce (RCVS, reversibile cerebral vasoconstriction syndrome).
Primární TCH
Primární TCH může být diagnostikována po vyloučení všech ostatních možných příčin TCH. Pro diagnózu musí být splněna kritéria ICHD ‑ II (tab. 1). Rychle nastupující cefalea s délkou trvání od 1 hod do 10 dnů není doprovázena žádným jiným neurologickým symptomem. Bolest hlavy se může v průběhu prvního týdne zopakovat, nesmí se však pravidelně navracet v následujících týdnech a měsících. Sekundární příčina TCH (tab. 2) musí být jednoznačně vyloučena anamnézou, neurologickým vyšetřením a zobrazovacími metodami včetně zobrazení intrakraniálního cévního řečiště a laboratorními paraklinickými metodami. Rovněž musí být odlišeny již zmíněné jiné primární bolesti hlavy, jako jsou bolesti hlavy v souvislosti s kašlem, fyzickou a sexuální aktivitou (kterou dělíme dále na preorgasmickou bolest hlavy a orgasmickou cefaleu), ale také např. migrénu nebo cluster headache. Incidence primární TCH není příliš vysoká, protože TCH je obvykle symptomem jiné sekundární nebo primární bolesti hlavy.
Table 2. Sekundární příčiny vzniku thunderclap headache. 
Sekundární příčiny TCH
Vaskulární i nevaskulární sekundární příčiny TCH ukazuje tab. 2. Ze všech těchto onemocnění je obvykle nejobtížnější diagnostika RCVS. Klinicky nejzávažnější jsou všechny typy krvácivých a ischemických cévních mozkových příhod, se zvláštním zřetelem na SAH, jež bývá často nesprávně diagnostikován. Diferenciálnědiagnostický problém přináší tzv. výstražná bolest hlavy (STH, sentinel headache), která předchází diagnóze SAH, protože podle dostupných dat 10 – 43 % pacientů se SAH má anamnézu výstražné bolesti hlavy [3], která má charakter TCH. Při negativním neurologickém vyšetření a výpočetní tomografii (CT) mozku bývá mylně tato výstražná cefalea často diagnostikována jako migréna nebo cervikokraniální syndrom. Diagnostické problémy mohou provázet v klinické praxi i TCH na podkladě trombózy splavů a disekce mozkových arterií.
Syndrom reverzibilní mozkové vazokonstrikce
RCVS byl v literatuře popsán u pacientů ve věku mezi 13 – 70 lety s četnější incidencí u žen [4 – 6,], ale větší epidemiologické studie chybí. RCVS je charakterizován TCH, s přítomností nebo bez ložiskových neurologických symptomů (hemiparéza, dysartrie, afázie, ataxie atd.), s epileptickým záchvatem nebo bez něj a s nálezem vazokonstrikce mozkových arterií [7]. Tento syndrom měl v minulosti mnoho eponymních a syndromologických označení, zahrnující Call‑Flemingův syndrom, benigní angiopatii centrálního nervového systému, TCH s reverzibilním vazospazmem, migrenózní vazospazmus a migrenózní angiopatie a léky vyvolaná mozková arteritida a angiopatie [8]. Název RCVS byl použit Calabresem v roce 2007 na podkladě zpracování dat a publikace případů tohoto syndromu během minulých let pod různými názvy [4,9 – 11]. Patofyziologický mechanizmus RCVS je neznámý, předpokládá se přechodná porucha kontroly cévního tonu vedoucí k segmentální a multifokální arteriální vazokonstrikci (obr. 1, 2). RCVS může být primární (idiopatický) nebo sekundární (tab. 3) [7,8]. Určité překrytí RCVS je patrno s jinou vzácnější jednotkou, tzv. zadním reverzibilním encefalopatickým syndromem (PRES, posterior reversible encephalopathy syndrome), ale vztah mezi RCVS a PRES, případně hypertenzní encefalopatií není vyjasněn. PRES je charakterizován edémem bílé a šedé hmoty symetricky predilekčně v parieto ‑ okcipitální oblasti, temporo‑okcipitální junkci, případně v mozkovém kmeni a mozečku a může být doprovázen až v 15 % případů intracerebrálním nebo subarachnoidálním krvácením a nebo mozkovým infarktem v oblastech těžké hypoperfuze (obr. 3). Hemoragie v rámci RCVS jsou pravděpodobně důsledkem reperfuzního postižení [9]. RCVS je častý, ale ne konstantně přítomen u PRES. Zhruba 20 – 30 % případů PRES není doprovázeno hypertenzí. PRES u normotenzních pacientů má extenzivnější vazogenní edém než u pacientů s hypertenzí, a proto se zvažuje, že by hypertenze mohla být reaktivní odezvou na zvýšení rychlosti mozkového průtoku [7,8,12 – 15].
Image 1. Vyšetření TCCS. Segmentální vazospazmy ve střední mozkové tepně vlevo u pacientky s RCVS, dva týdny po prvním TCH. 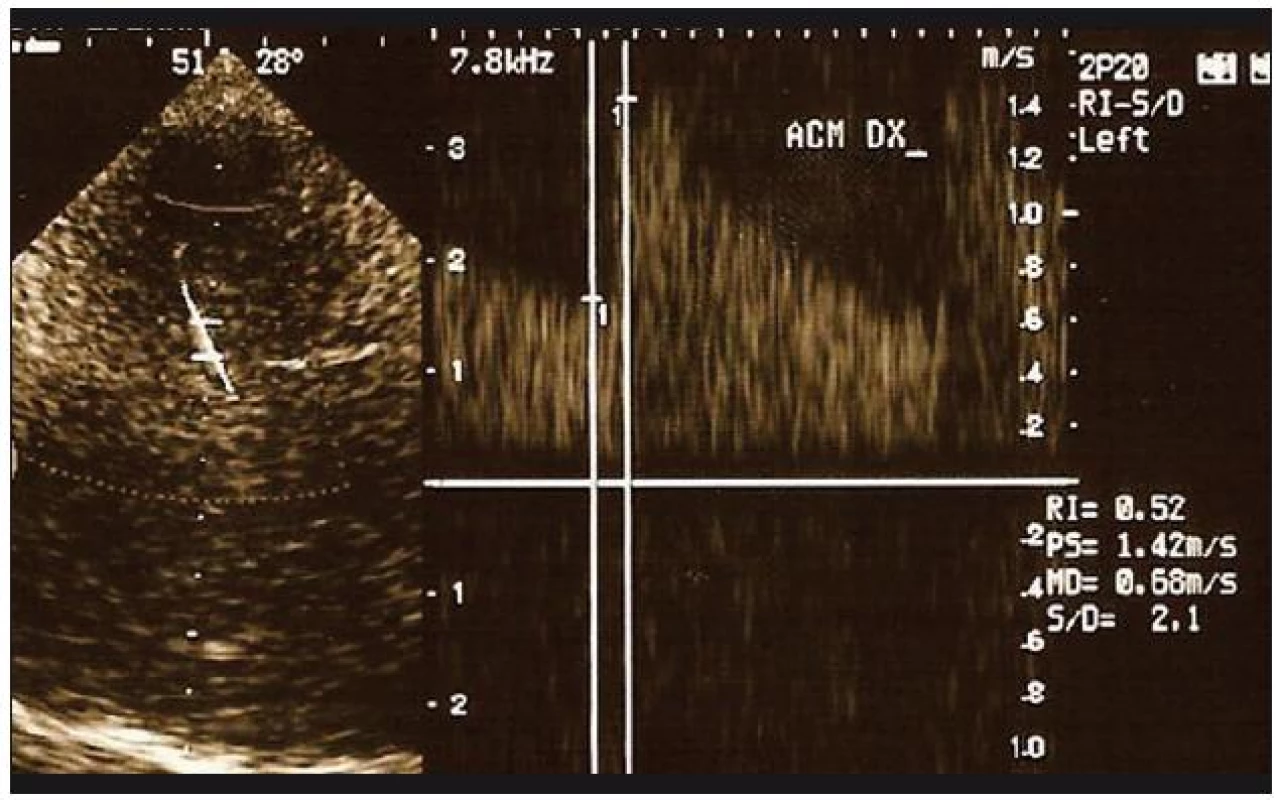
Image 2. Vyšetření TCCS. Normalizace průtoků ve střední mozkové tepně u téže pacientky – vyšetření s odstupem čtyř týdnů od prvního vyšetření. 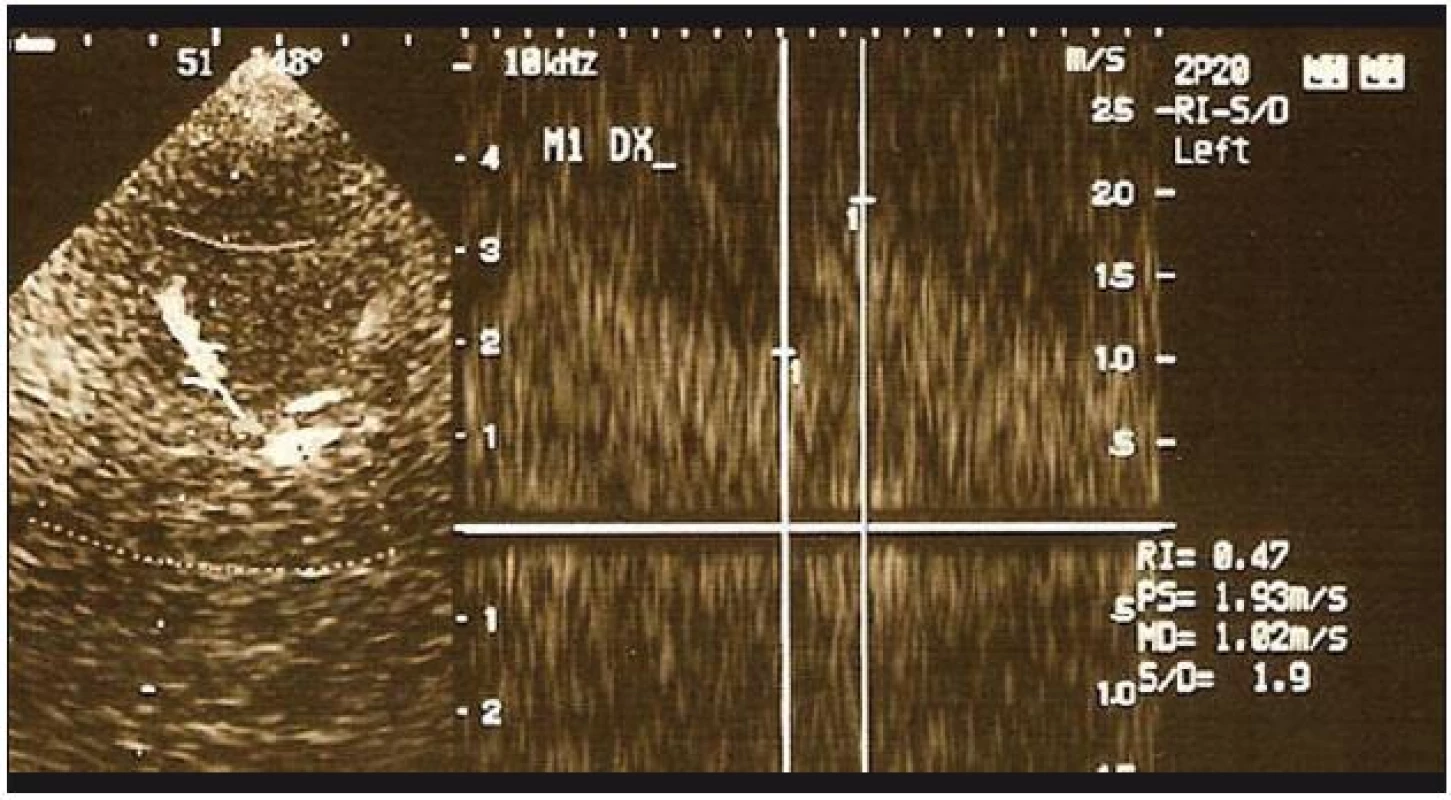
Table 3. Možné příčiny sekundárního RCVS. 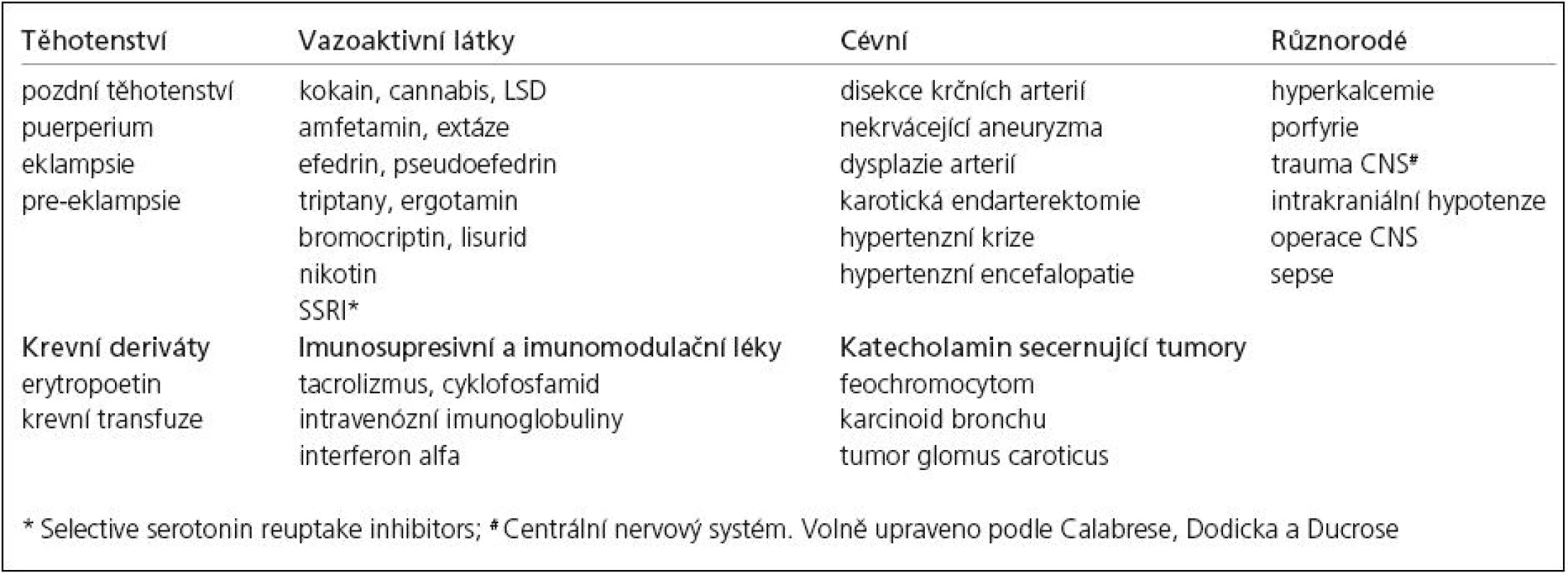
Image 3. Vyšetření MR mozku, FLAIR. Akutní ischemické ikty v polech obou okcipitálních laloků, vzniklých jako následek RCVS, odpovídající obrazu PRES. 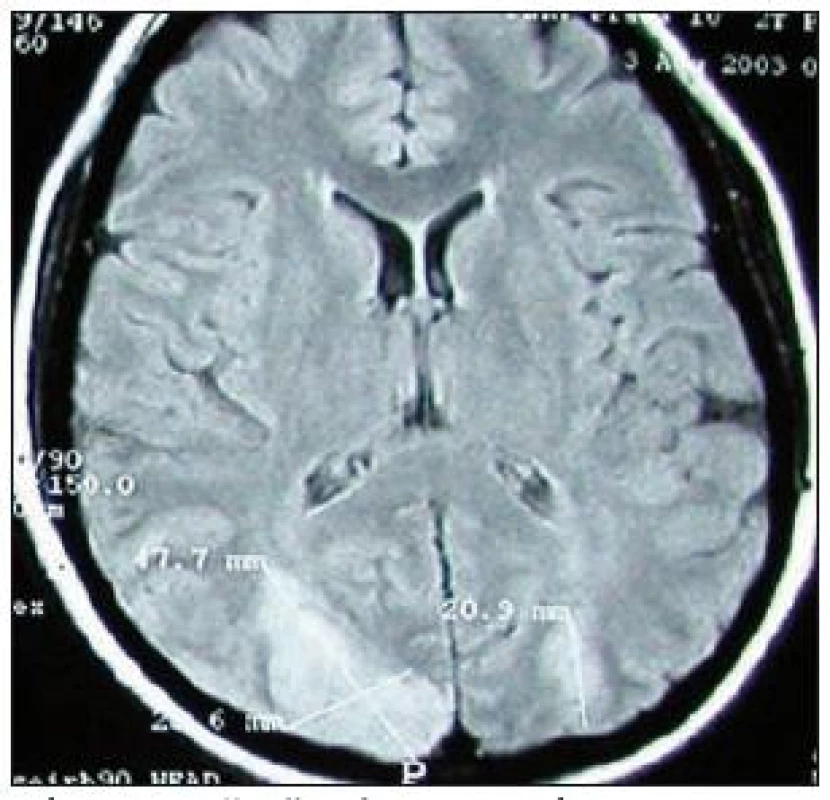
Klinický obraz RCVS je dán až v 75 % jen obrazem TCH. Patognomická je rekurence TCH, může se opakovat několikrát i v rámci jednoho dne a vracet se po období 1 – 4 týdnů. Bolest hlavy je lokalizována oboustranně se začátkem obvykle okcipitálně, charakteru TCH, doprovázena neklidem, agitovaností, nezřídka i s křikem a nářky. Často jsou také přítomny další symptomy, jako jsou nauzea, zvracení, fotofobie a fonofobie. RCSV však může být doprovázen obrazem jen jednotlivé ataky TCH. V zobrazovacích metodách – magnetické rezonanci (MR) nebo CT mozku – lze nalézt během prvního týdne ve zhruba 20 % případů lokalizované kortikální subarachnoidální krvácení, v 10 % případů pak nález MR mozku odpovídá obrazu PRES (obr. 3), fokální intracerebrální hemoragie se nachází v 6 % případů. Obvykle ve druhém týdnu trvání RCVS se vyskytne ve zhruba 4 % případů jednotlivý nebo vícečetný mozkový infarkt. Jsou známy i nálezy subdurálního hematomu. Na angiografickém vyšetření vidíme obraz segmentálních stenóz na jedné nebo více arteriích (obr. 4, 5). K vyšetření se primárně doporučuje jako zlatý standard katétrová angiografie, protože senzitivita MR angiografie (MRA) a nebo CT angiografie (CTA) je pouze 80%, nicméně dostupnost, neinvazivita a možnost opakování vyšetření ke sledování dynamiky činí MRA a nebo CTA nepostradatelným vyšetřením. První angiografické vyšetření, jestliže je provedeno v časné fázi, tedy do pátého dne od začátku symptomů, může být negativní, a proto se doporučuje angiografické vyšetření v případě potřeby opakovat za 7 – 14 dnů od začátku symptomů. Zásadní postavení v diagnóze má také ultrazvukové vyšetření, a to jak extrakraniální vyšetření k vyloučení disekce krčních tepen, tak transkraniální doppler, který můžeme použít k jednoduchému monitorování vazospazmů. Maximum intrakraniální průtokové rychlosti můžeme vidět okolo 22. dne po vzniku RCVS, nebo paradoxně v období, kdy bolest hlavy začíná ustupovat. Normalizace angiografického nálezu by měla nastat do 12 týdnů od začátku symptomů [7,8]. Vyšetření likvoru je u RCVS normální nebo lehce abnormální bez signifikantního obrazu pro RCVS (např. zvýšená bílkovina). Diagnostická kritéria RCVS ukazuje tab. 4.
Image 4. DSA obraz vícečetných segmentálních stenóz (vazospazmů) na pravé středních mozkové tepně u pacientky s RCVS. 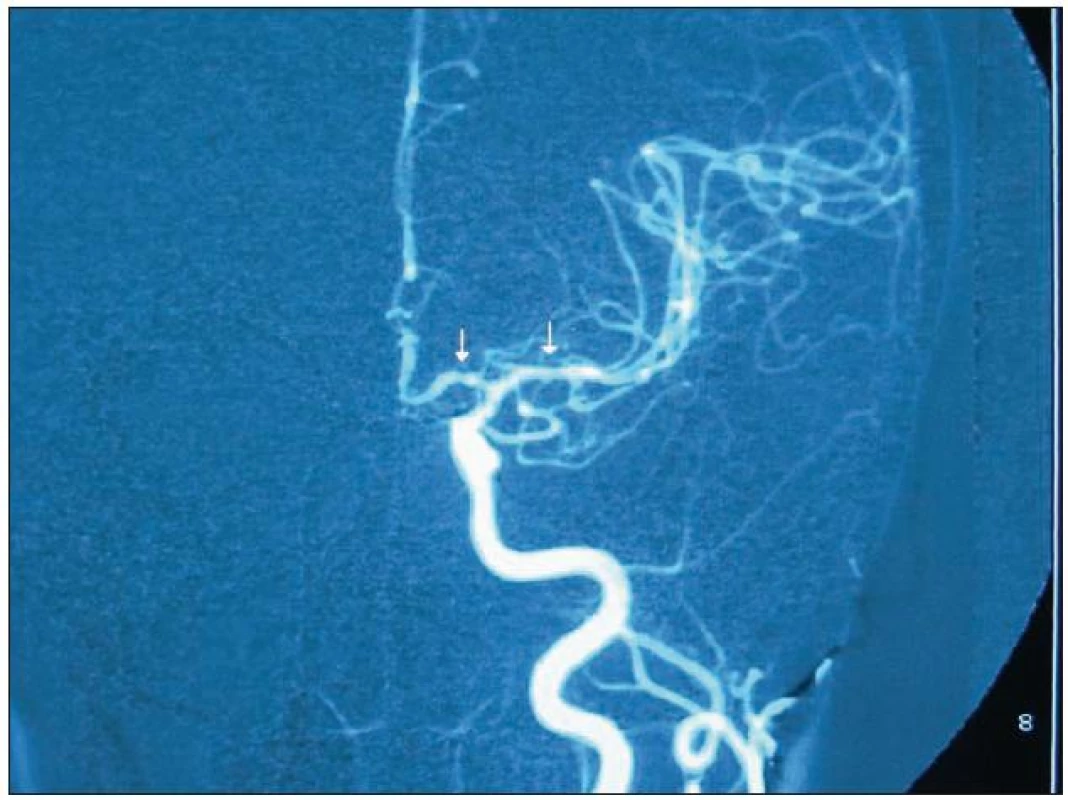
Image 5. DSA obraz segmentálních stenóz (vazospazmů) na zadních mozkových tepnách u pacientky s RCVS. 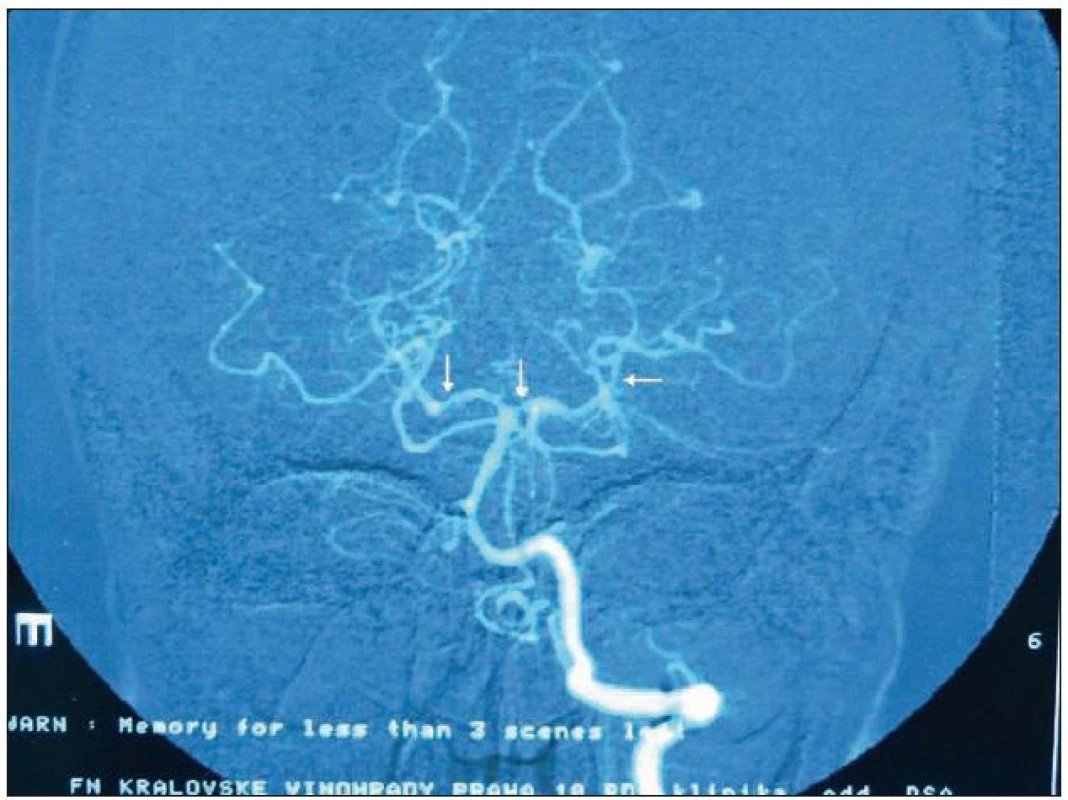
Table 4. Diagnostická kritéria pro RCVS. 
Další sekundární příčiny thunderclap headache
Z klinického hlediska je potřeba nejvíce upozornit na STH u nekrvácejícího nebo u tzv. plačícího aneuryzmatu, která předchází několik dnů anebo týdnů ruptuře aneuryzmatu s diagnostikovatelným SAH. Tyto bolesti hlavy mají charakter TCH a perzistují hodiny až dny. Nejpravděpodobněji vznikají aktivací vaskulární senzitivní aferentace na podkladě roztažení a rozepětí stěny aneuryzmatu anebo drobným nedetekovatelným krvácením (tzv. warning leak). Zhruba u 25 – 50 % pacientů s proběhlým SAH není STH před rupturou správně diagnostikována [3,16]. Chybná diagnóza může být způsobena nízkou citlivostí nativního CT vyšetření mozku u velmi malého krvácení anebo vyšetření CT mozku po více než 24 hod od začátků příznaků a neprovedením vyšetření likvoru v těchto případech. Pro správnou diagnózu se doporučuje vždy udělat vyšetření likvoru a MR mozku (T2 vážený obraz a sekvence gradientního echa) a MRA mozkových cév. Pokud má aneuryzma velikost 6 mm a více, je senzitivita MRA 95 % [17]. Jiná intracerebrální krvácení, která jsou spojena s obrazem TCH, jsou obvykle dobře diagnostikovatelná akutním CT vyšetřením mozku. Pro potvrzení ischemické cévní mozkové příhody jako příčiny TCH využíváme v akutní diagnostice difuzně vážené MR sekvence, hledáme časné známky ischemie v CT obraze nebo patologii v perfuzním CT mozku. Cefalea je vedoucím příznakem také u trombózy mozkových splavů (TMS) [8] a je přítomna spolu s dalšími neurologickými příznaky, ale u zhruba 15 – 30 % pacientů je bolest hlavy jediným příznakem, přičemž obraz TCH má 2 – 10 % pacientů s TMS [18,19]. Obraz TCH jako příznak TMS je častější v období šestinedělí [20]. Disekce mozkových arterií je doprovázena bolestí hlavy v 60 – 95 % případů, u disekce vertebrálních arterií je bolest hlavy reportována v 70 % případů, z toho asi ve 20 % případů má charakter TCH [21,22]. Ve shodě s klasifikací ICH ‑ II musí být bolest hlavy na podkladě karotické disekce ipsilaterální lokalizace, často se jedná také o bolest krku a prosopalgii. I když se bolest hlavy u disekce karotické nebo vertebrální arterie vyskytuje jen zřídka izolovaně bez jiné neurologické symptomatiky, může bolest hlavy tyto symptomy předcházet. Podle Silberta [21] je medián doby trvání od začátku bolestí hlavy k ložiskovým neurologickým projevům u disekce karotické arterie čtyři dny a u disekce vertebrální arterie 14,5 hod. U relativně vzácné pituitární apoplexie (pituitární krvácení obvykle do tumoru nebo ischemie) byl rovněž referován obraz TCH jako první příznak tohoto onemocnění [23 – 25]. V těchto případech se vždy doporučuje doplnit vyšetření MR mozku, protože případný nádor je izodenzní a na CT vyšetření hůře diagnostikovatelný. Zánětlivou etiologii TCH obvykle bez obtíží stanovíme na podkladě zobrazovacích a laboratorních nálezů, stejně tak jako tumor centrálního nervového systému (CNS) nebo Arnold ‑ Chiariho malformaci typ I. Diferenciálně‑diagnostické potíže mohou nastat v případě rozlišení RCVS a izolované mozkové arteritidy, nazývané také primární angiitis CNS (PACNS) [26]. V klinickém obraze PANCS je bolest hlavy se subakutním začátkem a má progresivní charakter, nemá tedy typický charakter TCH. V likvoru najdeme často zánětlivé změny, v MR obraze pak multiinfarktové postižení kůry a podkoří, s difuzním postižením bílé hmoty. Angiografické vyšetření nám ukáže stenózy a dilatace cév s uzávěry arterií a vytvořeným koletarálním řečištěm. Spontánní intrakraniální hypotenze (SIH), která se projevuje jako poziční bolest hlavy a přichází nebo se zhoršuje v sedu či ve stoji, se může až v 15 % případů také projevovat jako THC [27 – 29]. MR mozku s gadoliniem může odhalit některý z obrazů svědčící pro SIH (např. pachymeningeální enhancement, sestup mozečkových tonzil, redukce prepontinního prostoru), ale může být také zcela normální [8]. V dovyšetření stavu se doporučuje pátrat po úniku likvoru.
Terapie
Terapie se odvíjí od diagnózy primárního onemocnění, které je u výše popsaných stavů obecně známa. U RCVS jsou v literatuře jen kusé informace o terapii a terapeutickém efektu jednotlivých léků, např. kortikoidů [30], blokátorů kalciového kanálu [31,32], ale neexistují žádné randomizované studie, které by efekt některého léku v terapii RCVS potvrdily. Na podkladě empirických zkušeností a předpokládaného efektu se doporučuje podávat nimodipin ve stejném dávkovacím schématu jako u subarachnoidálního krvácení z aneuryzmatu, případně se doporučuje verapamil v obvyklých dávkách [7,8]. Recentně byla uveřejněna práce kanadských autorů o efektu intraarteriálně podávaného milrinonu [33]. V případě primárního TCH nebo obrazu TCH na podkladě jiné primární bolesti hlavy jsou základním lékem analgetika.
Doporučení
Základním doporučením je nepodcenit příznaky TCH a věnovat diagnostice a diferenciální diagnostice dostatek pozornosti v akutní neurologické ambulanci. Především je vždy potřeba vyloučit onemocnění, která při negativním neurologickém vyšetření a falešně negativním akutním CT mozku často unikají pozornosti, jako jsou zejména SAH, nekrvácející aneuryzma, trombóza splavů a disekce mozkových arterií. Pokud se v algoritmu vyšetření podaří tyto diagnózy vyloučit, je potřeba myslet na vzácnější jednotky, jako jsou RCVS, jež má pravděpodobně častější výskyt, než se dříve předpokládalo, nebo např. PRES syndrom. Teprve po vyloučení všech sekundárních příčin TCH lze stanovit diagnózu primární TCH nebo TCH jako symptomu jiné primární bolestí hlavy, jak jsme se o ní zmínili v úvodu. Tab. 5 přináší návrh doporučeného diagnostického postupu a praktických doporučení v diferenciální diagnostice sekundárního TCH. Pro MR vyšetření TCH v rámci tohoto algoritmu navrhujeme protokol vyšetření, který obsahuje standardně užívané sekvence k morfologickému vyšetření mozku i speciální techniky:
- T2 vážené sekvence rychlého spinového echa (TSE) v transverzální rovině,
- T1 vážené sekvence spinového echa (SE) v sagitální rovině,
- T2 vážené inversion recovery sekvence s potlačením signálu likvoru (FLAIR),
- sekvence k zobrazení difuze (DWI), jejíž součástí je ADC mapa detekující mozkovou ischemii, krvácení a přítomnost expanzivního procesu,
- MRA intrakraniálních tepen provádíme technikou Time ‑ Of ‑ Flight (TOF), v rozsahu od foramen magnum po úroveň větvení střední mozkové tepny v inzule,
- MRA venografie metodou fázového kontrastu (PC 3D),
- postkontrastní vyšetření provádíme po nitrožilní aplikaci Gd ‑ kontrastní látky v příslušném množství, vzhledem k její koncentraci a hmotnosti pacienta v T1 SE v transverzální a koronární rovině.
Table 5. Postup paraklinických vyšetření v diferenciální diagnostice thunderclap headache. 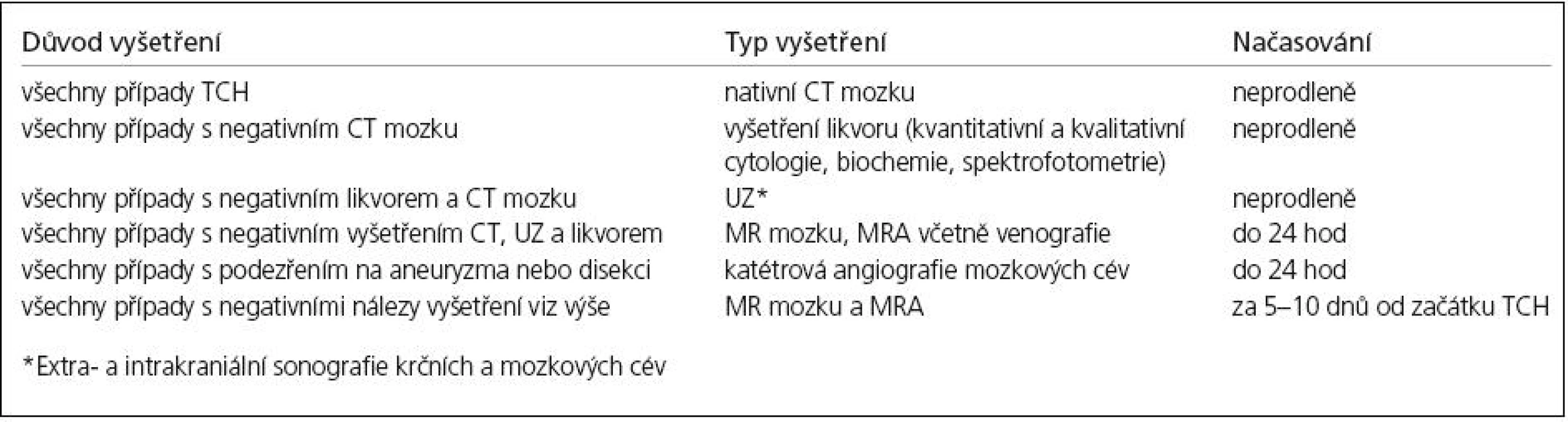
MUDr. David Doležil, Ph.D.
Univerzita Karlova v Praze, 3. LF,
Neurologická klinika a FN Královské Vinohrady, Praha
Šrobárova 50
100 34 Praha 10
e-mail: dolezil@fnkv.czPřijato k recenzi: 23. 11. 2009
Přijato do tisku: 20. 4. 2010
Sources
1. Headache Classification Subcommittee of the international Headache Society. The international classification of headache disorders. 2nd ed. Cephalalgia 2004; 2 (Suppl 1): 9 – 160.
2. Opavský J, Keller O, Kotas R, Mastík J, Marková J, Rejda et al. Česká verze revidované Mezinárodní klasifikace bolestí hlavy (ICHD ‑ II) navržené a předložené Mezinárodní společností pro bolesti hlavy. Cesk Slov Neurol N 2005; 68/ 101(2): 133 – 138.
3. Polmear A. Sentinel headaches in aneurysmal subarachnoid haemorrhage: what is the true incidence? A systematic review. Cephalalgia 2003; 23 : 935 – 941.
4. Ducros A, Boukobza M, Porcher R, Sarov M, Valade D, Bousser MG. The clinical and radiological spectrum of reversible cerebral vasoconstriction syndrome. A prospective series of 67 patients. Brain 2007; 130(12): 3091 – 3101.
5. Chen SP, Fuh JL, Lirng JF, Chang FC, Wang SJ. Recurrent primary thunderclap headache and benign CNS angiopathy: spectra of the same disorder? Neurology 2006; 67(12): 2164 – 2169.
6. Kirton A, Diggle J, Hu W, Wirrell E. A pediatric case of reversible segmental cerebral vasoconstriction. Can J Neurol Sci 2006; 33(2): 250 – 253.
7. Ducros A, Bousser MG. Reversible, cerebral vasoconstriction syndrome. Pract Neurol 2009; 9(5): 256 – 267.
8. Dodick DW, Wijdicks EF, Ducros A. Emergency headache, including thunderclap headache. In: Dalesio DJ (ed). Wolff’s Headache and other head pain. 8th ed. New York: Oxford University Press 2008 : 747 – 765.
9. Calabrese LH, Dodick DW, Schwedt TJ, Singhal AB. Narrative review: reversible cerebral vasoconstriction syndrome. Ann Intern Med 2007; 146(1): 34 – 44.
10. Dodick DW, Brown RD Jr, Britton JW, Huston J3rd. Nonaneurysmal thunderclap headache with diffuse, multifocal, segmental, and reversible vasospasm. Cephalalgia 1999; 19(2): 118 – 123.
11. Call GK, Fleming MC, Sealfon S, Levine H, Kistler JP, Fisher CM. Reversible cerebral segmental vasoconstriction. Stroke 1988; 19(9): 1159 – 1170.
12. Bartynski WS. Posterior reversible encephalopathy syndrome, part 1: fundamental imaging and clinical features. AJNR Am J Neuroradiol 2008; 29(6): 1036 – 1042.
13. Bartynski WS. Posterior reversible encephalopathy syndrome, part 2: controversies surrounding pathophysiology of vasogenic edema. AJNR Am J Neuroradiol 2008; 29(6): 1043 – 1049.
14. Lee VH, Wijdicks EF, Manno EM, Rabinstein AA. Clinical spectrum of reversible posterior leukoencephalopathy syndrome. Arch Neurol 2008; 65(2): 205 – 210.
15. Doss ‑ Esper CE, Singhal AB, Smith MS, Henderson GV. Reversible posterior leukoencephalopathy, cerebral vasoconstriction, and strokes after intravenous immune globulin therapy in Guillain‑Barre syndrome. J Neuroimaging 2005; 15(2): 188 – 192.
16. Edlow JA, Caplan LR. Avoiding pitfalls in the diagnosis of subarachnoidal hemorrhage. N Engl J Med 2000; 342(1): 29 – 36.
17. Sato M, Nakano M, Sasanuma J, Asari J, Watanabe K. Preoperative cerebral aneurysm assessment by three ‑ dimensional magnetic resonance angiography: feasibility of surgery without conventional catheter angiography. Neurosurgery 2005; 56(5): 903 – 912.
18. de Bruijn SF, Stam J, Kappelle LJ. Thunderclap headache as the first symptom of cerebral venous sinus thrombosis. CVTS study group. Lancet 1996; 348(9042): 1623 – 1625.
19. Cumurciuc R, Crassard I, Sarov M, Valade D, Bousser MG. Headache as the only neurological sign of cerebral venous thrombosis: a series of 17 cases. J Neurol Neurosurg Psychiatry 2005; 76(8): 1084 – 1087.
20. Cantú C, Barinagarrementeria F. Cerebral venous thrombosis associated with pregnancy and puerperium. Review of 67 cases. Stroke 1993; 24(12): 1880 – 1884.
21. Silbert PL, Mokri B, Schievink WI. Headache and neck pain in spontaneous internal carotid and vertebral artery dissections. Neurology 1995; 45(8): 1517 – 1522.
22. Mitsias P, Ramadan NM. Headache in ischemic cerebrovascular disease. Part I: clinical features. Cephalalgia 1992; 12(5): 269 – 274.
23. Embil JM, Matthias K, Kinnear R. A blinding headache. Lancet 1997; 350 : 182.
24. Dodick DW, Wijdicks EF. Pituitary apoplexy presenting as a thunderclap headache. Neurology 1998; 50(5): 1510 – 1511.
25. Macháčková M, Látr I, Hejcmanová D. Oční manifestace u pituitární apoplexie – kazuistika. Cesk Slov Neurol N 2009; 72/ 105(5): 456 – 460.
26.Koopman K, Uyttenboogaart M, Luijckx GJ, De Keyser J, Vroomen PC. Pitfalls in the diagnosis of reversible cerebral vasoconstriction syndrome and primary angiitis of the central nervous system. Eur J Neurol 2007; 14(10): 1085 – 1087.
27. Schievink WI, Wijdicks EF, Meyer FB, Sonntag VK. Spontaneous intracranial hypotension mimicking aneurysmal subarachnoid hemorrhage. Neurosurgery 2001; 48(3): 513 – 517.
28. Mokri B. Headaches caused by decreased intracranial pressure: diagnosis and management. Curr Opin Neurol 2003; 16(3): 319 – 326.
29. Ferrante E, Savino A. Thunderclap headache caused by spontaneous intracranial hypotension. Neurol Sci 2005; 26 (Suppl 2): S155 – S157.
30. Hajj ‑ Ali RA, Furlan A, Abou ‑ Chebel A, Calabrese LH. Benign angiopathy of the central nervous system: cohort of 16 patients with clinical course and long ‑ term follow‑up. Arthritis Rheum 2002; 47(6): 662 – 669.
31. Dodick DW. Reversible segmental cerebral vasoconstriction (Call‑Fleming syndrome): the role of calcium antagonists. Cephalalgia 2003; 23(3): 163 – 165.
32. Lu SR, Liao YC, Fuh JL, Lirng JF, Wang SJ. Nimodipine for treatment of primary thunderclap headache. Neurology 2004; 62(8): 1414 – 1416.
33. Bouchard M, Verreault S, Gariepy J, Dupre N. Intraarterial milrinone for reversible cerebral vasoconstriction syndrome. Headache 2009; 49(1): 142 – 145.
Labels
Paediatric neurology Neurosurgery Neurology
Article was published inCzech and Slovak Neurology and Neurosurgery

2010 Issue 3-
All articles in this issue
- Poraněný torakolumbální disk – indikace k náhradě předním přístupem podle magnetické rezonance
- Porovnání tíže afázie u demence a cévní mozkové příhody pomocí MASTcz a její vztah k tíži kognitivního deficitu
- Standardizace české verze The Confusion Assessment Method for the Intensive Care Unit (CAM‑ICUcz)
- Změny na perfuzní počítačové tomografii po konvenčním extra‑ intrakraniálním bypassu
- Zlomeniny pátého bederního obratle
- Sexuální dysfunkce a jejich výskyt u pacientů s epilepsií
- Využití regionální mozkové oxymetrie jako neinvazivní metody ke sledování pacientů v neurointenzivní péči
- Zhodnocení výsledků operací karotických tepen v letech 1997– 2009
- Chirurgická léčba neuroepitelových nádorů na přední straně kosti křížové – kazuistiky
- Komplikovaná herpetická nekrotizující meningoencefalitida s nutností neurochirurgické intervence – kazuistika
- Spondylogenní cervikální myelopatie
- Vyšetřovací metody cerebrovaskulární rezervní kapacity v nukleární medicíně a ostatní komplementární metody
- Thunderclap headache
- Kompletní úprava sluchu u vestibulárního schwannomu s opakovanou náhlou ztrátou sluchu
- Czech and Slovak Neurology and Neurosurgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Spondylogenní cervikální myelopatie
- Zlomeniny pátého bederního obratle
- Standardizace české verze The Confusion Assessment Method for the Intensive Care Unit (CAM‑ICUcz)
- Komplikovaná herpetická nekrotizující meningoencefalitida s nutností neurochirurgické intervence – kazuistika
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

