-
Medical journals
- Career
Pokročilé léčebné strategie metastatického kolorektálního karcinomu a karcinomu pankreatu
Published in: Klin Onkol 2024; 37(1): 68-73
Category:
„Cílem třetí a vyšších linií léčby onkologických onemocnění je především kontrola onemocnění a udržení kvality života nemocného i jeho výkonnostního stavu,“ uvedl úvodem minikolokvia pořádaného s podporou společnosti Servier v rámci programu letošního ročníku Pražského mezioborového onkologického kolokvia prof. Gerald Prager z Comprehensive Cancer Center MedUni Wien, Rakousko.
Prof. Prager dále uvedl, že přibližně devět z deseti pacientů s metastatickým kolorektálním karcinomem (mCRC), kteří dojdou až do třetí linie, již bylo předléčeno cílenou terapií, popřípadě jejich nádor není nositelem žádného v současnosti známého terapeuticky ovlivnitelného molekulárního cíle. Že i navzdory tomu lze ve vyšších liniích dosahovat lepších výsledků, aktuálně dokazují výsledky studie SUNLIGHT.
Poprvé překonána meta 10 měsíců přežití ve třetí linii léčby mCRC
Studie SUNLIGHT byla mezinárodní, otevřená, aktivně kontrolovaná, randomizovaná studie fáze III, která ověřila účinnost a bezpečnost přidání bevacizumabu k dosavadnímu standardu třetí linie léčby mCRC trifluridinu/ tipiracilu.
„Povoleny byly striktně jen dvě předchozí absolvované léčby – chemoterapie založená na fluoropyrimidinu, oxaliplatině a irinotekanu a léčba anti-VEGF protilátkami u pacientů s nemutovaným RAS protilátkami proti EGFR,“ připomněl prof. Prager.
Přidání bevacizumabu k trifluridinu/ tipiracilu přineslo oproti trifluridinu/ tipiracilu v monoterapii signifikantní prodloužení mediánu doby celkového přežití (OS) na 10,8 vs. 7,5 měsíce (p < 0,001), relativní riziko úmrtí bylo sníženo o 39 %. „Překonání hranice 10 měsíců celkového přežití jsme dosud v žádné studii třetí linie léčby mCRC neviděli. Snížení rizika úmrtí o 39 % je vynikající výsledek, obzvláště vezmeme-li v úvahu, že jej bylo dosaženo oproti aktivnímu komparátoru,“ zdůraznil prof. Prager.
Křivky celkového přežití se ve studii SUNLIGHT oddělily velmi časně, již po 3 měsících, a rozdíl přetrvával po celou dobu sledování. Míra 6měsíčního přežití pacientů dosáhla 77 vs. 61 % a 12měsíčního přežití 43 vs. 30 % ve prospěch kombinace trifluridinu/ tipiracilu s bevacizumabem oproti trifluridinu/ tipiracilu v monoterapii. Lepší přežívání bylo potvrzeno ve všech podskupinách pacientů. „Ve studii SUNLIGHT z kombinační léčby pacienti profitovali bez ohledu na mutační stav RAS. Nezáleželo ani na tom, zda v minulosti již užívali bevacizumab nebo nikoli,“ dodal prof. Prager (obr. 1).
Signifikantní bylo i prodloužení mediánu doby bez progrese onemocnění (PFS) na 5,6 vs. 2,4 měsíce (p < 0,001), což představuje snížení relativního rizika progrese onemocnění nebo smrti o 56 %. Také v tomto případě se od sebe začaly výsledky lišit velmi časně a efekt byl setrvalý – 6měsíčního PFS dosáhlo 43 vs. 16 % a 12měsíčního PFS 16 vs. 1 % pacientů.
Objektivní míra odpovědí (ORR) při kombinační léčbě činila 6,3 % oproti 0,9 % v kontrolním rameni – nemusí se zdát, že je to mnoho, ale jak zdůraznil prof. Prager, těžko lze ve třetí linii léčby očekávat nějaký lepší výsledek. Z tohoto pohledu je podle něj pozoruhodné, kolik pacientů dosáhlo kontroly onemocnění – 76,6 vs. 47 %, absolutní rozdíl je 39,6 % ve prospěch kombinace trifluridinu/ tipiracilu s bevacizumabem oproti trifluridinu/ tipiracilu v monoterapii.
Důležitým cílem v onkologické léčbě vyšších linií je, aby nevedla ke zhoršení celkového stavu pacientů. Přidání bevacizumabu k trifluridinu/ tipiracilu nejenže nemělo za následek zhoršení, ale naopak prodloužilo dobu prožitou v dobrém klinické stavu na 9,3 vs. 6,3 měsíce (p < 0,001). Relativní riziko zhoršení do ECOG PS ≥ 2 bylo sníženo o 46 %. Jak připomněl prof. Prager, souvisí to i s bezpečnostním profilem léčby. Ve studii SUNLIGHT nebyly po přidání bevacizumabu k trifluridinu/ tipiracilu zaznamenány rozdíly ve výskytu závažných nežádoucích účinků stupně ≥ 3 (72 vs. 70 %) ani nežádoucích účinků vedoucích k ukončení léčby (shodně 13 % v obou ramenech).
Celkově vyšší byl po přidání bevacizumabu jen výskyt neutropenie (62 vs. 51 %), která je ovšem, jak zdůraznil prof. Prager, v klinické praxi standardně dobře zvládnutelná, dále hypertenze (10 vs 2 %) a nevolnosti.
Ve studii SUNLIGHT byla hodnocena i kvalita života prostřednictvím dvou dotazníků – pro pacienty s karcinomem specifického dotazníku QLQ C30 a obecnějšího EQ-5D-5L. Skóre
QLQ C30 zůstávalo beze změny po celou dobu léčby – jak celkově, tak ve funkční i symptomatické doméně samostatně. Riziko definitivního zhoršení kvality života o 10 bodů podle QLC 30 bylo při léčbě kombinací trifluridinu/ tipiracilu s bevacizumabem oproti monoterapii sníženo o 50 % (medián 8,54 vs. 4,7 měsíce).
Image 1. Podskupinová analýza studie SUNLIGHT – celkové přežití dle předchozí léčby bevacizumabem (A) a stavu mutace KRAS G12 (B). 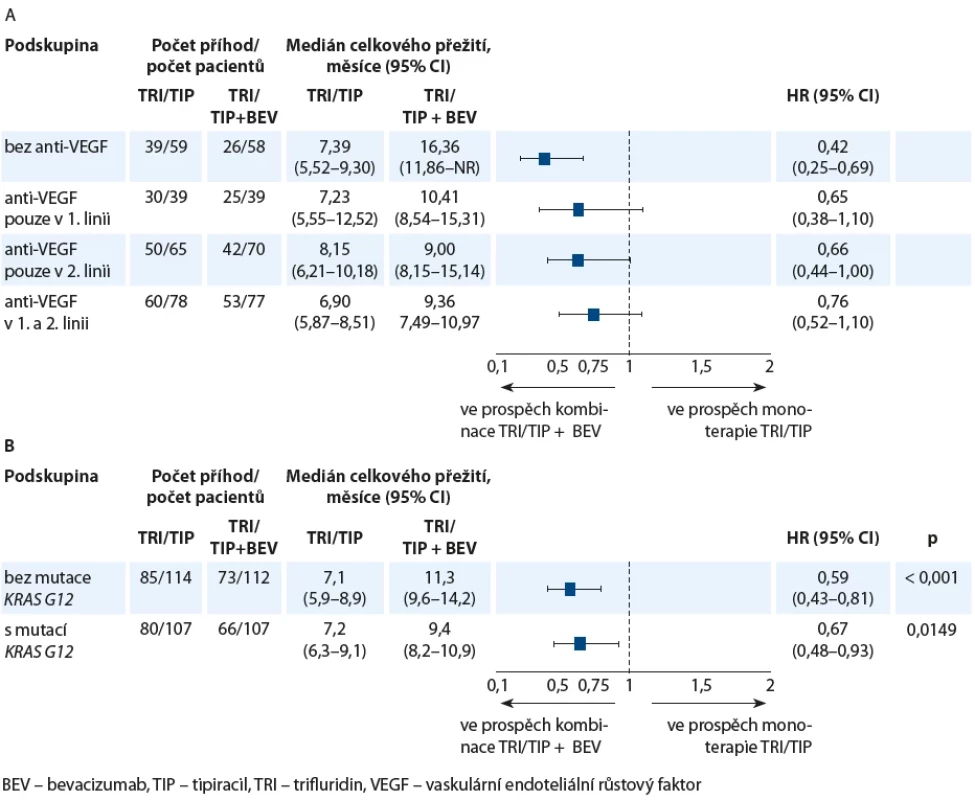
Zdroj: přednáška prof. Pragera. Trifluridin/ tipiracil s bevacizumabem – nový standard třetí linie léčby mCRC
Na výsledky studie SUNLIGHT zareagovala Evropská společnost klinické onkologie (ESMO) aktualizací svých doporučení. Kombinace trifluridinu/ tipiracilu s bevacizumabem je ve třetí linii léčby pacientů s pokročilým neresekabilním mCRC preferovanou volbou (se sílou důkazů a doporučení IA a s kalkulovaným skóre velikosti klinického prospěchu MCBS 4) pro všechny subtypy onemocnění, tedy RAS/ BRAF-nemutované, s mutací RAS i s mutací BRAF V600.
„Díky dostupnosti nových možností ve vyšších liniích léčby se zlepšuje i prognóza pacientů s mCRC. U malé podskupiny pacientů, jejichž nádorové buňky v sobě nesou řídicí mutaci, může i v této fázi onemocnění nahradit chemoterapii specifická cílená léčba, ale pro většinu bude novým standardem léčby třetí linie kombinace trifluridinu/ tipiracilu s bevacizumabem, která nejenže prodlužuje celkové přežití, ale zachovává pacientům kvalitu života a výkonnostní stav. To znamená, že se zvyšuje i jejich šance na absolvování čtvrté linie léčby,“ shrnul prof. Prager.
První zkušenosti s užitím kombinace trifluridinu/ tipiracilu s bevacizumabem v praxi demonstroval prof. Prager kazuistikou ze svého pracoviště. Mladou 27letou ženu, nekuřačku, bez významné rodinné anamnézy v lednu roku 2021 k lékaři přivedly bolesti lymfatických uzlin v levé axile. Následně jí byl diagnostikován stenozující adenokarcinom sigmoidea RAS-mutovaný se synchronními metastázami v játrech, plicích a lymfatických uzlinách. Po subtotální resekci byla zahájena chemoterapie FOLFOXFIRI s bevacizumabem, která byla u pacientky provázena nežádoucími účinky (diarea stupně 2, periferní neuropatie stupně 2–3 po osmém cyklu). CT vyšetření opakovaná po 8 týdnech prokázala parciální remisi onemocnění, bolest v levé axile vymizela, periferní polyneuropatie přetrvávala, sérové koncentrace karcinoembryonálního antigenu (CEA) poklesly na normální úroveň. Léčba byla deeskalována na podávání kapecitabinu s bevacizumabem.
V listopadu 2021 detekována progrese v retriperitoneálních lymfatických uzlinách, proto byla zahájena reindukce FOLFIRI s bevacizumabem. Pacientka na léčbu neodpovídá, v lednu 2022 potvrzena progrese onemocnění.
V únoru 2022 byla na základě individuálního léčebného programu zahájena léčba trifluridinem/ tipiracilem v kombinaci s bevacizumabem. Během prvního cyklu se u pacientky dostavila neutropenie stupně 4, která si vyžádala odložení dávky a přeléčení faktory stimulujícími kolonie granulocytů. Od té doby je pacientka stále na léčbě třetí linie a daří se jí dobře.
Pegylovaný lipozomální irinotekan v léčbě karcinomu pankreatu – data z klinické praxe ČR
Prezentace druhého tématu sympozia se ujala prof. MU Dr. Beatrice Mohelníková Duchoňová, Ph.D., z Onkologické kliniky LF UP a FN Olomouc.
Irinotekan je polosyntetický derivát alkaloidu kamptotecinu, jehož cytotoxický účinek spočívá v blokádě replikace DNA nádorových buněk. Zvláštní formou je pegylovaný lipozomální irinotekan (naI-IRI) – uzavření irinotekanu do lipidových vezikulů vede k pomalejšímu uvolňování, a tedy k delšímu působení léčiva. Při tzv. pegylaci je na povrch lipozomu navázána další látka, která brání jeho rychlému rozkladu bílými krvinkami.
Pro zhodnocení účinku naI-IRI u pacientů s metastatickým duktálním adenokarcinomem pankreatu (mPDAC) byla stěžejní studie fáze III NAPOLI-1. Po publikaci výsledků této studie se stala kombinace nal-IRI + 5-FU/ LV standardem léčby u pacientů s mPDAC, u nichž došlo k progresi po chemoterapii gemcitabinem.
Data z reálné praxe v ČR byla od roku 2021 do dubna 2023 shromažďována v registru VILP. Ze 142 pacientů s mPDAC léčených režimem nal-IRI + 5-FU/ LV jich bylo hodnotitelných 129. Cílem analýzy byla snášenlivost a účinnost kombinace nal-IRI + 5-FU/ LV u pacientů s mPDAC ve výkonnostním stavu ECOG PS 0–1, kteří progredovali na léčbě gemcitabinem podané v (neo)adjuvanci či v první linii léčby. Léčba probíhala do progrese nebo nezvládnutelné toxicity.
Parametry hodnocené při finální analýze dat odpovídají publikovaným cílům studie NAPOLI-1. Primárním sledovaným parametrem bylo celkové přežití (OS), sekundární sledované parametry pak zahrnovaly přežití bez progrese onemocnění (PFS), doba do selhání léčby (TTF), míra objektivní odpovědi (ORR) definovaná jako podíl pacientů, kteří dosáhli alespoň částečné odpovědi (PR), a bezpečnost léčby.
Co se týká základních charakteristik pacientů v registru při zahájení léčby nal-IRI + 5-FU/ LV, prof. Mohelníková Duchoňová poukázala na několik skutečností: ve sledovaném souboru lehce převládali muži (58 %), u větší části pacientů (67 %) byl nádor lokalizován v hlavě pankreatu, pětina pacientů v předchozí léčbě podstoupila radioterapii a čtvrtina byla předléčena irinotekanem. Většina pacientů (73,6 %) dostávala naI-IRI v druhé linii. Přes 81 % pacientů dostalo plnou dávku naI-IRI (70 mg/ m2), ostatní měli dávku redukovanou (≤ 50 mg/ m2). Ke snížení dávky (většinou z důvodu nežádoucích účinků) došlo u < 10 % pacientů. Medián doby trvání léčby byl 2,3 měsíce – zajímavý je široký rozptyl (0–18,8 měsíce), který svědčí o tom, že někteří pacienti z této léčby profitují déle než 1 rok, což je v případě karcinomu pankreatu nepochybně pozoruhodné.
Medián OS pacientů léčených nal-IRI + 5-FU/ LV byl v tuzemské klinické praxi podle registru VILP 10,1 měsíce a 6měsíčního přežití dosáhlo 57,1 % pacientů. To jsou lepší výsledky, než kterých bylo dosaženo ve studii NAPOLI-1 (medián OS 6,1 měsíce, 6měsíční OS 53 %) (obr. 2).
Medián PFS u pacientů z registru VILP léčených nal-IRI + 5-FU/ LV (3,5 měsíce) byl srovnatelný s mediánem PFS pacientů z registrační studie NAPOLI-1 (3,1 měsíce).
Míra objektivních odpovědí na léčbu (ORR), která zahrnuje parciální odpověď (PR) a kompletní odpověď (CR), dosáhla 10,1 % (1 pacient měl CR a 12 pacientů PR). Medián doby do dosažení léčebné odpovědi byl 3,1 měsíce.
Uvedená ORR se může zdát nízká, ale tento výsledek je třeba podle slov prof. Mohelníkové Duchoňové posuzovat s ohledem na malou chemosenzitivitu karcinomu pankreatu – už v neoadjuvanci nebo v první linii, tedy u dosud nepředléčených pacientů, ORR při aplikaci kombinovaných režimů zpravidla nepřesahuje 25 % (u tripletů cca 30 %). A např. běžně používaný gemcitabin vykazuje v první linii obdobnou míru odpovědí jako nal-IRI + 5-FU/ LV po progresi.
Vedle výše uvedených parametrů je neméně důležitá toxicita a snášenlivost léčby, se kterými souvisí míra kvality života pacientů s metastatickým karcinomem pankreatu. V registru VILP bylo u pacientů na režimu naI-IRI + 5-FU/ LV zaznamenáno 19 nežádoucích účinků (NÚ), které se objevily u 17 (13,2 %) pacientů. Nejčastěji se jednalo o průjem – u 9 (17 %) pacientů. Další NÚ zahrnovaly únavu (n = 3), anemii (n = 2), infekci herpes zoster (n = 1), sepsi (n = 1), hepatopatii (n = 1) a melénu (n = 1). U jednoho pacienta se v souvislosti s užíváním irinotekanu objevily poruchy střevní pasáže a zvracení (stupeň 3). Prof. Mohelníková Duchoňová proto konstatovala, že je-li léčba nal-IRI dobře indikována, je bezpečná. Z hlediska NÚ označila za pozoruhodné, že se v souboru nevyskytl ani jeden případ neutropenie, a to s ohledem na to, že čtvrtina pacientů užívala růstové faktory.
Závěrem shrnula, že nal-IRI + 5-FU/ LV potvrzuje v tuzemské klinické praxi u pacientů s mPDAC po selhání nebo intoleranci chemoterapie gemcitabinem výsledky, kterých dosáhl v klinické studie NAPOLI-1, a to jak z hlediska účinnosti, tak i dobré tolerance. Vypočtené delší přežití pacientů v tuzemském registru oproti registrační studii NAPOLI-1 poukazuje na racionální indikaci tohoto režimu v běžné české klinické praxi.
Image 2. Srovnání celkového přežití pacientů nal-IRI + 5-FU/LV českého registru VILP a pacientů z registrační studie NAPOLI-1. 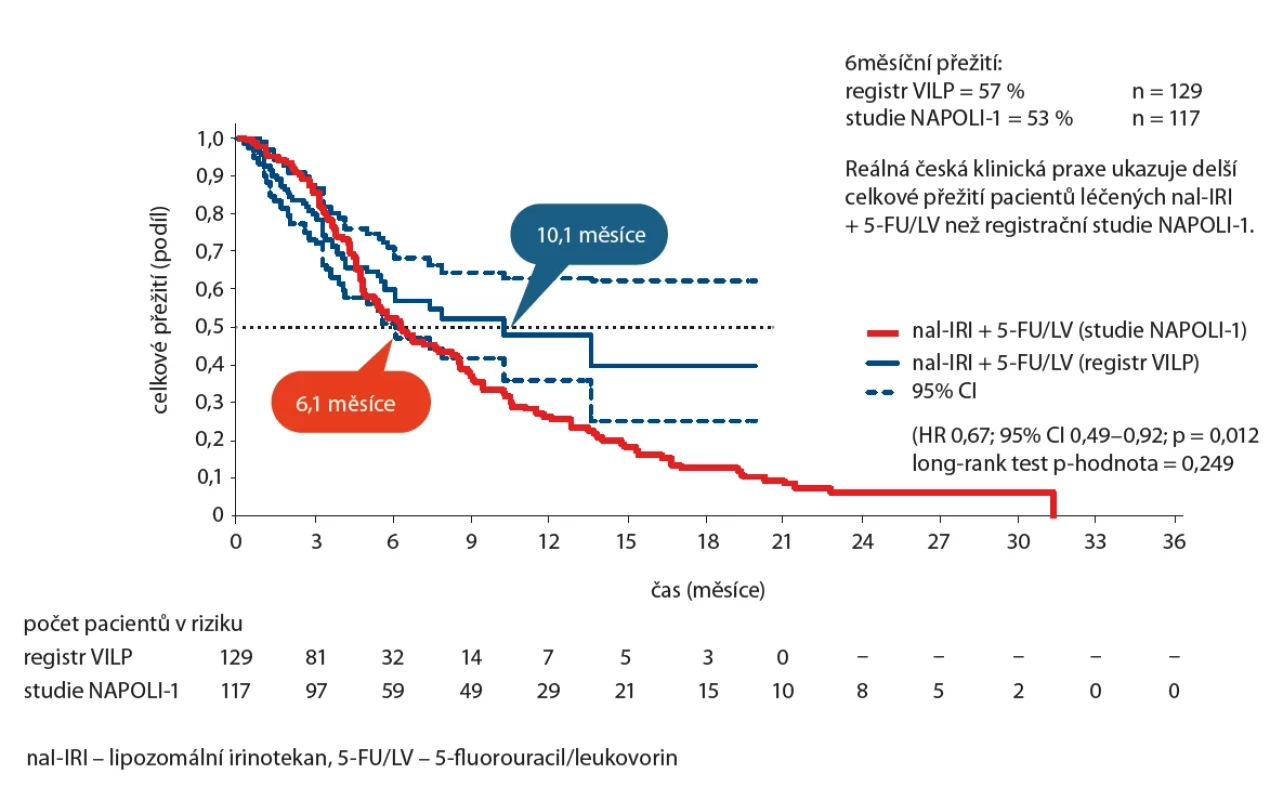
Kazuistika
Případ 68leté ženy s metastatickým karcinomem pankreatu prezentovala MU Dr. Věra Benešová z Onkologického oddělení Nemocnice Jihlava. Pacientka byla přijata na interní oddělení nemocnice pro náhlý obstrukční ikterus. Po diagnostikování lokálně pokročilého adenokarcinomu pankreatu s postižením pobřišnice a s ascitem byla multidisciplinárním týmem doporučena systémová paliativní chemoterapie. Pacientka byla ve výkonnostním stavu PS ECOG 1.
Jak zdůraznila MU Dr. Benešová, cílem onkologické léčby u takovýchto nemocných je především stabilizace nebo regrese onemocnění s prodloužením délky života při zachování nebo zlepšení jeho kvality. Při volbě chemoterapeutického režimu by kromě účinnosti a efektivity měla být zohledněna jeho toxicita, do úvahy je třeba brát i sociální situaci nemocného nebo dopravní dostupnost onkologického centra.
Léčba pacientky byla zahájena v září 2022 a v první linii byl podáván gemcitabin (inj.) v monoterapii, který pacientka velmi dobře snášela. Po měsíci léčba pokračovala aplikací kombinační chemoterapie gemcitabin + nab paklitaxel inj., také s dobrou tolerancí. Kontrolní vyšetření po 3 měsících kombinační léčby ukázalo parciální regresi onemocnění.
Po 8 měsících léčby první linie došlo k progresi onemocnění, nicméně pacientka byla stále v dobrém výkonnostním stavu. Genetické vyšetření u ní neprokázalo polymorfizmus genu DPYD související se sníženou funkcí enzymu dihydropyrimidindehydrogenázy.
Na základě Modré knihy ČOS ČLS JEP a pozitivních zkušeností pracoviště MU Dr. Benešové byla zahájena léčba druhé linie kombinací naI-IRI + 5-FU/ LV. K prevenci nauzey byla aplikována setronová antiemetika. Zde MU Dr. Benešová zdůraznila význam správného nastavení podpůrné léčby, která významně přispívá ke compliance pacientů.
Již po třech cyklech chemoterapie došlo k výraznému poklesu hodnot nádorového markeru Ca 19-9 na hodnotu 165 kU/ l, avšak po 6 týdnech došlo ke komplikacím – pacientka byla akutně přijata na onkologické oddělení pro týden trvající průjmy a dehydrataci. Laboratorní a zobrazovací vyšetření vyloučila náhlou příhodu břišní a postižení tlustého střeva, byla zjištěna leukopenie stupně 2, příčina průjmů nebyla odhalena. Během 4týdenní hospitalizace došlo k velmi pozvolné úpravě počtu i konzistence stolic a celkového klinického stavu a pacientka tak mohla být převedena na perorální stravu. Celkově byla léčba naI-IRI + 5-FU/ LV přerušena na dobu 7 týdnů.
V této době byl patrný výskyt ascitu, který nebyl tenzní, a byla zaznamenána elevace Ca 19-9 na 871 kU/ l. Vzhledem k dobré kondici pacientky a jejímu aktivnímu přístupu k léčbě bylo rozhodnuto pokračovat v kombinované chemoterapii naI-IRI + 5 FU/ LV. I přes prodlevu vzniklou přerušením léčby byl zaznamenán výrazný efekt a bylo dosaženo stabilizace onemocnění (pokles Ca 19-9 na 333 kU/ l). V současnosti pacientka pokračuje v ambulantní aplikaci kombinované chemoterapie naI-IRI + 5 FU/ LV a dobře ji toleruje. Pacientka tedy žije 17 měsíců od zjištění diagnózy, což je u metastatického karcinomu pankreatu nadstandardní výsledek, z toho na druhé linii léčby již i se 7týdenním přerušením strávila stejný čas (8 měsíců) jako na prvoliniové léčbě (obr. 3).
Závěrem MU Dr. Benešová shrnula, že léčba metastatického onemocnění pankreatu je velmi náročná, kdy nestačí podávat cytostatika dle doporučených postupů, ale pacienty je třeba hodnotit komplexně a přihlížet k potenciálním problémům, které jsou dány umístěním pankreatu v dutině břišní a mnoha funkcemi, které tento orgán zastává. Výskyt metastatického karcinomu pankreatu se oproti minulosti, kdy v rámci pracoviště MU Dr. Benešové byly zaznamenány cca dva případy za rok, rapidně zvyšuje na několik případů za měsíc. Doba života pacientů s touto diagnózou je velmi omezená (průměrně 11 měsíců), prioritou je tedy udržení či zlepšení kvality života. Péče o nemocné s metastatickým karcinomem pankreatu by tedy měla odrážet nejen klinické projevy onemocnění, ale také jejich přání.
Image 3. Kazuistika – časová osa léčby. Zdroj: prezentace MUDr. Benešové. 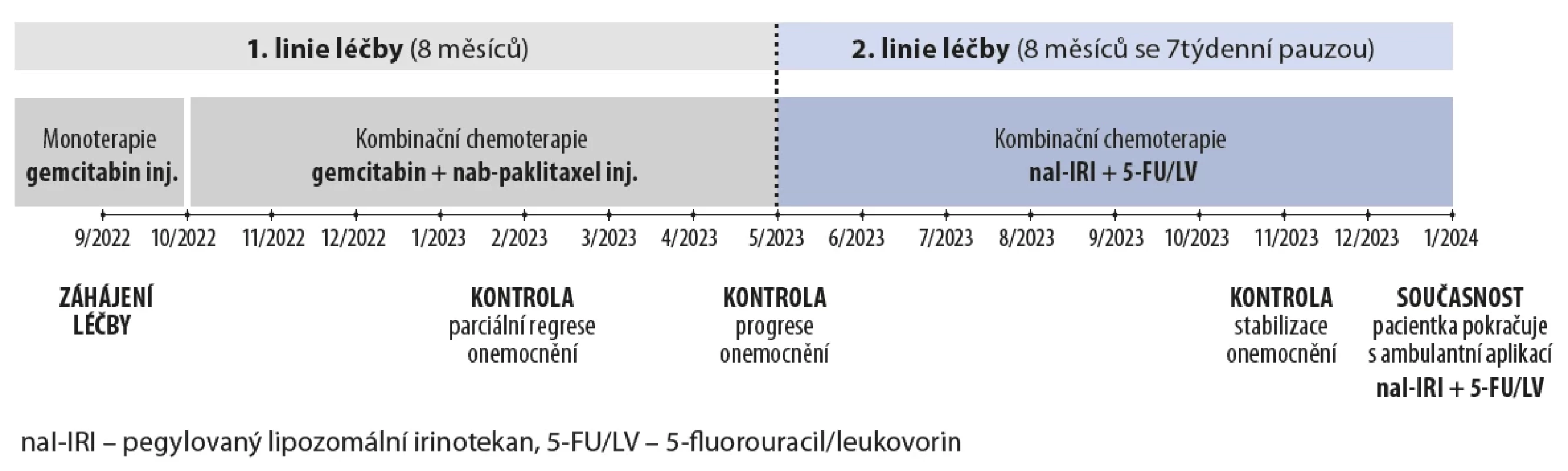
Ing. Kateřina Michnová
šéfredaktorka Care Comm s.r.o.
Labels
Paediatric clinical oncology Surgery Clinical oncology
Article was published inClinical Oncology

2024 Issue 1-
All articles in this issue
- Evropský plán boje proti rakovině a Mise rakovina – co nám přináší?
- Cardiac conduction system as a new organ at risk in radiotherapy
- Gut microbiome and pancreatic cancer
- Molecular basis of multiple myeloma
- Evaluation pattern within tumor microenvironment and consequent gene expression in oral cancer
- Analysis of the effect of baseline detection and early clearance of ct-DNA, on survival outcomes among patients with advanced EGFR-mutant non-small cell lung cancer
- Immunohistochemical analysis of CD9, CD29 and epithelial to mesenchymal transition in triple-negative breast cancer
- Klinická zkušenost s kabozantinibem u pacientů s metastatickým karcinomem ledviny
- Treatment of tobacco dependence in cancer patients - Recommendations of the Section of Supportive Treatment and Care and the Section of Preventive Oncology of the Czech Cancer Society of the Czech Medical Association of J. E. Purkyně, Working Group for the Prevention and Treatment of Tobacco Dependence of the Czech Medical Association of J. E. Purkyně, and the Society for Treatment of Tobacco Dependence
- Pokročilé léčebné strategie metastatického kolorektálního karcinomu a karcinomu pankreatu
- MU Dr. Libor Havel (1967–2023)
- Doc. Ing. Čestmír Altaner, DrSc. oslávil vzácne životné jubileum – 90 rokov
- Poděkování recenzentům
- Clinical Oncology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Molecular basis of multiple myeloma
- Gut microbiome and pancreatic cancer
- Analysis of the effect of baseline detection and early clearance of ct-DNA, on survival outcomes among patients with advanced EGFR-mutant non-small cell lung cancer
- Cardiac conduction system as a new organ at risk in radiotherapy
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

