-
Medical journals
- Career
Jsou moderní automatické kardiostimulátory skutečně automatické?
Medtronic Adapta a jeho automatické funkce
Authors: V. Vančura; J. Bytešník; K. Lefflerová; R. Krausová; R. Čihák; P. Peichl; J. Kautzner
Authors‘ workplace: Kardiologická klinika, IKEM, Praha
Published in: Kardiol Rev Int Med 2006, 8(4): 185-191
Category: Editorial
Overview
Úvod:
Koncepce automatického kardiostimulátoru, který by sám sledoval vývoj parametrů svědčících o integritě a funkčnosti celého stimulačního systému a sám dokázal reagovat na změny stimulačních prahů a amplitudy intrakardiálního signálu, je velmi stará. Cílem studie bylo zjistit, nakolik se jí moderní kardiostimulátor přiblížil.Metody:
Sledováni byli pacienti, kterým byl v období od 1. 6. 2005 do 31. 5. 2006 implantován kardiostimulátor Adapta ADDR01 (Medtronic). Data byla získána retrospektivně ze záznamů z první ambulantní kontroly. Hodnoceno bylo, u kolika nemocných jsou všechna potřebná data svědčící o integritě a funkčnosti systému zobrazena již na první obrazovce programovacího zařízení bezprostředně po vstupním načtení dat. Za potřebné informace byly považovány údaje o stavu baterií, o vývoji a aktuální hodnotě impedance elektrod, o vývoji a aktuální hodnotě síňového a komorového stimulačního prahu a o hodnotě amplitudy intrakardiálního signálu v síních a v komorách. Dále bylo sledováno, jak často naměřená data vyžadovala přeprogramování hodnot stimulační energie nebo sensingu z režimu automatických úprav na fixní hodnotu.Výsledky:
Do studie bylo zařazeno 27 nemocných (17 mužů). Průměrný věk nemocných byl 67,8 ± 12,1 roků. Celkem 20 nemocných mělo tento stimulátor implantováno v rámci primoimplantace, u 7 nemocných se jednalo o výměnu. Primární indikací k implantaci kardiostimulátoru byl syndrom chorého sinu v 19 případech. V 1 případě šlo o hypersenzitivní karotický sinus a v 7 případech o převodní AV-poruchu. Při první ambulantní kontrole po implantaci měli všichni nemocní na úvodní obrazovce údaj o životnosti baterie, aktuální hodnotě impedance obou elektrod a jejím vývoji v grafické podobě. Celkem u 26 nemocných byl zobrazen údaj o hodnotě komorového prahu. V 1 případě tento údaj chyběl, protože hodnota prahů byla příliš vysoká vzhledem k rozmezí, ve kterém algoritmus pracuje. U stejného počtu 26 nemocných byl prezentován údaj o hodnotě síňového prahu. U 1 pacienta chyběl, neboť u něj od výměny přístroje až do ambulantní kontroly trvala fibrilace síní. Hodnota síňového sensingu byla uvedena ve 12 případech, ostatní pacienti měli příliš vysoký podíl stimulovaných cyklů v síních. Amplituda signálu v komorovém kanálu byla uvedena ve 20 případech. Ostatní pacienti měli vysoký podíl stimulovaných cyklů. Hodnoty sensingu a energie stimulace byly ponechány v režimu automatických úprav, pouze u pacienta s nezměřeným komorovým prahem považoval ošetřující lékař za vhodné převedení na fixní hodnotu energie stimulace.Závěr:
U současných typů přístrojů je automatické sledování základních parametrů svědčících o správné funkci stimulačního systému na pokročilé úrovni. Moderní kardiostimulátor sám měří životnost baterie, impedanci elektrod, práh stimulace v síni a v komoře, stejně jako hodnoty sensingu. Tyto hodnoty pak uvádí na obrazovce programovacího zařízení bezprostředně po vstupním načtení dat. Pokud nejsou naměřené hodnoty sensingu či stimulačního prahu uvedeny na úvodní obrazovce, jde obvykle o důsledek vysokého stimulačního prahu, přítomnosti fibrilace síní nebo nízkého počtu snímaných cyklů při vyšším podílu stimulace v dané dutině. Režim automatických úprav hodnot sensingu a stimulační energie se jeví být vyhovujícím pro naprostou většinu nemocných.Klíčová slova:
kardiostimulace – automatický kardiostimulátor – kardiostimulátor Adapta – sensing – stimulační práhÚvod
Moderní kardiostimulátory jsou stále komplexnějšími přístroji s řadou funkcí, programovatelných parametrů a údajů ukládaných do paměti. Bez ohledu na míru komplexnosti těchto přístrojů zůstávají v centru pozornosti i nadále základní funkce, které umožňují stimulaci o nastavené frekvenci k zvládnutí pacientovy bradyarytmie. Cílem každé kontroly přístroje je proto ověřit integritu systému potvrzením přiměřené hodnoty impedancí elektrod, dostatečné rezervy baterií a stabilních hodnot prahů stimulace a sensingu, které odpovídají nastaveným parametrům. Ve snaze ulehčit lékařům kontrolu kardiostimulátorů vyvíjejí výrobci automatické algoritmy, jejichž úkolem je v pravidelných intervalech měřit tyto základní parametry, a naměřené hodnoty pak používat k automatickému „sebeřízení“ základních funkcí přístroje, jako je regulace parametrů sensingu nebo energie stimulace [1]. Informaci o posledních naměřených hodnotách a jejich časovém vývoji pak koncentrují na 1 místo tak, aby mohla být kontrola přístroje co nejkratší a mohla být soustředěna na ty oblasti, v nichž je to skutečně třeba, jako je analýza obsahu paměti nebo vyhodnocování účinnosti pokročilých funkcí.
Jedním z takových moderních automatických přístrojů je kardiostimulátor firmy Medtronic s názvem Adapta. Po vstupním načtení dat z přístroje se na obrazovce programovacího zařízení objeví okno, nazvané výrobcem QuickLook II (QLII) a současně se rozběhne tisk informací z tohoto okna. V tomto okně jsou koncentrovány všechny základní informace o kardiostimulátoru. Přístroj sám má všechny potřebné algoritmy vestavěny – sám tedy měří stav baterií a impedanci elektrod, hodnoty sensingu v síních a komorách i prahy v síních a v komorách. Přesnost těchto algoritmů byla opakovaně ověřena v minulosti [2–6]. Jsou-li naměřené hodnoty ve vyhovujícím rozmezí, kardiostimulátor podle nich reguluje jak stimulační energii, tak i úroveň sensingu.
Cílem této studie bylo zjistit, u kolika nemocných přinesla úvodní informační obrazovka komplexní informaci nevyžadující žádné další měření základních parametrů, případně jaké hodnoty bylo potřeba změřit manuálně a jak často. Dalším cílem bylo zkontrolovat, zda je možné ponechat automatické stanovování sensingu a stimulační energie dlouhodobě zapnuté.
Metody
Studie byla prováděna jako retrospektivní. Do studie byli zařazeni všichni nemocní, kterým byla na našem pracovišti provedena implantace přístroje Adapta ADDR01 (Medtronic, Minneapolis, MI, USA) v období od 1. 6. 2005-31. 5. 2006. Klinická data byla získána z příslušné dokumentace každého nemocného.
Kardiostimulátor Adapta je komplexní přístroj s řadou funkcí. Níže jsou popsány pouze algoritmy vztahující se k cílům této práce. Bezprostředně po telemetrickém načtení dat z přístroje se na obrazovce programovacího zařízení objeví okno nazývané QLII (obr. 1). Toto okno obsahuje základní informace, které jsou nezbytné pro posouzení integrity systému a očekávané životnosti přístroje. Informuje dále o podílu stimulovaných cyklů a výskytu síňových arytmií. V neposlední řadě obsahuje i oblast věnovanou případným varovným hlášením. V rámci automatického měření se v době načítání dat vyhodnotí na základě stavu baterie a naprogramovaných parametrů očekávaná životnost přístroje a vyjádří se v měsících nebo létech. Komu tato informace nestačí, má k dispozici další obrazovku s podrobnější informací včetně hodnot napětí a impedance baterií (obr. 2). Přístroj sám pravidelně každé 3 hodiny měří impedance elektrod a jejich vývoj prezentuje v grafické formě, přičemž poslední hodnotu uvádí i numericky. Automaticky měří i hodnotu stimulačního prahu komorové elektrody. Měřící algoritmus spočívá na posouzení přítomnosti tzv. stimulací evokované odpovědi v průběhu snižování hodnoty stimulační energie. Předem nastaveno je měření v intervalu 24 hodin, a to 1 hodinu po půlnoci. Ošetřující lékař může v případě potřeby tento interval prodloužit až na maximum 7 dnů nebo zkrátit na minimum 1 hodiny. Je možné zvolit i jinou dobu měření. Hodnota stimulační energie je přednastavena na adaptivní s rezervou dvojnásobku napětí stimulu oproti napětí stimulu prahového. Pokud lékař v některých případech nepovažuje dvojnásobek prahového napětí za vyhovující, může jej rovněž změnit. Současně má přístroj nastavitelnou minimální stimulační energii, která představuje dolní limit bez ohledu na naměřenou hodnotu stimulačního prahu. Tato hodnota je opět nastavitelná. Nestačí-li ošetřujícímu lékaři komprimovaná grafická informace na této obrazovce, může kliknutím na dvojitou šipku v obdélníčku při levém horním okraji grafu otevřít další okno s podrobnější informací (obr. 3).
Image 1. Obrazovka Quick Look II. 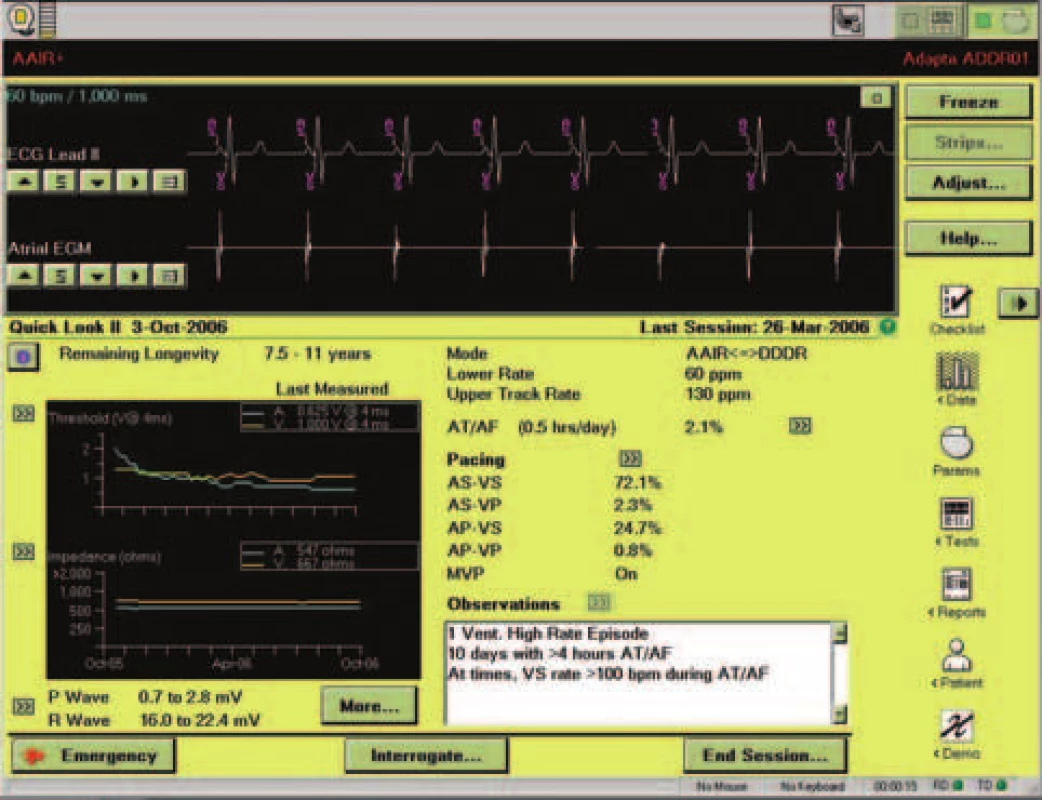
Image 2. Obrazovka obsahující detailní údaje o stavu baterií a energii stimulace. 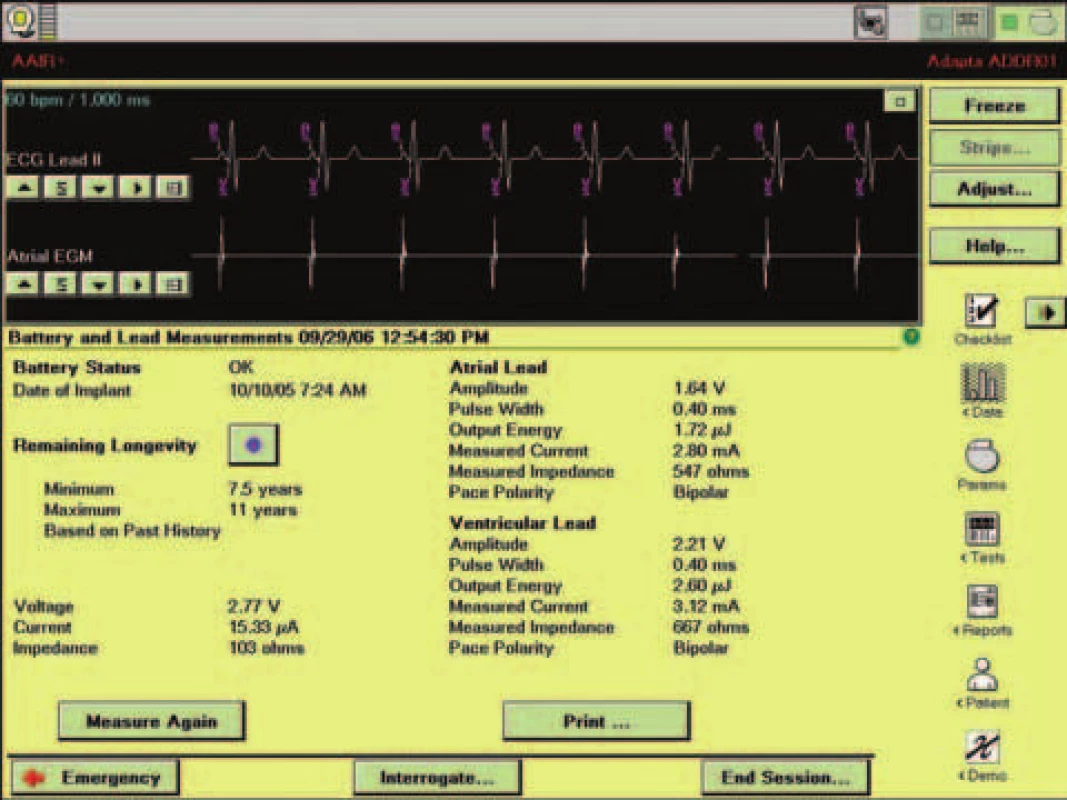
Image 3. Podrobnosti o průběhu automatického měření komorového prahu. 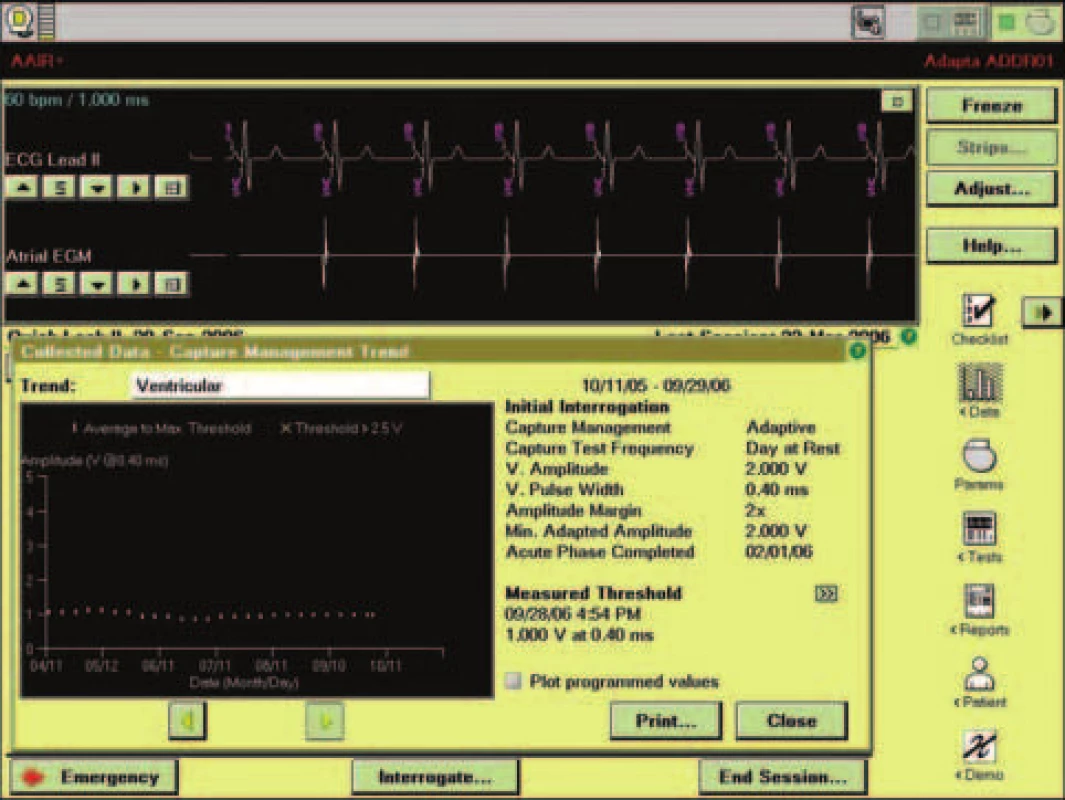
Kardiostimulátor měří automaticky i hodnotu síňového prahu. Vzhledem k nízké hodnotě evokované odpovědi v síních jsou použity jiné algoritmy, než při měření komorového prahu. Tyto algoritmy byly detailně popsány jinde [5], zde jsou uvedeny jen ve stručnosti. První z nich spočívá v tzv. resetu síňové aktivity. Jednoduše lze tento způsob měření popsat tak, že při vlastní síňové akci o frekvenci 50/min a stimulaci v síních nastavené na klidovou hodnotu 60/min není schopen přístroj s energií stimulace nad hodnotou stimulačního prahu v síňovém kanálu zaznamenat žádnou vlastní síňovou aktivitu. V okamžiku, kdy energie stimulace v síních poklesne při měření pod hodnotu stimulačního prahu, začne přístroj detekovat mezi stimulačními impulzy spontánní síňovou aktivitu (ve výše uvedeném případě o frekvenci okolo 50/min). Není-li vlastní síňová aktivita přítomna, je k dispozici druhý algoritmus, při němž používá přístroj k vyhodnocování účinnosti síňové stimulace metodu sledování komorové odpovědi. Výrobcem je nastavena adaptivní amplituda stimulace s dvojnásobným bezpečnostním rozdílem mezi hodnotou změřenou a použitou. Současně má přístroj, podobně jako v komorovém kanálu, nastavitelnou i v síňovém kanálu hodnotu minimální energie stimulace. Metoda selhává v méně častých případech, kdy chybí jak síňokomorové vedení, tak spontánní síňová aktivita. Nebezpečí pro pacienta však nehrozí, neboť lékař nastavuje při kontrole nejmenší energii, kterou smí pro stimulaci použít.
Kardiostimulátor Adapta měří sám i hodnoty amplitud intrakardiálního signálu. Je-li zapnuta funkce „sensing assurance“, což je tovární nastavení, upravuje podle naměřených hodnot automaticky hodnotu sensingu. Pro komorový signál není dostupné celé rozmezí možných hodnot sensingu – přístroj může volit pouze hodnoty v pásmu od 2,0 do 5,6 mV. Pro síňový signál je důležité, zda je sensing unipolární či bipolární. V bipolárním modu je pro algoritmus dostupné pásmo od 0,18 do 0,5 mV, v unipolárním modu od 0,5 do1,4 mV. Hodnoty mimo tyto intervaly je třeba nastavit manuálně a vypnout příslušný algoritmus. Ke správné funkci tohoto algoritmu měří amplitudu všech signálů, které detekuje v příslušném kanálu. Podle charakteru a časování je rozlišuje na možné rušení nebo na validní signál. Jinou váhu pro změnu sensingu mají signály detekované v období refrakterity daného kanálu než signály detekované mimo toto období. Sérii změřených amplitud signálu posléze přístroj používá k vlastní úpravě hodnoty sensingu. Cílem je zachovat bezpečnostní poměr mezi hranicí sensingu a amplitudou změřeného signálu v síni v poměru 4 : 1 až 5,6 : 1 a v komoře v poměru 2,8 : 1 až 4 : 1. Každých 7 dnů přístroj zaznamená do paměti maximální a minimální amplitudu změřeného signálu. Na základě těchto údajů vytváří graf hodnot sensingu (obr. 4, 5). Na obrazovce QLII se objevuje souhrnný údaj o intervalu, ve kterém se hodnoty sensingu nacházely. Tento údaj je prezentován v podobě intervalu ohraničeného 2 hodnotami. Pokud byl bezpečnostní poměr v rámci limitů algoritmu „sensing assurance“ zachován, pak jsou intervaly ohraničeny číselně např. 5,6-8 mV. Jestliže se hodnoty amplitudy intrakardiálního signálu dostaly pod bezpečnostní limit algoritmu, předchází číslu odpovídajícímu dolní hranici intervalu znaménko méně než, tedy například < 0,7-1,4 mV. V tom případě je vhodné kliknout na obdélník s dvojitou šipkou vlevo od těchto hodnot a prohlédnout si zobrazený graf (obr. 6). Zde je třeba zkontrolovat, zda byly hodnoty opakovaně nízké, či zda se jednalo o přechodný jev (např. po implantaci jako projev tzv. zrání elektrod nebo při fibrilaci síní jako výraz kolísání amplitudy intrakardiálního signálu). Pokud jsou hodnoty opakovaně nízké, je vhodné změřit práh manuálně. Pokud je výskyt senzovaných událostí nižší než 20 %, hodnoty sensingu se na obrazovce QLII neobjeví a místo nich se ukazuje údaj „ ≥80 % Paced“. V tom případě přístroj používá hodnotu sensingu tak, jak byla lékařem nastavena při posledním vyšetření.
Image 4. Průběh měření síňového sensingu. 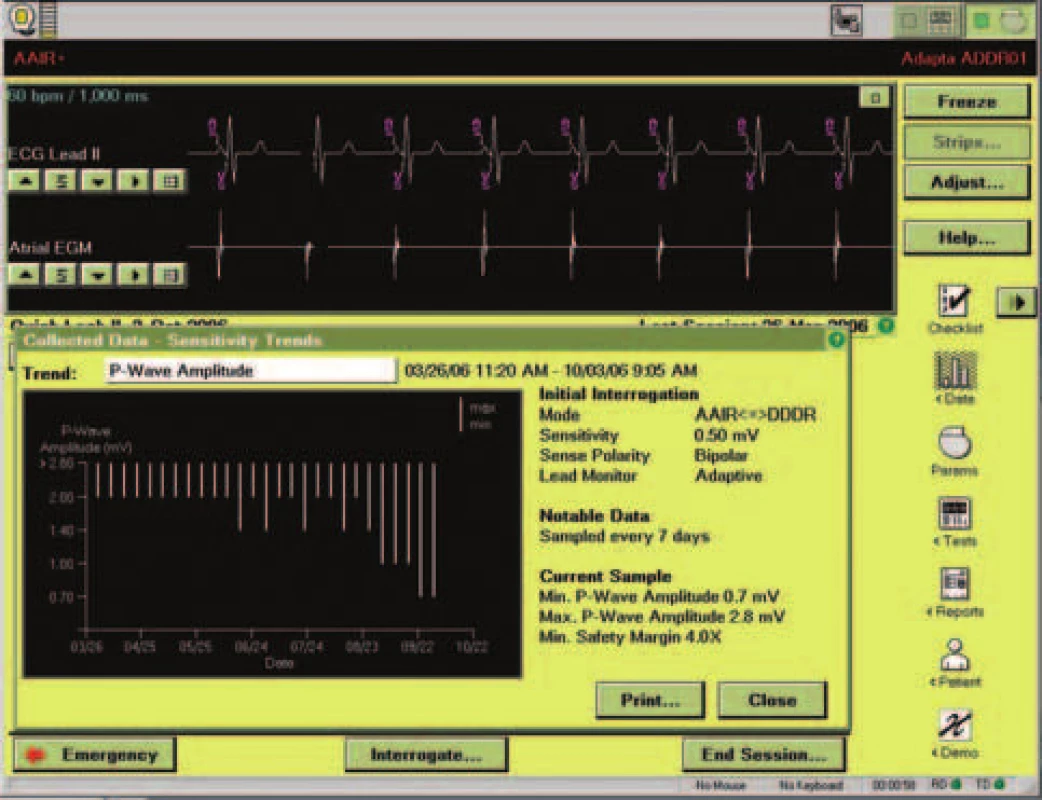
Image 5. Průběh měření komorového sensingu. 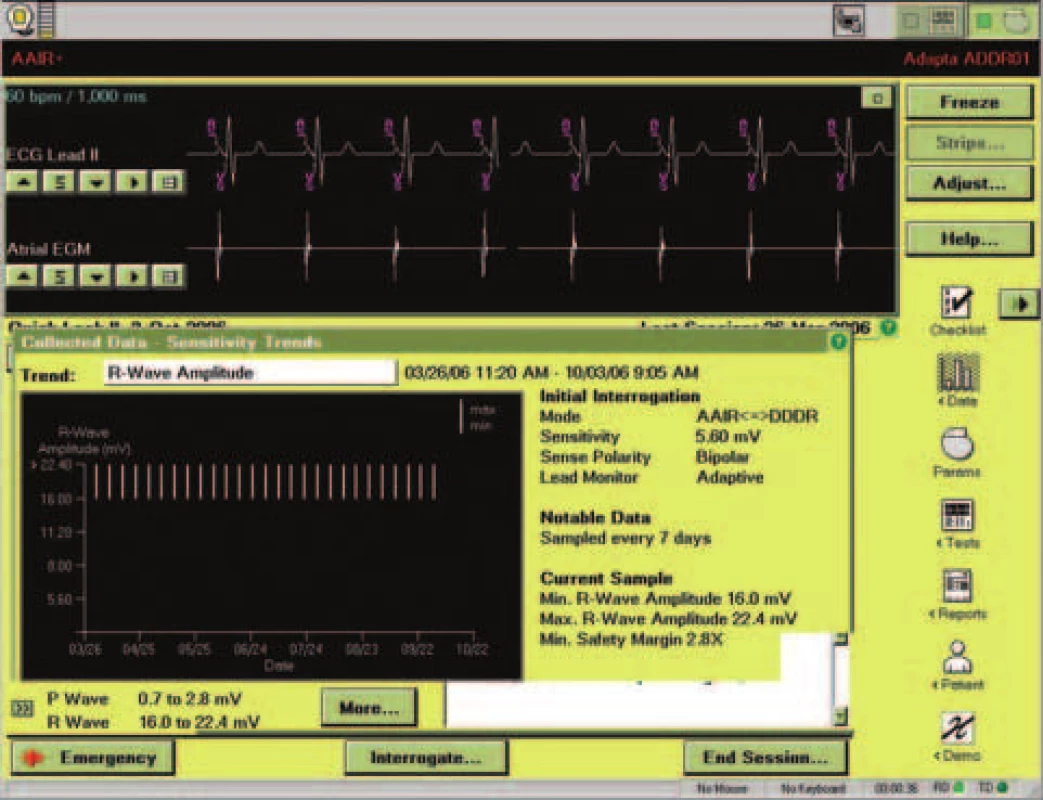
Image 6. Průběh měření síňového sensingu v situaci, kdy opakovaně není dodržen bezpečnostní limit algoritmu „sensing assurance“. 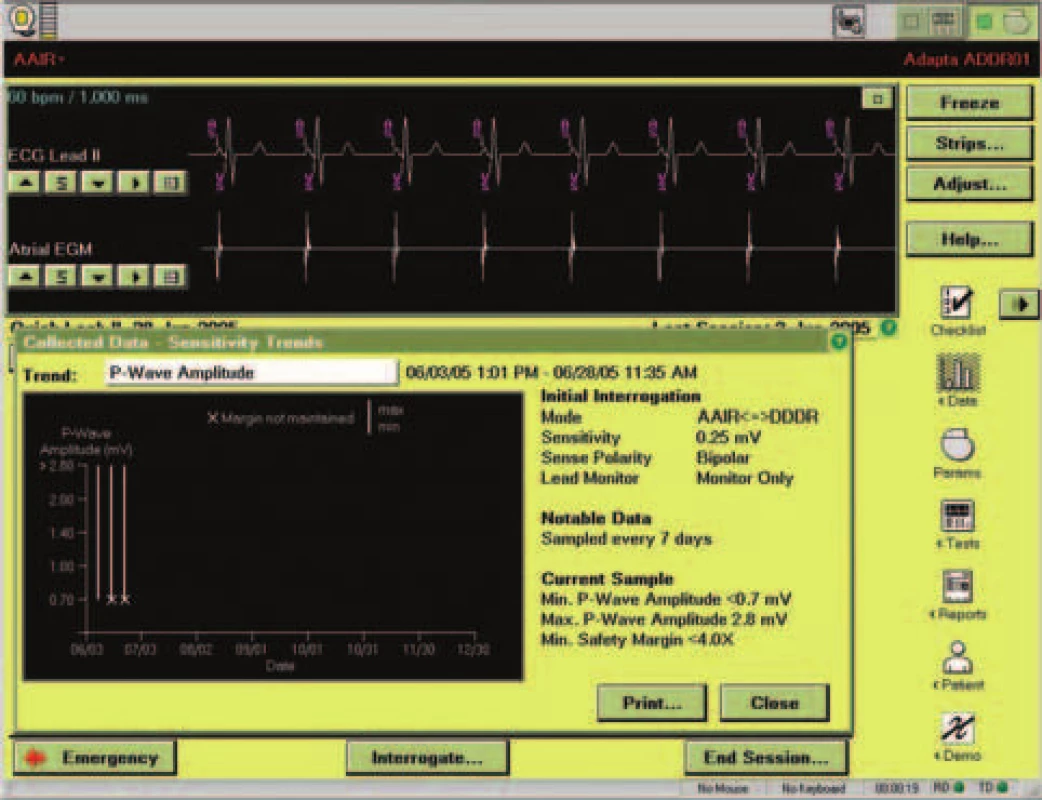
V rámci studie byla hodnocena úplnost údajů na obrazovce QLII, nutných k posouzení integrity systému. Údaje byly získány při první ambulantní kontrole po implantaci přístroje.
Za základní údaje nutné k posouzení integrity systému byly považovány následující:
- údaj o stavu baterie
- impedance elektrod
- práh stimulace v síni a v komoře
- hodnoty sensingu v síni a v komoře.
Jako doplňkové údaje významné pro další rozhodování byly sledovány následující:
- hodnota základní stimulační frekvence
- výskyt síňových tachyarytmií
- počet senzovaných či stimulovaných cyklů v síních a komorách.
K posouzení adekvátnosti uváděných údajů byly pro účely této studie sledovány i údaje o datech posledního měření prahů stimulace, které lze získat z obrazovky po kliknutí na dvojí šipku v rámečku vlevo nahoře od grafu (obr. 3). Z grafů na QLII lze tato data vyčíst pouze přibližně, neboť osa X na těchto grafech odpovídá času a poslední bod vpravo na této ose odpovídá dni kontroly. Chybí-li v pokračování křivky až k těmto hodnotám, je pravděpodobné, že poslední měření proběhlo před delší dobou.
Ze získaných dat a klinické dokumentace pak bylo zjišťováno, zda bylo nutno u některých nemocných automatické přizpůsobování sensingu nebo stimulační energie vypnout.
Výsledky
Soubor nemocných
Do studie bylo zařazeno 27 nemocných (17 mužů), průměrný věk nemocných byl 67,8 ± 12,1 roků. Primární indikací k implantaci kardiostimulátoru byl syndrom chorého sinu v 19 případech. V 1 případě šlo o hypersenzitivní karotický sinus a v 7 případech o převodní atrioventrikulární (AV) poruchu. U 20 nemocných se jednalo o primoimplantaci a u 7 nemocných o výměnu kardiostimulátoru. K první ambulantní kontrole po implantaci se nemocní dostavili průměrně po 46,7 ± 16,1 dnech. Celkem 23 pacientů mělo základní stimulační frekvenci nastavenu na 60/min, další 3 pacienti na 70/min a 1 pacient na 75/min. Průměrný podíl stimulovaných cyklů v síních byl 68,5 ± 37,0 % a v komorách 32,9 ± 42,0 %. U 7 nemocných nebyla zaznamenána žádná epizoda síňové tachyarytmie a u 9 nemocných byly zaznamenány krátké epizody po dobu menší než 0,1 % sledovaného časového období. Celkem 11 nemocných mělo častější epizody síňových tachyarytmií.
Údaje o stavu baterie a impedance elektrod
Očekávaná životnost přístroje byla podle předpokladu uvedena ve všech případech. Stejně tak byla ve všech případech změřena impedance síňové a komorové elektrody.
Údaje o stimulačním prahu
Síňový stimulační práh nebyl změřen pouze v 1 případě. Šlo o nemocnou, které byl přístroj naimplantován v rámci výměny staršího kardiostimulátoru s vyčerpaným bateriovým zdrojem a u které vznikla bezprostředně po implantaci fibrilace síní. V ostatních případech byly k dispozici hodnoty prahů. Při kontrole data, kdy byl poslední práh získán, bylo zjištěno, že v 21 případech byly hodnoty stimulačního prahu měřeny v den kontroly nebo v průběhu předchozího kalendářního dne. V 5 případech byl tento časový interval delší.
Práh komorové stimulace byl změřen automaticky ve 26 z 27 případů. V jednom případě měření nebylo provedeno, neboť brzy po implantaci byl zaznamenán přechodně vysoký stimulační práh. Přístroj totiž dokáže automaticky měřit pouze práh do hodnoty 2,5 V/0,4 ms. Pokud je při této energii stimulace neúčinná, přepne se automaticky adaptivní stimulace na hodnotu 5 V/1 ms. Z 26 případů změřeného prahu bylo 25 hodnot získáno v den měření či v předchozí kalendářní den. V 1 případě byla hodnota prahů získána 4 dny před datem kontroly. Důvodem delšího odstupu měření komorových prahů byla dle výpisu z paměti přístroje zřejmě rychlá komorová odpověď při paroxyzmu fibrilace síní, který byl zaznamenán v období několika dnů před ambulantní kontrolou. U všech nemocných byla ponechána automatická regulace energie stimulace, pouze u nemocného s vysokým prahem stimulační energie považoval ošetřující lékař za vhodné přeprogramování do režimu fixní energie stimulace.
Údaje o hodnotě sensingu
Amplituda intrakardiální vlny P byla změřena a byla shledána vyhovující v 9 případech. Ve 3 případech byla změřena, ale naměřené hodnoty si vyžádaly další analýzu – prvnímu číselnému údaji předcházelo znaménko „ < “ a v 15 případech byl podíl stimulovaných cyklů roven nebo vyšší než 80 %, a v takovém případě přístroj na této obrazovce hodnotu amplitudy nesděluje. V případě amplitudy komorového signálu byl tento údaj změřen v 18 případech a shledán vyhovujícím. V 2 dalších případech byl změřen, avšak vyžadoval další kontrolu – prvnímu číselnému údaji přecházelo znaménko „ < “ a v 7 případech byl podíl stimulovaných cyklů alespoň 80 %. Ve všech případech byl ponechán režim „sensing assurance“.
Během sledovaného období nebyla u žádného pacienta zachycena situace svědčící pro poruchu kardiostimulace či problémy s některým z algoritmů.
Diskuse
Počátky éry automatizace kardiostimulátorů se datují již do 60. let minulého století, kdy se objevila koncepce přístrojů „on demand“. Tyto přístroje dokázaly automaticky rozeznat, kdy je třeba aplikovat stimulus proto, že se vlastní akce srdeční zpomalila pod stimulační frekvenci kardiostimulátoru. Nicméně na skutečnou automatizaci základních stimulačních funkcí, tedy na stav, kdy si kardiostimulátor sám dokáže nastavit hodnotu sensingu podle amplitudy intrakardiálního signálu, kdy sám dokáže zvolit vhodnou energii stimulace tak, aby byla aplikace stimulu účinná a současně předcházet plýtvání energií, bylo třeba čekat až do nedávné doby [1].
Ještě před 10 lety nebylo neobvyklé, že se indikace k výměně kardiostimulátoru pro vyčerpání bateriových zdrojů posuzovala podle stimulační frekvence s přiloženým magnetem – tzv. magnetické stimulační frekvence. Podle její výše se určovalo, zda přístroj je nebo není indikován k výměně. Pokud tato kritéria k výměně nebyla splněna, nebylo možno zjistit, do jaké míry jsou baterie skutečně vyčerpány a jak je třeba načasovat termín další kontroly. Dokonalejší programovatelné přístroje začaly ukazovat napětí baterií, které se ale mění relativně málo a zejména ke konci životnosti lithihových baterií je pokles napětí zvláště pomalý. Proto se při kontrolách začala hodnotit též impedance baterií. Ta se zpočátku prakticky nemění, avšak s narůstající mírou vyčerpání baterií je její vzestup stále strmější, a proto je k posuzování životnosti baterií velmi užitečným parametrem [7]. Hodnota napětí a impedance baterií je i při stejném chemizmu baterií závislá na výrobci kardiostimulátoru a často i na konkrétním typu přístroje. Pro uživatele je nejnázornějším způsobem vyjádření míry vyčerpání bateriových zdrojů očekávaná doba životnosti přístroje. Tento parametr prezentují všechny moderní kardiostimulátory. Ani tato metoda však není dostatečně přesná. Například v případě vzniku fibrilace síní se odhadovaná životnost může zásadně prodloužit i přesto, že je nastavena vysoká hodnota stimulační energie, podle které je životnost kalkulována. Naopak životnost se může výrazně zkrátit při nečekaném vzestupu prahů některé z elektrod. Proto je potřeba při kontrole kardiostimulátoru posuzovat všechny parametry komplexně. Pro lékaře, kteří si potrpí na detailní analýzu všech parametrů, jsou v přístroji Adapta k dispozici i obvyklé hodnoty napětí a impedance baterií.
Impedance elektrod je důležitým údajem k posouzení jejich integrity. Všichni lékaři vstupující do oboru kardiostimulace získají jako jeden z prvních poznatků tu skutečnost, že pokles impedance elektrod svědčí pro poruchu izolace, zatímco vzestup impedance pro její nalomení nebo úplnou frakturu. Změna impedance oproti předchozí kontrole je tedy vždy důležitou informací [8]. Při hodnocení je potřeba vzít v úvahu i dynamiku změn. K tomu napomáhá grafické znázornění trendu vývoje impedancí elektrod. Jinou váhu má pozvolný vzestup impedance u nedávno naimplantované elektrody než náhlý vzestup impedance v určitém konkrétním období, zvláště když si pacient dodatečně vzpomene, že v té době prodělal nějaký na první pohled méně významný úraz. Taková informace může vést k indikaci skiaskopické kontroly elektrod nebo k volbě zcela jiného postupu sledování a léčby nemocného.
Automatické měření stimulačních prahů je velkou výhodou moderních přístrojů. Vede jednak k významné úspoře stimulační energie [9] a jednak umožňuje grafické zobrazení vývoje hodnot v čase. Tento časový trend je mnohem přínosnější, než jednorázová hodnota, naměřená při kontrole v ambulanci. Je možno sledovat historii vývoje prahů, a tak posoudit, zda i při relativně vyšší hodnotě prahu je již patrna tendence k poklesu, nebo hodnoty prahů trvale stoupají. Automatické měření síňových prahů u pacienta s paroxyzmální fibrilací síní pak přináší možnost podívat se na historii hodnot prahů z minulosti. Lze tak například posoudit, zda příčinou vzniku fibrilace síní nebyl vzestup síňového prahu do hodnot, při nichž byla stimulace v síních neúčinná.
Moderní přístroje dovolují i automatickou adaptaci stimulační energie podle hodnoty změřených stimulačních prahů. Tento proces výrazně prodlužuje životnost přístrojů a současně umožňuje bezpečné přizpůsobení v případě nečekaného vzestupu stimulačních prahů. Měření stimulačních prahů v komoře je k dispozici již řadu let. Opírá se o to, že stimulus s nadprahovou energií vyvolá tzv. evokovaný potenciál, který je možno zpětně po určité časové prodlevě zachytit elektrodou, která stimulus vydala. Algoritmus funguje i přes to, že aplikace stimulu vede vždy k určité polarizaci elektrody ztěžující adekvátní sensing potenciálu řádově 1 000krát menšího, než byla hodnota aplikovaného stimulu. Na úrovni síní tento algoritmus nelze použít. Masa myokardu síní je totiž mnohem menší a amplituda evokovaného potenciálu je výrazně nižší. Všechny dosavadní snahy o měření účinnosti stimulace touto cestou se proto nezdařilo dovést do komerční podoby. Konstruktéři přístroje Adapta proto volili takový postup, jaký k měření prahů v síni volí elektrofyziolog ve chvíli, kdy je amplituda vlny natolik nízká nebo kdy splývá s předchozím komplexem QRS a nezaručuje spolehlivé změření prahů z povrchového EKG-záznamu. V případě zachovalého síňokomorového převodu se totiž orientuje podle toho, zda odpovídá frekvence komor stimulační frekvenci v síních. Při síňokomorové blokádě sleduje na intrakardiálním signálu výskyt senzovaných cyklů v síních. Pokud síně mají vlastní aktivitu o pomalejší frekvenci, než je zvolená stimulační frekvence v síních, pak není mezi stimulačními artefakty žádná vlastní síňová aktivita detekovatelná. Ve chvíli, v níž se energie stimulace dostane pod hodnotu prahu, začne se v intrakardiálním signálu nezávisle na stimulačních artefaktech objevovat síňová aktivita s frekvencí odpovídající nativní frekvenci síní [5].
Automatické měření prahů má i řadu limitací, které je potřeba znát. Jednou z nich je skutečnost, že prahy lze měřit jen v určitém frekvenčním rozmezí. Je-li vlastní komorová aktivita rychlejší, než algoritmus dovoluje, nelze měření provést. Obdobně ruší měření prahů velké množství komorové ektopické aktivity. To byl zřejmě i důvod, proč byla v našem souboru v případě měření komorového prahu 1krát hodnota starší než z předchozího kalendářního dne – komorová odpověď při fibrilaci síní byla příliš rychlá. Měření síňového prahu má stejná úskalí, jako měření komorového prahu. K tomu navíc přistupuje možné selhání algoritmu v situaci současné absence vlastního síňového rytmu a vlastního síňokomorového převodu.
Automatické měření amplitudy intrakardiálního signálu je rovněž velmi důležité. Umožňuje přizpůsobit citlivost přístroje aktuální amplitudě signálu. Je například dobře známo, že amplituda síňového signálu má sklon k výraznému kolísání podle fyzické aktivity nemocného a podle denní doby [10]. Pokud jsme se v minulosti chtěli pokusit nastavit hodnotu, která by skutečně odpovídala kolísání amplitud vlny P, pak bylo třeba analyzovat histogram amplitudy vlny P a na jeho základě upravit nastavení přístroje [11]. Přesto bylo přesné naprogramování tohoto parametru obtížné. Nadměrná citlivost síňového kanálu totiž vede k jevu popisovanému jako „paradoxně nedostatečná citlivost“, protože takto detekované signály již mohou napodobovat rušení, síňový kanál může být těmito signály zahlcen, a to znemožňuje správnou reakci na vlastní síňovou aktivitu [12]. Nedostatečná citlivost zase zpomaluje nebo invalidizuje funkci změny režimu při vzniku fibrilace síní [13]. Vývoje amplitud vlny P pak umožňuje sledovat, zda je tato amplituda dostatečná i při vzniku fibrilace síní.
Měření sensingu má rovněž své limitace. Výrobce se rozhodl neuvádět hodnoty sensingu tehdy, jestliže je podíl stimulovaných dosahuje či přesahuje 80 %. Informace by mohla být za těchto okolností zavádějící a mohla by odrážet pouze amplitudu infrekventní ektopie. Periodické zpomalování frekvence stimulovaného rytmu pod hranici základní stimulační frekvenci za účelem získání adekvátní hodnoty sensingu asi není způsob, který by si lékaři či pacienti přáli. Na druhou stranu ponechání režimu „sensing assurance“ je možné i při absenci vlastního rytmu, neboť není-li >80 % cyklů vlastních, pak přístroj používá lékařem nastavenou hodnotu sensingu. V naší populaci pacientů byla ve všech případech tato funkce ponechána aktivní.
Na úvodní obrazovce programovacího zařízení jsou i další důležité informace. Jednou z nich je procento stimulovaných stahů v komorovém kanálu. Tato informace je zásadní ve světle výsledků studií MOST [14] nebo DAVID [15,16], které ukázaly na narůstající riziko vzniku fibrilace síní, srdečního selhání nebo mortality v závislosti na množství komorové stimulace. K posouzení klinického stavu pacienta je rovněž výhodné analyzovat informace o detekci epizod fibrilace síní nebo jiných síňových tachyarytmií.
Výše uvedený přehled ukazuje, že automatické funkce jsou v moderních přístrojích pokročilé a při kontrole nemocného jsou schopny dodat okamžitě řadu údajů potřebných k vyhodnocení správné funkce přístroje. Pozornost lékaře se tedy může obrátit jinam – může se obrátit k detailní analýze holterovských funkcí přístroje a ke skutečnému vyhodnocení klinického stavu pacienta. Díky těmto novým charakteristikám kardiostimulátorů se tak lékař vrací z pozice technika do své skutečné profese. Vrací se do pozice, kdy může zhodnotit komplexně stav pacienta a jeho interakci s implantovaným přístrojem a nemusí se zabývat tím, zda je dostatečná impedance baterie nebo zda vyžaduje zavést režim častějších kontrol přístroje. Nemusí se trápit hypotézou, že za vznikem současné epizody fibrilace síní je přechodně neúčinná stimulace síňové elektrody.
Závěr
Moderní kardiostimulátor je schopen sám změřit všechny důležité parametry svědčící pro jeho spolehlivou funkci a dobrý stav baterií. Tyto parametry dokáže nabídnout ošetřujícímu lékaři na obrazovce programovacího zařízení bezprostředně po telemetrickém načtení dat. Pokud některý ze zásadních údajů chybí, je to obvykle výrazem vysokého stimulačního prahu, fibrilace síní při měření síňového prahu nebo nízkého podílu senzovaných cyklů. Podle výsledků automatických měření je schopen nastavit hodnoty sensingu a energie stimulace bez zásahu ošetřujícího lékaře. Jsou-li parametry snímání a stimulace v přijatelném rozmezí, není důvod do automatického režimu nastavování těchto hodnot zasahovat.
Doručeno do redakce 9. 10. 06
Přijato k otištění po recenzi 20. 10. 06
MUDr. Vlastimil Vančura
MUDr. Jan Bytešník, CSc.
MUDr. Kateřina Lefflerová, CSc.
MUDr. Renata Krausová
MUDr. Robert Čihák, CSc.
MUDr. Petr Peichl, Ph.D.
prof. MUDr. Josef Kautzner, CSc.
Kardiologická klinika, IKEM, Praha
Sources
1.Neuzner J, Schwarz T, Sperzel J. Pacemaker automaticity. Am J Cardiol 2000; 86(Suppl 1): 104-110.
2.Wallmann D, Degeratu FT, Fuhrer J. Ventricular capture management – reliability in the clinical practice. Europace 2001; 2(Suppl B): 129.
3.Sperzel J, Hugl B, Michaelsen J et al. The European Kappa registry: Automatic ventricular capture management. Europace 2002; 3(Suppl A): 53.
4.Cohen MI, Buck K, Tanel RE et al. Capture management efficacy in children and young adults with endocardial and unipolar epicardial systems. Europace 2004; 6 : 248-255.
5.Sperzel J, Milasinovic G, Smith TW et al. Automatic measurement of atrial pacing thresholds in dual-chamber pacemakers: Clinical experience with atrial capture management. Heart Rhythm 2005; 2 : 1203-1210.
6.Guyomar Y, Graux P, Heuls S et al. Evaluation, during exercise, of atrial auto adjusting sensitivity algorithm. Eurpace 2001; 2(Suppl A): 59.
7.Untereker DF, Shepard RB, Schmidt CL et al. Power systems for implantable pacemakers, cardioverters, and defibrillators. In: Ellenbogen KA, Kay GN, Wilkoff BL. Clinical cardiac pacing and defibrillation. 2nd ed. Philadelphia: WB Saunders Company 2000 : 167-193.
8.Levine PA, Love CJ. Pacemaker diagnostics and evaluation of pacing system malfunction. In: Ellenbogen KA, Kay GN, Wilkoff BL. Clinical cardiac pacing and defibrillation. 2nd ed. Philadelphia: WB Saunders Company 2000 : 827-875.
9.Gelvan D, Crystal E, Dokumaci B et al. Effect of modern pacing algorithms on generator longevity: A predictive analysis. PACE 2003; 26 : 1796-1802.
10.Castro A, Liebold A, Vincente J et al. Evaluation of autosensing as an automatic means of maintaining a 2 : 1 sensing safety margin in an implanted pacemaker. PACE 1996; 19 : 1708-1713.
11.Boute W, Albers BA, Giele V. Avoiding atrial undersensing by assessment of P wave amplitude histogram data. PACE 1994; 17 : 1878-1882.
12.Kolb C, Halbfass P, Zrenner B, Schmitt C. Paradoxical atrial undersensing due to inappropriate atrial noise reversion of atrial fibrillation in dual-chamber pacemakers. J Cardiovasc Electrophysiol 2005; 16 : 696-700.
13.Leung SK, Lau CP, Lam CTF et al. Programmed atrial sensitivity: A critical determinant in atrial fibrillation detection and optimal automatic mode switching. PACE 1998; 21 : 2214-2219.
14.Sweeney MO, Hellkamp AS, Ellenbogen KA et al. Adverse Effect of Ventricular Pacing on Heart Failure and Atrial Fibrillation Among Patients With Normal Baseline QRS Duration in a Clinical Trial of Pacemaker Therapy for Sinus Node Dysfunction. Circulation 2003; 107 : 2932-2937
15.Wilkoff BL, Cook JR, Epstein AE et al. Dual-chamber pacing or ventricular backup pacing in patients with an implantable defibrillator: the Dual Chamber and VVI Implantable Defibrillator (DAVID) Trial. JAMA 2002; 288 : 3115-3123.
16.Sharma AD, Rizo-Patron C, Hallstrom AP et al. Percent right ventricular pacing predicts outcomes in the DAVID trial. Heart Rhythm 2005; 2 : 830-834.
Labels
Paediatric cardiology Internal medicine Cardiac surgery Cardiology
Article was published inCardiology Review

2006 Issue 4-
All articles in this issue
- Historie trvalé kardiostimulace
- Automatické funkce kardiostimulátorů
-
Jsou moderní automatické kardiostimulátory skutečně automatické?
Medtronic Adapta a jeho automatické funkce - Nová antiarytmika v léčbě fibrilace síní
- Akutní infarkt myokardu u žen
- Léčba hypertenze u chronické renální insuficience
- Studie SPARCL – the Stroke Prevention by Aggressive Reduction in Cholesterol Levels: komentář
- Vyšetřování srdeční stability
- Cardiology Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Automatické funkce kardiostimulátorů
- Vyšetřování srdeční stability
- Léčba hypertenze u chronické renální insuficience
- Nová antiarytmika v léčbě fibrilace síní
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

