-
Medical journals
- Career
Myopatie asociovaná se statiny: klinické doporučení Slovenskej asociácie aterosklerózy a České společnosti pro aterosklerózu
Authors: Daniel Pella; Anna Gvozdjáková; Ján Lietava; Jana Tisoňová; Katarína Rašlová; Branislav Vohnout (za Slovenskou Asociaci Aterosklerózy); Michal Vrablík; Vladimír Bláha; Renata Cífková; Richard Češka; Tomáš Freiberger; Pavel Kraml; Jan Piťha; Hana Rosolová; Vladimír Soška; Tomáš Štulc; Hana Vaverková; Zuzana Urbanová (za Českou Společnost Pro Aterosklerózu)
Published in: AtheroRev 2016; 1(1): 7-13
Category: Guidelines
*(za Slovenskou asociaci aterosklerózy)
**(za Českou společnost pro aterosklerózu)Overview
Nežádoucí účinky hypolipidemik a především statinů se dostaly v poslední době do popředí pozornosti. Obecně definujeme statinovou intoleranci jako přítomnost svalových obtíží nebo dalších nežádoucích příznaků (nebo laboratorních abnormalit) spojených s terapií statiny, které vede k jejímu vysazení, nebo znemožňují titraci léčby k dávce dostatečné k dosažení cílové hodnoty LDL-cholesterolu. Frekvence statinové intolerance se pohybuje v rozpětí od 1 % do 20 % v různých popsaných souborech. Nejdůležitější jsou se statiny spojené svalové obtíže, tzv. se statiny asociovaná myopatie (SAM). Protože neexistuje dostatečně specifický a senzitivní laboratorní marker SAM, je vhodné používání skórovacích systémů určujících pravděpodobnost SAM na základě charakteru symptomů. Existuje řada rizikových faktorů rozvoje SAM (včetně lékových interakcí), které musíme zhodnotit, a pokud možno, eliminovat, již před zahájením léčby. Z hlediska terapie je vhodné připomenout, že většina pacientů se SAM je schopna tolerovat jiný statin a/nebo jiné dávkování statinu. V případě úplné intolerance (po vyzkoušení nejméně 2 až 3 různých typů statinu) volíme terapii založenou na jiných hypolipidemicích. V tomto směru jsou jistě nadějí nové léčebné možnosti (především inhibitory PCSK9).
Klíčová slova:
alternativní léčba – hypolipidemika – myopatie asociovaná se statiny – nežádoucí účinky – skórovací systém – statiny – statinová intoleranceÚvod
Intoleranci hypolipidemik a zejména pak problémům se snášenlivostí statinů se v poslední době věnuje více pozornosti než dříve. Důvodů je několik. Narůstající absolutní počet uživatelů statinů provází pochopitelně narůstající počet těch z nich, kteří pociťují relativně vzácné nežádoucí účinky. V každodenní klinické praxi léčíme statiny i osoby s vyšším rizikem vzniku nežádoucích účinků, protože rizikové faktory kardiovaskulárních onemocnění a statinové intolerance se často překrývají. Navíc vývoj farmakologických možností hypolipidemické léčby umožní v dohledné době použití alternativ statinů s dostatečnou hypolipidemickou účinností při lepší toleranci ze strany nemocných.
Při terapii statiny přichází v úvahu více možných nežádoucích účinků – svalové, diabetogenní, elevace transamináz a ostatní (např. nauzea, kognitivní nežádoucí účinky, proteinurie aj). Intoleranci statinů můžeme definovat jako přítomnost svalových obtíží nebo dalších nežádoucích příznaků (nebo laboratorních abnormalit) spojených s terapií statiny, které vedou k jejich vysazení nebo znemožňují titraci léčby k dávce dostatečné k dosažení cílové hodnoty LDL-cholesterolu. Česká společnost pro aterosklerózu a Slovenská asociace aterosklerózy se rozhodly vytvořit stručné konsenzuální stanovisko, které by mělo být vodítkem použitelným při diagnostice i řešení svalových nežádoucích účinků statinů v každodenní praxi.
Epidemiologie
Obtíže spojené s léčbou statiny se vyskytují u 1 až 29 % pacientů uživatelů podle toho, zdali se jedná o údaje z randomizovaných klinických studií anebo ze studií observačních. Nejčastějšími subjektivními stesky při terapii statiny jsou svalové obtíže.
V randomizovaných klinických studiích se myalgie vyskytovala s frekvencí 1 % až 5 %, v observačních pracích pak výrazně více – 11 % až 29 %. V hlavních studiích se statiny nebyl zaznamenán nárůst výskytu svalových komplikací v porovnání s placebem. Jediná klinická studie sledující výskyt svalových komplikací při terapii statinem v randomizovaném uspořádání (studie STOMP) dokumentovala vyšší výskyt myalgie se zvýšením průměrné hladiny kreatinkinázy (CK) (výskyt myalgie 9,4 % ve skupině léčené 80 mg atorvastatinu vs 4,6 % v placebové větvi, p = 0,05). Mezi limitace randomizovaných studií patří metodologická různorodost, různé definice svalových obtíží, vyloučení pacientů se svalovými komplikacemi nebo s rizikovými faktory jejich rozvoje. Oproti tomu observačním studiím často chybí kontrolní skupiny (např. studie PRIMO uvádějící výskyt svalových symptomů u 10,5 % pacientů během podávání statinů) a v případě, že je mají, obvykle se svalové obtíže vyskytují relativně často i u těch, kteří statiny neužívají (např. údaje ze studie NHANES 1999–2004 – 23% výskyt u osob léčených statiny vs 18% u osob, kterým se statiny nepodávaly, P = 0,02). Randomizované i observační studie ukázaly relativně časný nástup myalgií většinou během 1. měsíce po zahájení léčby. Nejobávanější komplikace hypolipidemické farmakoterapie rabdomyolýza se vyskytuje s frekvencí 0,3–0,44/na 10 000 osobo-roků.
Patofyziologie
Myopatie asociovaná se statiny (SAM – statin-associated myopathy) vzniká nejčastěji při zvýšení jejich koncentrace v buňkách příčně pruhovaných svalů z různých důvodů. Je zajímavé, že na myokard mají statiny neutrální, či spíše příznivé účinky. Důvod této skutečnosti není zcela jasný, jedná se zřejmě o rozdílné transportní mechanizmy v buňkách myokardu a v příčně pruhovaných svalech kosterní svaloviny.
Spíše schematicky se účinky rozdělují na přímo toxické a imunologické. Mezi přímo toxické patří postižení mitochondrií, buněčných membrán, transportních mechanizmů včetně vápníkových a celkově k posunu osudu buněk k apoptóze/autofagii. Přitom zřejmě hraje významnou úlohu interakce statinů s metabolizmem farnezyl pyrofosfátu a geranylgeranyl pyrofosfátu. Druhou skupinou jsou účinky převážně imunologické, které se dále dělí na zánětlivé a nezánětlivé.
Agravující faktory jsou ty, které výrazně zvyšují dostupnost statinů v příčně pruhovaných svalech, případně činí svalové buňky citlivější k jejich nežádoucím účinkům, tedy především lékové interakce, které koncentrace a dostupnost statinů zvyšují, a větší svalová zátěž.
Rizikové faktory
Myopatie asociovaná se statiny je pravděpodobnější u nositelů rizikových faktorů jejího rozvoje. U takových pacientů musíme vedení terapie uzpůsobit a snažit se o optimalizaci podmínek podávání statinů včetně intenzivnějšího sledování snahy o eliminaci/zmírnění všech ovlivnitelných rizikových faktorů rozvoje SAM. Nejdůležitější rizikové faktory a podmínky shrnuje tab. 1.
Table 1. Rizikové faktory rozvoje myopatie asociované se statiny 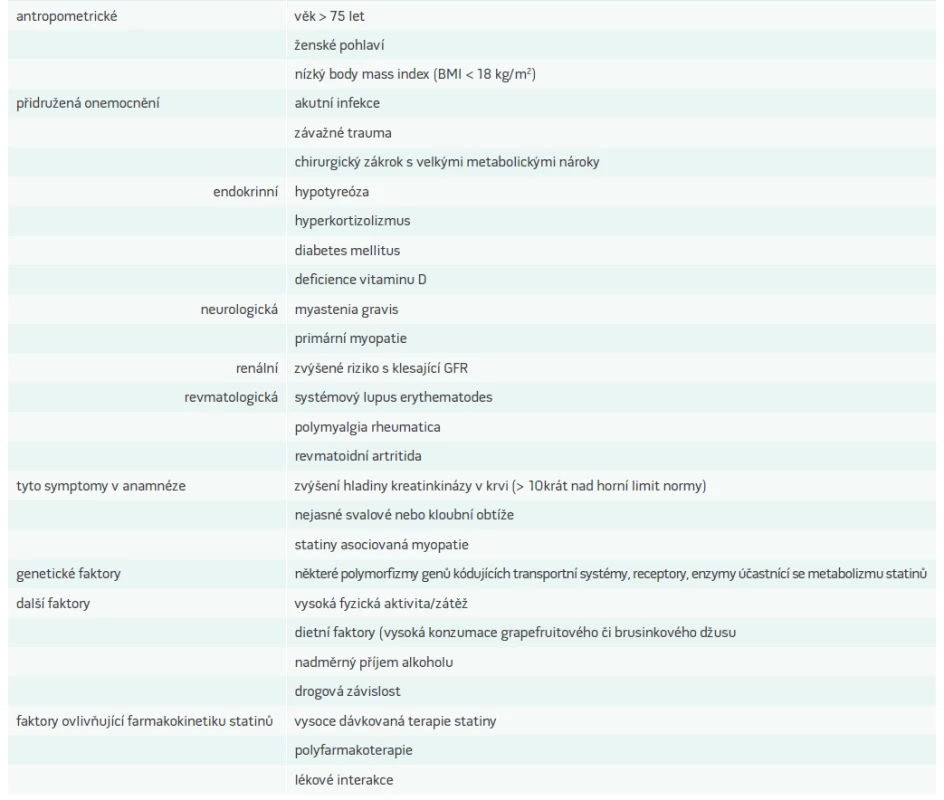
Lékové interakce právem představují jeden z nejdůležitějších rizikových faktorů rozvoje SAM i možnost jí předejít volbou farmakoterapie, která má na zřeteli problematiku lékových interakcí se statiny.
Lékové interakce statinů
Interakce statinů s jinými léky může být relativně častou příčinou intolerance a/nebo nežádoucích účinků statinů. Lékové interakce statinů mohou být několikerého typu:
- Vlivem jiného léků dochází ke zpomalené degradaci/eliminaci statinu, čímž narůstá riziko nežádoucích účinků statinů (myopatie, myalgie ap)
- Vlivem jiného léků dochází ke zrychlené degradaci/eliminaci statinu, a tím k jeho nedostatečnému účinku na snížení LDL-cholesterolu
- Vlivem statinu je ovlivněn metabolizmus/degradace jiného léku, který tak může sám způsobit některé nežádoucí účinky
Z hlediska myopatie asociované se statiny jsou významné pouze interakce uvedené pod bodem 1. – ty které vedou ke zpomalené degradaci/eliminaci statinů:
- Lovastatin a simvastatin (přibližně ve 20 % i atorvastatin) jsou metabolizovány systémem cytochromu P450 3A4. Tento systém významně inhibují následující léky, které by neměly být podávány současně s uvedenými statiny:
- makrolidová antibiotika, především klaritromycin, telitromycin a erytromycin, méně roxitromycin.
- antimykotika ze skupiny „azolů“, především ketokonazol, itrakonazol, posakonazol a vorikonazol.
- některá antihypertenziva ze skupiny blokátorů kalciových kanálů, především diltiazem a verapamil, částečně i amlodipin (zejména v kombinaci se simvastatinem, jehož denní dávka by při této kombinaci dle doporučení FDA neměla překročit 20 mg) a také antiarytmikum amiodaron
- většina inhibitorů proteáz (antivirotika), např. ritonavir, lopinavir, atazanavir, sachinavir, indinavir, darunavir, nelfinavir, fosamprenavir a další
- další léky: cyklosporin A a kyselina fusidová, slabým inhibitorem cytochromu P450 3A4 je i cimetidin
- Fluvastatin je metabolizován cytochromem P450 izoenzymem 2C9, který je významně inhibován flukonazolem a částečně i amiodaronem; slabým inhibitorem 2C9 je omeprazol.
- Pravastatin, rosuvastatin jsou vylučovány převážně v nezměněné podobě mimo systém cytochromu P450, ale pro jejich eliminaci jsou klíčové membránové transportní proteiny, především skupina transportérů OATP1B1, MRP a P-glykoprotein. Silným inhibitorem těchto transportních proteinů jsou především:
- Cyklosporin A, který je kontraindikován i s pravastatiem a rosuvastatinem a prakticky jediným bezpečným statinem do kombinace je fluvastatin
- Inhibitory proteáz (prakticky všechny výše uvedené) – i v tomto případě je zřejmě jediným relativně bezpečným statinem do kombinace fluvastatin.
Tab. 2 shrnuje podstatné interakce statinů s léčivy zpomalujícími jejich metabolizaci a zvyšujícími jejich sérové hladiny.
Table 2. Interakce statinů s léčivy zvyšujícími jejich plazmatické koncentrace 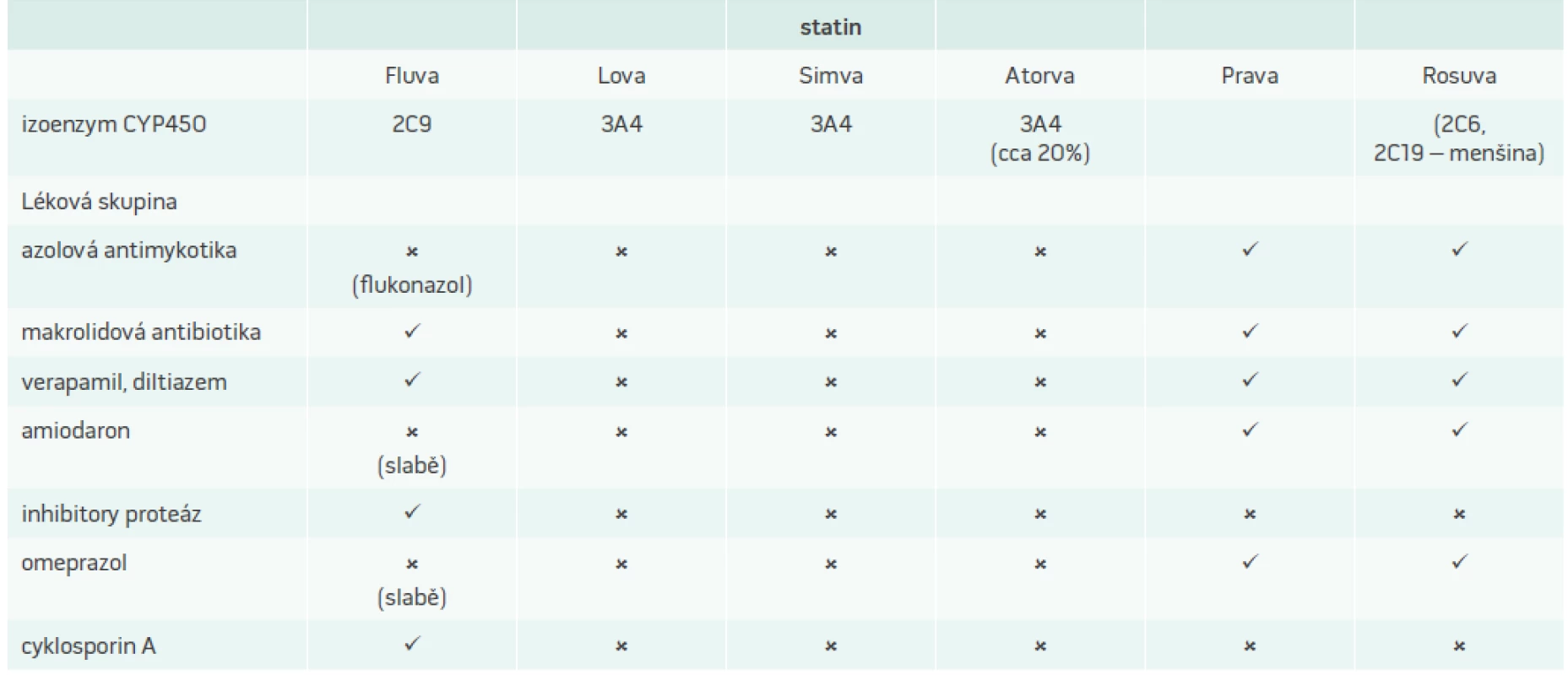
x – nevhodná kombinace – interakce pravděpodobná ✔ – kombinace možná – interakce nepravděpodobná Při předpisu statinů je nutné vždy odebrat farmakologickou anamnézu a stejně tak u nemocných užívajících dlouhodobě statin je třeba při předpisu dalších léků vždy zvážit, zda nebude hrozit riziko interakcí. U nemocných užívajících větší množství léků je vhodné preferovat statiny s menším rizikem interakcí, jako je fluvastatin, eventuálně rosuvastatin a pravastatin.
Myopatie asociovaná se statiny: diagnostika a současné definice
Diagnóza myopatie asociované se statiny (SAM) je obtížná, protože je založena na subjektivním nálezu a protože dosud nemáme k dispozici spolehlivý a objektivní diagnostický test.
Diagnostická kritéria dle konsenzu amerických odborných společnosti (American Heart Association/American College of Cardiology a National Lipid Association) jsou založena na výskytu symptomů a výši elevace kreatinkinázy (CK). K objektivnímu zhodnocení svalových symptomů navrhla americká Národní lipidová asociace skórovací systém (tab.3), který vychází ze studií STOMP a PRIMO.
Table 3. Hodnocení bolesti svalů při myopatii asociované se statiny 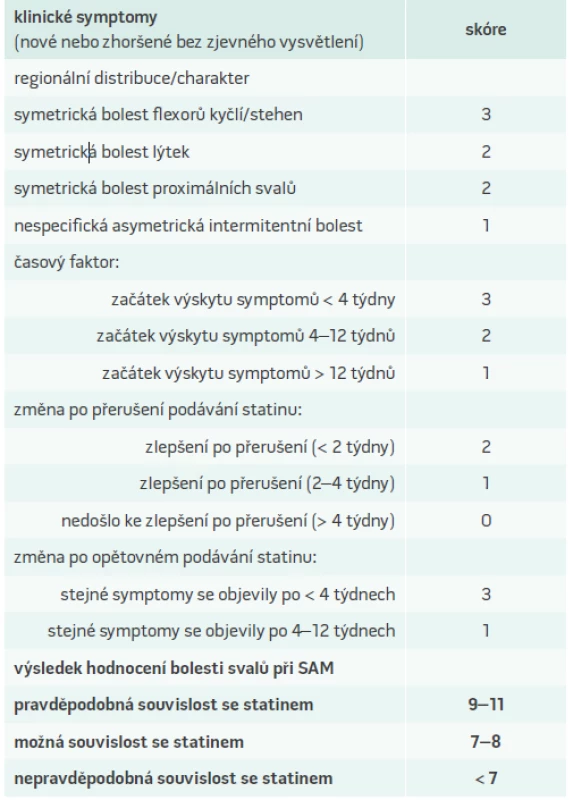
Podle konsensu European Atherosclerosis Society (EAS) je diagnóza SAM klinická a je postavena na základě charakteru svalových symptomů, elevace CK > 4krát nad stanovený horní limit ve 2 vyšetřeních v průběhu 2 týdnů a časového vztahu k léčbě statinem (zahájení, přerušení, opětovné podání). Dalšími testy, které mohou přispět k diagnóze myopatie asociované se statiny je objektivní vyšetření svalové síly, farmakogenetické vyšetření a svalová biopsie.
Experti EAS doporučují zahrnout do diagnózy myopatie asociované se statiny všechny typu svalových obtíží (bolesti, slabost, křeče), a ty dále rozdělit podle toho, zda je hodnota CK normální nebo zvýšená (tab. 4). Bolest a slabost je při SAM typicky symetrická a proximální, a obvykle postihuje velké svalové skupiny včetně svalů stehen, hýždí, lýtek a zad. Diskomfort a slabost se typicky objevují časně (4–6 týdnů po zahájení léčby statinem), ale mohou se vyskytnout i po mnohaleté léčbě. Nástup nových symptomů se může objevit po zvýšení dávky statinu nebo při interakci s jiným lékem. Symptomy se objevují častěji u fyzicky aktivních jedinců.
Table 4. Diagnóza myopatie asociované se statiny dle konsensu European Atherosclerosis Society 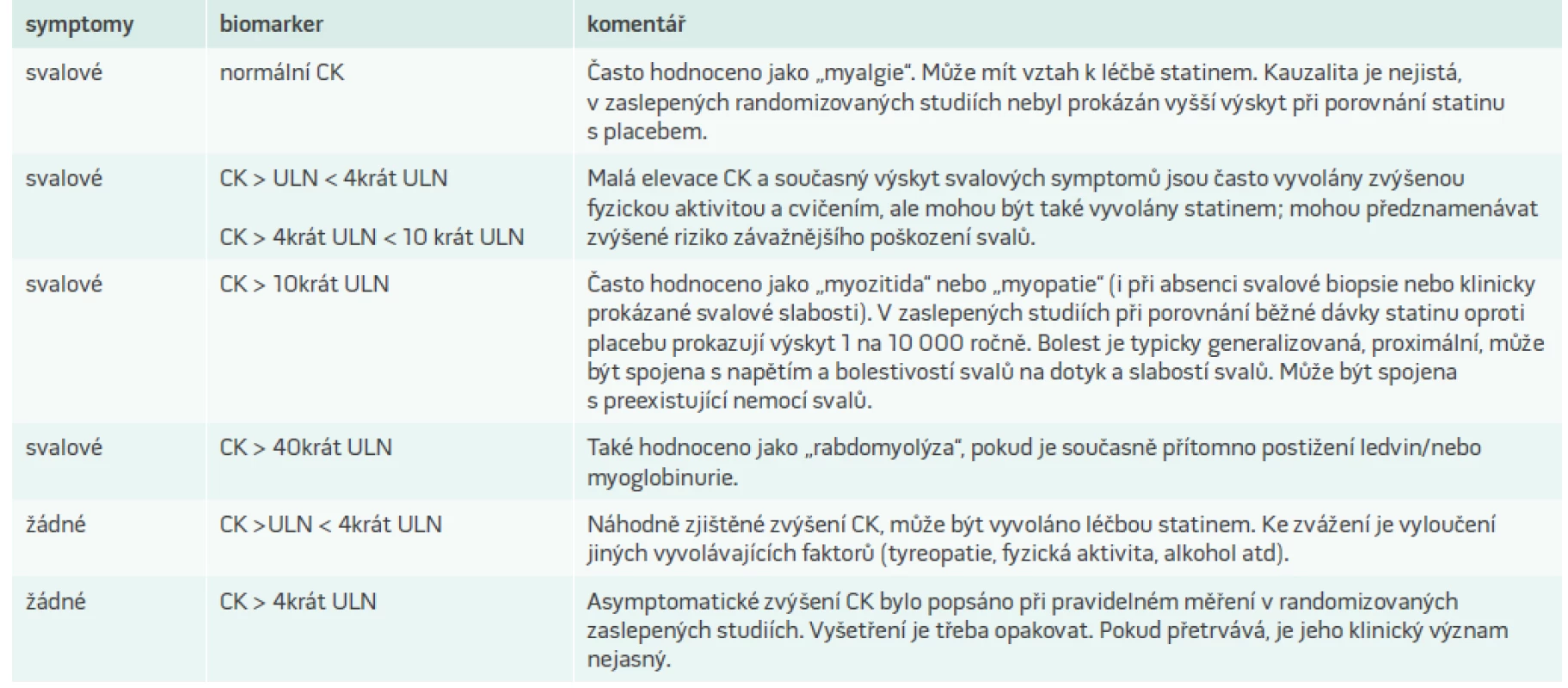
CK – kreatinkináza ULN – upper limits of normal/nad stanovenou horní hranicí normálních hodnot Terapeutický přístup k pacientům s intolerancí statinů
Nízké dávky statinů/alternativní dávky statinů
Celá řada nemocných, kteří mají nežádoucí účinky po určitém statinu (některém, po určité dávce) mohou tolerovat statin jiný, třeba v nízké dávce a v alternativním dávkování.
V každém případě je třeba zdůraznit, že robustní data, která potvrzují pozitivní a protektivní kardiovaskulární účinky statinů jsou jednoznačným zdůvodněním toho, abychom se snažili pacienty, nebo alespoň valnou většinu z nich, léčit statiny, třeba v netypickém režimu. Rozhodně bychom neměli vyřazovat statiny z našeho armamentária hypolipidemik jako lékovou skupinu při prvním potenciálním nežádoucím účinku.
I když se na tomto místě překrýváme s částí předešlého textu, je třeba i v odstavci o léčbě statiny zmínit fakt, že vždy musíme vyloučit eventuální jiné příčiny myalgie (elevace CK), jako jsou revmatologická a neurologická onemocnění, nadměrná fyzická zátěž u netrénovaných nebo alkohol. Stejně tak je třeba zmínit predisponující faktory, které mohou vyvolat nebo agravovat příznaky statinové intolerance. Jedná se tu především o faktory ovlivnitelné, jako jsou hypotyreóza, deficience vitaminu D nebo léková interakce.
Pokud má pacient myalgii a vyloučili jsme alespoň orientačně jinou příčinu jejího vzniku, eventuálně predisponující faktory, nabízí se několik možností řešení. To jaké řešení zvolíme, závisí na stupni rizika nemocného, zda je v primární prevenci či po akutní revaskularizaci a podobně. Nejjednodušším řešením je přerušení podávání statinu na období několika týdnů (2–6 týdnů) a posléze jeho opětovné podávání ve stejné dávce (pokud šlo o dávku základní nebo střední) nebo nižší (pokud byla původní dávka maximální). Druhou možností může být pouze snížení dávky a pokračování v léčbě za pečlivé laboratorní i klinické kontroly. Posléze existuje třetí možnost nahrazení některého z „nejúčinnějších“ statinů (atorvastatin, rosuvastatin), statinem „ze skupiny bezpečnějších“ (fluvastatin, pravastatin a u nás zatím nedostupný pitavastatin). Simvastatin stojí trochu mimo tuto klasifikaci a v současné době ho nepovažujme za statin volby pro nemocné, u nichž se s léčbou statinem začíná (ačkoli nezpochybňujeme pozitivní data z intervenčních studií, nežádoucích účinků má přece jen více než ostatní, zejména při vyšším dávkování).
V každém případě je třeba uvažovat o obnovení statinové terapie. Někteří považují za průkaz absolutní nesnášenlivosti statinu opětné objevení se symptomů po druhém, maximálně třetím opakovaném zahájení léčby nižší dávkou a/nebo zahájení podávání jiného statinu. Možná tato definice postačuje v běžné klinické praxi, specializovaná pracoviště by však měla pracovat i s jiným (alternativním) režimem podávání statinu. Lze používat minimální dávky statinu (např. 2,5 mg rosuvastatinu), nebo podávat statin v nízké dávce obden, popřípadě 2–3krát týdně. Samozřejmě, že k takovému režimu se budeme uchylovat především u nemocných s intolerancí běžných režimů podávání statinů v kontextu jejich naléhavé indikace. Je samozřejmě faktem, že dosažení cílových hodnot při alternativním dávkování každý druhý den s nízkou dávkou „bezpečného“ a méně účinného statinu je obtížné. Z jiného hlediska nazíráno je ale pravda, že výsledky jsou někdy až překvapivě výraznější, než bychom očekávali. A samozřejmě u převážné většiny nemocných léčených „minidávkou“ statinu využíváme, často s velmi dobrým efektem, kombinační léčby.
Ostatní hypolipidemika
U většiny pacientů netolerujících statiny je vhodné použití dalších hypolipidemik v kombinaci s malou dávkou statinu nebo v monoterapii (při intoleranci jakékoliv léčby statinem). V kombinaci s nízkou dávku statinu vedou k obdobnému snížení LDL-cholesterolu jako vyšší dávky statinů.
Ezetimib snižuje hladinu LDL-cholesterolu o 15–20 % a je velmi dobře snášen. U pacientů netolerujících statiny je proto používán velmi často.
Fibráty u pacientů se smíšenou hyperlipidemií vedou obvykle k výraznému snížení hladiny LDL-cholesterolu. Při nemožnosti podávat statiny jsou proto u těchto pacientů vhodnou volbou. Při kombinaci se statiny (u pacientů s jejich částečnou intolerancí) je však třeba opatrnosti, neboť fibráty mohou zhoršovat projevy myopatie.
Pryskyřice (sekvestranty žlučových kyselin) mají podobný vliv na LDL-cholesterol jako ezetimib, v současné době jsou v ČR obtížně dostupné.
Inhibitory proprotein konvertázy subtilizin/kexin 9 (PCSK9) jsou novou skupinou hypolipidemik, která bude uvedena na trh v nejbližších letech. Snižují hladinu LDL-cholesterolu přibližně o 50 %. Intolerance statinů bude zřejmě jednou z významných indikací těchto léků.
Dietní a režimová opatření
Nefarmakologická léčba příznivě ovlivňuje lipidogram i další rizikové faktory aterosklerózy. U většiny pacientů je obtížné dosáhnout, aby dietní a režimová opatření dodržovali. U pacientů, kteří špatně tolerují hypolipidemickou léčbu, je však motivace k jejich dodržování často vyšší. Důraz na důsledné dodržování dietních a režimových opatření tak může u pacientů s intolerancí statinů pomoci k dosažení cílových hodnot léčby v těchto případech. Připomeňme, že důsledné dodržování všech dietních opatření (snížení příjmu saturovaných tuků, zvýšení nesaturovaných tuků, eliminace konzumace trans-tuků, rostlinné steroly, zvýšení spotřeby vlákniny a konzumace ořechů atd) umožní snížit koncentraci LDL-cholesterolu o 20–25 %.
Ovlivnění dalších rizikových faktorů
Hlavním cílem léčby dyslipidemií je snížení kardiovaskulárního rizika. Pokud jsou možnosti hypolipidemické léčby omezené částečnou nebo úplnou intolerancí, je proto nezbytná snaha snížit toto riziko důslednou léčbou ostatních rizikových faktorů aterosklerózy, především arteriální hypertenze a nikotinizmu. Tato léčba také může pacienta přesunout do nižší kategorie rizika, s mírnějšími a snáze dosažitelnými cílovými hodnotami cholesterolu.
Koenzym Q 10
Suplementace koenzymem Q10 (CoQ10) se u pacientů se statiny asociovanou myopatií (SAM) užívá relativně často. Nedávno publikované studie ani metaanalýza však neprokázaly snížení výskytu myalgií při podávání CoQ10. Podávání CoQ10 v prevenci či léčbě SAM proto nelze doporučit.
Vitamin D
I když literární údaje jsou různorodé, významná deficience vitaminu D vede ke svalovým bolestem a snížení svalové síly a vitamin D deficientní pacienti mají větší svalové obtíže. Nedávná studie Khayznikova a spolupracovníků ukázala, že u vitamin D deficientních pacientů korekce deficience umožnila 80% dříve intolerantních pacientů užívat statin.
Management pacientů se SAM
Management pacientů se SAM včetně hodnocení hladin CK shrnuje schéma zpracované na podkladě dat uveřejněných Evropskou společností pro aterosklerózu (European Atherosclerosis Society Consensus Panel Statement on Assessment).
Schéma. Management pacientů se SAM včetně hodnocení hladin CK. Upraveno podle [3] ![Schéma. Management pacientů se SAM včetně hodnocení hladin CK. Upraveno podle [3]](https://pl-master.mdcdn.cz/media/image/2773df5fbcf67508416a7acfca455c78.png?version=1537793099)
Závěr
Nežádoucí účinky statinů limitují jejich použití a často znemožňují jejich podávání anebo dosažení cílových hodnot LDL-cholesterolu. Jejich přítomnost významně negativně ovlivňuje dlouhodobou adherenci k léčbě a je důležitou příčinou tzv. reziduálního vaskulárního rizika léčených. Nejvýznamnějším projevem statinové intolerance s největším dopadem na prognózu nemocného je vysazení terapie statinem. Identifikace (a odstranění) rizikových faktorů rozvoje nežádoucích účinků, přizpůsobení terapie individuálním potřebám pacienta, komunikace s nemocným včetně upozornění na možné (a opravdu relevantní) nežádoucí účinky spolu s jejich řešením zvyšuje pravděpodobnost dosažení dlouhodobé spolupráce a úspěchu v prevenci aterotrombotických cévních příhod. Více než polovina pacientů označených jako statin intolerantní je schopna tolerovat hypolipidemickou farmakoterapii po její úpravě. Příchod nových léčebných možností umožní dosažení cílových hodnot sérových lipidů i u nemocných s úplnou intolerancí statinů.
prof. MUDr. Daniel Pella, PhD.
Slovenská asociácia aterosklerózy
http://saa.sk
doc. MUDr. Michal Vrablík, Ph.D.
Česká společnost pro aterosklerózu
www.athero.cz
Doručeno do redakce 18. 1. 2016
Sources
1. Pasternak RC, Smith SC Jr, Bairey-Merz CN et al. American College of Cardiology. American Heart Association. National Heart, Lung and Blood Institute. ACC/AHA/NHLBI Clinical advisory on the use and safety of statins. Circulation 2002; 106(8):1024–1028.
2. Rosenson RS, Baker SK, JacobsonTA et al. An assessment by the statin muscle safety task force: 2014 update. J Clin Lipidol 2014; 8(3 Suppl): S58–S71.
3. Stroes ES, Thompson PD, Corsini A et al. European Atherosclerosis Society Consensus Panel. Statin-associated muscle symptoms: impact on statin therapy-European Atherosclerosis Society Consensus Panel Statement on Assessment, Aetiology and Management. Eur Heart J 2015; 36(17):1012–1022.
4. Finegold JA, Manisty CH, Goldacre B et al. What proportion of symptomatic side effects in patients taking statins are genuinely caused by the drug? Systematic review of randomized placebo-controlled trials to aid individual patient choice. Eur J Prev Cardiol 2014; 21(4):464–474.
5. Parker BA, Capizzi JA, Grimaldi AS et al. Effect of statins on skeletal muscle function. Circulation 2013; 127(1):96–103.
6. Bruckert E, Hayem G, Dejager S et al. Mild to moderate muscular symptoms with high-dosage statin therapy in hyperlipidemic patients--the PRIMO study. Cardiovasc Drugs Ther 2005; 19(6):403–414.
7. Buettner C, Rippberger MJ, Smith JK et al. Statin use and musculoskeletal pain among adults with and without arthritis. Am J Med 2012; 125(2):176–182.
8. Graham DJ, Staffa JA, Shatin D et al. Incidence of hospitalized rhabdomyolysis in patients treated with lipid-lowering drugs. JAMA 2004; 292(21): 2585–2590.
9. Guyton JR. Benefit versus Risk in Statin Treatment. Am J Cardiol 2006; 97(8A): 95C-97C.
10. Banach M, Rizzo M, Toth PP et al. Statin intolerance - an attempt at a unified definition. Position paper from an Internanational Lipid Expert Panel. Expert Opin Drug Saf 2015; 14(6): 935–955.
11. Khayznikov M, Hemachrandra K, Pandit R et al. Statin Intolerance Because of Myalgia, Myositis, Myopathy, or Myonecrosis Can in Most Cases be Safely Resolved by Vitamin D Supplementation. N Am J Med Sci 2015; 7(3):86–93.
Labels
Angiology Diabetology Internal medicine Cardiology General practitioner for adults
Article was published inAthero Review

2016 Issue 1-
All articles in this issue
- Myopatie asociovaná se statiny: klinické doporučení Slovenskej asociácie aterosklerózy a České společnosti pro aterosklerózu
- Boj s aterosklerózou: větší síla nebo lepší načasování?
- Familiární hypercholesterolemie: klinické nálezy, molekulární genetika a diferenciální diagnostika
-
Co je nejdůležitější pro pacienty s familiární hypercholesterolemií?
Projekt MedPed v České a Slovenské republice - Přelom v léčbě hypercholesterolemie – inhibitory PCSK9. Co zatím víme o alirokumabu (přípravku Praluent®)
- Inhibítory PCSK9 v manažmente pacientov s vysokým kardiovaskulárnym rizikom – efektívna liečba na dosah
- Athero Review
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Familiární hypercholesterolemie: klinické nálezy, molekulární genetika a diferenciální diagnostika
- Inhibítory PCSK9 v manažmente pacientov s vysokým kardiovaskulárnym rizikom – efektívna liečba na dosah
- Přelom v léčbě hypercholesterolemie – inhibitory PCSK9. Co zatím víme o alirokumabu (přípravku Praluent®)
- Myopatie asociovaná se statiny: klinické doporučení Slovenskej asociácie aterosklerózy a České společnosti pro aterosklerózu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

