-
Medical journals
- Career
Praxe podávání systémových kortikosteroidů kriticky nemocným pacientům s covidem-19 v České republice – dotazníkový průzkum (studie ASAP ‑ C)
Authors: J. Maláska 1,2; F. Keller 1; D. Chlebek 8; J. Stašek 1; J. Hudec 1,2; T. Prokopová 1,2; M. Kratochvíl 3; F. Duška 4; J. Máca 5; K. Brat 6; R. Štěpánová 7; A. Svobodník 7; J. Klučka 2,3; P. Štourač 2,3
Authors‘ workplace: Klinika anesteziologie, resuscitace a intenzivní medicíny, Fakultní nemocnice Brno a Lékařská fakulta Masarykovy univerzity Brno 1; Ústav simulační medicíny, Lékařská fakulta Masarykovy univerzity Brno 2; Klinika dětské anesteziologie a resuscitace, Fakultní nemocnice Brno a Lékařská fakulta Masarykovy univerzity Brno 3; Klinika anesteziologie a resuscitace Fakultní nemocnice Královské Vinohrady a 3. Lékařská fakulta Karlova Univerzita, Praha 4; Klinika anesteziologie a resuscitace, Fakultní nemocnice Ostrava a Lékařská fakulta Ostravské Univerzity 5; Klinika nemocí plicních a tuberkulózy, Fakultní nemocnice Brno a Lékařská fakulta Masarykovy univerzity Brno 6; Farmakologický ústav, Lékařská fakulta Masarykovy univerzity Brno 7; Lékařská fakulta Masarykovy univerzity Brno 8
Published in: Anest. intenziv. Med., 33, 2022, č. 1, s. 7-13
Category: Original Papers
Overview
Cíl studie: Léčba pacientů s těžkým průběhem onemocnění covid-19 (Coronavirus Disease 2019) kortikoidy je doporučena Světovou zdravotnickou organizací na základě výsledků studie RECOVERY. Stále však existuje mnoho otázek stran dávkování, načasování nebo volby konkrétní účinné látky. Toto dotazníkové šetření mělo za úkol zjistit, jakou strategii v podávání systémových kortikoidů skutečně praktikují lékaři ošetřující nemocné s covidem-19 na jednotkách intenzivní péče v České republice.
Typ studie: Průřezové dotazníkové šetření.
Materiál a metoda: Elektronický dotazník obsahující 15 otázek byl zaslán členům České společnosti anesteziologie, resuscitace a intenzivní medicíny, České společnosti intenzivní medicíny a České pneumologické a ftizeologické společnosti. Dotazník byl vyhodnocen pomocí deskriptivní statistické analýzy.
Výsledky: Dotazník vyplnilo celkem 233 respondentů, z toho 231 odpovědí bylo analyzováno. Nejvíce zastoupenou skupinou respondentů byli sekundární lékaři s ukončeným specializačním vzděláváním v oboru Anesteziologie a intenzivní medicína (AIM) (32 %, n = 74). Nejčastější indikací k zahájení podávání kortikoidů u pacientů s covidem-19 byla probíhající oxygenoterapie (maskou nebo nosní kanylou) (59,3 %, n = 137) a vysokoprůtoková nosní kanyla (HFNC) (21,6 %, n = 50). Nejčastěji aplikovaným kortikoidem byl dexamethason (75,8 %, n = 175) v dávce 8 mg i. v. (48,6 %, n = 85), nebo v dávce 6 mg i. v. (32,0 %, n = 56), následován metylprednisolonem (25,5 %, n = 59) v dávce 80 mg i. v. (35,6%, n = 21), nebo v dávce 40 mg i. v. (13,6 %, n = 8). Nejčastější délka terapie byla 10 dnů dexamethason (60,6 %, n = 106), metylprednisolon (20,3 %, n = 12).
Závěr: Zahájení kortikoidní terapie bylo nejčastěji indikováno u pacientů s covidem-19 a oxygenoterapií. Nejčastěji aplikovaným lékem byl dexamethason 8 mg i. v. a 6 mg i. v. po dobu 10 dnů.
Klíčová slova:
dotazník – kortikosteroidy – ARDS – intenzivní péče – COVID-19
Úvod
Pandemie onemocnění covid-19 (Coronavirus Disease 2019), způsobeného virem SARS‑‑CoV-2 (Severe Acute Respiratory Syndrome Coronavirus 2), znovu otevřela debatu o použití systémových kortikoidů v léčbě pacientů se syndromem akutní respirační tísně (ARDS). V teoretické rovině se účinnost kortikosteroidů u ARDS opírá o redukci dysregulované zánětlivé odpovědi. Toho kortikoidy dosahují kombinací genomických a negenomických účinků [1]. Genomické účinky se vyznačují pomalejším nástupem, jelikož spočívají v ovlivnění exprese konkrétních genů. Jmenovitě dochází například ke snížení zánětlivé odpovědi organismu inhibicí nukleárního faktoru kappa B (NF‑kB). Genomické účinky lze očekávat již při nižších dávkách kortikoidů. Oproti tomu negenomické účinky nastupují rychleji, jsou zprostředkovány přímým ovlivněním buněčných struktur a k jejich dosažení jsou potřebné vyšší dávky kortikoidů. Jedním z jejich účinků je např. inhibice degranulace neutrofilů. [1]. Efekt na mortalitu systémových kortikoidů v léčbě pacientů s těžkým průběhem onemocnění covid-19 prokázala studie RECOVERY, naopak u pacientů s lehkým průběhem benefit prokázán nebyl [2]. Na základě výsledků této studie následně Světová zdravotnická organizace (WHO) doporučila terapii systémovými kortikoidy u pacientů s těžkým průběhem (od zahájení oxygenoterapie) [3, 4]. Optimální strategie pro podávání kortikosteroidů je stále předmětem debat a probíhajících studií. Hledá se optimální účinná látka, forma podání i konkrétní dávkování [5, 6]. Tato dotazníková studie měla za cíl popsat aktuální praxi užití kortikosteroidů u pacientů s těžkým průběhem covidu-19 na jednotkách intenzivní péče v České republice. Znalost aktuálního postoje a praxe lékařů indikujících tuto léčbu je klíčová pro další optimalizaci léčby a tvorbu prakticky využitelných doporučených postupů.
Soubor a metody
Dotazník byl registrován na portálu Clinicaltrials.gov (NCT04648410) a následně zaslán v elektronické podobě (dostupné z: https://forms.gle/CW5RW1a4kha68YU96) členům České společnosti intenzivní medicíny (ČSIM), České společnosti anesteziologie, resuscitace a intenzivní medicíny (ČSARIM) a České pneumologické a ftizeologické společnosti (ČPFS). Sběr dat probíhal od 15. 2. 2021 do 31. 5. 2021. Dotazník obsahoval 15 otázek týkajících se demografických údajů respondenta a léčebných postupů, které volí při péči o kriticky nemocné pacienty s covidem-19. Prvních 14 otázek bylo uzavřených a polouzavřených. V poslední otevřené otázce se mohli respondenti k tématu volně vyjádřit. Text dotazníku je uveden v tabulce 1. Vyplnění dotazníku probíhalo anonymně. Data byla statisticky zpracována v součinnosti s Farmakologickým ústavem LF MU (projekt CZECRIN). Charakteristiky respondentů a volené léčebné postupy byly vyhodnoceny deskriptivně pomocí absolutního a relativního počtu uvedených odpovědí u každé otázky, případně jejich kombinace. Data získaná z dotazníkového šetření byla využita pro design celoevropského dotazníku na téma použití kortikosteroidů u kriticky nemocných pacientů s covidem-19, které autorský kolektiv zpracovává v součinnosti s European Society of Intensive Care Medicine (ESICM) a European Society of Anaesthesiology and Intensive Care (ESAIC). Dotazník určený pro členy ESICM a ESAC je registrován na portálu Clinicaltrials.gov pod identifikátorem NCT04866082 (ASAP‑‑ESICM/ESAIC Study).
Výsledky
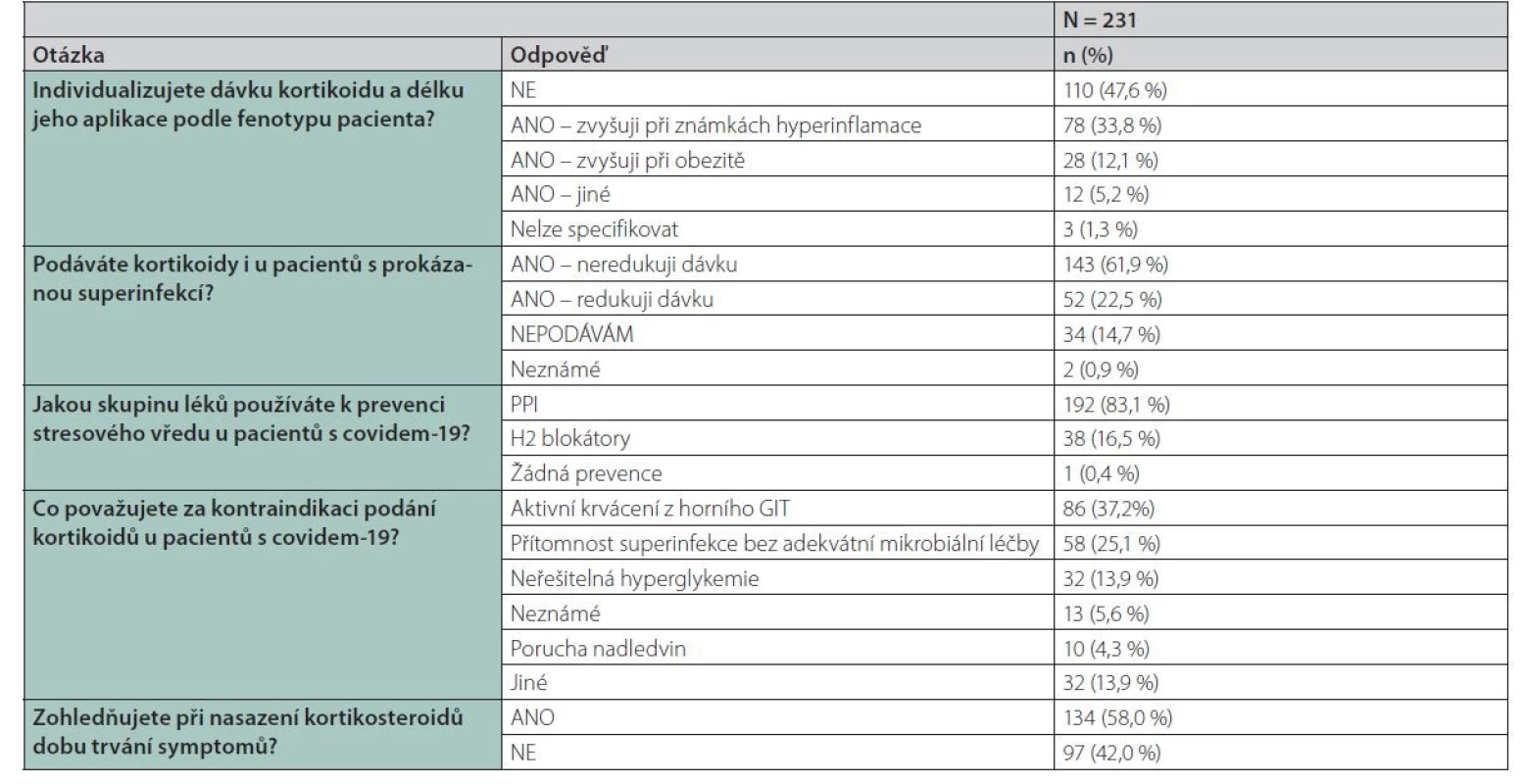
Z celkem 233 vyplněných dotazníků bylo následně statisticky vyhodnoceno 231 (2 dotazníky byly vyloučeny z důvodu absence péče o covid-19 pacienty). Dotazník byl rozeslán celkem 4 197 členům odborných společností (ČSIM – n = 711, ČSARIM – n = 2 762, ČFPS – n = 724), což představuje celkovou návratnost 5,55 %. Z hodnocených odpovědí nejvíce respondentů pracovalo na oddělení ARO/JIP (64,1 %, n = 148), následováno speciálně zřízenou covid-19 jednotkou (17,3 %, n = 40). Majorita respondentů měla ukončené specializační vzdělávání (81,4 %, n = 188), nejčastěji v oboru anesteziologie a intenzivní medicína (AIM) (51,9 %, n = 120) a pneumologie a ftizeologie (15,2 %, n = 35). Mezi respondenty byli nejvíce zastoupeni sekundární lékaři (58,0 %, n = 134) a vedoucí lékaři oddělení (24,7 %, n = 57) (viz tabulka č. 2). Kortikoidy v terapii pacientů s onemocněním covid-19 byly nejčastěji indikované (léčba iniciována) u pacientů vyžadujících oxygenoterapii (maskou nebo nosní kanylou) (59,3 %, n = 137) nebo u pacientů na vysokoprůtokové kyslíkové terapii (HFNC) (21,6 %, n = 50). Jenom minorita respondentů zahajovala kortikoidní terapii až u pacientů na umělé plicní ventilaci (9,5 %, n = 22) nebo na neinvazivní plicní ventilaci (NIV) (2,2 %, n = 5) nebo naopak již u pacientů ještě bez potřeby oxygenoterapie (7,4 %, n = 17) (obr. 1). Nejčastěji aplikovaným kortikoidem byl dexamethason (75,8 %, n = 175) v dávce 8 mg intravenózně (i. v.) (48,6 %, n = 85) nebo v dávce 6 mg i. v. (32,0 %, n = 56), následován metylprednisolonem (25,5 %, n = 59) v dávce 80 mg i. v. (35,6 %, n = 21), nebo v dávce 40 mg i. v. (13,6 %, n = 8) (obr. 2). Nejčastější délka terapie byla 10 dnů (dexamethason 60,6 %, n = 106, metylprednisolon 20,3 %, n = 12) (viz tabulka 3). Dávku kortikoidů individualizovalo celkem 118 respondentů (51,1 %), nejčastěji při známkách hyperinflamace (33,8 %, n = 78), při obezitě (12,1 % n = 28) nebo z jiného důvodu (5,2 %, n = 12). Naopak celkem 110 respondentů (47,6 %) používalo fixní schéma kortikoidů a neupravovali v individuálních případech dávku. U pacientů s prokázanou superinfekcí většina respondentů dávku kortikoidů neredukovala (61,9 %, n = 143). Redukovanou dávku aplikovalo celkem 52 respondentů (22,5 %) a 34 respondentů (14,7 %) kortikoidy vůbec neaplikovalo. Prevence stresového vředu byla indikovaná u naprosté majority respondentů (99,6 %, n = 230), nejčastěji byly podány inhibitory protonové pumpy (PPI) (83,1 %, n = 192) nebo blokátory H2 receptorů (16,5 %, n = 38). Nejčastější kontraindikací podání kortikoidů bylo aktivní krvácení z gastrointestinálního traktu (GIT) (37,2 %, n = 86), přítomnost superinfekce bez adekvátní antibiotické terapie (25,1 %, n = 58), neřešitelná hyperglykemie (13,9 %, n = 32), porucha funkce nadledvin (4,3 %, n = 10) nebo jiné příčiny (13,9 %, n = 32). Většina respondentů zohledňovala dobu trvání symptomů při nasazení kortikoidní terapie (58,0 %, n = 134) (viz tabulka 4).
Table 2. Charakteristika respondentů 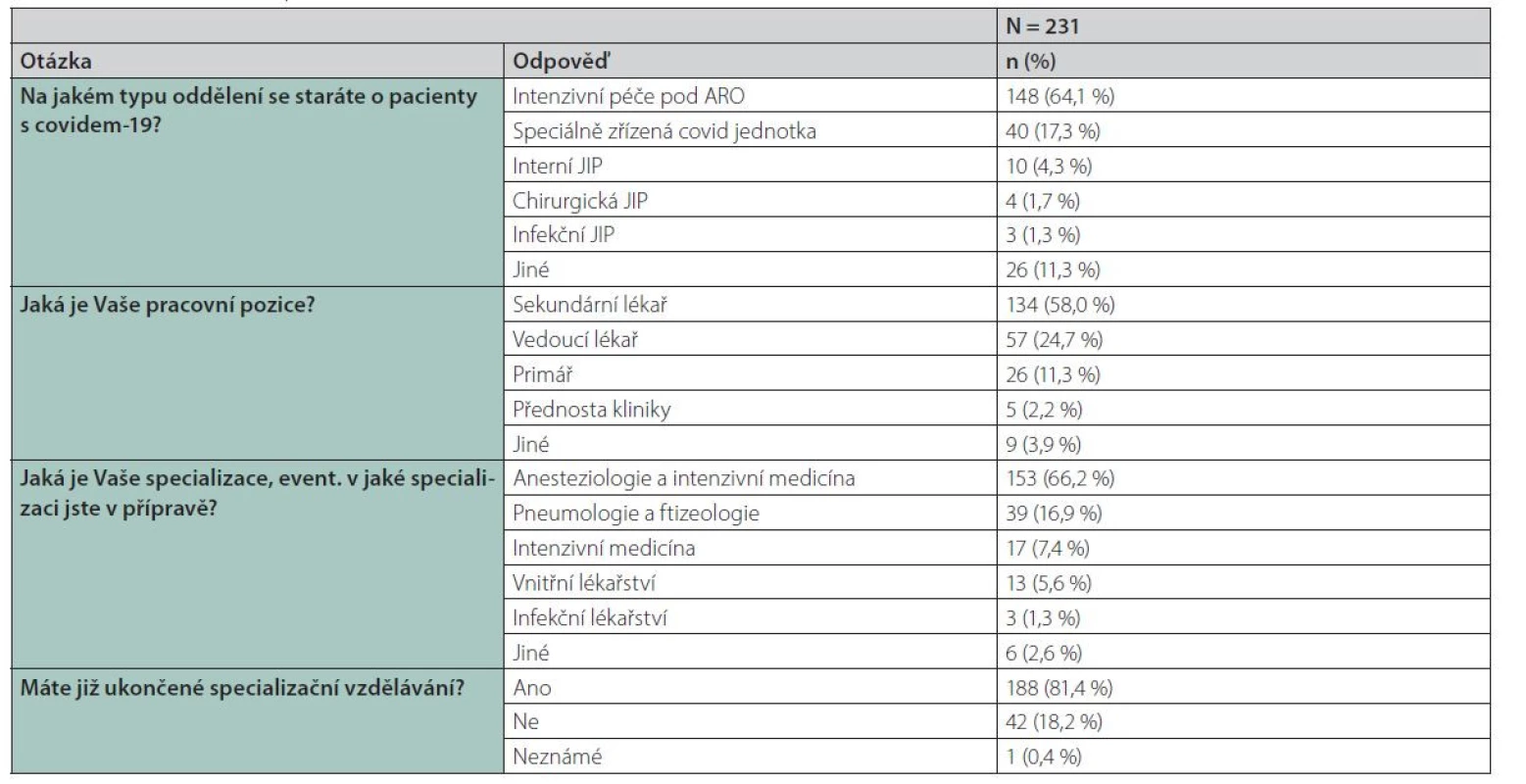
Table 3. Podávání a dávkování kortikoidů 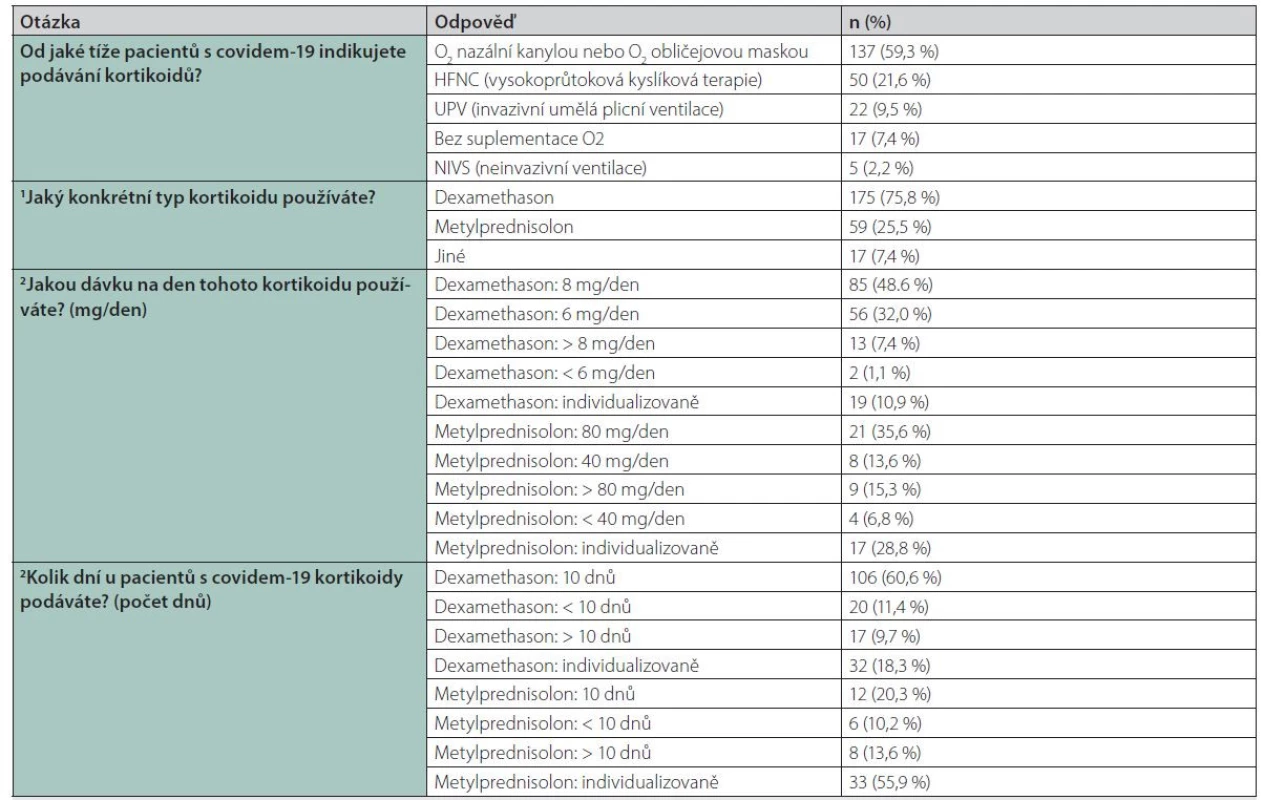
1Procenta jsou počítaná z počtu respondentů. Jeden respondent může označit více než jednu odpověď.
2Procenta jsou počítaná z počtu konkrétního typu kortikoidu.Image 1. Tíže pacientů indikující podávání kortikoidů 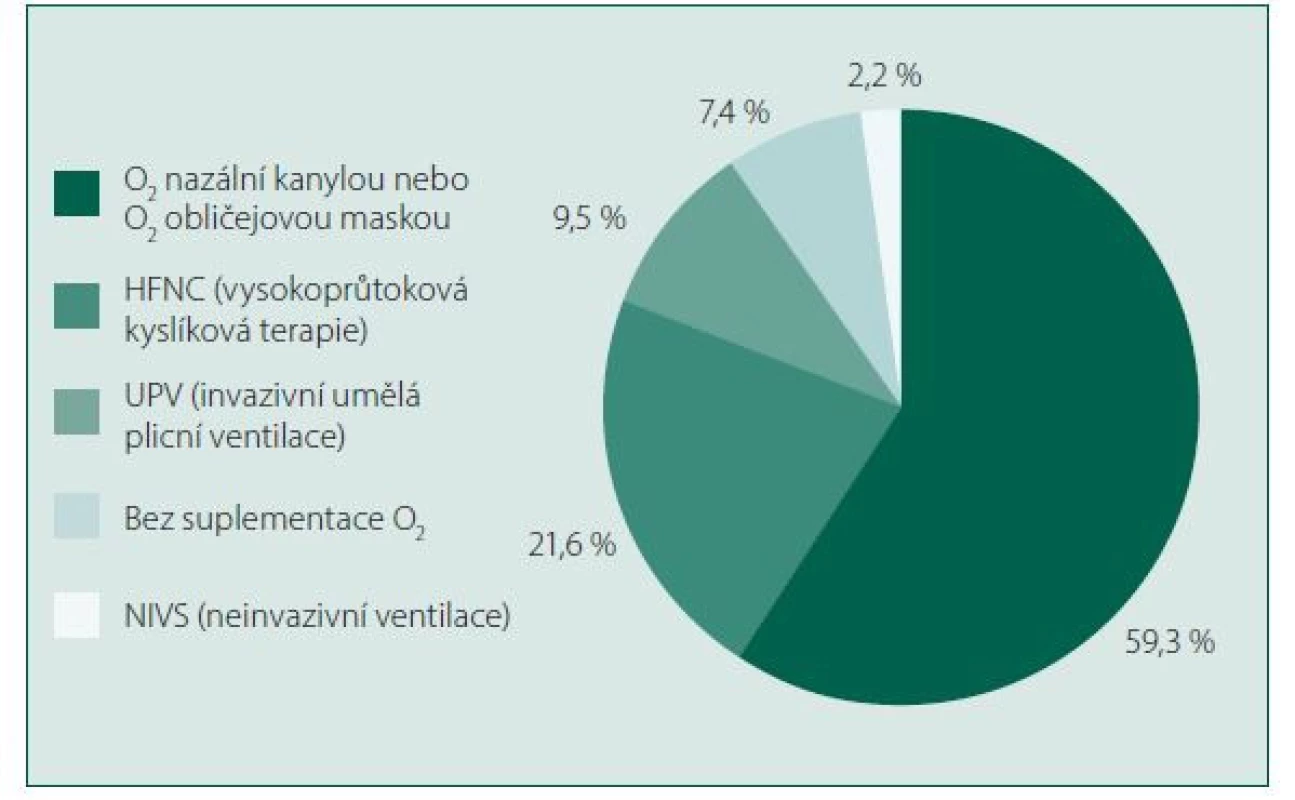
Image 2. Typ podávaných kortikoidů 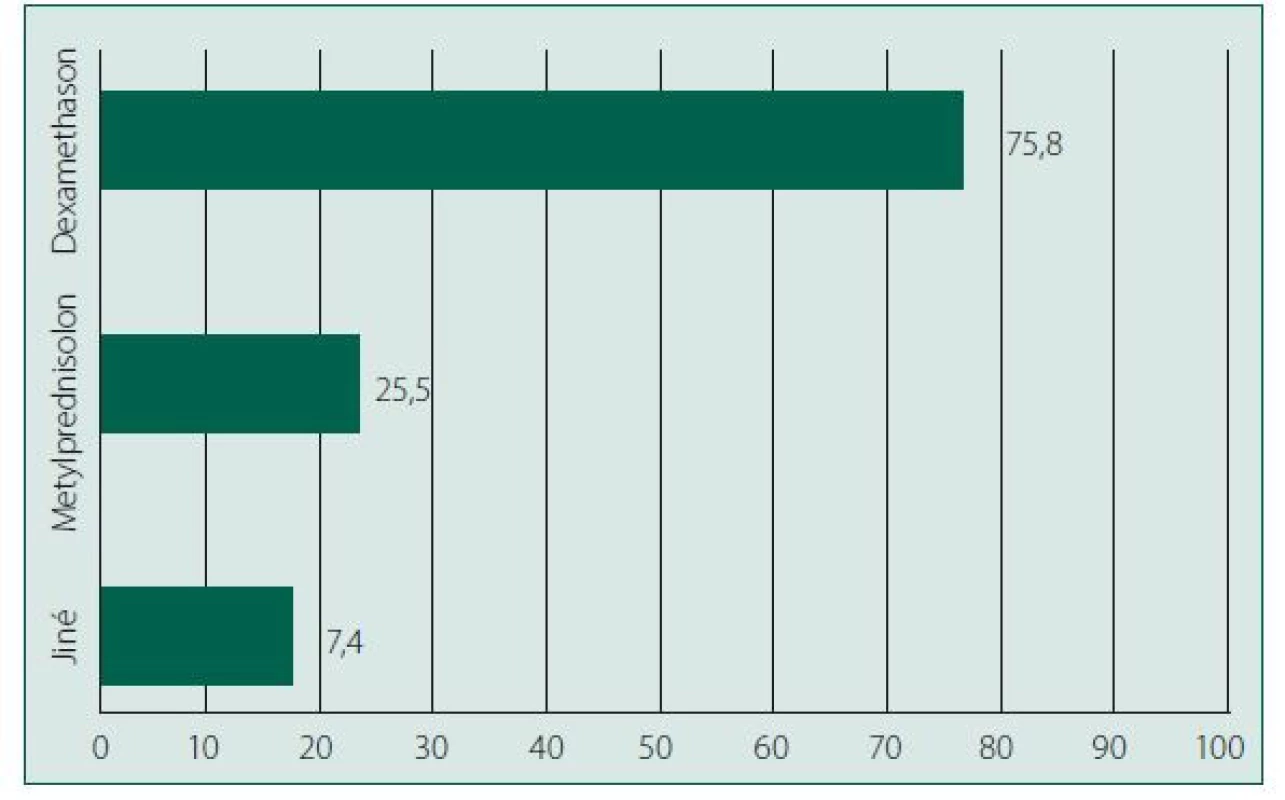
Diskuze
První oficiální případ potvrzeného pacienta s onemocněním covid-19 byl publikován v prosinci 2019 a následně byla 11. 3. 2020 WHO vyhlášená celosvětová pandemie covidu-19 [7]. Nový koronavirus SARS‑CoV-2 téměř okamžitě mobilizoval výzkumné týmy a odborné společnosti ve snaze unifikovat diagnosticko‑léčebný přístup k pacientům s covidem-19. SARS-CoV-2, stejně jako předchozí patogenní varianty koronavirů (Severe Acute Respiratory Synrome coronavirus 1-SARS‑CoV-1 a Middle East Respiratory Syndrome coronavirus MERS‑CoV), způsobuje infekci dýchacích cest až respirační selhání pod obrazem syndromu akutní respirační tísně (Acute Respiratory Distress Syndrome – ARDS) [8]. Pro pacienty s ARDS a respiračním selháním je aktuálně v intenzivní péči doporučena oxygenoterapie, event. vysokoprůtoková kyslíková terapie a v případě nutnosti umělé plicní ventilace tzv. protektivní ventilace (redukovaný dechový objem 4–6 ml/kg ideální tělesné hmotnosti, aplikace pozitivního end‑expiračního tlaku nad úroveň dolního inflexního bodu, permisivní hyperkapnie) ve snaze minimalizovat biotrauma způsobné nefyziologickou ventilací intermitentním přerušovaným přetlakem [9]. Jako rescue postupy při refrakterní hypoxemii je možno aplikovat pronační polohu [10, 11] a veno‑venózní extrakorporální membránovou oxygenaci (V ‑ V ECMO) [12]. Dané postupy jsou nicméně podpůrné metody používané k překlenutí kritického stavu respiračního selhání a neovlivňují samotný průběh nemoci. Na rozvoji ARDS se kromě iniciálního inzultu a samotného infekčního agens podílí významným způsobem obranná reakce imunitního systému, která může vést následně k rozvoji dekompenzované obranné reakce, pravděpodobně na podkladě rozdílného fenotypu konkrétního pacienta. Daná odpověď (ačkoliv iniciálně prospěšná) může být ve své pozdější fázi suprimována aplikací léků s imunomodulačním a imunosupresivním účinkem – typicky kortikoidy. Hlavní výhodou kortikoidů v období pandemie je jejich nízká cena a celosvětová dobrá dostupnost, což je činí potenciálně ideálním lékem. Doporučení pro aplikaci kortikoidů u těžkých případů covidu-19 bylo i přes relativní nedostatek důkazů publikováno jenom 17 dnů po vyhlášení celosvětové pandemie [13]. Benefit kortikoidní terapie byl následně potvrzen ve studii RECOVERY [2], která potvrdila benefit terapie kortikoidy (dexamethason 6 mg) u pacientů s těžkým průběhem covidu-19 (od nutnosti zahájení podávání oxygenoterapie).
Do našeho dotazníkového šetření (ASAP‑C) se zapojilo celkem 231 respondentů, z toho majorita s ukončeným specializačním vzděláváním, nejčastěji v oboru AIM nebo v oboru pneumologie a ftizeologie. Většina respondentů pracovala na pozici sekundární lékař (58 %, n = 134) nebo na pozici vedoucí lékař (24,7 %, n = 57). Majorita respondentů pracovala v době vyplnění dotazníku na oddělení/klinice ARO/JIP (64,1 %, n = 148) nebo na specializované covid-19 jednotce (17,3 %, n = 40). I přes relativně menší počet respondentů je možno považovat výsledky dotazníku za relevantní reflexi klinické praxe (přímá data z první linie od lékařů intenzivní péče pečující o pacienty s covidem-19). Na základě výsledků RECOVERY trial [2] je aktuálně indikovaná v případě absence závažných kontraindikací (kontraindikace je nicméně potřeba brát jako relativní) terapie kortikoidy (dexamethason 6 mg i. v. po dobu 10 dnů) u pacientů s těžkým průběhem covidu-19 (s nutností oxygenoterapie) [14]. Minorita respondentů indikovala kortikoidní terapii až u pacientů ve fázi napojení na umělou plicní ventilaci (9,5 %, n = 22) nebo na neinvazivní plicní ventilaci (NIV) (2,2 %, n = 5). Dané odpovědi můžou být nicméně ovlivněny příjmem těžkých případů na ARO/JIP přímo z domácí péče (tzn. absence postupného zhoršení klinického stavu s nutností oxygenoterapie). Z dostupných dat dle konceptu medicíny založené na důkazech (Evidence‑Based Medicine, EBM) je podání dexamethasonu 6 mg i. v. po dobu 10 dnů spojené se sníženou mortalitou i zkrácením pobytu v nemocnici v porovnání s placebem [2, 4]. Minorita respondentů indikovala kortikoidy také u pacientů bez potřeby oxygenoterapie (7,4 %, n = 17). Daný postup aktuálně není doporučen, nicméně může být indikován u pacientů s chronickým onemocněním typu astma bronchiale nebo chronickou obstrukční plicní nemocí (CHOPN) a zhoršujícím se klinickým stavem pacienta na podkladě infekce SARS‑CoV-2.
Nejčastěji aplikovaným kortikoidem byl dexamethason (75,8 %, n = 175) v dávce 8 mg i. v. (48,6 %, n = 85), nebo dávce 6 mg i. v. (32,0 %, n = 56). Dle výsledků RECOVERY trial je doporučeno dávkování dexamethasonu 6 mg/den intravenózně. Převažující aplikací dávky 8 mg je možno vysvětlit zjednodušením postupu při aplikaci, jelikož obsah jedné ampule je právě 8 mg. V situaci pandemie při péči o nadměrné množství pacientů mohlo takové zjednodušení vést k úspoře času. Druhým důvodem mohla být obava o riziko „poddávkování“ kortikoidů v terapii ARDS (např. při srovnání s tzv. Meduriho schématem pro unresovling ARDS – 1 mg/kg a den metylprednisolonu, nebo studie s pacienty s non‑COVID-19 ARDS používající 15 mg dexamethasonu) [6, 15]. Druhým nejčastěji používaným kortikosteroidem byl právě metylprednisolon (25,5 %, n = 59), a to v dávce 80 mg i. v. (35,6 %, n = 21), nebo dávce 40 mg i. v. (13,6 %, n = 8). Preferenci metylprednisolonu před dexamethasonem je možno vysvětlit právě klinickými zkušenostmi lékařů v indikaci unresolving ARDS a problematickou celosvětovou dostupností dexamethasonu v době sběru dat (celosvětová poptávka po dexamethasonu z důvodu pandemie covidu-19 přechodně významně zhoršila jeho dostupnost až do stavu přechodného totálního výpadku dodávky) [16]. Při srovnání jednotlivých druhů kortikoidů se majorita kvalitních a dostupných dat týká právě dexamethasonu [4], ačkoliv pozitivní vliv na výsledky léčby (nutnost a délku umělé plicní ventilace) byl pozorován při kortikoidní terapii per se (OR 0,72 (95%IS 0,57–0,87)) [5]. Denní dávka 6 mg dexamethasonu i. v. nekoresponduje s ekvivalentním dávkováním metylpredinisolonu (80 mg metylprednisolonu = 1 mg/kg pro 80 kg pacienta představuje ekvivalent 15 mg dexamethasonu), což vedlo řadu lékařů a autorů k myšlence možného vyššího dávkování a potenciální dalšího zlepšení outcome (např. studie REMED srovnávající terapii dexamethason 6 mg vs. 20 mg po dobu 5 dní, následovanou dávkou 10 mg po dalších 5 dní) [17]. Již nyní jsou k dispozici výsledky studie COVID STEROID 2, která porovnávala podávání dexamethasonu 12 mg vs. 6 mg i. v. u pacientů s covidem-19 ARDS od stádia nutnosti podávání oxygenoterapie. Výsledky nedosáhly statistické signifikance, nicméně ve skupině vyšší dávky byl trend ke zlepšení kompozitního primárního cíle studie, tedy počet dnů přežití bez orgánové podpory (invazivní ventilace, oběhová podpora a renální eliminační techniky) v průběhu 28 dnů [18]. Následná plánovaná sekundární bayesianská analýza výše uvedené studie COVID STEROID 2 ale signifikantně prokázala zlepšení kompozitního primárního cíle studie u skupiny pacientů s 12 mg dexamethasonu i. v. [19]. Skupina složená z investigátorů prospektivních studií zkoumajících rozdílné dávky dexamethasonu plánuje prospektivní metaanalýzu s předem publikovaným protokolem [20]. Pro silné doporučení stran velikosti dávky kortikoidů čekáme tedy na další výsledky [21].
Aplikovaná délka terapie dle respondentů byla nejčastěji 10 dnů (dexamethason 60,6 %, n = 106, metylprednisolon 20,3 %, n = 12), z toho dávku kortikoidů individualizovalo více jak polovina respondentů (51 %), nejčastěji při známkách hyperinflamace (33,8 %, n = 78), při obezitě (12,1 %, n = 28) nebo z jiného důvodu (5,2 %, n = 12). I když individualizace dávky není aktuálně podpořena robustními daty ve smyslu EBM, lze předpokládat, že určité skupiny pacientů z modifikované terapie kortikoidy profitují. Zde je k diskuzi jaké parametry k individualizované terapii používat, jedním z možných by mohl být C ‑ reaktivní protein (CRP) [22]. Téměř 100 % respondentů indikovalo u dané kohorty pacientů (covid-19 s kortikoidní terapií) farmakologickou prevenci stresového vředu (99,6 %, n = 230), a to nejčastěji inhibitory protonové pumpy (PPI) (83,1 %, n = 192). Kritické onemocnění ve spojitosti s kortikoidní terapií jsou rizikové faktory vzniku stresové eroze/ulcerace [23]. Nejčastější kontraindikací podání kortikoidů bylo aktivní krvácení z gastrointestinálního traktu (GIT) (37,2 %, n = 86), přítomnost superinfekce bez adekvátní antibiotické terapie (25,1%, n = 58), neřešitelná hyperglykemie (13,9 %, n = 32), porucha nadledvin (4,3 %, n = 10), nebo jiné příčiny (13,9 %, n = 32). Všechny uvedené stavy významně zvyšují riziko nežádoucích účinků kortikoidní terapie, nicméně je na ně potřeba nahlížet individuálně (case‑case přístupem) a zvažovat riziko vs. benefit nasazení kortikoidní terapie u dané skupiny pacientů (zlepšení plicního nálezu vs. zvýšení rizika komplikací kortikoidní terapie).
Přes některé odchylky (dávka dexamethasonu 8 mg i. v. nebo použití metylprednisolonu) prokazují výsledky dotazníkového šetření (studie ASAP‑C) vysokou míru adherence intenzivní péče o covid-19 pacienty s těžkým průběhem v České republice s aktuálně platným doporučením týkajícím se kortikoidní terapie u této skupiny pacientů.
Jako možnou limitaci výsledků lze brát počet respondentů (231 validních odpovědí). Vzhledem k vysoké incidenci sdíleného členství ČSIM a ČSARIM, event. ČPFS nelze přesně stanovit návratnost našeho dotazníku, nicméně toto sdílené členství se pravděpodobně týká méně než 20 % oslovených. Dle mínění autorů, a s ohledem na demografické zastoupení, výsledky reprezentují data z první linie péče o pacienty s covidem-19, a mají tím pádem vysokou reprezentativnost.
Závěr
Kortikoidní terapie byla nejčastěji zahajovaná u pacientů s covidem-19 vyžadujících oxygenoterapii. Nejčastěji aplikovaným lékem byl dexamethason 8 mg i. v. a 6 mg i. v. po dobu 10 dnů, což koresponduje s aktuálně platným doporučením pro terapii covid-19 s těžkým průběhem onemocnění.
PROHLÁŠENÍ AUTORŮ: Prohlášení o původnosti: Práce je původní a nebyla publikována ani není zaslána k recenznímu řízení do jiného média. Střet zájmů: Jan Maláska je národní koordinátor, Jan Stašek a František Duška jsou hlavní investigátoři klinického hodnocení REMED porovnávající dvě různé dávky dexamethasonu u pacientů s ARDS a COVID-19 (EudraCT No.:2020-005887-70 and ClinicalTrials.gov (Title: Effect of Two Different Doses of Dexamethasone in Patients With ARDS and COVID-19 (REMED) Identifier: NCT04663555). Podíl autorů: Všichni autoři rukopis četli, souhlasí s jeho zněním a zasláním do redakce časopisu Anesteziologie a intenzivní medicína, JM, JS, JK – koncept projektu a publikace, finální analýza dat, psaní manuskriptu, finální editorství, FK – rešeršní činnost, psaní manuskriptu, DCh – zpracování dat, JH, PK, MK, FD, JM, KB, PŠ – spolupodíl na analýze dat, finální editorství. RŠ, AS provedli deskriptivní analýzu, statistické zpracování a psaní manuskriptu. Financování: Supported by the national budget through MEYS, RI CZECRIN (LM2018128) and from ERDF Project CZECRIN_4 PATIENTS (CZ.02. 1. 01/0.0/0.0/16_013/0001826) and by MH CZ – DRO (FNBr, 65269705). Poděkování: Autoři by chtěli poděkovat vedení a všem členům České společnosti anesteziologie, resuscitace a intenzivní medicíny (ČSARIM), České společnosti Intenzivní medicíny (ČSIM), České pneumologické a ftizeologické společnosti (ČPFS) a všem respondentům. Registrace: Clinicaltrials.gov (NCT04648410) Projednání etickou komisí: N/A.
KORESPONDENČNÍ ADRESA AUTORA:
doc. MUDr. Jozef Klučka, Ph.D.
Článek přijat redakcí: 23. 12. 2021; Článek přijat k tisku: 21. 2. 2022
Cit. zkr: Anest intenziv Med. 2022;33(1):7-13
Sources
1. Meduri GU, Annane D, Confalonieri M, Chrousos GP, Rochwerg B, Busby A, et al. Pharmacological principles guiding prolonged glucocorticoid treatment in ARDS. Intensive Care Med. 2020 Dec;46(12):2284-2296. doi: 10.1007/s00134-020-06289-8. Epub 2020 Nov 4. PMID: 33150472; PMCID: PMC7641258.
2. Horby P, Lim WS, Emberson JR, Mafham M, Bell JL, Linsell Let al. Dexamethasone in Hospitalized Patients with Covid-19. N Engl J Med. 2021 Feb 25;384(8):693-704. doi: 10.1056/NEJMoa2021436. Epub 2020 Jul 17. PMID: 32678530; PMCID: PMC7383595.
3. World Health Organization. (2020). Corticosteroids for COVID-19: living guidance, 2 September 20WorldHealth Organization. https://apps.who.int/iris/handle/10665/334125. License: CC BY‑NC‑SA 3.0 IGO
4. Sterne JAC, Murthy S, Diaz JV, Slutsky AS, Villar J, Angus DC, et al. Association Between Administration of Systemic Corticosteroids and Mortality Among Critically Ill Patients With COVID-19: A Meta‑analysis. JAMA. 2020 Oct 6;324(13):1330-1341. doi: 10.1001/jama.2020.17023. PMID: 32876694; PMCID: PMC7489434.
5. van Paassen J, Vos JS, Hoekstra EM, Neumann KMI, Boot PC, Arbous SM. Corticosteroid use in COVID-19 patients: a systematic review and meta‑‑analysis on clinical outcomes. Crit Care. 2020 Dec 14;24(1):696. doi: 10.1186/s13054-020-03400-9. PMID: 33317589; PMCID: PMC7735177.
6. Villar J, Ferrando C, Martínez D, Ambrós A, Muñoz T, Soler JA, et al.; dexamethasone in ARDS network. Dexamethasone treatment for the acute respiratory distress syndrome: a multicentre, randomised controlled trial. Lancet Respir Med. 2020 Mar;8(3):267-276. doi: 10.1016/S2213-2600(19)30417-5. Epub 2020 Feb 7. PMID: 32043986.
7. Habas K, Nganwuchu C, Shahzad F, Gopalan R, Haque M, Rahman S, et al. Resolution of coronavirus disease 2019 (COVID-19). Expert Rev Anti Infect Ther. 2020 Dec;18(12):1201-1211. doi: 10.1080/14787210.2020.1797487. Epub 2020 Aug 4. PMID: 32749914.
8. Torres Acosta MA, Singer BD. Pathogenesis of COVID-19-induced ARDS: implications for an ageing population. Eur Respir J. 2020 Sep 24;56(3):2002049. doi: 10.1183/13993003.02049-2020. PMID: 32747391; PMCID: PMC7397945.
9. Griffiths MJD, McAuley DF, Perkins GD, Barrett N, Blackwood B, Boyle A, et al. Guidelines on the management of acute respiratory distress syndrome. BMJ Open Respir Res. 2019 May 24;6(1):e000420. doi: 10.1136/bmjresp-2019-000420. PMID: 31258917; PMCID: PMC6561387.
10. Gattinoni L, Carlesso E, Taccone P, Polli F, Guérin C, Mancebo J. Prone positioning improves survival in severe ARDS: a pathophysiologic review and individual patient meta‑analysis. Minerva Anestesiol. 2010 Jun;76(6):448-54. PMID: 20473258.
11. Sud S, Friedrich JO, Adhikari NK, Taccone P, Mancebo J, Polli F, et al. Effect of prone positioning during mechanical ventilation on mortality among patients with acute respiratory distress syndrome: a systematic review and meta‑‑analysis. CMAJ. 2014 Jul 8;186(10):E381-90. doi: 10.1503/cmaj.140081. Epub 2014 May 26. PMID: 24863923; PMCID: PMC4081236.
12. Tillmann BW, Klingel ML, Iansavichene AE, Ball IM, Nagpal AD. Extracorporeal membrane oxygenation (ECMO) as a treatment strategy for severe acute respiratory distress syndrome (ARDS) in the low tidal volume era: A systematic review. J Crit Care. 2017 Oct;41 : 64-71. doi: 10.1016/j.jcrc.2017. 04. 041. Epub 2017 Apr 27. PMID: 28499130.
13. Alhazzani W, Møller MH, Arabi YM, Loeb M, Gong MN, Fan E, et al. Surviving Sepsis Campaign: guidelines on the management of critically ill adults with Coronavirus Disease 2019 (COVID-19). Intensive Care Med. 2020 May;46(5):854-887. doi: 10.1007/s00134-020-06022-5. Epub 2020 Mar 28. PMID: 32222812; PMCID: PMC7101866.
14. Alhazzani W, Evans L, Alshamsi F, Møller MH, Ostermann M, Prescott HC, et al. Surviving Sepsis Campaign Guidelines on the Management of Adults With Coronavirus Disease 2019 (COVID-19) in the ICU: First Update. Crit Care Med. 2021 Mar 1;49(3):e219-e234. doi: 10.1097/CCM.0000000000004899. PMID: 33555780.
15. Meduri GU, Golden E, Freire AX, Taylor E, Zaman M, Carson SJ, et al. Methylprednisolone infusion in early severe ARDS: results of a randomized controlled trial. Chest. 2007 Apr;131(4):954-963. doi: 10.1378/chest.06-2100. PMID: 17426195.
16. Silverman E. Hospitals see shortages of a cheap steroid that one study says helps Covid-19 patients. STAT [online]. 25 Jun 20 [cit. 5 Dec 21]. Dostupné z: https://www.statnews.com/pharmalot/2020/06/25/covid19-coronavirus ‑ dexamethasone ‑ shortages/.
17. Maláska J, Stašek J, Duška F, Balík M, Máca J, Hruda J, et al.; REMED Study Group. Effect of dexamethasone in patients with ARDS and COVID-19 – prospective, multi‑centre, open‑label, parallel‑group, randomised controlled trial (REMED trial): A structured summary of a study protocol for a randomised controlled trial. Trials. 2021 Mar 1;22(1):172. doi: 10.1186/s13063-021-05116-9. PMID: 33648568; PMCID: PMC7917377.
18. Munch MW, Myatra SN, Vijayaraghavan BKT, Saseedharan S, Benfield T, Wahlin RR, et al. Effect of 12 mg vs 6 mg of Dexamethasone on the Number of Days Alive Without Life Support in Adults With COVID-19 and Severe Hypoxemia: The COVID STEROID 2 Randomized Trial. JAMA. 2021 Nov 9;326(18):1807-1817. doi: 10.1001/jama.2021.18295. PMID: 34673895; PMCID: PMC8532039.
19. Granholm A, Munch MW, Myatra SN, Vijayaraghavan BKT, Cronhjort M, Wahlin RR, et al. Dexamethasone 12 mg versus 6 mg for patients with COVID-19 and severe hypoxaemia: a pre‑planned, secondary Bayesian analysis of the COVID STEROID 2 trial. Intensive Care Med. 2021 Nov 10 : 1–11. doi: 10.1007/s00134-021-06573-1. Epub ahead of print. PMID: 34757439; PMCID: PMC8579417.
20. Granholm A. Higher vs. standard doses of dexamethasone in patients with COVID‑19 and hypoxia: a prospective meta‑analysis. OSF Registries. 31 May 2021. https://doi.org/10.17605/OSF.IO/FR5SV.
21. Webb SA, Higgins AM, McArthur CJ. Glucocorticoid Dose in COVID-19: Lessons for Clinical Trials During a Pandemic. JAMA. 2021 Nov 9;326(18):1801-1802. doi: 10.1001/jama.2021.16438. PMID: 34673891.
22. Smilowitz NR, Kunichoff D, Garshick M, Shah B, Pillinger M, Hochman JS, etl al. C‑reactive protein and clinical outcomes in patients with COVID-19. Eur Heart J. 2021 Jun 14;42(23):2270-2279. doi: 10.1093/eurheartj/ehaa1103. PMID: 33448289; PMCID: PMC7928982.
23. Butler E, Møller MH, Cook O, Granholm A, Penketh J, Rygård SL, et al. The effect of systemic corticosteroids on the incidence of gastrointestinal bleeding in critically ill adults: a systematic review with meta‑analysis. Intensive Care Med. 2019 Nov;45(11):1540-1549. doi: 10.1007/s00134-019-05754-3. Epub 2019 Sep 9. PMID: 31501997.
Labels
Anaesthesiology, Resuscitation and Inten Intensive Care Medicine
Article was published inAnaesthesiology and Intensive Care Medicine

2022 Issue 1-
All articles in this issue
- ČSARIM v roce 2022 – krátké ohlédnutí zpět a pohled dopředu
- Česká intenzivní medicína – výhledy do budoucnosti
- Praxe podávání systémových kortikosteroidů kriticky nemocným pacientům s covidem-19 v České republice – dotazníkový průzkum (studie ASAP‑ C)
- Základní autorskoprávní aspekty v kontextu lékařských publikací
- Nové supraglotické pomůcky v klinické praxi
- Principy systémové bezopioidní anestezie a pooperační analgezie, naše zkušenosti u bariatrických chirurgických výkonů
- Heparinem indukovaná trombocytopenie v perioperačním období
- Význam střevní mikrobioty u kriticky nemocných pacientů a možnosti jejího ovlivnění
- Perioperační neurokognitivní porucha – advanced narrative review
- Anesteziologické možnosti ovlivnění přehlednosti operačního pole při endonazální chirurgii
- Tracheální intubace při vědomí u dospělých za použití různých optických technik – přehledný článek a metaanalýza
- Deficit butyrylcholinesterázy aneb „Pamatuji si na intubaci“
- Botulotoxin A pro bederní sympatickou blokádu při syndromu regionální chronické bolesti
- Kombinace „hypertonický roztok NaCl a furosemid“ v léčbě srdečního selhání – 20 let od konceptu k účinné (ale stále možná opomíjené) klinické intervenci
- Předoperační POCT ultrazvuk významně zpřesňuje zhodnocení křehkosti a pooperační perspektívy
- K článku: Prevence venózní tromboembolie u pacientů v intenzivní péči
- Funkční kvalita života po zresuscitované nitronemocniční srdeční zástavě
- Odpověď autorů K článku: Prevence venózní tromboembolie u pacientů v intenzivní péči
- Doporučení Evropské kardiologické společnosti (ESC) pro diagnostiku a léčbu akutního a chronického srdečního selhání z roku 2021
- Desatero přikázání pro léčbu srdečního selhání podle ESC 2021
- Anaesthesiology and Intensive Care Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Principy systémové bezopioidní anestezie a pooperační analgezie, naše zkušenosti u bariatrických chirurgických výkonů
- Deficit butyrylcholinesterázy aneb „Pamatuji si na intubaci“
- Nové supraglotické pomůcky v klinické praxi
- Význam střevní mikrobioty u kriticky nemocných pacientů a možnosti jejího ovlivnění
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career