-
Medical journals
- Career
Léčba invazivní kandidózy – doporučení odborných společností*
: Haber Jan 1; Ráčil Zdenek 2; Mayer Jiří 2; Mallátová Naďa 3; Kouba Michal 4; Sedláček Petr 5; Faber Edgar 6; Herold Ivan 7; Múdry Peter 8; Drgoňa Luboš 9; Kocmanová Iva 10; Karas Michal 11; Buchta Vladimír 12; Vydra Jan 13; Kolář Michal 14; Trupl Jan 15; Marešová Vilma 16; Rozsypal Hanuš 16; Nyč Otakar 17; Cwiertka Karel 18
: I. interní klinika – klinika hematologie VFN, Praha 1; Interní hematoonkologická klinika FN Brno 2; Laboratoř lékařské parazitologie a mykologie, Centrální laboratoře, Nemocnice České Budějovice, a. s. 3; Ústav hematologie a krevní transfuze Praha 4; Klinika dětské hematologie a onkologie FN Motol, Praha 5; Hematoonkologická klinika FN Olomouc 6; ARO, Klaudiánova nemocnice Mladá Boleslav 7; Klinika dětské onkologie, FN Brno 8; Národný onkologický ústav, Bratislava, Slovensko 9; Oddělení klinické mikrobiologie FN Brno 10; Hematologicko-onkologické oddělení FN Plzeň 11; Ústav klinické mikrobiologie FN Hradec Králové 12; Oddělení klinické hematologie FNKV, Praha 13; KAR VFN, Praha 14; Klinika laboratorní medicíny SYNLAB, s. r. o., Bratislava, Slovensko 15; Infekční klinika FN Na Bulovce, Praha 16; Ústav lékařské mikrobiologie FN Motol, Praha 17; Onkologická klinika FN Olomouc 18
: Anest. intenziv. Med., 20, 2009, č. 1, s. 37-47
: The recommendations of professional societies
Předkládaný text shrnuje současné poznatky o léčbě invazivní kandidózy a kandidémie. Shrnuje výsledky klinických studií a na základě jejich zhodnocení formuluje doporučené postupy. Zahrnuje dospělé hematologické pacienty a nemocné na jednotkách intenzivní péče. Při hodnocení kvality studí byla použita celosvětově uznávaná kritéria IDSA (Infectious Diseases Society of America) a pro definice invazivní mykotické infekce aktualizované konsenzuální závěry skupiny EORTC/MSG. Současné doporučené postupy jsou rozšířenou a aktualizovano verzí těch, které byly publikovány v letech 2003–2004.
Práce je výsledkem týmu odborníků z oblasti hematologie, onkologie, infekce, intenzivní medicíny a mikrobiologie, kteří reprezentovali příslušné odborné společnosti a pracovní skupiny.Klíčová slova:
invazivní kadidóza – kandidémie – léčba – doporučené postupy1 Vývoj epidemiologie kandidózy
2 Změna spektra kandid – ovlivnění léčebných postupů
3 Léčba hematogenní kandidové infekce (kandidémie) a invazivního kandidového onemocnění (akutní diseminované kandidózy)
3. 1 Nefarmakologická léčba kandidémie – odstranění centrálního nitrožilního katétru
3. 1. 1 Diagnostika katétrové kandidémie
3. 2. Farmakologická léčba hematogenní kandidózy (kandidémie) a invazivního kandidového onemocnění (akutní diseminované kandidózy)
3. 2. 1 Amfotericiny
3. 2. 2 Amfotericiny na tukovém nosiči
3. 2. 3 Triazoly
3. 2. 4 Echinokandiny
3. 3 Délka léčby invazivní kandidózy a kandidémie
3. 4 Význam kultivačních vyšetření a stanovení citlivosti (MIC) na antimykotika
4 Doporučení a závěr
4. 1 Postup při časné léčbě hematogenní infekce před určením druhu kandidy
4. 2 Postup při časné léčbě hematogenní kandidové infekce způsobené Candida albicans, C. glabrata nebo C. krusei
4. 3 Obvyklé dávkování antimykotik
5 Závěr
6 Literatura
1 Vývoj epidemiologie kandidózy
Invazivní kandidová infekce je stále nejčastější oportunní mykotickou infekcí a negativně ovlivňuje morbiditu i mortalitu v hematoonkologických centrech a na jednotkách intenzivní péče (JIP) [1]. Vzestupný trend incidence kandidémie a invazivní kandidózy začal v 80. letech 20. století a incidence dosahovala až 8 % [2–6]. Od 90. let 20. století, po širokém zavedení flukonazolu do profylaxe, incidence kandidémie v hematologických a transplantačních centrech (tj. u neutropenických nemocných) postupně poklesla [7–14]. Na JIP (tj. převážně u non-neutropenických nemocných) se naopak kandidóza stává závažným problémem [15] s neměnnou nebo stoupající incidencí [5, 6, 16, 17]. Výskyt kandidémie se liší podle charakteru jednotky [18] a v současné době jsou kandidy na JIP čtvrtou nejčastější hematogenní infekcí s nejvyšší mortalitou [19]. Incidence kandidémie v Evropě se pohybuje se mezi 2,2–4,3/100 000 obyvatel [20–22], s nejvyšším výskytem ve velkých univerzitních nemocnicích [23–25]. U novorozenců se udává incidence až 32,6/100 000 narozených dětí [26]. V ČR nejsou globální epidemiologická data k dispozici.
S poklesem celkové incidence kandidózy klesá od počátku 90. let také celková mortalita na kandidózu [27–29]. V souvislosti se zlepšující se komplexní péčí, zejména o pacienty s hematologickými malignitami a po transplantaci kostní dřeně, je pokles mortality na kandidózu nejvíce patrný u této skupiny nemocných [30]. Tomu odpovídá i pokles kandid v sekčním materiálu [13, 31]. Přes celkový pokles mortality se však úmrtí na rozvinutou infekci zásadně ovlivnit nepodařilo a i přes nové léčebné postupy mortalita na kandidózu dosahuje stále 40–50 % (dříve až 60 %) [11, 22, 32], a to jak na hematologických pracovištích, tak na jednotkách intenzivní péče [19]. Souhrnný přehled o vývoji mortality na kandidózu recentně prezentoval Pfaller [33]. Konstatuje, že za posledních 20 let je mortalita na invazivní kandidózu prakticky neměnná, kolem 0,4/100 000 obyvatel.
2 Změna spektra kandid – ovlivnění léčebných postupů
V posledních dvou desetiletích dochází ke změně i v zastoupení jednotlivých druhů kandid izolovaných z hemokultur. Při absolutním poklesu C. albicans na cca 50 % významně stoupá relativní zastoupení non-albicans kandid [4, 12, 13, 16–18, 32, 34-38]. A to jak u neutropenických nemocných s hematologickými malignitami, či po transplantaci kostní dřeně [12, 30], kde bývají častěji infekce způsobené současně více druhy kandid [39], tak non-neutropenických nemocných na JIP [16, 17, 40, 41]. Údaje z rozsáhlých prospektivních observačních epidemiologických studií v USA (u dospělých i dětí) [16] a z Evropy [42] jsou uvedeny v tabulce 1, stejně tak i údaje o nejčastějších kmenech kandid v České a Slovenské republice [43–47].
1. Zastoupení jednotlivých kmenů kandid v hemokultuře – údaje z Evropy, USA (děti i dospělí), situace v České a Slovenské republice 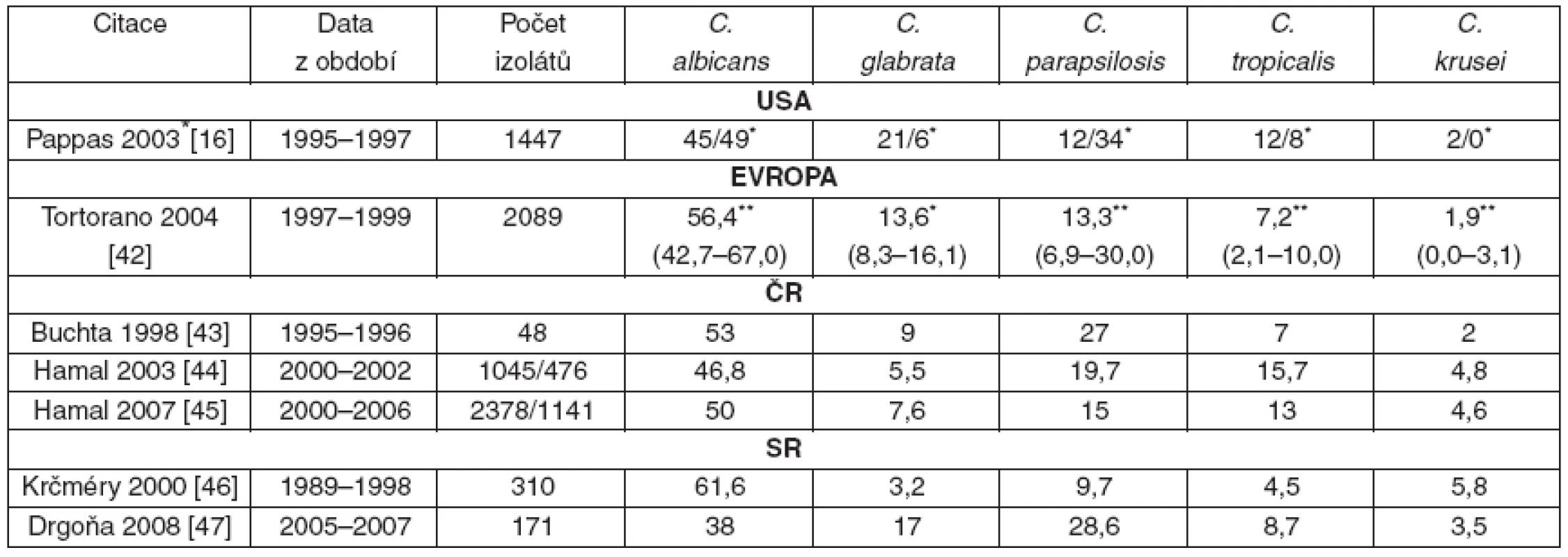
*dospělí/děti; **evropská studie, v závorce rozpětí výskytu 3 Léčba hematogenní kandidové infekce (kandidémie) a invazivního kandidového onemocnění (akutní diseminované kandidózy)
3. 1 Nefarmakologická léčba kandidémie – odstranění centrálního nitrožilního katétru
Odstranění centrálního žilního katétru je prvotní součástí léčby kandidémie. Jde o zásadní režimové opatření a při podezření na katétrový zdroj kandidémie je časné (do 48 hodin) odstranění katétru, kdykoli je to možné, absolutně indikováno [48–56]. Stejný postup platí i u dětí [57] a novorozenců [58]. I když v této oblasti neexistují randomizované srovnávací studie, zhodnocení dosavadních studií [59], doporučení [56, 60–62] a názory expertů [51, 56] opřené o řadu prací tento postup zásadně doporučují. Mortalita nemocných, dospělých, dětí i novorozenců, kterým při hematogenní kandidové infekci byl ponechán katétr in situ, byla statisticky významně vyšší i přes adekvátní antimykotickou léčbu [57, 58, 63–65]. Okamžité vynětí katétru při kandidémii vedlo naopak ke snížení mortality [22, 26, 66, 67].
Původ kandidémie je prakticky vždy endogenní, primárním zdrojem je převážně trávicí trakt [68], jen výjimečně je zdroj exogenní – z kůže, a to zpravidla při nesprávném ošetření katétru. U neutropenických nemocných je však v některých případech obtížné stanovit, zda primárním zdrojem kandidémie je skutečně GIT, nebo je zdrojem kandidémie katétr [69]. Některé zkušenosti uvádějí jako primární zdroj GIT v 60 % a katétr ve 27 % [70], jiné udávají katétrový zdroj nižší – 17% [57, 71]. Bez ohledu na to však stále platí základní imperativ vynětí katétru. Určité váhání může nastat v případě, že instalace nového katétru by byla velkým rizikem, např. při hluboké trombocytopenii. Při průkazu C. parapsilosis, která bývá jako původce katétrové kandidémie izolována nejčastěji, však platí zásadní doporučení okamžité odstranění katétru [7, 72].
3. 1. 1 Diagnostika katétrové kandidémie
Diagnóza katétrové kandidémie je založena na (semikvantitativním) průkazu téhož patogenu z odběru krve z katétru a současně z periferní žíly [73], s vyšším kvantitativním nálezem kandid v katétru proti periferní krvi v poměru více než 5 : 1 [74]. K rozpoznání napomůže časový rozdíl kultivační pozitivity hemokultury z katétru a z periferní žíly, kdy při katétrové infekci se kultivační pozitivita vzorku získaného z katétru objeví o hodiny (nejméně o dvě) dříve než ze vzorku krve získaného z periferní žíly [69, 74, 75] . Tento postup má v určení katétrového původu kandidémie 100% specificitu a 96,4% senzitivitu; praktické využití však může mít význam jen při nemožnosti okamžitého odstranění katétru. Možnosti diagnostiky s katétrem ponechaným in situ uvádějí některé dřívější práce [76]. Souhrnný přehled aktuálně uvádí Bouza [77, 78], který srovnává kultivační nálezy z kůže v místě zavedeného katétru s kultivačním nálezem z „hrdla“ katétru, dále výsledky hemokultury z odběru z katétru a současně z periferní žíly a nakonec časové rozdíly kultivačních pozitivit periferní a katétrové krve. Dodává však, že tento postup, tj. bez vynětí katétru, je možné zkusit jen u nemocných bez neutropenie a hematologické malignity, u kterých je katétr zaveden jen krátce (48 hodin) a kteří jsou hospitalizováni na JIP. Definitivní průkaz kolonizace katétru však získáme až po jeho vynětí. Nejčastěji se používá semikvantitativní kultivační metoda podle Makiho (špička odstraněného katétru se „roluje“ na kultivační půdě) [79]. Kvantitativní kultivační metody pomocí např. sonikace [80], nebo vortexování zachytí kolonizaci nejen exoluminální, ale i endoluminální; v celkovém srovnání diagnostického přínosu těchto metod pro klinickou praxi však není rozdíl [78].
3. 2 Farmakologická léčba hematogenní kandidózy (kandidémie) a invazivního kandidového onemocnění (akutní diseminované kandidózy)
Léčbu kandidémie je nutné zahájit co nejdříve, každý den prodlení zvyšuje mortalitu o více než 10 % [81, 82]. Nutná je proto včasná diagnostika a u nejrizikovějších nemocných je doporučeno již v den odběru hemokultur zahájit empirickou léčbu [82]. Délka léčby by měla trvat nejméně 14 dní po klinické stabilizaci a vymizení pozitivního kultivačního nálezu [83, 84].
V současné době je nabídka léků pro léčbu invazivní kandidózy a kandidémie širší než v případě invazivní aspergilózy. Patří mezi ně polyeny (amfotericin B a formy vázané na tukové vehikulum), triazoly (flukonazol, itrakonazol, vorikonazol) a echinokandiny (kaspofungin, anidulafungin, mikafungin). Postavení jednotlivých antimykotik v doporučení pro léčbu kandidózy je založeno na důkazech – na prokázané účinnosti ve srovnávacích studiích, a na kvalitě těchto studií hodnocených podle objektivních kritérií [85]. Stejným způsobem byla publikována řada guidelines [49, 56, 86–89]. Význam formulování doporučených léčebných postupů dokladují studie, ze kterých vyplývá, že nestandardní léčba je spojena s vyšší mortalitou [90] a že v některých případech je rozdíl v mortalitě statisticky významný [91].
Nejvíce studií bylo publikováno s konvenčním amfotericinem B (c-AmB), který byl do 90. let 20. století jediným lékem volby invazivní kandidózy a kandidémie. Většina srovnávacích studií byla prováděna u nemocných bez neutropenie. Studie, které se staly základem hodnocení a postavení jednotlivých léčiv, byly jednak prospektivní srovnávací nezaslepené [83, 92–94], jednak prospektivní observační [63, 95, 96], jednak retrospektivní [72] a také studie prospektivní randomizované zaslepené [97–99]. Nejvýznamnější z nich jsou uvedeny v tabulce 2.
2. Randomizované kontrolované srovnávací studie 1. linie léčby invazivní kandidózy a kandidémie 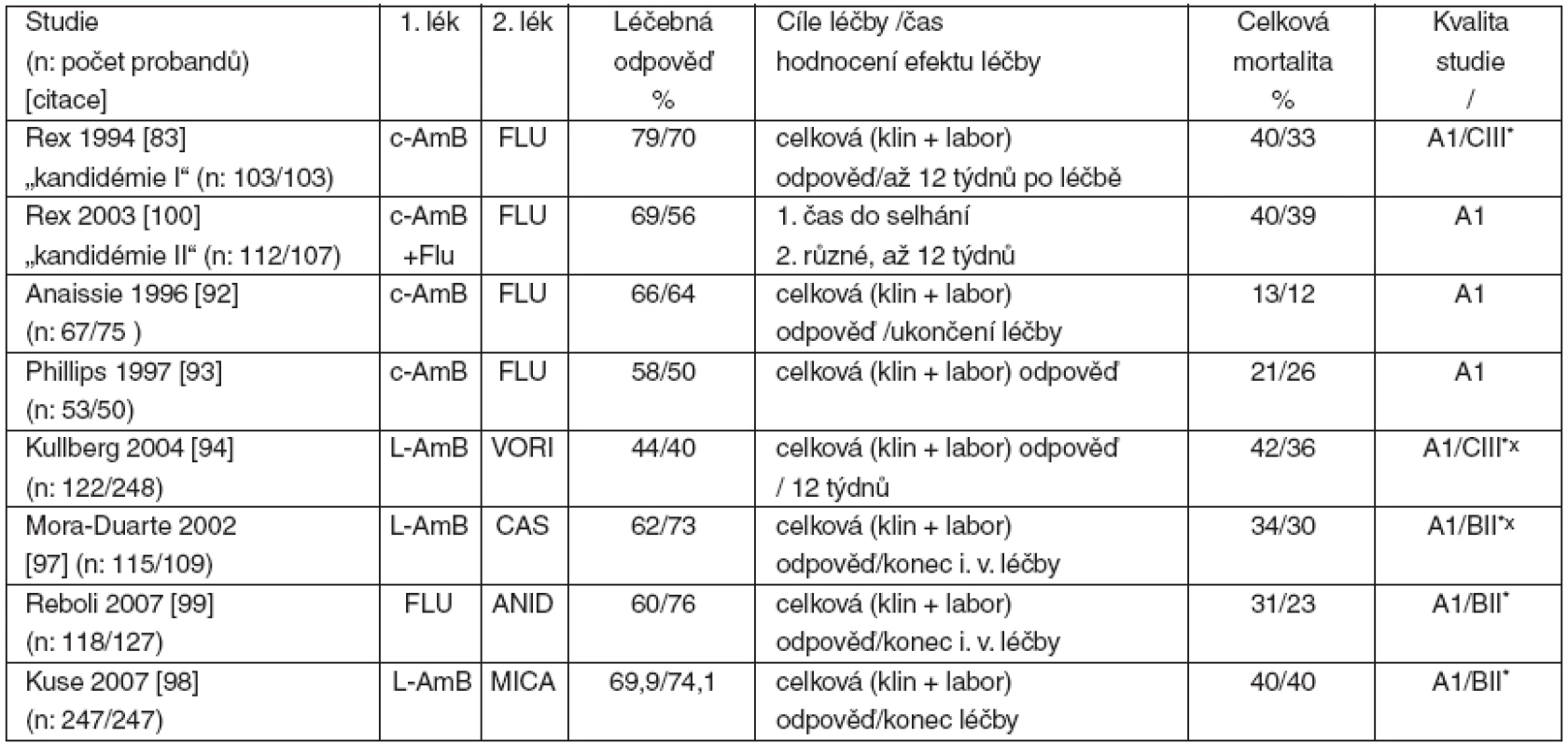
FLU – flukonazol; c-AmB – konvenční amfotericin B; CAS – kaspofungin; VORI – vorikonazol; L-AmB – liposomální amfotericin B, ANID – anidulafungin; MICA – mikafungin; n: počet probandů léčených 1. lékem/počet probandů léčených 2. (srovnávaným) lékem; *hodnocení pro neutropenické pacienty; xhodnocení pro infekce způsobené C. krusei a C. glabrata 3. 2. 1 Amfotericiny
První srovnávací studii (tzv. kandidémie I) konvenčního amfotericinu B (c-AmB) (n = 103) versus flukonazol (n =103) v léčbě kandidémie u non-neutropenických nemocných publikoval Rex [83]. Kritériem úspěšné léčby bylo úplné odeznění klinických známek infekce a negativita kultivačního nálezu, což de facto splňuje kritéria kompletní odpovědi. Výsledky léčby nebyly statisticky rozdílné (viz tab. 2), rozdílný nebyl ani počet selhání, ani procento úmrtí. Jediný rozdíl byl v menší toxicitě flukonazolu (37 % vs 2 %). Podobně ani v dalších studiích [92, 93, 100] nebyl zjištěn rozdíl v účinnosti mezi c-AmB a flukonazolem. Za zdůraznění stojí druhá studie Rexe [100], tzv. kandidémie II, ve které byla řešena jednak otázka vyšších dávek flukonazolu (800 mg . den-1, tj. cca 10 mg . kg-1) [101] a jednak efekt kombinace flukonazolu s c-AmB. Autoři nezjistili antagonismus kombinace flukonazolu s c-AmB, naopak z hlediska klinického hodnocení léčby byla tato kombinace blízko statistické významnosti úspěšnější jak v klinickém hodnocení léčby, tak i ve vyšším procentu a dřívější eradikaci infekce.
Roli konvenčního amfotericinu B, ve srovnání s tehdy novým flukonazolem, shrnuje metaanalýza [102] celkem 826 epizod kandidémie u nemocných bez neutropenie ze šesti prospektivních randomizovaných a observačních studií z let 1996–1999 [63, 83, 92, 93, 95, 96]. Metaanalýza prokazuje stejnou účinnost obou preparátů s výrazně nižší toxicitou flukonazolu. Limit těchto studií spočívá v tom, že nebyli zařazeni nemocní s infekcí C. krusei (primární rezistence na flukonazol) a C. glabrata (získaná rezistence na flukonazol 0–80 %).
3. 2. 2 Amfotericiny na tukovém nosiči
Amfotericiny na tukovém nosiči v žádné ze studií neprokázaly lepší účinnost než c-AmB [103–105]. Jejich zásadní výhodou je omezení rizika nefrotoxicity, většinou i snížení incidence a intenzity akutních nežádoucích účinků vázaných na aplikaci infuze (třesavka, horečka, hypotenze...). Indikace lipidových forem AmB je preferována, i když víme, že při lege artis podaném c-AmB [106–109] s dostatečně dlouhou aplikací infuze, s dostatečnou hydratací a suplementací iontů je možné riziko nefrotoxicity omezit [110–115] a při řádné premedikací omezit i výskyt akutních nežádoucích účinků.
Účinnost lipidového komplexu amfotericinu B (ABLC) u invazivní kandidózy a kandidémie v rámci CLEAR [116] byla hodnocena celkem u 979 nemocných s kandidózou – jde o největší kohortu nemocných s kandidózou léčených jedním lékem. Z toho bylo 207 nemocných s kandidémií (n = 123), s invazivní kandidózou (n = 58) nebo kombinací obou (n = 26). Soubor byl stratifikován a hodnocen podle různých kritérií včetně infekcí způsobené C. albicans oproti non-albicans, kde byly výsledky v zásadě obdobné – bylo dosaženo klinické odpovědi mezi 55–67 %. Ani u neutropenických pacientů nebyly výsledky rozdílné, i když významně horší, mezi 20–25 %. Anaissie [117] prezentoval v roce 1995 na ICAAC srovnávací studii ABLC (n = 153) vs c-AmB (n = 78). Výsledky byly v obou skupinách také obdobné jak v dosažení klinické odpovědi (ABLC vs c-AmB: 65 % vs 61 %), tak i v procentu mortality (40 % vs 49 %), eradikaci infekce (88 % vs 87 %) a rovněž u nemocných s neutropenií (27 % vs 33 %) či bez neutropenie (70 % vs 66 %). Práce však nebyla dále publikována.
Zkušenosti s koloidní disperzí amfotericinu B (ABCD) v léčbě invazivní mykózy jsou shrnuty v souboru s 220 nemocnými (data byla získána retrospektivně z pěti nekomparativních studií) po transplantaci kostní dřeně (167 allogenní, 53 autologní), z nichž 100 mělo kandidovou infekci [118]. ABCD byl podáván převážně ve 2. linii, po selhání předchozí léčby, nebo s projevy intolerance nebo nefrotoxicity po předchozí léčbě c-AmB. Hodnoceni byli jen nemocní s prokázanou infekcí, kteří dostávali ABCD nejméně 7 dní a žádná další antimykotika do kombinace. S invazivní kandidózou bylo proto hodnoceno jen 46 nemocných. Klinické odpovědi (kompletní + parciální) dosáhlo celkem 65 % z nich (30/46), z toho 64 % nemocných po alogenní transplantaci kostní dřeně (21/33) a 69 % pacientů po autologní transplantaci (9/13). Zemřelo 54 % nemocných s kandidózou (25/46), autoři uvádějí vyšší procento úmrtí po alogenní transplantaci, ale bez bližšího rozdělení. Podobně jako při léčbě ABLC, ani v případě ABCD nedocházelo u preexistujícího renálního poškození ke vzestupu kreatininu. Údaje ze stejné databáze jsou publikovány i v další práci Noskina [119].
Lipozomální amfotericin B (Ambisome) není v ČR registrován, nejsou s ním významnější zkušenosti, proto v tomto textu klinické studie neuvádíme.
Indikace lipidových amfotericinů byly v zásadě formulovány již dříve [120]. Rozhodujeme se pro ně zejména:
- po selhání předchozí léčby c-AmB,
- při projevech nefrotoxicity po předchozí léčbě c-AmB,
- při výrazných projevech akutní toxicity po c-AmB,
- při preexistujícím renálním poškození,
- při současné léčbě nefrotoxickými léky.
3. 2. 3 Triazoly
Výsledky studií s flukonazolem, které byly uvedeny výše, jsou podkladem zařazení flukonazolu mezi léky 1. volby léčby invazivní kandidózy a kandidémie u nemocných bez neutropenie, s výjimkou infekcí způsobených C. krusei a C. glabrata (viz tab. 2).
Vorikonazol, triazol 2. generace, byl v prospektivní randomizované otevřené studii srovnáván proti konvenčnímu postupu c-AmB + flukonazol (AmB/Flu) v primární léčbě kandidémie u non-neutropenických nemocných [94]. V primární analýze, po skončení léčby, v celkové mortalitě a v čase dosažení mykologické eradikace patogenu v hemokultuře byly zaznamenány stejné výsledky, rozdíly nebyly statisticky signifikantní. Vorikonazol tak rozšířil léky 1. linie v léčbě invazivní kandidózy a kandidémie u nemocných bez neutropenie (viz tab. 2)
Itrakonazol nemá validní studii v 1. linii léčby invazivní kandidózy, pouze na malém souboru (n = 37) byl srovnáván s flukonazolem (n = 44). Výsledky, které byly v obou skupinách stejné (92 % vs 91 %), byly prezentovány jen formou příspěvku na sympoziu intenzivistů [121]. Posakonazol dosud nemá studii invazivní kandidózy a kandidémie, proto není v uvedené indikaci hodnocen.
3. 2. 4 Echinokandiny
Významnou skupinou antimykotik jsou echinokandiny, které prokázaly velmi dobrý účinek při léčbě invazivní kandidózy. První z nich, kaspofungin, rozšířil spektrum léků 1. volby v roce 2002. Ve dvojitě slepé studii [97] invazivní kandidózy a kandidémie byl srovnáván kaspofungin (CAS) (n = 109) proti c-AmB (n = 115) – viz tab. 2. Soubor nemocných byl stratifikován podle: skóre APACHE II, neutropenie (< 0,5 . 10-9 . l-1 CAS vs c-AmB: 12,8 % (14/109) vs 8,7 % (10/115)) kandidémie, účinnosti u C. albicans a non-albicans a dalších kritérií. V globálním hodnocení souboru, ve kterém byli hodnoceni nemocní s prokázanou infekcí a alespoň s jednou dávkou antimykotika, dosáhl kaspofungin celkově podobných výsledků jako c-AmB (celková odpověď 73,4 % vs 61,7 %). V globálním hodnocení nebyly zásadní rozdíly ani v podskupinách podle APACHE II skóre > 20 (CAS 57,1 %; 12/21 vs AmB 43,5 %; 10/23) a podle neutropenie (CAS vs c-AmB 50 %; 7/14 vs 40 %, 4/10), ani ve výsledcích léčby kandidémie (71,7 % vs 62,8 %), ani v mortalitě.
Další echinokandin – anidulafungin – je v ČR v roce 2008 aktuálně registrován. Jeho účinnost byla ověřována v léčbě invazivní kandidózy ve dvojitě slepé randomizované studii proti flukonazolu. Anidulafungin v této studii prokázal lepší výsledky, a dosáhl tak nejen cíle studie – noninferiority [99], ale statisticky významně lepších výsledků, tj. superiority. Soubor nemocných byl stratifikován – kromě dalších kritérií – také podle APACHE II skóre a podle neutropenie; vyloučeni byli – kromě jiných kritérií – nemocní, kteří dostávali 30 dní před studií profylakticky jakékoli azoly po dobu 7 dní, nemocní s předchozí rezistentní kandidovou infekcí a s prokázanou infekcí Candida krusei. Celková odpověď, hodnocená na konci nitrožilní léčby, byla ve skupině léčených anidulafunginem významně lepší (75,6 % vs 60,2 %; rozdíl: 15,4 %; p = 0,01). Při hodnocení na konci léčby byly výsledky obdobné 74 % vs 56,8 %, stejně tak 2 týdny po skončení léčby (64,6 % vs 49,2 %) a po 6 týdnech po skončení léčby (55,9 % vs 44,1 %). U nemocných s izolovanou kandidémií dosáhlo příznivé odpovědi 75,9 % vs 61,2 % (p = 0,02). Ve skupině anidulafunginu zemřelo méně nemocných 22,8 % vs 31,4 %. Medián času do úmrtí byl 21 dní vs 14 dní. Celkově výsledky anidulafunginu jsou obdobné jako ve studii kaspofungin vs amfotericin [97], výsledky dosažené flukonazolem jsou obdobné jako ve studii Rexe [100].
Mikafungin, další echinokandin, se má objevit na trhu v ČR na podzim 2008. Velmi dobrou účinnost u kandidémie prokázal jak v nekomparativní studii [122], tak ve dvojitě zaslepené srovnávací studii mikafungin s lipozomálním amfotericinem [98] v primární léčbě kandidémie a invazivní kandidózy. Hodnoceni byli – s cílem posouzení non-inferiority – všichni nemocní s nejméně jednou dávku léčby (MICA: n = 247, L-AmB: n = 247). Terapeutickou účinnost (úplná a částečná klinická odpověď + laboratorní eradikace patogenu) hodnotila nezávislá „zaslepená“ komise na konci léčby, bez časového limitu, nemocní byli sledováni 12 týdnů. Celkový úspěch léčby se mezi oběma skupinami nelišil, MICA (74,1 %, 183/247) vs L-AmB (69,9 %, 172/247), a to ani v dosažení kompletní odpovědi (64,4 % vs 60,7 %). Rozdíl nebyl ani v podskupinách podle neutropenie (59,4 % vs 56 %), nebo primární lokalizace infekce, podle druhu infekce (C. albicans oproti non-albicans), ani podle APACHE II, či v procentu selhání laboratorní eradikace, ani v mortalitě (18 % vs 17 %), respektive 40 % na konci léčby v obou skupinách.
Ke skupině echinokandinů je nutné zdůraznit, že žádná ze studií nemá dostatečnou sílu důkazu k doporučení pro léčbu neutropenických nemocných (C III), neboť ve studiích byl hodnocen je malý počet nemocných (tab. 3). Výsledky jsou proto zatíženy chybou malých čísel.
3. Srovnání studií s echinokandiny u invazivní kandidózy a kandidémie: počty nemocných s neutropenií (leu < 0,5) a výsledky léčby. 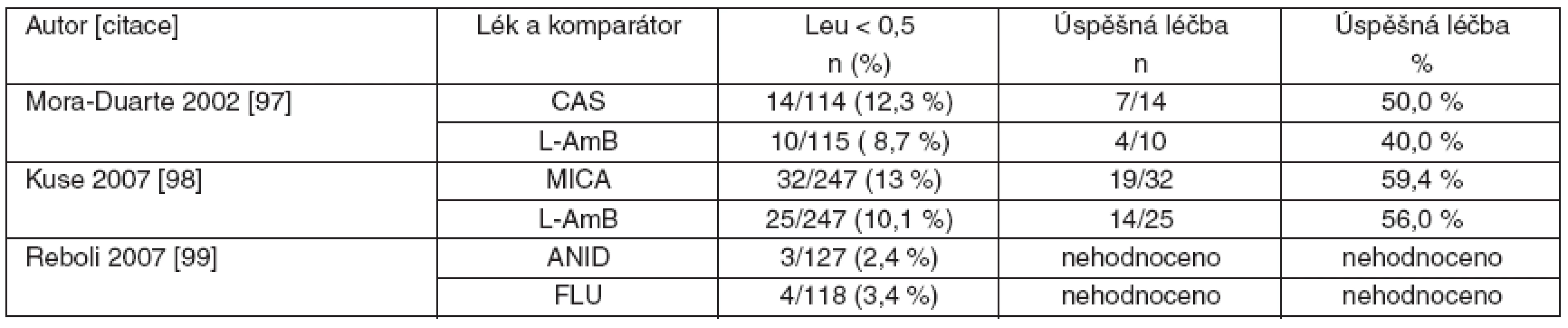
n – počet neutropenických nemocných/celkový počet nemocných ve studii, (%) – procento neutropenických nemocných z celkového počtu nemocných ve studii 3. 3 Délka léčby invazivní kandidózy a kandidémie
Současná doporučení pro délku léčby kandidózy a kandidémie u pacienta bez neutropenie je 14 dní po posledním pozitivním kultivačním nálezu za předpokladu vymizení odeznění všech klinických známek infekce [56, 87], prodloužení léčby se předpokládá při orgánové kandidóze, při hepatosplenické formě nejméně 6 týdnů až několik (12) měsíců, respektive do vymizení nebo do kalcifikace lézí v orgánech [89].
3. 4 Význam kultivačních vyšetření a stanovení citlivosti (MIC) na antimykotika
Skupina autorů ECIL doporučuje vyšetřovat citlivost na antimykotika u hematologických pacientů. Znalost výsledků umožní korelovat klinický efekt léčby s laboratorní eradikací infekce, eventuálně zjistit příčinu selhání léčby. Současně umožní v některých případech kvalifikovaně přejít z nitrožilní léčby na perorální antimykotikum.
4 Doporučení a závěr
Většina klinických studií léčby invazivní kandidózy a kandidémie se týkala nemocných bez neutropenie. Při přípravě doporučených postupů jsme vycházeli z práce skupiny ECIL (European Conference on Infection in Leukemia: ECIL 1 a ECIL 2) [84, 89], jejíž koncepce respektovala doporučení pro podskupinu nemocných bez neutropenie a pro nemocné s neutropenií, tj. především pro hematologické malignity.
Epidemiologická data svědčí pro absolutní pokles výskytu C. albicans a vzestup non-albicans kmenů kandid, zejména C. krusei [123–125], C. glabrata [126, 127] a C.parapsilosis [128]. Ty mají obecně nižší citlivost vůči flukonazolu, některé jsou primárně rezistentní na flukonazol (C. krusei), některé rezistenci získají (C. glabrata) [127–131].
4. 1 Postup při časné léčbě hematogenní infekce před určením druhu kandidy
U rizikových (neutropenických) nemocných je proto nevhodné před určením druhu kandidy podat flukonazol. Ten je indikován jen v případě, že jsou splněna kritéria pro aplikaci flukonazolu tj. „nerizikových“ nemocných (= bez neutropenie, klinicky stabilizovaný nemocný normální TK, P, klinicky trend ke zlepšení, bez komplikujících komorbidit) [86]. U rizikových nemocných se rozhodujeme v první linii pro echinokandiny; amfotericiny, respektive lipidové formy, a triazoly (vorikonazol) mají určité limity. V klinických studiích nemocných bez neutropenie však uvedené skupiny léků prokázaly stejnou efektivitu, proto byly označeny stupněm A I (tab. 4). Limitem c-AmB je nefrotoxicita, proto je nelze doporučit (stupeň D III) při současné léčbě [86] nefrotoxickými léky a zásadně nedoporučit (E III) při renální insuficienci. Indikace vorikonazolu je omezena na infekce Candida krusei.
4. Kvalita důkazů a síla doporučení podle CDC pro antimykotika u nemocných před identifikací druhu kandidy 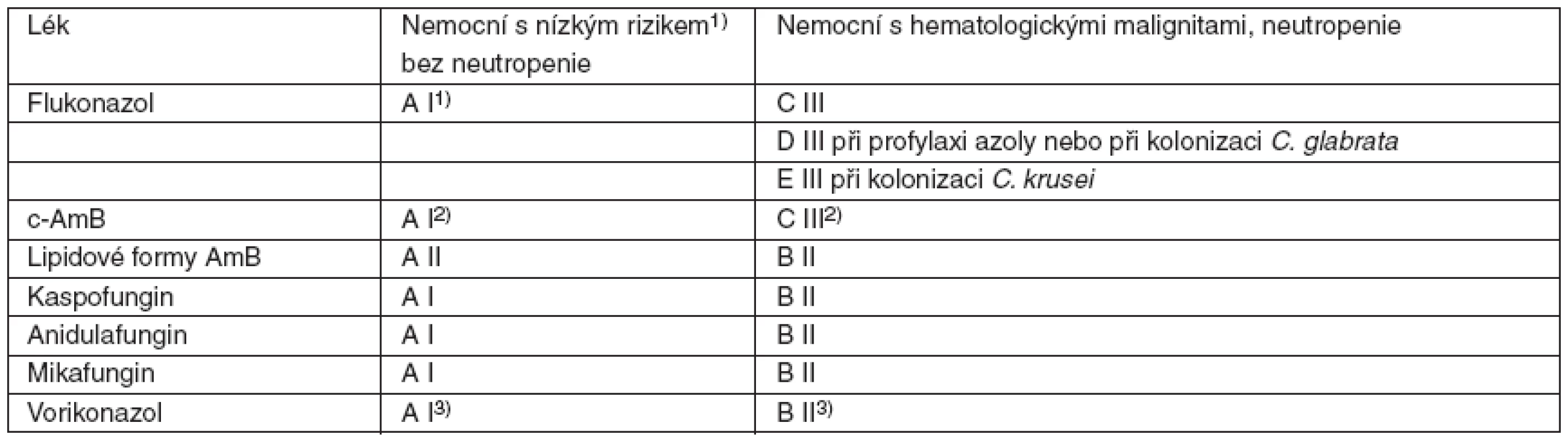
(podle Herbrechta [84, 89]) c-AmB – konvenční amfotericin B; 1)hemodynamicky stabilizovaný, bez závažných komorbidit, klinicky tendence ke zlepšení; 2)DIII při současné léčbě nefrotoxickými léky a E III při renální insuficienci; 3)pokud nejsou azoly v profylaxi 4. 2 Postup při časné léčbě hematogenní kandidové infekce způsobené Candida albicans, C. glabrata nebo C. krusei
Lékem volby jsou echinokandiny (tab. 5), ve výsledcích klinických studií není mezi nimi rozdíl (viz tab. 2, 3); volbu mezi jednotlivými preparáty lze zvažovat jen v mezních situacích (jaterní nebo renální selhání...). Pozice c-AmB je oslabena průvodní nefrotoxicitou, vorikonazol je alternativou pro infekci C. krusei, jinak se doporučuje jej spíše ponechat pro léčbu invazivní aspergilózy, kde je lékem první volby [132].
5. Kvalita důkazů a síla doporučení podle CDC pro antimykotika nemocných hematologickými malignitami s kandidémií při infekci C. albicans, C. glabrata, C. krusei 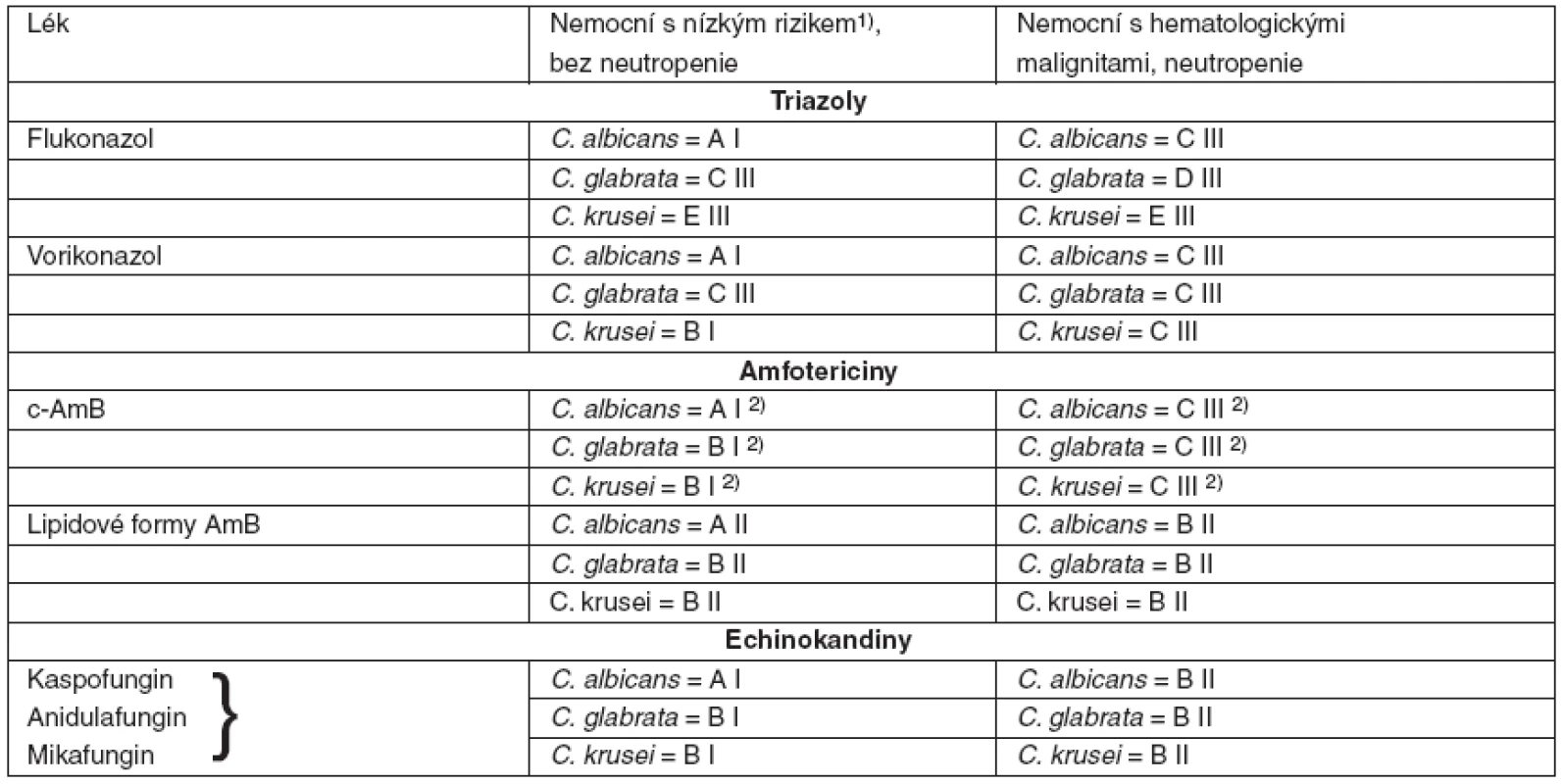
c-AmB – konvenční amfotericin B; 1)hemodynamicky stabilizovaný, bez závažných komorbidit, klinicky tendence ke zlepšení; 2)DIII při současné léčbě nefrotoxickými léky a EIII při renální insuficienci 4. 3 Obvyklé dávkování antimykotik
Toto dávkování uvádí tabulka 6.
6. Obvyklé dávkování antimykotik 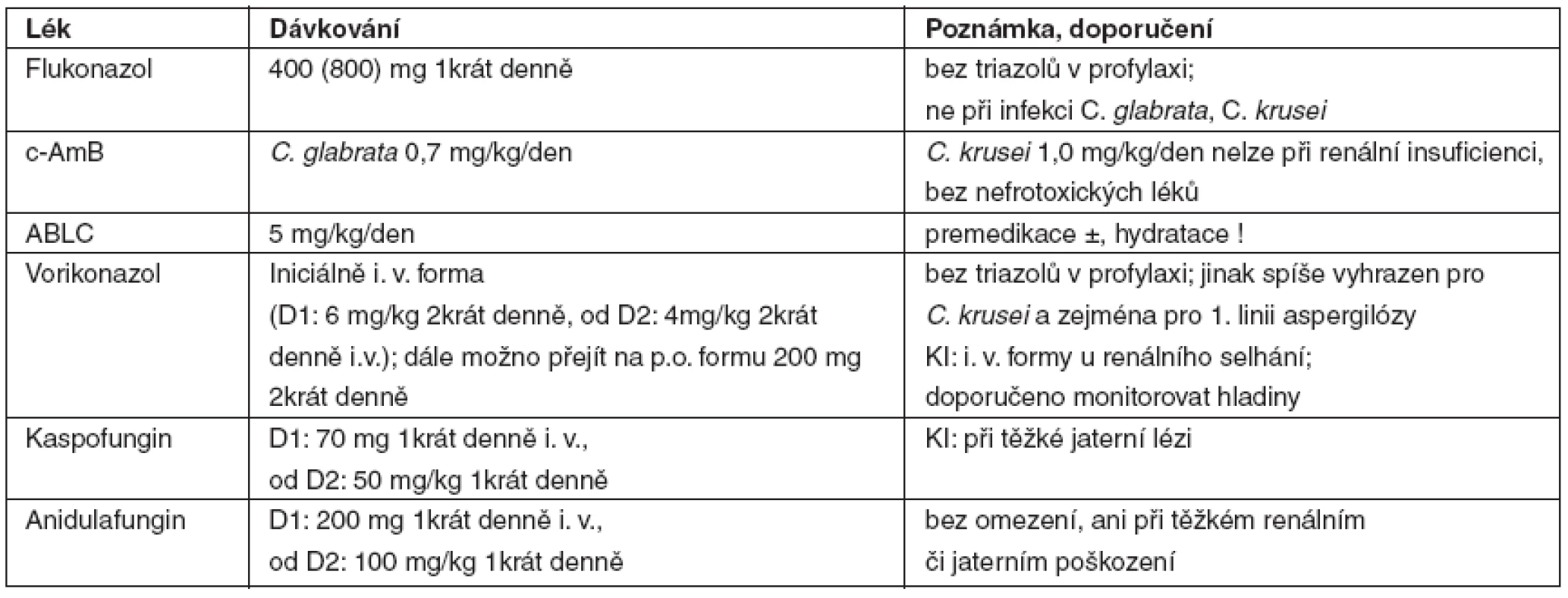
Mikafungin 100 mg denně i. v. registrace v ČR očekávána 10/2008 c-AmB – konvenční amfotericin B; ABLC – lipidový komplex amfotericinu B 5 Závěr
Závěrem chceme zdůraznit, že tato léčebná doporučení je nutné brát pouze jako zásadní informaci, která je časově omezená a kterou nelze mechanicky aplikovat v klinické praxi.
Všichni víme, že v případě konkrétního pacienta, při rozhodování u lůžka, je potřeba komplexní posouzení celkového stavu nemocného, což znamená zejména zhodnocení základního onemocnění, zvážení farmakologických vlastností antimykotik, současné medikace a dalších faktorů. Až pak se kvalifikovaně rozhodujeme pro lék 1. volby. Širší nabídka antimykotik také umožňuje využít sekvenční léčby, kdy po neúspěchu jedné skupiny antimykotik lze pokračovat v léčbě jinou, stejně tak je možné zvážit kombinaci antimykotik.
Adresa pro korespondenci:
MUDr. Jan Haber, CSc.
I. interní klinika – klinika hematologie
U Nemocnice 2
128 08 Praha 2
e-mail: jan.haber@vfn.cz
Sources
1. Morgan, J., Meltzer, M. I., Plikaytis, B. D. et al. Excess mortality, hospital stay, and cost due to candidemia: a case-control study using data from population-based candidemia surveillance. Infect. Control. Hosp. Epidemiol., 2005, 26, p. 540–547.
2. Pfaller, M., Wenzel, R. Impact of the changing epidemiology of fungal infections in the 1990s. Eur. J. Clin. Microbiol. Infect. Dis., 1992, 11, p. 287–291.
3. Beck-Sague, C., Jarvis, W. R. Secular trends in the epidemiology of nosocomial fungal infections in the United States, 1980–1990. National Nosocomial Infections Surveillance System. J. Infect. Dis., 1993, 167, p. 1247–1251.
4. Kao, A. S., Brandt, M. E., Pruitt, W. R. et al. The epidemiology of candidemia in two United States cities: results of a population-based active surveillance. Clin. Infect. Dis., 1999, 29, p. 1164–1170.
5. Diekema, D. J., Messer, S. A., Brueggemann, A. B. et al. Epidemiology of candidemia: 3-year results from the emerging infections and the epidemiology of Iowa organisms study. J. Clin. Microbiol., 2002, 40, p. 1298–1302.
6. Hajjeh, R. A., Sofair, A. N., Harrison, L. H. et al. Incidence of bloodstream infections due to Candida species and in vitro susceptibilities of isolates collected from 1998 to 2000 in a population-based active surveillance program. J. Clin. Microbiol., 2004, 42, p. 1519–1527.
7. Abi-Said, D., Anaissie, E., Uzun, O. et al. The epidemiology of hematogenous candidiasis caused by different Candida species. Clin. Infect. Dis., 1997, 24, p. 1122–1128.
8. Goodman, J. L., Winston, D. J., Greenfield, R. A. et al. A controlled trial of fluconazole to prevent fungal infections in patients undergoing bone marrow transplantation. N. Engl. J. Med., 1992, 326, p. 845–851.
9. Laverdiere, M., Rotstein, C., Bow, E. J. et al. Impact of fluconazole prophylaxis on fungal colonization and infection rates in neutropenic patients. The Canadian Fluconazole Study. J. Antimicrob. Chemother., 2000, 46, p. 1001–1008.
10. Junghanss, C., Marr, K. A. Infectious risks and outcomes after stem cell transplantation: are nonmyeloablative transplants changing the picture? Curr. Opin. Infect. Dis., 2002, 15, p. 347–353.
11. Gudlaugsson, O., Gillespie, S., Lee, K. et al. Attributable mortality of nosocomial candidemia, revisited. Clin. Infect. Dis., 2003, 37, p. 1172–1177.
12. Marr, K. A. The changing spectrum of candidemia in oncology patients: therapeutic implications. Curr. Opin. Infect. Dis., 2000, 13, p. 615–620.
13. Kami, M., Machida, U., Okuzumi, K. et al. Effect of fluconazole prophylaxis on fungal blood cultures: an autopsy-based study involving 720 patients with haematological malignancy. Br. J. Haematol., 2002, 117, p. 40–46.
14. Sendid, B., Cotteau, A., Francois, N. et al. Candidaemia and antifungal therapy in a French University Hospital: rough trends over a decade and possible links. BMC Infect. Dis., 2006, 6, p. 80.
15. Eggimann, P., Garbino, J., Pittet, D. Epidemiology of Candida species infections in critically ill non-immunosuppressed patients. Lancet Infect. Dis., 2003, 3, p. 685–702.
16. Pappas, P. G., Rex, J. H., Lee, J. et al. A prospective observational study of candidemia: epidemiology, therapy, and influences on mortality in hospitalized adult and pediatric patients. Clin. Infect. Dis., 2003, 37, p. 634–643.
17. Ostrosky-Zeichner, L., Pappas, P. G. Invasive candidiasis in the intensive care unit. Crit. Care Med., 2006, 34, p. 857–863.
18. Trick, W. E., Fridkin, S. K., Edwards, J. R. et al. Secular trend of hospital-acquired candidemia among intensive care unit patients in the United States during 1989–1999. Clin. Infect. Dis., 2002, 35, p. 627–630.
19. Wisplinghoff, H., Bischoff, T., Tallent, S. M. et al. Nosocomial bloodstream infections in US hospitals: analysis of 24,179 cases from a prospective nationwide surveillance study. Clin. Infect. Dis., 2004, 39, p. 309–317.
20. Asmundsdottir, L. R., Erlendsdottir, H., Gottfredsson, M. Increasing incidence of candidemia: results from a 20-year nationwide study in Iceland. J. Clin. Microbiol., 2002, 40, p. 3489–3492.
21. Poikonen, E., Lyytikainen, O., Anttila, V. J., Ruutu, P. Candidemia in Finland, 1995–1999. Emerg. Infect. Dis., 2003, 9, p. 985–990.
22. Almirante, B., Rodriguez, D., Park, B. J. et al. Epidemiology and predictors of mortality in cases of Candida bloodstream infection: results from population-based surveillance. Barcelona, Spain, from 2002 to 2003. J. Clin. Microbiol., 2005, 43, p. 1829–1835.
23. Sandven, P., Bevanger, L., Digranes, A. et al. Constant low rate of fungemia in norway, 1991 to 1996. The Norwegian Yeast Study Group. J. Clin. Microbiol., 1998, 36, p. 3455–3459.
24. Sandven, P., Bevanger, L., Digranes, A. et al. Candidemia in Norway (1991 to 2003): results from a nationwide study. J. Clin. Microbiol., 2006, 44, p. 1977–1981.
25. Richet, H., Roux, P,, Des Champs, C. et al. Candidemia in French hospitals: incidence rates and characteristics. Clin. Microbiol. Infect., 2002, 8, p. 405–412.
26. Rodriguez, D., Almirante, B., Park, B. J. et al. Candidemia in neonatal intensive care units: Barcelona, Spain. Pediatr. Infect. Dis. J., 2006, 25, p. 224–229.
27. McNeil, M. M., Nash, S. L, Hajjeh, R. A. et al. Trends in mortality due to invasive mycotic diseases in the United States, 1980–1997. Clin. Infect. Dis., 2001, 33, p. 641–647.
28. Hobson, R. P. The global epidemiology of invasive Candida infections – is the tide turning? J. Hosp. Infect., 2003, 55, p. 159–168; quiz 233.
29. Marr, K. A., Seidel, K., Slavin, M. A. et al. Prolonged fluconazole prophylaxis is associated with persistent protection against candidiasis-related death in allogeneic marrow transplant recipients: long-term follow-up of a randomized, placebo-controlled trial. Blood, 2000, 96, p. 2055–2061.
30. Marr, K. A. Invasive Candida infections: the changing epidemiology. Oncology, (Williston Park) 2004, 18, p. 9–14.
31. Chamilos, G., Luna, M., Lewis, R. E. et al. Invasive fungal infections in patients with hematologic malignancies in a tertiary care cancer center: an autopsy study over a 15-year period (1989-2003). Haematologica, 2006, 91, p. 986–989.
32. Peman, J., Canton, E., Gobernado, M. Epidemiology and antifungal susceptibility of Candida species isolated from blood: results of a 2-year multicentre study in Spain. Eur. J. Clin. Microbiol. Infect. Dis., 2005, 24, p. 23–30.
33. Pfaller, M. A., Diekema, D. J. Epidemiology of invasive candidiasis: a persistent public health problem. Clin. Microbiol. Rev., 2007, 20, p. 133–163.
34. Nguyen, M. H., Peacock, J. E., Jr., Morris, A. J. et al. The changing face of candidemia: emergence of non-Candida albicans species and antifungal resistance. Am. J. Med., 1996, 100, p. 617–623.
35. Antoniadou, A., Torres, H. A., Lewis, R. E. et al. Candidemia in a tertiary care cancer center: in vitro susceptibility and its association with outcome of initial antifungal therapy. Medicine (Baltimore), 2003, 82, p. 309–321.
36. Marchetti, O., Bille, J., Fluckiger, U. et al. Epidemiology of candidemia in Swiss tertiary care hospitals: secular trends, 1991–2000. Clin. Infect. Dis., 2004, 38, p. 311–320.
37. Martin, D., Persat, F., Piens, M. A., Picot, S. Candida species distribution in bloodstream cultures in Lyon, France, 1998–2001. Eur. J. Clin. Microbiol. Infect. Dis., 2005, 24, p. 329–333.
38. Richardson, M. D. Changing patterns and trends in systemic fungal infections. J. Antimicrob. Chemother., 2005, 56, Suppl 1, i5-i11.
39. Boktour, M. R., Kontoyiannis, D. P., Hanna, H. A. et al. Multiple-species candidemia in patients with cancer. Cancer, 2004, 101, p. 1860–1865.
40. Tortorano, A. M., Caspani, L., Rigoni, A. L. et al. Candidosis in the intensive care unit: a 20-year survey. J. Hosp. Infect., 2004, 57, p. 8–13.
41. Dimopoulos, G., Karabinis, A., Samonis, G., Falagas, M. E. Candidemia in immunocompromised and immunocompetent critically ill patients: a prospective comparative study. Eur. J. Clin. Microbiol. Infect. Dis., 2007, 26, p. 377–384.
42. Tortorano, A. M., Peman, J., Bernhardt, H. et al. Epidemiology of candidaemia in Europe: results of 28-month European Confederation of Medical Mycology (ECMM) hospital-based surveillance study. Eur. J. Clin. Microbiol. Infect. Dis., 2004, 23, p. 317–322.
43. Buchta, V. M. K,, Bergerová, T. Výskyt potenciálně patogenních kvasinek v krvi a moči pacientů ve velkých nemocnicích v České republice. Klin. Mikrobiol. Inf. Lék., 1998, 4, p. 10–17.
44. Hamal, P., Dobiášová, S., Kocmanová, I. Candidemia in large Czech hospitals, 2000–2002: An epidemiological study. In 15th Congress of the International Society for Human and Animal Mycology. San Antonio, 2003; p. 463.
45. Hamal, P., Kocmanová, I., Jedličková, A. et al. Epidemiological analysis of candidemia in Czech tertiary care hospitals in 2000–2006. J. Chemother., 2007, 19 (suppl. 3), S61–S62.
46. Krcmery, V., Jr., Kovacicova, G. Longitudinal 10-year prospective survey of fungaemia in Slovak Republic: trends in etiology in 310 episodes. Slovak Fungaemia study group. Diagn. Microbiol. Infect. Dis., 2000, 36, p. 7–11.
47. Drgona, L., Trupl, J., Roidova, A. et al. Fungaemia in Slovakia: a prospective, national study. . ECCMID 2008, Barcelona. 2008.
48. Rex, J. H., Bennett, J. E., Sugar, A. M. et al. Intravascular catheter exchange and duration of candidemia. NIAID Mycoses Study Group and the Candidemia Study Group. Clin. Infect. Dis., 1995, 21, p. 994–996.
49. Rex, J. H., Walsh, T. J., Sobel, J. D. et al. Practice guidelines for the treatment of candidiasis. Infectious Diseases Society of America. Clin. Infect. Dis., 2000, 30, p. 662–678.
50. Luzzati, R., Amalfitano, G., Lazzarini, L. et al. Nosocomial candidemia in non-neutropenic patients at an Italian tertiary care hospital. Eur. J. Clin. Microbiol. Infect. Dis., 2000, 19, p. 602–607.
51. Walsh, T. J., Rex, J. H. All catheter-related candidemia is not the same: assessment of the balance between the risks and benefits of removal of vascular catheters. Clin. Infect. Dis., 2002, 34, p. 600–602.
52. Viudes, A., Peman, J., Canton, E. et al. Candidemia at a tertiary-care hospital: epidemiology, treatment, clinical outcome and risk factors for death. Eur. J. Clin. Microbiol. Infect. Dis., 2002, 21, p. 767–774.
53. Fatkenheuer, G., Buchheidt, D., Cornely, O. A. et al. Central venous catheter (CVC)-related infections in neutropenic patients – guidelines of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO). Ann. Hematol., 2003, 82, Suppl 2, S149–157.
54. Fatkenheuer, G., Cornely, O., Seifert, H. Clinical management of catheter-related infections. Clin. Microbiol. Infect., 2002, 8, p. 545–550.
55. Maki, D. G., Crnich, C. J. Line sepsis in the ICU: prevention, diagnosis, and management. Semin. Respir. Crit. Care Med., 2003, 24, p. 23–36.
56. Pappas, P. G., Rex, J. H., Sobel, J. D. et al. Guidelines for treatment of candidiasis. Clin. Infect. Dis., 2004, 38, p. 161–189.
57. Pasqualotto, A. C., de Moraes, A. B., Zanini, R. R., Severo, L. C. Analysis of independent risk factors for death among pediatric patients with candidemia and a central venous catheter in place. Infect. Control. Hosp. Epidemiol., 2007, 28, p. 799–804.
58. Karlowicz, M. G., Hashimoto, L. N., Kelly, R. E., Jr., Buescher, E. S. Should central venous catheters be removed as soon as candidemia is detected in neonates? Pediatrics, 2000, 106, E63.
59. Nucci, M., Anaissie, E. Should vascular catheters be removed from all patients with candidemia? An evidence-based review. Clin. Infect. Dis., 2002, 34, p. 591–599.
60. Mermel, L. A., Farr, B. M., Sherertz, R. J. et al. Guidelines for the management of intravascular catheter-related infections. Clin. Infect. Dis., 2001, 32, p. 1249–1272.
61. O’Grady, N. P., Alexander, M., Dellinger, E. P. et al. Guidelines for the prevention of intravascular catheter-related infections. Infect. Control. Hosp. Epidemiol., 2002, 23, p. 759–769.
62. Vescia, S., Baumgartner, A. K., Jacobs, V. R. et al. Management of venous port systems in oncology: a review of current evidence. Ann. Oncol., 2008, 19, p. 9–15.
63. Nguyen, M. H., Peacock, J. E., Jr., Tanner, D. C. et al. Therapeutic approaches in patients with candidemia. Evaluation in a multicenter, prospective, observational study. Arch. Intern. Med., 1995, 155, p. 2429–2435.
64. Lecciones, J. A., Lee, J. W., Navarro, E. E. et al. Vascular catheter-associated fungemia in patients with cancer: analysis of 155 episodes. Clin. Infect. Dis., 1992, 14, p. 875–883.
65. Nucci, M., Colombo, A. L., Silveira, F. et al. Risk factors for death in patients with candidemia. Infect. Control. Hosp. Epidemiol., 1998, 19, p. 846–850.
66. Kibbler, C. C., Seaton, S., Barnes, R. A. et al. Management and outcome of bloodstream infections due to Candida species in England and Wales. J. Hosp. Infect., 2003, 54, p. 18–24.
67. Aliyu, S. H., Enoch, D. A., Abubakar, I. I. et al. Candidaemia in a large teaching hospital: a clinical audit. QJM, 2006, 99, p. 655–663.
68. Nucci, M., Anaissie, E. Revisiting the source of candidemia: skin or gut? Clin. Infect. Dis., 2001, 33, p. 1959–1967.
69. Blot, F., Schmidt, E., Nitenberg, G. et al. Earlier positivity of central-venous - versus peripheral-blood cultures is highly predictive of catheter-related sepsis. J. Clin. Microbiol., 1998, 36, p. 105–109.
70. Raad, I., Hanna, H., Maki, D. Intravascular catheter-related infections: advances in diagnosis, prevention, and management. Lancet Infect. Dis., 2007, 7, p. 645–657.
71. Pasqualotto, A. C., Severo, L. C. The importance of central venous catheter removal in patients with candidaemia: time to rethink our practice? Clin. Microbiol. Infect., 2008, 14, p. 2–4.
72. Anaissie, E. J., Rex, J. H., Uzun, O., Vartivarian, S. Predictors of adverse outcome in cancer patients with candidemia. Am. J. Med., 1998, 104, p. 238–245.
73. Pearson, M. L. Guideline for prevention of intravascular device-related infections. Hospital Infection Control Practices Advisory Committee. Infect. Control. Hosp. Epidemiol., 1996, 17, p. 438–473.
74. Seifert, H., Cornely, O., Seggewiss, K. et al. Bloodstream infection in neutropenic cancer patients related to short-term nontunnelled catheters determined by quantitative blood cultures, differential time to positivity, and molecular epidemiological typing with pulsed-field gel electrophoresis. J. Clin. Microbiol., 2003, 41, p. 118–123.
75. Blot, F., Nitenberg, G., Chachaty, E. et al. Diagnosis of catheter-related bacteraemia: a prospective comparison of the time to positivity of hub-blood versus peripheral-blood cultures. Lancet, 1999, 354, p. 1071–1077.
76. Kite, P., Dobbins, B. M., Wilcox, M. H., McMahon, M. J. Rapid diagnosis of central-venous-catheter-related bloodstream infection without catheter removal. Lancet, 1999, 354, p. 1504–1507.
77. Bouza, E., Alvarado, N., Alcala, L. et al. A randomized and prospective study of 3 procedures for the diagnosis of catheter-related bloodstream infection without catheter withdrawal. Clin. Infect. Dis., 2007, 44, p. 820–826.
78. Bouza, E., Alvarado, N., Alcala, L. et al. A prospective, randomized, and comparative study of 3 different methods for the diagnosis of intravascular catheter colonization. Clin. Infect. Dis., 2005, 40, p. 1096–1100.
79. Maki, D. G., Weise, C. E., Sarafin, H. W. A semiquantitative culture method for identifying intravenous-catheter-related infection. N. Engl. J. Med., 1977, 296, p. 1305–1309.
80. Sherertz, R. J., Raad, I. I., Belani, A. et al. Three-year experience with sonicated vascular catheter cultures in a clinical microbiology laboratory. J. Clin. Microbiol., 1990, 28, p. 76–82.
81. Morrell, M., Fraser, V. J., Kollef, M. H. Delaying the empiric treatment of candida bloodstream infection until positive blood culture results are obtained: a potential risk factor for hospital mortality. Antimicrob. Agents Chemother., 2005, 49, p. 3640–3645.
82. Garey, K. W., Rege, M., Pai, M. P. et al. Time to initiation of fluconazole therapy impacts mortality in patients with candidemia: a multi-institutional study. Clin. Infect. Dis., 2006, 43, p. 25–31.
83. Rex, J. H., Bennett, J. E., Sugar, A. M. et al. A randomized trial comparing fluconazole with amphotericin B for the treatment of candidemia in patients without neutropenia. Candidemia Study Group and the National Institute. N. Engl. J. Med., 1994, 331, p. 1325–1330.
84. Herbrecht, R., Flückiger, U., Gachot, B. et al. 2007 update of the ECIL-1 guidelines for Antifungal therapy in leukemia patients. In 2nd European Conference on Infections in Leukemia, Edition Juan-les-Pins-France 2007.
85. Kish, M. A. Guide to development of practice guidelines. Clin. Infect. Dis., 2001, 32, p. 851–854.
86. Edwards, J. E., Jr., Bodey, G. P., Bowden, R. A. et al. International Conference for the Development of a Consensus on the Management and Prevention of Severe Candidal Infections. Clin. Infect. Dis., 1997, 25, p. 43–59.
87. Bohme, A., Ruhnke, M., Buchheidt, D. et al. Treatment of fungal infections in hematology and oncology – guidelines of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO). Ann. Hematol., 2003, 82 Suppl 2, S133–140.
88. Slavin, M. A., Szer, J., Grigg, A. P. et al. Guidelines for the use of antifungal agents in the treatment of invasive Candida and mould infections. Intern. Med. J., 2004, 34, p. 192–200.
89. Herbrecht, R., Fluckiger, U., Gachot, B. et al. Treatment of invasive Candida and invasive Aspergillus infections in adult haematological patients. Eur. J. Cancer Supplements, 2007, 5, p. 49–59.
90. Horn, D., Neofytos, D., Fishman, J. et al. Use of the PATH Alliance database to measure adherence to IDSA guidelines for the therapy of candidemia. Eur. J. Clin. Microbiol. Infect. Dis., 2007, 26, p. 907–914.
91. Patel, M., Kunz, D. F., Trivedi, V. M. et al. Initial management of candidemia at an academic medical center: evaluation of the IDSA guidelines. Diagn. Microbiol. Infect. Dis., 2005, 52, p. 29–34.
92. Anaissie, E. J., Darouiche, R. O., Abi-Said, D. et al. Management of invasive candidal infections: results of a prospective, randomized, multicenter study of fluconazole versus amphotericin B and review of the literature. Clin. Infect. Dis., 1996, 23, p. 964–972.
93. Phillips, P., Shafran, S., Garber, G. et al. Multicenter randomized trial of fluconazole versus amphotericin B for treatment of candidemia in non-neutropenic patients. Canadian Candidemia Study Group. Eur. J. Clin. Microbiol. Infect. Dis., 1997, 16, p. 337–345.
94. Kullberg, B. J., Sobel, J. D., Ruhnke, M. et al. Voriconazole versus a regimen of amphotericin B followed by fluconazole for candidaemia in non-neutropenic patients: a randomised non-inferiority trial. Lancet, 2005, 366, p. 1435–1442.
95. Anaissie, E. J., Vartivarian, S. E., Abi-Said, D. et al. Fluconazole versus amphotericin B in the treatment of hematogenous candidiasis: a matched cohort study. Am. J. Med., 1996, 101, p. 170–176.
96. Nolla-Salas, J., Sitges-Serra, A., Leon-Gil, C. et al. Candidemia in non-neutropenic critically ill patients: analysis of prognostic factors and assessment of systemic antifungal therapy. Study Group of Fungal Infection in the ICU. Intensive Care Med., 1997, 23, p. 23–30.
97. Mora-Duarte, J., Betts, R., Rotstein, C. et al. Comparison of caspofungin and amphotericin B for invasive candidiasis. N. Engl. J. Med., 2002, 347, p. 2020–2029.
98. Kuse, E. R., Chetchotisakd, P., da Cunha, C. A. et al. Micafungin versus liposomal amphotericin B for candidaemia and invasive candidosis: a phase III randomised double-blind trial. Lancet, 2007, 369, p. 1519–1527.
99. Reboli, A. C., Rotstein, C., Pappas, P. G. et al. Anidulafungin versus fluconazole for invasive candidiasis. N. Engl. J. Med., 2007, 356, p. 2472–2482.
100. Rex, J. H., Pappas, P. G., Karchmer, A. W. et al. A randomized and blinded multicenter trial of high-dose fluconazole plus placebo versus fluconazole plus amphotericin B as therapy for candidemia and its consequences in nonneutropenic subjects. Clin. Infect. Dis., 2003, 36, p. 1221–1228.
101. Graninger, W., Presteril, E., Schneeweiss, B. et al. Treatment of Candida albicans fungaemia with fluconazole. J. Infect., 1993, 26, p. 133–146.
102. Kontoyiannis, D. P., Bodey, G. P., Mantzoros, C. S. Fluconazole vs. amphotericin B for the management of candidaemia in adults: a meta-analysis. Mycoses, 2001, 44, p. 125–135.
103. Barrett, J. P., Vardulaki, K. A., Conlon, C. et al. A systematic review of the antifungal effectiveness and tolerability of amphotericin B formulations. Clin. Ther., 2003, 25, p. 1295–1320.
104. Kleinberg, M. What is the current and future status of conventional amphotericin B? Int. J. Antimicrob. Agents, 2006, 27, Suppl 1, p. 12–16.
105. Torrado, J. J., Espada, R., Ballesteros, M. P., Torrado-Santiago, S. Amphotericin B formulations and drug targeting. J. Pharm. Sci., 2008, 97, p. 2405–2425.
106. Eriksson, U., Seifert, B., Schaffner, A. Comparison of effects of amphotericin B deoxycholate infused over 4 or 24 hours: randomised controlled trial. BMJ, 2001, 322, p. 579–582.
107. Furrer, K., Schaffner, A., Vavricka, S. R. et al. Nephrotoxicity of cyclosporine A and amphotericin B-deoxycholate as continuous infusion in allogenic stem cell transplantation. Swiss Med. Wkly., 2002, 132, p. 316–320.
108. Imhof, A., Walter, R. B., Schaffner, A. Continuous infusion of escalated doses of amphotericin B deoxycholate: an open-label observational study. Clin. Infect. Dis., 2003, 36, p. 943–951.
109. Peleg, A. Y., Woods, M. L. Continuous and 4 h infusion of amphotericin B: a comparative study involving high-risk haematology patients. J. Antimicrob. Chemother., 2004, 54, p. 803–808.
110. Wingard, J. R., Kubilis, P., Lee, L. et al. Clinical significance of nephrotoxicity in patients treated with amphotericin B for suspected or proven aspergillosis. Clin. Infect. Dis., 1999, 29, p. 1402–1407.
111. Bates, D. W., Su, L., Yu, D. T. et al. Mortality and costs of acute renal failure associated with amphotericin B therapy. Clin. Infect. Dis., 2001, 32, p. 686–693.
112. Bates, D. W., Su, L., Yu, D. T. et al. Correlates of acute renal failure in patients receiving parenteral amphotericin B. Kidney Int., 2001, 60, p. 1452–1459.
113. Mayer, J., Doubek, M., Doubek, J. et al. Reduced nephrotoxicity of conventional amphotericin B therapy after minimal nephroprotective measures: animal experiments and clinical study. J. Infect. Dis., 2002, 186, p. 379–388.
114. Mayer, J., Doubek, M., Vorlicek, J. Must we really fear toxicity of conventional amphotericin B in oncological patients? Support. Care Cancer, 1999, 7, p. 51–55.
115. Johnson, J. R. Reduction of nephrotoxicity associated with amphotericin B deoxycholate. Clin. Infect. Dis., 2004, 38, p. 303; author reply p. 306–307.
116. Ito, J. I., Hooshmand-Rad, R. Treatment of Candida infections with amphotericin B lipid complex. Clin. Infect. Dis., 2005, 40, Suppl 6, S384–391.
117. Anaissie, E. J., White, M. H., Uzun, O. et al. Amphotericin B Lipid Complex vs Amphotericin B for Treatment of invasive Candidiasis: A Prospective, Randomized Multicenter Trial. In ICAAC 35th, Interscience Conference on Antimicrobial Agents and Chemotherapy, Edition San Francisco: 1995.
118. Noskin, G., Pietrelli, L., Gurwith, M., Bowden, R. Treatment of invasive fungal infections with amphotericin B colloidal dispersion in bone marrow transplant recipients. Bone Marrow Transplant, 1999, 23, p. 697–703.
119. Noskin, G. A., Pietrelli, L., Coffey, G. et al. Amphotericin B colloidal dispersion for treatment of candidemia in immunocompromised patients. Clin. Infect. Dis., 1998, 26, p. 461–467.
120. Walsh, T. J., Hiemenz, J. W., Seibel, N. L. et al. Amphotericin B lipid complex for invasive fungal infections: analysis of safety and efficacy in 556 cases. Clin. Infect. Dis., 1998, 26, p. 1383–1396.
121. Tuil, O., Cohen, Y. Itraconazole IV solution in the treatment of candidemia in non-neutropenic patients. Critical Care Medicine, 2003, 7, P131–P132.
122. Ostrosky-Zeichner, L., Kontoyiannis, D., Raffalli, J. et al. International, open-label, noncomparative, clinical trial of micafungin alone and in combination for treatment of newly diagnosed and refractory candidemia. Eur. J. Clin. Microbiol. Infect. Dis., 2005, 24, p. 654–661.
123. Abbas, J., Bodey, G. P., Hanna, H. A. et al. Candida krusei fungemia. An escalating serious infection in immunocompromised patients. Arch. Intern. Med., 2000, 160, p. 2659–2664.
124. Safdar, A., Chaturvedi, V., Cross, E. W. et al. Prospective study of Candida species in patients at a comprehensive cancer center. Antimicrob. Agents. Chemother., 2001, 45, p. 2129–2133.
125. Safdar, A., van Rhee, F., Henslee-Downey, J. P. et al. Candida glabrata and Candida krusei fungemia after high-risk allogeneic marrow transplantation: no adverse effect of low-dose fluconazole prophylaxis on incidence and outcome. Bone Marrow Transplant., 2001, 28, p. 873–878.
126. Bodey, G. P,, Mardani, M., Hanna, H. A. et al. The epidemiology of Candida glabrata and Candida albicans fungemia in immunocompromised patients with cancer. Am. J. Med., 2002, 112, p. 380–385.
127. Safdar, A., Chaturvedi, V., Koll, B. S. et al. Prospective, multicenter surveillance study of Candida glabrata: fluconazole and itraconazole susceptibility profiles in bloodstream, invasive, and colonizing strains and differences between isolates from three urban teaching hospitals in New York City (Candida Susceptibility Trends Study, 1998 to 1999). Antimicrob. Agents Chemother., 2002, 46, p. 3268–3272.
128. Safdar, A., Perlin, D. S., Armstrong, D. Hematogenous infections due to Candida parapsilosis: changing trends in fungemic patients at a comprehensive cancer center during the last four decades. Diagn. Microbiol. Infect. Dis., 2002, 44, p. 11–16.
129. Bennett, J. E., Izumikawa, K., Marr, K. A. Mechanism of increased fluconazole resistance in Candida glabrata during prophylaxis. Antimicrob. Agents Chemother., 2004, 48, p. 1773–1777.
130. Pfaller, M. A., Messer, S. A., Boyken, L. et al. Geographic variation in the susceptibilities of invasive isolates of Candida glabrata to seven systemically active antifungal agents: a global assessment from the ARTEMIS Antifungal Surveillance Program conducted in 2001 and 2002. J. Clin. Microbiol., 2004, 42, p. 3142–3146.
131. Panackal, A. A., Gribskov, J. L., Staab, J. F. et al. Clinical significance of azole antifungal drug cross-resistance in Candida glabrata. J. Clin. Microbiol., 2006, 44, p. 1740–1743.
132. Herbrecht, R., Denning, D. W., Patterson, T. F. et al. Voriconazole versus amphotericin B for primary therapy of invasive aspergillosis. N. Engl. J. Med., 2002, 347, p. 408–415.
Labels
Anaesthesiology, Resuscitation and Inten Intensive Care Medicine
Article was published inAnaesthesiology and Intensive Care Medicine

2009 Issue 1-
All articles in this issue
- Robot-assisted laparoscopic surgery from the anaesthesiologist’s perspective
- Paediatric intensive care outcomes in the Czech Republic in 2007
- The importance of tidal volume and its monitoring during high-frequency ventilation
- Dosage and administration of antibiotics in critically ill patients
- Guidelines for the treatment of invasive fungal infections in immunocompromised patients
- Guidelines for the treatment of invasive candidiasis
- Guidelines for the treatment of invasive aspergillosis
- Anaesthesiology and Intensive Care Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Dosage and administration of antibiotics in critically ill patients
- Robot-assisted laparoscopic surgery from the anaesthesiologist’s perspective
- The importance of tidal volume and its monitoring during high-frequency ventilation
- Guidelines for the treatment of invasive candidiasis
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

