-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Antitrombotická léčba a digestivní endoskopie
Antithrombotic therapy and digestive endoscopy
Antithrombotic therapy and digestive endoscopy Antithrombotic therapy comprises anticoagulation and antiplatelet treatment. The number of patients treated with various forms of antithrombotic therapy is growing. Procedures of digestive endoscopy are very frequently indicated by general practitioners and doctors of various specialisations. Interdisciplinary cooperation and mutual understanding are required in order for digestive endoscopy to be effective and safe. Hence, we present an overview based on recent European, British (1), and North American guidelines (2) for endoscopic procedures, with respect to guidelines for perioperative care in general (3).
Antithrombotic therapy management in patients undergoing digestive endoscopy procedures is based on individual consideration of postprocedural bleeding (particularly a delayed one) on one hand, and thromboembolic risk on the other hand, ideally in cooperation with the physician prescribing antithrombotic therapy. Despite all efforts, patients taking antithrombotic medication are at a higher risk of postprocedural bleeding in comparison with those without this risk; this fact should be accepted by attending physicians and patients should be informed of it. Postprocedural bleeding is mostly manageable with a subsequent endoscopic procedure. By contrast, cerebral and cardiovascular thromboembolic complications are often life-threatening and not uncommonly disabling. One should always consider postponing an elective procedure in a patient with temporary antithrombotic therapy (after pulmonary embolism or after coronary stent insertion).
Basic principles of administration of antithrombotic therapy in the context of an endoscopic procedure are described in Table 1. Digestive endoscopy procedures can be categorized according to postprocedural bleeding risk (Table 2). Postprocedural bleeding risk can be specifically reduced in some procedures (ERCP with papillary balloon dilation instead of sphincterotomy, mechanical securing of polypectomy base, etc.).
Acetylsalicylic acid administered as secondary prevention (primary preventive indications are very narrow nowadays) should not be discontinued perioperatively (discontinuation is associated with an approximately threefold increase in thrombotic complications!). The riskiest procedures are the only exception in which discontinuation is explicitly requested by the digestive endoscopist. Reduction of dual antiplatelet therapy is better abandoned in high-risk patients – particularly those with recently implanted coronary stents (Table 3) – and postponement of an elective procedure should always be considered.
Bridging of warfarin with low-molecular-weight heparin (LMWH) is not indicated routinely (in some cases, this practice increases the bleeding risk). Bridging with LMWH is appropriate in patients with high (or moderate) thromboembolic risk (Table 5). Furthermore, LMWH therapy carries specific risks, particularly in patients with renal function impairment (Table 4). In patients with a high thromboembolic risk, a statement of the physician indicating anticoagulation is always appropriate before an elective procedure (Table 6).
Direct oral anticoagulants (DOACs) should not be administered on the day of the procedure, not even in one with a low risk (e.g., biopsy); a longer withdrawal is recommended in high-risk procedures (this cessation should not be bridged with LMWH given the rapid onset and elimination half-time) (Table 7).
Recommencement of antithrombotic therapy after a high-risk endoscopic procedure should always be determined by the endoscopist and the recommended intervals should be considered minimal: 1–2 days after the procedure in the case of P2Y12 inhibitors; 2–3 days after the procedure in the case of DOACs; in the evening of the day of the procedure for warfarin with a maintenance (not saturation) dose; and 48 hours after the procedure in the case of LMWH at a therapeutic dose. Earlier administration of a lower-than-therapeutic dose of LMWH (twice a day per weight) can be considered in this context: prophylactic (once a day) or higher prophylactic (once a day per weight) doses. In general, a full anticoagulation effect should not be achieved earlier than approximately 48 hours after the procedure.
The patient should be properly informed of the course of antithrombotic therapy before and after the endoscopic procedure, including a written form (a calendar can be downloaded online for this purpose)
Keywords:
Antiplatelet therapy – direct oral anticoagulants – anticoagulation therapy – antithrombotic therapy – digestive endoscopy – postprocedural bleeding
Autoři: Jiří Cyrany 1; Radovan Malý 2; Stanislav Rejchrt 1; Ilja Tachecí 1
Působiště autorů: II. interní gastroenterologická klinika, Lékařská fakulta Univerzity Karlovy a Fakultní nemocnice Hradec Králové 1; I. interní kardioangiologická klinika, Lékařská fakulta Univerzity Karlovy a Fakultní nemocnice Hradec Králové 2
Vyšlo v časopise: Vnitř Lék 2022; 68(8): 538-542
Kategorie: Ve zkratce
doi: https://doi.org/10.36290/vnl.2022.113Souhrn
Antitrombotická léčba zahrnuje léčbu antikoagulační a protidestičkovou. Pacientů léčených různými formami antitrombotické terapie přibývá. Výkony digestivní endoskopie jsou velmi často indikovány praktickými lékaři a specialisty jiných odborností než gastroenterologie. Efektivita a bezpečnost digestivní endoskopie proto vyžaduje v tomto bodě mezioborovou spolupráci a vzájemné porozumění – proto nabízíme stručný přehled zpracovaný dle aktuálních doporučení evropských, britských (1) a severoamerických (2) pro endoskopické výkony, se zohledněním doporučení pro perioperační péči obecně (3).
Vedení antitrombotické terapie u pacientů podstupujících výkon digestivní endoskopie je dáno individuálním vážením rizika krvácení (především odloženého) v souvislosti s výkonem na straně jedné; proti riziku tromboembolické komplikace na straně druhé; nejlépe ve spolupráci s lékařem indikujícím antitrombotickou terapii. Přes veškerou snahu mají nemocní užívající antitrombotickou medikaci v souvislosti s endoskopickým výkonem vyšší riziko krvácení než pacienti bez této terapie – toto by měli ošetřující lékaři akceptovat a pacienti by o tom měli být poučeni. Krvácení po digestivní endoskopii je většinou zvladatelné dalším endoskopickým výkonem. Naproti tomu cerebrální a kardiovaskulární tromboembolické komplikace často ohrožují život a jsou nezřídka invalidizující. Je vhodné vždy zvážit odložení elektivního výkonu u pacienta s dočasnou antitrombotickou terapií (po plicní embolii, po zavedení koronárního stentu).
Základní pravidla podávání antitrombotické terapie v souvislosti s endoskopickým výkonem popisuje tabulka 1. Výkony digestivní endoskopie lze empiricky rozdělit dle rizika krvácení po výkonu (Tab. 2). Riziko postprocedurálního krvácení lze u některých endoskopických procedur snížit (ERCP s balónovou dilatací papily místo sfinkterotomie, mechanické zajištění stopky před nebo po polypektomii apod.).
Kyselina acetylsalicylová podávaná v indikaci sekundární prevence (primárně preventivní indikace jsou v současnosti velmi úzké) nemá být v souvislosti s endoskopickým výkonem vysazována (vysazení je spojeno s přibližně trojnásobným nárůstem trombotických komplikací!). Výjimkou jsou jen procedury s nejvyšším rizikem, kde si vysazení výslovně vyžádá digestivní endoskopista.
Redukci duální antiagregační terapie je vhodné se vyhnout u vysokorizikových pacientů – především časně po implantaci koronárního stentu (Tab. 3) – vždy zvažujeme odložení elektivní procedury.
Přemostění vysazeného warfarinu pomocí nízkomolekulárního heparinu (LMWH) není indikováno rutinně (v některých případech tento postup významně zvyšuje riziko krvácení). Vhodné je přemostění pomocí LMWH u pacientů s vysokým (případně středním) tromboembolickým rizikem (Tab. 5). LMWH navíc přináší specifická rizika zvláště u pacientů s poruchou ledvinných funkcí (Tab. 4) (4). U pacientů s vysokým tromboembolickým rizikem je před elektivním výkonem vždy vhodné vyjádření lékaře indikujícího antikoagulaci.
Terapie přímými orálními antikoagulancii (DOAC) by neměla být podávána v den výkonu ani před procedurami s nízkým rizikem krvácení (např. biopsie), delší vysazení je doporučeno u vysokorizikových procedur (toto vysazení nemá být přemosťováno LMWH vzhledem k rychlému nástupu účinku a poločasu eliminace DOAC, Tab. 7) (5).
Znovunasazení antitrombotické terapie po endoskopickém výkonu s vysokým rizikem by měl vždy určit endoskopující lékař, doporučené intervaly nutno považovat za minimální: v případě P2Y12 inhibitorů za 1–2 dny po výkonu, v případě warfarinu večer v den výkonu udržovací (nikoliv saturační) dávkou, v případě DOAC za 2–3 dny po výkonu a v případě LMWH v terapeutické dávce 48 hodin po výkonu. Dříve lze zvážit podání nižší než terapeutické dávky LMWH (2× denně dle hmotnosti): profylaktickou (jednou denně) nebo vyšší profylaktickou dávku (jednou denně dle hmotnosti). Obecně by terapeutické úrovně antikoagulace nemělo být dosaženo dříve než za cca 48 hodin od výkonu (Tab. 6).
Pacient by měl být o podávání antitrombotik před a po endoskopickém výkonu řádně poučen včetně písemné formy (kalendář ke stažení on ‑ line – https://www.cgs-cls.cz/antitromboticka-terapie-a-endoskopicky-vykon/).
Klíčová slova:
antikoagulační terapie – protidestičková léčba – přímá orální antikoagulancia – antitrombotická terapie – digestivní endoskopie – povýkonové krvácení
Tab. 1. Přehled úprav antitrombotické terapie u pacienta podstupujícího endoskopický výkon 
1předpokládaná indikace sekundární prevence; vysazení zvážit jen na žádost endoskopisty 7 dní před výkony s velmi vysokým rizikem např. ampulektomie; EMR/ESD v horním GIT a rozsáhlé
2cave nemocní s vysokým trombotickým rizikem – viz tabulka 3
3déle u nemocných s vyšším cílovým INR, s velmi nízkou dávkou warfarinu a vysokého věku s komorbiditami
4indikace přemostění (bridging) u vysokorizikových nemocných – viz tabulka 5
5zvážit prodloužení intervalu u LMWH určeného k podávání jednou denně (FORTE)
Seznam zkratek: ASA – acetylsalicylová kyselina; P2Y12i – inhibitor receptoru P2Y12 (clopidogrel, prasugrel, ticagrelor); DAPT – duální protidestičková terapie; DOAC – přímá orální antikoagulancia (apixaban, edoxaban, rivaroxaban, dabigatran); GF – glomerulární filtrace; INR – international normalized ratio; LMWH – nízkomolekulární heparin; GIT – gastrointestinální traktTab. 2. Empirická stratifikace procedur dle rizika krvácení 
Zkratky: PEG – perkutánní endoskopická gastrostomie; PEJ – perkutánní endoskopická jejunostomie; EMR – endoskopická slizniční resekce; ESD – endoskopická submukózní disekce; ERCP – endoskopická retrográdní cholangiopankreatografie; EUS – endoskopická ultrasonografie; APC – argonová plasmakoagulace; POEM – perorální endoskopická myotomie
Upraveno dle: Abraham NS et al. ACG-CAG clinical practice guideline: management of anticoagulants and antiplatelets during acute gastrointestinal bleeding and the periendoscopic period. Am J Gastroenterol 2022;117:542-558.Tab. 3. Pacient s vysokým rizikem trombózy při vysazení duální antiagregační terapie 
*možno zohlednit také počet, délku a lokalizaci stentu
Upraveno dle: Douketis JD et al. Perioperative management of antithrombotic therapy: an American College of Chest Physicians clinical practice guideline executive summary. Chest 2022, doi: https://doi.org/10.1016.j.chest.2022.08.004Tab. 4. Podávání nízkomolekulárního heparinu s ohledem na renální funkce 
1UFH přerušit 4 hodiny před výkonem, nasadit zpět ≥ 24 hodin po výkonu
2< cca 50 kg, těžká obezita
3děti, > 80 let (terapeutické dávky)
Seznam zkratek: GF – glomerulární filtrace; UFH – nefrakcionovaný heparin, BMI-body mass index
Upraveno dle: SÚKL. Clexane. SPC – Souhrn údajů o přípravku.Tab. 5. Přemostění (bridging) při vysazení warfarinu pomocí nízkomolekulárního heparinu. Přemostění (bridging) při vysazení warfarinu (nikoliv DOAC) pomocí LMWH je indikováno dle tromboembolického rizika (indikováno u vysokého a neindikováno u nízkého rizika, k individuálnímu zvážení u středního rizika) 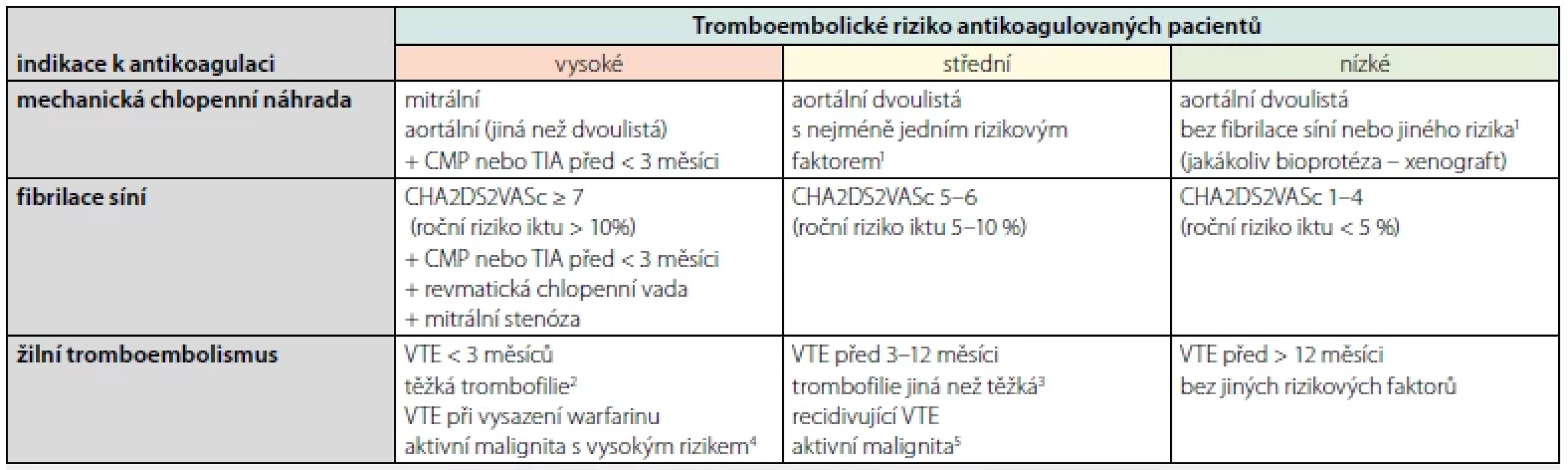
1fibrilace síní, anamnéza CMP nebo TIA, arteriální hypertenze, diabetes mellitus, městnavé srdeční selhání, věk > 75 let
2např. deficit proteinu C, proteinu S nebo antitrombinu, homozygot mutace faktoru V Leiden nebo mutace protrombinového genu nebo smíšený heterozygot těchto mutací, antifosfolipidový syndrom, mnohočetné abnormality
3např. heterozygot mutace faktoru V Leiden nebo protrombinu
4karcinom jícnu, žaludku, pankreatu, myeloproliferativní onemocnění a primární mozkový nádor
5léčba v posledních 6 měsících nebo paliativní péče (zvláště během aktivní léčby a při metastatickém postižení)
Seznam zkratek: LMWH – nízkomolekulární heparin; DOAC – přímé orální antikoagulans; CMP – cévní mozková příhoda; TIA – tranzitorní ischemická ataka; CHA2DS2VASc – skóre rizika iktu při fibrilaci síní; VTE – venózní tromboembolismus (žilní trombóza a/nebo plicní embolie)
Upraveno dle: Abraham NS et al. ACG-CAG clinical practice guideline: management of anticoagulants and antiplatelets during acute gastrointestinal bleeding and the periendoscopic period. Am J Gastroenterol 2022;117:542-558.Tab. 6. Podávání antitrombotické terapie před a po endoskopickém výkonu s vysokým rizikem krvácení 
Postup po endoskopickém výkonu určuje endoskopista ve spolupráci s odborností indikující antitrombotikum.
Plné antikoagulace by nemělo být dosaženo dříve než za 48 hodin!
1warfarin v udržovací (nikoli saturační) dávce
2LMWH přemostění warfarinu pouze v případě vysokého tromboembolického rizika
3terapeutická dávka LMWH ne dříve než za 48 h, dříve možno podávat nižší dávku
4LMWH podávat do účinného INR
5dabigatran při GF 30-50 ml/min vysadit 4 dny
6u vybraných pacientů s vysokým trombotickým rizikem možno během prvních 48 hodin použít nízké dávky LMWH
Seznam zkratek: ASA – acetylsalicylová kyselina; P2Y12i – inhibitor receptoru P2Y12 (clopidogrel, prasugrel, ticagrelor); INR – international normalized ratio; LMWH – nízkomolekulární heparin; DOAC – přímá orální antikoagulancia (apixaban, edoxaban, rivaroxaban, dabigatran)
Upraveno dle: Douketis JD et al. Perioperative management of antithrombotic therapy: an American College of Chest Physicians clinical practice guideline executive summary. Chest 2022, doi: https://doi.org/10.1016.j.chest.2022. 08. 004Tab. 7. Základní farmakodynamické parametry antitrombotik 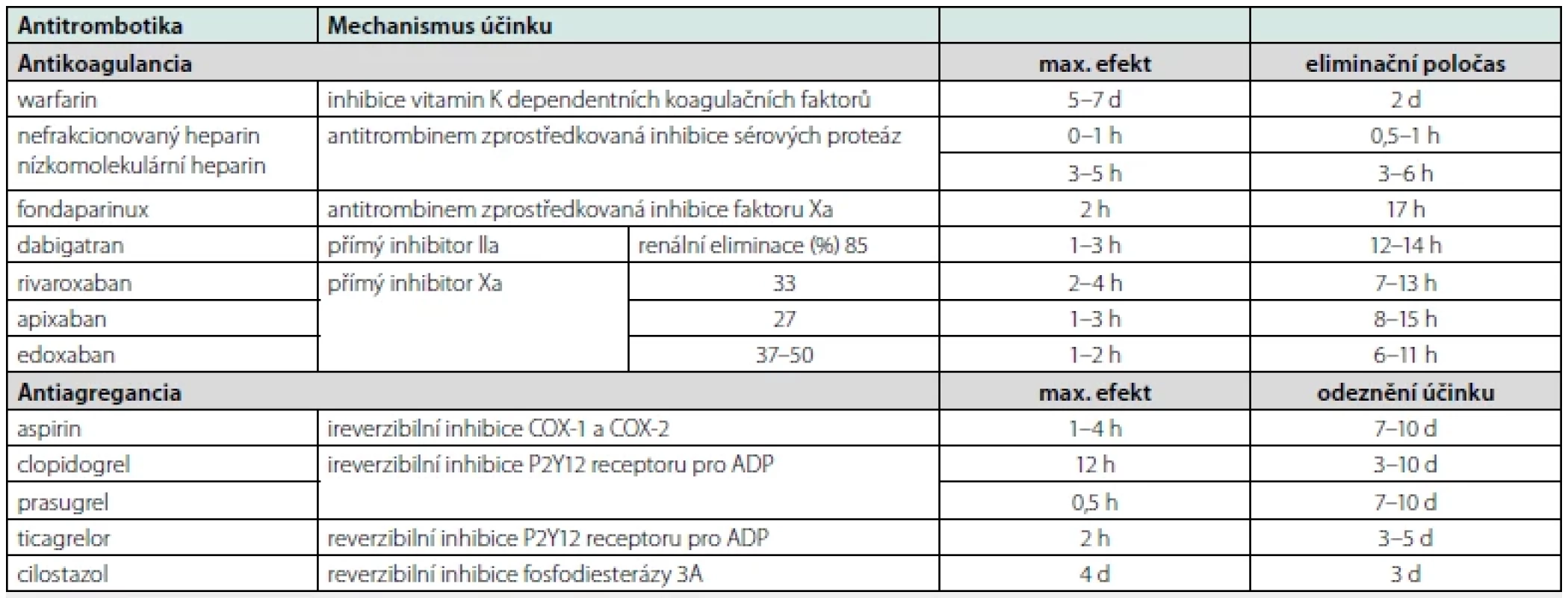
Upraveno dle: Ortel TL. Perioperative management of patients on chronic antithrombotic therapy. Blood 2012;120:4699-4705. Halvorsen S, Mehilli J et al. 2022 ESC guidelines on cardiovascular assessment and management of patients undergoing non-cardiac surgery. Eur Heart J 2022;43:3826-3924. Dedikace: Tento výstup vznikl v rámci programu Cooperatio, vědní oblast CARD.
KORESPONDENČNÍ ADRESA AUTORA:
MUDr. Jiří Cyrany, Ph.D.
jiri.cyrany@fnhk.cz
Fakultní nemocnice Hradec Králové, 2. interní gastroenterologická klinika
Sokolská 581, 500 05 Hradec KrálovéCit. zkr: Vnitř Lék. 2022;68(8):538-542
Článek přijat redakcí: 22. 9. 2022
Článek přijat po recenzích: 10. 11. 2022
Zdroje
1. Veitch AM et al. Endoscopy in patients on antiplatelet or anticoagulant therapy: BSG and ESGE guideline update. Endoscopy. 2021;53 : 947-69.
2. Abraham NS et al. ACG‑CAG clinical practice guideline: management of anticoagulants and antiplatelets during acute gastrointestinal bleeding and the periendoscopic period. Am J Gastroenterol. 2022;117 : 542-558.
3. Douketis JD et al. Perioperative management of antithrombotic therapy: an American College of Chest Physicians clinical practice guideline executive summary. Chest. 2022;162:E207-E243.
4. Státní ústav pro kontrolu léčiv. Clexane, SPC – Souhrn údajů o přípravku. https://www.sukl. cz/modules/medication/download.php?file=SPC182993.pdf & type=spc & as=clexane‑spc.
5. Ortel TL. Perioperative management of patients on chronic antithrombotic therapy. Blood. 2012;120 : 4699-4705.
6. Halvorsen S, Mehilli J et al. 2022 ESC guidelines on cardiovascular assessment and management of patients undergoing non‑cardiac surgery. Eur Heart J. 2022;43 : 3826-3924.
Štítky
Diabetologie Endokrinologie Interní lékařství
Článek vyšel v časopiseVnitřní lékařství
Nejčtenější tento týden
2022 Číslo 8- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- S prof. Vladimírem Paličkou o racionální suplementaci kalcia a vitaminu D v každodenní praxi
-
Všechny články tohoto čísla
- Hlavní téma – Hematologie
- Dnešní pohled na dědičné trombofilie
- Venózní tromboembolismus u antifosfolipidového syndromu
- Vybrané závažné „hematologické“ syndromy u dospělých pacientů v intenzivní péči
- Vývoj léčby žilní trombózy od pijavic k mechanické trombektomii
- Tradiční a nové biomarkery kongesce u srdečního selhání
- Alergenová imunoterapie v léčbě alergického eozinofilního astmatu
- Plicní střádání
- Porucha kognitivních funkcí a hrozba pandemie demence aneb cesta hypertoniků k nesoběstačnosti
- Antitrombotická léčba a digestivní endoskopie
- Jak dobře jsme léčili hypertenzi v posledních 25 letech?
- Vnitřní lékařství
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Vybrané závažné „hematologické“ syndromy u dospělých pacientů v intenzivní péči
- Dnešní pohled na dědičné trombofilie
- Alergenová imunoterapie v léčbě alergického eozinofilního astmatu
- Antitrombotická léčba a digestivní endoskopie
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



