-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Další linie cílené léčby u nemocných s metastatickým renálním karcinomem s progresí na léčbě pazopanibem: expertní stanovisko České kooperativní skupiny pro metastatický renální karcinom
Autoři: T. Büchler 1; J. Fínek 2; J. Hájek 3; I. Kocák 4; K. Kubáčková 5; R. Lakomý 4; B. Melichar 6; L. Petruželka 7; A. Poprach 4; I. Puzanov 8; H. Šiffnerová 9; J. Tomášek 4
; R. Vyzula 4; M. Zemanová 7
Působiště autorů: Onkologická klinika 1. LF UK a Thomayerovy nemocnice, Praha 1; Onkologické a radioterapeutické oddělení FN Plzeň 2; Klinika onkologická FN Ostrava 3; Klinika komplexní onkologické péče, Masarykův onkologický ústav, Brno 4; Radioterapeuticko-onkologické oddělení FN Motol, Praha 5; Onkologická klinika FN Olomouc a LF UP Olomouc 6; Onkologická klinika 1. LF UK a Všeobecné fakultní nemocnice, Praha 7; Division of Hematology-Oncology, Vanderbilt University Medical Center, Nashville, USA 8; Onkologické oddělení Nemocnice České Budějovice 9
Vyšlo v časopise: Klin Onkol 2013; 26(1): 55-57
Kategorie: Aktuality v onkologii
Úvod
Pazopanib (Votrient) je registrován pro první linii léčby metastatického renálního karcinomu (mRCC) pro pacienty s dobrou a střední prognózou a pro druhou linii léčby u nemocných s progresí na léčbě cytokiny. Je tyrozinkinázovým inhibitorem (TKI) s účinností hlavně na receptory VEGFR (Vascular Endothelial Growth Factor Receptor)-1, -2 a -3, PDGFR (Platelet-Derived Growth Factor Receptor) a c-kit. Doporučená dávka pazopanibu je 800 mg perorálně jednou denně. Ve studii fáze III prodloužil pazopanib signifikantně přežití bez progrese (PFS) ve srovnání s placebem (9,2 vs 4,2 měsíce HR (95% CI) = 0,46 (0,34–0,62)) [1]. Podle nedávno zveřejněných výsledků studie COMPARZ je pazopanib v první linii léčby ekvivalentní dalšímu TKI sunitinibu (Sutent) z hlediska léčebných výsledků (PFS pazopanib 8,4 měsíce, sunitinib 9,5 měsíce, HR (95% CI) = 1,047 (0,898–1,22)) a výhodnější v řadě parametrů z hlediska toxicity [2]. Studie COMPARZ a další randomizovaná studie PISCES dále prokázaly lepší subjektivní snášenlivost pazopanibu ve srovnání se sunitinibem [3]. Léčbu pazopanibem zahajujeme v dávce 800 mg jednou denně (IB) [1]. Zahájení nižší dávkou s postupnou titrací nemá oporu v randomizovaných studiích.
Možnosti terapie po progresi na pazopanibu a důkazy z klinických studií
V České republice je pazopanib dostupný od roku 2011 a podle poslední aktualizace registru RENIS jím bylo nebo je léčeno 111 pacientů s mRCC [4]. Většina z těchto nemocných je při progresi schopna další cílené terapie. Dosud nemáme k dispozici výsledky randomizovaných studií, na nichž by bylo možné postavit doporučení pro další cílenou terapii u nemocných progredujících na pazopanibu. Úhradový dodatek Státního ústavu pro kontrolu léčiv (SÚKL) rovněž neposkytuje vodítko pro sekvenční terapii v této situaci [5].
Zásadními randomizovanými studiemi sekvenčním terapie jsou studie RECORD-1 a studie AXIS [6,7].
Podklad pro indikaci perorálního inhibitoru mTOR (Mammalian Target Of Rapamycin) everolimu (Afinitor) u pacientů s nádory progredujícími při léčbě TKI přinesla randomizovaná studie fáze III RECORD-1. V této studii byl everolimus srovnáván s placebem u pacientů se světlebuněčným mRCC po progresi na léčbě sunitinibem, multikinázovým inhibitorem sorafenibem (Nexavar) nebo oběma jmenovanými cílenými léky. Část pacientů byla navíc předléčena cytokiny a/nebo bevacizumabem (Avastin), protilátkou proti VEGF. Překřížení (cross-over) z ramene s placebem do aktivního ramene po progresi bylo povoleno a tuto možnost využilo až 76 % pacientů. Studie prokázala prodloužení přežití bez progrese u pacientů léčených everolimem, ale možná i vzhledem ke značnému překřížení ramen se nepodařilo prokázat prodloužení celkového přežití [6,8].
Axitinib (Inlyta) je velmi potentní tyrozinkinázový inhibitor druhé generace s účinností na VEGFR-1, -2 a -3, PDGFR a c-kit. Iniciální dávka axitinibu je 5 mg per os dvakrát denně s možností eskalace až na 10 mg dvakrát denně u pacientů, u nichž nenastala dekompenzace hypertenze nebo jiné závažné nežádoucí účinky. Do studie AXIS, která se stala podkladem pro registraci axitinibu, byli zařazováni nemocní po předchozí léčbě sunitinibem, bevacizumabem, cytokiny nebo temsirolimem. Axitinib prodlužoval PFS více než sorafenib, i když nikoli v podskupinách nemocných předléčených bevacizumabem nebo temsirolimem (obě kohorty byly však velmi malé) [7].
Z hlediska současných poznatků o systémové terapii mRCC je několik možností následující terapie pacientů s progresí na pazopanibu, jejichž stav umožňuje a vyžaduje systémovou léčbu (tab. 1). U této léčby je kromě důkazů ve smyslu medicíny založené na důkazech nutné posuzovat i možnost úhrady dané léčby v klinické praxi v ČR.
Tab. 1. Výhody a nevýhody sekvenční léčby jednotlivými cílenými léky u pacientů s progresí na léčbě pazopanibem. 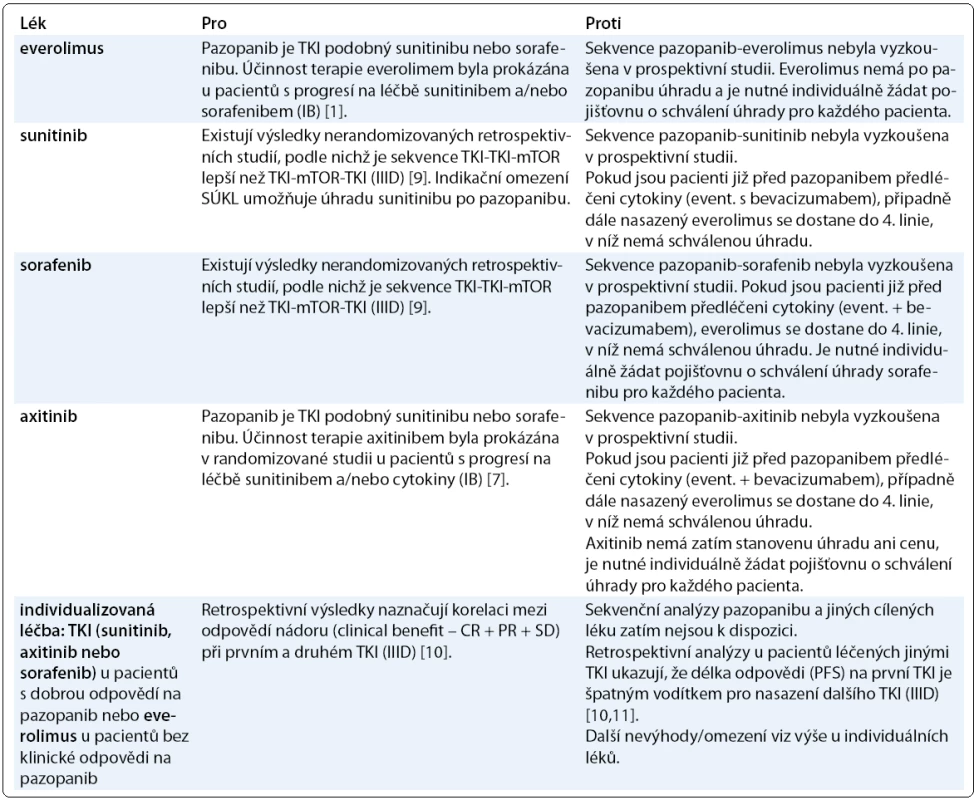
Doporučení expertů
U nemocných s mRCC by mělo být vždy preferenčně zvažováno zařazení do klinické studie.
Všechna níže uvedená doporučení jsou úrovně stupně E (založené na důkazech úrovně IV a V), pokud není uvedeno jinak. Léky označené * nemají v této situaci úhradu a je nutné o jejich úhradu u konkrétního pacienta žádat příslušnou zdravotní pojišťovnu.
- U nemocných, kteří dosáhnou během terapie pazopanibem stabilizaci onemocnění nebo regrese nádoru (hodnoceno podle restagingu po třech měsících léčby), lze doporučit ve druhé linii nasazení jiného tyrozinkinázového inhibitoru - sunitinibu nebo axitinibu* (možnost podání sorafenibu* v této indikaci je při kontraindikacích sunitinibu a axitinibu).
- Při další progresi (tj. po dvou TKI, z nichž jeden je sunitinib nebo sorafenib) je doporučena terapie everolimem (IB).
- U nemocných s prokázanou progresí po třech měsících léčby pazopanibem lze doporučit ve druhé linii nasadit everolimus*.
- U nemocných s progresí po pazopanibu a everolimu je možno zvážit další linii léčby některým TKI (sunitinib*, axitinib*).
Tab. 2. Stupně doporučení a úrovně důkazů podle zásad medicíny založené na důkazech. 
TB, BM, JT a MZ dostali honoráře za přednášky, publikace a konzultace do společností GSK, Pfizer, Novartis a Bayer.
TB, BM, JT and MZ received lecture, publication and consultation honoraria from GSK, Pfizer, Novartis and Bayer.
doc. MUDr. Tomáš Büchler, Ph.D.
Onkologická klinika 1. LF UK a Thomayerovy nemocnice
Vídeňská 800140 59 Praha
e-mail: tomas.buchler@ftn.cz
Zdroje
1. Sternberg CN, Davis ID, Mardiak J et al. Pazopanib in locally advanced or metastatic renal cell carcinoma: results of a randomized phase III trial. J Clin Oncol 2010; 28(6): 1061–1068.
2. Motzer R, Hudson TE, Reeves J et al. Randomized, open-label, phase III trial of pazopanib versus sunitinib in first-line treatment of patients with metastatic renal cell carcinoma (mRCC): results of the COMPARZ trial. Presented at: 2012 European Society for Medical Oncology; Vienna, Austria; October 1, 2012. Abstract LBA 8.
3. Escudier B, Porta C, Bono B et al. Patient preference between pazopanib and sunitinib: Results of a randomized double-blind, placebo-controlled, cross-over study in patients with metastatic renal cell carcinoma – PISCES study, NCT 01064310. ASCO 2012; Abstract CRA4502.
4. Hejduk K, Brabec P, Borlíček Z et al. Analytický report z klinického registru Renis (Votrient/pazopanib) k 8.10.2012. http://www.linkos.cz/prehled-registru/klinicky-registr-renis-1/#Votrient (přístup 14. 11. 2012).
5. SÚKL. http://www.sukl.cz/modules/medication/ (přístup 14. 12. 2012).
6. Motzer RJ, Escudier B, Oudard S et al. Efficacy of everolimus in advanced renal cell carcinoma: a double--blind, randomised, placebo-controlled phase III trial. Lancet 2008; 372(9637): 449–456.
7. Rini BI, Escudier B, Tomczak P et al. Comparative effectiveness of axitinib versus sorafenib in advanced renal cell carcinoma (AXIS): a randomised phase 3 trial. Lancet 2011; 378(9807): 1931–1939.
8. Motzer RJ, Escudier B, Oudard S et al. Phase 3 trial of everolimus for metastatic renal cell carcinoma: final results and analysis of prognostic factors. Cancer 2010; 116(18): 4256–4265.
9. Iacovelli R, Santoni M, Di Lorenzo et al. Progression free survival (PFS) and overall survival (OS) in patients receiving 3 targeted therapies (TTs) for metastatic renal-cell carcinoma (mRCC). Ann Oncol 2012; 23 (Suppl 9). Abstract 818P.
10. Büchler T, Pavlik T, Bortlicek Z et al. Objective response and time to progression on sequential treatment with sunitinib and sorafenib in metastatic renal cell carcinoma. Med Oncol 2012; 29(5): 3321–3324.
11. Al-Marrawi MY, Rini BI, Harshman LC et al. The association of clinical outcome to front-line VEGF-targeted therapy with clinical outcome to second-line VEGF-targeted therapy in metastatic renal cell carcinoma (mRCC) patients (Pts). J Clin Oncol 2011; 29 (Suppl): A 4555.
Štítky
Dětská onkologie Chirurgie všeobecná Onkologie
Článek Chirurgie plicních metastázČlánek Editorial
Článek vyšel v časopiseKlinická onkologie
Nejčtenější tento týden
2013 Číslo 1- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Nejasný stín na plicích – kazuistika
- Metamizol v léčbě různých bolestivých stavů – kazuistiky
-
Všechny články tohoto čísla
- Inhibitory proteazomu v léčbě mnohočetného myelomu
- Germinatívne nádory pineálnej oblasti: prehľad
- Molekulárně biologická diagnostika mutací genu KRAS a BRAF u pacientů s kolorektálním karcinomem – zkušenosti laboratorního pracoviště
- Primární rakovina žlučníku diagnoastikovaná pooperačně po elektivní a hospitalizační cholecystektomii
- Chirurgie plicních metastáz
- Maligní melanom léčený intenzivní chemoterapií, podobnost histologického obrazu maligního melanomu a nádorů měkkých tkání, kazuistika pacientky
- Hepatotoxicita po cyproteron acetátu v léčbě karcinomu prostaty – kazuistika
- Recidivující krvácení z jater a hemoperitoneum jako následek masivního postižení AL amyloidózou: popis případu a přehled literatury
- Editorial
- Zpráva z „malých“ registrů – Pemetrexed, Tarceva a Yondelis
- Další linie cílené léčby u nemocných s metastatickým renálním karcinomem s progresí na léčbě pazopanibem: expertní stanovisko České kooperativní skupiny pro metastatický renální karcinom
- Informace z České onkologické společnosti
- Tematický seznam publikací vydaných v Klinické onkologii v roce 2012
- Klinická onkologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Germinatívne nádory pineálnej oblasti: prehľad
- Inhibitory proteazomu v léčbě mnohočetného myelomu
- Maligní melanom léčený intenzivní chemoterapií, podobnost histologického obrazu maligního melanomu a nádorů měkkých tkání, kazuistika pacientky
- Chirurgie plicních metastáz
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



