-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Současné možnosti léčby plicní arteriální hypertenze
Current alternatives of pulmonary arterial hypertension treatment
Pulmonary arterial hypertension is a significant medical problem, when serious pulmonary vascular resistance leads to dysfunction, right ventricle failure and eventually to death. Author presents an overview of contemporary knowledge of pulmonary arterial hypertension treatment.
Keywords:
pulmonary arterial hypertension (PAH) – pulmonary vasoreactivity – therapy of PAH
Autoři: H. Al-Hiti
Působiště autorů: Centrum pro diagnostiku a léčbu plicní hypertenze ; Klinika kardiologie IKEM, Praha
Vyšlo v časopise: Kardiol Rev Int Med 2005, 7(2): 90-94
Kategorie: Redakční článek
Souhrn
Plicní arteriální hypertenze je významný medicínský problém, při kterém závažná plicní vaskulární rezistence vede k dysfunkci, selhání pravé komory srdeční a nakonec k úmrtí. Autor podává přehled současných znalostí o léčbě plicní arteriální hypertenze.
Klíčová slova:
plicní arteriální hypertenze (PAH) – plicní vazoreaktivita - terapie PAHÚvod
Plicní arteriální hypertenze (PAH) je charakterizována progresivním vzestupem plicní vaskulární rezistence (PVR) vedoucí k dysfunkci a selhání pravé komory srdeční a nakonec k úmrtí.
V terapie PAH došlo v posledním desetiletí k výraznému pokroku. Tento pokrok byl umožněn díky novým možnostem léčby, které byly ověřeny řadou randomizovaných kontrolovaných studií (RKS).
V 80. letech minulého bylo ve snaze o ovlivnění PAH testováno mnoho vazodilatátorů. Ukázalo se, že účinku dosahují pouze vysoké dávky blokátorů kalciových kanálů (CCB) a že z léčby profitoval pouze malý počet pacientů. Byli to nemocní – respondeři, u kterých byla prokázána plicní vazoreaktivita při akutním testování. Antikoagulační léčba byla doporučována na základě retrospektivního sledování. Hlavním pilířem léčby se v 90. letech stala terapie epoprostenolem, která byla potvrzena ve 3 nezaslepených RKS. Ve stejném období byly prezentovány nekontrolované studie s atriální septostomií a transplantací plic. Díky proběhlým RKS z posledního období máme nová farmaka, kterými můžeme ovlivnit nejen symptomy PAH, ale také prognózu těchto závažně nemocných pacientů.
Akutní test plicní vazoreaktivity
Nemocní s idiopatickou PAH (dříve používaný termín primární plicní hypertenze), kteří mají pozitivní akutní plicní vazodilatační test, profitují z léčby CCB.
V minulosti byla ke zjištění plicní vazoreaktivity podávána různá vazodilatancia a k určení pozitivity testu byly používány různé definice. Pacient býval označován jako responder. V současnosti je definována pozitivita testu poklesem středního tlaku v plicnici (mPAP) ≥10 mmHg či pokles mPAP < 40 mmHg se vzestupem či nezměněnou hodnotou minutového srdečného výdeje. Stěžejní práci s akutním testováním plicní vazoreaktivity publikovali roce 1992 Rich et al [1] u 64 pacientů s idiopatickou PAH, kterým byly podávány CCB. Pozitivní test byl hodnocen při poklesu mPAP a PVR o 20 %. Respondeři byli následně léčeni vysokými dávkami CCB a tato skupina dosáhla 94% přežívaní po 5 letech.
Je nutné zdůraznit, že akutní testování s CCB může vést ke zhoršení klinického a hemodynamického stavu u pacienta, který na terapii neodpovídá a prodlužuje se biologický poločas CCB. Po několika závažných nežádoucích příhodách při testování PAH pomocí CCB byl další vývoj zaměřen na podávání krátkodobě působících vazodilatátorů. V roce 1993 začali provádět Groves et al [2] u nemocných s idiopatickou PAH akutní test pomocí i.v. epoprostenolu. Zahajovací dávka byla 1 ng/kg/min, další zvyšování dávky bylo o 1-2 ng/kg/min každých 5-15 min do maximální dávky 12 ng/kg/min. Pokles plicní vaskulární rezistence (PVR) o 30 % a pokles mPAP o 10 % byl hodnocen jako pozitivní. Teprve tito nemocní byli dále dlouhodobě léčeni CCB.
Dalším lékem užívaným pro akutní testování je adenozin. Lék způsobuje koronární vazodilataci, pokles systémové vaskulární rezistence (SVR) a relaxaci hladkých svalových buněk, včetně plicních arterií. Shrader et al [3] podávali při akutním testování i.v. adenozin v dávce 50 µg/kg/min, po 2 minutách zvyšovali dávku o 50 µg/kg/min až do maximální dávky 500 µg/kg/min. Následně byla plicní reaktivita testována nifedipinem. Tam kde nebyla zjištěna reaktivita po i.v. podání adenosinu, nebyla přítomna ani po podání nifedipinu.
Vzhledem k tomu, že podávání epoprostenolu i adenozinu vede k poklesu SVR a systémové hypotenzi, hledají se selektivnější vazodilatancia pro plicní řečiště. V roce 1998 prezentovali Sitbon et al [4] výsledky práce u 33 pacientů s idiopatickou PAH, kterým byl podáván kysličník dusnatý (10 ppm). Pozitivní test byl hodnocen poklesem mPAP a PVR o 20 %. 10 nemocných mělo pozitivní test a 9 z nich byl podán akutně CCB bez komplikací. V případech, kde nebyla prokázána plicní reaktivita po podání kysličníku dusnatého, nebyl pozitivní test ani po podání CCB.
Opitz et al [5] porovnávali při akutním testování inhalační iloprost, kyslík, i.v. epoprostenol a i.v. iloprost. Podávání epoprostenolu a i.v. iloprostu přineslo podobné hemodynamické výsledky. Inhalačním iloprostem byla potvrzena selektivita pro plicní řečiště a došlo k poklesu PVR i PAP, aniž byla ovlivněna SVR. Tato studie prokázala, že jak inhalační iloprost, tak i.v. podávání epoprostenolu nebo inhalace kysličníku dusnatého predikuji pozitivní odpověď na podávání CCB.
Blokátory kalciových kanálů
Rich et al [1] prezentovali v roce 1992 výsledky prospektivní, nerandomizované studie s použitím vysokých dávek CCB u pacientů s idiopatickou PAH. Přežívání responderů po 3 a 5 letech dosahovalo 94 % a u nonresponderů činilo přežívání 47 % a 38 %. RKS s použitím CCB k léčbě idiopatické PAH zatím nebyly provedeny. Z CCB je nejčastěji užíván nifedipin nebo diltiazem. Podávají se vysoké denní dávky, nifedipin 120-240 mg/den a diltiazem 240-720 mg/den. Hlavní limitací léčby je systémová hypotenze a perimaleolární otoky dolních končetin. Pouze 10-15 % nemocných s idiopatickou PAH jsou respondeři, kteří mohou být léčeni CCB [6].
Antikoagulační terapie
U nemocných s PAH bylo prokázáno zvýšené riziko tromboembolizmu nebo trombóz in situ [7]. Ke snížení tohoto rizika se doporučuje antikoagulační léčba perorálnimi antikoagulancii s cílovými hodnotami INR 1,5-2,5. Kontroverzní je antikoagulační terapie u nemocných se systémovým onemocněním a vrozenými srdečními vadami. U sklerodermie je zvýšené riziko krvácení do gastrointestinálního traktu, u vrozených srdečních vad riziko hemoptýzy. V recentních RKS byla antikoagulační léčba podávána u 51-86 % pacientů, kteří byli zařazeni do studie - nejčastěji u nemocných s idiopatickou PAH ve stadiu NYHA III-IV, nejméně často u pacientů se sklerodermií.
Diuretika
Diuretika jsou indikována především u manifestního pravostranného srdečního selhání. Podle registrů RKS jsou podávána u 49-70 % nemocných. Není přitom specifikována dávka ani skupina diuretik; jedná se o symptomatickou léčbu.
Balonková atriální septostomie
Princip této metody spočívá v tom, že je v oblasti mezisíňového septa provedena dilatace speciálním balonkem tak, aby byla vytvořena komunikace mezi oběma síněmi. To vede k okamžitému poklesu tlaku v pravé síni, zvýšení minutového výdeje a krátkodobému zlepšení tolerance zátěže. V pozdější době dochází k progresi srdečního selhání díky enormní zátěži levé srdeční komory. Balonková septostomie se proto v současné době používá jen jako metoda k překonání časového intervalu do transplantace plíce/plic. Vzhledem k tomu, že je výkon provázen mortalitou okolo 16 % a 1roční přežívání je menší než 40 % [8], nebývá ve vyspělých zemích často indikována.
Transplantace plic
První kombinovaná transplantace srdce a plic byla provedena u pacienta s idiopatickou PAH. Výsledky tohoto náročného postupu však nejsou povzbuzující. Proto bývají v současnosti indikováni pouze pacienti s dysfunkcí pravé komory srdeční. Hlavní terapeutickou metodou se proto stala transplantace jedné plíce, popřípadě obou plic.
I tato metoda má své limitace, a to nejen v mediánu čekací doby na listině kandidátů transplantace (průměrně 256 dnů), ale především díky omezenému přežívání po transplantaci. Dlouhodobé přežívání je horší než po transplantaci srdce, jater nebo ledviny, a dosahuje 70 %, 62 % a 55 % po 1, 2 resp. 3 letech [9].
Syntetický prostacyklin a jeho analoga
Prostacyklin je endogenní prostaglandin, který má kromě vazodilatačního účinku také cytoprotektivní vliv, snižuje adhezi leukocytů k cévní stěně, inhibuje agregaci destiček, snižuje tvorbu a sekreci endotelinu a vede k inhibici migrace a proliferace buněk .
Kontinuální intravenózní aplikace syntetického epoprostenolu (Flolan, GlaxoSmithKline) vede ke zlepšení hemodynamiky, tolerance zátěže a zlepšení přežívání u nemocných s velmi závažnou PH ve stadiu NYHA III-IV, kteří neodpovídali na konzervativní terapii [10]. Dlouhodobé sledování nemocných ukázalo 5leté přežívání v 65 %. Tento výsledek je lepší než u transplantace plíce, kde se 5leté přežívání se pohybuje kolem 50 % [11].
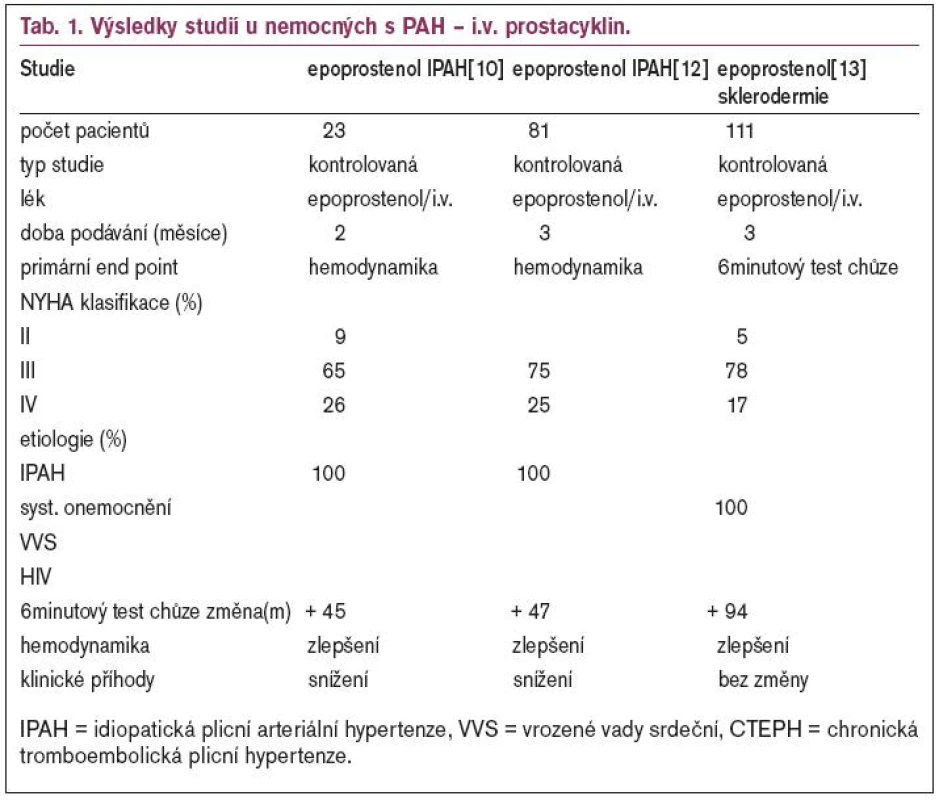
Účinek i.v. epoprostenolu byl potvrzen 3 nezaslepenými kontrolovanými studiemi u nemocných s idiopatickou PAH [10,12] a PAH při sklerodermii (tab. 1) [13].
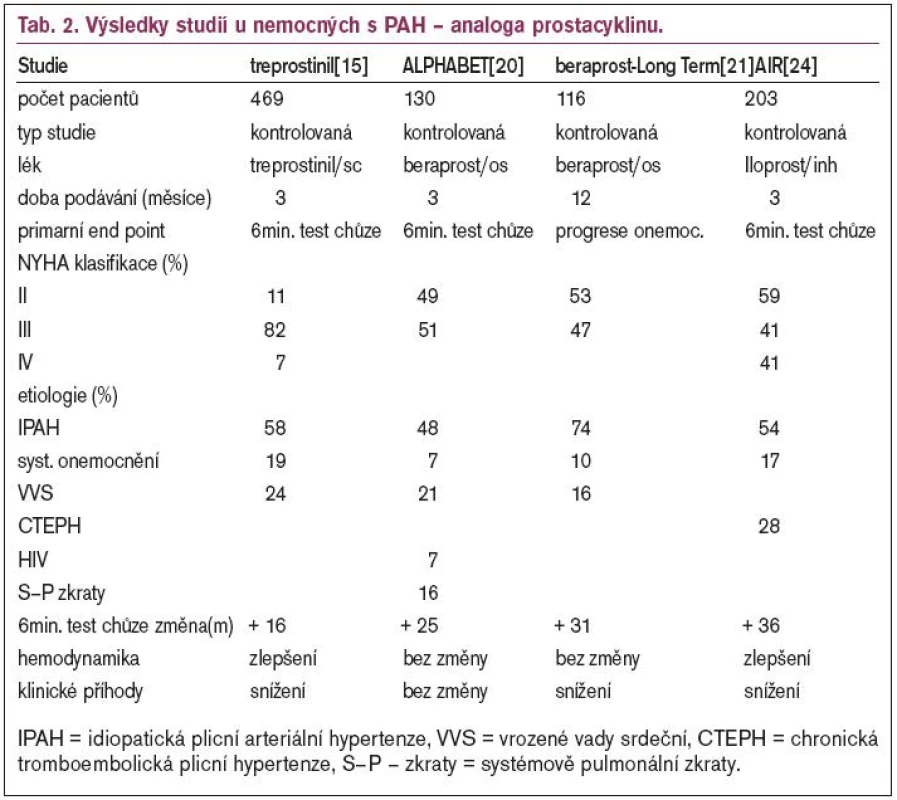
Vzhledem ke krátkému biologickému poločasu (3-5 min) je nutná trvalá kontinuální infuze, která je provázena řadou nežádoucích účinků. Patří mezi ně lokální celulitida, vznik septikemie, artralgie, pokles systémového tlaku a v neposlední řadě i tachyfylaxe. Proto byli vyvinuty alternativní formy aplikace, které využívají stabilních analogů prostacyklinu. Treprostinol je jeden z nich, s biologickým poločasem okolo 3 hod. Hypotéza, že účinek treprostinolu je podobný jako i.v. podávání epoprostenolu byla potvrzena při akutním hemodynamickém testování [14]. Největší RKS kontrolovaná placebem u nemocných s PAH byla provedena koncem 90. let v Severní Americe a 16 centech v Evropě, Austrálii a Izraeli [15]. Do této studie bylo zařazeno 469 pacientů s vysokou hodnotou plicní rezistence na podkladě PPH nebo PH u nemocných se systémovým onemocněním pojiva a vrozených systémových plicních zkratů. Výsledky prokázaly zvýšení tolerance zátěže, zlepšení symptomů a příznivé ovlivnění hemodynamiky. Nebyly prokázány žádné významné rozdíly v nežádoucích účincích mezi treprostinolem a placebem. Výsledky shrnuje tab. 2.
Beraprost sodný je první chemicky stabilní analog prostacyklinu k perorální aplikaci [16]. Vstřebává se velmi rychle, za 30 min se objevuje vrcholná koncentrace a jeho biologický poločas je 35-40 min [17]. V Japonsku byl beraprost podáván nemocným s PAH již od roku 1995. První nekontrolované studie [16,18] byly velmi nadějné, došlo ke zlepšení hemodynamických parametrů. Nagaya et al [19] prezentovali výsledky retrospektivní studie nemocných s idiopatickou PAH, kteří byli sledováni po dobu 3 let. Jejich přežívání po 3 letech dosahovalo 76 % ve skupině léčené beraprostem versus 44 % pacientů léčených konvenční léčbou. Následně byly provedeny 2 RKS v Evropě [20] a v USA [21]. V první studii došlo po 3 měsících ke zlepšení tolerance zátěže. Druhá studie potvrdila tyto výsledky i po 6 měsících, nedošlo však ke zlepšení hemodynamických parametrů v malém oběhu (tab. 2).
Iloprost je chemicky stabilní analog prostacyklinu, aplikovatelný 3 možnými cestami: intravenózně, perorálně i inhalačně (ve formě aerosolu). Biologický poločas je 20-25 min [22]. Zejména inhalační forma (Ventavis, Schering AG) je atraktivní pro dlouhodobou léčbu. Akutní inhalace iloprostu u nemocných s idiopatickou PAH má větší vazodilatační efekt na plicní řečiště než inhalační podávání kysličníku dusnatého [23]. Podává se obvykle 6-9krát denně. V mezinárodní muticentrické RKS, do které bylo zařazeno 203 pacientů s PAH, bylo prokázáno zlepšení tolerance zátěže, zmírnění symptomů a u nemocných s idiopatickou PAH pokles PVR (tab. 2) [24]. Další nekontrolovaná studie sledovala efekt inhalačního iloprostu u nemocných s idiopatickou PAH po 1 roce [25]. I v tomto případě byly potvrzeny výsledky předchozích pozorování.
Blokátory endotelinových receptorů
Endotelin–1 je produkován endoteliálními buňkami a je považován za nejsilnější endogenní vazokonstriktor [26]. Faktory, které stimulují uvolňování endotelinu-1, jsou mnohočetné: pulzativní stres, pH, hypoxie, angiotenzin II, trombin, cytokiny a růstový faktor. Endotelin působí prostřednictvím receptorů ET-1 (na oba pod receptory ETA a ETB), které byly nalezeny téměř ve všech buňkách, včetně hladkých svalových cévních buněk. Je prokázáno, že zvýšené hladiny endotelinu-1 mají vztah k přítomnosti a stupni PH. Pro léčebné použití byly vyvinuty blokátory endotelinových receporů, z nichž nejznámější je bosentan (Tracleer, Actelion).
Bosentan účinkuje na oba receptory ET1, je tedy duálním endotelinovým blokátorem. S bosentanem byla provedena řada RKS, z nichž největší byla studie BREATHE-1[27]. Bylo do ní zařazeno 213 pacientů s idiopatickou PAH a PAH při systémovém onemocnění. Podávání bosentanu vedlo ke zvýšení tolerance zátěže, zmírnění dušnosti a zlepšení celkové kvality života. Lék byl dobře tolerován (tab. 3).
Sitaxentan je selektivní blokátor A. Prozatím proběhla jedna RKS, do které bylo zařazeno 178 pacientů s PAH. Podávání sitaxentanu vedlo ke zlepšení tolerance zátěže a hemodynamických parametrů [28,29].
Ambrisentan je další selektivní antagonista endotelinových receptorů, typ A. Zatím byla provedena pouze jedna pilotní studie, do které bylo zařazeno 64 pacientů s PAH. Předběžné výsledky jsou stejně pozitivní jako u ostatních antagonistů endotelinových receptorů [30].
Inhibitory fosfodiesterázy-5
Sildenafil je perorální selektivní inhibitor cGMP fosfodiesterázy-5. Zvyšuje intracelulární koncentraci cyklického guanozsin-monofosfátu, který má vazodilatační účinek v plicním cévním řečišti. Se sildenafilem byla provedena řada studií [31-34], které prokázaly příznivý efekt. Výsledky velké mezinárodní RKS, do které bylo zařazeno více než 200 pacientů s PAH, zatím nebyly publikovány, ale očekává se, že ovlivní léčebný algoritmus PAH.
L-arginin se podílí na zvýšení produkce přirozeného vazodilatátoru, kysličníku dusnatého a následně vede k poklesu PAH. Toto bylo ověřeno Nagayamou et al [35], kteří podávali L-arginin 19 nemocným s idiopatickou PAH nebo jinou prekapilární PH. Po 1týdenním podávání došlo u těchto pacientů ke zlepšení tolerance zátěže a poklesu PAH. Zatím ale s L-argininemneexistují žádné rozsáhlé klinické studie.
Kombinovaná terapie
Kombinovaná terapie je atraktivní možnost ovlivnění PAH různými patofyziologickými cestami. Významné ovlivnění PAH bylo dokumentováno v placebem kontrolované prospektivní studii BREATHE-2, do které bylo zařazeno 33 pacientů se závažnou PAH. Nemocní byli léčeni epoprostenolem v kombinaci s bosentanem [36]. Další možností je kombinovaná léčba inhalačním iloprostem spolu se sildenafilem [37].
Závěr
Léčba PAH se v poslední dekádě dramaticky a velmi rychle změnila. Díky velkým RKS byly ověřeny nové léčebné možnosti k ovlivnění PAH. Jeden z možných algoritmů léčby PAH je zobrazen na schématu 1.
Schéma 1. Algoritmus léčby PAH. 
Úroveň evidence A – data získaná z multicentrické RKS nebo metaanalýzy. Úroveň evidence B – data získaná z 1 RKS. Úroveň evidence C – data získaná z malých nerandomizovaných studií a/nebo z názorů expertů. Přes veškerý pokrok je léčba nemocných s PAH obtížná. Vzhledem k tomu, že vyžaduje hemodynamické monitorování, testování reverzibility PH a široké spektrum vyšetřovacích metod, měla by být omezena na specializovaná centra s dlouhodobými zkušenostmi.
MUDr. Hikmet Al-Hiti
Narodil se 1970 v Praze. V roce 1995 promoval na 3. LF UK v Praze. Po ukončení studia nastoupil na Kliniku kardiologie v IKEM. V roce 1998 složil atestaci I. stupně z vnitřního lékařství, v roce 2002 atestaci z kardiologie. Od počátku se věnuje problematice plicní hypertenze a možnostem jejího ovlivnění. Je autor nebo spoluautor více než 15 kongresových sdělení na domácích i zahraničních konferencích a kongresech věnovaných této problematice.
Zdroje
1.Rich S, Kaufmann E, Levy PS. The effect of high doses of calcium-channel blockers on survival in primary pulmonary hypertension. N Engl J Med 1992; 327(2): 76-81.
2.Groves BM, Badesch DM, Turkevich D et al. Correlation of acute prostacyclin response in primary (unexplained) pulmonary hypertension with efficacy of treatment with calcium channel blockers and survival. In: Weir K (ed). Ion flux in pulmonary vascular control. New York: Plenum Press 1993 : 317-330.
3.Schrader BJ, Invar S, Kaufmann L et al. Comparison of the effect of adenosine and nifedipine in pulmonary hypertension. J Am Coll Cardiol 1992; 29 : 1060-1064.
4.Sitbon O, Hubert M, Jagot JL et al. Inhaled nitric oxide as a screening agent for safety identifying responders to oral calcium-channel blockers in primary pulmonary hypertension. Eur Respir J 1998; 12 : 265-270.
5.Opitz CF, Wensel R, Bettmann M et al. Assessment of the vasodilator response in primary pulmonary hypertension: comparing prostacyclin and iloprost administered by either infusion or inhalation. Eur Heart J 2003; 24 : 356-365.
6.Sitbon O, Hubert M, Ioos V et al. Who benefits from long-term calcium-channel blockers therapy in primary pulmonary hypertension? Am J Respir Crit Care Med 2003; 167: A440.
7.Frank H, Mlczoch, Huber K et al. The effect of anticoagulant therapy in primary and anorectic drug-included pulmonary hypertension. Chest 1997; 112(3): 714-421.
8.Sandoval J, Gaspar J, Pulido T et al. Graded balloon dilation atrial septostomy in severe primary pulmonary hypertension. A therapeutic alternative for patients nonresponsive to vasodilatator treatment. J Am Coll Cardiol 1998; 32 : 297-304.
9.Hosenpud JD, Bennett L E et al. The registry of the International society for Heart and Lung Transplantation: Seventeenth official report 2000. J Heart Lung Transplant 2000; 19(10): 909-931.
10.Barst RJ, Rubin LJ, Long WA et al. A comparison of continuous intravenous epoprostenol (prostacyclin) with conventional therapy for primary pulmonary hypertension. The Primary Pulmonary Hypertension Study Group. N Engl J Med 1996; 334(5): 296-302.
11.Higenbottam T. Treatment of pulmonary hypertension by inhaled delivery. New York: The Parthenon Publishing Group 1999 : 9-17.
12.Rubin LJ, Mendoza J, Hood M et al. Treatment of primary pulmonary hypertension with continuous intravenous prostacyclin (epoprostenol). Results of
randomized trial. Ann Intern Med 1990; 112(7): 485-491.
13.Badesch DB, Tapson VF, McGoon MD et al. Continuous intravenous epoprostenol for pulmonary hypertension due to the scleroderma spectrum disease. A randomized, controlled trial. Ann Intern Med 2000; 132(6): 425-434.
14.McLaunghlin VV, Gaine SP, Barts RJ et al. Efficacy and safety of treprostinil: an epoprostenol analog for primary pulmonary hypertension. J Cardiovasc Pharmacol 2003; 41(2): 293-299.
15.Simonneau G, Barts RJ, Galie N et al. Continuous subcutaneous infusion of treprostinil, a prostacyclin analogue, in patients with pulmonary arterial hypertsion. A double-blind, randomized, placebo-controlled trial. Am J Respir Crit Care Med 2002; 165(6): 800-804.
16.Okano Y, Yoshioka T, Schimouchi A et al. Orally active prostacyclin analogue in primary pulmonary hypertension. Lancet 1997; 349(9062): 1365.
17.Galie N, Manes A, Branzi A. The new clinical trials on pharmacological treatment in pulmonary arterial hypertension. Eur Respir J 2002; 20(4): 1037-1049.
18.Saji T, Ozawa Y, Ishikita T et al. Short-term hemodynamic effects of new oral PGI 2 analogue, beraporost, in primary and secondary pulmonary hypertension. Am J Cardiol 1996; 78(2): 244-247.
19.Nagaya N, Uematsu M, Okano Y et al. Effects of beraprost podium, an oral prostacyclin analogue on survival of outpatients with primary pulmonary hypertension. J Am Coll Cardiol 1999; 34(4):1188-1192.
20.Galie N, Hubert M, Vachiery JL et al. Effect of beraprost sodium, an oral prostacyclin analogue, in patinets with pulmonary arterial hypertension: a randomized, double-blind, placebo-controlled trial. J Am Coll Cardiol 2002; 39 : 1496-1502.
21.Barts RJ, McGoon M, McLaughlin VV et al. Beraprost therapy for pulmonary arterial hypertension. J Am Coll Cardiol 2003; 41 : 2119-2125.
22.Krause W, Krais T. Pharmacokinetics and phramacodynamics of the prostacyclin analogue iloprost in man. Rur J Clin Pharmacol 1986; 30(1): 61-68.
23.Hoeper MM, Olschewski H, Ghofrani HA et al. A comparison of the acute hemodynamic effects of inhaled nitric oxide and aerosolized iloprost in primary pulmonary hypertension. German PPH Study Group. J Am Coll Cardiol 2000; 35(1): 176-182.
24.Olschewski H, Simonneau G, Galie N et al. Inhaled iloprost in severe pulmonary hypertension. N Engl J Med 2002; 347(5): 322-329.
25.Hoeper MM, Schwarze M, Ehlerging S et al. Long-term treatment of primary pulmonary hypertension with aerosolized iloprost, a prostacyclin analogue. N Engl J Med 2000; 342(25): 1866-1870.
26.Yanagisawa M. The endothelin system. A new target for therapeutic intervention. Circulacion 1994; 89(3): 1320-1322.
27.Rubin LJ, Badesch DB, Barst RJ et al. Bosentan therapy for pulmonary arterial hypertension. N Engl J Med 2002; 346(16): 869-903.
28.Barts R, Langleben D, Frost A et al. Sitaxsentan, a selective ETA receptor antagonist, improves exercise capacity and NYHA functional class in pulmonary arterial hypertension (abstr). Am J Respir Crit Care Med 2003; 167: A440.
29.Barts R, Langleben D, Frost A et al. Sitaxsentan, a selective ETA receptor antagonist, improves cardiopulmonary hemodynamics in pulmonary hypertension (abstr). Am J Respir Crit Care Med 2003; 167: A273.
30.Rubin LJ, Galie N, Badesch BD et al. Ambisertan improves exercise capacity and clinical measures in pulmonary arterial hypertension (PAH). Am J Respir Crit Care Med 2004. (v tisku)
31.Prasad S, Wilkinson J, Gatzoulis MA. Sildenafil in primary pulmonary hypertension. N Engl J Med 2000; 343(18): 343-1342.
32.Bhatia S, Frantz RP, Severson CJ et al. Immediate and long-term hemodynamic and clinical effects of sildenafil in patient with pulmonary arterial hypertension receiving vasodilaror therapy. Mayo Clin Proc 2003; 78(10): 1207-13.
33.Michelakis ED, Tymchak W, Noga M et al. Long - term treatment with oral sildenafil safe and improves functional capacity and hemodynamics in patient with pulmonary arterial hypertension. Circulation 2003; 108(17): 2006-2069.
34.Sastry BKS, Narasimhan C, Reddy NK et al. Clinical efficacy of sildenafil in primary pulmonary hypertension: a randomized, placebo–controlled, double-blind, crossover study. J Am Coll Cardiol 2004; 43(7): 1149-1153.
35.Nagaya N. Short–term oral administration of L-arginin improves hemodynamics and exercise capacity in patients with precapillary pulmonary hypertension. Am J Respir Crit Care Med 2001; 163(4): 887-891.
36.Hubert M, Barst R, Robbins I et al. Safety and efficacy of bosentan combined with epoprostenol in patients with severe pulmonary arterial hypertension (abstr). Am J Respir Crit Care Med 2003; 167: A441.
37.Ghofrani HA, Rose F, Schermuly RT et al. Oral sidenafil as long-term adjunct therapy to inhaled iloprost in severe pulmonary arterial hypertension. J Am Coll Cardiol 2003; 42(1): 158-164.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie Kardiologie
Článek Choroby venózního systémuČlánek Aortální regurgitace
Článek vyšel v časopiseKardiologická revue – Interní medicína
Nejčtenější tento týden
2005 Číslo 2- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
-
Všechny články tohoto čísla
- Klinické studie ukončené, přednesené nebo publikované v poslední době
- Srdce v obrazech lidových rčení II.
- Srovnání řízeného a nekontrolovaného aerobního tréninku nemocných s chronickou ischemickou chorobou srdeční
- Rehabilitace po infarktu myokardu (II): způsoby zátěže
- Choroby venózního systému
- Srovnání léčby hypertenze na interní klinice FN, na interním oddělení malé nemocnice a na specializované kardiologické klinice
- Současné možnosti léčby plicní arteriální hypertenze
- Denní a týdenní variace ve výskytu akutního srdečního infarktu
- Aortální regurgitace
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Aortální regurgitace
- Rehabilitace po infarktu myokardu (II): způsoby zátěže
- Choroby venózního systému
- Současné možnosti léčby plicní arteriální hypertenze
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání