-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaSurveillance invazivního meningokokového onemocnění a doporučená vakcinace proti meningokokovým nákazám v České republice
Surveillance of invasive meningococcal disease and recommended vaccination against meningococcal infections in the Czech Republic
The nationwide surveillance of invasive meningococcal disease in the Czech Republic has been conducted since 1993 by the National Reference Laboratory (NRL) for Meningococcal Infections in close cooperation with epidemiologists, microbiologists and clinicians. NRL has been involved in national and international research projects and networks and performs molecular characterization of Neisseria meningitidis that is helpful in both national and international surveillance of invasive meningococcal disease, provides background information for vaccination strategy updates and contributes to the development of novel meningococcal vaccines. Two noteworthy events occurred in 2010: a worldwide recommendation was issued on a booster conjugate vaccine dose and conjugate tetravaccine A,C,Y,W135 was registered for use in Europe. According to the latest recommendations of the world experts, the first dose of conjugate vaccine should be given in childhood and should be followed by a booster dose at the pre-adolescent age. The recommended booster is conjugate tetravaccine A,C,Y,W135 that provides long-term broad immunity and should also be available in the Czech Republic as soon as possible. It is necessary to keep up to date with the development of novel vaccines against meningococcal infections caused by serogroup B (MenB) and to test them for suitability for use in the Czech Republic. As soon as such a MenB vaccine is developed and registered, it will be desirable to include it into the routine childhood immunization scheme in the Czech Republic because of the high incidence of Meningococcus B infections in the youngest age group.
Key words:
surveillance of invasive meningococcal disease – meningococcal vaccine – vaccination strategy.
Autoři: P. Křížová
; M. Musílek
Působiště autorů: Národní referenční laboratoř pro meningokokové nákazy, Státní zdravotní ústav, Praha
Vyšlo v časopise: Epidemiol. Mikrobiol. Imunol. 59, 2010, č. 4, s. 173-182
Souhrn
Celorepubliková surveillance invazivního meningokokového onemocnění je v České republice prováděna od roku 1993 v úzké spolupráci Národní referenční laboratoře (NRL) pro meningokokové nákazy s epidemiology, mikrobiology a klinickými lékaři. Zapojení NRL do tuzemských i mezinárodních výzkumných projektů umožňuje provádění molekulární charakterizace Neisseria meningitidis, která zpřesňuje národní i mezinárodní surveillance invazivního meningokokového onemocnění, dává podklady k aktualizaci vakcinační strategie a přispívá k vývoji nových meningokokových vakcín. Rok 2010 je významný tím, že bylo celosvětově doporučeno provádění přeočkování (booster) u konjugované vakcíny a že v Evropě byla úspěšně dosažena centrální registrace konjugované tetravakcíny A,C,Y,W135. Podle nejnovějších doporučení světových expertů je vhodné provést základní očkování konjugovanou vakcínou v dětském věku a přeočkování v pre-adolescentním věku. Je doporučeno provádět přeočkování konjugovanou tetravakcínou A,C,Y,W135 k zajištění co nejširší dlouhodobé imunity a je žádoucí, aby tato tetravakcína byla co nejdříve dostupná i v České republice. Je nezbytné sledovat vývoj nových očkovacích látek proti meningokokovým nákazám vyvolaným séroskupinou B (MenB) a hodnotit vhodnost jejich použití v České republice. Jakmile bude vyrobena a následně registrována MenB vakcína vhodná pro Českou republiku, bude žádoucí zahrnout ji do očkovacího schématu malých dětí, vzhledem k vysoké nemocnosti způsobené meningokokem B v nejmladší věkové skupině.
Klíčová slova:
surveillance invazivního meningokokového onemocnění – meningokoková vakcína – vakcinační strategie.Úvod
Surveillance invazivního meningokokového onemocnění je nezbytným předpokladem možnosti určení vakcinační strategie odpovídající aktuální epidemiologické situaci.
Koncepce surveillance byla založena již v 60. letech 20. století prof. Karlem Raškou [1, 2], který byl v té době ředitelem Divize přenosných nemocí Světové zdravotnické organizace (WHO) a v roce 1968 byly na 21. zasedání World Health Assembly přijaty tři základní prvky surveillance: a) systematický sběr dat; b) analýza a hodnocení dat; c) předávání dat a jejich využití k akcím, které vedou ke snížení nemocnosti a smrtnosti a ke zlepšení zdravotního stavu populace. V praxi programy surveillance jednotlivých infekčních onemocnění spočívají ve sledování nemocnosti, úmrtnosti, smrtnosti, geografické distribuce, detailní charakterizace agens a sledování imunity populace. Na základě získaných komplexních poznatků jsou stanoveny postupy prevence, profylaxe a vakcinační strategie pro jednotlivá infekční onemocnění.
Aktivní surveillance invazivního meningokokového onemocnění byla v České republice zahájena v roce 1993, kdy zde byla zaznamenána přítomnost hypervirulentního meningokokového klonu C:2a:P1.2,5:cc11. Provádění surveillance bylo v České republice zajišťováno metodickým návodem publikovaným ve Věstníku MZ ČR [3] a od roku 2008 je legislativně podloženo vyhláškou č. 473/2008 Sb., o systému epidemiologické bdělosti pro vybrané infekce [4]. Definice invazivního meningokokového onemocnění je v souladu s evropskou definicí [5]. Součástí surveillance je molekulární charakterizace všech izolátů z invazivního onemocnění zaslaných do Národní referenční laboratoře pro meningokokové nákazy (NRL) k dourčení [6, 7]. Surveillance data jsou hlášena do evropské epidemiologické databáze TESSy, spravované Evropským centrem pro prevenci a kontrolu nemocí (ECDC), které od členských států EU požaduje i hlášení molekulární charakterizace izolátů z invazivního meningokokového onemocnění [8]. Poskytování kvalitních surveillance dat do TESSy vyžaduje dobrou spolupráci NRL s epidemiology, mikrobiology i klinickými lékaři. Základní role NRL členských států definovalo ECDC v dokumentu publikovaném v červnu 2010 [9].
Vývoj meningokokových vakcín má již dlouhou historii, je k dispozici řada kvalitativně odlišných vakcín, avšak stále není k dispozici vakcína univerzálně účinná proti všem meningokokovým onemocněním. Není stanovena vakcinační strategie, která by byla univerzálně použitelná pro všechny země a jednotlivé vakcinační strategie jsou utvářeny podle epidemiologické situace a vhodnosti meningokokových vakcín pro použití v jednotlivých zemích.
Epidemiologická situace invazivního meningokokového onemocnění v České republice
Zavedení celorepublikového programu surveillance v roce 1993 poskytuje validní srovnatelná data. V období 1993–2009 bylo v České republice v programu surveillance hlášeno celkem 2087 invazivních meningokokových onemocnění, z nichž 830 způsobila séroskupina B a 800 séroskupina C. Nemocnost způsobená séroskupinou B má za celé období téměř stabilní trend (průměrná hodnota 0,5/100 000), pouze s mírným vzestupem v posledních letech – graf 1. Naopak, nemocnost způsobená séroskupinou C v průběhu sledovaných 17 let vykazuje velké výkyvy: v polovině 90. let se pohybovala na několikanásobně vyšších hodnotách (s maximem 1,3/100 000 v roce 1995) ve srovnání se současnou situací (0,1/100 000 v roce 2009). Celková nemocnost invazivního meningokokového onemocnění vykazovala ve sledovaném období stejnou dynamiku vývoje jako nemocnost způsobená sérokupinou C.
Graf 1. Nemocnost (na 100 000) IMO – celková a specifická podle séroskupin, Česká republika 1993–2009 Fig. 1. IMD cases per 100,000 population – overall and serogroup-specific incidence rates, Czech Republic, 1993–2009 
Věkově specifická nemocnost ukazuje, že za celou dobu surveillance jsou nejvyšší hodnoty zjišťovány v nejmladší věkové skupině 0–11měsíčních dětí, o druhé a třetí místo se dělí 1–4leté děti s 15–19letými adolescenty – graf 2. Sledování séroskupinově specifické nemocnosti v těchto třech nejvíce postižených věkových skupinách ukazuje, že séroskupina B vyvolává výrazně nejvyšší nemocnost (3–5krát vyšší) u 0–11měsíčních dětí – grafy 3 a 4.
Graf 2. IMO – věkově specifická nemocnost, Česká republika 1993–2009 Fig. 2. IMD cases – age-specific incidence rates, Czech Republic, 1993–2009 
Graf 3. Nemocnost (na 100000) IMO N. m. B – specifická podle věku, Česká republika 1993–2009 Fig. 3. N. meningitidis B IMD cases per 100,000 population – age-specific incidence rates, Czech Republic, 1993–2009 
Graf 4. Nemocnost (na 100000) IMO N.m.C – specifická podle věku, Česká republika 1993–2009 Fig. 4. N. meningitidis C IMD cases per 100,000 population – age-specific incidence rates, Czech Republic, 1993–2009 
Celková smrtnost invazivního meningokokového onemocnění za 17leté období surveillance byla 10,4 %, přičemž nejvyšší smrtnost způsobila séroskupina Y (20,7 %), následovaná séroskupinou C (12,2 %). Rozdíly ve smrtnosti způsobené jednotlivými séroskupinami v České republice jsou v souladu s rozdíly zjištěnými v Evropě – graf 5. Vysokou smrtnost, kterou má na svědomí séroskupina Y, způsobuje hypervirulentní komplex Neisseria meningitidis Y:cc23, který se v České republice objevil teprve v roce 1995 a jeho výskyt postupně stoupá – graf 6. Identický hypervirulentní komplex byl popsán v USA a Kanadě, kde rovněž způsobuje vysokou smrtnost invazivního meningokokového onemocnění. Studium izolátů z invazivního meningokokového onemocnění, které je v NRL systematicky prováděno díky řešení tuzemských i zahraničních projektů, ukazuje zásadní změnu ve výskytu hypervirulentních klonálních komplexů v současné době oproti situaci v 90. letech – graf 7. V roce 1993 se v České republice poprvé objevil hypervirulentní klonální komplex N. meningitidis C:cc11, který se zde prokazatelně v předchozích dvaceti letech nevyskytoval [6, 7], byl však znám v zemích západní Evropy, kde způsoboval zvýšení nemocnosti i smrtnosti. Převaha tohoto hypervirulentního klonu v polovině devadesátých let byla výrazná (v roce 1995 dosáhl 75,4 %), od druhé poloviny 90. let docházelo k jeho poklesu, přerušenému dočasným vzestupem v letech 2002–2004. V současné době je tento hypervirulentní komplex zjišťován v nízkém procentu, a naopak dochází k postupnému zvyšování výskytu hypervirulentních komplexů typických pro N. meningitidis B: cc18, cc32, cc41/44 a cc269.
Graf 5. Smrtnost IMO – podle séroskupin, Česká republika 1993–2009 a Evropa 2007 Fig. 5. IMD case fatality rates by serogroup, Czech Republic, 1993–2009, and Europe, 2007 
Graf 6. Procento N. meningitidis Y z IMO, Česká republika 1993–2009 Fig. 6. Percentages of N. meningitidis Y IMD cases Czech Republic, 1993–2009 
Graf 7. Hlavní hypervirulentní komplexy N. meningitidis z IMO, Česká republika 1993–2009 Fig. 7. Major hypervirulent complexes in N. meningitidis from IMD cases Czech Republic, 1993–2009 
Z uvedené analýzy epidemiologické situace invazivního meningokokového onemocnění v České republice vyplývá, že v současné době musí být vakcinační strategie odlišná oproti devadesátým letům či konci minulého století.
Meningokokové vakcíny
Do současné doby byly ve světě vyvinuty tři druhy meningokokové vakcíny: polysacharidová, proteinová a konjugovaná. Všechny tyto vakcíny poskytují specifickou imunitu pouze proti těm antigenům (polysacharidovým či proteinovým), z nichž jsou vyrobeny. Nejnovější zprávy o vývoji meningokokových vakcín napovídají, že nová vakcína, která by byla univerzálně účinná na všechny meningokoky, bez ohledu na jejich kapsulární či nekapsulární antigeny, bude vyvinuta genetickými metodami (reverzní vakcinologie) [10]. Tento vývoj však bude trvat ještě řadu let. Tabulka 1 uvádí přehled již vyvinutých a vyvíjených meningokokových vakcín ve světě. Některé z těchto vakcín jsou připravovány cíleně pro určitou zemi (proteinové vakcíny či kombinace skupinových polysacharidů v konjugovaných vakcínách), jiné vakcíny mají široké použití (např. MenC konjugovaná vakcína, konjugovaná tetravakcína A, C, Y, W135). Široké použití je rovněž očekáváno po ukončení vývoje MenB vakcín vyrobených reverzní vakcinologií.
Tab. 1. Meningokokové vakcíny Table 1. Meningococcal vaccines 
1. Polysacharidové vakcíny
Polysacharidové vakcíny vznikly extrakcí skupinově specifického polysacharidového pouzdra N. meningitidis proti séroskupinám A, C, Y a W135. Zpočátku byly k dispozici monovakcíny proti jednotlivým séroskupinám, později se výroba ustálila na bivakcíně A, C a tetravakcíně A, C, Y, W135. Samotný skupinově specifický polysacharid N. meningitidis je málo imunogenní. V důsledku toho polysacharidová vakcína vyvolává krátkodobou ochranu: anti-A maximálně 5 let, anti-C maximálně 3 roky. Po uplynutí tohoto období klesají protilátky na nulové hodnoty a další očkování nevyvolává booster efekt. Recentně bylo zjištěno nebezpečí vzniku imunotolerance [11], kdy nedochází ke vzniku ochranných protilátek při četnější opakované aplikaci polysacharidové vakcíny. Z důvodu nízké imunogenicity samotného polysacharidu není polysacharidová vakcína účinná u dětí pod dva roky věku.
2. Konjugované vakcíny
Konjugované vakcíny vznikly navázáním (konjugováním) skupinově specifických polysacharidů N. meningitidis na proteinový nosič, který sám nemá žádnou antigenní odezvu, způsobuje však významné zvýšení imunogenicity skupinově specifických meningokokových polysacharidů. U meningokokové konjugované vakcíny jsou používány dva proteinové nosiče:
- tetanický toxoid (TT),
- zkříženě reagující protein derivovaný z difterického toxinu (CRM197).
Nejdříve byly vyvinuty konjugované vakcíny proti séroskupině C (vakcíny MenC), poprvé byly použity v Anglii v roce 1999 v rozsáhlé vakcinační kampani [12] a následně v dalších zemích. Na počátku tohoto století byla vyvinuta trivakcína A, C, W135 (používaná k vakcinační kampani v Rwandě) a posléze tetravakcína A, C, Y, W135, která je registrována v USA a v Kanadě a je zde používána k vakcinaci 11–12letých dětí [13]. V dubnu 2010 proběhla centrální registrace této konjugované tetravakcíny A, C, Y, W135 pro Evropu a v evropských zemích se diskutuje o možnosti jejího zařazení do očkovacího schématu dětí [14].
Srovnání kvality polysacharidové a konjugované vakcíny vychází jednoznačně ve prospěch konjugované vakcíny, která vyvolává dlouhodobou imunitu, vykazuje booster efekt, je účinná i u dětí pod 2 roky věku a redukuje nosičství N. meningitidis. U dětí do jednoho roku věku je nutné aplikovat dvě či tři dávky konjugované vakcíny (počet dávek se u jednotlivých výrobců liší). Pojem dlouhodobá ochrana není u konjugované vakcíny v současné době zcela jednoznačně vyjasněn. Různí výrobci udávají 7–10 roků. Zkušenosti ze zemí, kde byla konjugovaná MenC vakcína zařazena do pravidelného očkování, ukazují, že trvání ochranné imunity je ovlivněno věkem očkovaných: čím nižší věk očkovaného, tím kratší doba ochranné imunity [15].
Nejnovější studie dokumentují nutnost přeočkování (booster) pro dosažení dlouhodobé (celoživotní) imunity a doporučení mezinárodních expertů [14] pro očkování konjugovanou meningokokovou vakcínou zní:
- Provést očkování u malých dětí (věk závisí na epidemiologické situaci dané země).
- Provést revakcinaci podle epidemiologické situace v dětském nebo v pre-adolescentním věku.
Zkušenosti z vakcinační kampaně v Anglii ukázaly, že konjugovaná vakcína C snižuje procento nosičů N. meningitidis C ve zdravé populaci [16]. Nosičství N. meningitidis ostatních séroskupin a nezařaditelných do některé ze známých sérologických skupin (= typicky nosičských) však zůstává konjugovanou vakcínou C neovlivněno.
3. Proteinové vakcíny
Proti N. meningitidis B není k dispozici polysacharidová, a tudíž ani konjugovaná vakcína. Současné vakcíny proti N. meningitidis B jsou proteinové a vznikly extrakcí nekapsulárních antigenů z buněčné stěny N. meningitidis B, sérotypově a subtypově specifických („porin based“ vakcíny). Tyto proteinové vakcíny však nejsou univerzálně účinné proti všem meningokokům B. Meningokoky séroskupiny B jsou antigenně i geneticky velmi heterogenní populace a skupinově specifický polysacharid B je málo imunogenní. Populace N. meningitidis B jsou v jednotlivých zemích odlišné a z tohoto důvodu je proteinová vakcína vždy zaměřena na nekapsulární antigeny odpovídajícího epidemického kmene v určité zemi. Do současné doby bylo ve světě vyrobeno šest subtypově specifických vakcín proti N. meningitidis B (viz tab. 1). Čtyři z těchto vakcín byly vyrobeny z epidemického/endemického klonu meningokoka v dané zemi: Norsko N. meningitidis B:15:P1.7,16; Kuba N. meningitidis B:4:P1.19,15; Chile N. meningitidis B:15:P1.3; Nový Zéland N. meningitidis B:4:P1.7,4. V nizozemském Národním institutu veřejného zdraví a životního prostředí (RIVM) byla vyrobena nejprve hexavakcína a následně nonavakcína z meningokoků séroskupiny B nejvíce zastoupených v západní Evropě.
4. Vakcíny vyráběné genetickými metodami
Nová a převratná metodologie vývoje meningokokových vakcín genetickými metodami, nazývaná reverzní vakcinologie, byla zahájena sekvenací celého genomu N. meningitidis B, díky níž byly identifikovány geny kódující povrchové proteiny bakteriální buňky potencionálně použitelné pro širokospektrou vakcínu, která by vyvolávala tvorbu protilátek proti celé heterogenní populaci meningokoků séroskupiny B [10]. Metodou reverzní vakcinologie byla detekována řada nových proteinových antigenů N. meningitidis B, které indukovaly baktericidní aktivitu u myší, některé z nich však byly vysoce konzervované a bylo pravděpodobné, že budou vyvolávat ochranu pouze proti části meningokoků B. Byly proto hledány antigeny široce zastoupené u celé populace N. meningitidis B – pražská NRL se jedné z těchto studií účastnila [17].
Finálně byly vybrány antigeny (Factor H binding protein = LP2086, NadA, GNA), které jsou v různých kombinacích užity v nově vyvíjených vakcínách proti meningokoku B, připravovaných metodou reverzní vakcinologie. Od těchto vakcín se očekává široká účinnost proti všem meningokokům B, bez ohledu na jejich vybavení sérotypy a subtypy. V České republice probíhá v současnosti klinická studie jedné z těchto vakcín.
Meningokokové vakcíny v České republice
Z polysacharidových vakcín je v České republice desítky let registrovaná bivakcína A, C. Polysacharidová tetravakcína A, C, Y, W135 není v naší republice registrována, pouze přechodně se podařil její dovoz v letech 2004–2005. Z konjugovaných vakcín je v České republice registrována vakcína proti N. meningitidis C: od roku 2001 NeisVac-C a od roku 2003 Menjugate – tabulka 2. V dubnu 2010 proběhla centrální evropská registrace konjugované tetravakcíny A, C, Y, W135 a její dostupnost v České republice je žádoucí.
Tab. 2. Dostupnost meningokokových vakcín v České republice Table 2. Meningococcal vaccines available in the Czech Republic 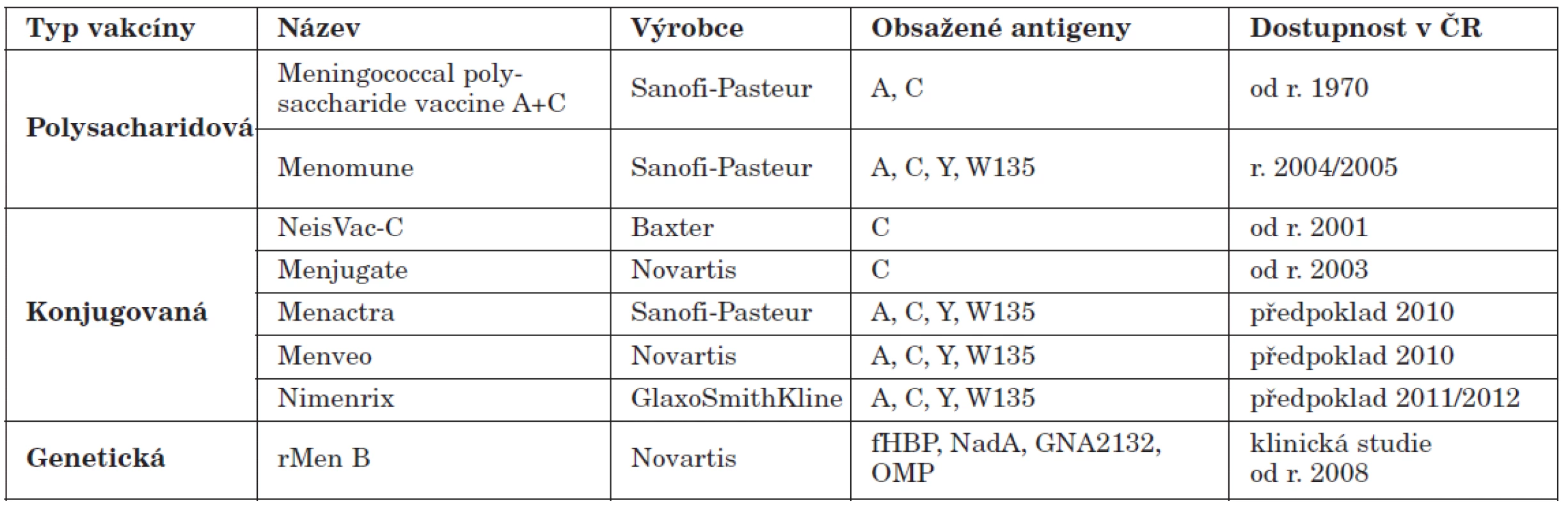
Dosud vyvinuté zahraniční vakcíny proti N. meningitidis B (subtypově specifické, „porin based“) vykazují nízké pokrytí nekapsulárních antigenů izolátů N. meningitidis B působících invazivní onemocnění v České republice v letech 1997–2007 [6, 7], a proto jejich použití u nás nedoporučujeme. Navíc, populace českých meningokoků B je velmi heterogenní a nelze najít žádný fenotyp, který by ve významném procentu převládal tak, aby bylo účelné vyrobit z něj vakcínu vhodnou pro Českou republiku.
Vakcinační strategie
Vakcinační strategie ve světě
Polysacharidová vakcína (bivakcína A, C nebo tetravakcína A, C, Y, W135) se nikde ve světě nepoužívá k plošné vakcinaci, protože zajišťuje pouze krátkodobou imunitu a není účinná u dětí pod 2 roky věku. Před dostupností konjugované vakcíny byla polysachariová vakcína používána k cílené vakcinaci ohrožené části populace. V současnosti je polysacharidová vakcína (A, C nebo A, C, Y, W135) aplikována cestovatelům do oblastí se zvýšenou nemocností invazivního meningokokového onemocnění uvedených séroskupin za předpokladu, že cestovatelům postačí zajištění krátkodobé imunity (3–5 roků).
K plošné vakcinaci je vhodná konjugovaná vakcína, ve většině zemí Evropy se však stále plošně neočkuje a nemocnost se zde pohybuje v rozmezí 0,3–3,8/100 000. V zemích, kde bylo na přelomu století zahájeno plošné očkování konjugovanou MenC vakcínou (Anglie, Belgie, Island, Irsko, Nizozemsko, Španělsko, Portugalsko) se nemocnost způsobená N. meningitidis C před zahájením vakcinační kampaně pohybovala v rozmezí 1,5–4,5/100 000 obyvatel [18], což je několikanásobně vyšší, než byly maximální hodnoty nemocnosti způsobené séroskupinou C v České republice v polovině devadesátých let. V poslední době nastupuje trend zařazování konjugované MenC vakcíny do očkovacího kalendáře dětí i v zemích, kde je nemocnost na nižší úrovni (Německo, Francie). Po zařazení konjugované MenC vakcíny do očkovacího schématu malých dětí nebyl zaznamenán „replacement“ séroskupiny působící invazivní meningokokové onemocnění.
Kromě očkování malých dětí jsou v těchto zemích zároveň prováděny vakcinační kampaně („catch-up“) pokrývající celou dětskou a adolescentní populaci. Modelování s prognózováním nemocnosti a její srovnání se skutečnou nemocností po různých vakcinačních kampaních ukázalo na důležitost těchto „catch-up“ kampaní pro zajištění rychlého a významného snížení nemocnosti (90 %) a pro dlouhodobé udržení kolektivní imunity, která je nezbytná k redukci cirkulace agens v populaci a následně vede k trvalému snížení nemocnosti. Toto následně umožňuje uvažovat o snížení počtu dávek v základním očkování – při snížené cirkulaci agens v populaci nehrozí nebezpečí selhání vakcíny při nižším počtu dávek základního očkování.
Nejnovější poznatky ze zemí, kde byla konjugovaná MenC vakcína zařazena do očkovacího schématu dětí, nejdříve ukázaly, že k získání celoživotní imunity je potřeba provést přeočkování. V zemích s nízkou postvakcinační MenC nemocností je plánováno snížení počtu dávek základního očkování malých dětí a zavedení booster vakcinace v dětském nebo pre-adolescentním věku (podle epidemiologické situace). Tímto bude jednak uvolněn prostor v dětském očkovacím kalendáři pro nové pediatrické vakcíny, jednak bude dosaženo celoživotní antimeningokokové protektivní imunity. Pro booster vakcinaci v pre-adolescentním věku je plánováno použít konjugovanou tetravakcínu Men A, C, Y, W135.
V USA je prováděno očkování konjugovanou tetravakcínou A, C, Y, W135 u 11–12letých dětí [13]. Diskutuje se o možnosti zařazení této vakcíny do očkovacího schématu malých dětí, což by rozšířilo možnost kontroly invazivního meningokokového onemocnění.
Ve všech zemích EU doporučuje EMGM (The European Meningococcal Disease Society) provádět vakcinaci pracovníků mikrobiologických laboratoří meningokokovou vakcínou vzhledem ke zvýšenému riziku vzniku profesionální meningokokové nákazy [19].
Vakcinační strategie v České republice
Před dostupností konjugované meningokokové vakcíny byla polysacharidová A + C vakcína použita k cílené vakcinaci ohrožené části populace: její rychlá realizace zastavila zvýšenou nemocnost způsobenou N. meningitidis C:2a:P1.2,5;cc11 u adolescentů na Olomoucku [20, 21].
Za současné epidemiologické situace a při současně dostupných meningokokových vakcínách doporučuje NRL pro meningokokové nákazy následující vakcinační strategii v České republice:
- cílenou vakcinaci rizikové části populace;
- vakcinaci osob po kontaktu s invazivním meningokokovým onemocněním způsobeným séroskupinou, proti níž je dostupná vakcína;
- vakcinaci osob v pracovním riziku;
- vakcinaci pacientů s poruchou imunity;
- vakcinaci cestovatelů;
- vakcinaci na žádost za úhradu (bez epidemiologické či zdravotní indikace).
NRL doporučuje provádět očkování konjugovanou vakcínou u dětí před ukončením základní školní docházky a podporuje očkování konjugovanou vakcínou na žádost. Tak jako v řadě evropských zemí je žádoucí spoluúčast zdravotních pojišťoven při hrazení tohoto očkování. Podle nejnovějších doporučení světových expertů je u konjugované vakcíny vhodné provést základní očkování v dětském věku a přeočkování v pre-adolescentním věku. Je doporučeno provádět přeočkování konjugovanou tetravakcínou A,C,Y,W135 k zajištění co nejširší dlouhodobé imunity a je žádoucí, aby tato tetravakcína po úspěšné centrální evropské registraci byla dostupná i v České republice.
Rovněž je vhodné prosazovat očkování osob v pracovním riziku vzniku invazivního meningokokového onemocnění, zejména vybraných pracovníků mikrobiologických laboratoří. U těchto je aplikace konjugované vakcíny velmi vhodná pro vyvolání dlouhodobé imunity a prevenci možného vzniku imunotolerance, k níž může dojít po opakované aplikaci polysacharidové vakcíny.
Je žádoucí, aby konjugovaná tetravakcína A,C,Y,W135 byla dostupná i v České republice, vzhledem k vysoké smrtnosti invazivního meningokokového onemocnění způsobeného v České republice séroskupinou Y.
Při očkování do zahraničí a při současně dostupných vakcínách je nezbytné aplikovat vakcínu podle cílové země. Očkovací centra mají většinou přesné informace o aktuální situaci v jednotlivých zemích. Do tropů a subtropů je vhodná vakcína se složkou A, do arabských zemí vakcína se složkou W135, do některých zemí vakcína se složkou C. Konjugovaná tetravakcína A,C,Y,W135 je vakcínou volby při očkování do zahraničí.
Je nezbytné sledovat vývoj nových MenB vakcín a hodnotit vhodnost jejich použití v České republice (tj. pokrytí zde cirkulujících meningokoků B těmito vakcínami). Jakmile bude vyrobena a následně registrována MenB vakcína vhodná pro Českou republiku, bude žádoucí zahrnout ji do očkovacího schématu malých dětí vzhledem k vysoké nemocnosti způsobené meningokokem B v nejmladší věkové skupině.
Poděkování: Sekvenční charakteristika izolátů N. meningitidis byla podpořena projektem CZ0127 „Sekvenční charakterizace vybraných bakteriálních agens působících závažná onemocnění v ČR“ [http://www.sekvenace.cz/]. Definování alel a sekvenčních typů bylo provedeno srovnáním sekvenčních dat s MLST databází Neisseria [http://pubmlst.org/neisseria/]. Díky patří i pracovníkům NRL pro meningokokové nákazy, všem mikrobiologům, epidemiologům a klinickým lékařům za spolupráci při realizaci programu surveillance invazivního meningokokového onemocnění v České republice.
Do redakce došlo 23. 7. 2010.
MUDr. Pavla Křížová, CSc.
NRL pro meningokokové nákazy
Státní zdravotní ústav
Šrobárova 48
100 42 Praha 10
e-mail: pavla.krizova@szu.cz
Zdroje
1. Raska, K. National and international surveillance of communicable diseases. WHO Chron., 1966, 20, 9, p. 315–321.
2. Raska, K. Epidemiologic surveillance in the control of infectious disease. Rev. Infect. Dis., 1983, 5, 6, p. 1112–1117.
3. Věstník MZ ČR: Metodický návod k epidemiologickým opatřením v ohnisku invazivního meningokokového onemocnění. 1994, 8, 25, 2.
4. Vyhláška MZ ČR ze dne 17. prosince 2008 o systému epidemiologické bdělosti pro vybrané infekce. Sbírka zákonů č.473/2008; částka 151: p. 8010–843.
5. Úřední věstník Evropské unie 2008/426/ES, Rozhodnutí komise ze dne 28.dubna 2008, kterým se mění rozhodnutí 2002/253/ES, kterým se stanoví definice případů pro hlášení přenosných nemocí do sítě Společenství podle rozhodnutí Evropského parlamentu a Rady č. 2119/98/ES (oznámeno pod číslem K(2008) 1589): L 159/46-159/90.
6. Křížová, P., Kalmusová, J., Musílek, M. Molekulární epidemiologie invazivního meningokokového onemocnění v České republice. Epidemiol. Mikrobiol. Imunol. 2006, 55, 4, p. 140–150.
7. Křížová, P., Kalmusová, J., Musílek, M. Studium hypervirulentních komplexů Neisseria meningitidis metodami molekulární biologie a možnosti prevence jejich výskytu v České republice vakcinací. Epidemiol. Mikrobiol. Imunol., 2009, 58, 4, p. 188–196.
8. ECDC Annual epidemiological reports 2007, 2008, 2009. Dostupné na WWW: http://www.ecdc.europa.eu/en/ publications/surveillance_reports/Pages/index.aspx
9. ECDC Core functions of microbiology reference laboratories for communicable disease. Dostupné na WWW: http://www.ecdc.europa.eu/en/publications/Publi cations/Forms/ECDC_DispForm.aspx?ID=538
10. Rappuoli, R. Reverse vaccinology, a genome-based approach to vaccine development. Vaccine, 2001, 19, 17–19, p. 2688–2691.
11. Richmond, P., Kaczmarski, E., Borrow, R. et al. Meningococcal C polysaccharide vaccine induces immunologic hyporesponsiveness in adults that is overcome by meningococcal C conjugate vaccine. J. Infect. Dis., 2000, 181, p. 761–764.
12. Maiden, M. C., Spratt, B. G. Meningococcal conjugate vaccines: New opportunities and new challenges. Lancet, 1999, 354, p. 615–616.
13. Granoff, D. M., Harrison, L. H., Borrow, R. Meningococcal vaccines. In Plotkin, S. A., Offit, P., Orenstein, W. A. (Eds.) Vaccines (5th Edition). WB Sandeurs Company, PA, USA, 2008, p. 399–434.
14. Meningococcal Leadership Forum, Nice, Francie, 3.5.2010.
15. Snape, M. D., Kelly, D. F., Lewis, S., et al. Sero-protection against serogroup C meningococcal is more sustained following immunisation in the second decade of life than the first. BMJ, 2008, 336, p. 1487–1491.
16. Maiden, M. C. J., Ibarz-Pavón, A. B., Urwin, R. et al. Impact of meningococcal serogroup C conjugate vaccines on carriage and herd immunity. J. Infect. Dis., 2008, 197, p. 737–743.
17. Murphy, E., Andrew, L., Lee, K.-L.,et al. Sequence Diversity of the Factor H Binding Protein (fHBP) Vaccine Candidate in Epidemiologically Relevant Strains of Serogroup B Neisseria meningitidis. J. Infect. Dis., 2009, 200, 3, p. 379–389.
18. Trotter, C. L., Ramsay, M. R. Vaccination against meningococcal disease in Europe: review and recommendations for the use of conjugate vaccines. FEMS Microbiol. Rev., 2007, 31, 1, p. 101–107.
19. Sejvar, J. J., Johnson, D., Popovic, T., et al. Assessing the risk of laboratory-acquired meningococcal disease. J. Clin. Microbiol., 2005, 43, 9, p. 4811–4814.
20. Kriz, P., Vlckova, J., Bobak, M. Targeted vaccination with meningococcal polysaccharide vaccine in one district of the Czech Republic. Epidemiol. Infect, 1995, 115, p. 411–418.
21. Křížová, P., Vlčková, J., Bobák, M. Zhodnocení účinnosti cílené vakcinace meningokokovou polysacharidovou vakcínou A+ C v jedné lokalitě České republiky. Epidemiol. Mikrobiol. Imunol., 1995,44, 1, p. 9–14.
Štítky
Hygiena a epidemiologie Infekční lékařství Mikrobiologie
Článek vyšel v časopiseEpidemiologie, mikrobiologie, imunologie
Nejčtenější tento týden
2010 Číslo 4- Stillova choroba: vzácné a závažné systémové onemocnění
- Jak souvisí postcovidový syndrom s poškozením mozku?
- Diagnostika virových hepatitid v kostce – zorientujte se (nejen) v sérologii
- Perorální antivirotika jako vysoce efektivní nástroj prevence hospitalizací kvůli COVID-19 − otázky a odpovědi pro praxi
-
Všechny články tohoto čísla
- Leptospiróza v České republice a možnosti laboratorní diagnostiky
- Protilátky proti pôvodcom niektorých prírodne ohniskových nákaz v sérach darcov krvi zo západného Slovenska
- Surveillance invazivního meningokokového onemocnění a doporučená vakcinace proti meningokokovým nákazám v České republice
- Kolistin v léčbě multirezistentních kmenů Pseudomonas aeruginosa u těžce popálených pacientů
- Sekvenční charakterizace izolátů Haemophilus influenzae působících závažná onemocnění v České republice v letech 2001–2009
- Lipofilné kvasinky rodu Malassezia a choroby kože.II. Atopická dermatitída
- Sporicidní činidla schopná s vysokou účinností inaktivovat spóry Bacillus anthracis
- Významné životní jubileum – MUDr. Vladimír Verhun
- Prof. MUDr. Ctirad John, DrSc. – doyen českých a slovenských lékařských mikrobiologů a imunologů
- 24. Pečenkovy epidemiologické dny
- Epidemiologie, mikrobiologie, imunologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Leptospiróza v České republice a možnosti laboratorní diagnostiky
- Kolistin v léčbě multirezistentních kmenů Pseudomonas aeruginosa u těžce popálených pacientů
- Lipofilné kvasinky rodu Malassezia a choroby kože.II. Atopická dermatitída
- Sporicidní činidla schopná s vysokou účinností inaktivovat spóry Bacillus anthracis
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



