-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Fibrózní dysplazie
Fibrous dysplasia
Fibrous dysplasia (FD) is a congenital skeletal disease characterized by the presence of bone lesions containing fibrous connective tissue. FD occurs in monoostotic or polyostotic form. Rarely, fibrous dysplasia is part of McCune-Albright syndrome together with “café au lait” cutaneous hyperpigmentations and endocrine hyperfunction (especially pubertas praecox, thyrotoxicosis, Cushing’s syndrome, etc.). Clinical symptomatology depends on the extent of the bone disease. Most bone lesions in FD are asymptomatic, with a minority of bone lesions manifesting as pain, bone deformity, or pathological fracture. The following article provides a brief overview of current knowledge about fibrous dysplasia.
Keywords:
bone deformity – fibrous dysplasia – McCune-Albright syndrome – pathological fracture
Autoři: Raška Ivan
Působiště autorů: III. interní klinika – endokrinologie a metabolismu 1. LF UK a VFN v Praze
Vyšlo v časopise: Clinical Osteology 2021; 26(3): 143-146
Kategorie: Přehledové články
Souhrn
Fibrózní dysplazie (FD) je vrozené onemocnění skeletu charakterizované přítomností kostních lézí obsahujících fibrózní pojivovou tkáň. FD se vyskytuje v monoostotické nebo polyostotické formě. Vzácněji je fibrózní dysplazie součástí McCuneova-Albrightova syndromu společně s kožními hyperpigmentacemi charakteru bílé kávy (café au lait) a endokrinními abnormitami ve smyslu jejich hyperfunkce (zejména pubertas praecox, tyreotoxikóza, Cushingův syndrom, atd). Klinická symptomatologie závisí od rozsahu kostního onemocnění. Většina kostních lézí při FD je asymptomatická, menší část kostních lézí se projevuje bolestí, deformitou kosti nebo patologickou frakturou. Následující článek podává stručný přehled současných vědomostí o fibrózní dysplazii.
Klíčová slova:
fibrózní dysplazie – kostní deformita – McCuneův-Albrightův syndrom – patologická zlomenina
Úvod
Fibrózní dysplazie (FD) je benigní vrozené onemocnění skeletu charakterizované přítomností kostních lézí obsahujících fibrózní pojivovou tkáň. FD se vyskytuje v monoostotické nebo polyostotické formě. Monoostotická forma FD patří mezi relativně častá onemocnění, podle některých prací představuje až 7 % benigních kostních lézí [1]. Fibrózní dysplazie může být součástí McCuneova-Albrightova syndromu (MAS) společně s kožními hyperpigmentacemi charakteru bílé kávy (café au lait) a hyperfunkcí endokrinních žláz, který popsal v roce 1936 McCune [2]. MAS je onemocnění s odhadovanou prevalencí mezi 1 : 100 000 až 1 : 1000 000 osob.
Etiologie
FD vzniká v důsledku sporadické postzygotické aktivační somatické mutace genu GNAS1 (Guanine Nucleotide Binding Protein, alpha stimulating) kódujícího alfa podjednotku G-proteinu. Mutace genu GNAS1 způsobuje nadměrnou mitotickou aktivitu a hyperfunkci buněk [3]. Zvýšená stimulace preosteoblastů vede k jejich nadměrné proliferaci a nedostatečné diferenciaci v osteoblasty. V důsledku toho dochází k tvorbě nezralé vláknité kosti, která tvoří obsah kostních lézí a v místě léze nahrazuje kost zdravou. V případě McCuneova-Albrightova syndromu dochází také k hyperfunkci melanocytů, hyperfunkci endokrinních žláz, případně k dalším onemocněním.
Klinická symptomatologie
Klinická symptomatologie závisí na rozsahu a lokalizaci onemocnění. Klinický obraz FD je variabilní se širokým spektrem od asymptomatických forem až po těžké mnohočetné skeletální postižení. Nejčastěji se vyskytuje monoostotická asymptomatická forma FD, která je v typickém případě zachycena jako náhodný rentgenový (RTG) nález. Nejčastěji postihuje metafýzu femuru a lebku [4]. Symptomatická forma FD se projevuje bolestivostí, kulháním (při postižení apendikulárního skeletu), deformitami nebo patologickou zlomeninou. Kostní postižení u závažnějších polyostotických forem FD se manifestuje zpravidla již v dětském věku. Při postižení proximálního femuru dochází v místě největšího zatížení k tvorbě deformity ve tvaru „pastýřské hole“. Postižení obratlů může vést k těžké skolióze. Při postižení kraniofaciální oblasti se rozvíjí deformity kostí, které mohou vést i k funkčnímu postižení. Často jsou do ložiska FD zavzaty oční nervy, ale jen vzácně vedou ke zrakovému postižení. Postižení maxilárních sinů může vést k nazální kongesci [5], postižení zubních alveolů nebo mandibuly či k poruchám okluze [6].
V případě McCune Albrightova syndromu dochází kromě kostních změn, které jsou nejčastěji polyostotické, také k postižení kůže a některých endokrinních orgánů. První manifestace tohoto onemocnění jsou kožní hyperpigmentace typu cafe au lait, které lze zjistit již při narození. Typické jsou nepravidelné okraje pigmentových skvrn. Zajímavá je typická lokalizace skvrn, které obvykle respektují středovou osu těla reflektující tak embryonální migraci buněk (tzv. vývojové linie podle Blaschka) [1]. Z endokrinopatií se u MAS vyskytuje zejména na gonadotropinu nezávislá předčasná puberta charakterizovaná přítomností recidivujících ovariálních cyst u dívek a autonomní nadprodukcí testosteronu u chlapců. Mezi endokrinní poruchy spojené s MAS patří také hyperfunkce štítné žlázy, hyperkortizolismus, nebo hypofosfatemie, která se může manifestovat různým stupněm hypofosfatemické osteomalacie při renálních ztrátách fosfátů způsobené nadprodukcí FGF23 v kostních lezích FD. Zajímavé zjištění přinesla retrospektivní studie hodnotící výskyt akromegalie u pacientů s MAS, v níž až 20 % pacientů s MAS mělo diagnostikovanou akromegalii [7]. Autoři konstatují, že fibrózní dysplazie v kraniofaciální oblasti může být považována za dysmorfické změny obličeje při akromegalii. Podle uvedené studie všichni pacienti s MAS a akromegalii měli postižení báze lební fibrózní dysplazií [7]. Vzácněji mohou být součástí MAS některá postižení gastrointestinálního traktu ve formě hepatitidy, cholestázy, hepatálních adenomů, gastroezofagiálních polypů nebo gastroezofageálního refluxu [1]. Vzhledem k tomu, že kostní léze u FD postihují také kostní dřeň, v případě těžkého polyostotického postižení může být v krevním obrazu přítomna pancytopenie a zjištěna splenomegalie z důvodu extramedulární hematopoézy. V literatuře je v některých případech popisována nutnost splenektomie [8]. Je diskutováno také zvýšené riziko karcinomu prsu v mladším věku u žen s MAS při nadprodukci estrogenů [9]. Riziko malignizace samotné kostní léze při FD je popisováno jako nízké, podle některých prací se riziko malignizace kostní léze zvyšuje při nadprodukci IGF1 [7].
Diagnostika a diferenciální diagnostika
Diagnóza FD je stanovena na základě klinického, radiologického, eventuálně histopatologického vyšetření. Ke stanovení rozsahu onemocnění FD je vhodné scintigrafické vyšetření skeletu (obr. 1, obr. 2) a rentgenové vyšetření postižených lokalit skeletu. Typickým RTG-nálezem při FD je kostní léze charakterizovaná přítomností „kouřového matného skla“ (obr. 3) [1], dále přítomnost deformit (např. deformita typu pastýřské hole v oblasti femuru). Některé části skeletu (obratle, žebra, lebka a pánev) mohou být běžným RTG-snímkem obtížně hodnotitelné a jejich interpretace vyžaduje zkušeného radiologa. Někdy je nápomocné vyšetření výpočetní tomografií (CT – Computed Tomography), obr. 4, obr. 5. V případě MAS je ke stanovení diagnózy potřebná přítomnost minimálně dvou a více klinických znaků typických pro FD/ MAS. V případě podezření na MAS a nálezu „pouze“ monoostotické formy FD se doporučuje genetické potvrzení diagnózy především z genetického vyšetření postižené tkáně. Molekulárně genetické vyšetření zahrnuje vyšetření mutace GNAS1. Detekce patologické mutace genu GNAS závisí na stupni mozaicizmu genu.
Obr. 1. Scintigrafické změny při fibrózní dysplazii odpovídající CT-nálezům (viz obr. 4 a obr. 5, s. 144) 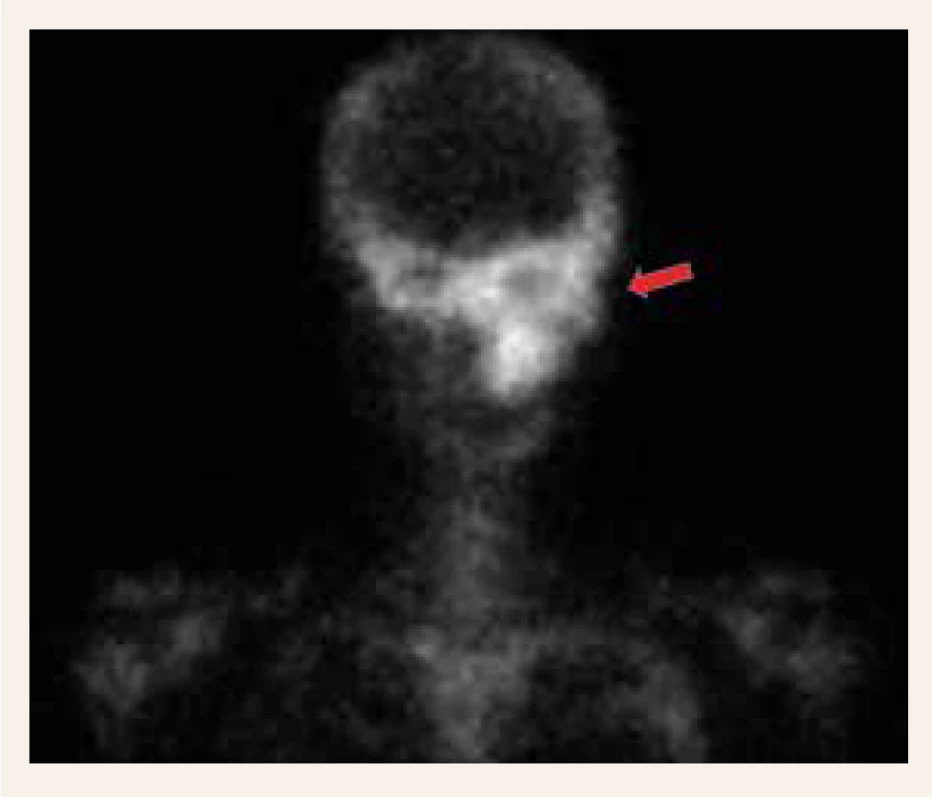
Obr. 2. Scintigrafické změny při fibrózní dysplazii. Postižení žeber, především na levé straně hrudníku, dále v pánvi, v levé kosti kyčelní, mnohočetná drobná ložiska jsou patrná v dlouhých kostech, a to v obou femurech, tibiích v levé fibule a v obou humerech 
Obr. 3. RTG-snímek tibie l. dx. se změnami odpovídajícími fibrózní dysplazii 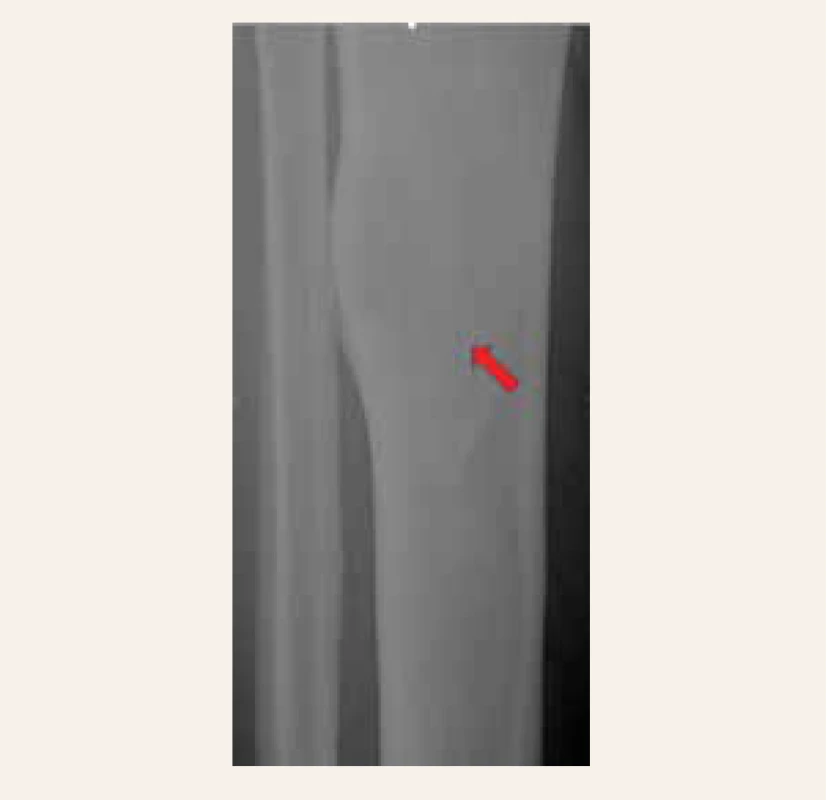
Obr. 4 a obr. 5. CT-zobrazení mnohočetných fibrodysplastických změn kraniofaciálního skeletu při fibrózní dysplazii (označeno šipkou). Kosti jsou zesílené, rozšířené, setřelá struktura trámčité kosti, patrný obraz mléčného skla (ground glass) 
V diferenciální diagnostice kostního postižení u závažnějších polyostotických forem FD může být nápomocná doba manifestace onemocnění. Závažnější formy polyostotického postižení u FD se manifestují především deformitami či zlomeninami již v dětském věku, naopak např. Pagetova kostní choroba se manifestuje obvykle po 4.–5. deceniu [1]. V diferenciální diagnostice kostních lézí při FD činí častěji větší obtíže monoostotická forma FD. Zvažujeme přítomnost dalších kostních afekcí jako např. solitární kostní cysty, neosifikujícího kostního fibromu, enchondromu, ev. dobře diferencovaného osteosarkomu. Histopatologické vyšetření je indikované při diagnostických nejasnostech. Biopsie kostní léze by měla být však indikována s náležitou rozvahou. K diferenciální diagnostice kostních lézí může být nápomocné také vyšetření kalciofosfátového metabolizmu včetně vyšetření sérové koncentrace fosforu a hladiny vitaminu D. Při klinickém podezření na možnost MAS vyšetřujeme také funkci štítné žlázy, sérovou koncentraci ranního kortizolu a koncentraci IGF1. V diferenciální diagnostice MAS přichází v úvahu neurofibromatóza typu 1(NF1), která má s MAS několik překryvných znaků včetně přítomnosti skvrn typu cafe au lait. Okraje skvrn při NF1 však nebývají členité jako u MAS [1].
Management FD
Péče o pacienta s FD/MAS v závislosti na rozsahu a lokalizaci onemocnění může vyžadovat multidisciplinární péči (osteologa, ortopeda, endokrinologa, oftalmologa, otorinolaryngologa atd) s cílem zabránit vzniku deformit, patologických zlomenin a časně detekovat komplikace, ev. komorbidity spojené s onemocněním FD/MAS. V případě klinické potřeby je vhodná RTG - či scintigrafická kontrola k určení progrese onemocnění, ev. detekce nových ložisek. V případě postižení kraniofaciální oblasti je vhodné časné a následně pravidelné vyšetření zraku a sluchu, při postižení páteře detekce, ev. sledování progrese skoliózy. Je doporučena pravidelná kontrola kalciofosfátového metabolizmu, vyšetření IGF1, TSH, ranního kortizolu a některých dalších hormonů jednou ročně.
Léčba FD
Léčbu kostních lézí při FD lze rozdělit na symptomatickou a chirurgickou. V symptomatické léčbě dominuje léčba bolesti vhodným typem analgetik a šetrná rehabilitace. Některé studie i zkušenosti našeho pracoviště poukazují za prospěšné podávání aminobisfosfonátů za účelem zmírnění bolesti a také zpomalení růstu kostních lézí [4], v našich podmínkách zůstává ale užití aminobisfosfonátu off-label léčbou. Cílem chirurgické léčby je zabránit vzniku kostních deformit a patologické zlomenině. Obecně je snaha postupovat konzervativně vzhledem k tomu, že existuje riziko recidivy ložiska FD. Některé studie prokazují, že opakované pokusy o exkochleaci a výplň ložiska kostními štěpy nemusí vést k jejich zhojení, ale naopak mohou způsobit oslabení trabekulární struktury kosti. Riziko recidivy onemocnění snižuje široká excize ložiska nebo jejich radikální resekce a rovněž výběr vhodného osteosyntetického materiálu [10]. V některých případech je však chirurgická intervence nutná. Velkou roli hraje správné načasování výkonu ve snaze včas zabránit vzniku deformity. Deformity typu pastýřské hole v oblasti femuru jsou řešeny korekční osteotomií a nitrodřeňovou fixací kosti hřeby. Obtížná je chirurgická léčba kostních lézí v kraniofaciální oblasti, i zde je v případě nutnosti potřebné zákrok pečlivě naplánovat a kostní lézi odstranit v celém rozsahu. Problematická zůstává rekonstrukční operace resekované části obličejového skeletu. Jsou popsány kazuistiky rozsáhlých operací v oblasti obličeje s následnou náhradou kosti titanovým implantátem vymodelovaným pomocí 3D tiskárny [11]. Léčba přidružených endokrinopatií v případě MAS se v zásadě neliší od standardní klasické léčby dané endokrinopatie.
Závěr
Fibrózní dysplazie patří mezi onemocnění s širokým spektrem klinické symptomatologie počínaje asymptomatickou monoostotickou formou onemocnění a konče těžkým deformizujícím polyostotickým postižením skeletu. Vždy je důležité pomyslet na možnost přitomnosti McCuneova-Albrightova syndromu a náležitě pátrat po přidružených onemocněních. Léčba FD je zejména symptomatická, v případě nutnosti chirurgické intervence je důležité správné načasování výkonu s cílem zabránit vzniku deformit, zlomenin a dalších komplikací spojených s FD.
Práce byla podpořena MZ ČR – RVO VFN64165.
MUDr. Ivan Raška, Ph.D.
Zdroje
- Boyce AM, Florenzano P, de Castro LF et al. Fibrous Dysplasia/McCune-Albright Syndrome. Gene Reviews 2015. In: GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993–2021.
- McCune DJ. Osteitis fibrosa cystica: The case of a nine-year-old girl who also exhibits precocious puberty, multiple pigmentation of the skin and hyperthyroidism. Am J Dis Child 1936; 52 : 743–744.
- Weinstein LS, Shenker A, Gejman PV et al. Activating mutations of the stimulatory G protein in the McCune-Albright syndrome. N Engl J Med 1 991; 3 25(24): 1 688–1695. D ostupné z DOI: < http://dx.doi.org/10.1056/NEJM199112123252403>.
- Kelly MH, Brillante B, Collins MT. Pain in fibrous dysplasia of bone: age-related changes and the anatomical distribution of skeletal lesions. O steoporos I nt 2 008; 1 9(1): 5 7–63. D ostupné z DOI: < http://dx.doi.org/10.1007/s00198–007–0425-x>.
- Cruz-Ferreira AM. Craniofacial Polyostotic Fibrous Dysplasia Initially Diagnosed in a Primary Care Unit. Korean J Fam Med 2019; 40(1): 58–60. Dostupné z DOI: <http://dx.doi.org/10.4082/kjfm.17.0129>.
- Gupta S, Jain S, Newaskar V, Ali M et al. Craniofacial fibrous dysplasia with facial asymmetry, canted occlusion and open bite: a case report with 2 years follow-up. J Contemp Dent Pract 2014; 15(5): 636–645. Dostupné z DOI: <http://dx.doi.org/10.5005/jp-journals-10024–1592>.
- Salenave S, Boyce AM, Collins M et al. Acromegaly and McCune-Albright syndrome. J Clin Endocrinol Metab 2014; 99(6): 1955–1969. <Dostupné z DOI: http://dx.doi.org/10.1210/jc.2013–3826>.
- Mahdi AJ, Connor P, Thakur I. McCune-Albright syndrome-associated bone marrow failure and extramedullary haematopoeisis secondary to fibrous dysplasia. Br J Haematol 2017; 178(2): 179. Dostupné z DOI: <http://dx.doi.org/10.1111/bjh.14690>.
- Majoor BC, Boyce AM, Bovée JV et al. Increased Risk of Breast Cancer at a Young Age in Women with Fibrous Dysplasia. J Bone Miner Res 2018; 3 3(1): 8 4–90. Dostupné z DOI: <http://dx.doi.org/10.1002/jbmr.3286>.
- Pečený J, Šťastný E, Wagenknecht L et al. Fibrózní dysplazie – patofyziologie aortopedická léčba. Pediatr Praxi 2018; 19(2): 72–78. Dostupné z DOI: <http://dx.doi.org/10.36290/ped.2018.015>.
- Kurinec F; Rudinský B; Marinčák L. Chirurgická liečba rozsiahlej fibróznej dysplázie v kraniofaciálnej oblasti – kazuistika. Cesk Slov Neurol N 2016; 79/112(6): 723–727.
Štítky
Biochemie Dětská gynekologie Dětská radiologie Dětská revmatologie Endokrinologie Gynekologie a porodnictví Interní lékařství Ortopedie Praktické lékařství pro dospělé Radiodiagnostika Rehabilitační a fyzikální medicína Revmatologie Traumatologie Osteologie
Článek vyšel v časopiseClinical Osteology
Nejčtenější tento týden
2021 Číslo 3- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
-
Všechny články tohoto čísla
- Q-OSTEOPORÓZA: program pro komplexní hodnocení kvality péče o pacienty v riziku osteoporotických zlomenin
- Fracture Liaison Services: Program koordinované sekundární prevence osteoporotických zlomenin
- Pilotní projekt FLS OSTEO – Sekundární prevence osteoporotických zlomenin
- Fibrózní dysplazie
- Výber z najnovších vedeckých informácií v osteológii
- Lékařská sekce
- Sesterská sekce
- Posterová sekce
- Clinical Osteology
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Fibrózní dysplazie
- Q-OSTEOPORÓZA: program pro komplexní hodnocení kvality péče o pacienty v riziku osteoporotických zlomenin
- Lékařská sekce
- Fracture Liaison Services: Program koordinované sekundární prevence osteoporotických zlomenin
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



