-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
LAPAROSKOPICKÁ CYSTEKTOMIE – PRVNÍ ZKUŠENOSTI
LAPAROSCOPIC RADICAL CYSTECTOMY – FIRST EXPERIENCE
Aims:
The evaluation of our first experience with laparoscopic radical cystectomy.Methods:
A cohort of 12 patients who underwent laparocopic radical cystectomy from April 2014 to June 2015 was assessed. The cohort comprised 11 men and one woman; the mean age was 64.5 (54–74) years. All patients received extensive pelvic lymphadenectomy and cystectomy via laparoscopic approach. The diversion of urine was created extracorporally, eleven ileal conduits and one continent neobladder.Results:
The median follow-up was 10 months. The mean time of surgery was 358 (279–420) minutes. The average blood loss was 266 (100–1000) ml and the mean length of hospital stay was 16.5 (12–30) days. No patient had infection in surgical wounds. One patient died 8 months after surgery from renal failure without subrenal obstruction. One patient with confirmed metastasis in one lymph node underwent adjuvant chemotherapy and palliative chemotherapy for local recurrence and died 9 months after surgery. The patient with continent neobladder developed stenosis in both ureteroileal and urethroileal anastomoses and undergo revision surgery. Nine remaining patients were without complications and in remission.Conclusion:
Laparoscopic radical cystectomy is a minimally invasive and safe alternative to open procedure. We observed lower blood loss, no complication in surgical wounds and shorter convalescence.Key words:
Laparoscopic radical cystectomy, extracorporeal ileal conduit, extensive pelvic lymphadenectomy
Autoři: Michal Balík; Petr Hušek; Lukáš Holub; Josef Košina; Miloš Broďák
Působiště autorů: Urologická klinika FN a LF UK Hradec Králové
Vyšlo v časopise: Ces Urol 2015; 19(3): 194-200
Kategorie: Originální práce
Souhrn
Cíl:
Zhodnocení prvních zkušeností s laparoskopickou radikální cystektomií.Soubor pacientů a metoda:
Byl hodnocen soubor 12 pacientů, kteří podstoupili radikální cystektomii v období od dubna 2014 do června 2015. Jednalo se o jedenáct mužů a jednu ženu, průměrný věk byl 64,5 (54–74) let. Všem pacientům byla provedena rozšířená pánevní lymfadenektomie a cystektomie laparoskopickým přístupem. Derivace moči byla provedena pomocí minilaparotomie, a to jedenáctkrát ileální konduit a jednou kontinentní neovezika.Výsledky:
Medián doby sledování byl 10 měsíců. Průměrná délka celého operačního výkonu byla 358 (279–420) minut. Průměrná krevní ztráta 266 (100–1 000) ml. Průměrná doba hospitalizace byla 16,5 dne (12–30). U žádného pacienta nebyla infekce v operační ráně. Jeden pacient zemřel osm měsíců po operaci na komplikace renální insuficience bez subrenální obstrukce. U jednoho pacienta byla nalezena nádorová infiltrace jedné pánevní uzliny. Pacient podstoupil adjuvantní a později paliativní chemoterapii, ale zemřel devět měsíců po operaci. Pacient s kontinentní neovazikou měl stenózy ureteroileálních anastomóz a uretroileální anastomózy, které musely být reoperovány. Zbylých devět pacientů je bez komplikací a v remisi.Závěr:
Laparoskopická cystektomie je bezpečnou minimálně invazivní alternativou otevřené cystektomie. Byla spojena s nižšími krevními ztrátami, menším počtem raných komplikací a kratší rekonvalescencí.Klíčová slova:
Laparoskopická cystektomie, extrakorporální konduit, laparoskopická pánevní lymfadenektomie.ÚVOD
Otevřená radikální cystektomie je zlatým standardem v léčbě lokálně pokročilého karcinomu močového měchýře. Jedná se o náročnou operaci, při které se odstraňuje močový měchýř a poté se provádí různé typu derivace moči, nejčastěji ze střevní stěny (1). V posledních letech se začíná prosazovat také minimálně invazivní přístup (2). Laparoskopický přístup má určité výhody, zejména lepší přehled v operačním poli, menší krevní ztráty a pro pacienty rychlejší rekonvalescenci (3–5). Nevýhodou je velmi náročný a často dlouhý operační výkon. Cílem této práce je zhodnotit první zkušenosti našeho centra s laparoskopickou radikální cystektomií.
SOUBOR PACIENTŮ A METODA
Byl hodnocen soubor 12 pacientů, kteří mezi dubnem 2014 a červnem 2015 podstoupili laparoskopickou radikální cystektomii na Urologické klinice FN Hradec Králové. Všichni pacienti měli lokálně pokročilý nebo na léčbu refrakterní vysoce rizikový recidivující lokální karcinom močového měchýře (6). Šest pacientů mělo před cystektomií refrakterní karcinom stadia cT1-GIII s mnohočetnými recidivami po BCG terapii a šest pacientů mělo karcinom stadia T2 po transuretrální resekci nádoru. Kontraindikace k laparoskopické cystektomii u našeho souboru byla anamnéza předešlých operací v malé pánvi, lokálně pokročilé nádory (T3–4) nebo rozsáhlé nádory měchýře větší než 7 cm. Průměrný věk pacientů byl 64,5 (54–74) roků. Jednalo se o 11 mužů a jednu ženu. Průměrný body mass index (BMI) byl 28,1 (21,7–40,3).
Všem pacientům byla provedena 2D laparoskopická radikální cystektomie. Následným krokem byla provedena minilaparotomie s extrakorporálně vytvořeným různým typem derivace moči. V jedenácti případech byl vytvořen ileální konduit a u jednoho pacienta kontinentní neovezika (7). Kromě standardních laparoskopických nástrojů byly použity k bezpečné hemostáze moderní, počítačem řízené koagulační nástroje. Pečetící bipolární koagulační nástroj Ligasure byl použit ve třech případech a koagulačně-preparační nástroj Thunderbeat u devíti pacientů. Pacienti měli pouze minimální střevní přípravu a vlastní operace se prováděly v antibiotické cloně. První dávka byla podána v úvodu do anestezie a bylo v ní pokračováno další tři dny. Prevence tromboembolické nemoci byla zajištěna nízkomolekulárním heparinem. První dávka byla podána večer před operací, pokračovala dále v jedné dávce po celou dobu hospitalizace a po propuštění bylo doporučeno jeho podávání ještě minimálně tři týdny. Dvěma pacientům byla podána neodjuvantní chemoterapie doxorubicin‑cisplatina.
Operace začala vytvořením kapnoperitonea punkcí břišní dutiny Veresovou jehlou nad pupkem a pak se vějířovitě založily čtyři porty (obr. 1). Prvním krokem byla oboustranná rozšířená lymfadenektomie. Byla kompletně odstraněna tukově lymfatická tkáň z ilické a obturatorní oblasti. Při této preparaci byly uvolněny močovody, a to v místě zkřížení se společnou ilickou arterií. Ty byly dále vypreparovány až k močovému měchýři a po zajištění klipy a přerušeny. Distální konce ureterů byly zaslány na rychlé histologické vyšetření. Dalším krokem bylo vlastní odstranění močového měchýře. U mužů společně s prostatou a u žen společně s dělohou a adnexy. Propojením otvorů v nástěnném peritoneu na ilickými cévami a preparací mezi zadní stěnou močového měchýře a stěnou rekta byly skeletizovány pedikly močového měchýře a u mužů prostaty. Na tyto byly aplikovány Hem ‑ -o-lock klipy a nakonec přerušeny. Velké cévy byly klipovány samostatně, k jejich lepší vizualizaci přispělo zvětšení laparoskopického obrazu. U mužů se následně protne endopelvická fascie a oddělí prostata od pánevního dna, podobně jako u radikální prostatektomie. U žen se před vlastní cystektomií oddělí ovaria a tuby. S výhodou se využije koagulační pečetící nástroj. Děloha se odděluje a odstraňuje společně s močovým měchýřem. Pro zamezení úniku vzduchu pochvou při oddělování děložního čípku je vhodné zavézt do pochvy Foleyův katétr a napustit balon na minimálně 15 ccm.
Obr. 1. Umístění laparoskopických portů Legenda: 1 – Port pro kameru (10 eventuálně 5 mm), 2 – Pracovní port 10 mm pro koagulaci a klipování, 3–5 – Pracovní porty 5 mm Fig. 1. Placement of laparoscopic ports Legend: 1 – Port for optic (10 eventually 5 mm), 2 – Working port 10 mm for coagulation and clipping, 3–5 – Working ports 5 mm 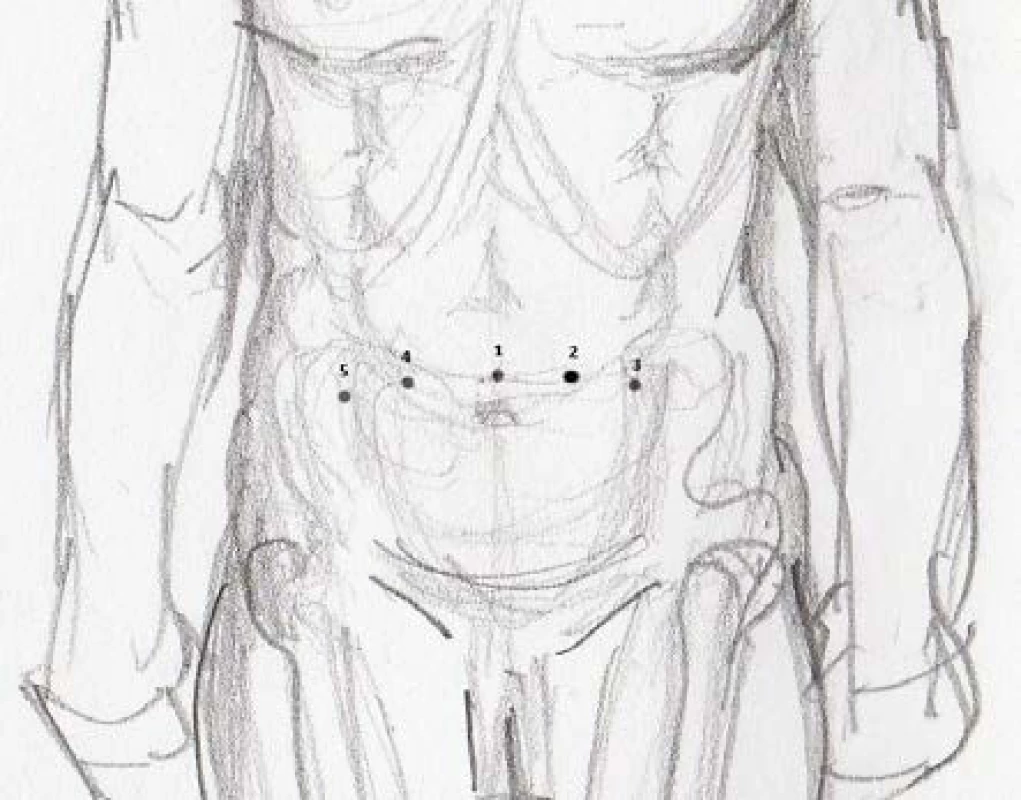
Následně byla provedena všem pacientům profylaktická appendektomie a levostranný močovod byl podvlečen pod esovitou kličkou doprava. Dále byla provedena minilaparotomie podélným řezem délky 7 cm dlouhým vlevo podél pupku (obr. 2). Ileální konduit a v jednom případě kontinentní pouch byl proveden extrakorporálně. Zaklapované distální močovody byly vytaženy před laparotomií a byly do nich zavedeny uretrální cévky Ch 6. Distální konce byly incidovány v posledních 3 cm a byly sešity k sobě (8). Vše bylo šito vstřebatelným materiálem Vicryl 3.0. Takto vytvořené spojení ureterů bylo anastomozováno k orálnímu konci exkludované kličky. Po exkluzi preterminální kličky ilea byl k obnovení kontinuity střeva použit stapler. Uretrální cévky byly ponechány deset dnů od operace. U nekontinentní derivace byla vytvořena ileostomie v pravém podbřišku a u kontinentního pouche byla uretrovezikální anastomóza provedena opět laparoskopicky, a to pokračujícím stehem VLoc.
Obr. 2. Minilaparotomie – schema Fig. 2. Mini-laparotomy – pattern 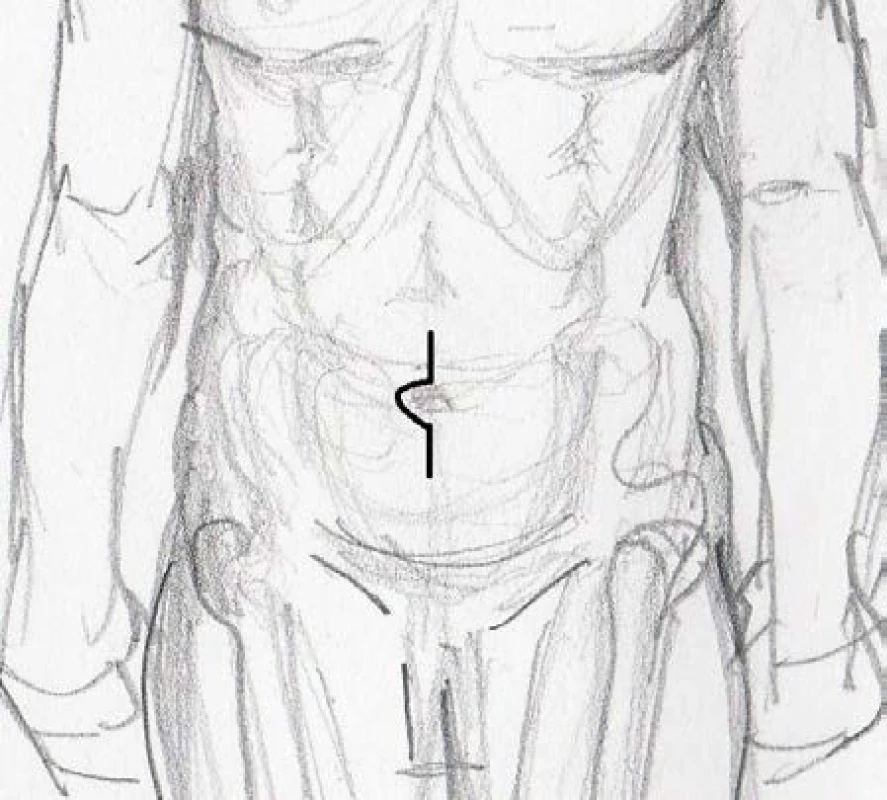
U sledovaného souboru byly hodnoceny operační výsledky a komplikace a dále byly analyzovány onkologické a funkční výsledky. Pacienti byli sledováni v pravidelných tříměsíčních intervalech první dva roky po operaci. Pokud byli pacienti bez recidiv a komplikací, byl interval prodloužen na šest měsíců.
VÝSLEDKY
Medián doby sledování byl deset měsíců. Průměrná délka celého operačního výkonu byla 358 (279–420) minut. Průměrná krevní ztráta 266 (100–1 000) ml. Největší krevní ztráta byla u prvního pacienta, a to 1 000 ml. U žádného z dalších pacientů krevní ztráta nepřesáhla 350 ml. Všechny rychlé histologie z distálních ureterů byly negativní. Definitivní histologie byla třikrát uroteliální karcinom stadia pT3a, pětkrát pT2, dvakrát pT1+Cis a dvakrát pTa+Cis. Průměrná doba hospitalizace byla 16,5 dne (12–30). U žádného pacienta nebyla infekce v operační ráně, ani jiná komplikace v operačních ranách po portech nebo po minilaparotomii.
Průměrný počet odebraných lymfatických uzlin v rámci pánevní lymfadenektomie byl deset (5–18).
U jednoho pacienta byla prokázána metastáza do jedné lymfatické uzliny, u zbylých 11 pacientů byly uzliny bez nádorové infiltrace. U dvou pacientů byl v rámci definitivního histologického vyšetření náhodně prokázán karcinom prostaty. Pacient s nádorovou infiltrací pánevních uzlin prodělal adjuvantní chemoterapii a po sedmi měsících od operace měl prokázanou lokální recidivu. I přes záchrannou chemoterapii pacient zemřel v souvislosti se základním onemocněním devět měsíců po operaci. Všichni ostatní pacienti byli bez lokální recidivy nebo vzdálených metastáz.
Pacient po ortotopické náhradě měl strikturu ureteroileálních junkcí a podstoupil reoperaci. Byla vytvořena oboustranná nová ureteroileální anastomóza. Další komplikací u tohoto pacienta byla stenóza uretroneovezikální junkce. Jako léčba byla provedena bipolární transuretrální resekce jizvy v anastomóze. Tato jizva po měsíci recidivovala.
Pacient odmítl autokatetrizaci a souhlasil se zavedením permanentního katétru.
Další pacient zemřel osm měsíců od operace na komplikace renální insuficience, ale bez známek subrenální obstrukce. Pacient neměl prokázanou recidivu uroteliálního karcinomu.
Zbylých devět pacientů je bez obtíží, bez recidivy uroteliálního karcinomu a bez zhoršení ledvinných funkcí.
DISKUZE
Minimálně invazivní přístup se v mnoha urologických centrech prosadil u radikální prostatektomie, nefrektomie a částečně u resekce ledvin. Výhody jsou menší operační trauma pro pacienta, menší krevní ztráty a rychlejší rekonvalescence (2–5). Další výhodou je výrazně menší operační incize a podle našich zkušeností také menší tendence k serózní sekreci z operační rány. Na druhou stranu je cystektomie velmi náročný operační výkon s rizikem častých a nezřídka závažných komplikací (1). První publikované zkušenosti s laparoskopickou radikální cystektomií pocházejí z devadesátých let minulého tisíciletí (9–11). Laparoskopická cystektomie byla zpočátku brána s určitými rozpaky, ale s přibývajícími zkušenostmi se postupně stále více prosazuje (12). Kromě čistě laparoskopického přístupu se také prosazuje robotem asistovaná radikální cystektomie (13). Laparoskopický přístup umožňuje také provádět velmi precizně rozšířenou pánevní lymfadenektomii (14). Tím lze dosáhnout odstranění většího počtu lymfatických uzlin, a to může být spojeno s pozitivním terapeutickým efektem (14, 15).
Radikální cystektomie přestavuje velký operační zákrok s velkým rizikem komplikací, a to během operace nebo v časném pooperačním období (do 90 dnů od operace). Celková četnost komplikací u otevřené cystektomie se pohybuje okolo 50 %, ale v drtivé většině se jedná o méně závažné komplikace (1). Podle publikovaných studií se pohybuje celková četnost komplikací u laparoskopické radikální cystektomie v rozmezí od 30 do 59 %. Jednalo se většinou o méně závažné komplikace a mortalita se pohybovala v publikovaných studiích v rozmezí 0–2 % (16–18). Při porovnání laparoskopické nebo otevřené radikální cystektomie nebyla četnost komplikací výrazně odlišná (19, 20).
Hodnocení dlouhodobých onkologických výsledků je problematické. Zejména pro krátkou historii laparoskopické radikální cystektomie. Podle prvních srovnávacích studií porovnávajících otevřenou, laparoskopickou a robotem asistovanou cystektomii nebyl prokázán významný rozdíl (16, 21).
Důkladnější zhodnocení by měly přinést výsledky rozsáhlejších a nejlépe randomizovaných studií. Naše vlastní zkušenosti ukazují, že se jedná o komplikovaný operační výkon, který je ovšem proveditelný a pro pacienta bezpečný. Rychlejší rekonvalescence všech pacientů nám byla povzbuzením k dalším výkonům. Dalším pozitivem, který jsme potvrdili na našem souboru, byly výrazně nižší krevní ztráty. Nejvyšší byly u prvního pacienta, kde došlo ke krvácení z vnitřní ilické arterie. Krvácení bylo ošetřeno klipy. U tohoto pacienta byla celková krevní ztráta 1 000 ml. U dalších pacientů již byla výrazně nižší. Riziko vyšších krevních ztrát u prvních pacientů operovaných laparoskopicky bylo publikováno Hemalem et al. 2004 (22). Po získání větších zkušeností je bezpečnější ošetření laterálních pediklů. U našeho souboru nedošlo k jinému poškození okolních orgánů nebo podobné komplikaci. Všem pacientům byla provedena profylaktická appendektomie, která se v našem centru dlouhodobě provádí u otevřené cystektomie. Extrakorporální vytvoření konduitu nebo neoveziky bylo zvoleno s cílem neprodlužovat tento operační výkon. Do budoucna počítáme také s intrakorporálním prováděním derivace moči. K této operaci byli vybráni pacienti, kteří neměli lokálně pokročilé karcinomy stadia cT3b-4 nebo pacienti po více předešlých břišních operacích. Těmto pacientům byla provedena otevřená cystektomie. Výběr tedy nebyl randomizovaný. Nejednalo se o srovnatelné soubory, proto nebyly tyto soubory srovnávány.
Největší výhodou laparoskopického přístupu je lepší operační přehled pomocí kamerou snímaného obrazu. Současně používané systémy jsou vysoce kvalitní, používají techniku vysokého rozlišení (HDTV) a umožňují také zvětšení operované oblasti. Všechny operace byly provedeny 2D optikou a je pravděpodobné, že 3D kamera by přinesla další zpřesnění. Zvětšení obrazu umožňuje provést velmi precizní pánevní lymfadenektomii (14, 15). Další výhodou, které přináší zvětšení obrazu, je možnost separátního klipování velkých cév v laterálních pediklech. Tím se výrazně snižuje riziko většího krvácení. Renomovaná centra udávají průměrné krevní ztráty u otevřené radikální cystektomie v rozmezí 400–1 700 ml (2, 23). Velkou výhodou nám byly zkušenosti s laparoskopické radikální prostatektomie nebo podobných operací v malé pánvi. Po získání dalších zkušeností by se mohly minimálně invazivní metody stát první volbou u radikální cystektomie. Podle recentně publikovaných prací nebyl zjištěn v onkologických výsledcích mezi otevřeným a minimálně invazivním přístupem (24–26). Čas ukáže, zda to bude čistě laparoskopická nebo robotem asistovaná, jak se tomu stalo například ve Spojených státech nebo v nejvyspělejších státech Evropské Unie.
ZÁVĚR
Prokázali jsme, že laparoskopická radikální cystektomie je minimálně invazivní alternativa radikální cystektomie. Nevýhodou je delší operační čas, a to zejména u prvních výkonů. Velkou výhodou je možnost precizní preparace, nižší krevní ztráty a kratší rekonvalescence. U našeho souboru byla také výrazně nižší incidence komplikací spojených s hojením operačních ran. Předběžné onkologické výsledky byly srovnatelné s otevřeným přístupem.
Poděkování
Laparoskopická radikální cystektomie by si jen obtížně hledala své místo mezi modalitami léčby pokročilého uroteliálního karcinomu močového měchýře na našem pracovišti bez neutuchající podpory primáře urologického oddělení nemocnice v Novém Jičíně – MUDr. Miroslava Štursy. Za to mu patří náš velký dík.
Podpořeno programem PRVOUK 37/04 .
Došlo: 25. 8. 2015
Přijato: 22. 9. 2015
Střet zájmů: žádný
Prohlášení o podpoře: Autor prohlašuje, že zpracování článku nebylo podpořeno farmaceutickou firmou.
Kontaktní adresa:
MUDr. Michal Balík
Urologická klinika FN a LF UK Hradec Králové
Sokolská 518, 500 05 Hradec Králové
e-mail: balikmic@fnhk.cz
Zdroje
1. Witjes JA, Compérat E, Cowan NC, et al. EAU guidelines on muscle-invasive and metastatic bladder cancer: summary of the 2013 guidelines. Eur Urol. 2014; 65 : 778–792.
2. Khan MS, Challacombe B, Elhage O, et al. A dual-centre, cohort comparison of open, laparoscopic and robotic-assisted radical cystectomy. Int J Clin Pract. 2012; 66 : 656–662.
3. Basillote JB, Abdelshehid C, Ahlering TE, Shanberg AM. Laparoscopic assisted radical cystectomy with ileal neobladder: a comparison with the open approach. J Urol 2004; 172 : 489–493.
4. Haber GP, Crouzet S, Gill IS. Laparoscopic and robotic assisted radical cystectomy for bladder cancer: a critical analysis. Eur Urol 2008; 54 : 54–62. 5. Hora M, Eret V, Ürge T, et al. Role laparoskopie v urologii, Ces Urol 2011; 15 : 93–100.
6. Babjuk M, Burger M, Zigeuner R, et al. European Association of Urology. EAU guidelines on non-muscle‑invasive urothelial carcinoma of the bladder: update 2013. Eur Urol. 2013; 64 : 639–653.
7. Pagano F, Artibani W, Aragona F, et al. Vesica ileale Padovana (VIP): surgical technique, long-term functional evaluation, complications and management. Arch Esp Urol. 1997; 50 : 785–793.
8. Kouba E, Sands M, Lentz A, et al. A comparison of the Bricker versus Wallace ureteroileal anastomosis in patients undergoing urinary diversion for bladder cancer. J Urol. 2007; 178 : 945–948.
9. Sánchez de Badajoz E, Gallego Perales JL, Reche Rosado A, et al. Laparoscopic cystectomy and ileal conduit: case report. J Endourol. 1995; 9 : 59–62.
10. Denewer A, Kotb S, Hussein O, El-Maadawy M. Laparoscopic assisted cystectomy and lymphadenectomy for bladder cancer: initial experience. World J Surg. 1999; 23 : 608–611.
11. Gill IS, Fergany A, Klein EA, et al. Laparoscopic radical cystoprostatectomy with ileal conduit performed completely intracorporeally: the initial 2 cases. Urology. 2000; 56 : 26–29.
12. Rassweiler J. Laparoscopic radical cystectomy. Where are we really? Eur Urol 2008; 54 : 19–20.
13. Challacombe BJ1, Bochner BH, Dasgupta P, et al. The role of laparoscopic and robotic cystectomy in the management of muscle-invasive bladder cancer with special emphasis on cancer control and complications. Eur Urol. 2011; 60 : 767–775.
14. Chlosta P, Drewa T, Siekiera J, et al. Lymph node dissection during laparoscopic (LRC) and open (ORC) radical cystectomy due to muscle invasive bladder urothelial cancer (pT2–3, TCC). Wideochir Inne Tech Maloinwazyjne. 2011; 6 : 127–131.
15. Mmeje CO, Nunez-Nateras R, Nielsen ME, et al. Oncologic outcomes for lymph node-positive urothelial carcinoma patients treated with robot assisted radical cystectomy: with mean follow-up of 3.5 years. Urol Oncol. 2013; 31 : 1621–1627.
16. Musch M, Janowski M, Steves A, et al. Comparison of early postoperative morbidity after robot-assisted and open radical cystectomy: results of a prospective observational study. BJU Int. 2014; 113 : 458–467.
17. Albisinni S, Oderda M, Fossion L, et al. The morbidity of laparoscopic radical cystectomy: analysis of postoperative complications in a multicenter cohort by the European Association of Urology (EAU)-Section of Uro-Technology. World J Urol. 2015 Jul 2. [Epub ahead of print].
18. Montes SF, Rodríguez IG, Ugarteburu RG, et al. Intraoperative laparoscopic complications for urological cancer procedures. World J Clin Cases. 2015; 16 : 450–456.
19. Albisinni S, Rassweiler J, Abbou CC, et al. Long-term analysis of oncological outcomes after laparoscopic radical cystectomy in Europe: results from a multicentre study by the European Association of Urology (EAU) section of Uro-technology. BJU Int. 2015; 115 : 937–945.
20. Sterrett S, Mammen T, Nazemi T, et al. Major urological oncological surgeries can be performed using minimally invasive robotic or laparoscopic methods with similar early perioperative outcomes compared to conventional open methods. World J Urol. 2007; 25 : 193–198.
21. Challacombe BJ, Bochner BH, Dasgupta P, Gill I, et al. The role of laparoscopic and robotic cystectomy in the management of muscle-invasive bladder cancer with special emphasis on cancer control and complications. Eur Urol. 2011; 60 : 767–775.
22. Hemal AK, Kumar R, Seth A, Gupta NP. Complications of laparoscopic radical cystectomy during the initial experience. Int J Urol. 2004; 11 : 483–488.
23. Fonseka T, Ahmed K, Froghi S, et al. Comparing robotic, laparoscopic and open cystectomy: a systematic review and meta-analysis. Arch Ital Urol Androl. 2015; 87 : 41–48.
24. Snow-Lisy DC, Campbell SC, Gill IS, et al. Robotic and laparoscopic radical cystectomy for bladder cancer: long-term oncologic outcomes. Eur Urol. 2014; 65 : 193–200.
25. Khan MS, Elhage O, Challacombe B, et al. Long-term outcomes of robot-assisted radical cystectomy for bladder cancer. Eur Urol. 2013; 64 : 219–224.
26. Yuh B, Wilson T, Bochner B, et al. Systematic review and cumulative analysis of oncologic and functional outcomes after robot-assisted radical cystectomy. Eur Urol. 2015; 67 : 402–222.
Štítky
Dětská urologie Nefrologie Urologie
Článek vyšel v časopiseČeská urologie
Nejčtenější tento týden
2015 Číslo 3- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Kterým pacientům se SLE nasadit biologickou léčbu?
- Nostiriazyn – spolehlivá 1. volba u nekomplikovaných infekcí močových cest
- Nitrofurantoin s řízeným uvolňováním: osvědčená účinnost, lepší snášenlivost a méně tablet při akutní cystitidě
- Jak souvisí časné zahájení biologické léčby SLE/LN s prevencí nevratného poškození?
-
Všechny články tohoto čísla
- Editorial
- FOTOSELEKTIVNÍ VAPORIZACE PROSTATY (PVP) S LAPAROSKOPICKOU DIVERTIKULEKTOMIÍ (LD) MOČOVÉHO MĚCHÝŘE
- EXTRA-ANATOMICKÉ STENTY JAKO ALTERNATIVA NEFROSTOMIE
- LAPAROSKOPICKÁ CYSTEKTOMIE – PRVNÍ ZKUŠENOSTI
- LYMFOMY UROGENITÁLNÍHO TRAKTU
- SROVNÁNÍ CHARAKTERISTIKY SEMINOMŮ A NONSEMINOMŮ U SOUBORU PACIENTŮ, KTEŘÍ PODSTOUPILI RADIKÁLNÍ ORCHIEKTOMII PRO TUMOR VARLETE
- IATROGENNÍ LÉZE MOČOVODU DIAGNOSTIKOVÁNA PO MĚSÍCI
- ANOMÁLIE URACHU – VZÁCNÁ PŘÍČINA BOLESTÍ BŘICHA A HOREČNATÝCH STAVŮ
- ASYNCHRONNÍ NÁDOROVÁ KVADRUPLICITA (TRIPLICITA UROLOGICKÝCH MALIGNIT)
- PAGE KIDNEY – POZDNÍ PREZENTACE SUBKAPSULÁRNÍHO HEMATOMU LEDVINY U MLADÉHO CHLAPCE
- VÝROČNÁ KONFERENCIA SLOVENSKEJ UROLOGICKEJ SPOLOČNOSTI V PREŠOVE 10.–12. 6. 2015
- ZPRÁVA Z WORKSHOPU SEKCE PRO URODYNAMIKU, NEUROUROLOGII A UROGYNEKOLOGII (SUNU) KONANÉHO V ČERVNU LETOŠNÍHO ROKU V KYJOVĚ
- Česká urologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- ANOMÁLIE URACHU – VZÁCNÁ PŘÍČINA BOLESTÍ BŘICHA A HOREČNATÝCH STAVŮ
- EXTRA-ANATOMICKÉ STENTY JAKO ALTERNATIVA NEFROSTOMIE
- IATROGENNÍ LÉZE MOČOVODU DIAGNOSTIKOVÁNA PO MĚSÍCI
- LAPAROSKOPICKÁ CYSTEKTOMIE – PRVNÍ ZKUŠENOSTI
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



