-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Ranibizumab v léčbě choroidální neovaskularní membrány z jiné příčiny než věkěm podmíněná makulární degenerace
Autoři: A. Stepanov; M. Středová; J. Dusová; N. Jirásková; J. Studnička
Působiště autorů: Fakultní nemocnice Hradec Králové, Oční klinika, přednostka prof. MUDr. Naďa Jirásková, Ph. D., FEBO ; Univerzita Karlova, Lékařská fakulta v Hradci Králové, katedra očního lékařství
Vyšlo v časopise: Čes. a slov. Oftal., 75, 2019, No. 3, p. 138-144
Kategorie: Původní práce
doi: https://doi.org/10.31348/2019/3/4Souhrn
Cíl: Zjistit bezpečnost a účinnost ranibizumabu v léčbě choroidální neovaskularizace (CNV) způsobené jinými chorobami než věkem podmíněnou makulární degenerací (VPMD).
Soubor: Bylo zařazeno 21 pacientů průměrného věku 61 17,2 let (min. 16, max. 85) s CNV způsobenou jinými příčinami než VPMD, konkrétně patologickou myopií (n=11), angioidními pruhy (n=3), centrální serózní chorioretinopatií (n=2), makulární dystrofií Severní Karolíny (n=1), dominantními familiárními drúzami sítnice (n=1) a idiopatickou CNV (n=3).
Metodika: Pacienti byli léčeni na Oční klinice Fakultní nemocnice v Hradci Králové třemi úvodními intravitreálními injekcemi přípravku ranibizumab (Lucentis) 0,5 mg s měsíčním odstupem jednotlivých dávek a následnými dávkami dle potřeby - léčebný režim pro re nata (PRN). Nejlépe korigovaná zraková ostrost (NKZO) byla zhodnocena na ETDRS optotypech (Early Treatment Diabetic Retinopathy Study), centrální retinální tloušťka (CRT) byla měřena pomocí optické koherenční tomografie (OCT) (Cirrus, Zeiss). Tyto parametry byly sledovány před zahájením studie a dále v době 1 (pouze NKZO), 4, 8 a 12 měsíců v průběhu léčby. Sledovali jsme také výskyt očních i systémových nežádoucích účinků.
Výsledky: Zaznamenali jsme statisticky významné zlepšení průměrné hodnoty NKZO o 11,4 písmen (p<0,001) na konci sledovacího období v podskupině pacientů s myopickou CNV. V podskupině pacientů s CNV z jiných příčin bylo zlepšení NKZO o 5,9 písmen (p=0,043). Průměrná hodnota CRT po 12 měsících statisticky významně poklesla o 42,2 µm (p=0,028) u pacientů s myopickou CNV a o 119,4 µm (p=0,002) u pacientů s CNV z jiných příčin. Nezjistili jsme žádné závažné oční ani systémové nežádoucí účinky související se samotným přípravkem Lucentis ani s jeho injekčním podáním.
Závěr: Léčba intravitreální injekcí ranibizumabu podávaná v režimu pro re nata po úvodních třech měsíčních dávkách prokázala efektivitu a bezpečnost v léčbě CNV jiné etiologie než VPMD během ročního sledování.
Klíčová slova:
myopická CNV – jiné příčiny CNV – anti-VEGF – Lucentis – ranibizumab
ÚVOD
Choroidální neovaskularizace (CNV) je charakterizována přítomností patologických choroidálních cév pod retinálním pigmentovým epitelem (RPE) nebo pod sítnicí. Příčina vzniku CNV není známa, v její patogenezi je však prokázána role angiogenních faktorů, například vaskulárního endoteliálního růstového faktoru (VEGF) [3,10,14].
Nejčastější příčinou vzniku CNV je věkem podmíněná makulární degenerace (VPMD), která, pokud není léčena, vede k významnému poklesu zrakové ostrosti u pacientů ve věku nad 55 let [5]. Mezi další příčiny vzniku CNV patří patologická myopie, syndrom předpokládané oční histoplazmózy, angioidní pruhy, uveitidy, choroidální ruptura nebo trauma, centrální serózní chorioretinopatie a centrální dystrofie.
Choroidální neovaskularizace z jiných příčin, než je VPMD a patologická myopie, je vzácná a obvykle se vyskytuje u dospělých v produktivním věku [2].
Myopie je nejčastější příčinou poklesu zrakové ostrosti v celkové populaci, zejména ve východní Asii, kde postihuje přibližně 40 % dospělých ve věku nad 40 let [20]. Patologická myopie je nejtěžší formou myopie a její definice zahrnuje refrakční chybu minimálně -6,0 dioptrií nebo axiální délku bulbu 26,5 mm a více a také degenerativní změny skléry, cévnatky a sítnice [6,15,17].
Choroidální neovaskularizace na podkladě patologické myopie (myopická CNV) je jednou z nejzávažnějších komplikací patologické myopie u pacientů v produktivním věku s prevalencí 0,04 % až 0,05 % v celkové populaci [4,7].
V této práci hodnotíme léčbu intravitreálně podávaným ranibizumabem m v režimu pro re nata (PRN) u pacientů s CNV způsobené jinými chorobami než VPMD.
SOUBOR A METODIKA
Do studie prováděné na Oční klinice ve Fakultní nemocnici v Hradci Králové v období od ledna 2016 do listopadu 2017 bylo zahrnuto 21 pacientů. Tabulka 1 ukazuje základní demografické a klinické charakteristiky souboru. K potvrzení diagnózy byla použita fluorescenční angiografie (FA), fotografie fundu a optická koherenční tomografie (OCT Cirrus, Zeiss). Pacienti byli zařazeni do studie, pokud podepsali písemný informovaný souhlas a byla jim diagnostikována CNV z jiné příčiny než VPMD. Konkrétně se jednalo o následující diagnostické jednotky: angioidní pruhy, centrální serózní chorioretinopatie, patologická myopie (obrázek 1), makulární dystrofie Severní Karolíny, dominantní familiární drúzy sítnice a idiopatická CNV (obrázek 2). Pacienti s patologickou myopií měli průměrnou axiální délku oka 29,21 mm a průměrná refrakce činila -11,67 dioptrií. Léčba ranibizumabem byla v dávkovacím režimu PRN, tedy po prvních třech měsíčních injekcích následovaly kontroly s eventuálním podáním další injekce při přetrvávání známek aktivity CNV podle OCT (intra a subretinální tekutina, ablace RPE) a také při nálezu čerstvé makulární hemoragie. Příprava léku i jeho podání probíhalo za aseptických podmínek. Aplikace ranibizumabu (0,5 mg v 0,05 ml) byla provedena v lokální anestezii za pomoci 30-gauge jehly transsklérálně 3,5 až 4,0 mm od limbu.
Tab. 1. Vstupní demografické a klinické charakteristiky 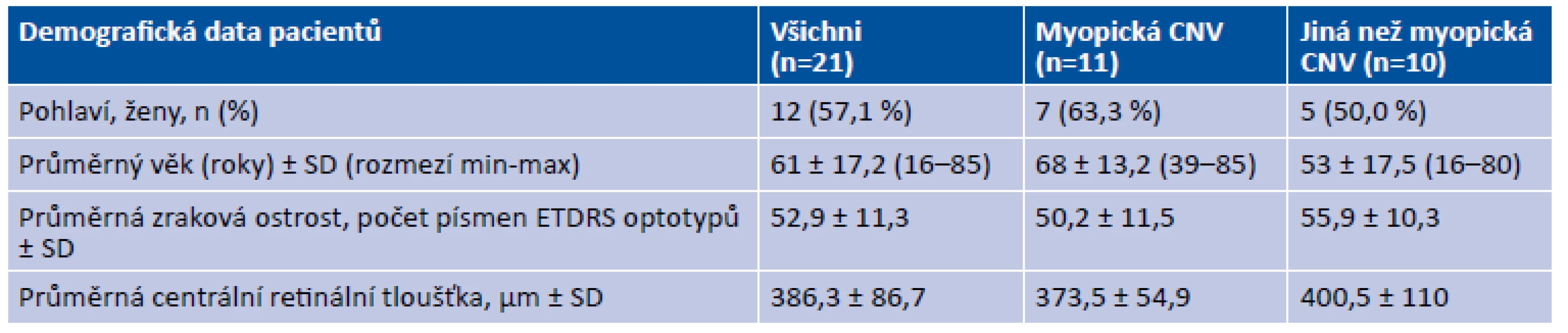
n = počet očí; CNV = choroidální neovaskularizace; ETDRS = Early Treatment Diabetic Retinopathy Study; SD = standardní odchylka Obr. 1. Choroidální neovaskularizace u pacienta s patologickou myopií
A. Foto fundu před zahájením léčby ranibizumabem. Ložisko neovaskulární membrány, v nasální části subretinální hemoragie B-C. HD-OCT před léčbou. Hyperreflektivní tkáň, prorůstající retinální pigmentový epitel. Edém neuroretiny s centrální
retinální tloušťkou 675 μm D-E. HD-OCT po léčbě. Pokles edému, náznak foveolární deprese
F. Foto fundu po léčbě. Ložisko se ohraničuje, hemoragie nejsou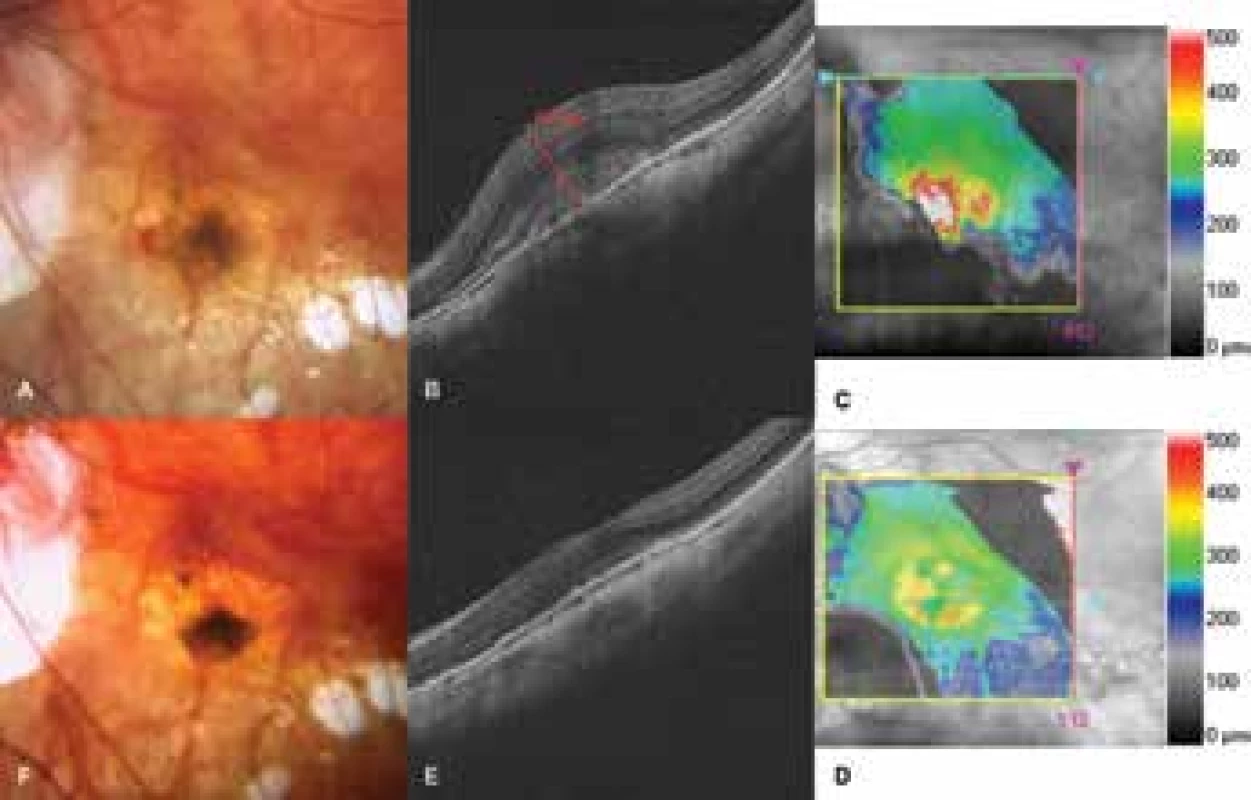
Obr. 2. Idiopatická choroidální neovaskularizace
A. Foto fundu před zahájením léčby ranibizumabem. Ložisko neovaskulární membrány, kolem ložiska subretinální hemoragie
B. HD-OCT před léčbou. Ablace a edém neuroretiny, elevace retinálního pigmentového epitelu
C-D. FAG nález při první návštěvě. Postupně gradující hyperfluorescence neovaskulární membrány, blokáda fluorescence z důvodu subretinální hemoragie
E. HD-OCT po léčbě. Pokles edému neuroretiny a retinálního pigmentového epitelu
F. Foto fundu po léčbě. Ohraničeno ložisko s pigmentem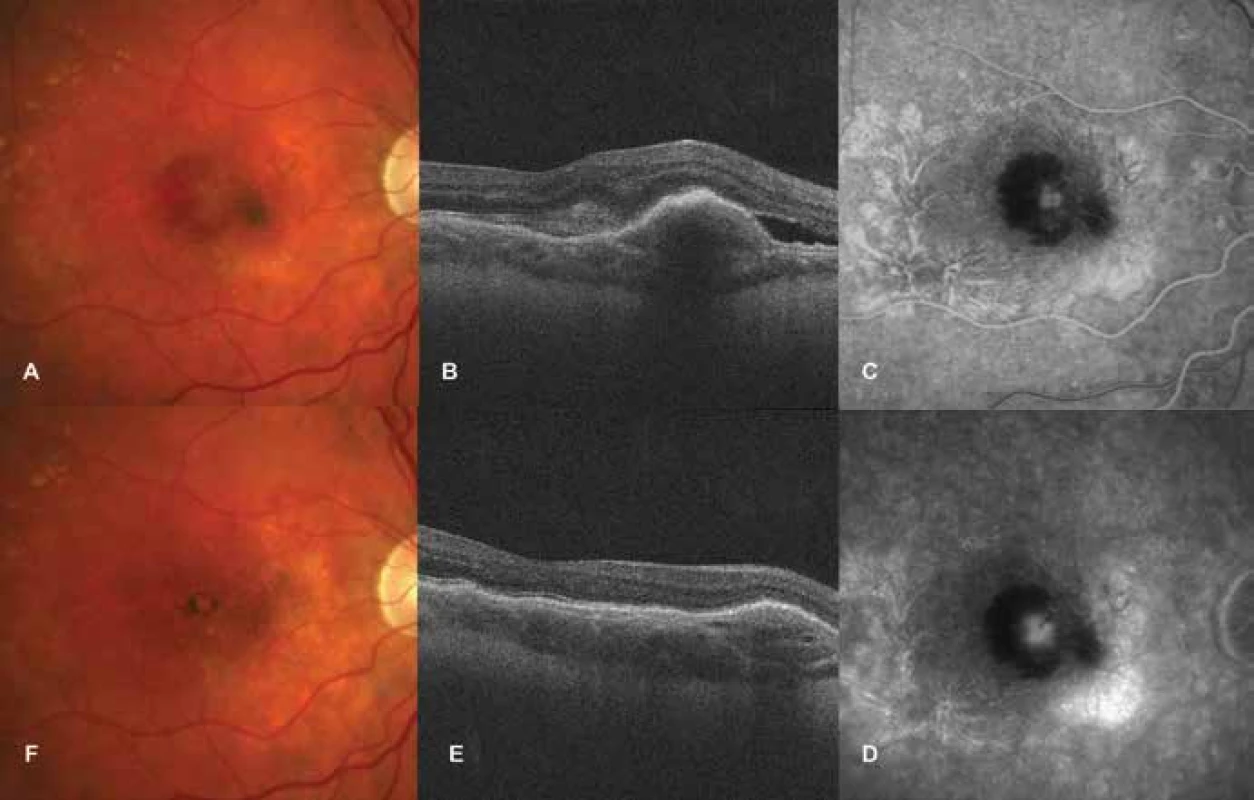
Hodnotili jsme výskyt očních a systémových nežádoucích účinků, procento pacientů, kteří získali 15 a více písmen nejlépe korigované zrakové ostrosti (NKZO) na ETDRS optotypech a také vývoj centrální retinální tloušťky (CRT) dle OCT. Vyšetření byla prováděna s odstupem 1 (pouze NKZO), 4, 8 a 12 měsíců od zahájení léčby.
Statistická analýza
Statistická analýza byla provedena za pomoci softwaru IBM SPSS Statistics 23. Kvantitativní údaje jsou vyjádřeny průměrem a rozsahem. Hodnoty NKZO a CRT byly analyzovány testem normality Kolmogorova-Smirnova. Změny NKZO a CRT byly hodnoceny pomoci párového Friedmanova testu. Statistická významnost byla definována jako p<0,05.
VÝSLEDKY
Nejčastější příčinou vzniku CNV v naší studii byla patologická myopie, která byla diagnostikována přibližně u poloviny léčených pacientů (tabulka 2). V celé skupině byl průměrný počet injekcí aplikovaných jednomu pacientovi 4,82,1 (rozmezí 3–10) dle léčebného protokolu PRN. Průměr aplikovaných injekcí u pacientů s patologickou myopií byl 4,1 (rozmezí 3-7 injekcí), u pacientů s centrální serózní chorioretinopatií byl 8,0 (rozmezí 7-9 injekcí), u pacientů s angioidními pruhy byl 6,0 (rozmezí 4-7 injekcí), u pacientů s idiopatickou CNV byl 8,0 (rozmezí 3-10 injekcí). Pacient s makulární dystrofií Severní Karolíny a pacient s dominantními familiárními drúzami sítnice byli léčení třemi injekcemi.
Tab. 2. Etiologie choroidální neovaskularizace a počet injekcí ranibizumabu 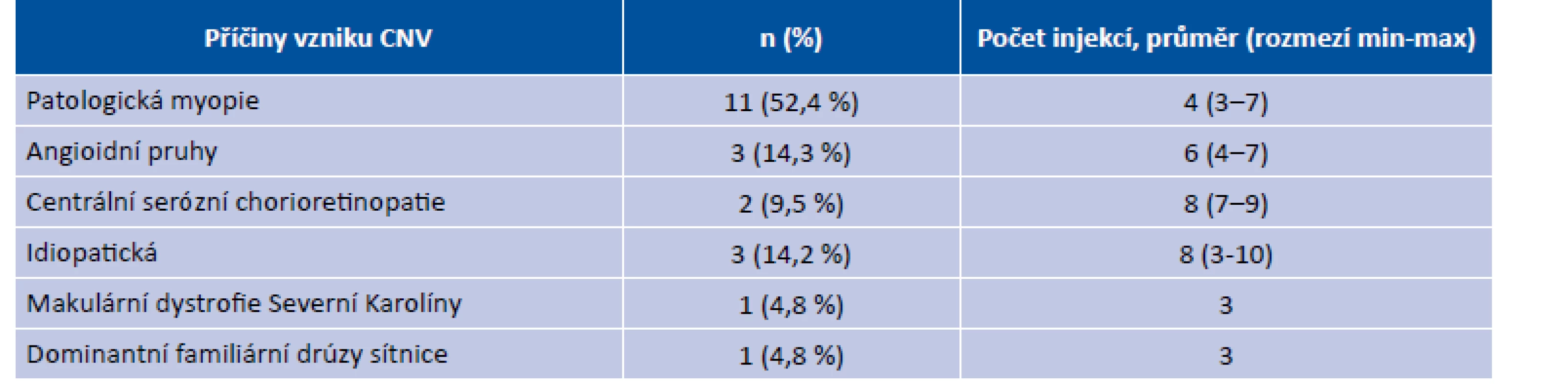
n = počet očí; CNV = choroidální neovaskularizace Změna NKZO
V celkové skupině 21 pacientů získalo 5 pacientů (23,8 %) po první injekci ranibizumabu v porovnání se vstupními hodnotami 15 a více písmen NKZO a po 12 měsících získalo 15 a více písmen 6 pacientů (28,6 %) (graf 1).
Graf 1. Změna nejlépe korigované zrakové ostrosti v průběhu ročního sledování v podskupině myopické choroidální neovaskularizace a choroidální neovaskularizace z jiných příčin ve sledovaném souboru 
V podskupině pacientů s myopickou CNV jsme zaznamenali hned po 1. injekci ranibizumabu statisticky signifikantní zlepšení NKZO o 14,2 písmen ETDRS optotypů (p<0,001), v podskupině pacientů s CNV z jiné příčiny bylo zlepšení o 5 písmen také statisticky významné (p=0,003). V období 1 měsíc až 8 měsíců od zahájení léčby jsme zjistili mírný statisticky nesignifikantní pokles NKZO v případě myopické CNV o 2,4 písmen ETDRS optotypů (p=0,167) a v případě CNV jiných příčin o 0,6 písmen (p=0,402). V období sledování 8-12 měsíců od zahájení léčby jsme dokumentovali další nevýznamný pokles NKZO o 0,7 písmen ETDRS optotypů (p=0,353) u pacientů s myopickou CNV a signifikantní zlepšení NKZO o 1,5 písmen (p=0,045) u pacientů s CNV z jiných příčin (graf 1).
Po ročním sledování jsme zjistili zlepšení zrakové ostrosti ve srovnání s hodnotami před léčbou u všech očí kromě dvou. U jednoho pacienta s idiopatickou CNV byl zjištěn pokles NKZO o 1 řádek ETDRS optotypu i přes aplikaci třech úvodních injekcí ranibizumabu. U druhého pacienta s CNV při angioidních pruzích sítnice bylo aplikováno 7 injekcí, NKZO se i přes tuto léčbu zhoršila o 7 písmen ETDRS optotypů. Vzhledem k ireverzibilním fibrozním změnám v makule u těchto pacientů byla léčba ukončena. Po roční léčbě u 4 pacientů (36,4 %) přetrvávaly známky aktivity CNV, a proto u nich bylo pokračováno v léčbě ranibizumabem. Ostatní pacienti zůstávají v našem sledování.
Anatomické výsledky
Významné zlepšení CRT bylo u všech pacientů zaznamenáno hned po prvních 3 injekcích ranibizumabu s průměrným statisticky signifikantním poklesem CRT o 59,9 µm od vstupních hodnot (p<0,001) ve skupině pacientů s myopickou CNV a o 59,9 µm (p<0,001) ve skupině pacientů s CNV z jiných příčin.
Od 4. do 8. měsíce sledování došlo k statisticky nesignifikantnímu nárůstu CRT o 17,3 µm (p=0,19) u pacientů s myopickou CNV a dalšímu poklesu CRT o 5,5 µm ve skupině s CNV z jiné příčiny (p=0,41).
V období sledování 8-12 měsíců od zahájení léčby jsme dokumentovali další statisticky nesignifikantní narůst CRT o 0,4 µm (p=0,56) u pacientů s myopickou CNV a o 7,4 µm (p=0,231) u pacientů s CNV z jiných příčin (Graf 2).
Graf 2. Změna centrální retinální tloušťky v průběhu ročního sledování v podskupině myopické choroidální neovaskularizace a choroidální neovaskularizace z jiných příčin ve sledovaném souboru 
Bezpečnost léčby
Nebyly pozorovány žádné závažné komplikace jako endoftalmitida, trhlina sítnice nebo její odchlípení, sklivcové krvácení, glaukom, aktivní uveitida nebo systémové nežádoucí účinky. U jednoho pacienta byla po aplikaci ranibizumabu zaznamenána přechodná nitrooční hypertenze, která dobře reagovala na lokální hypotenzivní léčbu Cosoptem gtt. Nejčastějším očním nežádoucím účinkem během roční léčby byly 3 případy podspojivkového krvácení.
DISKUSE
V řadě klinických studií byl prokázán benefit léčby blokátory VEGF u pacientů s jinou příčinou CNV než VPMD. Studie RADIANCE, která jako první na světě hodnotila účinnost léčby ranibizumabem v případě myopických CNV u 116 očí v režimu PRN, prokázala signifikantní zlepšení NKZO o 14,4 písmen ETDRS optotypů na konci ročního sledování s průměrným počtem 3,5 injekcí ranibizumabu [19]. V naši studii jsme zaznamenali zisk 11,4 písmen po 12 měsících od zahájení léčby s průměrným počtem 4,1 injekcí v průběhu roční léčby v podskupině myopických CNV. Menší zisk NKZO přisuzujeme malému počtu pacientů v našem souboru a také horším vstupním hodnotám NKZO (50,2 písmen ETDRS optotypu proti 55,8 písmen ve studii RADIANCE). Průměrný pokles CRT ve studii RADIANCE byl na konci ročního sledování -71,3 µm oproti vstupní hodnotě 373,1 µm. V našem souboru jsme zaznamenali zlepšení CRT o 42,2 µm z původní hodnoty 373,5 µm, což považujeme za srovnatelné.
Studie MINERVA hodnotila účinnost léčby ranibizumabem u 119 pacientů s CNV z jiných příčin než VPMD a u patologické myopie v režimu léčby PRN [13]. Výsledky hodnocení NKZO ukazují, že v průběhu ročního sledování došlo ke zlepšení o 9,5 písmen ETDRS optotypů při průměrném počtu 5,8 injekcí ranibizumabu (vstupní hodnoty NKZO byly 62,4 písmen). V našem souboru jsme prokázali zlepšení o 5,9 písmen oproti vstupní hodnotě NKZO 55,9 písmen v podskupině pacientů s CNV z jiných příčin než VPMD a z patologické myopie. Průměrný počet injekcí ranibizumabu za rok byl v této podskupině 5,6. Menší zisk NKZO v našem souboru přisuzujeme malému počtu pacientů a také horším vstupním hodnotám NKZO v porovnání se studií MINERVA. Průměrný pokles CRT ve studii MINERVA byl na konci ročního sledování -77,0 µm oproti vstupní hodnotě 392,5 µm. V našem sledování jsme zaznamenali pokles CRT o 119,4 µm z původních 400,5 µm, což považujeme za srovnatelné.
Troutbeck a kol. sledoval po dobu jednoho roku soubor 41 pacientů se sekundárními CNV, kam bylo zahrnuto 15 pacientů s myopií, 7 s multifokální choroiditidou a 8 pacientů s idiopatickou CNV a prokázal efektivitu léčby ranibizumabem [18]. Průměrné zlepšení NKZO v průběhu sledování bylo o 10 písmen ETDRS optotypů v podskupině myopických CNV (průměr 3,5 injekcí za rok) a o 12 písmen v podskupině CNV z jiných příčin (průměr 5,6 injekcí za rok). Pokles CRT byl v průměru o 76 µm ze vstupních 334 µm v případě myopických CNV a o 132 µm ze vstupních 405 µm ve skupině pacientů s CNV z jiných důvodů. Naše výsledky jsou srovnatelné s prací Troutbecka a kol. Podobné proporcionální rozdělení pacientů v obou skupinách naší studie (myopické CNV a CNV z jiných příčin) prokázalo klinicky významné zlepšení NKZO a u žádného z pacientů nedošlo ke klinicky významnému poklesu NKZO (zde definováno jako zhoršení o 15 písmen) během ročního sledování.
Chrapek a kol. hodnotil účinnost léčby ranibizumabem v průběhu jednoho roku u 6 pacientů s idiopatickou CNV [9]. Průměrné zlepšení NKZO během sledování bylo o 11 písmen ETDRS optotypů, pokles CRT byl v průměru o 233 µm ze vstupních 480 µm (průměr 3,0 injekcí za rok). Menší zisk NKZO a redukci CRT v naší skupině pacientů s CNV z jiných příčin vysvětlujeme tím, že jsme sledovali heterogenní populaci pacientů, u které idiopatická CNV byla zaznamenána jen u 3 pacientů (14,2 %).
Nárůst NKZO o 15 a více ETDRS písmen byl v našem souboru po ročním sledování dosažen u 28,6 % očí. Tyto výsledky jsou mírně horší ve srovnání s prací Carneiro a kol., který uvádí, že v případech CNV souvisejícími s angioidními pruhy, zánětlivými chorioretinálními onemocněními, centrální serózní chorioretinopatií a idiopatickou CNV, dochází po jednom roce léčby ke zlepšení zrakových funkcí o 15 a více ETDRS písmen u 43 % očí [1]. Menší zisk NKZO přisuzujeme menšímu počtu pacientů v našem souboru (11 proti 21 v prací Carneiro a kol.) a také horším vstupním hodnotám NKZO (50,2 písmen ETDRS optotypu proti 54,5 písmen v souboru Carneiro a kol.)
Během našeho sledování byly ve skupinách pacientů s myopickou CNV a CNV z jiných příčin patrné rozdíly ve změnách NKZO a CRT v průběhu léčby, které lze přisoudit případům, kdy pacient na léčbu zareagoval rapidně rychle. Například pacient s dominantními familiárními drúzami sítnice získal po první injekci ranibizumabu 22 písmen ETDRS optotypů, tento nárůst byl následně stabilní po dobu celého sledování. U jednoho ze třech pacientů s idiopatickou CNV došlo k poklesu CRT o 351 µm po úvodních třech nasycovacích dávkách ranibizumabu, zlepšení zůstalo stabilní během celého sledování.
Variabilita individuálních reakcí na ranibizumab v této studii není překvapující vzhledem k tomu, že se jedná o heterogenní populaci pacientů s různými příčinami vzniku CNV.
Pozoruhodné je, že pacienti s myopickou CNV dostali během 12ti měsíců průměrně o 26,8 % méně injekcí (průměrně 4,1) než pacienti ve skupině CNV z jiných příčin (průměrně 5,6). Naše výsledky nicméně jsou v tomto poměru v souladu s výsledky jiných studií [11,12,13,16,18,19]. Vysvětlit to můžeme tím, že myopická CNV má převážně klasickou složku (typ 2 CNV) na rozdíl od CNV při VPMD a CNV z jiných příčin, která rychleji reaguje na léčbu inhibitory VEGF [21].
V naší studie jsme prokázali, že aplikace ranibizumabu je bezpečnou léčebnou metodou u pacientů s myopickou CNV a CNV z jiných příčin. Studie SUSTAIN hodnotila bezpečnostní profil intravitreálně podávaného ranibizumabu v režimu PRN u pacientů s CNV s následujícím závěrem – u 18,5 % pacientů došlo k poklesu NKZO, u 7,2 % pacientů bylo dokumentováno zvětšení plochy intra/subretinální hemoragie, u 7,0 % bylo zaznamenáno přechodné zvýšení nitroočního tlaku ve studijním oku a 5,5 % pacientů mělo po injekci podspojivkovou sufuzi [8]. U žádného pacienta v našem souboru během sledování nedošlo k rozvoji zrak ohrožujících komplikací, souvisejících s léčbou ranibizumabem. U dvou pacientů (9,5 %) jsme zaznamenali pokles NKZO na základě ireverzibilních fibrozních změn v makule, u třech pacientů (14,3 %) došlo k rozvoji podspojivkové sufuze a jeden pacient (4,8 %) měl přechodné zvýšení nitroočního tlaku, které jsme úspěšně zaléčili lokálním podáním Cosoptu gtt. Bezpečnostní profil léčby ranibizumabem v našem souboru je porovnatelný se studií SUSTAIN.
K omezením této studie patří relativně malý soubor pacientů a také chybějící kontrolní skupina.
ZÁVĚR
Závěrem lze konstatovat, že léčba CNV vzniklé v důsledku jiných příčin než VPMD, byla dosud velmi omezená. Klinický benefit ranibizumabu prokázaný ve velkých klinických studiích u pacientů s CNV při VPMD umožnil jeho použití i u CNV z jiných příčin. Ačkoliv se jedná o malou skupinu pacientů, výsledky naší studie prokazují, že intravitreální léčba ranibizumabem u pacientů s CNV z jiné příčiny než VPMD je efektivní a bezpečná.
Autoři práce prohlašují, že vznik i téma odborného sdělení a jeho zveřejnění není ve střetu zájmu a není podpořeno žádnou farmaceutickou firmou.
Do redakce doručeno dne: 14.1.2019
Do tisku přijato dne: 21.2.2019
MUDr. Alexandr Stepanov, Ph.D., FEBO
Oční klinika Fakultní nemocnice Hradec Králové
Hradec Králové, Sokolská 581, 500 05
Zdroje
1. Carneiro, AM., Silva, RM., Veludo, MJ., et al.: Ranibizumab treatment for choroidal neovascularization from causes other than age-related macular degeneration and pathological myopia. Ophthalmologica, 225(2); 2011 : 81-8.
2. Cohen, SY., Laroche, A., Leguen, Y., et al.: Etiology of choroidal neovascularization in young patients. Ophthalmology, 103(8); 1996 : 1241–1244.
3. Cui, JZ., Kimura, H., Spee, C., et al.: Natural history of choroidal neovascularization induced by vascular endothelial growth factor in the primate. Graefes Arch Clin Exp Ophthalmol, 238(4); 2000 : 326 –33.
4. Curtin, BJ.: The prevalence of myopia. In: The Myopias: Basic Science and Clinical Management. Philadelphia, PA: Harper & Row 1985 : 39–59.
5. Klein, R., Chou, CF., Klein, BE., et al.: Prevalence of age-related macular degeneration in the US population. Arch Ophthalmol, 129(1); 2011 : 75-80.
6. Fredrick, DR.: Myopia. BMJ, 324(7347); 2002 : 1195–9.
7. Grossniklaus, HE., Green, WR.: Pathologic findings in pathologic myopia. Retina, 12(2); 1992 : 127–33.
8. Holz, FG., Amoaku, W., Donate, J., et al.: SUSTAIN Study Group. Safety and efficacy of a flexible dosing regimen of ranibizumab in neovascular age-related macular degeneration: the SUSTAIN study. Ophthalmology, 118(4); 2011 : 663-71.
9. Chrapek, O., Vostrovská, Z., Šínová, I., et al.: Léčba idiopatické choroidální neovaskulární membrány ranibizumabem – naše zkušenosti. Cesk Slov Oftalmol,XX (XX); 2019: XXX
10. Ishibashi, T., Hata, Y., Yoshikawa, H., et al.: Expression of vascular endothelial growth factor in experimental choroidal neovascularization. Graefes Arch Clin Exp Ophthalmol, 235(3); 1997 : 159–67.
11. Konstantinidis, L., Mantel, I., Pournaras, JA., et al.: Intravitreal ranibizumab (Lucentis) for the treatment of myopic choroidal neovascularization. Graefes Arch Clin Exp Ophthalmol, 247(3); 2009 : 311–8.
12. Lai, TY., Chan, WM., Liu, DT., et al.: Intravitreal ranibizumab for the primary treatment of choroidal neovascularization secondary to pathologic myopia. Retina, 29(6); 2009 : 750–6.
13. Lai, TYY., Staurenghi, G., Lanzetta, P., et al.: MINERVA study group. Efficacy and safety of ranibizumab for the treatement of choroidal neovascularization due to uncommon cause: Twelve-Month Results of the MINERVA Study. Retina. 38(8); 2018 : 1464-1477.
14. Martin, G., Schlunck, G., Hansen, LL., et al.: Differential expression of angioregulatory factors in normal and CNVderived human retinal pigment epithelium. Graefes Arch Clin Exp Ophthalmol, 242(4); 2004 : 321–6.
15. Miller, DG., Singerman, LJ.: Natural history of choroidal neovascularization in high myopia. Curr Opin Ophthalmol, 12(3); 2001 : 222–4.
16. Mones, JM., Amselem, L., Serrano, A., et al.: Intravitreal ranibizumab for choroidal neovascularization secondary to pathologic myopia: 12-month results. Eye (Lond), 23(6); 2009 : 1275 – 80.
17. Neelam, K., Cheung, CM., Ohno-Matsui, K., et al.: Choroidal neovascularization in pathological myopia. Prog Retin Eye Res, 31(5); 2012 : 495–525.
18. Troutbeck, R., Bunting, R., van Heerdon, A., et al.: Ranibizumab therapy for choroidal neovascularization secondary to non-age-related macular degeneration causes. Clinical and Experimental Ophthalmology, 40(3); 2012 : 67–72.
19. Wolf, S., Balciuniene, VJ., Laganovska, G., et al.: RADIANCE Study Group. RADIANCE: a randomized controlled study of ranibizumab in patients with choroidal neovascularization secondary to pathologic myopia. Ophthalmology, 121(3); 2014 : 682-92.e2.
20. Wong, TY., Foster, PJ., Hee, J., et al.: Prevalence and risk factors for refractive errors in adult Chinese in Singapore. Invest Ophthalmol Vis Sci, 41(9); 2000 : 2486–94.
21. Wong, TY., Ohno-Matsui, K., Leveziel, N., et al.: Myopic choroidal neovascularisation: current concepts and update on clinical management. Br J Ophthalmol, 99(3); 2015 : 289-96.
Štítky
Oftalmologie
Článek vyšel v časopiseČeská a slovenská oftalmologie
Nejčtenější tento týden
2019 Číslo 3- Stillova choroba: vzácné a závažné systémové onemocnění
- Familiární středomořská horečka
- Diagnostický algoritmus při podezření na syndrom periodické horečky
- Možnosti využití přípravku Desodrop v terapii a prevenci oftalmologických onemocnění
- Selektivní laserová trabekuloplastika nesnižuje nitroční tlak více než argonová laserová trabekuloplastika
-
Všechny články tohoto čísla
- Vliv rohovky na měření nitroočního tlaku tonometry ICARE PRO a ORA
- Využití optické koherenční tomografie u pacientů s útlakem optického chiasmatu
- Možnosti zlepšení zrakových funkcí u pacientů se stabilní makulopatií-pilotní výsledky nové studie
- Ranibizumab v léčbě choroidální neovaskularní membrány z jiné příčiny než věkěm podmíněná makulární degenerace
- Anomálie funkcie zrenice u detských pacientov – 2 kazuistiky
- Selektivní angiografie s možností trombolýzy u nemocných s okluzí arteria centralis retinae
- Doc. MUDr. Karel Kuběna, CSc. - zemřel
- 23. Zimný kongres ESCRS
- Kongres SOE
- Očná klinika Lekárskej fakulty Univerzity Komenského v Bratislave oslavuje 100-té výročie činnosti – 2. časť
- Česká a slovenská oftalmologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Anomálie funkcie zrenice u detských pacientov – 2 kazuistiky
- Vliv rohovky na měření nitroočního tlaku tonometry ICARE PRO a ORA
- Možnosti zlepšení zrakových funkcí u pacientů se stabilní makulopatií-pilotní výsledky nové studie
- Ranibizumab v léčbě choroidální neovaskularní membrány z jiné příčiny než věkěm podmíněná makulární degenerace
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



