-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Komplikace u nepenetrujících hlubokých sklerektomií
Complications of Deep Nonpenetrating Sclerectomy
Objective:
The purpose of this retrospective study was to evaluate an incidence of complications after deep nonpenetrating sclerectomy with different type of implant.Methods:
A total of consecutive 92 eyes (76 patients) that underwent deep sclerectomy were divided into 3 groups according to the type of nonpenetrating surgery.
The first group underwent deep sclerectomy without implant (34 eyes, 29 patients), the second group underwent deep sclerectomy with absorbable collagen implant Staar© (31 eyes, 25 patients) and the third group underwent deep sclerectomy with non-absorbable implant
T-Flux© (27 eyes, 22 patients). The complications were divided into 3 types – peroperative, early postoperative and late postoperative.Results:
The incidence of complications in above mentioned 3 groups was as follows: Peroperative complications: Perforation of trabeculo-Descemet’s membrane (2.6; 4.2; 3.7 % respectively). Early postoperative complications: Filtrating operating wound (no occurrence in our groups), Choroideal detachment (17; 19; 16 % resp.), Hypotony (10; 8; 5 % resp.), Hyphaema (7; 3; 0 % resp.), Infectious complications (no incidence of blebitis or endophthalmitis in our groups), Flat anterior chamber (7; 5.7; 5.5 % resp.), Dislocation of implant (1 case of dislocation of Staar©, 1 case of dislocation of T-Flux©). Late postoperative complications: Fibrosis of filtering bleb (30; 36; 24 % resp.), Encapsulated filtering bleb (2.9; 10.3; 0 %), Peripheral anterior synechiae (0; 4.2; 3.7 % resp.), Cataract progression (total incidence 5.5 %), there was no incidence of chronic hypotony, scleral ectasia and late endophthlamitis in our groups.Conclusions:
Deep sclerectomy allows effective lowering of intraocular pressure, without necessity of opening anterior chamber. It brings lower incidence of complications compared to classical penetrating trabeculectomy. Use of implant increases success of surgery due to intrascleral fibrosis reduction. We documented better effect of non-absorbable implant T-Flux© compared to absorbable collagen implant Staar©. The highest incidence of intrascleral fibrosis was in group of patients that underwent deep sclerectomy without implant.Key words:
deep sclerectomy, T-Flux©, collagen implant Staar©, laser goniopuncture
Autoři: P. Strnad; J. Svačinová; E. Vlková
Působiště autorů: Oční klinika LF MU a FN, Brno přednosta prof. MUDr. Eva Vlková, CSc.
Vyšlo v časopise: Čes. a slov. Oftal., 68, 2012, No. 3, p. 109-113
Kategorie: Původní práce
Souhrn
Cíl:
cílem této retrospektivní studie bylo zhodnocení výskytu komplikací u nepenetrujících hlubokých sklerektomií s užitím různých typů intrasklerálních implantátů.Metody:
celkový počet 92 očí (76 pacientů), jež podstoupily filtrující operaci technikou hluboké sklerektomie, byl rozdělen do 3 souborů dle užití intrasklerálního implantátu a jeho typu. První soubor tvořily oči operované technikou prosté hluboké sklerektomie bez implantátu (34 očí, 29 pacientů), druhý soubor podstoupil operaci technikou hluboké sklerektomie s resorbovatelným implantátem Staar© (31 očí, 25 pacientů) a třetí soubor podstoupil hlubokou sklerektomii s neresorbovatelným implantátem T-Flux© (27 očí, 22 pacientů). Komplikace byly rozděleny do 3 skupin – peroperační, časné pooperační a pozdní pooperační.Výsledky:
výskyt komplikací ve výše zmíněných souborech byl následující (incidence komplikací je udána v pořadí jako výše uvedené soubory). Peroperační komplikace: perforace trabekulo-Descemetské membrány (2,6; 4,2; 3,7 %). Časné pooperační komplikace: filtrující rána (nebyl zaznamenán výskyt této komplikace v našich souborech), ablace cévnatky (17; 19; 16 %), hypotonie (10; 8; 5 %), hyféma (7; 3; 0 %), infekční komplikace (nebyl zaznamenán výskyt této komplikace v našich souborech), změlčení přední oční komory ( 7; 5,7; 5,5 %), dislokace intrasklerálního implantátu (1 případ dislokace Staar© implantátu, 1 případ dislokace T-Flux© implantátu). Pozdní pooperační komplikace: fibróza filtračního puchýře (30; 36; 24 %), enkapsulovaný filtrační puchýř (2,9; 10,3; 0 %), přední periferní synechie (0; 4,2; 3,7 %), progrese katarakty (celková incidence 5,5 %). V našich souborech jsme nezaznamenali výskyt chronické hypotonie, sklerální ektázie ani pozdní endoftalmitidy.Závěr:
operace technikou hluboké sklerektomie vede k efektivnímu snížení nitroočního tlaku bez nutnosti penetrace přední oční komory. Hluboká sklerektomie se vyznačuje nižší incidencí komplikací ve srovnání s klasickou penetrující trabekulektomií. Užití intrasklerálních implantátů vede k lepší a dlouhodobé kompenzaci nitroočního tlaku v důsledku redukce intrasklerálních fibrotických procesů. Ve dlouhodobém sledování jsme prokázali výrazně lepší redukci nitroočního tlaku při užití neresorbovatelného implantátu T-Flux© oproti implantátům resorbovatelným, event. oproti hluboké sklerektomii prosté bez užití implantátu.Klíčová slova:
hluboká sklerektomie, T-Flux©, kolagenový implantát Staar©, laserová goniopunkturaÚvod
Glaukom patří k nejčastějším příčinám slepoty. Přibližně 1,5–2 % populace nad 40 let věku má glaukomové onemocnění. Jedná se o ireverzibilní a zejména bez terapie o progresivní neuropatii optického nervu, jež může vést ke slepotě.
V posledním desetiletí dochází postupně k porozumění patologie glaukomu. Jsou známy rizikové faktory rozvoje a progrese glaukomového onemocnění. Na prvním místě stále stojí zvýšený nitrooční tlak. Cílem léčby je zachování zrakových funkcí pacienta. V terapii glaukomu se diskutuje o snížení nitroočního tlaku, zlepšení oční perfuze (nepřímá neuroprotekce) a o přímé neuroprotekci. V současné době zůstává jedinou ověřenou a dostupnou metodou terapie snížení nitroočního tlaku na tzv. cílový nitrooční tlak, tj. na takovou hodnotu nitroočního tlaku, při které nedochází k progresi glaukomového poškození a zrakové funkce zůstávají stabilizovány.
V léčbě glaukomu používáme zejména terapii konzervativní, jež zahrnuje široké spektrum lokálně i celkově podávaných preparátů. Pokud se však nedaří dosáhnout cílového nitroočního tlaku konzervativními postupy, je nutná léčba chirurgická. Samostatnou kapitolu tvoří možnost terapie laserové. Podstatou chirurgických výkonů je usnadnění odtoku nitrooční tekutiny. Nejčastěji pod spojivku, ev. ve spojení s otevřením Schlemmova kanálu, či odvod komorové tekutiny do suprachoroidálního prostoru. V současné době se v chirurgii glaukomu používají filtrující zákroky penetrující a nepenetrující.
Mezi filtrující zákroky penetrující řadíme klasickou trabekulektomii s množstvím modifikací a dále penetrující zákroky s drenážními implantáty, které jsou zaváděny přímo do přední oční komory, ev. do sklivcové dutiny.
Evoluce nepenetrujících filtrujících operací byla nastartována snahou chirurgů o snížení výskytu komplikací, jež penetrující výkony v peroperačním i pooperačním období provázely. Mezi nepenetrující filtrační zákroky řadíme sinusotomii provedenou poprvé v roce 1962 Krasnovem [21], dále postupnými modifikacemi vytvořenou trabekulektomii ab externo – poprvé navrženou De Lagge de Meuxem a Kantelipem v roce 1976 [4] a později Zimmermannem v roce 1984 [61].
Mezi v současnosti užívané nepenetrující filtrační zákroky patří hluboká sklerektomie (HS) a viskokanalostomie, s jejich modifikacemi. Podstatou obou nepenetrujících typů operací je vytvoření hlubokého sklerálního lůžka pod sklerální lamelou, tak aby byl otevřen Schlemmův kanál a byla obnažena Descemetská membrána, avšak aby nedošlo k otevření přední komory oční (PK). Přes tzv. trabekulo-Descemetskou membránu (TDM) poté může komorová tekutina volně prosakovat. Při viskokanalostomii, poprvé popsané Stegmannem v roce 1995 [46, 47], je do Schlemmova kanálu aplikován viskoelastický materiál. Hluboká sklerektomie byla poprvé popsána Fyodorovem [10] a Kozlovem [19]. Hlubokou sklerektomii lze provádět v mnoha modifikacích. Jednak jako tzv. prostou hlubokou sklerektomii a dále je možno při hluboké sklerektomii užít různé typy implantátů, které se vkládají do hlubokého sklerálního lůžka a slouží jako prevence fibrotických procesů a selhání filtrace. Samostatnou kapitolu tvoří kanaloplastika Schlemmova kanálu se zavedením trakčního stehu.
Ačkoliv je všeobecně známo, že nepenetrující filtrační operace glaukomu jsou zatíženy nižším výskytem komplikací oproti penetrujícím filtračním výkonům, je nutné ev. komplikacím věnovat dostatečnou pozornost. Jedná se o komplikace peroperační a dále komplikace, které se mohou objevit v časném a pozdním pooperačním období.
Cíl studie
Cílem této studie bylo analyzovat výskyt komplikací vyskytujících se u nepenetrujících filtračních operací glaukomu a dokumentovat jejich četnost výskytu na souboru pacientů, kteří podstoupili operaci glaukomu na naší klinice.
Soubor a metodika
Sledovaný soubor tvořilo celkem 92 očí operovaných nepenetrující filtrační technikou hluboké sklerektomie. Soubor byl tvořen 3 skupinami, v závislosti na modifikaci provedené operace, dané přítomností a typem filtračního implantátu umístěného peroperačně do sklerálního lůžka.
První skupina podstoupila prostou hlubokou sklerektomii bez vložení filtračního implantátu (34 očí, 29 pacientů, průměrného věku 62,9 ± 11,1 let; 31 očí s dg. primárního glaukomu otevřeného úhlu (PGOÚ), 2 oči s dg. pseudoexfoliativního glaukomu (PEXG), 1 oko s dg. sekundárního glaukomu po implantaci nitrooční čočky). Druhá skupina podstoupila hlubokou sklerektomii s resorbovatelným kolagenovým implantátem Staar® (31 očí, 25 pacientů, průměrného věku 65,8 ± 11,5 let; 27 očí s dg. PGOÚ, 2 oči s dg. PEXG, 1 oko s dg. pigmentového glaukomu a 1 oko s kongenitální aniridií).
Třetí skupina podstoupila hlubokou sklerektomii s neresorbovatelným implantátem T-Flux® (27 očí, 22 pacientů, průměrného věku 67,3 ± 9,2 let; 24 očí s dg. PGOÚ, 1 oko s dg. PEXG, 1 oko s dg. pigmentového glaukomu a 1 oko s dg. juvenilního glaukomu).
Ve výše uvedených souborech byl sledován výskyt těchto peroperačních komplikací: perforace trabekulo-Descemetské membrány a peroperační krvácení. Z časných pooperačních komplikací byly sledovány: filtrující operační rána, pooperační zánětlivá reakce v přední oční komoře, choroidální ablace, hypotonie, elevace nitroočního tlaku (NOT), maligní glaukom, infekce, mělká přední oční komora a dislokace filtračního implantátu. V pozdním pooperačním období byl hodnocen výskyt těchto komplikací: elevace NOT v pozdním pooperačním období, fibróza spojivkového puchýře, enkapsulovaný filtrační puchýř, fibróza intrasklerálního prostoru a TDM, ruptura TDM v pozdním pooperačním období, výskyt předních periferních synechií a progrese katarakty.
Chirurgická technika provedení hluboké sklerektomie obsahuje následující kroky. Spojivkový lalok může být otevřený k limbu či fornixu. Následuje vytnutí povrchové sklerální lamely o velikosti 5 x 5 mm, do 1/3 tloušťky skléry s ponecháním rohovkového můstku. Povrchová sklerální lamela by měla zasahovat 1 mm do čiré rohovky, aby bylo možné v pozdější fázi operace odkrýt Descemetskou membránu. Pod povrchovou lamelou je dále vytnuta hluboká sklerální lamela o velikosti 4 x 4 mm. Spodinu hluboké sklerektomie tvoří zbývajících 10 % tloušťky skléry a otevřený Schlemmův kanál, následován okénkem Descemetské membrány. Následně je vhodné provést důkladný peeling endotelové výstelky Schlemmova kanálu. Jako prevence vzniku intrasklerální fibrózy může být v dalším kroku do sklerálního lůžka, po vytnutí hluboké sklerální lamely, vložen filtrační implantát [1, 13, 15, 16, 17, 19, 23, 26, 41, 43, 44, 48, 49, 56, 57, 58]. U prosté hluboké sklerektomie je lůžko ponecháno bez implantátu. V závěru operace je provedena těsná sutura povrchové sklerální lamely a spojivky.
Výsledky a diskuse
Esenciálním momentem úspěšně fungující HS je vytnutí hluboké sklerální lamely a dále rohovky v optimální tloušťce tak, aby za odtokovou rezistenci odpovídala pouze tzv. trabekulo-Descemetská membrána [55]. Tato membrána, tvořená trabekulem a periferní částí Descemetské membrány, je velice fragilní a na pečlivosti a zručnosti operatéra závisí výsledek operace. Různé studie uvádějí výskyt ruptury TDM v 5–20 % [1, 6, 9, 16, 17, 28, 35, 40, 50, 51, 52, 53, 54, 56, 57, 58]. Mermoud uvádí výskyt perforace TDM ve 30 % při prvních 10 operacích, s následným poklesem výskytu na 3 % u následujících 100 výkonů [28]. V našich souborech byla četnost výskytu následující: u prosté HS bez implantátu v 2,6 %, u HS se Staar® implantátem ve 4,2 % a ve skupině HS s T-Flux® implantátem ve 3,7 %.
Peroperačnímu krvácení, jež může vést k horším pooperačním výsledkům, lze ve většině případů předejít šetrně vedeným chirurgickým postupem, s minimální traumatizací v oblasti operačního pole. Tím lze předejít vystupňované fibrogenezi v pooperačním období. Výskyt krvácení do PK, po provedené HS, je v literatuře uváděn v 0,8–20 % [1, 17, 22, 23, 35, 43, 50, 51, 52, 53, 54, 56, 57, 58]. V našich souborech jsme zaznamenali mírná povrchová krvácení spojivkového a sklerálního původu. Krvácení do PK se v našich souborech vyskytovalo u prosté hluboké sklerektomie bez implantátu v 7 %, u hluboké sklerektomie se Staar® implantátem ve 3 % a v souboru hluboké sklerektomie s T-flux® implantátem jsme krvácení do PK nezaznamenali.
Časné pooperační komplikace jsou po nekomplikovaném průběhu nepenetrujících výkonů vzácnější, ve srovnání s výskytem po trabekulektomii [26, 60]. Taktéž výskyt těchto komplikací lze omezit použitím precizní a šetrné operační techniky za přísně aseptických podmínek. Tím je snížena možnost peroperační bakteriální kontaminace, nebezpečí ruptury TDM a vystupňování zánětlivé a fibrogenní pooperační reakce. Na konci operace je vhodné provést těsnou suturu Tenonské fascie a spojivky.
Je nutné zdůraznit, že je přísně kontraindikováno provádět masáž očního bulbu v pooperačním období, neboť hrozí ruptura TDM s následnými komplikacemi.
Filtrující operační ránu jsme v našich souborech nezaznamenali. V literatuře je výskyt této komplikace popisován až v 18,8 % [1, 6, 18, 26, 43, 50, 51, 52, 53, 54, 56, 57, 58].
Choroidální ablace je uváděna v literatuře po nepenetrujících filtračních operacích v 0 - 15,8 % [6, 10, 17, 19, 22, 23, 26, 41, 43, 50, 51, 52, 53, 54, 56, 57, 58, 61], hodnoceno oftalmoskopicky, zatímco po trabekulektomii až ve 20 % [3]. Pomocí UBM lze však přítomnost choroidální ablace po HS prokázat až ve 40 % [13]. V našich souborech byl výskyt choroidální ablace následující: u prosté HS bez implantátu v 17 %, u HS se Staar® implantátem v 19 % a u HS s T-Flux® implantátem v 16 %.
Hypotonie je udávána různými autory v literatuře až ve 43 % [16, 17, 18, 26, 35, 43, 50, 51, 52, 53, 54, 56, 57, 58]. V našich souborech byl výskyt pooperační hypotonie následující: u prosté HS bez implantátu v 10 %, u HS se Staar® implantátem v 8 % a u HS s T-Flux® implantátem v 5 %.
Elevaci nitroočního tlaku v časném pooperačním období, po operaci technikou hluboké sklerektomie, jsme v našich souborech zaznamenali v ojedinělých případech ve spojitosti s kortikosteroidní terapií. Vysazení této terapie vedlo k poklesu nitroočního tlaku. Maligní glaukom [2,25] jako příčinu elevace nitroočního tlaku jsme v pooperačním období nezaznamenali.
Infekční komplikace v časném pooperačním období probíhající pod obrazem blebitidy je v literatuře popisována v 0–1,2 % [6]. Endoftalmitida nebyla po nepenetrujících filtračních výkonech zaznamenána. V našich souborech se infekční pooperační komplikace nevyskytly.
Změlčení PK je popisováno v literatuře až v 15,8 % [6, 18, 22, 43, 50, 51, 52, 53, 54, 56, 57, 58]. V našich souborech jsme změlčenou PK zaznamenali u HS bez implantátu v 7 %, u HS se Staar® implantátem v 5,7 % a u HS s T-Flux® implantátem v 5,5 %.
Dislokace filtračního implantátu je vzácná komplikace popisovaná v literatuře v ojedinělých případech. V našich souborech jsem zaznamenali jeden případ parciální dislokace Staar® implantátu do PK, který byl řešen reoperací a vynětím implantátu. Dále jsme zaznamenali 1 případ částečné dislokace T-flux® implantátu zpod sklerální lamely pod spojivku [50, 51, 52, 53, 54]. Řešením byla chirurgická repozice implantátu.
Pozdní pooperační komplikace se na rozdíl od časných vyskytují po penetrujících i nepenetrujících filtračních antiglaukomových operacích ve stejné míře [26]. Tato skutečnost zřejmě souvisí s faktem, že většina pozdních pooperačních komplikací souvisí s vystupňovanými hojivými procesy v oblasti operační rány. To následně vede k selhání filtrace a elevaci NT s opětovným navýšením lokální antiglaukomové terapie, ev. k reoperaci.
Výskyt fibrózy filtračního puchýře je v literatuře uváděn až ve 23 % [6, 26, 50, 51, 52, 53, 54, 56, 57, 58]. V našich souborech se vyskytovala tato pozdní pooperační komplikace s následující četností: u HS bez implantátu ve 30 %, u HS se Staar® implantátem ve 36 % a u HS s T-Flux® implantátem ve 24 %.
Enkapsulace filtračního puchýře taktéž souvisí s vystupňovanými fibrotickými procesy v oblasti Tenonské fascie a subkonjunktiválně. V literatuře je výskyt enkapsulace filtračního puchýře uváděn až v 15 % [1]. V našich souborech jsme enkapsulovaný filtrační puchýř zaznamenali u HS bez implantátu v 2,9 %, u HS se Staar® implantátem v 10,3 %. U HS s T-Flux® implantátem jsme enkapsulovaný puchýř nezaznamenali.
Jako prevence vzniku intrasklerální fibrózy jsou u HS používány filtrační implantáty vkládané peroperačně do sklerálního lůžka [1, 13, 15, 16, 17, 19, 23, 26, 41, 43, 44, 48, 49, 56, 57, 58]. V našich souborech se nejlépe v prevenci intrasklerální fibrózy osvědčil neresorbovatelný implantát T-Flux® oproti resorbovatelnému kolagenovému implantátu Staar®, ev. prosté hluboké sklerektomii bez implantátu, kde byly vyjádřeny fibrotické procesy v našich souborech v nejvyšší míře. S tím souvisí i kompenzace nitroočního tlaku a nutnost opětovného nasazení lokální antiglaukomové terapie v pooperačním období.
Užití Nd-YAG laserové goniopunktury je v literatuře jednotlivými autory uváděno ve 21–62,2 % [1, 5, 6, 16, 17, 19, 22, 27, 42, 43, 44, 48, 49, 50, 51, 52, 53, 54]. Nd-YAG laserovou goniopunkturu jsme provedli ve 22 % případů u pacientů po nepenetrující operaci technikou hluboké sklerektomie s T-flux implantátem.
Výskyt předních periferních synechií je v literatuře popisován v 5,1 - 47,6 % [1, 8, 18, 35, 40, 50, 51, 52, 53, 54, 56, 57]. V našich souborech se periferní synechie vyskytovaly s následující četností: u prosté HS bez implantátu v 0 %, u HS se Staar® implantátem ve 4,2 % a u HS s T-Flux® implantátem v 3,7 %.
Progrese preexistující katarakty je v literatuře uváděna ve 2 – 25 % [11, 17, 22, 44, 50, 51, 52, 53, 54]. V našich souborech po HS byl výskyt progrese preexistující katarakty celkově v 5,5 %.
Odchlípení Descemetské membrány [20, 24, 26, 28, 36], rupturu TDM [6, 12, 31] ani chronickou hypotonii či sklerální ektázii [30] v pozdním pooperačním období jsme v našich souborech nezaznamenali.
Srovnání výskytu komplikací v našich souborech s jinými autory uvádí přehledně tabulka č. 1.
Tab. 1. Srovnání výskytu komplikací udávaných v pracích jednotlivými autory s výskytem komplikací v našich souborech. Četnost výskytu jednotlivých komplikací je udána v % 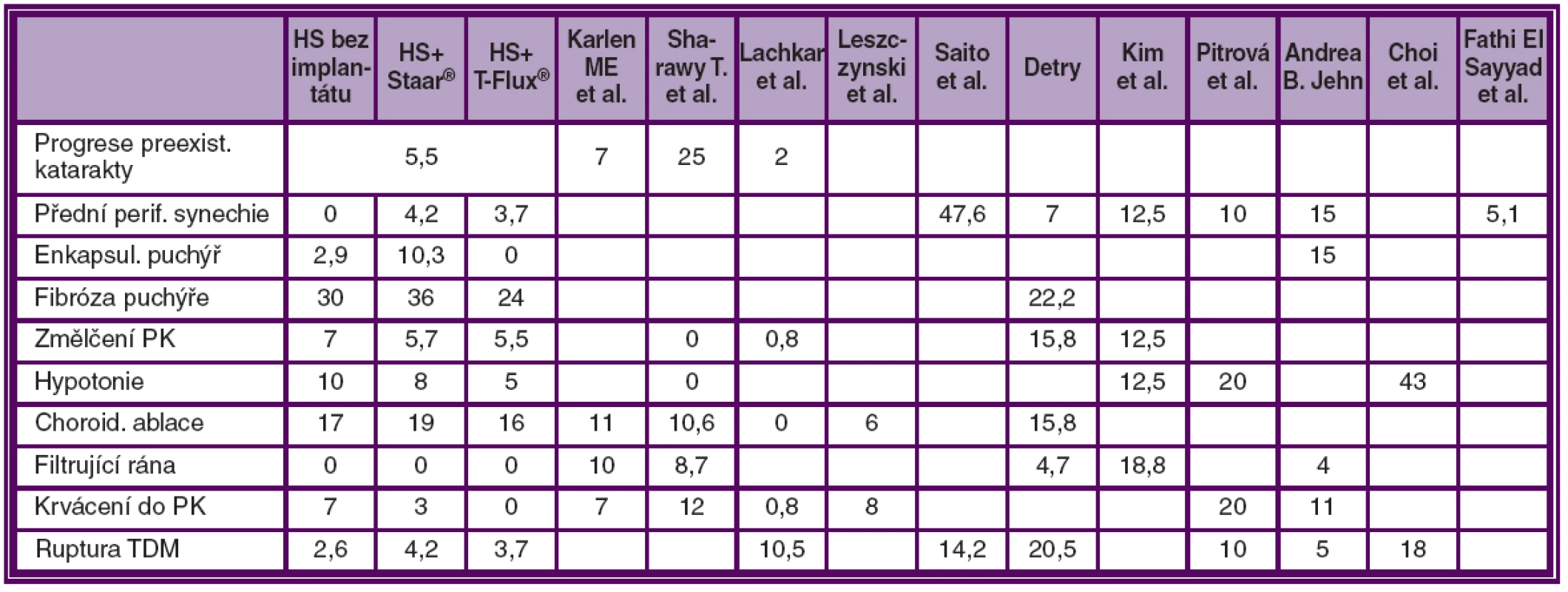
Úspěšnost nepenetrujících filtrujících výkonů závisí mimo jiné i na správné indikaci. Mezi relativní KI provedení HS patří glaukom úzkého úhlu. Jedním z důvodů selhání filtrace, po provedené HS u glaukomu úzkého úhlu, mohou být změny v komorovém úhlu, jako jsou preexistující goniosynechie, neboť úspěšnost filtrace u HS závisí na neporušené trabekulární trámčině. Druhým důvodem selhání filtrace může být samotný úzký úhel, který je predispozicí ke vzniku pooperačních synechií. Z tohoto důvodu na našem pracovišti volíme jako operační řešení u glaukomu úzkého úhlu klasickou trabekulektomii, při níž je provedena peroperačně bazální iridektomie jako prevence vzniku periferních předních adherencí.
Další relativní KI k provedení HS jsou operace tam, kde byla v minulosti provedena laserová trabekuloplastika. Trabekulární trámčina může být po provedení laserového zákroku fragilní a výrazně se zvyšuje riziko peroperační ruptury TDM.
Poúrazový sekundární glaukom patří taktéž k relativním KI provedení HS. Selhání filtrace u tohoto glaukomu po provedené HS souvisí s možností výskytu nefunkčního trabekula po recessu komorového úhlu.
Mezi absolutní KI provedení HS patří neovaskulární glaukom. Neovaskularizace v komorovém úhlu vedou k selhání filtrace ještě rychleji než po provedení klasické trabekulektomie. V takových případech bývá řešením užití filtračních implantátů typu Molteno [29], ev. jiných.
Závěr
Nepenetrující filtrační operace umožňují efektivní snížení nitroočního tlaku u pacientů s glaukomem bez nutnosti otevření PK jako je tomu u klasické trabekulektomie. S tím souvisí i nižší výskyt, zejména časných pooperačních komplikací.
Základem úspěchu je indikace vhodného typu glaukomu k provedení HS, precizní a šetrný operační postup a důkladná znalost komplikací, které se mohou ve spojení s nepenetrujícími filtračními operacemi glaukomu vyskytnout. Včasné rozpoznání komplikací a přijetí správného řešení a terapie, tvoří nedílnou část úspěchu.
Užití implantátů zvyšuje úspěšnost operace redukcí intrasklerální fibrózy v pooperačním období. Ve dlouhodobém sledování jsme v našich souborech prokázali lepší redukční efekt neresorbovatelného akrylátového implantátu T-flux® oproti kolagennímu implantátu Staar®, z čehož vyplývá i menší množství nutné lokální antiglaukomové terapie opětovně nasazené v pooperačním období. Největší výskyt intrasklerální fibrózy jsme pozorovali u hluboké sklerektomie bez použití filtračního implantátu. Ke zlepšení filtrace lze v pooperačním období provést laserovou goniopunkturu.
Do redakce doručeno dne 8. 2. 2012
Do tisku přijato dne 20. 6. 2012
MUDr. P. Strnad
Oční klinika FN Brno
Jihlavská 20
625 00 Brno
e-mail: p.strnad@email.cz
Zdroje
1. Jehn, A. B., Bohnke, M., Mojon, D. S.: Deep sclerectomy with collagen Implant: Initiale experience. Ophthalmologica, 2002; 216 : 235–238.
2. Brooks, A. M., Harper, C. A., Gillies, W. E.: Occurrence of malignant glaucoma after laser iridotomy. Brit J Ophthalmol, 1989; 73(8): 617–620.
3. Brubaker, R. F., Pederson, J. E.: Ciliochoroidal detachement. Surv Ophthalmol, 1983; 27 : 281–289.
4. De Laage de Meux, P., Kantelip, B.: Surgical anatomy of corneoscleral limbus. Arch Ophthalmol, 1976; 36 : 39–50.
5. Demailly, P., Lavat, P., Kretz, G. et al.: Non-penetrating deep sclerectomy with or without collagen device in primary open-angle glaucoma: modele-term retrospective study. Inter Ophthlamol, 1996; 20 : 131–140.
6. Detry-Morel, M., Detry, M. B.: Five-year experience with non-penetrating deep sclerectomy. Bull Belg Soc Ophthalmol, 2006; 299 : 83–94.
7. Ewing, R. H., Stamper, R. L.: Needle revision with and without 5-fluorouracil for the treatment of failed filtering blebs. Amer J Ophthalmol, 1990; 110 : 254–259.
8. El-Sayyad, F., Helal, M., El-Kholify, H. et al.: Nonpenetrating deep sclerectomy versus trabeculectomy in bilateral primary open-angle glaucoma. Ophthalmology, 2000; 107 (9): 1671–1674
9. Price, F. W., Zeh, W. G.: Viscoelastic material as an adjunct to dissection and to treat microperforations during non-penetrating filtering surgery. J Cataract Refract Surg, 2001; 27 : 639–641.
10. Fyodorov, S. N.: Non-penetrating deep sclerectomy in open-angle glaucoma. Eye Microsurg, 1989; 52–55.
11. Henchoz, L., Schnyder, C., Shaarawy, T. et al.: Surgery-induced cataract and cataract progression following deep sclerecomy with collagen implant compared to trabeculectomy. Ophthalmology, 2000; 107 : 205.
12. Hyams, M., Geyer, O.: Iris prolapse at the surgical site: A late complication of Nonpenetrating Deep Sclerectomy. Ophthalmic surgery, lasers & Imaging, 2003; 34 : 132-135.
13. Chiou, A. G. Y., Mermoud, A., Hediguer, S. E. A. et al.: Ultrasound biomicroscopy of eyes undergoing deep sclerectomy with collagen implant. British Journal of Ophthalmology, 1996; 80 : 541-544.
14. Chiou, A. G. Y., Mermoud, A., Hediguer, S. E. A.: Malignant glaucoma after deep sclerectomy-ultrasound biomicroscopy imaging. Klein Monatsbl Augenheilkd, 1996; 208 : 279–281.
15. Chiou, A. G. Y., Mermoud, A., Jewelewicz, D. A.: Comparison of post-operative inflammation following deep sclerectomy with collagen implant versus standard trabeculectomy. Graefeęs Arch Clin Exper Ophthalmol, 1998; 236 : 593–96.
16. Choi, S. S., Kim, S. S., Kim, C. Y. et al.: Short term surgical outcomes of modified deep sclerectomy with catgut implant. Kor J Ophthalmol, 2001; 15 : 113–117.
17. Karlen, M. E., Sanchez, E., Schnyder, C. C. et al.: A deep sclerectomy with collagen implant: medium results. Brit J Ophthalmol, 1999; 83 : 6–11.
18. Kim, J. I., Bae, J. H., Song, J. K.: The efficacy of nonpenetrating deep sclerectomy with 0,02% Mytomycin C. Kor J Ophthalmol, 2001; 42 : 1284–1288.
19. Kozlov, V. I., Bagrov, S. N., Anisimova, S. Y. et al.: Deep sclerectomy with collagen. Eye Microsurg, 1990; 3 : 44–46.
20. Kozobolis, V. P., Christodoulakis, E. V., Siganos, Ch. S. et al.: Hemorrhagic Descement`s membrane detachement as a complication of deep sclerectomy: A case report. J Glauc, 2001; 10 : 497–500.
21. Krasnov, M. M.: Externalization of Schlemm’s canal (sinusotomy) in glaucoma. Brit J Ophthalmol, 1968; 52 : 157–161.
22. Lachkar, Y., Neverauskiene, J., Jeanteur-Lunel, M. N. et al.: Nonpenetrating deep sclerectomy: A 6-year retrospective study. Europ J Ophthalmol, 2004; 14 : 26–36.
23. Leszczynski, R., Gierek-Ciaciura, S., Forminska-Kapuscik, M. at al.: Nonpenetrating very deep sclerectomy with reticulated hyaluronic acid implant in galucoma treatment. Med Sci Monitor, 2008; 14 : 86–89.
24. Luke, C., Dietlein, T, Jacobi, P. et al.: Intracorneal inclusion of high-molecular-weight sodium hyaluronate following detachment of Descemet`s membrane during viscocanalostomy. Cornea, 2000; 19 : 556–557.
25. Manku, M. S.: Spontaneous bilateral malignant glaucoma. Clin Exper Ophthalmol, 2007; 13 (3): 249–250.
26. Mermoud, A., Schnyder, C. C., Sickenberg, M. et al.: Comparison of deep sclerecomy with collagen implantand and trabeculectomy in open-angle glaucoma. J Cataract Refract Surg, 1999; 25 : 323–331.
27. Mermoud, A., Karlen, M. E., Schnyder, C. C. et al.: Nd:YAG goniopuncture after deep sclerectomy with collagen implant. Ophthal Surg Lasers, 1999; 30 : 120–125.
28. Mermoud, A., Ravinet, E.: Complications and reoperations. In: Mermoud, A., Shaarawy, T., Ritch, R. et al.: Non-Penetrating Glaucoma Surgery, London, UK: Martin Dunitz, 2001; 140–159.
29. Mermoud, A., Salmon, J. F., Alexander, P. et al.: Molteno tube implantation for neovascular glaucoma. Long-term results and factors influencing the outcome. Ophthalmology, 1993; 100 : 897–902.
30. Milazzo, S., Turut, P., Malthieu, D. et al.: Scleral ectasia as a complication of deep sclerectomy. J Cataract Refract Surg, 2006; 26 : 785–787.
31. Moreno-MontaĖés, J., Rodríguez-Conde, R.: Bleeding during gonioscopy after deep sclerectomy. J Glaucoma, 2003; 12 : 427–429.
32. Ophir, A., Ticho, U.: Encapsulated filtering bleb and subconjunctival 5-fluorouracil. Ophthalm Surg , 1992; 23 : 339–341.
33. Othenin-Girard, P., Tritten, J. J., Pittet, N. et al.: Dexamethasone versus Diclofenac sodium eyedrops to treat inflammation after cataract surgery. J Cataract Refract Surg, 1994; 20 : 9–12.
34. Pederson, J. E., Smith, S. G.: Surgical management of encapsulated filtering blebs. Ophthalmology, 1985; 92 : 955–958
35. Pitrová, Š., Pešková, H., Lešták, J.: První klinické zkušenosti s hlubokou sklerektomií v ambulantní chirurgii glaukomů. Čs. Oftalmol, 1999; 1 : 3–9.
36. Ravinet, E., Tritten, J. J., Roy, S. et al.: Descemet membrane detachment after nonpenetrating filtering surgery. J Glaucoma, 2002; 11 : 244–52.
37. Roth, S. M., Spaeth, G. L., Starita, R. J. et al.: The effects of postoperative corticosteroids on trabeculectomy and the clinical course of glaucoma: Five-year follow-up study. Ophthalmic Surg, 1991; 22 : 724–729.
38. Roy, S., Mermoud, A.: Complications deep nonpenetrating sclerectomy. J Franc DęOphtalmol, 2006; 29 : 1180–1197.
39. Ruderman, J. M., Harbin, T. S., Campbell, D. G.: Postoperative suprachoroidal hemorrhage following filtration procedures. Arch Ophthalmol, 1986; 104 : 201–205.
40. Saito, A., Amemiya, T., Dake, Y. et al.: Short-term outcome of nonpenetrating trabeculectomy with deep sclerectomy for glaucoma. Japan J Clin Ophthalmol, 2001; 55 : 553–556.
41. Sanchez, E., Schnyder, C. C., Sickenberg, M. et al.: Deep sclereclomy: results with and without collagen implant. Inter Ophthalmol, 1997; 20 : 157–162.
42. Shaarawy, T., Karlen, M. E., Sanchez, E. et al.: Long term results of deep sclerectomy with collagen implant. Acta Ophthalmol Scand, 2000; 78 : 323–328.
43. Sharawy, T., Nguyen, C., Schnyder, C. et al.: Comparative study between deep sclerectomy with and without collagen implant: long term follow-up. Brit J Ophthalmol, 2004; 88 : 95–98.
44. Shaarawy, T., Mansouri, K., Schnyder, C. et al.: Long-term results of deep sclerectomy with collagen implant. J Cataract Refract Surg, 2004; 30 : 1225–1231.
45. Skuta, G. L., Beeson, C. C., Higginbotham, E. J. et al.: Intraoperative mitomycin versus postoperative 5-fluorouracil in high-risk glaucoma filtering surgery. Ophthalmology, 1992; 99 : 438–444.
46. .Stegmann, R., Pienaar, A., Miller, D.: Viscocanalostomy for open-angle glaucoma in black African patiens. J Cataract Refract Surg, 1999; 25(3): 316–322.
47. Stegmann, R. C.: Viscocanalostomy: a new surgical technique for open angle glaucoma. Anales del Instituto Barraquer, 1995; 25 : 225–232.
48. Strnad, P., Svacinova, J., Vlkova, E.: Long-term follow up after non-penetrating glaucoma surgery, 11. In: Book of abstracts: 6th I.G.S., Athens, Greece, 2007, 209 p.
49. Strnad, P., Svačinová, J., Vlková, E.: Dlouhodobá kompenzace pacientů po nepenetrující filtrační operaci, 147. In: Sborník abstrakt XIV. výročního sjezdu ČOS, Galén, Praha, 2006, 232 s., ISBN 80-71777-974-1.
50. Strnad, P., Svačinová, J., Vlková, E.: Komplikace u neperforujících operací glaukomu, 45. In: Sborník abstrakt, kongres ČGS, Luhačovice, 2008, 61 s., ISBN 978-80-254-1568-9.
51. Strnad P., Svačinová J., Vlková E.: Neperforující operace glaukomu – komplikace, 43. In: Sborník abstrakt, Mezinárodní kongres ČSRKCH, Praha, 2008, ISBN 978-80-254-1569-6.
52. Strnad P., Svačinová J., Vlková E.: Deep nonpenetrating sclerectomy – complications, 344. In: Book of abstract, World Glaucoma Congress, Boston, July 8–11, 2009.
53. Strnad P., Svačinová J., Vlková E.: Komplikace u nepenetrujících hlubokých sklerektomií, 103-104. In: Sborník abstrakt XVII. výročního sjezdu ČOS, Praha, 2009, ISBN 978-80-254-5321-6.
54. Strnad P., Svačinová J., Vlková E.: Complications of non-penetrating glaucoma surgery, 56. In: Book of abstract, 4th International Congress on Glaucoma Surgery, Geneva, 2009.
55. Vaudaux, J., Mermoud, A.: Aqueous dynamics after deep sclerectomy: ex-vivo study. Ophthalmic Practice, 1998; 16 : 204–209.
56. Vlková, E., Svačinová, J., Danielová, L.: Hluboká sklerektomie v chirurgii glaukomu, 42. In: Sborník abstrakt VIII. výročního sjezdu ČOS, Galén, Praha, 2000, 166 s., ISBN 80-7262-066-5.
57. Vlková, E., Svačinová, J., Neugebauerová, T.: Hluboká sklerektomie s použitím dvou typů implantátů, In: Sborník abstrakt IX. výročního sjezdu ČOS, Galén, 2001, Praha, ISBN 80-7262-123-8.
58. Vlková, E., Svačinová, J., Schoříková, L.: Neperforující hluboká sklerektomie, 56. In: Sborník abstrakt VII. výročního sjezdu ČOS, Galén, Praha, 1999, 154 s., ISBN 80-7262-011-8.
59. Vouri, M. L.: Complications of Nd:YAG laser goniopuncture after deep sclerectomy. Acta Ophthalmol Scand; 2003; 81 : 573–576.
60. Watson, P. G., Jakeman, C., Ozturk, M. et al.: The complications of trabeculectomy. Eye, 1990; 4 : 425–438.
61. Zimmerman, T. J., Kooner, K. S., Ford, V. J. et al.: Effectiveness of non penetrating trabeculectomy in aphakic patients with glaucoma. Ophthalmic Surg, 1984; 15 : 44–50.
Štítky
Oftalmologie
Článek Aplázia zrakového nervu
Článek vyšel v časopiseČeská a slovenská oftalmologie
Nejčtenější tento týden
2012 Číslo 3- Stillova choroba: vzácné a závažné systémové onemocnění
- Familiární středomořská horečka
- Léčba chronické blefaritidy vyžaduje dlouhodobou péči
- První schválený léčivý přípravek pro terapii Leberovy hereditární optické neuropatie dostupný rovněž v ČR
- Kontaktní dermatitida očních víček
-
Všechny články tohoto čísla
- Psychometrická validácia verzie „Dotazníka zrakových funkcií-25“ v podmienkach Slovenska
- Komplikace u nepenetrujících hlubokých sklerektomií
- Srovnání měření tloušťky a zakřivení rohovky pomocí Scheimpflugovy kamery, laserové interferometrie, automatické keratometrie a ultrazvukové pachymetrie
- Stav chirurgie katarakty na Slovensku v rokoch 2008–2010
- Aplázia zrakového nervu
- Současný pohled na diabetický makulární edém
- Léčba vlhké formy věkem podmíněné makulární degenerace fotodynamickou terapií s verteporfinem – dlouhodobé výsledky
- Česká a slovenská oftalmologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Současný pohled na diabetický makulární edém
- Srovnání měření tloušťky a zakřivení rohovky pomocí Scheimpflugovy kamery, laserové interferometrie, automatické keratometrie a ultrazvukové pachymetrie
- Psychometrická validácia verzie „Dotazníka zrakových funkcií-25“ v podmienkach Slovenska
- Komplikace u nepenetrujících hlubokých sklerektomií
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



