-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Naše zkušenosti s maravirocem u HIV pozitivních pacientů
Autoři: Hana Vondráčková 1; Marie Staňková 2; Ladislav Machala 3; František Perlík 1; Ondřej Slanař 1
Působiště autorů: Univerzita Karlova v Praze, 1. lékařská fakulta, Farmakologický ústav 1; Univerzita Karlova v Praze, 1. lékařská fakulta, AIDS centrum FN Na Bulovce, Infekční klinika 1. LF UK a FN Na Bulovce 2; Univerzita Karlova v Praze, 2. lékařská fakulta, AIDS centrum FN Na Bulovce, Infekční klinika FN Na Bulovce 3
Vyšlo v časopise: Čas. Lék. čes. 2011; 150: 447-450
Kategorie: Původní práce
Souhrn
Východisko.
Přestože antiretrovirová terapie změnila klinický průběh HIV infekce, zůstává onemocnění AIDS nevyléčitelnou chorobou. Vznikají skupiny antiretrovirotik s novými mechanismy účinku. Mezi nimi inhibitory vstupu, jejichž jediným registrovaným zástupcem je maraviroc. Primárním cílem práce je vyhodnotit klinickou účinnost maravirocu pomocí parametru virové nálože změřené do 4. týdne od zahájení léčby, sekundárním cílem je vyhodnotit účinnost léčiva do 125. týdne sledováním změn hodnot virové nálože a změn počtu CD4+ lymfocytů. Rovněž je hodnocena bezpečnost léčiva.Metody a výsledky.
Do skupiny pacientů jsme zařadili celkem 23 subjektů, dva pacienty z České republiky a 21 pacientů z Francie. Virová nálož poklesla ve 4., 24. i 48. týdnu více než o dva řády (-2,136; -2,448; -2,452 log10 kopií/ml). V počtu CD4+ lymfocytů docházelo k nárůstu hodnot (71,71; 142,00; 196,43 buněk/mm3). Bezpečnost léčiva byla hodnocena sledováním četnosti výskytu nežádoucích účinků. Získaná data jsme porovnali s registračními klinickými studiemi III. fáze. Během léčby se objevilo jedenáct podezření na nežádoucí účinky, žádné z těchto podezření nebylo dáno do příčinné souvislosti s terapií maravirocem. Nejčastější z nich patří do skupiny neurologických nežádoucích účinků.Závěry.
Naše zkušenosti s maravirocem byly pozitivní, léčivo se osvědčilo jako účinné antiretrovirotikum pro kombinační léčbu HIV infekce.Klíčová slova:
maraviroc, CCR5 inhibitory, HIV, AIDS.ÚVOD
Syndrom získaného selhání imunity (AIDS) je soubor příznaků a infekcí, který je důsledkem stupňujícího se poškození imunitního systému člověka virem lidské imunodeficience HIV. Tato progrese a s tím spojený klinický obraz byly rozděleny do šesti etap podle Walter-Reedova klasifikačního systému. Zjednodušeně se infekce HIV rozděluje častěji na tři fáze: fáze primoinfekce, chronická fáze a fáze rozvinutého onemocnění AIDS (1).
Původce onemocnění AIDS – virus HIV – patří do čeledi Retroviridae, rod Lentivirus. V současné době jsou známy dva typy HIV: predominantní HIV 1 a méně patogenní HIV 2. Na základě genetických rozdílů především v env oblasti genomu se HIV-1 člení do tří skupin: M, N a O. Skupina M je v podstatě zodpovědná za světovou epidemii. Kmeny v ní zahrnuté se rozdělují do odlišných subtypů, které vykazují určitou geografickou preferenci. Například subtyp B dominuje zejména v Americe, v Evropě a je dominantním subtypem i v České republice. Mezi jednotlivými subtypy jsou patrné biologické rozdíly. Jedna a tatáž osoba a stejně tak jedna a tatáž buňka může být nakažena zároveň více typy viru HIV (2).
Vývoj léčby HIV infekce znamenal obrovský pokrok a přínos pro mnoho pacientů. Nicméně i přes již dosažené úspěchy zůstávají virová rezistence a tolerance limitujícími faktory léčby (3). Objevují se proto nové třídy antiretrovirotik s novými mechanismy účinku. Mezi ně patří i inhibitory vstupu viru HIV do hostitelské buňky. V současné době je jediným registrovaným zástupcem této třídy maraviroc, který se selektivně váže na lidský chemokinový koreceptor CCR5 a zabraňuje tak R5-tropnímu HIV-1 viru ve vstupu do buněk (4). Vedle molekuly CD4 je právě CCR5 či CXCR4 koreceptor nezbytný pro vstup viru HIV do hostitelské buňky (5, 6). Varianty viru HIV-1 se odlišují využitím vazebných koreceptorů. Buď virus může využít pouze CCR5 koreceptor, nebo výhradně CXCR4 koreceptor nebo může používat střídavě oba (7). Maraviroc byl v Evropské unii registrován v říjnu roku 2008, na území USA již v říjnu roku 2007 (8). Maraviroc je v kombinaci s ostatními antiretrovirovými léčivými přípravky indikován k léčbě pacientů infikovaných jen prokazatelným R5-tropním HIV-1 virem. Na základě výsledků klinické studie byla nejprve schválena indikace maravirocu pro léčbu HIV+ dospělých pacientů, kteří již dříve byli léčeni antiretrovirovými přípravky.Nicméně v listopadu roku 2009 byla ve Spojených státech amerických FDA (Úřad pro kontrolu potravin a léků – Food and Drug Administration) rozšířena indikace maravirocu i pro terapeuticky naivní dospělé pacienty infikované R5-tropním HIV-1 virem (4). Maraviroc je substrátem cytochromu P450 CYP3A4. Pokud je maraviroc podáván současně s inhibitory a/nebo induktory CYP3A4, může být ovlivněna jeho koncentrace i terapeutický účinek, a proto se doporučuje úprava dávkování. Renální clearance představuje přibližně 23 % celkové clearance maravirocu, pokud je podáván bez inhibitorů CYP3A4. Nejčastěji zaznamenanými nežádoucími účinky během studií III. fáze při doporučeném dávkování – bez ohledu na incidenci v porovnání k samotné optimalizované základní terapii (OBT) – byly průjem, nauzea a bolest hlavy. Tyto nežádoucí účinky byly časté (0,01–0,1%). Dosavadní studie prokázaly, že maraviroc je aktivní vůči virům rezistentním na dosud existující antiretrovirovou terapii. V budoucnosti však lze předpokládat, že ani maraviroc nebude v problematice rezistence výjimkou (9).
SOUBOR NEMOCNÝCH A POUŽITÉ METODY
Do skupiny pacientů jsme zařadili celkem 23 osob užívajících jako součást své antiretrovirové terapie maraviroc (Celsentri®, Pfizer). Dva pacienti jsou léčeni v pražském AIDS centru Fakultní nemocnice Na Bulovce a 21 pacientů se léčí ve fakultní nemocnici Lapeyronie (Centre Hospitalier Universitaire Montpellier) v jihofrancouzském městě Montpellier. Zařazovacími kritérii bylo absolvování minimálně již jedné léčebné linie či terapeutický neúspěch v anamnéze (tzn. virová nálož vyšší než 5000 kopií HIV RNA/ml nebo nutnost přerušení léčby), stabilní léčba nebo bez léčby po dobu minimálně 4 týdnů před nasazením maravirocu, věk nad 16 let a prokázaný R5-tropní HIV-1. U každého pacienta jsme před zahájením léčby odebrali čerstvý vzorek krve, podmínkou byla minimální hodnota virové nálože 1000 kopií HIV RNA/ml krve pro zajištění dostatečné citlivosti vyšetření. V současné době je nejpoužívanější Trofile Assay (9), který se provádí v laboratořích v San Franciscu. Výsledky testu jsou v České republice i ve Francii k dispozici za 3–4 týdny po odebrání vzorku.
Klinicky jsme sledovali dva hlavní parametry získávané z imunologické a sérologické laboratoře. Prvním parametrem byla hodnota virové nálože (VL), jež odráží rychlost vývoje nemoci a představuje množství virové RNA (nebo jejich kopií) v 1 ml krve. Detekční metoda měřící hladinu virové nálože má citlivost 20 kopií RNA/ml. Hodnoty virové nálože jsme zlogaritmovali, a sledovali jsme tak pokles virové nálože v řádech. Druhým hodnoceným parametrem byl počet CD4+ lymfocytů reflektující imunologický stav nemocného. Oba dva parametry účinnosti jsme zaznamenávali v určených časových intervalech; zde uvádíme hodnoty těsně před zahájením léčby, dále ve 4., 24. a 48. týdnu od zahájení léčby maravirocem. Primárním parametrem účinnosti byl stanoven rozdíl ve virové náloži ve 4. týdnu léčby oproti vstupní hodnotě. Kromě uvedených laboratorních parametrů jsme se zaměřili také na četnost výskytu nežádoucích účinků v našem souboru pacientů. Všechny nežádoucí účinky jsme identifikovali a vyhodnotili dle údajů v SPC a závěrů III. fáze klinických studií MOTIVATE 1 a MOTIVATE 2.
Statistická analýza
Pro statistické vyhodnocení změny virové nálože a počtu CD4+ buněk byl použit neparametrický párový Wilcoxonův test (statistický software Unistat 5.1.). Statistická významnost byla hodnocena při p < 0,05.
VÝSLEDKY
Základní demografická data jsou shrnuta v tabulce 1. Minimální doba léčby infekce HIV byla 9 let. Rozdíly hodnot virové nálože oproti výchozí hodnotě v čase včetně procentuálních podílů pacientů dosahujících na snížení virové nálože pod 50 nebo 400 kopií HIV RNA/ml krve jsou shrnuty v tabulce 2. Rozdíly mezi výchozí hodnotou a následujícími hodnotami v dalších časových intervalech jsou statisticky vysoce významné (p < 0,01). Procento pacientů dosahující hodnot virové nálože pod 400 kopií/ml se v průběhu léčby statisticky signifikantně zvyšovalo (p < 0,01). Rovněž procento pacientů dosahující hodnot virové nálože pod 50 kopií HIV RNA/ml v čase statisticky významně narůstalo (p < 0,01).
Tab. 1. Základní demografická charakteristika souboru – x̄ (SD) 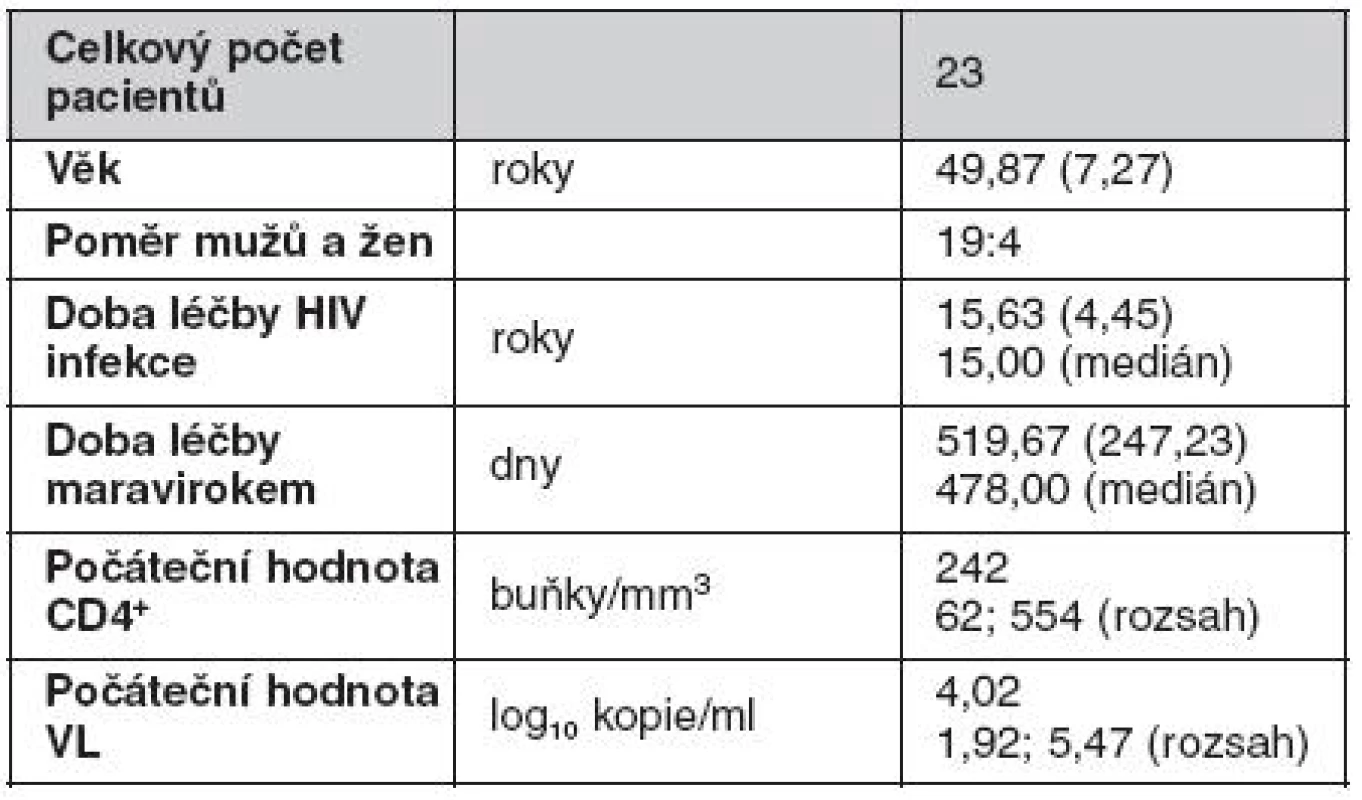
Tab. 2. Rozdíl hodnot virové nálože proti výchozí hodnotě ve 4., 24. a 48. týdnu po zahájení léčby 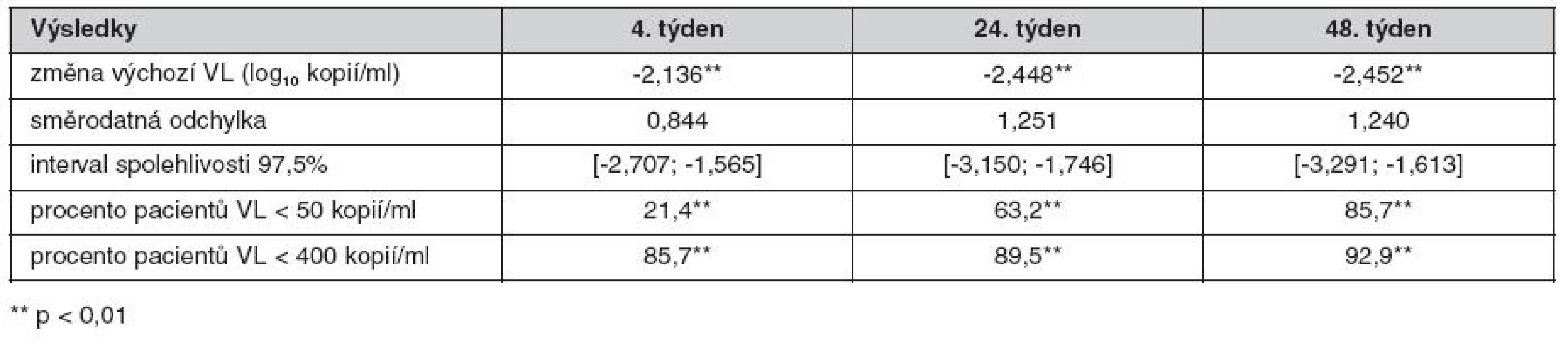
Statisticky významné rozdíly v absolutním počtu CD4+ buněk v daných časových intervalech jsou uvedeny v tabulce 3.
Tab. 3. Rozdíl počtu CD4<sup>+</sup> lymfocytů proti výchozí hodnotě ve 4., 24. a 48. týdnu po zahájení léčby 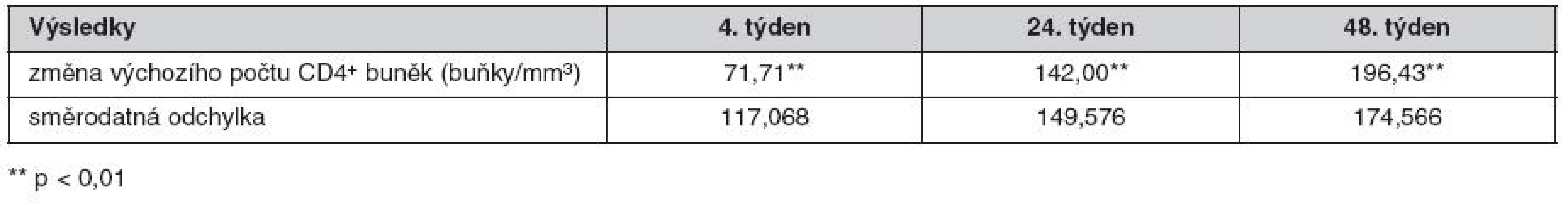
Hodnoty virové nálože a CD4+ lymfocytů v průběhu léčby znázorňují obrázky 1 a 2. Pokles virové nálože probíhal po dvou exponenciálách. Do 8. týdne se virová nálož rychle snižovala (T1/2 = 1,7 týdne). Následovala pomalá fáze mizení (T1/2 = 404,9 týdne). Pozvolný vzestup CD4+ lymfocytů byl v negativním regresním vztahu s virovou náloží (r = -0,80; p < 0,01). V průběhu léčby pacientů maravirocem žádný pacient z léčby neodstoupil a nebyl ošetřujícím lékařem ani pacientem hlášen žádný nežádoucí účinek, a to jak ve francouzském zdravotnickém zařízení, tak v českém AIDS centru. Problém se snášenlivostí nevznikl ani u „komplikovaných“ pacientů těžce tolerujících předchozí terapeutické linie. V průběhu léčby bylo zaznamenáno celkem jedenáct podezření na nežádoucí účinky u osmi pacientů, nejčastější z nich byly neurologické obtíže, akutní obstrukční renální nedostatečnost, srdeční ischémie a dále bolesti kostí, zvýšená hladina kyseliny močové, hypercholesterolémie, hypertriglyceridémie a imunorestituční zánětlivý syndrom. U těchto nežádoucích účinků nebyla ale shledána příčinná souvislost s terapií maravirocem.
Obr. 1. Hodnoty virové nálože v průběhu léčby (x̄, SD) ** p < 0,01; * p < 0,05 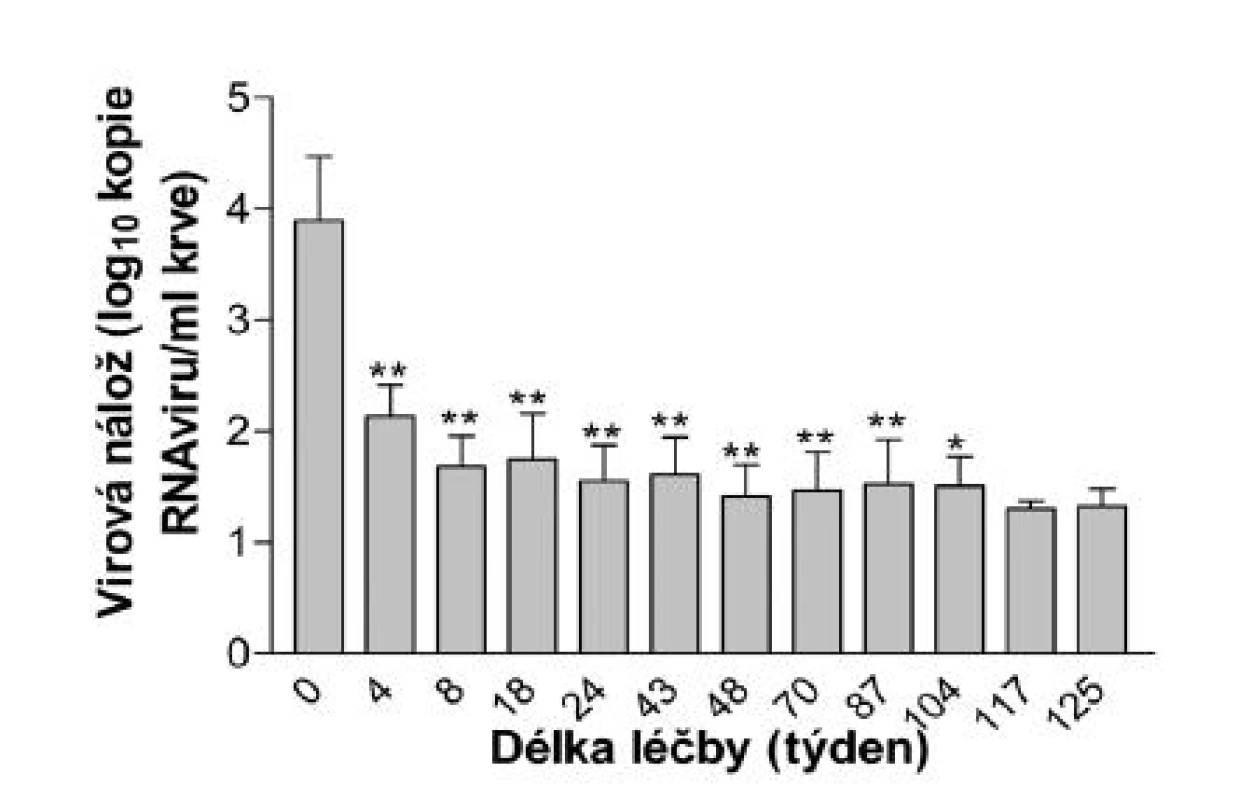
Obr. 2. Hodnoty CD4+ lymfocytů v procentech v průběhu léčby (x̄, SD) ** p < 0,01; * p < 0,05 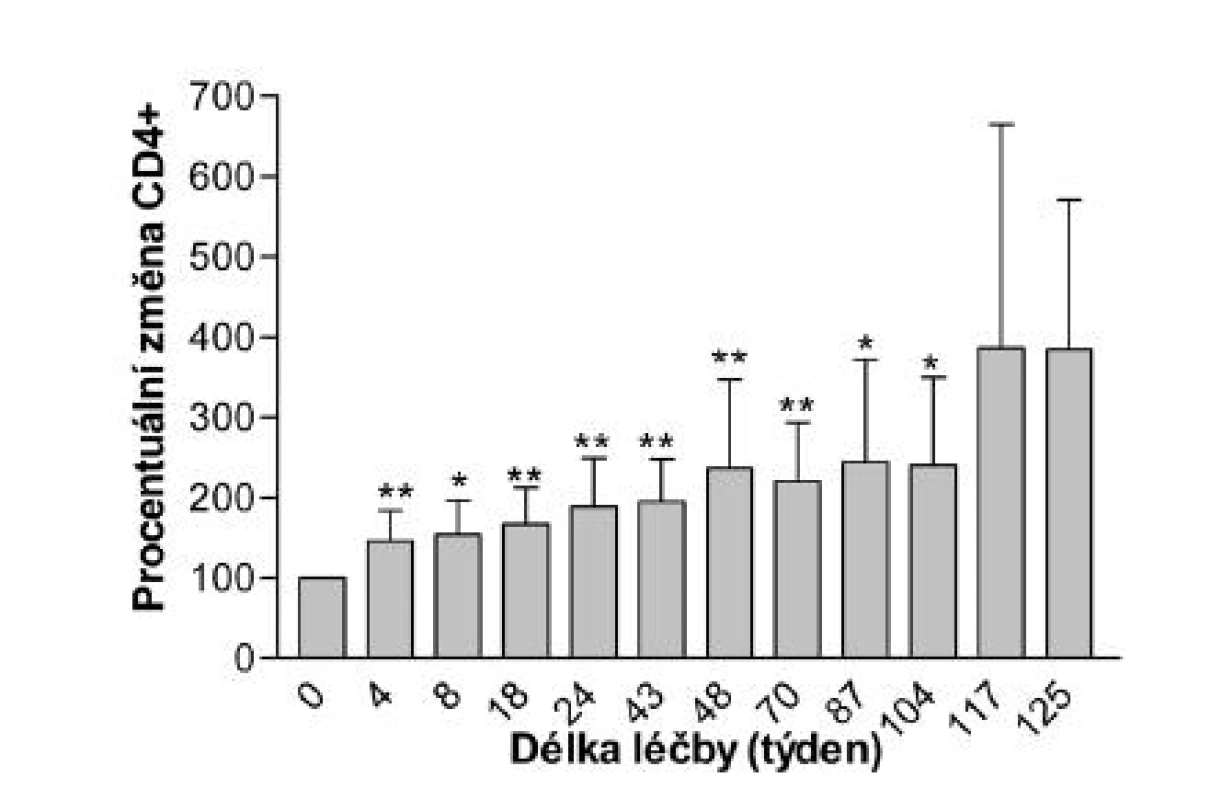
DISKUZE
Problematika viru HIV a s ním spojeného onemocnění AIDS zůstává mezi významnými celosvětovými problémy (10). Evidentní nárůst přenosu tohoto viru je pravidelně zaznamenáván v řadě zemí včetně České republiky, kde bylo mezi říjnem roku 1985 a lednem roku 2011 nahlášeno celkem 1536 HIV pozitivních osob s každoročně stoupající prevalencí (11). Navzdory poklesu morbidity a mortality na onemocnění AIDS v důsledku zavedení kombinované antiretrovirové terapie (cART) je účinnost léčby stále významně limitována řadou faktorů. Třemi nejčastějšími důvody selhání léčby, které spolu logicky souvisí, jsou špatná compliance, jež je vyžadována ze strany pacienta minimálně na 95 %, špatná tolerance léčby a nedostatečná účinnost léčby. Navíc je třeba si uvědomit, že všechna dostupná antiretrovirotika zajišťují pouze dočasnou supresi virové nálože. Kauzální lék, který by vedl ke kompletní eradikaci infekce, zatím neexistuje (12).
Změna virové nálože po přibližně měsíci léčby maravirocem představovala markantní pokles virové nálože, a to přibližně o dva řády (2,136). U naprosté většiny pacientů užívání maravirocu výrazně snížilo hodnotu virové nálože a dokázalo tuto hodnotu udržet po celé období, které bylo v této práci sledováno, tj. až po 125. týden. V průběhu času lze vysledovat klesající trend, který však vykazuje jistou variabilitu jednotlivých pacientů podmíněnou řadou faktorů, jako je compliance daného pacienta a jeho celkový stav s ohledem na přítomnost či absenci superponujících infekcí. Pozitivním výstupem je rovněž vysoké procento pacientů dosahujících virové nálože pod 400 kopií HIV RNA/ml krve již záhy po zahájení léčby a v čase vzrůstající procento pacientů, jež dosahují hodnot nižších než 50 kopií HIV RNA/ml krve. Pozorované výsledky se shodují s výsledky dosaženými v průběhu III. fáze klinického hodnocení léčiva. Maximální redukce virové nálože po co možná nejdelší dobu je jedním z hlavních terapeutických cílů,neboť vede k zastavení či alespoň zpomalení progrese onemocnění a pomáhá zabránit nebo alespoň oddálit rozvoj rezistence (13). V současné době by se účinnost antiretrovirového léčiva měla již po měsíci léčby projevit poklesem hladiny virové nálože minimálně o jeden řád, aby bylo možné prohlásit terapii léčivem za úspěšnou (12).
Druhým pozorovaným parametrem je hodnota CD4+ lymfocytů zobrazující imunologický stav nemocného. Reflektuje ne/rovnováhu mezi produkcí a destrukcí CD4+ lymfocytů (12). V našem souboru pacientů jsme zaznamenali postupný nárůst CD4+ lymfocytů. U individuálních pacientů je nárůst pozvolný a kolísá, což lze vysvětlit obecně obtížně dosažitelnou reparací lidského imunitního systému, rozdílnou compliance a rovněž odlišným celkovým zdravotním stavem každého pacienta. Obnovu imunitního systému rovněž komplikuje výskyt imunorestitučního zánětlivého syndromu (z angl. „Immune reconstitution inflammatory syndrome IRIS), který se vyskytuje v 10–32 % případů, a objevuje se zejména u pacientů, jimž byla nasazena antiretrovirová léčba vůbec poprvé či po terapeutické pauze. Syndrom se projevuje zhoršením celkového klinického stavu manifestujícího se zvýšeným počtem oportunních infekcí virového, bakteriálního i mykotického původu (14). Podezření na výskyt tohoto syndromu jsme měli u jednoho pacienta, u něhož se krátce po zahájení léčby objevily příznaky akutního chřipkového onemocnění, které nevyžadovalo farmakologickou léčbu. Je možné, že se jednalo o nežádoucí účinek maravirocu. I v případě hodnot CD4+ lymfocytů naše výsledky potvrzují výsledky z registračních studií III. fáze klinického hodnocení maravirocu.
Během této práce žádný pacient nevysadil léčbu z důvodu špatné tolerance. V průběhu léčby se vyskytlo několik možných podezření na nežádoucí účinky maravirocu, nicméně u žádného z nich nebyla prokázána příčinná souvislosti s maravirocem. Pacienti užívali kombinaci více antiretrovirotik současně, nežádoucí jevy tedy mohly souviset i s ostatními léčivy v kombinaci. Dle výsledků klinických studií se dal předpokládat výskyt zejména průjmů, nauzey a bolestí hlavy, které se ve III. fázi studií objevovaly často, tj. v 0,01–0,1 % případů. V souboru pacientů zahrnutém v této práci se z těchto obtíží vyskytla jedenkrát bolest hlavy.
ZÁVĚR
Naše práce celkově potvrzuje výsledky klinických studií A4001027 a A4001028, uskutečněných na území USA, Kanady, Evropy a Austrálie (15).
Maraviroc byl ve studii účinným a dobře tolerovaným léčivem, které v kombinovaném terapeutickém režimu bylo a jistě i nadále bude významným přínosem pro terapii HIV infekce.
Zkratky
- AIDS – syndrom získaného selhání imunity
- cART – kombinovaná antiretrovirová terapie
- FDA – Úřad pro kontrolu potravin a léků (USA)
- HIV – lidský virus imunitní nedostatečnosti
- IRIS – imunorestituční zánětlivý syndrom
- OBT – optimalizovaná základní terapie
- RNA – ribonukleová kyselina
- SD – směrodatná odchylka
- SPC – souhrn údajů o přípravku
- T1/2 – terapeutický poločas
- VL – virová nálož
Děkujeme Sylvie Hansel-Esteller a Nicolas Terrail z podílejícího se pracoviště Centre Hospitalier Universitaire Montpellier pod záštitou Université Montpellier 1.
ADRESA PRO KORESPONDENCI:
PharmDr. Hana Vondráčková
Farmakologický ústav 1. LF UK
Albertov 4, 128 00 Praha 2
fax: +420 224 968 149
e-mail: hana.vondrackova@centrum.cz
Zdroje
1. Montagnier L. AIDS: fakta – naděje. 2 ed. Praha: Státní zdravotní ústav 1996.
2. Osmnact A, Gimenez F. Pharmacie clinique et thérapeutique. Paříž: Masson 2000.
3. Smith S, Raymond A. Encyclopedia of AIDS – a social, political, cultural, and scientific record of the HIV epidemic. 1 ed. Chicago: Fitzroy Dearborn Publishers 1998.
4. Souhrn údajů o přípravku Celsentri [cited 4. 1. 2010]; http://www.pfizer.cz/files/spc/pfizer/Celsentri/Celsentri-150mg_SPC_dec_2009.pdf
5. Hans P S, Schellhorn S, Dezube B J, et al. New approaches in the treatement of HIV/AIDS – focus on maraviroc and other CCR5 anatgonists. Ther Clin Risk Manag 2008; 4(2): 473–485.
6. Armour D, Groot M J, Edwards M, et al. The discovery of CCR5 receptor antagonists for the treatment of HIV infection: hit-to-lead studies. Chem Med Chem 2006; 1(7): 706–709.
7. Jeannette MW, Wei H. Development and Charakteriaztion of a Novel Single-Cycle Recombinant-Virus Assay To Determine Human Immunodeficiency Virus Type 1 Coreceptor Tropisme. Antimicrob Agents and Chemother 1997; 51(2): 566-575.
8. Souhrn rozhodnutí Společenství o registraci léčivých přípravků od 1. října 2008 do 31. října 2008, Úřední věstník Evropské unie, Editor. 2008. C305/3.
9. Neelanjana R. Maraviroc in the treatement of HIV infection. Drug Des Devel Ther, 2008; (2): 151–161.
10. Matýšková M, Snopková S. HIV/AIDS a patologie v krevním obrazu. Čas Lék čes, 2007; (146): 68–73.
11. Zpráva o výskytu a šíření HIV/AIDS v ČR za rok 2011; www.szu.cz/tema/prevence/ zprava-o-vyskytu-a-sireni-aids-za-rok-2011
12. Yeni P. Prise en charge médicale des personnes infectés par le VIH: recommandations du group d’experts. Paříž: Flammarion SA 2008.
13. Staňková M. Novinky v antiretrovirové terapii HIV/AIDS infekce. Interní Med. 2008; 10(11): 498-502.
14. Beishuizen SJ, Geerlings SE. Immune reconstitution inflammatory syndrome: immunopathogenesis, risk factors, diagnosis, treatment and prevention. Neth J Med 2009; 67(10): 327-331.
15. EPAR Celsentri – Scientific Discussion/human. [cited 23. 02. 2010]; http://www.ema.europa.eu/docs/en_GB/document_ library/EPAR_-_Scientific_Discussion/human/000811/ WC500022194.pdf
Štítky
Adiktologie Alergologie a imunologie Anesteziologie a resuscitace Angiologie Audiologie a foniatrie Biochemie Dermatologie Dětská dermatologie Dětská gastroenterologie Dětská gynekologie Dětská chirurgie Dětská kardiologie Dětská nefrologie Dětská neurologie Dětská onkologie Dětská otorinolaryngologie Dětská pneumologie Dětská psychiatrie Dětská radiologie Dětská revmatologie Dětská urologie Diabetologie Endokrinologie Farmacie Farmakologie Fyzioterapie Gastroenterologie a hepatologie Genetika Geriatrie a gerontologie Gynekologie a porodnictví Hematologie a transfuzní lékařství Hygiena a epidemiologie Hyperbarická medicína Chirurgie cévní Chirurgie hrudní Chirurgie plastická Chirurgie všeobecná Infekční lékařství Intenzivní medicína Kardiochirurgie Kardiologie Logopedie Mikrobiologie Nefrologie Neonatologie Neurochirurgie Neurologie Nukleární medicína Nutriční terapeut Obezitologie Oftalmologie Onkologie Ortodoncie Ortopedie Otorinolaryngologie Patologie Pediatrie Pneumologie a ftizeologie Popáleninová medicína Posudkové lékařství Praktické lékařství pro děti a dorost Protetika Psychologie Radiodiagnostika Radioterapie Rehabilitační a fyzikální medicína Reprodukční medicína Revmatologie Sestra Sexuologie Soudní lékařství Stomatologie Tělovýchovné lékařství Toxikologie Traumatologie Urgentní medicína Urologie Laboratoř Domácí péče Foniatrie Algeziologie Zdravotnictví Dentální hygienistka Student medicíny
Článek Laureáti Nobelovy ceny
Článek vyšel v časopiseČasopis lékařů českých
Nejčtenější tento týden
- Psilocybin je v Česku od 1. ledna 2026 schválený. Co to znamená v praxi?
- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
-
Všechny články tohoto čísla
- Reaktivní kyslíkové a dusíkové sloučeniny v klinické medicíně
- Současné možnosti léčení poranění pánevního kruhu
- Klinický význam nemoci spojené s imunoglobuliny IgG4
- Nejčastěji využívané metodiky k analýze DNA metylačních změn
- Udělení Ceny Jana Evangelisty Purkyně
- Naše zkušenosti s maravirocem u HIV pozitivních pacientů
- Antiepileptické léky a lékové interakce: klinická kazuistika
- Plánované akce odborných složek ČLS JEP
- Hazard u dětí a dospívajících
-
Hygiena ženy II
Doba rudolfínská -
XI. jihočeské Timrovy dny
Hluboká nad Vltavou, 21.–22. dubna 2011 -
VI. sympozium o léčbě bolesti*
Brno, 29.–30. dubna 2011 -
26. pracovní dny – Dědičné metabolické poruchy
Mikulov, 11–13. května 2011 -
Evropské perspektivy v personalizované medicíně
Brusel, 12.–13. května 2011 - Jiří Mareš, Eva Vachková a kol.: PACIENTOVO POJETÍ NEMOCI II
- Laureáti Nobelovy ceny
- Časopis lékařů českých
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Současné možnosti léčení poranění pánevního kruhu
- Klinický význam nemoci spojené s imunoglobuliny IgG4
- Reaktivní kyslíkové a dusíkové sloučeniny v klinické medicíně
- Nejčastěji využívané metodiky k analýze DNA metylačních změn
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



