-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Fixní léčba CLL – realita, nebo fikce?
15. 2. 2023
Na 23. pražských hematologických dnech uspořádala 20. ledna 2023 společnost Abbvie sympozium věnované aktuálním postupům v terapii chronické lymfocytární leukémie (CLL).
Úvod
Pod předsednictvím prof. MUDr. Michaela Doubka, Ph.D., prezentoval prof. MUDr. Lukáš Smolej, Ph.D., aktualizované 5leté výsledky studie CLL14, které potvrzují klinický přínos časově omezeného režimu venetoklax + obinutuzumab v 1. linii léčby CLL v porovnání s režimem chlorambucil + obinutuzumab z hlediska prodloužení přežití bez progrese (PFS), doby do další terapie a zvýšení šance na dosažení negativity minimální reziduální nemoci (MRN), a to při absenci nových bezpečnostních signálů. Na kazuistice 72leté pacientky demonstroval efekt tohoto terapeutického postupu současně s potřebou podpůrné léčby, prevence syndromu z rozpadu nádoru (TLS) a prevence a léčby infekcí.
Prim. MUDr. Martin Špaček, Ph.D., se ve své přednášce zaměřil na stávající doporučení pro léčbu CLL a výsledky klinických studií, z nichž tato doporučení vycházejí. Shrnul také aktuální terapeutické přístupy v Česku, které již zahrnují režimy venetoklax + obinutuzumab s fixní délkou podání 12 měsíců v 1. linii a režim venetoklax + rituximab s délkou podání 24 měsíců ve 2. linii, a dal posluchačům nahlédnout do blízké budoucnosti léčby CLL, která by mohla přinést kombinaci venetoklaxu s ibrutinibem, léčbu vedenou podle dosažení negativity MRN, a možná i buněčnou terapii.
InzerceRežim venetoklax + obinutuzumab v teorii a praxi
prof. MUDr. Lukáš Smolej, Ph.D., IV. interní hematologická klinika LF UK a FN Hradec Králové
Aktualizované výsledky studie CLL14 po 5letém sledování
CLL14 je studie fáze III,1 ve které bylo randomizováno 432 pacientů s neléčenou aktivní CLL s komorbiditami (skóre komorbidit CIRS > 6 nebo clearance kreatininu < 70 ml/min) k podávání venetoklaxu (400 mg/den p.o. po dobu maximálně 12 měsíců) + obinutuzumabu (1000 mg i.v. 1., 8. a 15. den cyklu a poté 1. den 2.–6. cyklu) nebo chlorambucilu (0,5 mg/kg p.o. 1. a 15. den každého z ≤ 12 cyklů) + obinutuzumabu ve stejném dávkování s délkou cyklu 28 dní. Dávka venetoklaxu byla postupně navyšována z 20 na 400 mg/den z důvodu snížení rizika TLS. Primárním sledovaným parametrem bylo PFS.
Randomizace proběhla v poměru 1 : 1 a vstupní charakteristiky pacientů byly v obou terapeutických skupinách srovnatelné: průměrný věk 72, resp. 71 let, medián CIRS 9, resp. 8, stadium Binet C v obou skupinách u 43 % a absence mutace IGHV u 61, resp. 59 % pacientů. Zařazeni byli i nemocní s delecí 17p (9, resp. 7 %) a mutací TP53 (11, resp. 8 %). Také distribuce nízkého/středního/vysokého rizika TLS byla podobná, přičemž většina pacientů (64, resp. 68 %) měla střední riziko definované jako mízní uzliny 5–10 cm nebo absolutní počet lymfocytů (ALC) ≥ 25 × 109/l. Vysoké riziko definované jako mízní uzliny ≥ 10 cm nebo ALC ≥ 25 × 109/l + mízní uzliny ≥ 5 cm bylo přítomno u 22, resp. 20 % zařazených.
Na kongresu EHA byly v roce 2022 prezentovány výsledky této studie po > 5 letech sledování (medián délky sledování 65 měsíců).2 Medián PFS nebyl ve skupině s venetoklaxem dosažen, ve skupině s chlorambucilem dosáhl 36 měsíců. Po 5 letech bylo naživu bez progrese onemocnění 63 % pacientů s venetoklaxem v porovnání s 27 % pacientů s chlorambucilem (poměr rizik = 0,35; p < 0,0001) (obr. 1).
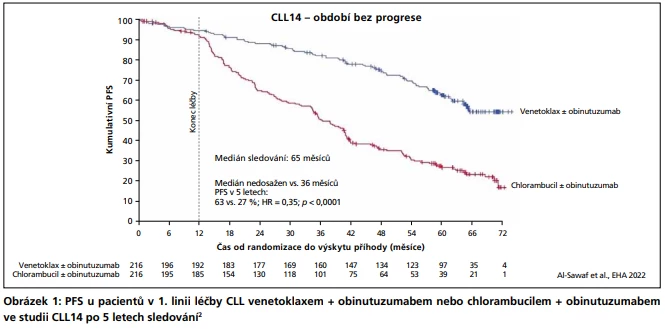
Přínos přidání venetoklaxu k obinutuzumabu v porovnání s chlorambucilem z hlediska PFS byl prokázán nezávisle na stavu mutace IGHV či TP53, což jsou nezávislé prognostické faktory PFS.2, 3 I při léčbě venetoklaxem měli ale pacienti s nemutovaným IGHV a pacienti s mutací TP53 kratší PFS. Jako jediné nezávislé prognostické faktory PFS byly v rameni s venetoklaxem + obinutuzumabem identifikovány ale jen delece 17p a vysoká nádorová nálož (definovaná podle rizika TLS).2, 3 Ve skupině s chlorambucilem bylo nezávislých prognostických faktorů PFS zjištěno více.
Kombinace venetoklax + obinutuzumab prokázala přínos také z hlediska období do další léčby (TTNT), což je klinicky významný parametr zejména z pohledu pacienta. Po 5 letech užívalo 2. linii léčby 31 pacientů ze skupiny s venetoklaxem (medián TTNT nedosažen) a 94 pacientů ze skupiny s chlorambucilem (TTNT 53 měsíců). Následná léčba spočívala převážně v podávání inhibitorů Brutonovy tyrosinkinázy (BTKi), (58 vs. 54 %).
Medián celkového přežití (OS) nebyl v žádné z terapeutických skupin dosažen. Po 5 letech bylo naživu 82 % nemocných zařazených do skupiny s venetoklaxem a 77 % v kontrolním rameni, rozdíl není statisticky významný (p = 0,12).
Dalším důležitým zjištěním je, že venetoklax + obinutuzumab dokáže u většiny nemocných s CLL navodit negativitu MRN. Na konci léčby dosáhlo negativity MRN (hodnoceno pomocí ASO-PCR) v periferní krvi 76 % pacientů s venetoklaxem a 35 % s chlorambucilem (p < 0,001), negativita MRN v kostní dřeni pak byla zjištěna u 57 % pacientů s venetoklaxem a pouze u 17 % s chlorambucilem (p < 0,001). Negativita MRN na konci léčby byla spojena s delším obdobím do progrese po ukončení terapie. Při použití sekvenování nové generace (NGS) pro stanovení MRN bylo u pacientů s MRN < 10–4 na konci terapie zjištěno také delší OS po skončení léčby. Tyto výsledky jsou v souladu s nálezem pomalejšího růstu klonu CLL po léčbě venetoklaxem.1–3
Podíl pacientů s celkovou odpovědí na léčbu (ORR) dosáhl při léčbě venetoklaxem 85 % včetně 50 % kompletních remisí (CR), v porovnání s ORR 71 % a CR 23 % při léčbě chlorambucilem.
5leté sledování nepřineslo žádné nové bezpečnostní signály týkající se podávání venetoklaxu v kombinaci s obinutuzumabem oproti předchozím zjištěním. Výskyt nežádoucích příhod stupně ≥ 3 byl podobný jako při chemoimunoterapii chlorambucilem + obinutuzumabem. Nejčastěji se jednalo o neutropenii (53 vs. 48 %), trombocytopenii (14 vs. 15 %), infekce (18 vs. 15 %), syndrom nádorového rozpadu (TLS; 2 vs. 3 %), výskyt druhé primární malignity (26 vs. 21 %) a Richterův syndrom (1 % v obou skupinách). Po skončení léčby byla toxicita minimální.1–3 TLS se ve skupině s venetoklaxem vyskytl v obou případech 1. den 1. cyklu po aplikaci obinutuzumabu ještě před podáním venetoklaxu.
Léčba režimem venetoklax + obinutuzumab v praxi – kazuistika
U ženy narozené v roce 1950 byla v listopadu 2017 diagnostikována CLL. Jedná se o pacientku ve starobním důchodu s dobrou rodinnou podporou. V osobní anamnéze má hypotyreózu, polyartrózu a chronické žilní onemocnění. Zjištěná CLL byla stadia Rai I a tato dobře spolupracující nemocná byla zpočátku pouze sledována. Měla ale nepříznivé prognostické faktory – nemutovaný gen IGHV a deleci 11q + 13q. Nebyla přítomná mutace TP53.
K progresi onemocnění došlo po necelých 5 letech a léčba CLL byla zahájena v lednu 2022. Přítomná byla hyperleukocytóza (Leu 242 × 109/l), závažná anémie (Hb 77 g/l; MCV 99,6 fl), trombocytopenie (PLT 21 × 109/l) a neutropenie (ANC 0,51 × 109/l) s masivní infiltrací kostní dřeně (klon CLL 96 %). Zjištěn byl také generalizovaný uzlinový syndrom s maximem nitrobřišně (110 × 60 mm) a zvětšení sleziny na 165 mm. Riziko TLS bylo vyhodnoceno jako vysoké. Indikován byl režim obinutuzumab + venetoklax. Podpůrná léčba zahrnovala druhou dávku očkování proti COVID-19 před léčbou, za hospitalizace i.v. hydrataci, alopurinol, transfuze erytrocytů a trombocytů a podávání faktoru stimulujícího kolonie granulocytů (G-CSF). Podání obinutuzumabu proběhlo bez závažné reakce. V únoru během postupného navyšování dávky venetoklaxu však pacientka onemocněla COVID-19. Byla léčena ve spádové ambulanci remdesivirem i.v. po dobu 3 dnů. Infekce u ní měla prolongovaný průběh, pozitivita dle PCR i příznaky přetrvávaly přes 4 týdny. Antileukemická léčba byla přerušena a pro pozitivitu kultivace sputa byla nasazena antibiotika.
Léčba venetoklaxem (opět s postupným navyšováním dávky) v kombinaci s obinutuzumabem pokračovala po 6týdenním přerušení od konce března již bez významných komplikací. Byl podáván G-CSF k udržení ANC > 1,0 × 109/l po dobu prvních 3 dnů denně a poté 1× týdně. Kontroly krevního obrazu probíhaly u praktické lékařky a 6. cyklus léčby absolvovala pacientka v srpnu 2022. V září z důvodu prevence infekce COVID-19 obdržela tixagevimab + cilgavimab. Krevní obraz ukázal postupné navýšení počtu trombocytů i hladiny hemoglobinu s dosažením normálních hodnot po 3 měsících léčby, což bylo spojeno se zvýšením kvality života. Po 6 cyklech venetoklaxu ukázala ultrasonografie břicha kompletní regresi lymfadenopatie a normální velikost sleziny.
Poslední kontrola proběhla v lednu 2023. Pacientka se cítí dobře, kromě mírné chronické rýmy je bez infekcí, nehubne. Fyzikální nález má normální, stejně jako krevní obraz (Leu 5,2 × 109/l; Hb 147 g/l; MCV 90 fl; PLT 207 × 109/l; ANC 2,4 × 109/l) a biochemická vyšetření včetně laktátdehydrogenázy (LDH) a C-reaktivního proteinu (CRP). Rovněž vyšetření MRN z periferní krve je negativní. Pacientka nadále užívá venetoklax 400 mg/den s cílem dokončit 12 cyklů léčby. Nepotřebuje G-CSF. V plánu je dokončení léčby venetoklaxem v březnu 2023 a poté kontrolní CT a MRI.
Závěr
Režim venetoklax + obinutuzumab nabízí vysokou účinnost v 1. linii léčby CLL s dosažením dlouhých remisí časté negativity MRN. Výhodou jeho podávání je časově omezená léčba, která je přínosem z hlediska compliance pacientů a farmakoekonomiky. Během této terapie je důležité využívat podpůrnou terapii, předcházet TLS a infekcím a v případě infekční komplikace dočasně přerušit antileukemickou léčbu.
Přehled aktuálních doporučení a hlavních směrů v terapii CLL
prim. MUDr. Martin Špaček, Ph.D., Ústav lékařské biochemie a laboratorní diagnostiky 1. LF UK a VFN v Praze
Aktuální doporučení NCCN pro léčbu CLL
Podle nových doporučení NCCN (verze 1.2023) pro léčbu CLL4 je v 1. linii u pacientů bez aberace del(17p)/TP53 (obr. 2A)
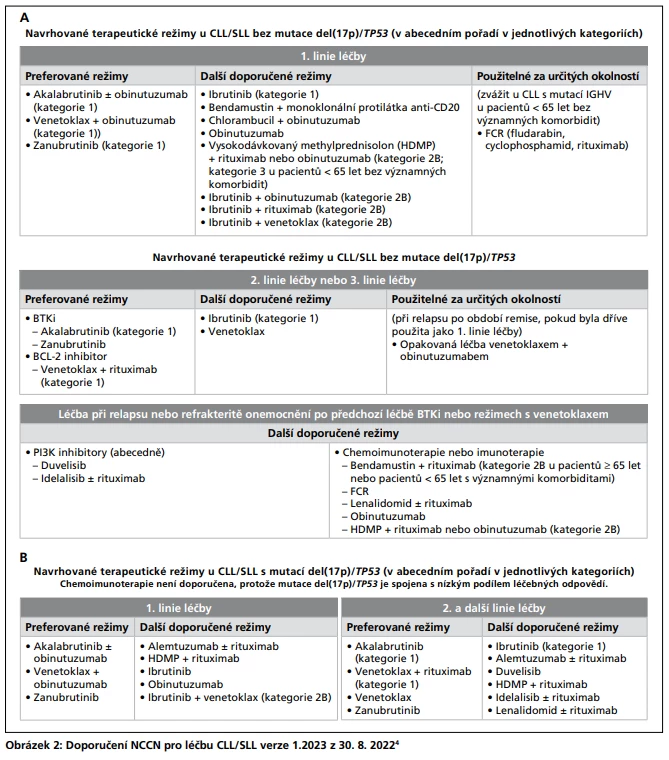
upřednostňován obinutuzumab v kombinaci s akalabrutinibem nebo s venetoklaxem, popřípadě zanubrutinib v monoterapii. Další možnosti zahrnují ibrutinib, bendamustin v kombinaci s anti-CD20 protilátkou, kombinaci chlorambucil + obinutuzumab, samotný obinutuzumab, vysokodávkovaný methylprednisolon (HDMP) + rituximab/obinutuzumab, nebo ibrutinib s obinutuzumabem, s rituximabem či s venetoklaxem.Ve 2. linii u relabujícího/refrakterního onemocnění jsou doporučeny inhibitory Brutonovy tyrosinkinázy (BTKi) akalabrutinib či zanubrutinib nebo kombinace venetoklaxu s rituximabem. Další doporučené postupy zahrnují monoterapii ibrutinibem nebo venetoklaxem.
Pro léčbu CLL v 1. linii u pacientů s aberací del(17p)/TP53 (obr. 2B) není doporučena chemoimunoterapie, protože je spojená s nízkým podílem léčebných odpovědí. Doporučen je přednostně opět obinutuzumab v kombinaci s akalabrutinibem nebo s venetoklaxem, popřípadě zanubrutinib v monoterapii. Z dalších možností doporučuje NCCN alemtuzumab + rituximab, HDMP + rituximab, ibrutinib, obinutuzumab nebo kombinaci ibrutinibu s venetoklaxem. Ve 2. linii léčby jsou pak preferovány akalabrutinib či zanubrutinib v monoterapii nebo venetoklax v kombinaci s rituximabem, případně ibrutinib či venetoklax v monoterapii. Další doporučené možnosti zahrnují duvelisib, idelalisib v monoterapii nebo s rituximabem, bendamustin s rituximabem, FCR, lenalidomid v monoterapii nebo s rituximabem, obinutuzumab a HDMP s rituximabem či obinutuzumabem.
Výsledky klinických studií s cílenou terapií u pacientů s CLL
Kombinace venetoklaxu s obinutuzumabem byla v 1. linii léčby CLL hodnocena v již popsané 12měsíční studii CLL14. Tato práce ukázala, že u pacientů s CLL s komorbiditami vede venetoklax + obinutuzumab k významně delšímu PFS než režim chlorambucil + obinutuzumab. Přínos režimu s venetoklaxem byl patrný nezávisle na přítomnosti mutace IGHV či aberace TP53.1–3
Účinnost ibrutinibu v 1. linii léčby CLL byla prokázána v registrační studii RESONATE. V roce 2022 byly publikovány výsledky analýzy 4 studií zahrnující pacienty v 1. linii léčby CLL s aberací TP53. Po 4 letech bylo naživu bez progrese 79 % těchto nemocných a po mediánu sledování 50 měsíců pokračovalo v léčbě 46 % pacientů.5
Studie ELEVATE-TN porovnávala v 1. linii léčby CLL akalabrutinib + obinutuzumab, samotný akalabrutinib a obinutuzumab + chlorambucil. Po 4 letech léčby činil podíl pacientů s přežitím bez progrese 87 % ve skupině s akalabrutinibem + obinutuzumabem a 78 % se samotným akalabrutinibem, což znamená statisticky nevýznamný rozdíl, a 25 % s režimem chlorambucil + obinutuzumab, což je statisticky významný rozdíl v porovnání s oběma dalšími hodnocenými režimy (obě p < 0,0001).6
Zanubrutinib je v 1. linii léčby CLL porovnáván s kombinací bendamustin + rituximab ve studii SEQUOIA. Již po 2 letech byl patrný významný přínos zanubrutinibu pro PFS: 85,5 vs. 69,5 % (p < 0,0001).7
Ve 2. linii léčby CLL byl hodnocen režim venetoklax + rituximab podávaný po dobu 24 měsíců v porovnání s bendamustinem + rituximabem ve studii MURANO.8, 9 Po mediánu sledování 5 let dosáhl medián PFS 53,6 % ve skupině s venetoklaxem v porovnání se 17,0 % ve skupině s bendamustinem (p < 0,0001). V této studii prodloužil režim s venetoklaxem v porovnání s režimem s bendamustinem také OS, se snížením rizika úmrtí o 60 % (p < 0,0001), přestože u 80 % pacientů byla po selhání bendamustinu s rituximabem ve 2. linii nasazena cílená terapie.8, 9 To ukazuje, že cílenou léčbu je třeba nasazovat v terapeutické strategii u CLL co nejdříve.
Akalabrutinib byl u relabující/refrakterní CLL porovnáván s ibrutinibem ve studii ELEVATE-RR. V obou terapeutických ramenech bylo dosaženo srovnatelného PFS 38,4 měsíce.10
S ibrutinibem byl ve 2. linii léčby CLL porovnáván také zanubrutinib ve studii ALPINE.11 Jak ukázaly výsledky prezentované na ASH 2022, po 2 letech bylo naživu bez progrese 79,5 % pacientů se zanubrutinibem v porovnání s 67,3 % s ibrutinibem (p = 0,0024).
Aktuální terapeutický přístup k CLL v Česku
Přístup k léčbě CLL je v Česku ovlivněn důkazy z klinických studií, stávajícími standardy péče a úhradovými kritérii.
V 1. linii léčby CLL se u pacientů s aberací TP53 používá akalabrutinib nebo ibrutinib, případně 12měsíční režim venetoklax + obinutuzumab. Méně možností je k dispozici u nemocných mladších 65 let bez komorbidit (CIRS ≤ 6), kde je hrazen pouze režim FCR (fludarabin, cyklofosfamid, rituximab). U pacientů ve věku > 65 let nebo s komorbiditami (CIRS > 6) se podává na základě výsledků studie CLL14 venetoklax + obinutuzumab po dobu 12 měsíců.
U relabující/refrakterní CLL se při aberaci TP53 podává akalabrutinib či ibrutinib, případně 24měsíční režim venetoklax + rituximab, opouštěnou možností je idelalisib + rituximab. U pacientů bez aberace TP53 se využívá 24měsíční režim venetoklax + rituximab, případně akalabrutinib či ibrutinib. Jestliže jde o pacienty po progresi na léčbě kovalentními BTKi (cBTKi), lze použít 24měsíční režim venetoklax + rituximab nebo kontinuální podávání venetoklaxu. U nemocných s intolerancí akalabrutinibu/ibrutinibu se provádí záměna za druhý BTKi nebo změna léčby na venetoklax + rituximab. Při relapsu po venetoklaxu podávaném ve fixní délce terapie se v případě časného relapsu nasazuje BTKi a v případě pozdního relapsu (> 1–2 roky) BTKi nebo venetoklax. Novou výzvu v léčbě CLL představují pacienti po selhání cBTKi a venetoklaxu. Možností je zařazení do probíhající klinické studie s nekovalentním inhibitorem BTK.
Další směřování terapie CLL
V současné době je v léčbě CLL hodnocena kombinace ibrutinib + venetoklax v řadě studií se slibnými výsledky. Probíhají také studie s novým nekovalentním BTKi pirtobrutinibem. Aktuálně je dále hodnocena léčba vedená dle dosažené negativity MRN, na jejímž základě se volí délka terapie, podávání udržovací terapie nebo strategie stop/start terapie. Zkouší se i buněčná CAR-T cell terapie a bispecifické protilátky.
Brzy očekáváme výsledky studie CAPTIVATE, která hodnotí kombinaci ibrutinib + venetoklax.12 Studie má 2 kohorty – s fixní délkou podávání a dle MRN. Pacienti v kohortě s léčbou dle dosažení negativity MRN byli po 12 měsících léčby randomizováni k dalšímu podávání ibrutinibu nebo placeba, pokud měli nedetekovatelnou MRN, a k podávání ibrutinibu nebo ibrutinibu + venetoklaxu, pokud u nich negativity MRN nebylo dosaženo. Výsledky v rameni nedetekovatelné MRN prezentované na kongresu ASH 2022 ukázaly podíl pacientů s PFS po 48 měsících léčby 95 % při pokračující léčbě ibrutinibem a 88 % při podávání placeba. 3leté přežití bez onemocnění (DFS) bylo podobné ve skupině s ibrutinibem (93 %) i s placebem (85 %; p = 0,1621). To naznačuje, že pro dosažení terapeutického efektu by měla stačit fixní délka léčby.
Závěr
Cílené léky již v léčbě CLL téměř nahradily chemoterapii. V praxi se chemoterapie využívá u CLL pouze u mladších pacientů bez komorbidit, u nichž není hrazená žádná cílená léčba. Realitou jsou již také režimy s fixní délkou léčby. Jejich nevýhodou v klinické praxi je riziko TLS, výhody naopak zahrnují menší zatížení zdravotního systému z hlediska péče i finančních nákladů a možnost života bez CLL medikace pro pacienty. V blízké budoucnosti se na základě výsledků dokončovaných probíhajících studií očekává příchod kombinace ibrutinibu s venetoklaxem a nových inhibitorů BTK do klinické praxe. Ve výhledu je také terapie vedená dle dosažení negativity MRN a možná i buněčná terapie.
Literatura:
1. Fischer K., Al-Sawaf O., Bahlo J. et al. Venetoclax and obinutuzumab in patients with CLL and coexisting conditions. N Engl J Med 2019; 380 (23): 2225–2236.
2. Al-Sawaf O., Zhang C., Robrecht S. et al. Abstract S148: Venetoclax-O for previously untreated chronic lymphocytic leukemia: 5-year results of the randomized cll14 study. EHA Congress 2022.
3. Al-Sawaf O., Zhang C., Tandon M. et al. Venetoclax plus obinutuzumab versus chlorambucil plus obinutuzumab for previously untreated chronic lymphocytic leukaemia (CLL14): follow-up results from a multicentre, open-label, randomised, phase 3 trial. Lancet Oncol 2020; 21 (9): 1188–1200.
4. Chronic Lymphocytic Leukemia/Small Lymphocytic Lymphoma. NCCN guidelines, version 1.2023. Dostupné na: www.nccn.org/guidelines/guidelines-detail?category=1&id=1478
5. Allan J. N., Shanafelt T., Wiestner A. et al. Long-term efficacy of first-line ibrutinib treatment for chronic lymphocytic leukaemia in patients with TP53 aberrations: a pooled analysis from four clinical trials. Br J Haematol 2022; 196 (4): 947–953.
6. Sharman J. P., Egyed M., Jurczak W. et al. Acalabrutinib ± obinutuzumab versus obinutuzumab + chlorambucil in treatment-naïve chronic lymphocytic leukemia: five-year follow-up of ELEVATE-TN. J Clin Oncol 2022 Jun 1; 40 (16_suppl.): 7539–7539.
7. Tam C. S., Brown J. R., Kahl B. S. et al. Zanubrutinib versus bendamustine and rituximab in untreated chronic lymphocytic leukaemia and small lymphocytic lymphoma (SEQUOIA): a randomised, controlled, phase 3 trial. Lancet Oncol. 2022 Aug; 23 (8): 1031–1043.
8. Kater A. P., Wu J. Q., Kipps T. et al. Venetoclax plus rituximab in relapsed chronic lymphocytic leukemia: 4-year results and evaluation of impact of genomic complexity and gene mutations from the MURANO phase III study. J Clin Oncol 2020; 38 (34): 4042–4054.
9. Kater A. P., Kipps T. J., Eichhorst B. F. et al. Oral presentation 125: Five-year analysis of MURANO study demonstrates enduring undetectable minimal residual disease (UMRD) in a subset of relapsed/refractory chronic lymphocytic leukemia (R/R CLL) patients following fixed-duration venetoclax-rituximab (VenR) therapy. ASH Congress 2020.
10. Byrd J. C., Hillmen P., Ghia P. et al. First results of a head-to-head trial of acalabrutinib versus ibrutinib in previously treated chronic lymphocytic leukemia. J Clin Oncol 2021; 39 (15_suppl.): 7500–7500.
11. Brown J. R., Eichhorst B., Hillmen P. et al. Zanubrutinib demonstrates superior progression-free survival (PFS) compared with ibrutinib for treatment of relapsed/refractory chronic lymphocytic leukemia and small lymphocytic lymphoma (R/R CLL/SLL): results from final analysis of ALPINE randomized phase 3 study. Blood 2022; 140 (Suppl. 2): LBA-6.
12. Allan J. N., Siddiqi T., Kipps T. J. et al. Treatment outcomes after undetectable MRD with first-line ibrutinib (Ibr) plus venetoclax (Ven): fixed duration treatment (placebo) versus continued Ibr with up to 5 years median follow-up in the CAPTIVATE study. Blood 2022; 140 (Suppl. 1): 224–227.Převzato z časopisu Aktuální témata v onkologii očima českých lékařů 2023; 8 (1), se souhlasem vydavatele a autorů.
Líbil se Vám článek? Rádi byste se k němu vyjádřili? Napište nám − Vaše názory a postřehy nás zajímají. Zveřejňovat je nebudeme, ale rádi Vám na ně odpovíme.
Štítky
Hematologie a transfuzní lékařství
Přihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




