-
Medical journals
- Career
Ileální neovezika a její varianty
: G. Gakis; A. Stenzl
: Department of Urology Eberhard-Karls University Tuebingen
: Urol List 2011; 9(3): 27-33
Náhrada močového měchýře pomocí ortotopického rezervoáru představuje významný pokrok ve vývoji technik derivace moči a v současné době je považována za derivační techniku volby u většiny pacientů (obou pohlaví) podstupujících cystektomii, se kterou bychom měli srovnávat ostatní typy derivace. Před výkonem je nutné pacientovi podrobně vysvětlit všechny dostupné techniky derivace moči a potenciální krátkodobá i dlouhodobá rizika a benefity s nimi spojené. Vzhledem k možnému riziku uretrální recidivy závisí rozhodnutí o vytvoření neoveziky na výsledku histologického vyšetření vzorku biopsie „nazmrzlo" z okraje distální části uretry (odebraného během výkonu). Princip konstrukce neoveziky spočívá v detubulizaci a složení materiálu, čímž se vytvoří nízkotlaký rezervoár. Pro tyto účely byly zkoumány nejrůznější části tenkého i tlustého střeva a žaludku. Většina publikací se shoduje na tom, že nejlepší anatomické a funkční vlastnosti nabízí terminální část ilea. Vzhledem k nedostatečnému počtu prospektivních randomizovaných studií stále existují rozpory, která technika konstrukce neoveziky je nejvhodnější a která metoda je nej-lepší pro prevenci refluxu (v případě, že je detubulizovaný střevní segment do sférického tvaru o vhodné velikosti). V současné době dostupné údaje dokazují, že náhrada močového měchýře pomocí ortotopické neoveziky představuje u většiny pacientů (obou pohlaví) podstupujících cystektomii derivační techniku volby.
Klíčová slova:
antirefluxní, derivace, ileum, nízkotlaký rezervoár, ortotopická neovezikaZkušenosti s užíváním ileální neoveziky se datují až do roku 1893, kdy Rosenberg jako první vyzkoušel vložení segmentu ilea mezi močovody a močovou trubici. Camey a Le Duc v roce 1979 popisují první klinickou zkušenost se substitucí ortotopické neoveziky [1]. U pacientů (mužského pohlaví), kteří podstoupili cystektomii, byla vytvořena anastomóza mezi ileálním rezervoárem a intaktní močovou trubicí. Nevýhodou prvních pokusů s užitím tubulizovaného segmentu ilea bylo vytvoření rezervoáru o malém objemu a vysokém intraluminálním tlaku a poškození ledviny na aborální straně v důsledku peristaltiky.
Ortotopická neovezika vytvořená pomocí moderních technik se téměř blíží (jak s ohledem na funkci, tak i lokalizaci) přirozenému močovému měchýři a lze ji považovat za „přirozené rozšíření“ kontinentní kutánní derivace. Ortotopická rekonstrukce dolních cest močových představuje dnes ve velkých centrech nej-častější typ močové derivace [2].
Močení je vyvoláno pomocí Valsalvova manévru, peristaltiky a současné relaxace svaloviny pánevního dna. Tato technika vyžaduje funkční rabdosfinkter, který je nutné během preparace zachovat [3]. Až do počátku 90. let minulého století byla ortotopická rekonstrukce dolních cest močových u žen kontraindikována. Hlavním důvodem byla skutečnost, že v této době byla během radikální operace pánve odstraněna celá močová trubice (tento postup byl považován za nezbytný pro dosažení adekvátní kontroly karcinomu) a předpokládalo se, že zbývající rabdo-sfinkter nemůže zajistit dostatečnou močovou kontinenci [4].
Na základě nejnovějších údajů prokazujících onkologickou bezpečnost a technickou proveditelnost konstrukce neoveziky u žen [5,6] a studií zkoumajících anatomii ženského rabdosfinkteru [7] lze v současné době doporučit konstrukci ortotopické neoveziky jako techniku volby pro močovou derivaci u pacientů obou pohlaví.
PRINCIPY ORTOTOPICKÉ DERIVACE MOČI
Základní pravidla
Základní principy konstrukce kontinentního močového rezervoáru zahrnují konfiguraci, akomodaci a komplianci materiálu [8]. Podle Laplaceova zákona je tlak (P) rezervoáru definován jako P = T × 2D / R, kde T představuje povrchové napětí stěny, D tloušťku stěny a R poloměr [9]. Intraluminální tlak je tedy nepřímo úměrný poloměru rezervoáru (sférického tvaru). Tubulizovaný segment o malém poloměru dosáhne již při nízkém objemu vysokého intraluminálního tlaku, jenž poškozuje ledvinu. Sférický rezervoár si však díky většímu poloměru udrží největší kapacitu při nejnižším tlaku. Vzhledem k detubulizaci a přehnutí ilea [10] má i tvar významnou roli pro vytvoření skutečně sférického tvaru, protože umožní snížit vnitřní tlak během plnění na fyziologickou kapacitu [8].
Kterou část střeva je vhodné využít pro konstrukci ileální neoveziky?
Řada studií se zabývá otázkou, která část střeva nabízí ideální materiál pro vytvoření ortotopické neoveziky. Jedním z hlavních principů ortotopické derivace moči je zajistit jímání moči při co nejnižším tlaku, abychom předešli vzniku refluxu a inkontinence. Pro tyto účely byly zkoumány nejrůznější části tenkého i tlustého střeva a žaludku.
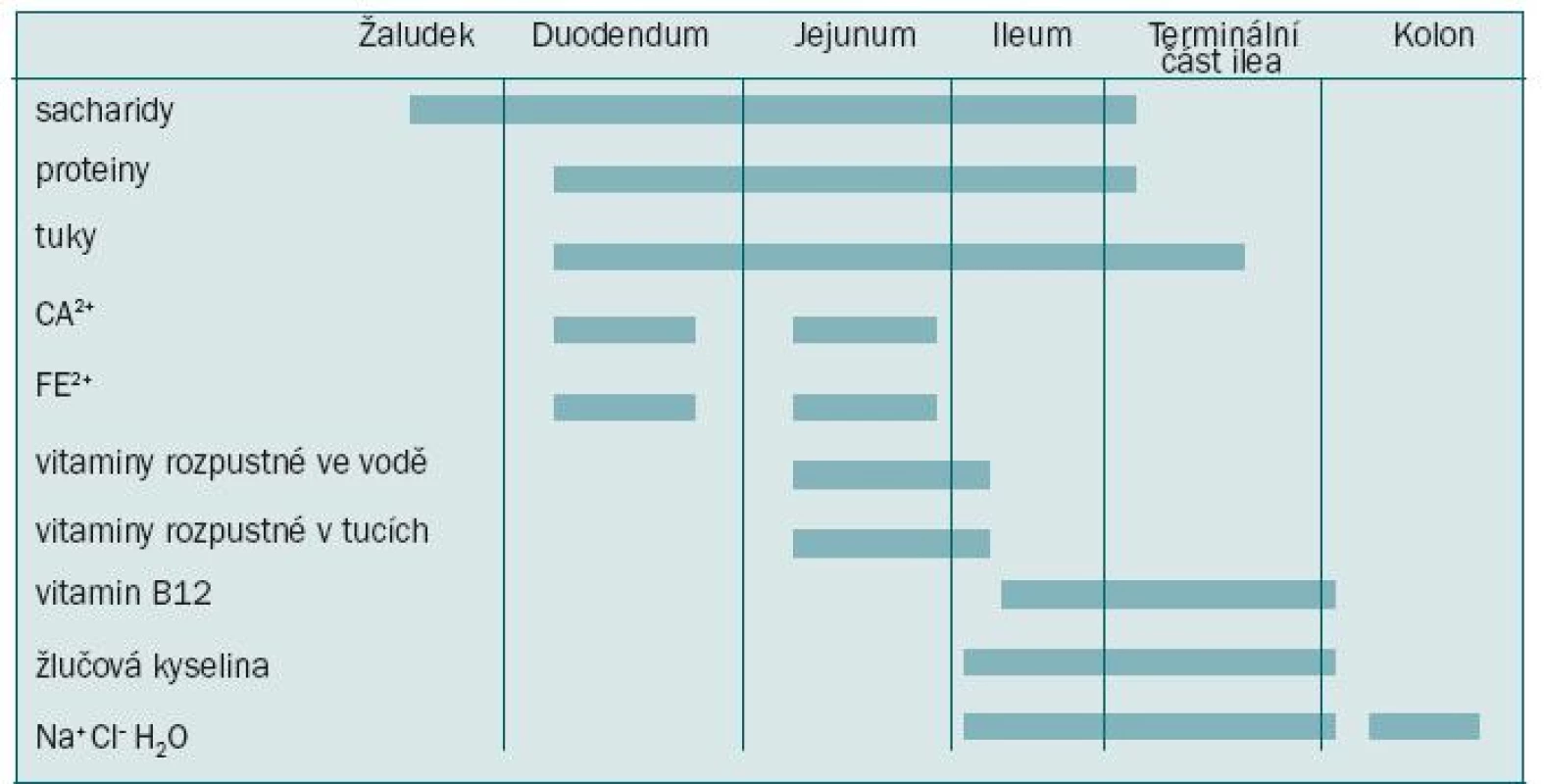
Neovezika vytvořená z tlustého střeva má menší complianci než neovezika vytvořená z ileálního segmentu. Při užití tohoto materiálu je navíc moč jímána při vyšším tlaku. Schrier et al při srovnání rezervoáru vytvořeného ze sigmoidea a ilea (pomocí urodynamického vyšetření) zjistili, že ileum vykazuje lepší vlastnosti: větší kapacitu, nižší tlak plnění i lepší complianci [11]. Na psím modelu in vivo bylo prokázáno, že cirkulární vrstva ilea umožňuje větší distenzi než cirkulární vrstva céka i podélná vrstva ilea [12]. Podélná vrstva kolon je naopak neroztažitelná. Dalším významným aspektem užívání ileálního segmentu při tvorbě kontinentního rezervoáru je vznik atrofie sliznice snižující reabsorpci iontů vodíku a chloru, což je pravděpodobnější při užití ileálního segmentu než při užití segmentu kolon [13]. Metabolické důsledky sekrece ze střevní stěny a následné reabsorpce moči z neoveziky (ze střevního segmentu) lze nejlépe kompenzovat v koncové části ilea (ve srovnání s proximální částí ilea nebo jejuna). Tyto údaje tedy jasně ukazují, že koncová část ilea představuje nejvhodnější materiál pro vytvoření ortotopické neoveziky [14].
U dětské populace se doporučuje užívat segment ze žaludku. Své zkušenosti s gastrocystoplastikou popisují Nguyen et al [15]. Segment ze žaludku ve skutečnosti poskytuje v některých klinických situacích určité výhody. Vylučování iontů vodíku a chloru přináší benefit u pacientů s narušenou renální funkcí, ale rovněž snižuje riziko vzniku recidivující infekce močových cest a tvorby hlenu. Tento materiál rovněž usnadňuje provedení antirefluxní ureterální anastomózy, neboť žaludeční stěna je mnohem silnější než ostatní části střeva. U pacientů, u nichž byl pro vytvoření neoveziky užit segment ze žaludku, však může dojít ke vzniku výkyvů elektrolytu, jako je např. hypochloremická alkalóza [16]. Lin et al publikovali v roce 2000 dlouhodobé výsledky osmi pacientů (na základě urodynamického vyšetření), kteří podstoupili konstrukci neoveziky ze žaludečního segmentu. Autoři uvádí významně menší kapacitu rezervoáru a vyšší míru výskytu inkontinence [17]. U těchto pacientů byla rovněž zaznamenána hematurie a dysurie jako důsledek podráždění močové trubice zvýšenou kyselostí moči. Tyto komplikace však lze účinně řešit pomocí blokátorů iontů H2 nebo protonové pumpy. Při kombinaci obou materiálů (střevního a žaludečního segmentu) lze pravděpodobně u vybrané populace pacientů některé z výše popisovaných komplikací eliminovat [18].
KRITÉRIA PRO VÝBĚR PACIENTŮ
U pacientů podstupujících radikální cystektomii se konstrukce ortotopické neoveziky obecně doporučuje jako technika volby derivace moči. Před výkonem je však nutné pacientovi podrobně vysvětlit všechny dostupné derivační techniky a potenciální krátkodobá a dlouhodobá rizika a benefity s nimi spojené. Dále je pacientovi nutné vysvětlit, že rozhodnutí, zda provádět substituci neoveziky, závisí na histologickém vyšetření vzorku z distální části močové trubice odebraném pomocí biopsie „nazmrzlo“ během výkonu [19].
Vzhledem k tomu, že histologické vyšetření umožňuje velmi přesně detekovat maligní uroteliální okraje (při radikální cystektomii) [20,21], mají pacienti s pozitivními okraji vysoké riziko recidivy, a nejsou tedy vhodnými kandidáty pro ortotopickou derivaci [19]. U všech pacientů by měl zkušený lékař nebo sestra před výkonem označit místo pro vytvoření kožního stomatu a pacienta instruovat, jak v případě retence moči katetrizovat neoveziku.
Vyšší věk nemusí nutně představovat kontraindikaci pro substituci neoveziky. Navzdory tomu, že nejnovější údaje prokazují statisticky vyšší míru kontinence u pacientů mladších 70 let, poskytuje několik studií dostatečné důkazy, že s přihlédnutím k individuálním okolnostem je indikace ortotopické derivace bezpečná i u pacientů po osmdesátce. U této populace pacientů je nutné jako hlavní kritérium pro indikaci ortotopické neoveziky uvážit rozdíl mezi kalendářním a biologickým věkem [22,23].
V důsledku zvyšující se úrovně materiálního zabezpečení a ekonomické prosperity západních zemí neustále narůstá prevalence obézních pacientů, kteří musí podstoupit cystektomii a derivaci moči [24]. Obézní pacient může být vhodným kandidátem pro ortotopickou substituci i abdominální kontinentní/inkontinentní derivaci moči. Potenciální komplikace kutánní inkontinentní i kontinentní derivace u obézních pacientů zahrnují každodenní manuální aplikaci urostomie, provádění selfkatetrizace kontinentního rezervoáru skrze silnou břišní stěnu a objemné úpony mezenteria omezující mobilitu a schopnost manipulace s rezervoárem [25].
Očekávaná délka života pacienta hraje významnou roli při zvažování ortotopické derivace. Primární cíl radikální cystektomie by měl v každém případě spočívat v kontrole karcinomu. Extravezikální rozšíření onemocnění ani pozitivní lymfatické uzliny však nemusí nutně představovat kontraindikaci pro vytvoření ileální neoveziky [26]. Několik studií prokázalo, že riziko uretrální recidivy u těchto pacientů je velmi nízké – v rozmezí 1,1–2,5 % [20,27]. Konstrukce neoveziky je absolutně kontra-indikována u pacientů s tumorem loka-lizovaným na okraji močové trubice (vzhledem k vysokému riziku recidivy tumoru). Navíc vzhledem k náročnému nácviku a rehabilitaci, která může zabrat velký objem času, může být u některých starších pacientů vhodnější volbou jednodušší typ derivace moči. Během předoperačního vyšetření je nutné odhalit všechny fyzické i mentální poruchy, které by mohly být překážkou v provádění selfkatetrizace neoveziky (v případě nutnosti) vzhledem k tomu, že některé studie uvádí, že pět let po ortotopické derivaci vyžaduje čistou intermitentní katetrizaci přibližně 4–10 % mužů a 15–40 % žen [23,28,29].
Zásadním kritériem pro konstrukci ileální neoveziky je pacientova renální funkce. Reabsorpce kyseliny chlorovodíkové skrze ileální segment způsobuje metabolické poruchy, jako je např. hyperchloremická acidóza, v důsledku čehož dochází ke zhoršení renální funkce. Před výkonem je tedy nutné pečlivě vyšetřit renální funkci pacienta a vyloučit případné zhoršení funkce ledviny v důsledku obstrukce ureteru způsobené tumorem. V případě postrenální obstrukce lze renální funkci lépe posoudit provedením desobstrukce horních cest močových zavedením perkutánní nefrostomie nebo ureterálního stentu. Minimální hodnota clearance kreatininu je 60 ml/min [30]. U pacientů s narušenou renální funkcí může být vhodnější vytvoření neoveziky ze žaludečního segmentu [11].
JAK PŘIPOJIT MOČOVODY K ILEÁLNÍ NEOVEZICE?
Obecné informace
Dosud byly popsány nejrůznější techniky implantace močovodu s vytvořením chlopně i bez ní (valvulární/nonvalvulární). Na rozdíl od kontinentních kožních rezervoárů a ureterosigmoidostomie (vysokotlaké nesterilní systémy vyžadující valvulární antirefluxní implantaci močovodů z důvodu ochrany horních cest močových) panují v případě nízkotlakých ortotopických rezervoárů dosud protichůdné názory s ohledem na nejvhodnější typ antirefluxního mechanizmu.
1. Kombinovaná neovezika (vytvořená z různých segmentů). 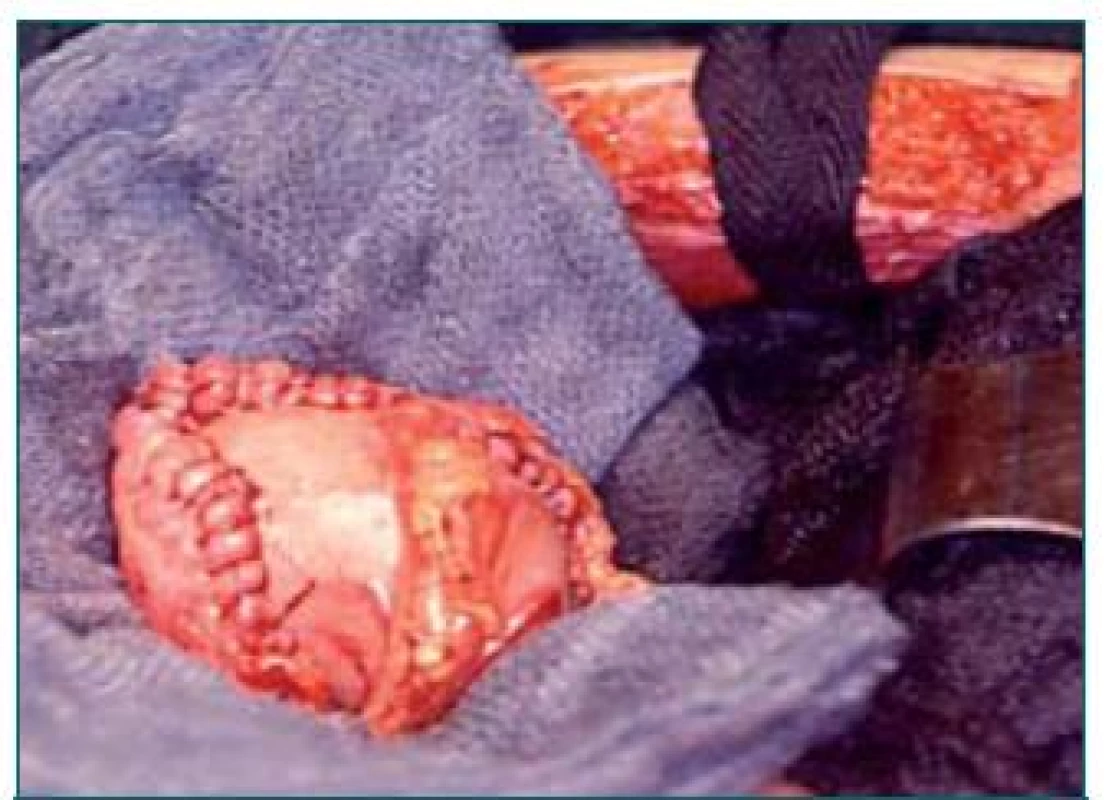
Argumenty pro podporu vytvoření valvulárního antirefluxního mechanizmu u ortotopické neoveziky zahrnují vysokou incidenci bakterií v ileálním rezervoáru [31] a potřebu valvulární antirefluxní ochrany horních cest močových u pacientů s neomočovým měchýřem. Vzhledem k tomu, že z dlouhodobého hlediska mají pacienti s neovezikou vysoké riziko, že budou vyžadovat intermitentní katetrizaci [23,29,32], která podporuje osazování neoveziky bakteriemi, může být určitá forma antirefluxního mechanizmu nezbytná. Ačkoli je neovezika vytvořená z ileálního segmentu považována za nízkotlaký rezervoár, urodynamické vyšetření u pacientů s ileální neovezikou podle Kocka prokázalo, že během jímání moči je intraluminální tlak skutečně nízký (průměr: přibližně 33 cm vodního sloupce), ovšem při močení se může signifikantně zvyšovat (až na 77–150 cm vodního sloupce) [33].
Bylo prokázáno, že poškození horních cest močových se nemusí během 10–20 let po vytvoření neoveziky vůbec projevit. K této komplikaci může dojít i v případě, že radiografické vyšetření prokáže absenci obstrukce v horních cestách močových. Řada valvulárních antirefluxních metod je navíc technicky poměrně náročná a je spojena s výskytem závažných komplikací jako např. ureteroenterická striktura nebo stenóza papily anastomózy, jež vedou k poškození horních cest močových (u přibližně 3–10 % pacientů) [22,28,34]. Užití nonvalvulárního aferentního isoperistaltického ileálního segmentu o délce minimálně 20 cm, jak popisují Studer et al, zabraňuje vzniku refluxu prostřednictvím přenosu intraabdominálního tlaku na aferetní ileální segment během Valsalvova manévru [35].
V současné době probíhá randomizovaná prospektivní studie srovnávající funkční výsledky implantace ileálního rezervoáru podle Studera a implantace T-pouche, výsledky budou publikovány v několika následujících letech [36].
Můžeme tedy říci, že v současné době neexistují žádné přesvědčivé důkazy, které by jasně prokazovaly, zda poskytuje lepší dlouhodobou ochranu horních cest močových rezervoár vytvořený pomocí nonvalvulárního isoperistaltického ileálního segmentu nebo valvulární (např. subserózní, papilární) implantace ureteru [2]. V další části uvádíme stručný přehled nejrůznějších valvulárních a nevalvulárních technik implantace močovodu.
Le Ducova technika
Jednu z prvních valvulárních technik implantace popisuje Le Duc. Tato technika spočívala ve vytvoření ileální pochvy, do níž byl následně implantován močovod a zaveden do lumen rezervoáru skrze transmurální nerefluxní kanál a ponechán bez fixace intraluminálně. Modifikace této techniky spočívá v široké spatulaci distálního konce močovodu, čímž je vytvořena ureterální ploténka, která je přímo adaptována ke sliznici ilea [1,37].
Implantace močovodu s vytvořením papily („nipple“)
Další antirefluxní implantační technikou je implantace močovodu s vytvořením papily a nastřihnutím manžety, jak popisují Sagalowsky et al. Močovod je spatulován přibližně 1 cm a přehnut tak, abychom vytvořili papilu z přehnuté manžety. Rohy sešijeme a ponecháme pouze malou mezeru na proximální straně, abychom zabránili vzniku konstrikce [38].
Ileální chlopeň podle Kocka
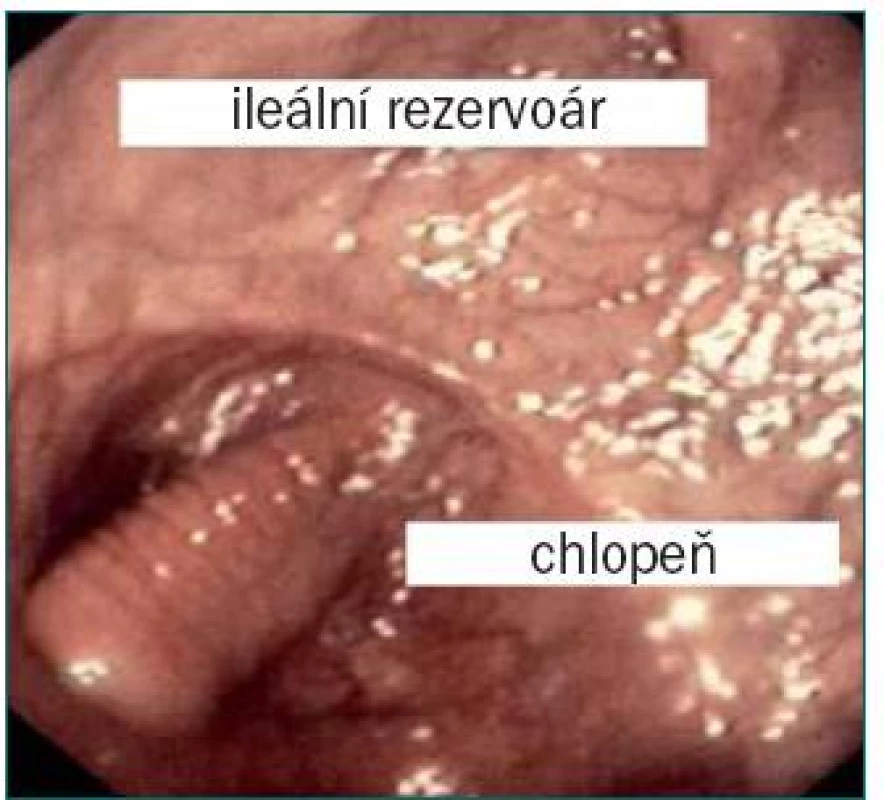
Při antirefluxní technice podle Kocka se užívá segment ilea jako antirefluxní mechanizmus k intususcepci ileální chlopně [39]. Chlopeň je připevněna pomocí čtyř řad svorek uvnitř chlopně a na zadní straně mimo rezervoár (viz dále).
Zúžený ileální segment (T-pouch)
Stein et al popisují alternativní techniku s užitím zúženého subserózního ileálního segmentu, který umožní prodloužit spojení močovodů (viz dále) [28].
Extramurální tunel krytý serózou
Snazší formou antirefluxního mechanizmu je umístění močovodů přímo do extramurálního tunelu krytého serózou (viz dále) [26].
Nevalvulární isoperistaltický ileální segment („Studerova technika“)
Při nevalvulární antirefluxní technice se užívá aferentní izoperistaltický ileální segment o délce alespoň 20 cm, který slouží jako kanál pro antegrádní transport moči (viz dále) [35,40].
TECHNIKY ILEÁLNÍ ORTOTOPICKÉ SUBSTITUCE
Dosud byly popsány nejrůznější techniky konstrukce ileální neoveziky s užitím různých střevních segmentů a různých přístupů napojení rezervoáru a ochrany horních cest močových [1,22,26,28,32, 35,36,39]. Následující přehled se zaměřuje na techniky, u nichž máme k dispozici výsledky dlouhodobého sledování a které byly zkoumány ve studiích zahrnujících dostatečný počet pacientů. Funkční dlouhodobé výsledky všech technik derivace jsou uvedeny v tab. 1.
1. Funkční dlouhodobé výsledky nejčastějších technik konstrukce ileální neoveziky. 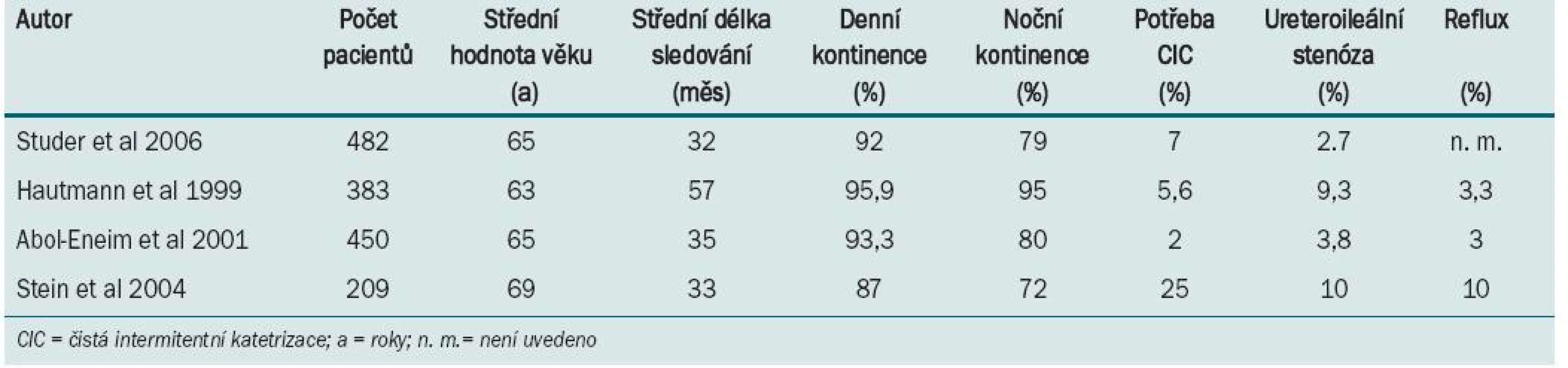
Ortotopická substituce s vytvořením rezervoáru ve tvaru U („Goodwinovo pravidlo“)
Studerova ileální neovezika
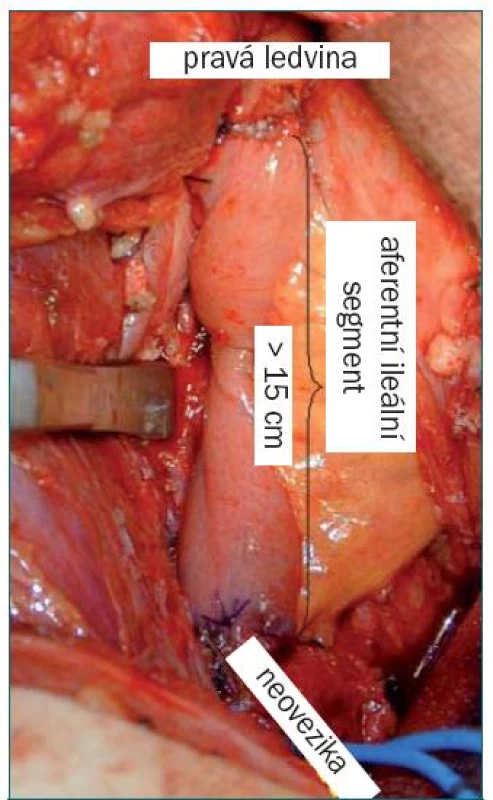
Při konstrukci neoveziky podle Studera se užívá segment z koncové části ilea o délce 60–65 cm, který je vypreparován při-bližně 20–25 cm proximálně od ileocekální chlopně. Po obnovení kontinuity střeva a uzavření otvorů v mezenteriu je distálních 40–45 cm segmentu otevřeno na antimezenteriální straně a slouží jako rezervoár, zatímco proximálních 20–25 cm ileálního segmentu zůstává intaktní a je využito pro implantaci močovodu a prevenci refluxu díky peristaltickým vlnám (obr. 4). Následně je vytvořena posteriorní ploténka rezervoáru ve tvaru písmene U spojením mediálních ramen pomocí pokračovací sutury. Proximální konec aferentního intaktního segmentu je uzavřen a po spatulaci močovodů a zavedení stentů je provedena ureterointestinální anastomóza (zvlášť pro oba močovody) pomocí techniky end-to-side na proximálním konci („Nesbitova technika“). Před kompletním uzavřením laterálních okrajů rezervoáru je vytvořen samostatný otvor v bodě lokalizovaném nejvíce kaudálně a je vytvořena uretroileální anastomóza. Následně je rezervoár kompletně uzavřen [40]. Tento typ derivace představuje v současné době jednu z nejoblíbenějších forem ortotopické derivace.
Ortotopická ileální neovezika podle Kocka
Ileální rezervoár podle Kocka byl poprvé užit jako kontinentní kožní rezervoár se dvěma vloženými chlopněmi papilárního typu, které sloužily jako antirefluxní mechanizmus a mechanizmus pro zajištění kontinence. Později se z této techniky vyvinula ortotopická substituce, která spočívala v připojení aferentních intususceptovaných ramen k močovodům s cílem zabránit vzniku refluxu do horních cest močových. Po incizi na antimezenteriální straně je ileální segment o délce přibližně 22 cm užit k vytvoření rezervoáru (ve tvaru písmene U), zatímco segment o délce 17 cm byl užit pro intususcepci ileální chlopně (o délce 5–7 cm). Chlopeň je připevněna pomocí čtyř řad svorek k listům chlopně a k zadní stěně mimo rezervoár [39]. Vzhledem k technické náročnosti vytvoření trvalého a účinného antirefluxního systému, riziku vzniku konkrementu na odhalené svorce a vzniku stenózy (v důsledku narušené vaskularizace chlopně) vyvíjí řada operatérů nové formy antirefluxních mechanizmů jako např. extramurální tunel krytý serózou a tzv. T-pouch [26,28].
Ileální neovezika – T-pouch
Jako jednu z alternativ popisuje Stein v roce 1998 vytvoření neoveziky T-pouche, který má stejný sférický tvar jako Kockova ileální neovezika, jediným rozdílem je užití aferentního ileálního segmentu místo intususceptované ileální chlopně v rámci antirefluxního systému (tzv. T-limb). Pro zajištění adekvátní vaskularizace 3–4cm segmentu distální části aferentního ileálního segmentu (jenž tvoří antirefluxní mechanizmus) jsou vytvořeny otvory v mezenteriu (tzv. „Windows of Deaver“) a do každého z nich je zaveden drén. Následně je těmito otvory zavedeno několik řad sutur, pomocí nichž připevníme aferentní ileální segment k seróze dvou 22cm kraniálních ileálních segmentů rezervoáru. Aferentní rameno je zúženo a dva ileální segmenty jsou otevřeny podél mezenteria od kónického zakončení směrem nahoru k ústí aferentního segmentu. Následně je provedena incize laterálně k antimezenteriálnímu okraji a je vedena směrem nahoru. Tím vytvoříme dva ileální laloky, které umístíme na aferentní ileální segment, čímž vytvoříme antirefluxní mechanizmus [28].
VIP („vesica ileale Padovana“)
Segment z koncové části ilea o délce 40 cm je otevřen na antimezenteriálním okraji a nakonfigurován do sférického tvaru. Pomocí dvou pokračovacích sutur vytvoříme dolní nálevku na anteriorní/ /posteriorní straně o délce přibližně 5 cm, což nám usnadní provedení uretroileální anastomózy. Následně je proximální smyčka složena ve tvaru obráceného písmene S a vnitřní protilehlé okraje jsou sešity tak, že vytvoří ileální pohárek.
Uretery jsou implantovány skrze dva intestinální kanálky kryté serózou, jak popisují Abol-Eneim et al [26]. Uzavření rezervoáru zakončíme na anteriorním aspektu přehnutím horního okraje ileálního pohárku směrem dolů, čímž vytvoříme sférický rezervoár [41].
Implantace se spojením močovodů subserózně do zkřížené složeného I-Pouch
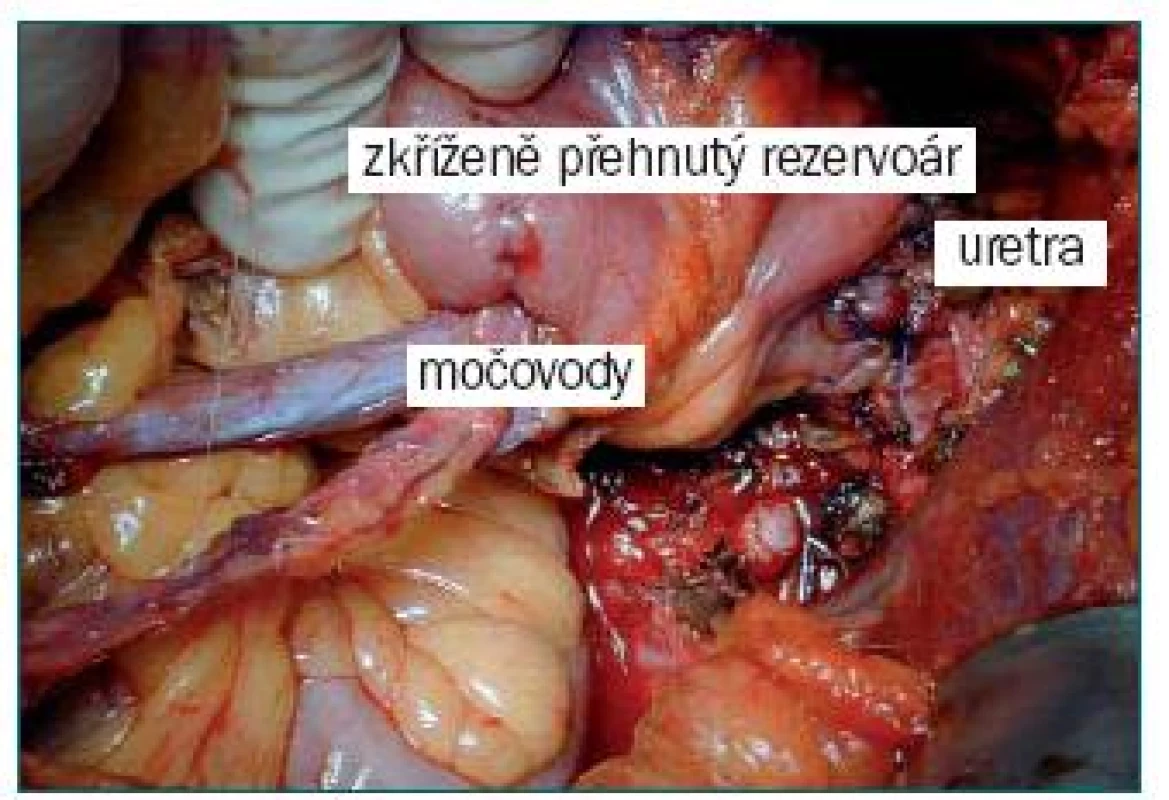
Při této technice se užívá pouze přibližně 40cm segment z koncové části ilea. Ve své podstatě je vytvořen Goodwinův rezervoár s ileální ploténkou ve tvaru písmene U (každé rameno má délku 20 cm), který je následně zkříženě složen. Spatulované a spojené močovody („Wallaceova technika“) jsou umístěny do subserózního kanálu (o délce přibližně 8 cm) v horním konci ileální ploténky ve tvaru písmena U. Neovezika má stejnou konfiguraci jako Studerův rezervoár, Hemi-Kockův rezervoár nebo T-pouch. Rezervoár je připevněn k pahýlu uretry buď pomocí samostatného otvoru (u žen), nebo ponecháním malého otvoru v linii sutury uzavírající zkřížené přehnutí (muži). Rozdíl spočívá v kratší délce ilea (pouze 40 cm) a v umístění implantovaných ureterů na dorzální stěnu rezervoáru (obr. 5), což usnadní instrumentaci horních cest močových, pokud je později potřebná [42]. Termín I-pouch vychází ze skutečnosti, že na rozdíl od T-pouch jsou oba spojené močovody implantovány přímo k rezervoáru ve vertikální linii.
Konfigurace ileálního segmentu do tvaru písmena W nebo M
Ileální neovezika podle Hautmanna
Ileální neovezika podle Hautmanna je sférický rezervoár ve tvaru písmena W, pro jehož vytvoření se užívá segment z distální části ilea o délce přibližně 70 cm. Cílem je zlepšit noční kontinenci díky velké kapacitě. Celý segment je otevřen na antimezenteriální straně s výjimkou 5cm laloku, pomocí něhož lze nejsnáze dosáhnout močové trubice v místě, kde je provedena incize ve směru anteriorního okraje mezenteria ve tvaru U. Čtyři ramena detubulizovaného střeva jsou uzavřeny pomocí pokračovací sutury. Po vytvoření otvoru ve zmiňovaném ileálním segmentu ve tvaru písmena U je provedena uretrointestinální anastomóza z vnitřní strany neoveziky. Následně jsou močovody implantovány refluxním způsobem a anteriorní stěna je uzavřena [43]. S ohledem na délku ileálního segmentu (pro vytvoření rezervoáru o velké kapacitě pro zlepšení noční inkontinence) je třeba zdůraznit, že tento typ derivace moči je spojen s vyšší incidencí metabolických poruch.
Rezervoár ve tvaru písmena W s vytvořením serózního extramurálního tunelu
Abol-Enein a Ghoneim popsali v roce 2001 techniku vytvoření ileální neoveziky kryté serózou ve tvaru písmena W. Tato technika představuje účinnou metodu prevence refluxu. 60cm segment ilea je otevřen na antimezenteriálním okraji. Mediální ra-mena jsou uzavřena pomocí pokračovací sutury, zatímco dva laterální laloky jsou spojeny pomocí seromuskulární pokračovací sutury, čímž vytvoříme dva serózní intestinální kanály. Do spatulovaných močovodů jsou zavedeny stenty, které jsou pomocí anastomózy připevněny ke sliznici střeva. Následně je tunel uzavřen přes močovody, čímž vytvoříme antirefluxní mechanizmus. Anteriorní stěna je uzavřena pomocí pokračovací sutury side-to-side a rezervoár je pomocí anastomózy připevněn (po otevření bodu lokalizovaného nejvíce kaudálně) k močové trubici. Abol--Enein a Ghoneim uvádí, že tato implantační technika poskytuje několik výhod: močovody jsou chráněny před stykem s močí, což zlepšuje hojení rány a snižuje riziko vzniku zjizvení. Při této technice rovněž není nutné preparovat dlouhý segment ilea pro vytvoření antirefluxního mechanizmu (jako např. u T-pouche) [28], díky čemuž je celá technika snazší [44].
RIZIKA A VÝSLEDKY KONSTRUKCE ORTOTOPICKÉ NEOVEZIKY U PACIENTŮ S KARCINOMEM
Rekonstrukce neoveziky představuje časově i technicky velmi náročnou techniku, která však pacientovi zajistí výhody v podobě vyššího sebevědomí, lepší sexuální funkce a kontinence [45]. Hautmann et al hodnotí, zda ochota na straně chirurga nabízet pacientovi tuto modalitu a zájem na straně pacienta rekonstrukci neoveziky podstoupit mohou vést k časnější indikaci cystektomie a zlepšení výsledků (souvisejících s karcinomem) [46]. Nejnovější studie totiž nasvědčují tomu, že oddálení radikální cystektomie o tři měsíce může vést ke snížení doby přežití specifické pro karcinom [47]. Hautmann et al zjistili, že průměrný interval mezi prvním diagnostikováním onemocnění a provedením cystektomie byl významně delší u pacientů, u nichž byl vytvořen ileální konduit, než u pacientů, kteří podstoupili konstrukci neoveziky. U pacientů s ileálním konduitem byla rovněž zaznamenána významně nižší míra přežití po pět let (přizpůsobeno všem stadiím karcinomu), což jasně ukazuje, že možnost konstrukce neoveziky může snižovat neochotu lékaře indikovat radikální cystektomii a neochotu pacienta ji podstoupit [46]. Existují důkazy, že konstrukce neoveziky u žen, které tuto techniku podstoupily v důsledku maligního onemocnění, nezhoršuje onkologické výsledky, pakliže jsou dodržována předem stanovená pravidla týkající se anatomických i funkčních patologických postupů [6,48].
Porter et al provedli přehled cel-kem 378 studií, v němž hodnotí obtíže při interpretaci výsledků a vyvozování smysluplných závěrů ze studií týkajících se kvality života. Do analýzy bylo zařazeno pouze 15 z celkových 378 studií, které splňovaly následující kritéria stanovená autory: dospělý pacient, karcinom močového měchýře, komparativní studie, původní výzkum, primární výsledný parametr týkající se kvality života, užívání validovaných instrumentů pro hodnocení kvality života. Žádná z 15 analyzovaných studií neužívala randomizaci. Jediná studie měla prospektivní design. Pouze dvě třetiny studií užívaly validované instrumenty pro hodnocení kvality života a jen 73 % studií instrumenty navržené speciálně pro hodnocení karcinomu močového měchýře. Autoři tedy dospěli k závěru, že v současné době dostupné důkazy (týkající se hodnocení kvality života) neumožňují vyvodit jakékoli smysluplné závěry s ohledem na ideální typ derivace moči.
ZÁVĚR
V současné době dostupné údaje prokazují, že substituce močového měchýře pomocí ortotopické neoveziky představuje derivační techniku volby u většiny pacientů (obou pohlaví) podstupujících cystektomii. Pro docílení co nejlepší compliance a optimálních funkčních výsledků je nutné s pacientem podrobně prodiskutovat všechny možnosti derivace moči a s nimi spojená krátkodobá i dlouhodobá rizika i benefity. Pro minimalizaci rizika recidivy je nutné během výkonu provést histologické vyšetření vzorku distální části močové trubice odebraného pomocí biopsie „nazmrzlo“.
Hlavní myšlenka konstrukce neoveziky spočívá v detubulizaci a složení segmentu a vytvoření nízkotlakého rezervoáru. Většina publikací se shoduje na tom, že nejlepší anatomické a funkční vlastnosti poskytuje koncová část ilea. Vzhledem k nedostatku prospektivních randomizovaných studií stále existují rozpory, která technika konstrukce neoveziky je nejvhodnější a která metoda je nejlepší pro prevenci refluxu (v případě, že je detubulizovaný střevní segment vytvarován do sférického tvaru o vhodné velikosti).
Prof. Arnulf Stenzl, MD
Department of Urology Eberhard-Karls University Tuebingen
Hoppe-Seyler Strasse 3 D-72076 Tübingen
urologie@med.uni-tuebingen.de
Sources
1. Le Duc A, Camey M. A procedure for avoiding reflux in uretero-ileal implantations during enterocystoplasty. J Urol Nephrol 1979; 85(7–8): 449–454.
2. World Health Organization (WHO) Consensus Conference in Bladder Cancer, Hautmann RE, Abol--Enein H, Hafez K, Haro I et al. Urinary diversion. Urology 2007; 69 (1 Suppl):17–49.
3. Iwakiri J, Gill H, Anderson R et al. Functional and urodynamic characteristics of an ileal neobladder. J Urol 1993; 149(5): 1072–1076.
4. Gerber WL. Is urethral sparing at cystectomy a safe procedure? Urology 1990; 36(4): 303–304.
5. Stenzl A, Draxl H, Posch B et al. The risk of urethral tumors in female bladder cancer: can the urethra be used for orthotopic reconstruction of the lower urinary tract? J Urol 1995; 153 (3 Pt 2): 950–955.
6. Stein JP, Penson DF, Lee C et al. Long-term oncological outcomes in women undergoing radical cystectomy and orthotopic diversion for bladder cancer. J Urol 2009; 181(5): 2052–2058.
7. Colleselli K, Stenzl A, Eder R et al. The female urethral sphincter: a morphological and topographical study. J Urol 1998; 160(1): 49–54.
8. Hinman F Jr. Selection of intestinal segments for bladder substitution: physical and physiological characteristics. J Urol 1988; 139(3): 519–523.
9. Basford JR. The Law of Laplace and its relevance to contemporary medicine and rehabilitation. Arch Phys Med Rehabil 2002; 83(8): 1165–1170.
10. Goodwin WE, Winter CC. Technique of sigmoidocystoplasty. Surg Gynecol Obstet 1959; 108(3): 370–372.
11. Schrier BP, Laguna MP, van der Pal F et al. Comparison of orthotopic sigmoid and ileal neobladders: continence and urodynamic parameters. Eur Urol 2005; 47(5): 679–685.
12. Hohenfellner M, Bürger R, Schad H et al. Reservoir characteristics of Mainz pouch studied in animal model. Osmolality of filling solution and effect of oxybutynin. Urology 1993; 42(6): 741–746.
13. Mills RD, Studer UE. Metabolic consequences of continent urinary diversion. J Urol 1999; 161(4): 1057–1066.
14. Stenzl A. Bladder Substitution. Curr Opin Urol 1999; 9(3): 241–245.
15. Nguyen DH, Mitchell ME. Gastric bladder reconstruction. Urol Clin North Am 1991; 18(4): 649–657.
16. Adams MC, Mitchell ME, Rink RC. Gastrocystoplasty: an alternative solution to the problem of urological reconstruction in the severely compromised patient. J Urol 1988; 140 (5 Pt 2): 1152–1156.
17. Lin DW, Santucci RA, Mayo ME et al. Urodynamic evaluation and long-term results of the orthotopic gastric neobladder in men. J Urol 2000; 164(2): 356–359.
18. Lockhart JL, Davies R, Cox C et al. The gastroileoileal pouch: an alternative continent urinary reservoir for patients with short bowel, acidosis and/or extensive pelvic radiation. J Urol 1993; 150(1): 46–50.
19. Stenzl A, Cowan NC, De Santis M et al. The updated EAU guidelines on muscle-invasive and metastatic bladder cancer. Eur Urol 2009; 55(4): 815–825.
20. Stein JP, Clark P, Miranda G et al. Urethral tumor recurrence following cystectomy and urinary diversion: clinical and pathological characteristics in 768 male patients. J Urol 2005; 173(4): 1163–1168.
21. Gakis G, Schilling D, Perner S et al. Sequential resection of malignant ureteral margins at radical cystectomy: a critical assessment of the value of frozen section analysis. World J Urol 2010; DOI 10.1007/s00345-010-0581-z.
22. Elmajian DA, Stein JP, Esrig D et al. The Kock ileal neobladder: updated experience in 295 male patients. J Urol 1996; 156(3): 920–925.
23. Steven K, Poulsen AL. The orthotopic Kock ileal neobladder: functional results, urodynamic features, complications and survival in 166 men. J Urol 2000; 164(2): 288–295.
24. Hafron J, Mitra N, Dalbagni G et al. Does body mass index affect survival of patients undergoing radical or partial cystectomy for bladder cancer? J Urol 2005; 173(5): 1513–1517.
25. Kouba E, Sands M, Lentz A et al. Incidence and risk factors of stomal complications in patients undergoing cystectomy with ileal conduit urinary diversion for bladder cancer. J Urol 2007; 178 (3 Pt 1): 950–954.
26. Abol-Enein H, Ghoneim MA. Functional results of orthotopic ileal neobladder with serous-lined extramural ureteral reimplantation: experience with 450 patients. J Urol 2001; 165(5): 1427–1432.
27. Kassouf W, Spiess PE, Brown GA et al. Prostatic urethral biopsy has limited usefulness in counseling patients regarding final urethral margin status during orthotopic neobladder reconstruction. J Urol 2008; 180(1): 164–167.
28. Stein JP, Dunn MD, Quek ML et al. The orthotopic T pouch ileal neobladder: experience with 209 patients. J Urol 2004; 172(2): 584–587.
29. Stenzl A, Jarolim L, Coloby P et al.Urethra-sparing cystectomy and orthotopic urinary diversion in women with malignant pelvic tumors. Cancer 2001; 92(7): 1864–1871.
30. Minervini A, Boni G, Salinitri G et al. Evaluation of renal function and upper urinary tract morphology in the ileal orthotopic neobladder with no antireflux mechanism. J Urol 2005; 173(1): 144–147.
31. Månsson W, Colleen S, Mårdh PA. The microbial flora of the continent cecal urinary reservoir, its stoma and the peristomal skin. J Urol 1986; 135(2): 247–250.
32. Hautmann RE, Volkmer BG, Schumacher MC et al. Long-term results of standard procedures in urology: the ileal neobladder. World J Urol 2006; 24(3): 305–314.
33. Gotoh M, Yoshikawa Y, Sahashi M et al. Urodynamic study of storage and evacuation of urine in patients with a urethral Kock pouch. J Urol 1995; 154(5): 1850–1853.
34. Stein JP, Freeman JA, Esrig D et al. Complications of the afferent antireflux valve mechanism in the Kock ileal reservoir. J Urol 1996; 155(5): 1579–1584.
35. Studer UE, Spiegel T, Casanova GA et al. Ileal bladder substitute: antireflux nipple or afferent tubular segment? Eur Urol 1991; 20(4): 315–326.
36. Skinner EC, Skinner DG. Does reflux in orthotopic diversion matter? A randomized prospective comparison of the Studer and T-pouch ileal neobladders. World J Urol 2009; 27(1): 51–55.
37. Le Duc A, Camey M, Teillac P. An original antireflux ureteroileal implantation technique: long-term follow--up. J Urol 1987; 137(6): 1156–1158.
38. Sagalowsky A. Early results with split-cuff nipple ureteral reimplants in urinary diversion. J Urol 1995; 154(6): 2028–2031.
39. Kock NG, Nilson AE, Nilsson LO et al. Urinary diversion via a continent ileal reservoir: clinical results in 12 patients. J Urol 1982; 128(3): 469–475.
40. Studer UE, Burkhard FC, Schumacher M et al. Twenty years experience with an ileal orthotopic low pressure bladder substitute--lessons to be learned. J Urol 2006; 176(1): 161–166.
41. Pagano F, Artibani W, Ligato P et al. Vescica Ileale Padovana: a technique for total bladder replacement. Eur Urol 1990; 17(2): 149–154.
42. Stenzl A, Hobisch A, Strasser H et al. Ureteroileal anastomosis in orthotopic urinary diversion: how much or how little is necessary? Tech Urol 2001; 7(3): 188–195.
43. Hautmann RE, de Petriconi R, Gottfried HW et al. The ileal neobladder: complications and functional results in 363 patients after 11 years of followup. J Urol 1999; 161(2): 422–427.
44. Pantuck AJ, Han KR, Perrotti M et al. Ureteroenteric anastomosis in continent urinary diversion: long-term results and complications of direct versus nonrefluxing techniques. J Urol 2000; 163(2): 450–455.
45. Hobisch A, Tosun K, Kinzl J et al. Life after cystectomy and orthotopic neobladder versus ileal conduit urinary diversion. Semin Urol Oncol 2001; 19(1): 18–23.
46. Hautmann RE, Paiss T. Does the option of the ileal neobladder stimulate patient and physician decision toward earlier cystectomy? J Urol 1998; 159(6): 1845–1850.
47. Chang SS, Hassan JM, Cookson MS et al. Delaying radical cystectomy for muscle invasive bladder cancer results in worse pathological stage. J Urol 2003; 170 (4 Pt 1): 1085–1087.
48. Stenzl A, Höltl L. Orthotopic bladder reconstruction in women--what we have learned over the last decade. Crit Rev Oncol Hematol 2003; 47(2): 147–154.
49. Porter MP, Penson DF. Health related quality of life after radical cystectomy and urinary diversion for bladder cancer: a systematic review and critical analysis of the literature. J Urol 2005; 173(4): 1318–1322.
Labels
Paediatric urologist Urology
Article was published inUrological Journal

2011 Issue 3-
All articles in this issue
- METHODS OF NON-INVASIVE DIAGNOSTICS AND MONITORING OF URINARY BLADDER CANCER
- THE ROLE OF SURGICAL TREATMENT OF SUPERFICIAL BLADDER TUMOUR
- INTRAVESICAL INSTILLATION THERAPY IN THE TREATMENT OF SUPERFICIAL BLADDER CARCINOMA
- ILEAL NEOBLADDER AND ITS VARIANTS
- BLADDER CANCER – LATEST CHANGES IN SURGICAL AND MEDICAL THERAPY
- CHEMOTHERAPY IN INVASIVE AND METASTATIC BLADDER CANCER
- Role of botulinum toxin in the management of multiple sclerosis lower urinary tract dysfunctions
- EAU Guidelines on non–muscle–invasive urothelial carcinoma of the bladder – the 2011 Update
- Treatment of muscle-invasive and metastatic bladder cancer – update of the EAU Guidelines
- Urological Journal
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- ILEAL NEOBLADDER AND ITS VARIANTS
- INTRAVESICAL INSTILLATION THERAPY IN THE TREATMENT OF SUPERFICIAL BLADDER CARCINOMA
- Treatment of muscle-invasive and metastatic bladder cancer – update of the EAU Guidelines
- METHODS OF NON-INVASIVE DIAGNOSTICS AND MONITORING OF URINARY BLADDER CANCER
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career