-
Medical journals
- Career
Poranění močových cest a genitálu
: J. Sánchez Gómez; L. Martínez-Pineiro
: Hospital Infanta Sofia , Urology Section Madrid
: Urol List 2011; 9(1): 21-31
Včasná identifikace a léčba poranění močopohlavního systému umožňuje minimalizovat morbiditu spojenou s traumatem (která může zahrnovat narušení močové inkontinence i sexuální funkce). Okamžitá identifikace vyžaduje systematické vyšetření, které zohledňuje mechanizmus poranění, nálezy fyzikálního vyšetření a zahrnuje rozbor moči a vhodné diagnostické testy, indikované ve správném pořadí. Poranění břicha se téměř ve všech případech vyšetřuje pomocí počítačové tomografie (CT). Až na výjimečné případy roztříštění ledviny nebo závažných lacerací renální žíly spojených s masivním krvácením, poranění močopohlavního systému obvykle neohrožuje život pacienta. U pacientů s poraněním v dolní části břicha probíhá vyšetřování (po stabilizaci života ohrožujícího stavu) retrográdním způsobem – od vyšetření zevního genitálu a močové trubice až po vyšetření močového měchýře. Často jsou v rámci CT vyšetření akutního stavu zároveň hodnoceny dolní i horní cesty močové. Při CT by měla být intravenózně aplikována iv. kontrastní látka. Rovněž se doporučuje provedení pozdních snímků, které umožní vyloučit přítomnost lézí v močovodu nebo močovém měchýři. Tento článek se zabývá diagnostikou a možnostmi léčby poranění močopohlavního ústrojí.
Klíčová slova:
renální trauma, ureterální trauma, trauma močového měchýře, uretrální trauma, genitourinární traumaPoranění močových cest a genitálu je příčinou významné morbidity a mortality. V oblasti léčby tohoto poranění došlo v uplynulých deseti letech k výrazným změnám. Při léčbě renálního traumatu je v současné době upřednostňována konzervativnější léčba než v minulosti. Autoři článku se pokouší vymezit nejdůležitější fáze diagnostiky a léčby poranění močových cest a genitálu [1].
Poranění ledviny
Poranění ledviny představuje přibližně 1–5 % všech případů traumatu [2]. Ledvina je nejčastěji postiženým orgánem ze všech orgánů lokalizovaných v břiše/močopohlavním systému. Nejčastější příčinou traumatu ledviny je tupé poranění. Závažnějším traumatem obvykle bývá otevřené poranění, nejčastěji zapříčiněné střelnou nebo bodnou ranou [3].
1. Grade (stupně) poranění ledviny. 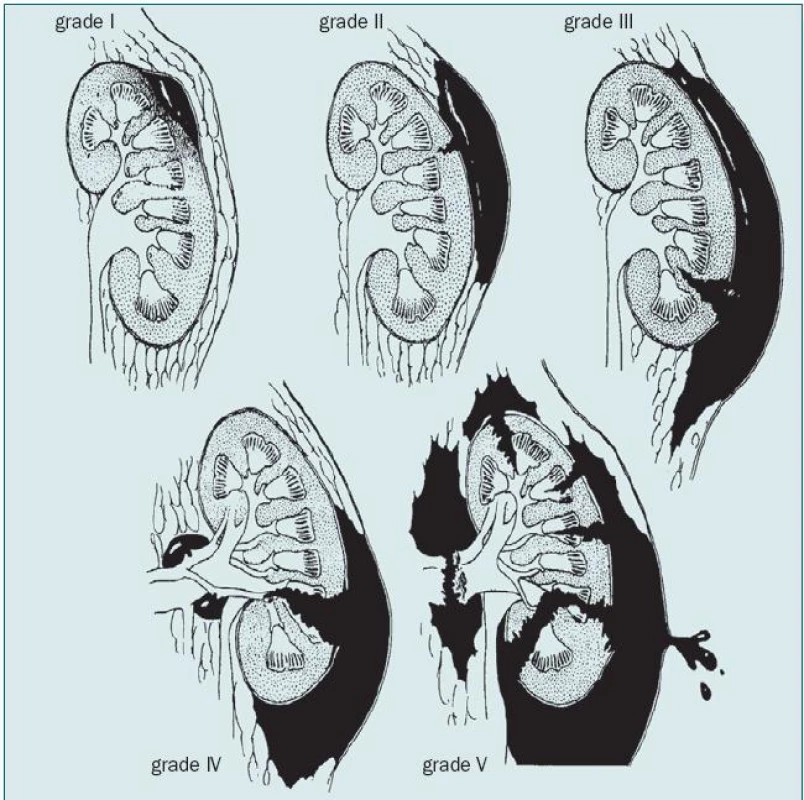
1. Diagnostický algoritmus při léčbě poranění ledviny. 
*V případě bilaterálního poranění (až po stupeň III) přidej jeden stupeň. Diagnostika
Anamnéza a fyzikální vyšetření
Rozhodující kritérium při léčbě poranění ledviny představuje hemodynamická stabilita.
V případě tupého traumatu poskytne informace o mechanizmu poranění lékaři představu o závažnosti potenciálního poranění ledviny (prudké zpomalení, pád, přímý úder do boku atd.). V případě penetrujícího poranění má pro lékaře zásadní význam informace o typu a kalibru zbraně. Tento typ poranění vyžaduje pečlivé vyšetření pacienta. Přítomnost onemocnění ledviny (striktura pyeloureterální junkce, velké cysty, litiáza) zvyšuje riziko vzniku léze v důsledku poranění. Následující faktory mohou být indikátory potenciálního poranění ledviny: hematurie, bolest, ekchymóza nebo abraze, fraktura žebra, abdominální distenze nebo hmatná rezistence. U 30 % pacientů s penetrujícím poraněním ledviny není přítomna hematurie. U 25 % pacientů s tupým poraněním a nálezem makroskopické hematurie budou přítomny závažné renální léze. U 30 % pacientů s poraněním způsobeným prudkým zpomalením nebude vůbec přítomna hematurie, u 50 % bude přítomna makroskopická hematurie nebo mikrohematurie a šok.
Laboratorní výsledky
Za základní vyšetření pacienta s podezřením na poranění ledviny se považuje rozbor moči. Hematurie nijak nesouvisí se stupněm závažnosti poranění ledviny. Přítomnost mikroskopické hematurie (> 5 erytrocytů/hrf) nebo makroskopické hematurie nemá dostatečnou senzitivitu ani specifitu pro rozlišení mezi závažným a méně závažným traumatem [4]. Opakované hodnocení hematokritu a potřeba krevní transfuze jsou nepřímými známkami ztráty krve a mají zásadní význam pro volbu terapie.
Hodnocení hladiny kreatininu v séru umožňuje identifikovat ty pacienty, u nichž byla renální funkce narušena již před poraněním.
Zobrazovací vyšetření
U pacientů s tupým traumatem a mikroskopickou hematurií, u nichž nebylo trauma zapříčiněno prudkým zpomalením a kteří nevykazují známky šoku, je incidence závažného poranění ledviny velmi nízká, a není tedy nutné provádět žádné zobrazovací vyšetření [5] (v tomto případě je přehlédnuto 0,03 % závažných lézí).
Provedení zobrazovacího vyšetření se doporučuje u pacientů s penetrujícím poraněním břicha nebo hrudníku, kdy máme podezření na poranění ledviny, a u pacientů s hematurií jakéhokoli stupně [6].
Za zlatý standard mezi radiologickými modalitami pro vyšetřování hemodynamicky stabilních pacientů s poraněním ledviny lze považovat počítačovou tomografii (CT) [7], jež umožňuje morfologické a funkční vyšetření traumatu: zobrazení renálních lézí jako např. kontuze a devitalizovaný segment vyvolaných změnami na ledvině v minulosti, zobrazení retroperitonea, břišní dutiny a pánve [8]. Absence kontrastního zvýraznění („enhancement“) v ledvině nebo přítomnost centrálního parahilárního hematomu může nasvědčovat poranění pediklu ledviny. Přítomnost velkého hematomu lokalizovaného mediálně od ledviny způsobujícího defiguraci cévního zásobení může být známkou žilní léze. V případě, že je provedeno CT vyšetření, je nutné po 10–15 minutách scan opakovat pro vyloučení potenciální extravazace moči.
Tab. 1 zobrazuje AAST klasifikaci podle závažnosti poranění ledviny [9].
Role ultrazvukového vyšetření je zde poměrně omezená, ačkoli ultrazvuk lze užít jako úvodní test umožňující rozhodnout, u kterých pacientů bude nutné provedení dalších radiologických testů, a při hodnocení pacientů s méně závažným poraněním ledviny. Ultrazvukové vyšetření umožňuje detekovat přítomnost lacerací, nikoli však hloubku jejich lokalizace ani rozsah. Rovněž neposkytuje žádnou informací týkající se funkce ledviny nebo močové extravazace [10].
Intravenózní urografie, magnetická rezonance (MRI) ani scintigrafie se v současné době při vyšetřování pacientů s poraněním ledviny neužívají, mohou však být indikovány v centrech, která nedisponují CT scanem.
Intravenózní urografie umožňuje správně stanovit stupeň postižení u 85 % případů tupého poranění a 65 % případů poranění penetrujícího orgán. Ve 30 % případů závažného poranění ledviny však tato diagnostická modalita neposkytuje potřebnou informaci a neumožňuje rozlišit méně a více závažné trauma. V 60 % případů, kdy má pacient nefunkční ledvinu, je přítomen intaktní pedikl ledviny [11].
Provedení peroperační IVU 10 minut po intravenózní aplikaci 2 ml/kg jednorázového bolusu kontrastní látky může pomoci při hodnocení funkce kontralaterální ledviny u pacientů, jejichž klinický stav vyžaduje akutní provedení laparotomie [12].
MRI může být užitečná u pacientů s alergií na kontrastní látku obsahující jód v centrech, která nemají k dispozici CT scan [13] a ve výjimečných případech, kdy je výsledek CT nejednoznačný.
Angiografie umožňuje stanovit přesnou lokalizaci a stupeň (grade) renální léze. Toto vyšetření lze užít pro selektivní embolizaci při léčbě přetrvávajícího nebo opožděného krvácení. Zavedení endovaskulárního stentu do trombotické arterie v důsledku jejího natažení představuje vhodnou alternativu pouze v případě, že je provedeno během prvních čtyř hodin po vzniku traumatu [14–16].
Léčba
Indikace pro exploraci ledviny
V případě, že je nutné přistoupit k chirurgickému řešení, by se měl operatér snažit o zachování orgánu [17].
Absolutní indikací pro chirurgickou léčbu jsou [18]:
- hemodynamická nestabilita
- pulzující a rozšiřující se perineální hematom detekovaný během laparotomie
- renální léze V. stupně (grade)
- incidentální nález postižení ledviny během operace
Většinu traumat (včetně traumat spojených s močovou extravazací a přítomností devitalizovaných fragmentů) lze vyléčit pomocí konzervativní neoperační léčby, která zahrnuje klid na lůžku, aplikaci antibiotik a kontrolu hemodynamické stability až do vymizení hematurie. Neoperační léčba močové extravazace představuje u pacientů, kteří utrpěli poranění ledviny bez současného poranění břicha nebo vaskulárního poranění, bezpečnou volbu a vede k vyléčení u více než 90 % případů. U pacientů s přetrvávajícím únikem moči může být nezbytné endoskopické zavedení ureterálního stentu. Toto řešení je obvykle účinné.
Mezi relativní indikace pro chirurgickou léčbu patří přetrvávající krvácení a podezření na přítomnost léze v ledvinné pánvičce nebo v močovodu.
2. Poranění ledviny II. grade (stupně). 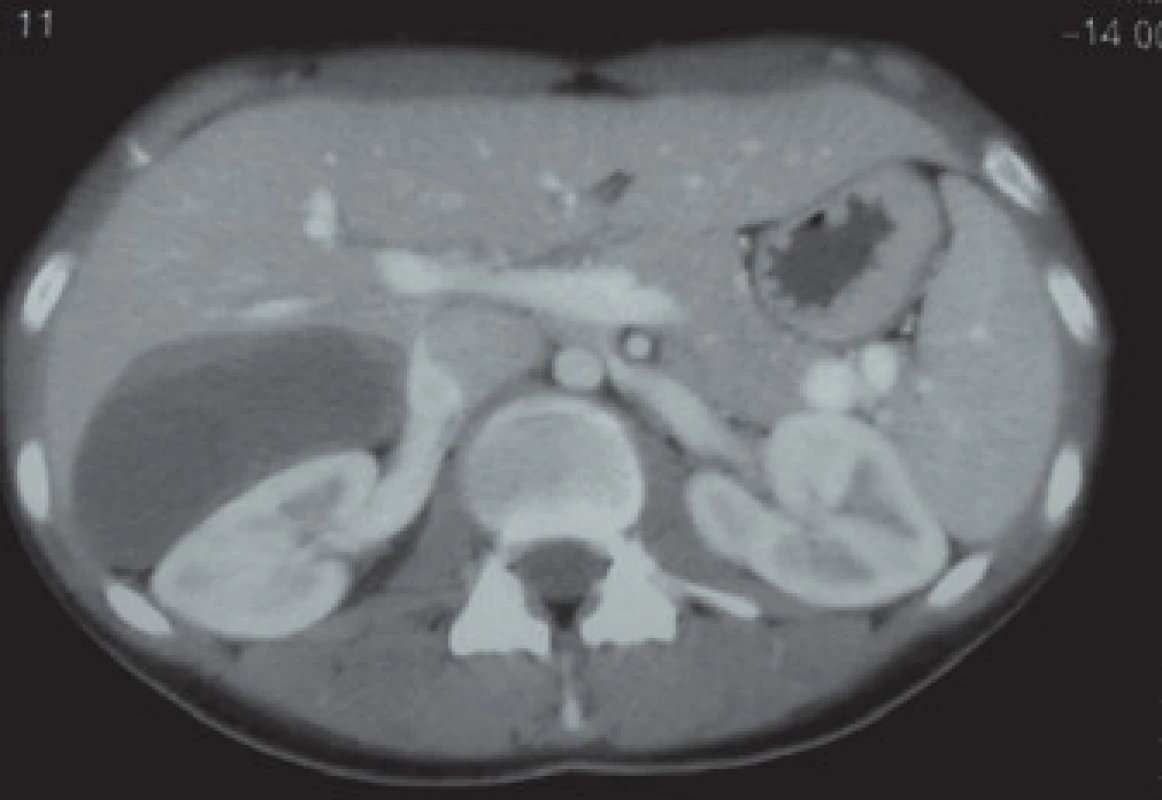
3. Poranění ledviny III. grade (stupně). 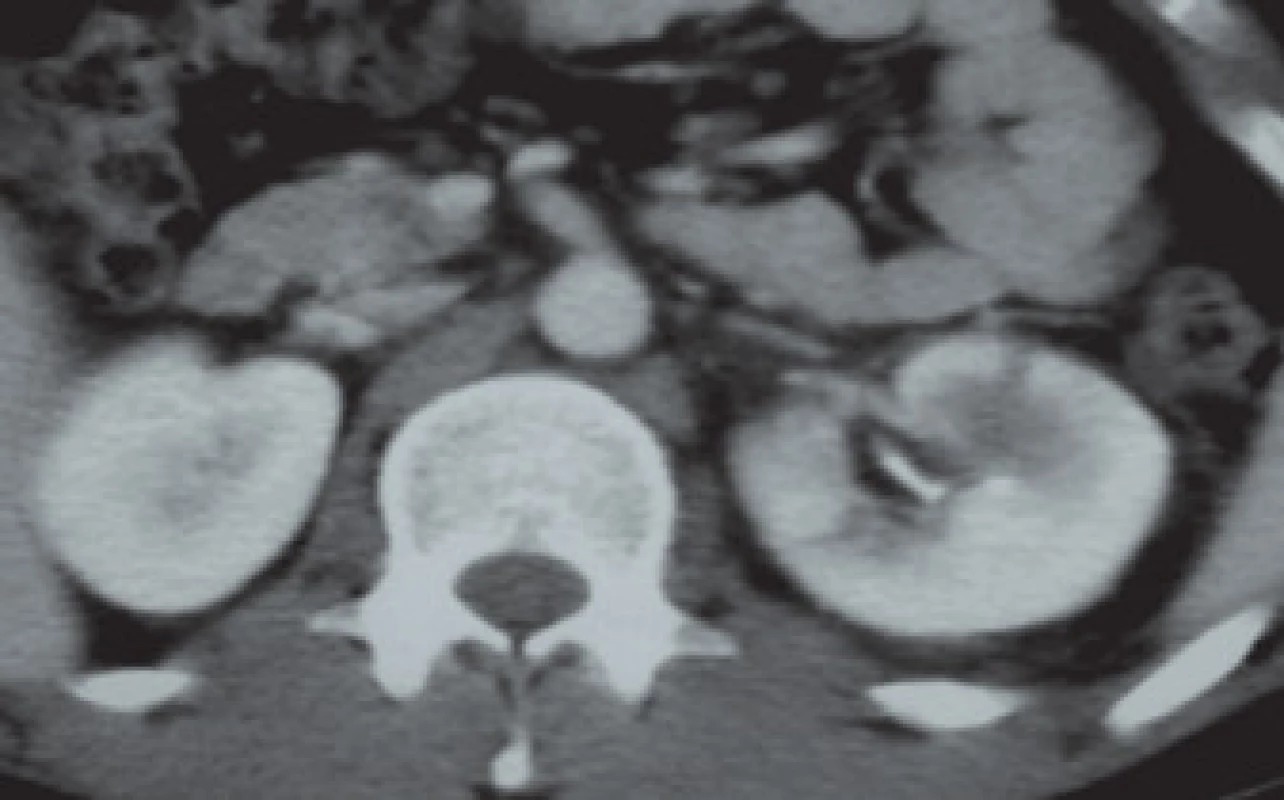
4. Poranění ledviny IV. grade (stupně). 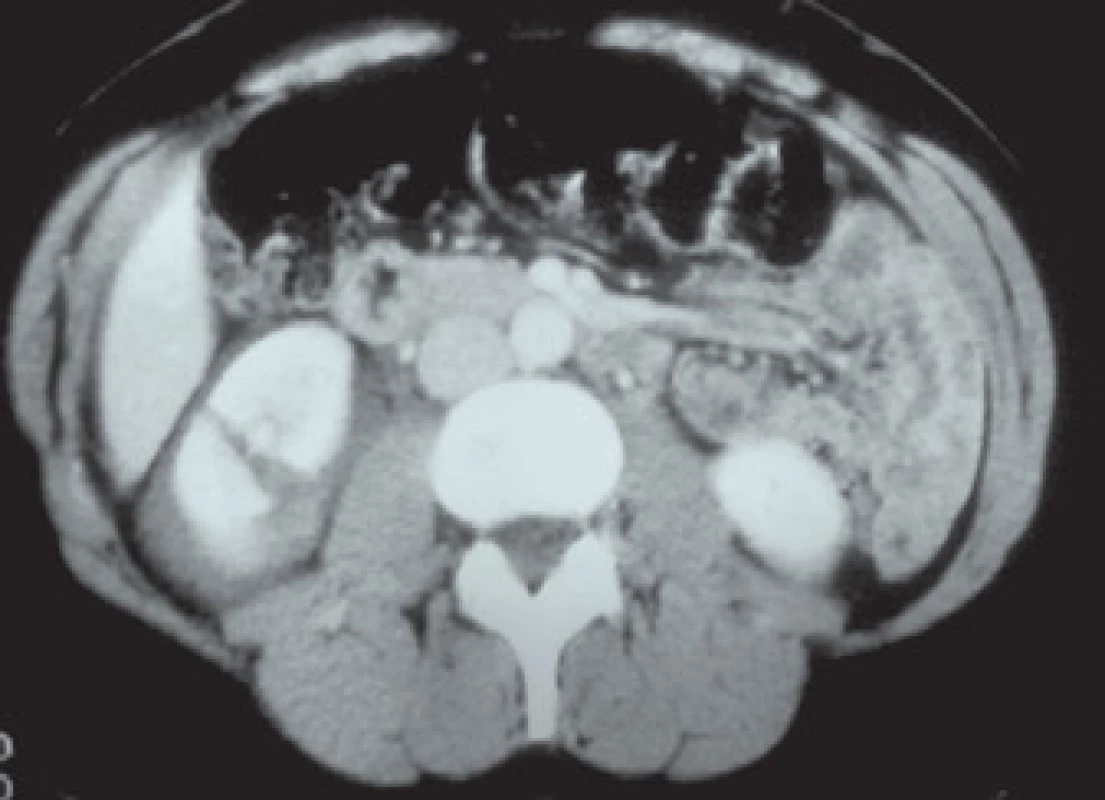
5. Poranění ledviny V. grade (stupně). 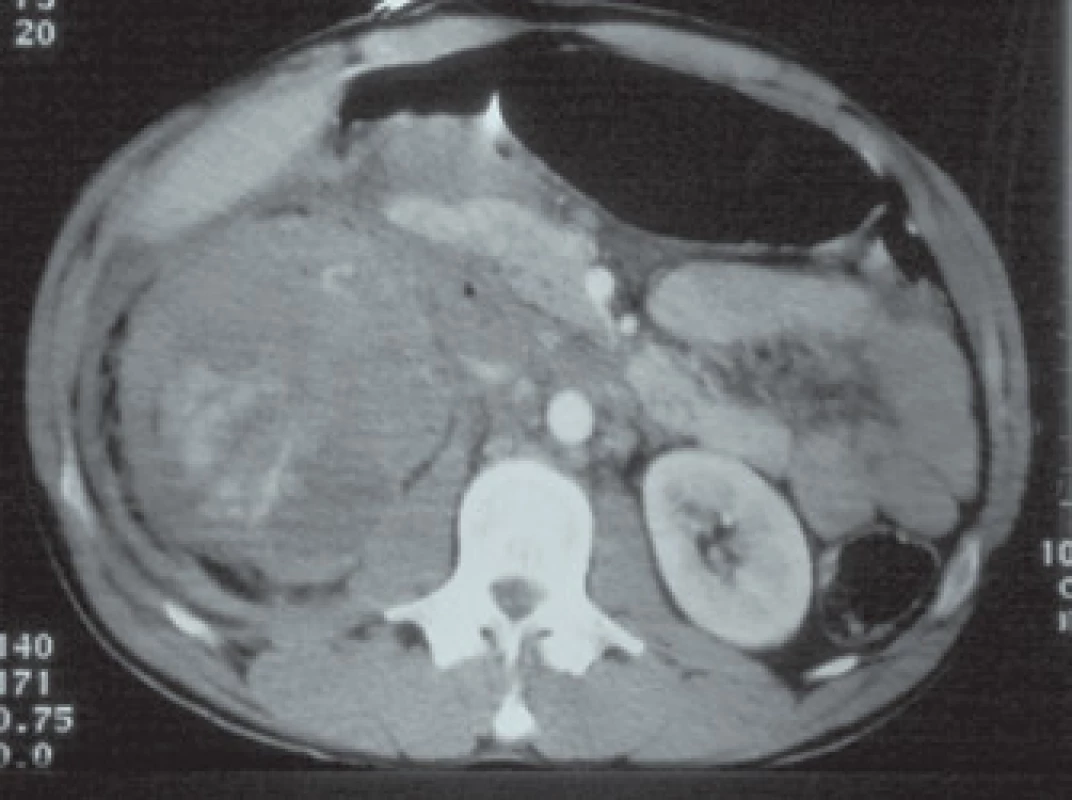
Doporučuje se transperitoneální přístup a provedení dočasné vaskulární okluze před otevřením Gerotovy fascie. Obvykle je indikována chirurgická korekce léze nebo parciální resekce ledviny. Naprosto nezbytné je vodotěsné uzavření vývodného systému, jež se provádí buď přímo, nebo obšitím renálního parenchymu. Rovněž je možné užití štěpu z velkého omenta. Na konci výkonu by měl být v ipsilaterální části retroperitonea zaveden drén.
Za zlatý standard pro léčbu poranění vaskulárního zásobení ledviny je považována nefrektomie (s výjimkou pacientů se solitární ledvinou a pacientů s bilaterálními lézemi) [20].
Arteriografie s embolizací pro kontrolu krvácení představuje u vybraných pacientů vhodnou alternativu k laparotomii [21]. Zavedení endovaskulárního stentu do trombotické renální arterie (vyvolané tupým poraněním) představuje vhodnou alternativu v případě, že je provedena během prvních čtyř hodin po vzniku poranění [22–24].
Neoperační léčba
Pouze u malého procenta stabilizovaných pacientů, u nichž je indikována konzervativní léčba, je nutné provedení nefrektomie (bez zvýšení morbidity). Všechna traumata prvního nebo druhého stupně lze řešit pomocí konzervativní léčby. Konzervativní léčba může být indikována rovněž u pacientů s traumatem III. stupně [25]. V současné době lze léčit konzervativně i izolované renální léze IV. stupně.
V tomto případě je hlavní indikací pro chirurgickou intervenci přetrvávající krvácení [26].
U hemodynamicky stabilních pacientů s penetrujícím poraněním je nutné provedení pečlivého vyšetření, jež umožní posoudit plný rozsah traumatu. V případě střelné rány je nutné zjistit, zda poranění zasahuje hilus ledviny, zda je doprovázeno známkami aktivního krvácení a zda existuje podezření na přítomnost léze v močovodu nebo ledvinné pánvičce [27]. Většinu renálních lézí způsobených bodnou ranou posteriorně vzhledem k anteriorní axilární linii lze léčit konzervativně.
Pooperační péče a komplikace
U pacientů se závažným poraněním, u nichž není indikována chirurgická léčba, a rovněž u pacientů s horečkou, bolestí v boku a jedinců, u nichž došlo k poklesu hematokritu, je nutné zobrazovací vyšetření opakovat každé 2–4 dny.
Mohou se vyskytnout následující komplikace: močová extravazace, krvácení, hydronefróza, litiáza, chronická pyelonefritida, hypertenze, arteriovenózní píštěl a pseudoaneurysma.
6. A–C. Endovaskulární stent trombotické arterie vyvolané poraněním močové trubice natažením představuje adekvátní terapeutickou modalitu, pakliže je provedeno během prvních čtyř hodin po poranění. A. CT nález trombózy pravé renální arterie. B. Arteriografie zobrazující parciální trombózu pravé renální arterie způsobené přerušením intimy. C. Arteriografie ledviny zobrazující úplnou trombózu pravé renální arterie. 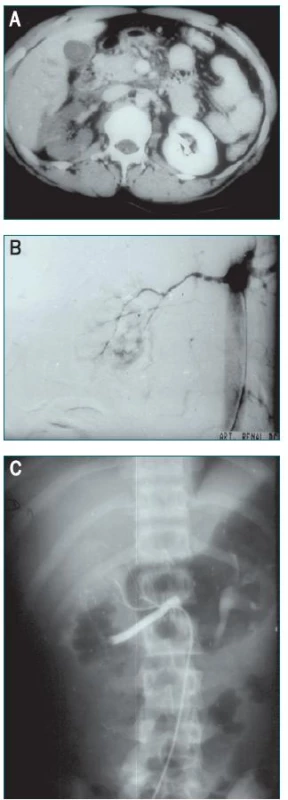
Opožděné retroperitoneální krvácení lze řešit pomocí selektivní embolizace při arteriografii. Perinefritický absces se obvykle léčí perkutánně, v některých případech však může být nutné provedení drenáže během otevřené operace. Močová extravazace často sama vymizí bez potřeby chirurgické intervence, pakliže není přítomna obstrukce močovodu nebo infekce. Retrográdní zavedení stentu do močovodu zlepšuje drenáž a často usnadňuje hojení poranění [28].
Provedení radioizotopové scintigrafie před propuštěním pacienta z nemocnice je vhodné pro dokumentaci obnovy funkce ledviny.
Monitorování pacienta během prvních tří měsíců by mělo zahrnovat následující:
- fyzikální vyšetření
- rozbor moči
- radiologické vyšetření dle individuálních potřeb
- kontrolu krevního tlaku
- posouzení funkce ledviny z vyšetření séra
Při dlouhodobém sledování je vhodné kontrolovat hodnotu krevního tlaku, ačkoli incidence hypertenze je nízká – méně než 10 %. Přibližně u 6 % pacientů, u nichž dojde v důsledku poranění segmentální větve renální arterie ke vzniku trombózy, se vyvine hypertenze. Hypertenze se rovněž vyvine v dlouhodobém horizontu u 2,5 % dětských pacientů s poraněním ledviny IV.–V. stupně, kteří jsou léčeni konzervativně [29,30]. Léčba hypertenze spočívá v medikamentózní terapii, excizi ischemického segmentu parenchymu, vaskulární rekonstrukci nebo kompletní nefrektomii.
Schéma 1 zobrazuje diagnostický algoritmus u pacientů s poraněním ledviny (zahrnujícím trombózu hlavní renální arterie).
7. Diagnostické postupy při léčbě poranění ledviny. 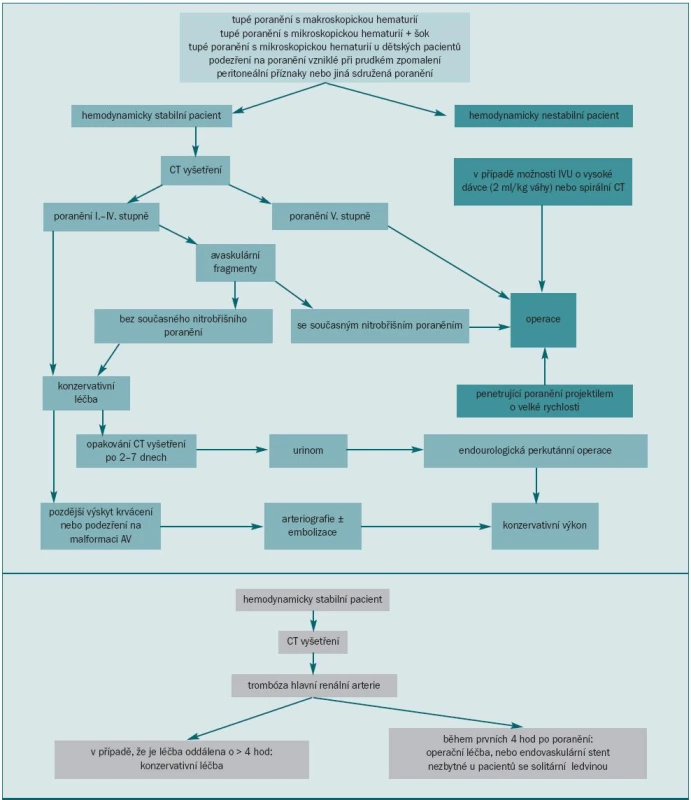
Souhrn
- V případě, že je pacient stabilizován, lze trauma I.–IV. stupně (grade) vzniklé tupým poraněním léčit konzervativně.
- Trombózu hlavní renální arterie se doporučuje řešit zavedením intravaskulárního stentu.
- U pacientů s tupým poraněním, u nichž je z důvodu souvisejících intraabdominálních lézí indikována akutní laparotomie, není nutné zasahovat do retroperitonea, pakliže hematom není pulzní nebo expandující a pakliže předoperační CT vyloučilo přítomnost kontrastní extravazace a poranění V. grade.
- V případě, že je pacient stabilizován, lze trauma I.–III. stupně (grade) vzniklé penetrujícím poraněním léčit konzervativně.
- Renální lézi vzniklou střelným poraněním je třeba revidovat, jestliže zasahuje do hilu ledviny, je doprovázena známkami krvácení nebo pokud existuje podezření na přítomnost léze v močovodu nebo ledvinné pánvičce.
Poranění močovodu
Celková revize 452 případů poranění močovodu odhalila, že v 75 % případů bylo trauma iatrogenní, v 18 % případů bylo způsobeno tupým poraněním a v 7 % případů otevřeným poraněním. 73 % iatrogenních lézí vzniklo při gynekologické, 14 % při chirurgické a 14 % při urologické operaci [31,32].
Poranění močovodu je poměrně vzácné. 74 % traumat se vyskytuje v dolní třetině močovodu. V případě, že CT sken neumožní diagnostikovat poranění, je nejúčinnější diagnostickou technikou intravenózní urografie a retrográdní ureteropyelografie.
V řadě případů je diagnóza stanovena během výkonu. Nejzávažnější komplikací, k níž může dojít po léčbě, je vznik ureterální stenózy.
8. 8 A–C. Poranění močové trubice. Natržení ureteropelvické junkce. A. Retrográdní urografie zobrazující extravazaci kontrastní látky v blízkosti ureteropelvické junkce (UPJ). B. CT vyšetření zobrazující extravazaci kontrastní látky v pravé UPJ v důsledku přerušení UPJ. C. CT vyšetření zobrazující extravazaci kontrastní látky podél m. psoas v důsledku přerušení levé UPJ. 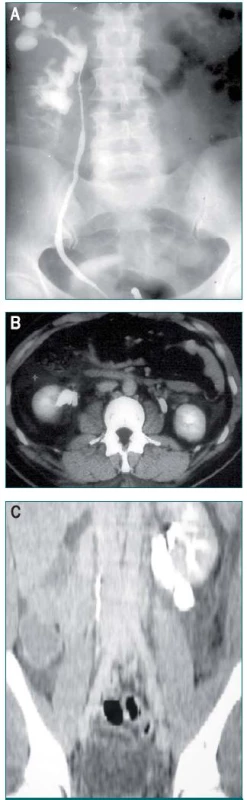
2. AAST stupnice závažnosti poranění močovodu. 
*V případě bilaterálního poranění (až po stupeň III) přidej jeden stupeň. Tab. 2 ukazuje AAST stupnici závažnosti poranění močovodu.
Parciální léze lze léčit zavedením ureterálního katétru nebo derivací moči nefrostomií [33].
U lézí II., nebo III. stupně (grade) detekovaných během operace se doporučuje primární sutura močovodu se zavedením stentu a nevakuové drenáže v místě poranění.
Při korekci lézí III.–V. stupně (grade) je nutné dodržovat následující pravidla:
- očištění konců močovodu pro uvolnění tkáně
- spatulace konců močovodu
- zavedení ureterálního stentu
- vytvoření vodotěsné sutury pomocí vstřebatelných stehů
- izolace rekonstruované léze pomocí peritonea nebo omenta
Volba operační techniky závisí na charakteru a lokalizaci léze. K dispozici máme následující možnosti:
Horní třetina
- ureteroureteroanastomóza
- transureteroureteroanastomóza
- ureterokalikoanastomóza
Prostřední třetina
- ureteroureteroanastomóza
- transureteroureteroanastomóza
- technika s užitím Boariho laloku a reimplantace
Dolní třetina
- přímá reimplantace
- technika s užítím techniky “psoas hitch”
- cystoplastika podle Blandyho
Úplná ztráta močovodu
- nahrazení segmentem ilea (později)
- autotransplantace (později)
V případě, že ureterální léze komplikuje korekci aneuryzmatu v abdominální části aorty či jinou cévní operaci, při níž je implantována cévní protéza, měla by být z důvodu snížení rizika sepse a infekce štěpu provedena okamžitá nefrektomie.
Poranění močového měchýře
Tupá poranění tvoří přibližně 67–86 % lézí močového měchýře, penetrující poranění 14–33 % lézí [34]. Tupá poranění, z nichž je většina způsobena při dopravních nehodách, klasifikujeme jako intraperitoneální a extraperitoneální. Tato traumata jsou většinou spojena s frakturou pánve.
9. Cystografie zobrazující extraperitoneální rupturu močového měchýře. 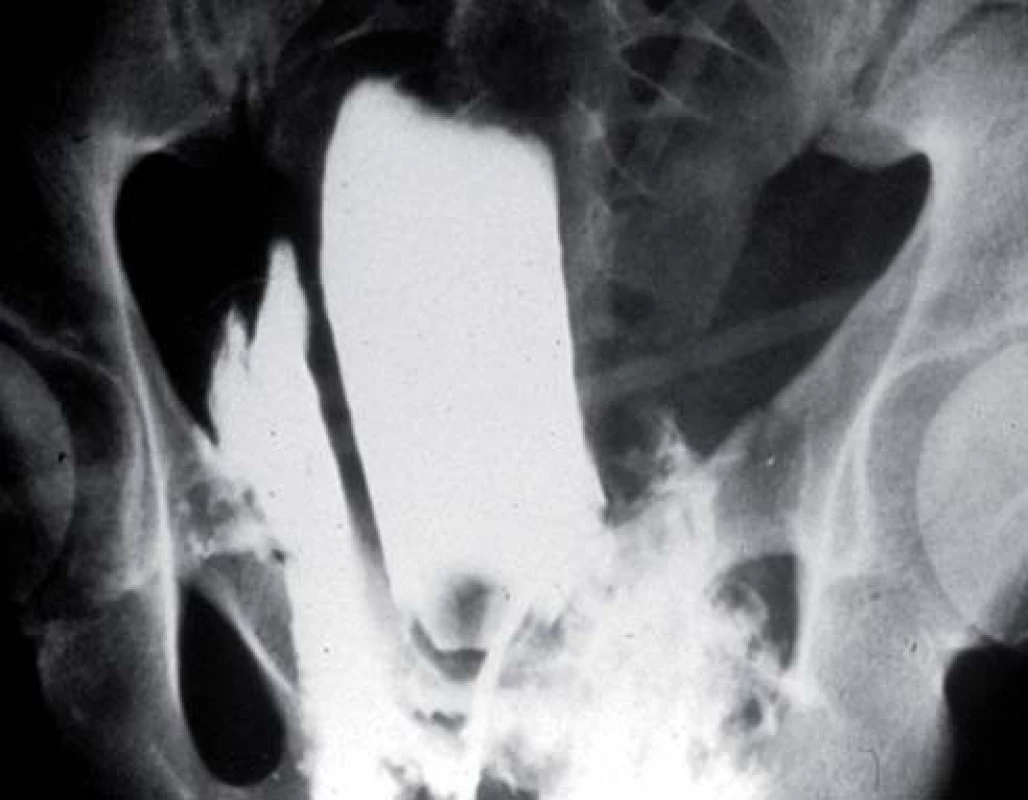
10. Cystografie zobrazující intraperitoneální rupturu močového měchýře. 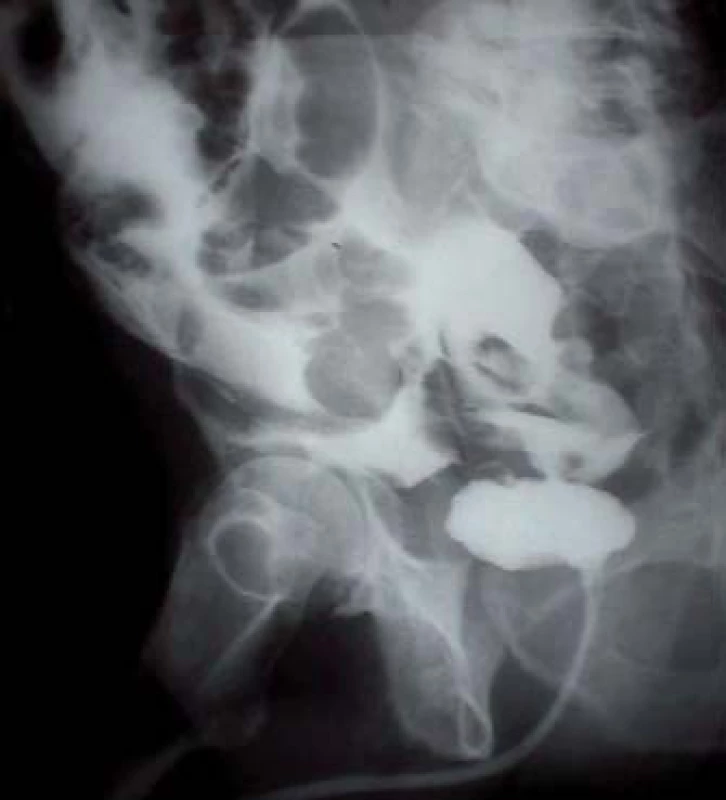
3. AAST stupnice závažnosti poranění močového měchýře. 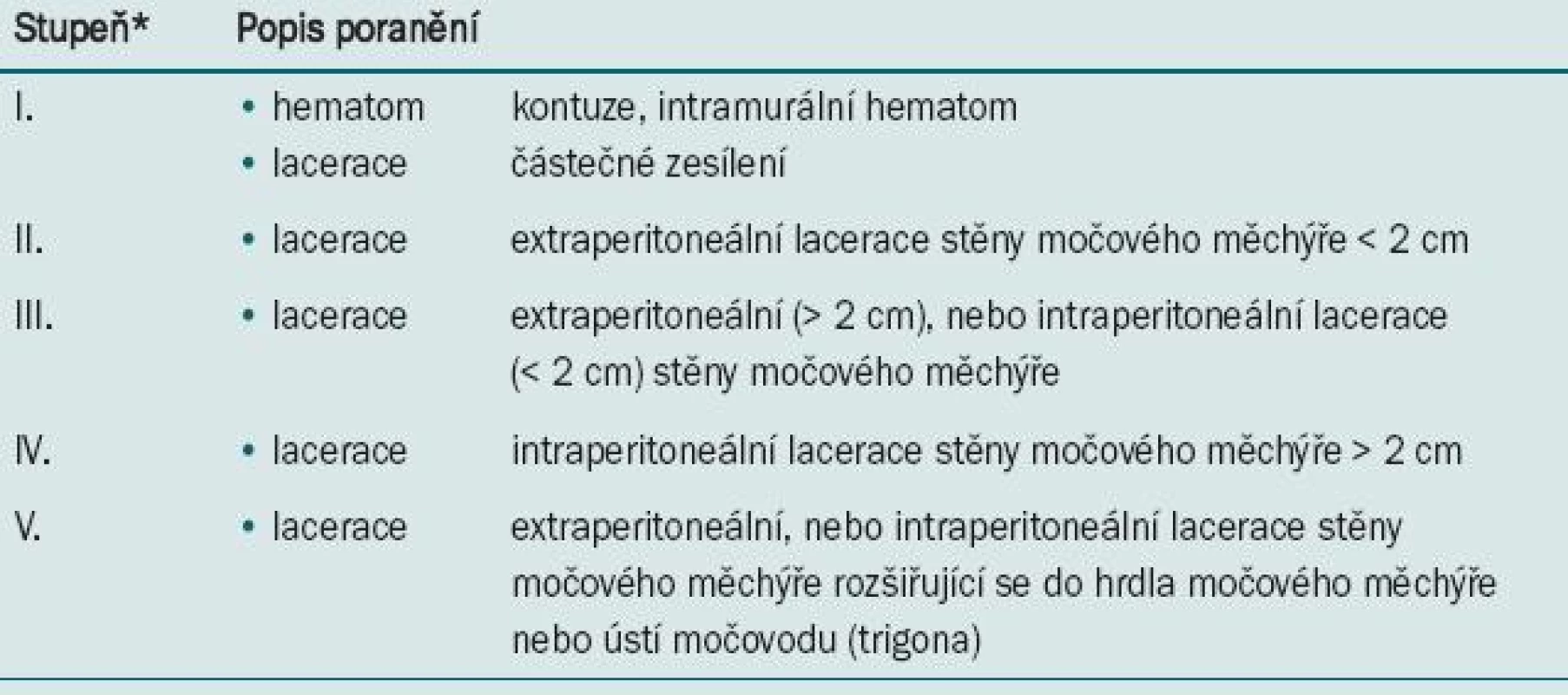
*V případě bilaterálního poranění (až po stupeň III) přidej jeden stupeň. Tab. 3 zobrazuje AAST stupnici závažnosti poranění močového měchýře.
Klinické symptomy zahrnují makroskopickou hematurii (80–90 %), abdominální citlivost (60 %), neschopnost močit, pohmoždění v suprapubické oblasti a abdominální distenzi. Močová extravazace se může dále šířit skrze peritoneum, skrotum, stehna a anteriorní stěnu břišní.
Kombinace fraktury pánve a makroskopické hematurie představuje absolutní indikaci pro akutní provedení cystografie. Cystografie by se měla provádět při adekvátní distenzi (alespoň 350 ml kontrastní látky). Abychom předešli falešně-negativním výsledkům, je vhodné po močení provést RTG snímek. Ideální alternativou běžné cystografii může být CT cystografie, zejména u pacientů, kteří musí podstoupit CT z důvodu dalších sdružených poranění. Velmi důležité je provedení i opožděného zobrazení a instilace kontrastní látky.
U většiny pacientů s extraperitoneální lézí v močovém měchýři je vhodným přístupem zavedení drenážního katétru do močového měchýře, dokonce v případě extravazace moči do retroperitonea nebo do skrota [35] (93% míra úspěšnosti, 87 % pacientů je zhojeno během 10 dnů).
V případě zasažení hrdla močového měchýře, přítomnosti fragmentů ve stěně močového měchýře nebo jejího zachycení mezi kostními fragmenty je v každém případě nutné indikovat chirurgickou léčbu. Chirurgické řešení rovněž vyžaduje intraperitoneální ruptura (vysoká míra mortality: až 30 % z důvodu souvisejících poranění) a penetrující trauma.
Poranění močové trubice
Léze v anteriorní části močové trubice mohou být způsobeny tupým nebo penetrujícím poraněním, zavedením kompresních struktur a iatrogenním poraněním při instrumentaci. Penetrující poranění, jehož příčinou je obvykle střelná rána, postihuje stejně často bulbární i pendulózní močovou trubici [36–38].
K poranění posteriorní části močové trubice obvykle dochází v důsledku nestabilní fraktury pánevní kosti a bilaterální fraktury ramene ischiopubické kosti při autonehodách. Léze mohou mít nejrůznější podobu: od prostého natažení (25 %), přes částečné natržení (50 %) až po úplné přerušení močové trubice (25 %) [39]. U žen je výskyt poranění uretry velmi vzácný. Léze u dětí jsou stejné jako u dospělých.
Tab. 4 ukazuje AAST stupnici závažnosti poranění močové trubice.
4. AAST stupnice závažnosti poranění močové trubice. 
*V případě bilaterálního poranění (až po stupeň III) přidej jeden stupeň. Klinická léčba lézí močové trubice vyvolaných traumatem je indikována na základě závažnosti poranění:
- léze I. grade nevyžadují žádnou léčbu
- léze II. a III. grade lze léčit konzervativně zavedením suprapubické cystostomie nebo uretrálního stentu
- léze IV. a V. grade vyžadují endoskopickou obnovu kontinuity uretry a/nebo pozdější provedení uretroplastiky V některých případech může být z důvodu závažnosti uretrální léze (a všech souvisejících lézí) nutná primární sutura.
Diagnostika
U pacientů s poraněním anteriorní části močové trubice jsou obvykle v meatu uretry známky krve. V tomto případě je kontraindikována jakákoli instrumentace v močové trubici do doby, než bude provedeno adekvátní zobrazovací vyšetření.
U nestabilizovaných pacientů se doporučuje jeden pokus o zavedení uretrálního stentu, v případě jakýchkoli obtíží by měl být zaveden pod ultrazvukovou kontrolou suprapubický stent. Poranění močové trubice je nutné dále zhodnotit pomocí radiologického vyšetření. Nebylo prokázáno, že by jediný pokus o zavedení uretrálního stentu zvyšoval frekvenci výskytu infekce nebo uretrální stenózy. Jestliže máme podezření na přítomnost uretrální léze, je v každém případě nejvhodnější provedení uretrografie.
Mohou se vyskytovat i další symptomy jako hematurie, bolest při močení, neschopnost močit, krev ve vaginálním introitu nebo hematom v perineální oblasti.
Za zlatý standard je při úvodním vyšetření poranění močové trubice považována retrográdní uretrografie. V případě podezření na poranění posteriorní části močové trubice se doporučuje zavedení suprapubické drenáže současně s cystografií. Pro stanovení lokalizace, závažnosti a délky léze je možné následně provést retrográdní uretrografii. Pakliže tato metoda neumožní zobrazit proximální část močové trubice, může být indikováno antegrádní endoskopické vyšetření (prostřednictvím suprapubického katétru) nebo zobrazovací vyšetření pomocí magnetické rezonance.
11. Poranění přední části močové trubice. 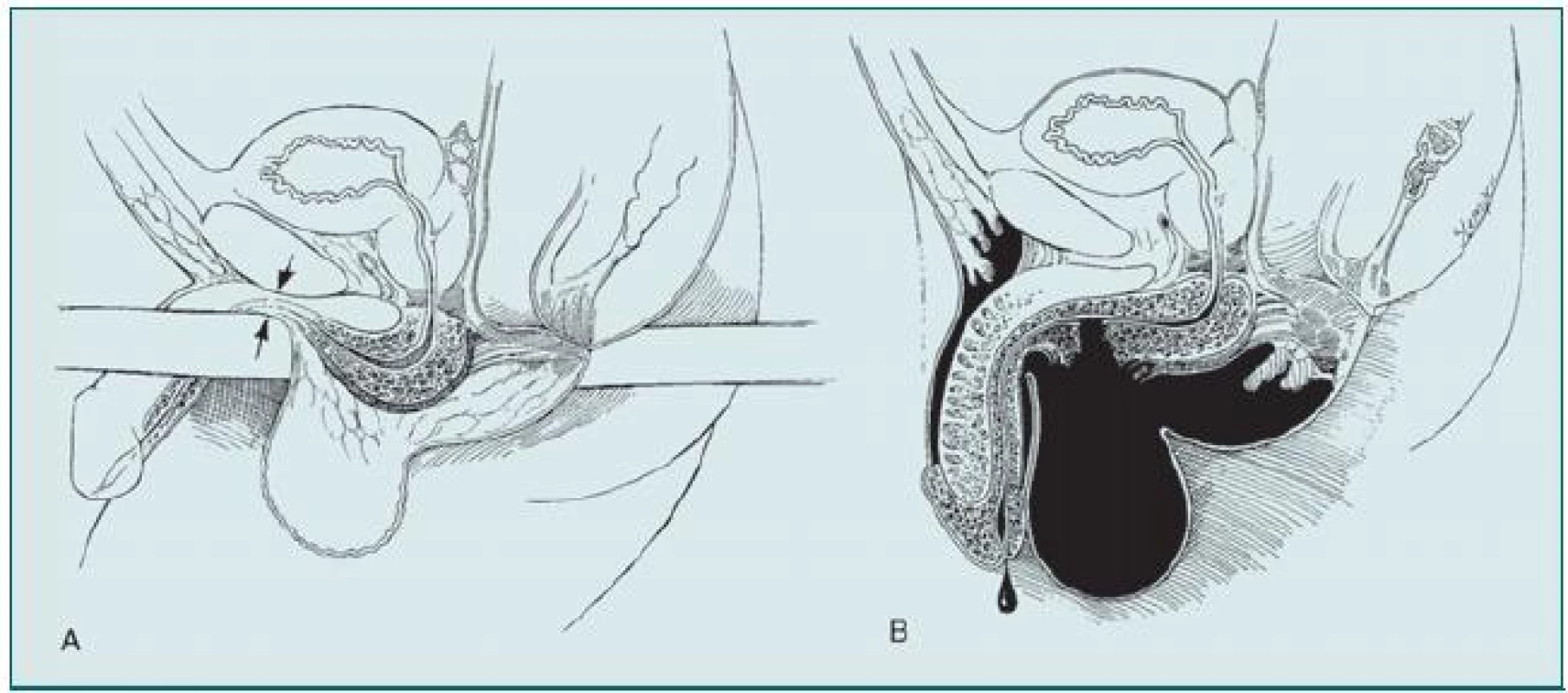
12. Uretrální striktura bulbární a penilní močové trubice v důsledku tupého traumatu. Uretrografie 4 měsíce po poranění. 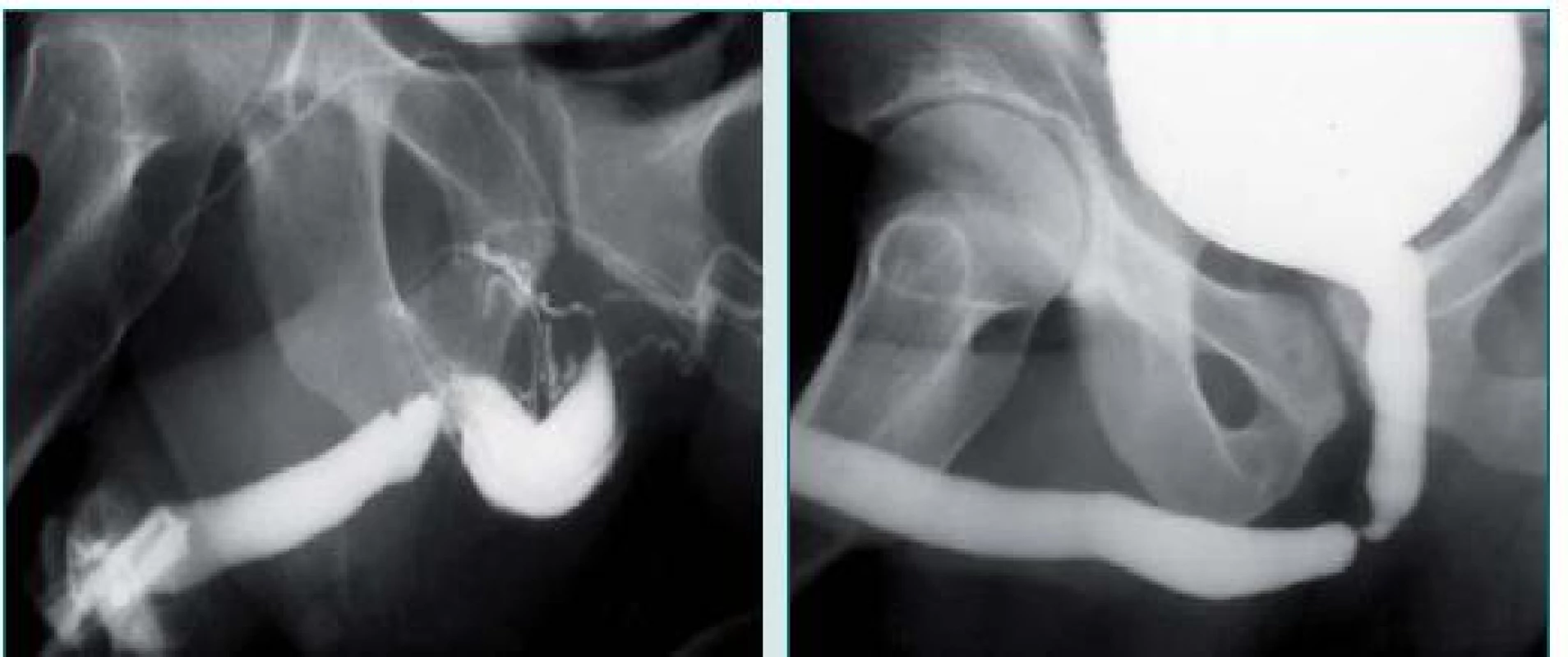
13. End-to-end uretroplastika striktury bulbární močové trubice. 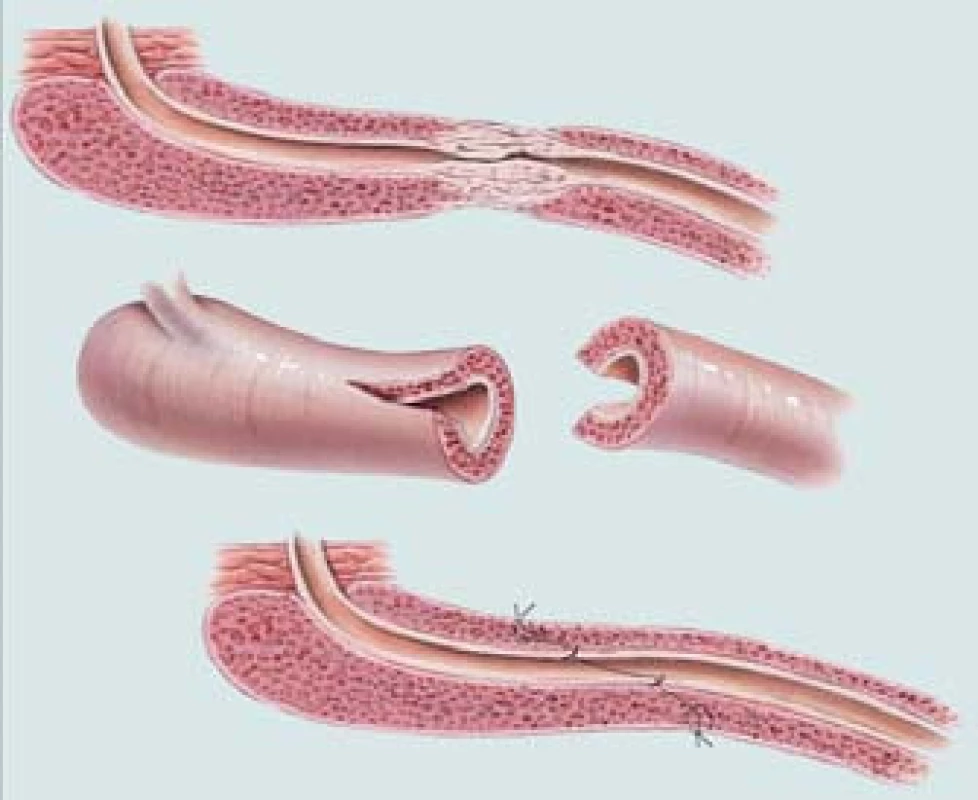
14. Distrakční defekt zadní části močové trubice. Kombinovaná mikční a retrográdní uretrografie. 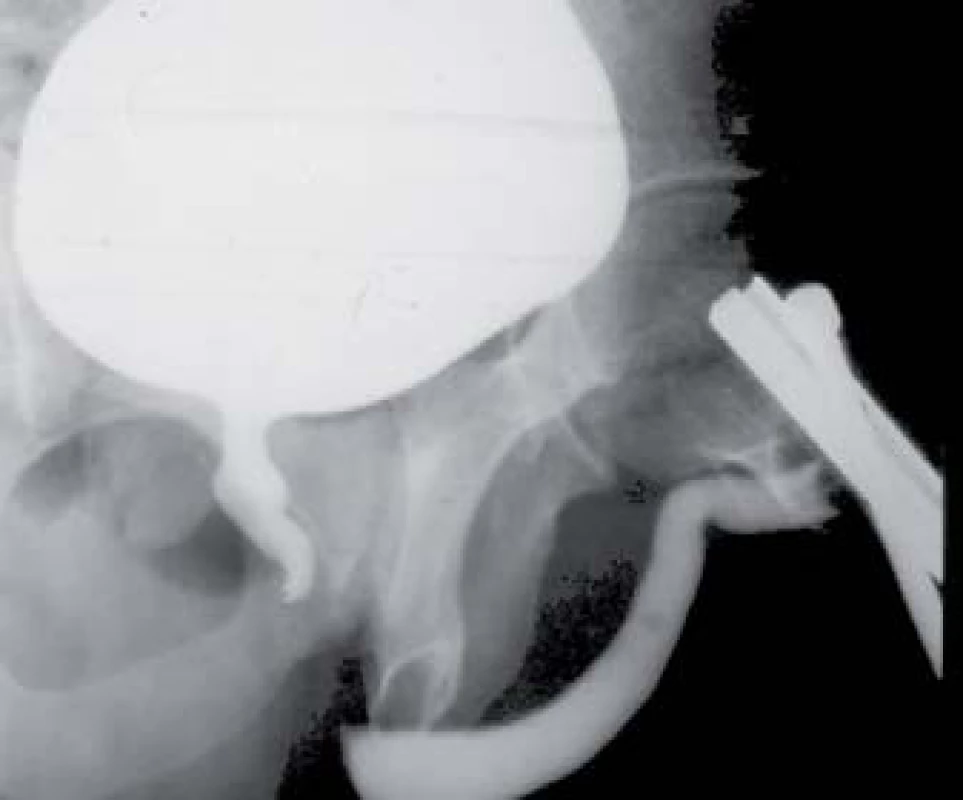
Léčba
Anteriorní část močové trubice
Tupé poranění lze řešit zavedením suprapubického nebo uretrálního katétru [40], upřednostňuje se však suprapubický katétr, abychom předešli poranění močové trubice a kontaktu moči s místem poranění. Aplikace antibiotik snižuje riziko vzniku lokálních komplikací v místě léze a zabraňuje vzniku abscesů. U 50 % pacientů dojde ke vzniku striktury, jež lze následně léčit (na základě charakteru striktury). Většinu lézí v močové trubici u žen lze sešít vaginálním přístupem.
Otevřené poranění vyžaduje okamžitou operační léčbu. Malé lacerace lze sešít jemnou vstřebatelnou suturou. V případě úplného přerušení močové trubice lze provést anastomózu konců vzájemně. Během prvního zákroku na lézi v anteriorní části močové trubice není vhodné provádět žádný typ rekonstrukční operace, neboť kontaminace a nedostatečné krevní zásobení mohou mařit výsledek rekonstrukce močové trubice. V případě, že délka defektu přesahuje 1–1,5 cm, je vhodné 3 měsíce po vzniku poranění provést elektivní rekonstrukci.
Posteriorní část močové trubice
Malé lacerace lze ve většině případů řešit zavedením uretrálního nebo suprapubického katétru.
Při léčbě kompletních lézí v posteriorní části močové trubice je vhodné zavedení suprabického katétru. V případě, že je z traumatologického hlediska nebo z důvodu přítomnosti lézí v hrdle močového měchýře nebo rektu indikována chirurgická léčba, doporučuje se během sedmi dnů po vzniku poranění u pacientů s úplným roztržením močové trubice okamžitá endoskopická obnova kontinuity uretry. Léčba stenózy, která se vyskytuje u 70 % pacientů, je mnohem snazší. K dispozici máme řadu technik, jako např. pouhé zavedení katétru nebo endoskopická obnova kontinuity uretry pomocí biplanární skiaskopie.
Otevřená primární obnova kontinuity uretry s evakuací pánevního hematomu a preparací apexu prostaty se v případě tupého poranění nedoporučuje. Tato technika je náročná, potenciálně nebezpečná a je spojena s nepřijatelně vysokou mírou impotence a inkontinence.
Jakoukoli strikturu vzniklou během poranění nebo v pozdější fázi lze léčit pomocí dilatace močové trubice nebo vnitřní uretrotomie (pakliže je striktura krátká a křehká) nebo pomocí uretroplastiky anastomózou (pakliže je tužší) [41,42]. Léze v prostatické nebo bulbární části močové trubice lze obvykle léčit pomocí perineální anastomózy.
Schéma 2 zobrazuje diagnostický algoritmus při léčbě lézí v posteriorní části močové trubice.
Poranění genitálu
Přímý úder do ztopořeného penisu může způsobit jeho frakturu, k čemuž často dochází během pohlavního styku. Při faktuře penisu dochází k ruptuře tuniky albuginea, může být rovněž doprovázena vznikem lézí v corpus spongiosum a močové trubici nebo podkožního hematomu. Ve 20 % případů je poranění penisu doprovázeno poraněním močové trubice.
15. Poranění zadní části močové trubice. Obnovení kontinuity močové trubice pomocí endoskopického přístupu. 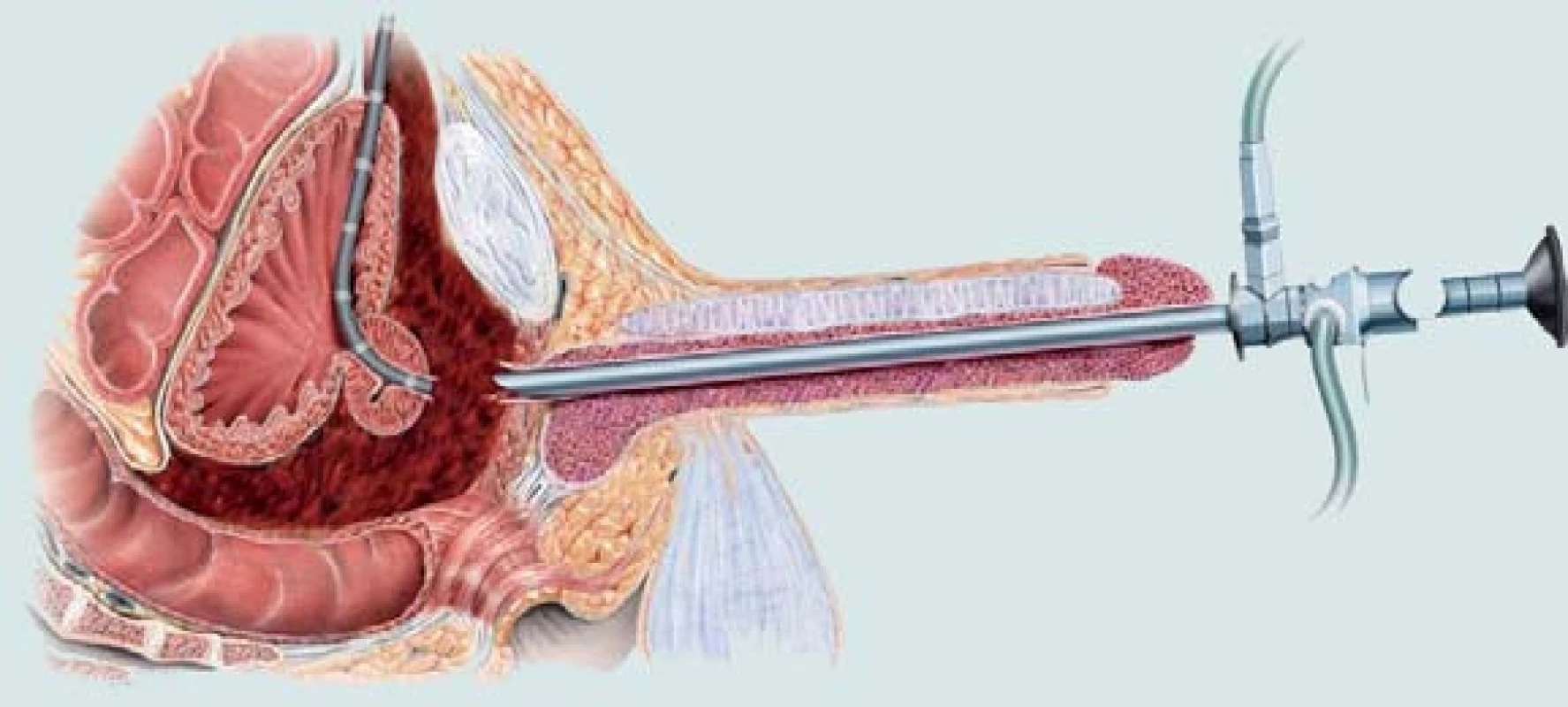
16. Poranění zadní části močové trubice. Obnovení kontinuity močové trubice pomocí otevřeného přístupu. 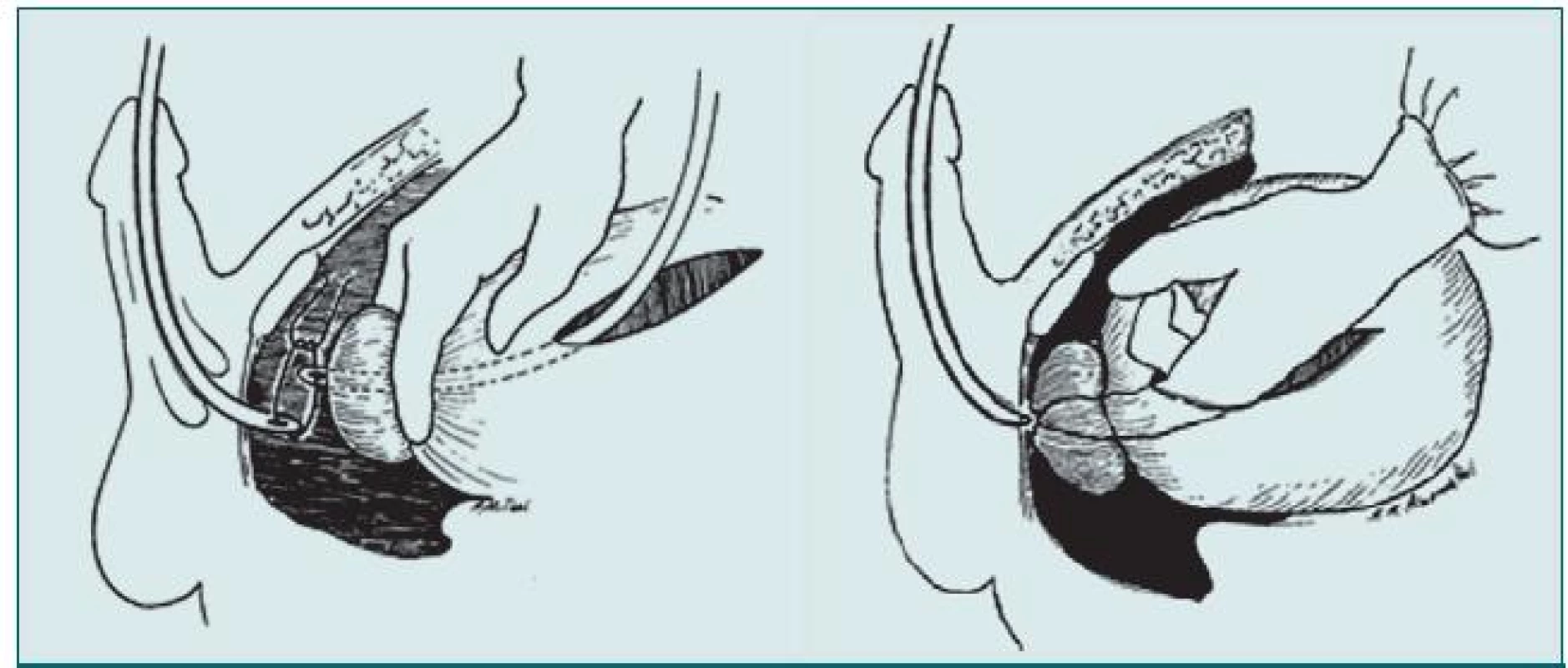
Poranění penisu bez okamžité detumescence lze léčit konzervativně. V případě fraktury penisu je však doporučována okamžitá chirurgická léčba.
Diagnostický postup obvykle zahrnuje odebrání anamnézy, fyzikální vyšetření, kavernosografii (u malých lézí často dochází k falešně negativním nálezům) a uretrografii (v případě, že pacient není schopen močit nebo má krev v meatu uretry či hematurii). Konzervativní léčba se vzhledem k riziku přehlédnutí poškození močové trubice (5 %), vzniku abscesu na penisu (8 %), rozšiřujícího hematomu vyžadujícího operační léčbu (14 %), signifikantní angulace (23 %) a impotence (až 62 %) nedoporučuje. Při časné korekci může dojít k mírné angulaci penisu [43].
17. Progresivní perineální rekonstrukce pomocí anastomózy. 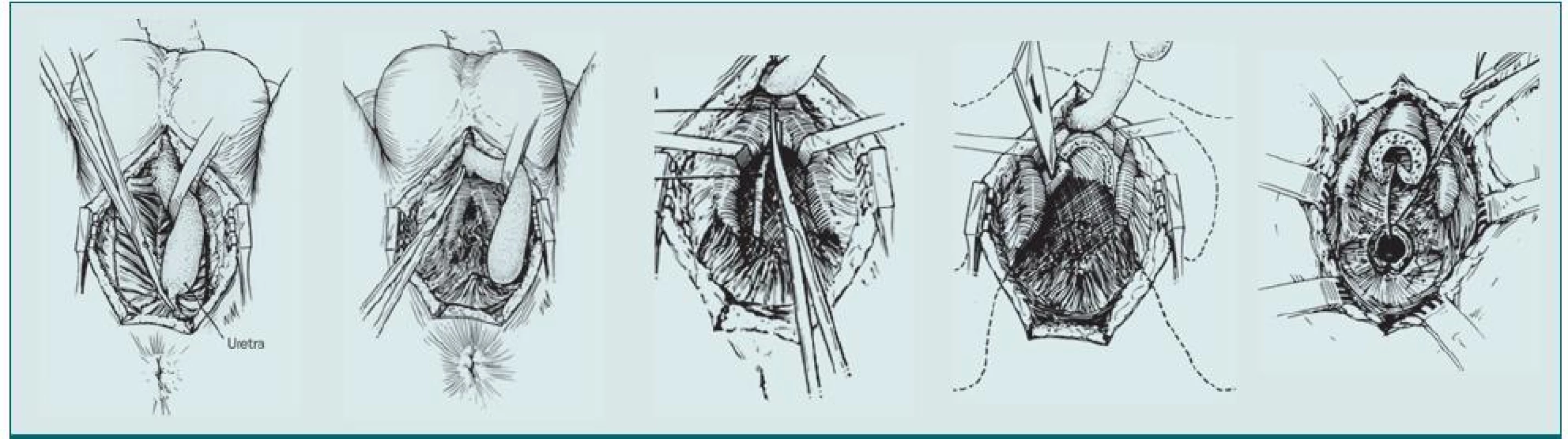
U penetrujícího poranění genitálu se doporučuje provedení uretrografie pro vyloučení poranění močové trubice. V případě, že je to možné, se doporučuje chirurgické odstranění nekrotické tkáně a provedení primární sutury.
U tupého poranění skrota může dojít ke vzniku podkožního nebo intraskrotálního hematomu (hematoskrotum). K dislokaci varlete dochází pouze ojediněle, v 50 % přímého poranění skrota dochází k ruptuře.
Testikulární trauma (s malou hematokélou nebo bez ní) lze léčit aplikací nesteroidních analgetik a ledováním. V případě, že je hematokéla větší velikosti, doporučuje se operační léčba. Ruptura varlete vyžaduje odstranění nekrotické tkáně a uzavření tuniky albuginea.
18. Diagnostický postup při léčbě močové trubice. 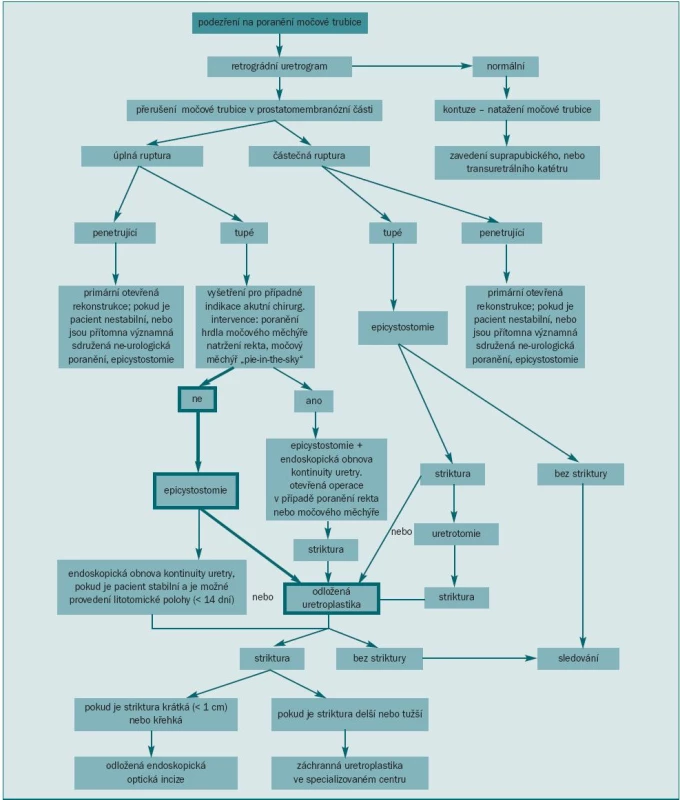
Rozsáhlé lacerace ve skrotu je nutné uzavřít chirurgicky.
K tupému poranění vulvy dochází velmi ojediněle a obvykle se manifestuje vznikem hematomu. V tomto případě je obvykle dostačující konzervativní léčba.
J. Sánchez Gómez
L. Martínez-Pineiro
Hospital Infanta Sofia
Urology Section
Paseo de Europa 34
28702 San Sebastián de los Reyes
Madrid, SPAIN
MARTINEZ-PINEIRO@telefonica.net
Sources
1. Lynch T, Martinez-Pineiro L et al. EAU Guidelines on Urological Trauma. Eur Urol 2005; 47 : 1–15.
2. Meng MV, Brandes SB, McAninch JW. Renal trauma: indications and techniques for surgical exploration. World J Urol 1999; 17(2): 71–77.
3. Paparel P, N’Diaye A, Laumon B et al. The epidemiology of trauma of the genitourinary system after traffic accidents: analysis of a register of over 43,000 victims. BJU Int 2006; 97(2): 338–341.
4. Buchberger W, Penz T, Wicke K et al. Diagnosis and staging of blunt kidney trauma. A comparison of urinalysis, i.v. urography, sonography and computed tomography. Rofo 1993; 158(6): 507–512. [article in German]
5. Hardeman SW, Husmann DA, Chinn HK, Peters PC. Blunt urinary tract trauma: identifying those patients who require radiological diagnostic studies. J Urol 1987; 138(1): 99–101.
6. Mee SL, McAninch JW. Indications for radiographic assessment in suspected renal trauma. Urol Clin North Am 1989; 16(2): 187–192.
7. Bent C et al. Urological injuries following trauma. Clin Radiol 2008, doi:10.1016/j.crad.2008.03.011 (in press).
8. Kawashima A, Sandler CM et al. Imaging of renal trauma: a comprehensive review. Radiographics 2001; 21 : 557.
9. Moore EE et al. Organ injury scaling: spleen, liver and kidney. J Trauma 1989, 972 : 54.
10. Rosales A, Arango O, Coronado J et al. The use
of ultrasonography as the initial diagnostic exploration in blunt renal trauma. Urol Int 1992; 48(2): 134–137.
11. Qin R, Wang P, Qin W et al. Diagnosis and treatment of renal trauma in 298 patients. Chin J Traumatol 2002; 5(1): 21–23.
12. Morey AF, McAninch JW, Tiller BK et al. Single shot intraoperative excretory urography for the immediate evaluation of renal trauma. J Urol 1999; 161(4): 1088–1092.
13. Leppäniemi A, Lamminen A, Tervahartiala P et al. MRI and CT in blunt renal trauma: an update. Semin Ultrasound CT MR 1997; 18(2): 129–135.
14. Memon S, Cheung BY. Long-Term Results of Blunt Traumatic Renal Artery Dissection Treated by Endovascular Stenting. Cardiovasc Intervent Radiol 2005. [Epub ahead of print]
15. Dobrilovic N, Bennett S, Smith C et al. Traumatic renal artery dissection identified with dynamic helical computed tomography. J Vasc Surg 2001; 34(3): 562–564.
16. Long JA, Manel A, Penillon S et al. Traumatic dissection of the renal pedicle. Modalities of management in adults and children. Prog Urol 2004; 14(3): 302–309.
17. Broghammer J et al. Conservative management of Renal Trauma. A Review. Urology 2007; 70 : 623–629.
18. McAninch JW, Carroll PR et al. Renal reconstruction after injury. J Urol 1991; 145 : 932.
19. Alsikafi NF, McAninch JW†, Elliott WP et al. Nonoperative Management Outcomes of Isolated Urinary Extravasation Following Renal Lacerations Due to External Trauma. J Urol 176(6): 2494–2497.
20. Tillou A, Romero J. Renal vascular injuries. Surg Clin North Am 2001; 81 : 1417.
21. Hagiwara A, Sakaki S. The role of interventional radiology in the Management of blunt renal injury:
a practical protocol. J Trauma 2001; 51 : 526.
22. Memon S, Cheung BY. Long-Term Results of Blunt Traumatic Renal Artery Dissection Treated by Endovascular Stenting. Cardiovasc Intervent Radiol 2005. [Epub ahead of print]
23. Dobrilovic N, Bennett S, Smith C et al. Traumatic renal artery dissection identified with dynamic helical computed tomography. Vasc Surg 2001; 562–564.
24. Haas CA et al. Use of ureteral stents in the management of major renal trauma with urinary extravasation: is there a role? J Endourol 1998; 12 : 545.
25. el Khader K et al. Conservative treatment of stage III kidney injuries. Acta Urol Belg 1998; 66 : 25.
26. Santucci RA et al. Grade IV renal injuries: evaluation, treatment and outcome. World J Surg 2001; 25 : 1565.
27. Velmahos CG et al. Selective Management of renal gunshot rounds. Br J Surg, 1998; 85 : 1121.
28. Palmer LS, Rosenbaum RR et al. Penetrating ureteral trauma at an urban trauma center: 10-year experience. Urology 1999; 54 : 34.
29. Henderson CG et al. Management of high grade renal trauma: 20-year experience at a pediatric level I trauma center. J Urol 2007; 178(1): 246–250.
30. Cass AS, Luxenberg M. Traumatic thrombosis of
a segmental branch of the renal artery. J Urol 1987; 137(6): 1115–1116.
31. Palmer LS et al. Penetrating ureteral trauma at an urban trauma center: 10-year experience. Urology 1999; 54 : 34.
32. Dobrowolski Z et al. Renal and ureteric trauma: diagnosis and management in Poland. BJU Int 2002; 89(7): 748–751.
33. Armenakas NA. Ureteral trauma: surgical repair. Atlas Urol Clin North Am 1998; 6 : 71–84.
34. Corriere JN Jr, Sandler CM. Management of the ruptured bladder: seven years of experience with 111 cases. J Trauma 1986; 26(9): 830–833.
35. Morey AF et al. Reconstructive surgery for trauma of the lower urinary tract. Urol Clin North Am 1999; 26 : 49.
36. Sevitt S. Fatal road accidents. Injuries, complications, and causes of death in 250 subjects. Br J Surg 1968; 55(7): 481–505. http://www.ncbi.nlm.nih.gov/ pubmed/5663432
37. Koraitim MM, Marzouk ME, Atta MA et al. Risk factors and mechanism of urethral injury in pelvic fractures. Br J Urol 1996; 77(6): 876–880. http://www. ncbi.nlm.nih.gov/pubmed/8705225
38. Dixon CM. Diagnosis and acute management of posterior urethral disruptions, In: McAninch JW (ed). Traumatic and reconstructive urology. Philadelphia: WB Saunders 1996 : 347–355.
39. Devine PC et al. Posterior urethral injuries associated with pelvic fractures. Urology 1982; 20 : 467.
40. Koraitim et al. Pelvic fracture urethral injuries: the unresolved controversy. J Urol 1999; 161 : 1433.
41. Chapple CR, Png D. Contemporary management of urethral trauma and the post-traumatic stricture. Curr Opin Urol 1999; 9 : 253.
42. Martinez-Pineiro JA et al. Excision and anastomotic repair for urethral stricture disease. Experience with 150 cases. Eur Urol 1997; 32 : 433.
43. Nicolaisen GS et al. Rupture of the corpus cavernosum: surgical management. J Urol 1983; 130(5): 917–919.
Labels
Paediatric urologist Urology
Article was published inUrological Journal

2011 Issue 1-
All articles in this issue
- Technique of harvesting oral mucosa for urethral reconstruction. Evaluation of postoperative complications and patient satisfaction
- Management of urethral stricture: dorsal flap from buccal mucosa – the gold standard
- Urinary tract and genital trauma
- Neuro-urological assessment and treatment
- Stress urinary incontinence in women: diagnostics and treatment based on AUA guidelines review
- Percutaneous nephrolithotomy (PNL): a review of current procedural techniques and developments
- Hormone therapy in the management of prostate cancer: treating the cancer without hurting the patient
- Cancer treatment induced bone loss (CTIBL): burning issue in prostate cancer patients – our experience
- EAU Guidelines on Urethral Trauma
- Urological Journal
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Management of urethral stricture: dorsal flap from buccal mucosa – the gold standard
- Hormone therapy in the management of prostate cancer: treating the cancer without hurting the patient
- Urinary tract and genital trauma
- Technique of harvesting oral mucosa for urethral reconstruction. Evaluation of postoperative complications and patient satisfaction
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

